A szénhidrátkémia kisszótár:
|
|
|
- Etelka Barnané
- 8 évvel ezelőtt
- Látták:
Átírás
1 A szénhidrátkémia kisszótár: akirális: királis tulajdonággal nem rendelkez molekula anomer -atom: a ciklofélacetál gyrben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer aszimmetriás -atom: A molekula egy olyan sp3-as szénatomja amelyhez 4 különböz atom vagy atomcsoport kapcsolódik. ciklofélacetál gyr: akkor képzdik addíció útján, ha a vagy csoport és egy alkoholos térben közel kerülnek diszacharid: két monoszachariddá hidrolizálható diasztereomer(ek): nem enantiomer tulajdonságú sztereoizomerek. enantiomer: egymással fedésbe nem hozható tükörképi pár térszerkezetek epimer: egy másik molekula olyan sztereoizomerja, amelynek bár több sztereocentruma van, de a köztük lév sztereokémiai különbség mindössze egy sztereocentumra vonatkozik. furanóz gyr: öttagú furán gyrt tartalmazó molekuláris rendszer. homokirális molekulák: molekulák, amelyek azonos kiralitással rendelkeznek. 1
2 konstitúció: a molekulát alkotó atomok összessége, amely figyelembe veszi az atomok közötti kötéseket, de nem azok térbeli elrendezdését. konstitúciós izomerek: szerkezeti izomerek konfiguráció: egy központi atomhoz kémiai kötéssel közvetlenül kapcsolódó atomok térbeli elrendezdése, ami jellemzi a molekula térszerkezetét királis (kiralitás): az a molekula, amelyik saját tükörképi párjától különbözik, azaz tükörképi párjával fedésbe nem hozható. laktolgyr: ciklofélacetál gyr mezo-forma: olyan molekula, amely bár 2 vagy több aszimmetria-centrumot tartalmaz mégis bels kompenzáció folytán optikailag inaktívvá vagy akirálissá válik. monoszacharid: nem hidrolizálható további cukrokká mutarotáció: az a folyamat, amely során a cukrok félacetáljainak tiszta anomerjei azok egyensúlyi keverékét hozzák létre. oligoszacharid: 2-10 monoszacharid építi fel piranózok: olyan monoszacharidok, amelyek hattagú, egy heteroatomos gyrt tartalmaznak. poliszacharid: >10 monoszacharid építi fel pszeudo aszimmetriás -atom: hamis-, ál-, látszólagosan aszimmetriás -atom sztereoizomerek: olyan izomer molekulák, amelyekben rendre azonos kötések kötik össze az azonos atomokat, noha azok térbeli elrendezdése különböz. szerkezeti izoméria: az izoméria egy formája, ahol az azonos összegképlet molekulák atomjai eltér módon kapcsolódnak egymáshoz. triszacharid: három monoszachariddá hidrolizálható 2
3 A cukorkémia koronázatlan királyai, kémiai Nobel-díjak: Emil Fischer 1902 Nobel-díj molecular structures of fructose, glucose, and many other sugars Eduard Buchner 1907 Nobel-díj enzyme causes sugar to break up into carbon dioxide and alcohol. ans von Euler- helpin Sir Arthur arden 1929 Nobel-díj fermentation of sugar Sir Norman.W aworth 1937 Nobel-díj succeeded in synthesizing vitamin Szent-Györgyi Albert rvosi Nobel-díj
4 monoszacharidok A méz kb. 82%-a szénhidrát. Monoszacharidok közül fruktózt (38,2%) és glükózt (31%), diszacharidok közül (~9%) szacharózt, maltózt, izomaltózt, maltulózt, turanózt és kojibiózt tartalmaz. ligoszacharid tartama (4.2%) viszonylag alacsony. 4
5 A szénhidrát, mint a felismerés eszköze I: a sejtközi térben lév fehérvérsejtek szolgálat közben. fehérvérsejtek vörösvértest fehérvérsejtek felületén lév szialil Lewis-X glikopeptidek Sérülés esetén a helyszínen megjelen szelektin nev fehérjék a Lewis-X glikopeptidek segítségével fehérvérsejteket (leukocitákat) kötnek meg. E felületre adhézió során kötd és az érfalon kilép leukociták fontos szerephez jutnak a további védekezésben. kapilláris kapilláris fal endotél sejtek szelektin (fehérje) 5
6 A szénhidrát, mint a felismerés eszköze II: Az A, B és 0 vércsoportok A B, A és 0 gén gyakorisága 4 etnikum esetében: GB J ongkong Eltér konstitúciójú sejtfelszíni glikoproteinek: Vértranszfúzió során sokan meghaltak addig, míg ben Landsteiner meg nem fejtette a agglutináció rejtélyét. Karl Landsteiner rvosi Nobel-díj (1930) Fuc α-1,2 Gal β-1,3 GlcNAc β-1,3 Gal Fuc α-1,2 Gal GlcNAc α-1,3 β-1,3 GlcNAc β-1,3 Gal Fuc Gal α-1,2 Gal α-1,3 β-1,3 GlcNAc Gal β-1,3 6
7 A sztereokémia nagy hatása. cellulóz (lineáris) keményít (spirális) hidrolízis cellobióz (β-forma) hidrolízis maltóz (α-forma) 2 2 β cellobióz = 4-(β-D-glükozil<1,5>) -D-glükóz <1,5> celloboióz A cellulóz (Földünk legelterjedtebb szénvegyülete): - minden - -kötés akceptor és donor, ezért nem oldódik vízben a cellulóz 2 2 α maltóz = 4-(α-D-glükozil<1,5>)- D-glükóz <1,5> (maláta cukor) maltóz A keményít hélixében: - vannak szabad --k, ezért vízben oldható a keményít, - a hidrofób részek vannak befelé 7 (I 2 )
8 A vízoldhatatlanság titka: vízoldható di- és oligomer, de vízoldhatatlan polimer [β-d-glükozil<1,5>)] n 8
9 Életünk alapja: a fotoszintézis során elállított energia és annak felhasználása x 2 + y 2 napfény x ( 2 ) y + x 2 szénhidrát x ( 2 ) y + x 2 szénhidrát x 2 + y 2 + E energia 9
10 Életünk alapja a fotoszintézis során elállított energia x 2 + y 2 napfény x ( 2 ) y + x 2 szénhidrát 10
11 Életünk alapja a fotoszintézis során elállított energia cél: fényenergiából kémiai energiát állít el a kloroplasztisz A fényfügg reakció: A víz, mint redukálószer, aminek mellékterméke az NADP ADP + 2 P i + fény 2 NADP ATP + 2 A sötét reakció, szénfixálás vagy alvin-ciklus: ATP + 6 NADP foszfát + 9 ADP + 8 P i + 6 NADP A bruttó egyenlet: 6 2 (gáz) (folyadék) + fotonok (folyadék) (gáz) (folyadék) redukálószer cukor melléktermék memo: a növény tipikusan nem mono-, hanem diszacharidot állít el, mint pl. a nádcukor, répacukor vagy más néven szacharóz α β α D-Glükozil<1,5>-β-D-fruktozid<1,5>
12 A szénhidrátok sokrét biológiai szerepe: Tartalék tápanyag (az energia molekuláris tárolása): - keményít (növények) - glikogén (állatvilág) Energiaforrás (prekurzorok): pl. ATP Genetikai információ (építelemek): DNS, RNS Szerkezeti elemek: peptidoglikán (bakteriális sejtfal) cellulóz (növényi sejtfal, váz) exoszkeleton (gerinctelenek) Glikokonjugátumok: glikolipid glikopeptid, glikoprotein Glikolipidek: foszfatidil-inozit (sejtmembrán) Glikoproteidek: sejt sejt felismerés célbajuttatás ( targeting ) szállítás sejtmembrán vércsoport 12
13 Szénhidrátok etimológiája m ( 2 ) n cukor: - hétköznapi értelemben a cukor, az a szacharóz (Eng.: sucrose) - tudományos értelemben a cukor vagy szacharid, az a monoszacharid Szacharid (lat. saccharum, <cukor>) mono-, di-, tri-, oligo-, poliszacharid szacharóz: egy nem redukáló diszacharid (szukróz, nádcukor, répacukor, asztali cukor) α β szacharin: mesterséges édesítszer (megtéveszt név, mert bár édes nem szénhidrát) α D-Glükozil<1,5>-β-D-fruktozid<1,5> Gliko eltag (gör. glüküsz, <édes>) glikolipid, glikopeptid, glikoprotein, glikokonjugátum, glikobiológia, stb. szacharin S N 13
14 Szénhidrátok (polihidroxi-aldehidek és polihidroxi-ketonok) méretszerinti osztályozása: monoszacharid: nem hidrolizálható további cukrokká diszacharid: két monoszachariddá hidrolizálható mól maltóz diszacharid 2 mól glükóz monoszacharid mól szacharóz diszacharid 1 mól glükóz monoszacharid 1 mól fruktóz monoszacharid triszacharid: három monoszachariddá hidrolizálható oligoszacharid: 2-10 monoszacharid építi fel, poliszacharid: >10 monoszacharid építi fel 1 mól keményítõ vagy 1 mól cellulóz poliszacharid n n sok mól glükóz monoszacharid 14
15 A glükóz konstitúciójának meghatározása E. Fischer ( ) D-glükóz kvalitatív analízis:,, kvantitatív analízis: : 40,0 % : 6,7 % : 53,3 % m ( 2 ) m molekulatömeg: 180 Da 6 ( 2 ) 6 kérdés: milyen lehet az oxigénatom konstitúciós helyzete?,, = tapasztalat: Ac [ 6 7 ](Ac) 5 5 Br [ 6 7 ](Ac) 2 / 2 5 [ 5 6 (Ac) 5 ] [ 5 6 () 5 ] I/P válasz: tehát egyenes szénláncú polihidroxi-oxovegyület n- 3 ( 2 ) 5 1 = 15 Egyenes szénlánc
16 A glükóz konfigurációjának és sztereoizomerjeinek meghatározása * * * * 2 = 2,3,4,5,6-pentahidroxihexanal 16
17 A monoszacharidok polihidroxioxovegyületek = () n 2 2 = () n 2 szénatomok száma (trióz, tetróz, pentóz, hexóz, heptóz) aldehid keton Polihidroxialdehid aldotetróz n=2 aldopentóz n=3 aldohexóz n=4 aldoheptóz n=5 Polihidroxiketon ketotetróz n=1 ketopentóz n=2 ketohexóz n=3 kérdés: ány kiralitáscentrummal rendelkezik egy (a) aldotetróz, (b) ketopentóz, (c) n-atomos aldóz, (d) n-atomos ketóz? 17
18 Konfiguráció, kiralitás, D/L-konvenció gliceraldehid (egy aldotrióz) dihidroxi-aceton (egy ketotrióz) egy kiralitáscentrum nincs kiralitáscentrum 2 (+)-gliceraldehid (R)-(+)-gliceraldehid D-(+)-gliceraldehid D-cukor: 2 ( )-gliceraldehid (S)-( )-gliceraldehid L-( )-gliceraldehid L-cukor az a monoszacharid, amelyikben a legmagasabb sorszámú avagy a karbonil csoport legtávolabbi kiralitáscentruma (leggyakrabban az utolsó eltti szénatom), a D-(+)-gliceraldehiddel {L-( )-gliceraldehiddel} azonos konfigurációjú. 18
19 Az abszolút konfiguráció meghatározása, IP szabály: (b) (c) 3 (d) (,,) F (a) 1) a sztereocentrumhoz közvetlenül kapcsolódó atomok (szubsztituensek) rangsorának felállítása: az atomok rangja az atomszámmal n (<<N<<F<l< ) a a (,,) 2) ha két szubsztituens királis szénhez kapcsolódó atomtípus azonos, akkor a konnektivitás mentén az els különbséget keressük (szférák) R.S.ahn,.K.Ingold és V.Prelog (1966) c b c R b R: rectus (egyenes) S: sinister (bal) 3) R vagy S meghatározása: úgy nézzük a királis szenet, hogy a legkisebb rangú 19 szubsztituenst ne lássuk : ha a rang az óramutató járása szerint növekszik akkor R, amúgy S
20 4) A többszörös kötés esetén duplikálás, triplikálás Y Y (Y) () (Y) () pl. () () () () pl. () () (N) () Y Y N N megjegyzés: prioritás sorrendek példák: 2 l 2 (Y) () () () a ( ) atomok "meztelen" atomok, azaz nincs "f olytatás" -l > -S > - > Br > - 2 l > - 2 > > - > - 3 > ( 3 ) > 2 > () 2 () (N) () 3 b d a c d a a c b c (S) b (R) d (S) 20
21 A Fischer-projekció Pozicionálás a síkban: Az aciklusos monoszacharidok gerince függleges; a formil- vagy a karbonilcsoport mindig felül helyezkedik el egy D-aldopentóz 5 D-cukor: A -tól legtávolabbi, most az utolsó eltti szénatom -csoportja jobbra áll. Kódolási konvenció: a függleges vonal a papír síkjában elhelyezked vagy a sík mögé mutató kötést jelentik, míg a vízszintes a papír síkjából kiemelked kötésre utal. Kiralitáscentrumok: Értelmezésük és meghatározásuk különkülön történik egy L-ketohexóz 6 L-cukor A -tól legtávolabbi, most az utolsó eltti szénatom 21 -csoportja balra áll.
22 Aldotrióz abszolút konfigurációjának meghatározása: b d a 2 c 2 (R)-glicerinaldehid D-glicerinaldehid (S)-glicerinaldehid L-glicerinaldehid d b a a b b a a b d 2 c 2 c 2 c 2 22 c
23 2 2 (R)-glicerinaldehid [ ] 25 α = D (S)-glicerinaldehid [ ] 25 α = 13.5 D M.A. Rosanoff, 1906: D/L D-glicerinaldehid D-(+)-glicerinaldehid L-glicerinaldehid L-( )-glicerinaldehid D-glicerinaldehid E. Fischer, 1906 dextro (d) (+) levo (l) ( ) mezo (dl) (±) 23
24 Aldotrióz (glicerinaldehid 1 királis ): enantiomer (antipód) térszerkezetek 2 enantiomerek azonosak (S)-glicerinaldehid (S)-glicerinaldehid (S)-glicerinaldehid (R)-glicerinaldehid 24
25 25 B D A A B D A D B A B D B A D B D A B A D D B A B D A A D B D A B D A B D B A enantiomer A Fischer-projekció: konvencionálisan egy a 12 közül
26 Aldotetróz (2 királis ): 4 diasztereomer térszerkezet kérdés: milyen viszonyban vannak a sztereoizomerek egymással? válasz: - D-erit. és L-erit. egymás tükörképi párja: azaz enantiomerek - D-treo. és L-treo. egymás tükörképi párja: azaz enantiomerek - 1 és 3 vagy 2 és 4 nem tükörképi párok, de sztereoizomerek azaz diasztereomerek: azonos enant. dia.(2 epi) dia.(3 epi) 2 azonos dia.(3 epi) dia.(2 epi) 3 azonos enant. 4 azonos R R 2 D-eritróz 1 S S 2 L-eritróz 2 memo: Az 1-es és 3-as molekulák 3-as szénatomjainak konfigurációja azonos, míg a 2-szénatomok konfigurációja különböz: ezért ez a diasztereomer pár egymás 2-epimere. S R R S memo: A diasztereomer molekulák (fizikai tulajdonságaik) olvadás- és forráspontja eltér, a törésmutatójuk különböz, az oldhatóságuk, az IR- és NMR-spektrumuk más és más. A két molekula különböz tulajdonságokkal rendelkezik. 2 D-treóz 3 L-treóz
27 Aldopentóz (3 királis ): 8 db diasztereomer térszerkezet D-ribóz D-arabinóz D-xilóz D-lixóz D- vagy L-? A legmagasabb sorszámú kiralitáscentrum és a glicerin aldehid konfigurációja D-glicerinaldehid L-ribóz L-arabinóz L-xilóz L-lixóz kiemelt fontosságú cukor 27 2 L-glicerinaldehid
28 Aldohexóz (4 királis ): 16 diasztereomer térszerkezet a 8 db D-sorozatbeli aldohexóz nyílt formája: 2-epimerek 2-epimerek D-allóz D-altróz D-glükóz D-mannóz 4-epimerek D-gülóz D-idóz D-galaktóz D-talóz kiemelt fontosságú cukor 28
29 Ketohexóz (3 királis ): 8 diasztereomer térszerkezet a 4 db D-sorozatbeli hexulóz nyílt formája: D-pszikóz D-fruktóz D-szorbóz D-tagatóz ribohexulóz arabinohexulóz xilohexulóz lixohexulóz 29 kiemelt fontosságú cukor
30 Ketohexózok (3,2,1 és 0 királis -vel): 8,4,2,és 0 diasztereomer térszerkezet D-ketohexózok 2 D-pszikóz 2 D-fruktóz 2 D-szorbóz 2 D-tagatóz 2 2 D-ketopentózok 2 D-ribulóz (D-eritro-pentulóz) 2 D-xilulóz (D-treo-pentulóz) D-ketotetrózok 2 2 D-eritrulóz (D-glicero-tetrulóz) β-d-fruktofuranóz ketotrióz 2 dihidroxi-aceton 30
31 * szter. izom. (db) (db) D-sorozatbeli aldózok sematikus rajza: 2x
32 Az aldohexózok tényleges szerkezete: nem lineáris, hanem ciklusos (2R,3S,4R,5R)-2,3,4,5,6- pentahidroxi-hexanal avagy D-glükóz 2 Fischer-projekció Reeves-képletek 2 2 sztereo imitáció 2 α-d-(+)-glükopiranóz β-d-(+)-glükopiranóz 2 aworth-képletek 2 memo: átírási szójáték bal (3 bet): => fel (3 bet) jobb (4 bet): => lent (4bet) piros kék töltés
33 Az aldohexózok tényleges szerkezete: nem lineáris, hanem ciklusos A f élacetál képzõdés a gyûrûs f ormához vezet: nyílt láncú D-glükóz nyílt láncú D-glükóz 2 1 iklizálással félacetál képzdik, kiralitáscentrummá válik a 1-atom (anomer szénatom) az így kialakuló diasztereomerek anomerek α-anomer ill. β-anomer 2 2 α-d-(+)-glükopiranóz β-d-(+)-glükopiranóz α/β -D-(+)-glükopiranóz: az anomer konfiguráció nem definiált
34 A legfontosabb aldohexózok gyrs szerkezete 2 α-d-glükopiranóz 2 β-d-glükopiranóz 2 α-d-glükopiranóz 2 β-d-glükopiranóz 2 2 α-d-mannopiranóz β-d-mannopiranóz 2 α-d-mannopiranóz 2 β-d-mannopiranóz 2 2 α-d-galaktopiranóz β-d-galaktopiranóz 2 α-d-galaktopiranóz 2 β-d-galaktopiranóz 34
35 iklusos félacetál képzdése, avagy hogyan rajzoljunk ügyesen: 2 D-glükóz o 5 -körüli elforgatás fent lent D-glükóz 2 gyûrûs alak preformálása D-glükóz 2 intramolekuláris félacetál képzdés β D-glükóz memo: 2 β D-glükóz piranóz forma a β-d-glükóz piranóz gyrs szerkezetének különböz ábrázolása 2 D-glükóz aldehido forma 2 aworth-böeseken képlet síkalkat impresszió 2 α D-glükóz piranóz forma 2 Reeves képlet 35
36 36 glükóz galaktóz talóz mannóz gülóz idóz altróz allóz A 8 D-aldohexóz (kockacukor-cukorkocka) 2 epimerizáció 3 epimerizáció 4 epimerizáció
37 iklusos félacetál képzdése, avagy hogyan rajzoljuk a furanózokat: A nyílt láncú D-fruktóz különbözö konformációi nyílt láncú D-fruktóz nyílt láncú D-fruktóz 1 2 memo: pirán furán β-d-f ruktofuranóz α-d-f ruktofuranóz 1 2 tetrahidro-2 -pirán tetrahidrofurán 37
38 A mutarotáció jelensége: 2 2 Ac-ból kristályosítva α-d-(+)-glükopiranóz p. 146 o [α] D 25 = +112 o 36 % egyensúlyi oldatban 2 Et-ból kristályosítva β-d-(+)-glükopiranóz p. 150 o [α] D 25 = +18,7 o 64 % egyensúlyi oldatban nyílt láncú D-(+)-glükóz egy id múlva beáll az egyensúlyi oldat, amely forgatása : +52,7 o (= 0,36*112 o + 0,64*18,7 o ) kérdés: miért stabilabb a β-, mint az α-anomer? válasz: a nagyobb térigény - (és nem a kisebb -) van ekvatoriális pozícióban. kérdés: van-e számottev nyílt forma jelen az oldatban? válasz: nincs, sem UV-ban, sem IR-ben a = sávok nem azonosíthatók! 38
39 kérdés: minden hexopiranóz esetében a β- stabilabb, mint az α-anomer? tapasztalat: anomer α β T( o ) iklohexanol Glükóz 36* Galaktóz Mannóz 69** * 3-szoros növekedés a referenciához képest és **7-szeres növekedés a referenciához képest kérdés: miért fordul meg a stabilitási sorrend a mannóz esetében? válasz: az anomer-effektus miatt. magyarázat: elektronegatív szubsztituensek (pl. hidroxil-, alkoxicsoport, halogénatom) elnyben részesíthetik az axiális helyzetet a sztérikusan kedvezbb ekvatoriális állással szemben, ha a gyr szomszédos atomja nemköt elektronpárral rendelkezik. 2 2 α-d-mannopiranóz 69 % egyensúlyi oldatban β-d-mannopiranóz 31 % egyensúlyi oldatban magyarázat: (1) hiperkonjugáció az endociklusos heteroatom nemköt elektronpárja és az axiális σ* molekulapálya között; (2) exo- és endociklusos heteroatomok dipólusai közel ellentétes állásúak axiális szubsztituens esetén, míg ekvatoriálisnál közel párhuzamosak. 39
40 Glikozid képzés: D-(+)-glükóz l (-) 3 metil-α-d-glükopiranozid p. 165 o [α] 25 D = 158 o metil-β-d-glükopiranozid p. 107 o [α] 25 D = 33 o glikozidok: szénhidrátok acetáljai, bázikus oldatban stabilak, sav hatására cukorra és alkoholra hidrolizálnak, glükozid: glükóz acetálja, mannozid: mannóz acetálja, fruktozid: fruktóz acetálja,... 40
41 A glikozid képzdés mechanizmusa (E + Ad): A A β-d-glükopiranóz rezonancia által stabilizált karbokation A A 2 3 metil-β-d-glükopiranozid 2 memo: az alkohol mindkét oldalról kvázi egyforma eséllyel támadhat. 3 A A 3 metil-α-d-glükopiranozid 41
42 Glikozidok hidrolízise: 2 2 R R glükozid (bázikus oldatban stabil savban hidrolizál) cukor aglikon (egy glikozid cukormentes alkotórésze) definíció: aglikon: glikozid hidrolízisével nyert alkohol példa: a szalicin (fzfa és nyárfa kérgébl izol. [1830.]) - a köszvény és reuma hatásos gyógyszere - aszpirin szintézisére használható alapanyag glükóz 2 szalicilalkohol aglikon Ac 2 aszpirin szalicin 42
43 Glikozidok hidrolízisének mechanizmusa (E + Ad): metil-β-d-glükopiranozid metil-β-d-glükopiranozid rezonancia által stabilizált karbokation β-d-glükopiranóz 2 memo: a víz mindkét oldalról kvázi egyforma eséllyel támadhat α-d-glükopiranóz 43
44 ukrok epimerizációja lúgos közegben: kísérlet: D-Glükóz 24h vizes a() 2 tapasztalat: D-Mannóz, D-Fruktóz is megjelenik az oldatban. következtetés: védcsoport alkalmazása, ha bázikus közegben akarunk dolgozni: Pl. Me-glikozidot készítünk a cukorból, és mivel az acetál lúgos körülmények között stabilis, ezért elvégezhetjük a kívánt reakciót, majd savval elhidrolizáljuk az acetál védcsoportot. = 2 ornelius Adrian van Troostenbery Willem = 2 Lobry de Bruyn Alberda van Ekenstein (1895)
45 Enolizáció, tautomerizáció, izomerizáció Védcsoportok alkalmazása a szénhidrátkémiában D-glükóz 2 enolátion 2 2 D-mannóz 2 tautomerizáció 2 2 éndiol 2 D-f ruktóz 45
46 ukoréterek elállítása (S N 2): bázis (Na v. K), alkil-halogenid (benzilbromid), DMF v. DMS (standard Williamson féle éter szintézis) Bzl Br Na/DMF, hõ Bzl Bzl Bzl 2 3 benziléter Bzl 3 ukoréterek elbontása: hidrálás (Pd/) Bzl Bzl Bzl 2, Pd Bzl
47 ukor metiléterek elállítása (S N 2): bázis (vizes Na), felesl. dimetilszulfáttal 3 memo: Et- + vizes Na nem lesz alkoholát, de a cukorban a sok e- csop. miatt mindegyik rendre -lesz és ezért megy a metilezés. 3 3 S 3 3 metilglikozid 3 3 ismételt metilálás pentametil származék ukor metiléterek stabilitása vizes savban: vizes savban az acetál igen, de az éter kötés nem hidrolizál! 3 3 pentametil származék ,3,4,6-tetra--metil-D-glükóz 2 3 memo: A nyitott formában a 5-, ami nem metilezett azaz piranóz a gyr! 47
48 ukoréter elállítása (regioszelektív szintézis során): a primer alkohol reagál (S N ) TBDPS 3 TBDPS l AgN 3 vagy imidazol 3 TBDPS 3 3 Si 3 ukoréter hasítása: kvaterner bázissal terc-butil-difenil-szilil TBDPS 3 Bu 4 N + F TF 3 48
49 Észterek szintézise: gyenge bázis (pl. piridin, nátrium-acetát), savanhidrid (ecetsavanhidrid); alacsony hmérsékleten a reakció sztereospecifikus: α-anomer α-acetát β-anomer β-acetát ( 3 ) 2 piridin, 0 o iklikus acetálok szintézise: aldehid, keton + 1,2-diol: csak cisz állású vicinális hidroxilcsoportokkal pl. α-d-galaktópiranóz esetében megy a reakció. cisz cisz S acetonid 49
50 ukrok oxidációs reakciói I. (cukrok kimutatása): Tollens-reagens Ag(N 3 ) 2 + Ag 0 Fehling-reagens u 2+ -tartarát u 2 borkõsav 2,3-dihidroxiborostyánkõsav Benedict-reagens u 2+ -citrát u 2 citromsav 2-hidroxipropán-1,2,3-50 trikarbonsav
51 Tollens-próba (ezüsttükör-próba): alifás és aromás aldehidek kimutatása R aldehid Ag(N 3 ) R + Ag ezüsttükör 0 2(+1) (+1) +1 Kísérleti körülmények: N 3 (5 ml) + AgN 3 (vizes) 150 ml kevertetés közben. A keletkez csapadék feloldódik további N 3 (5 ml) hatására. Az oldathoz adjuk a cukor vizes oldatát (4g Glü. 10 ml dest. 2 ), lombikba öntjük és kevertetés közben vízfürdn melegítjük 70. Eredmény: 4 perc múlva a lombik falát ezüsttükör fedi. memo: ketonokkal nem megy kivéve az α-hidroxi ketonok R keton R' Ag(N 3 ) nincs reakció +1 a szén +1-rõl +3-ra oxidálódik az ezüst +1-rõl 0-ra redukálódik. +3 R R' α-hidroxi-keton Ag(N 3 ) R R' + Ag ezüsttükör 51
52 Monoszacharidok oxidációs reakciói: Benedict-próba: alifás aldehidek és redukáló cukrok kimutatása; a reagens u(ii) citrát komplexe bázikus oldatban, jól eltartható (szemben a Fehling-oldattal) u 2+ (komplex) + ( ) n vagy ( 2 ) n oxidációs termékek + u 2 Benedict-oldat (kék) 2 aldóz 2 ketóz téglapiros redukciós termék szacharóz: egy nem redukáló diszacharid α β α D-Glükozil<1,5>-β-D-fruktozid<1,5> 52
53 Redukáló cukrok: azok a cukrok, amelyek pozitív Benedict- vagy Tollens-próbát adnak félacetálcsoportot tartalmazó szénhidrátok: vizes oldatukban aciklusos aldehid vagy α-hidroxi-keton is megjelenik redukáló cukor nem redukáló cukor R' R' R félacetál pozitív Tollens- és Benedict-próbát ad acetál nem ad pozitív Tollensvagy Benedict-próbát R: alkilcsoport vagy egy másik cukor R': vagy 2 Nem redukáló cukrok: azok a cukrok, amelyek negatív Benedict- vagy Tollens-próbát adnak azok a glikozidos szénatomon acetálcsoportot tartalmazó szénhidrátok: lúgos oldatukban nincs jelen aciklusos aldehid vagy α-hidroxi-keton 53
54 Monoszacharidok oxidációs reakciói II: aldonsavak szintézise a kíméletesebb ox. bruttó egyenlete: memo: ( a Br-os ox. preparatív célra is alkalmas. ) n 2 aldóz Br Br ( ) n 2 aldonsav 0 2(+1) memo: 0 2(+1) a szén +1-rõl +3-ra oxidálódik, az elektrofil Br 2 0-rõl -1-re redukálódik. 2 Br 2-2Br β-d-glükopiranóz β-d-glükonsav-δ-lakton (glükonolakton) 2 D-glükonsav β-d-glükonsav-γ-lakton memo: - a glükonsavnál inkább a δ-lakton dominál - a galaktonsav esetében jelentsebb a γ-lakton mennyisége 1 kcal/mol (14%) 0 kcal/mol (86%) 54 RF/3-21G T=300K
55 Monoszacharidok oxidációs reakciói II: aldársavak az erélyesebb oxidáció bruttó egyenlete: ( ) n 2 aldóz N 3 (α ω-polihidroxidikarbonsavak) szintézise ( aldársav ) n memo: ketózok esetében lánchasadáshoz vezet: kisebb tagszámú cukorsavakat kapunk. 2 2 N 3 0 2(+1) N 3 0 2(+1) a szén +1-rõl +3-ra oxidálódik a N +5-rõl +4-re redukálódik. +2N D-glükóz D-glükársav memo: a δ- mellett γ- lakton is képzdik. aldársav (aldohexózból) 2 vagy 55 aldársav γ-laktonjai
56 kérdés: melyik az az aldohexóz amelyik N 3 -as oxidációt követen optikailag inaktív aldársavat eredményez? (Racemizáció nem lép fel.) kérdés: melyik D-aldársav a D-glükársav enantiomerje? kérdés: melyik D-aldársav azonos sztereokémiájú a D-altársavval? All. Alt. Glü. inaktív Man. Gül. Ido. Gal. Tal. 56
57 Monoszacharidok oxidációs reakciói II: perjodátos oxidáció: polihidroxi-vegyületek oxidatív hasítása a még erélyesebb oxidáció bruttó egyenlete: memo: vicinális diolok oxidálhatók, perjódsavval vízben vagy Pb(Ac ) 4 organikus közegben. + I4 2 + I az ox. részletei: memo: -1-1 ciklusos köztitermék I4 I + I aldehidet, ketont vagy savat kapunk az oxidáció végén. - kivitelezhet kvanti. módon, analitika, - minden - kötés hasadásra egy - kötés kialakulása esik. I
58 kérdés: ány mól I 4 oxidálja a glicerint és mik a kapott termékek? glicerinaldehid + 2 I hangyasav hangyasav f ormaldehid kérdés: ány mól I 4 oxidálja a dihidroxi-acetont és mik a kapott termékek? + 2I 4 glicerin + 2 I 4 dihidroxi-aceton formaldehid hangyasav f ormaldehid kérdés: ány mól I 4 oxidálja a glicerinaldehidet és mik a kapott termékek? f ormaldehid szén-dioxid f ormaldehid 58
59 kérdés: ány mól I 4 oxidálja a propán- 1,3-diolt és mik a kapott termékek? I R gyakorló feladatok: ány mól I 4 + I 4 2 kérdés: Mivé oxidál a I 4 egy β-hidroxi-étert? oxidálja és mivé az alábbi vegyületeket? Me Me D-eritróz butane-2,3-diol butane-1,2,3-triol 3,4-dimethoxybutane-1,2-diol I termék: 2 acetaldehid aceton +ecetsav +acetaldehid aceton + 2,3-dimetoxipropánal hangyasav + formaldehid 3,4-dihydroxybutan- 2-one 3-hydroxypentane-2,4-dione (1R,2S)-cyclopentane- 1,2-diol 2-methylpropane-1,2- diol I termék:formaldehid +hangyasav +ecetsav hangyasav +2ecetsav α ω-dialdehid formaldehid +aceton 59
60 Összefoglaló: a D-glükóz oxidációja = N 3 Br 2 / 2 D-glükársav aldársav D-cukorsav 2 D-glükóz??? 2 D-glükonsav aldonsav D-glükuronsav alduronsav = 2 60
61 Monoszacharidok redukciója I.: alditok vagy alditolok a redukció bruttó egyenlete: ( ) n 2 aldóz NaB 4 vagy 2 /Pt ( 2 ) n 2 aldit v. alditol 2 A D-glükóz redukciója: memo: allit, altrit, glücit, mannit, gülit, idit, galaktit, talit 2 D-glükóz 2 NaB 4 2 D-szorbit D-szorbitol (D-glucit) kérdés: ptikailag aktív-e a D-glücit? igen Allit Galaktit inaktív kérdés: Rajzoljon fel optikailag inaktív D-alditot! 61
62 Érdekes alditok: D-mannit 2 D-xilit 2 Madárberkenye (Sorbus aucuparia) cseresznye szilva körte alma moszat alga ondó 2 2 D-glucit L-gulit D-szorbit 2 növényi manna kôrisfa, olajfa platán D-galaktit dulcit 2 2 fogszuvasodás gátló rágógumi Fogszuvasodást okozó baktériumoknak emészthetetlen diabetikus édesítôszer 2 madagaszkári manna szürkehályog 62
63 Monoszacharidok reakciója II. (fenil-hidrazinnal) oszazonok: N N NN 2 N N N 2 + N ( ) n ( ) n 2 aldóz fenil-hidrazin 2 f enil-oszazon mechanizmus: és N hasonlóan viselkedik A A N N 6 5 tautomerizáció N N A N 2 cukorf enilhidrazon N N 6 5 N N N 6 5 cukoroszazon + N NN 2 imino-oxo intermedier 63
64 kérdés: Mi a különbség a D-glükóz és a D-mannóz oszazonjai között? N N 6 5 N N NN NN 2 2 D-glükóz 2 ugyanaz az oszazon, mert 2 epimerek 2 D-mannóz Aldózok láncrövidítése: a Ruff-lebontás Br Fe 2 (S 4 ) tto Ruff (német: ) 2 D-( )-ribóz 2 D-( )-ribóz 2 D-( )-eritróz kérdés: Melyik másik aldopentóz lánclebontása eredményez szintén D-eritrózt? (D-Arabinóz) 64
65 Aldózok lánchosszabbítása: Kiliani-Fischer-szintézis memo: aldóz lánchosszabbítása ciánhidrinen keresztül einrich Kiliani ( ) Emil Fischer ( ) D-( )-eritróz N N 2 (1) Ba() 2 (2) Na/g 2 p D-glicerinaldehid 3 N 2 (1) Ba() 2 (2) Na/g 2 p epimer cianohidrinek (elválaszthatók mert diasztereomerek) memo: a kapott diasztereomerek könnyedén elválaszthatók kérdés: hogyan állítana el L-treózt? epimer γ-aldonolaktonok D-( )-treóz 65
66 D-( )-eritróz kérdés: hogyan döntenénk el egyszeren, hogy melyik aldotetróz melyik? oprtikailag inaktív mezo-borkõsav 2 N 3 válasz: a megfelel két aldársav közül az egyik optikailag inaktív (mezo-borksav), az származik az D-eritrózból, míg a másik forgat, tehát az keletkezett a D-treózból. 2 D-( )-treóz D-(+)-borkõsav opt. aktív α D 15 = +12 o L-(+)-eritróz kérdés: melyik aldotetróz oxidációs terméke lenne az L-borksav? oprtikailag inaktív mezo-borkõsav 2 N 3 2 L-(+)-treóz L-(-)-borkõsav opt. aktív α D 15 = -12 o 66
67 D-aldózok generikus-fája (Kiliani-Fischer-lánchosszabítás, Ruff-láncrövidítés) D-aldohexózok D-(+)-allóz D-(+)-altóz D-(+)-glükóz D-(+)-mannóz D-( )-gülóz D-(+)-idóz D-(+)-galaktóz D-(+)-talóz D-aldopentózok D-( )-ribóz D-( )-arabinóz D-(+)-xilóz D-( )-lixóz D-aldotetrózok 2 2 D-( )-eritróz D-( )-treóz D-aldotrióz 2 D-(+)-glicerinaldehid 67
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
Táptalaj E. coli számára (1000 ml vízben) H 2 O 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen ion 1%
 Az E. coli kémiai összetétele Táptalaj E. coli számára (1000 ml vízben) Na 2 P 4 6,0 g K 2 P 4 3,0 g Glükóz 4,0 g N 4 l 1,0 g MgS 4 0,13g 2 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen
Az E. coli kémiai összetétele Táptalaj E. coli számára (1000 ml vízben) Na 2 P 4 6,0 g K 2 P 4 3,0 g Glükóz 4,0 g N 4 l 1,0 g MgS 4 0,13g 2 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
Táptalaj E. coli számára (1000 ml vízben) H 2 O 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen ion 1%
 Követelmények a Természetes szénvegyületek tárgyból 1. A félév végén az előadás vizsgával zárul. Ez írásbeli és szóbeli részből áll.az irásbeli vizsga eredményes, ha az elért eredmény 50 %-nál jobb. Amennyiben
Követelmények a Természetes szénvegyületek tárgyból 1. A félév végén az előadás vizsgával zárul. Ez írásbeli és szóbeli részből áll.az irásbeli vizsga eredményes, ha az elért eredmény 50 %-nál jobb. Amennyiben
SZÉNHIDRÁTOK (H 2. Elemi összetétel: C, H, O. O) n. - Csoportosítás: Poliszacharidok. Oligoszacharidok. Monoszacharidok
 Szénhidrátok SZÉNIDRÁTK - soportosítás: Elemi összetétel:,, n ( 2 ) n Monoszacharidok (egyszerű szénhidrátok) pl. ribóz, glükóz, fruktóz ligoszacharidok 2 6 egyszerű szénhidrát pl. répacukor, tejcukor
Szénhidrátok SZÉNIDRÁTK - soportosítás: Elemi összetétel:,, n ( 2 ) n Monoszacharidok (egyszerű szénhidrátok) pl. ribóz, glükóz, fruktóz ligoszacharidok 2 6 egyszerű szénhidrát pl. répacukor, tejcukor
A szénhidrátkémia kisszótára:
 A szénhidrátkémia kisszótára: akirális: királis tulajdonággal nem rendelkező molekula anomer -atom: a ciklofélacetál gyűrűben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer
A szénhidrátkémia kisszótára: akirális: királis tulajdonággal nem rendelkező molekula anomer -atom: a ciklofélacetál gyűrűben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Szénhidrátok I. (Carbohydrates)
 sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
Szénhidrátok. Szénhidrátok. Szénhidrátok. Csoportosítás
 Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
A szénhidrátkémia kisszótára:
 A szénhidrátkémia kisszótára: akirális: királis tulajdonággal nem rendelkező molekula anomer -atom: a ciklofélacetál gyűrűben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer
A szénhidrátkémia kisszótára: akirális: királis tulajdonággal nem rendelkező molekula anomer -atom: a ciklofélacetál gyűrűben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer
A szénhidrátkémia kisszótára:
 A szénhidrátkémia kisszótára: akirális: királis tulajdonággal nem rendelkező molekula anomer -atom: a ciklofélacetál gyűrűben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer
A szénhidrátkémia kisszótára: akirális: királis tulajdonággal nem rendelkező molekula anomer -atom: a ciklofélacetál gyűrűben a heteroatom melletti -atom, amelyhez a glikozidos kapcsolódik. antipód: enantiomer
3.6. Szénidrátok szacharidok
 3.6. Szénidrátok szacharidok általános összegképlet: C n (H 2 O) m > a szén hidrátjai elsődleges szerves anyagok mert az élő sejt minden más szerves anyagot a szénhidrátok további átalakításával állít
3.6. Szénidrátok szacharidok általános összegképlet: C n (H 2 O) m > a szén hidrátjai elsődleges szerves anyagok mert az élő sejt minden más szerves anyagot a szénhidrátok további átalakításával állít
SZÉNHIDRÁTOK. 3. Válogasd szét a képleteket aszerint, hogy aldóz, vagy ketózmolekulát ábrázolnak! Írd a fenti táblázat utolsó sorába a betűjeleket!
 funkciós kimutatása molekulák csoport betűjele neve képlete helye 1. Írd a táblázatba a szénhidrátok összegképletét! általános képlet trióz tetróz 2. Mi a különbség az aldózok és a ketózok között? ALDÓZ
funkciós kimutatása molekulák csoport betűjele neve képlete helye 1. Írd a táblázatba a szénhidrátok összegképletét! általános képlet trióz tetróz 2. Mi a különbség az aldózok és a ketózok között? ALDÓZ
Név: Pontszám: / 3 pont. 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
 Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája Készítették: Horváth Márton és Pánczél József Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája Készítették: Horváth Márton és Pánczél József Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
MONOSZACHARIDOK, OLIGO- ÉS POLISZACHARIDOK
 MNSZACAIDK, LIG- ÉS PLISZACAIDK Monoszacharidok nyíltláncú és laktol-gyűrűs szerkezete, mutarotáció. Aldóz-ketóz átalakulás. A monoszacharidok redukciója és oxidációja, cukoralkoholok és cukorsavak. Monoszacharidok
MNSZACAIDK, LIG- ÉS PLISZACAIDK Monoszacharidok nyíltláncú és laktol-gyűrűs szerkezete, mutarotáció. Aldóz-ketóz átalakulás. A monoszacharidok redukciója és oxidációja, cukoralkoholok és cukorsavak. Monoszacharidok
A legfontosabb szénhidrátok a szervezetben és a táplálékokban.
 Orvosi Biokémiai Intézet Semmelweis Egyetem Dr. Komorowicz Erzsébet, Dr. Törőcsik Beáta A legfontosabb szénhidrátok a szervezetben és a táplálékokban. 2017. 03. 27. 2017. 03. 30. A szénhidrátok szerepe:
Orvosi Biokémiai Intézet Semmelweis Egyetem Dr. Komorowicz Erzsébet, Dr. Törőcsik Beáta A legfontosabb szénhidrátok a szervezetben és a táplálékokban. 2017. 03. 27. 2017. 03. 30. A szénhidrátok szerepe:
6. Előadás. Oxovegyületek. Szénhidrátok: monoszacharidok. Szénhidrátszármazékok.
 6. Előadás xovegyületek. Szénhidrátok: monoszacharidok. Szénhidrátszármazékok. 23. xovegyületek ALDEIDEK, KETNK - származtatás aldehid keton Nomenklatura Típusnév: alkánal alkénal alkinal Típusnév: alkánon
6. Előadás xovegyületek. Szénhidrátok: monoszacharidok. Szénhidrátszármazékok. 23. xovegyületek ALDEIDEK, KETNK - származtatás aldehid keton Nomenklatura Típusnév: alkánal alkénal alkinal Típusnév: alkánon
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szabó Dénes Molekulák és reakciók három dimenzióban
 Szabó Dénes Molekulák és reakciók három dimenzióban Alkímia ma, 2012. április 19. Egy kis tudománytörténet -O azonos kémiai szerkezet -O Scheele (1769) -O különböző tulajdonságok -O Kestner (1822) borkősav
Szabó Dénes Molekulák és reakciók három dimenzióban Alkímia ma, 2012. április 19. Egy kis tudománytörténet -O azonos kémiai szerkezet -O Scheele (1769) -O különböző tulajdonságok -O Kestner (1822) borkősav
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
OXOVEGYÜLETEK. Levezetés. Elnevezés O CH 2. O R C H aldehid. O R C R' keton. Aldehidek. propán. karbaldehid CH 3 CH 2 CH 2 CH O. butánal butiraldehid
 XVEGYÜLETEK Levezetés 2 aldehid ' keton Elnevezés Aldehidek propán karbaldehid 3 2 2 butánal butiraldehid oxo karbonil formil Példák 3 3 2 metanal etanal propanal formaldehid acetaldehid propionaldehid
XVEGYÜLETEK Levezetés 2 aldehid ' keton Elnevezés Aldehidek propán karbaldehid 3 2 2 butánal butiraldehid oxo karbonil formil Példák 3 3 2 metanal etanal propanal formaldehid acetaldehid propionaldehid
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
SZÉNHIDRÁTOK. Biológiai szempontból legjelentősebb a hat szénatomos szőlőcukor (glükóz) és gyümölcscukor(fruktóz),
 SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
Javító vizsga követelményei kémia tantárgyból augusztus osztály
 Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Bevezetés a biokémiába fogorvostan hallgatóknak - Munkafüzet 2. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak - Munkafüzet 2. hét Sztereokémia (Bevezetés a biokémiába gyakorlatok, 4-6. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás,
Bevezetés a biokémiába fogorvostan hallgatóknak - Munkafüzet 2. hét Sztereokémia (Bevezetés a biokémiába gyakorlatok, 4-6. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás,
IX. Szénhidrátok - (Polihidroxi-aldehidek és ketonok)
 IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
R-OH H + O H O H OH H O H H OH O H OH O H OH H H
 3. Előadás ligo- és poliszacharidok Diszacharidok Definició: Két monoszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésben résztvevő C-atomok
3. Előadás ligo- és poliszacharidok Diszacharidok Definició: Két monoszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésben résztvevő C-atomok
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Sztereokémia, királis molekulák: (királis univerzum, tükörképi világ?) memo: a földi élet királis elemek sokasága!
 Sztereokémia, királis molekulák: (királis univerzum, tükörképi világ?) memo: a földi élet királis elemek sokasága! (pl. a földön az L-aminosavak vannak túlnyomó többségben. - Az enantiomer szelekció, módját
Sztereokémia, királis molekulák: (királis univerzum, tükörképi világ?) memo: a földi élet királis elemek sokasága! (pl. a földön az L-aminosavak vannak túlnyomó többségben. - Az enantiomer szelekció, módját
O 2 R-H 2 C-OH R-H 2 C-O-CH 2 -R R-HC=O
 Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
1. feladat (3 pont) Az 1,2-dibrómetán főként az anti-periplanáris konformációban létezik, így A C-Br dipólok kioltják egymást, a molekula apoláris.
 1. feladat (3 pont) Az 1,2-dibrómetán apoláris molekula. Az etilénglikol (etán-1,2-diol) molekulának azonban mérhető dipólusmomentuma van. Mi ennek a magyarázata? Az 1,2-dibrómetán főként az anti-periplanáris
1. feladat (3 pont) Az 1,2-dibrómetán apoláris molekula. Az etilénglikol (etán-1,2-diol) molekulának azonban mérhető dipólusmomentuma van. Mi ennek a magyarázata? Az 1,2-dibrómetán főként az anti-periplanáris
Aromás vegyületek II. 4. előadás
 Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
R-OH H + O H O H OH H O H H OH O H OH O H OH H H
 3. Előadás ligo- és poliszacharidok Diszacharidok Defiició: Két mooszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésbe résztvevő C-atomok
3. Előadás ligo- és poliszacharidok Diszacharidok Defiició: Két mooszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésbe résztvevő C-atomok
H 3 C CH 2 CH 2 CH 3
 3. Előadás Konstitució, konfiguráció, konformáció. Az izoméria fajtái. A sztereoizoméria. A kettős kötéshez kapcsolódó izoméria jelenségek. Az optikai izoméria. Az optikai aktivitás és mérése. 9. Konstitúció,
3. Előadás Konstitució, konfiguráció, konformáció. Az izoméria fajtái. A sztereoizoméria. A kettős kötéshez kapcsolódó izoméria jelenségek. Az optikai izoméria. Az optikai aktivitás és mérése. 9. Konstitúció,
OXOVEGYÜLETEK. Levezetés. Elnevezés O CH 2. O R C R' keton. O R C H aldehid. funkciós csoportok O. O CH oxocsoport karbonilcsoport formilcsoport
 XVEGYÜLETEK Levezetés 2 aldehid ' keton funkciós csoportok oxocsoport karbonilcsoport formilcsoport Elnevezés Aldehidek nyíltláncú (racionális név: alkánal) 3 2 2 butánal butiraldehid gyűrűs (cikloalkánkarbaldehid)
XVEGYÜLETEK Levezetés 2 aldehid ' keton funkciós csoportok oxocsoport karbonilcsoport formilcsoport Elnevezés Aldehidek nyíltláncú (racionális név: alkánal) 3 2 2 butánal butiraldehid gyűrűs (cikloalkánkarbaldehid)
SZERVES KÉMIA: BEVEZETÉS SZTEREOKÉMIA. Debreceni Egyetem ÁOK Orvosi Vegytani Intézet
 SZERVES KÉMIA: BEVEZETÉS SZTEREOKÉMIA Debreceni Egyetem ÁOK Orvosi Vegytani Intézet www.medchem.unideb.hu A szén allotróp módusulatai a) gyémánt b) grafit c) amorf szén (nincs ábrázolva) A grafénő egyetlen
SZERVES KÉMIA: BEVEZETÉS SZTEREOKÉMIA Debreceni Egyetem ÁOK Orvosi Vegytani Intézet www.medchem.unideb.hu A szén allotróp módusulatai a) gyémánt b) grafit c) amorf szén (nincs ábrázolva) A grafénő egyetlen
KARBONIL-VEGY. aldehidek. ketonok O C O. muszkon (pézsmaszarvas)
 KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
SZERVES KÉMIAI REAKCIÓEGYENLETEK
 SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
Aldehidek, ketonok és kinonok
 Aldehidek, ketonok és kinonok 3 3 3 innamomum camphora Agócs Attila rvosi Kémia 2018 kámfor Tanulási célok: Az oxovegyületek elnevezése és fizikai tulajdonságai Nukleofil addíció, az oxovegyületek legfontosabb
Aldehidek, ketonok és kinonok 3 3 3 innamomum camphora Agócs Attila rvosi Kémia 2018 kámfor Tanulási célok: Az oxovegyületek elnevezése és fizikai tulajdonságai Nukleofil addíció, az oxovegyületek legfontosabb
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
7. évfolyam kémia osztályozó- és pótvizsga követelményei Témakörök: 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2.
 7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
Helyettesített karbonsavak
 elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
Di-, Oligo és Poliszacharidok
 Di-, ligo és Poliszacharidok A méz kb. 82%-a szénhidrát. Monoszacharidok közül fruktózt (38.2%) és glükózt (31%), diszacharidok közül (~9%) szacharózt, maltózt, izomaltózt, maltulózt, turanózt és kojibiózt
Di-, ligo és Poliszacharidok A méz kb. 82%-a szénhidrát. Monoszacharidok közül fruktózt (38.2%) és glükózt (31%), diszacharidok közül (~9%) szacharózt, maltózt, izomaltózt, maltulózt, turanózt és kojibiózt
Sztereokémia, királis molekulák: (királis univerzum, tükörképi világ?) Izomerek felosztása
 Sztereokémia, királis molekulák: (királis univerzum, tükörképi világ?) memo: a földi élet királis! Pl. a földön az L-aminosavak vannak túlnyomó többségben. - Az enantiomer szelekció, módját idejét és okát
Sztereokémia, királis molekulák: (királis univerzum, tükörképi világ?) memo: a földi élet királis! Pl. a földön az L-aminosavak vannak túlnyomó többségben. - Az enantiomer szelekció, módját idejét és okát
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
O S O. a konfiguráció nem változik O C CH 3 O
 () ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
() ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
Konstitúció, izoméria, konfiguráció, konformáció
 Konstitúció, izoméria, konfiguráció, konformáció Konstitúció: A molekula színezett gráffal leírható szerkezete De: a konstitúciós képlet kifejezhet egyéb információt is: cisz-transz izomériát (Z - zusammen,
Konstitúció, izoméria, konfiguráció, konformáció Konstitúció: A molekula színezett gráffal leírható szerkezete De: a konstitúciós képlet kifejezhet egyéb információt is: cisz-transz izomériát (Z - zusammen,
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
Szerves Kémia. Farmakológus szakasszisztens képzés 2012/2013 ősz
 Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Laboratóriumi technikus laboratóriumi technikus Drog és toxikológiai
 A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
Polihidroxi-aldehidek vagy -ketonok, vagy ezek származékai. Monoszacharid: polihidroxi-keton vagy -aldehid
 Szénhidrátok Polihidroxi-aldehidek vagy -ketonok, vagy ezek származékai. Általános képletük: ( 2 ) n ahol n 3 Monoszacharid: polihidroxi-keton vagy -aldehid ligoszacharid: 2 10 monoszacharid glikozidkötéssel
Szénhidrátok Polihidroxi-aldehidek vagy -ketonok, vagy ezek származékai. Általános képletük: ( 2 ) n ahol n 3 Monoszacharid: polihidroxi-keton vagy -aldehid ligoszacharid: 2 10 monoszacharid glikozidkötéssel
hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) olajsav (cisz-9 oktadecénsav) néhány, állatokban előforduló zsírsav
 Lipidek: zsírsavak hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) sztearinsav (oktadekánsav) olajsav (cisz-9 oktadecénsav) Szénatomszám Kettős kötések száma néhány, állatokban
Lipidek: zsírsavak hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) sztearinsav (oktadekánsav) olajsav (cisz-9 oktadecénsav) Szénatomszám Kettős kötések száma néhány, állatokban
Biokémia 1. Béres Csilla
 Biokémia 1 Béres Csilla Élő szervezetek kémiai összetétele Szénvegyületek Időben és térben rendezett folyamatok Sejt az egység Biogén elemek: C, H, O, N, P Biofil elemek: Na, K, Ca, Mg, Fe, Cu, Ni, Zn,
Biokémia 1 Béres Csilla Élő szervezetek kémiai összetétele Szénvegyületek Időben és térben rendezett folyamatok Sejt az egység Biogén elemek: C, H, O, N, P Biofil elemek: Na, K, Ca, Mg, Fe, Cu, Ni, Zn,
Kémia fogorvostan hallgatóknak Munkafüzet 14. hét
 Kémia fogorvostan hallgatóknak Munkafüzet 14. hét Szerves anyagok vizsgálata III. (177-180. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás, Nagy Veronika, Radó-Turcsi
Kémia fogorvostan hallgatóknak Munkafüzet 14. hét Szerves anyagok vizsgálata III. (177-180. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás, Nagy Veronika, Radó-Turcsi
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Cukorkémia = Szénhidrátkémia
 Cukorkémia = Szénhidrátkémia Cukrok fontossága: A Földön évente 200 milliárd tonna biomassza képződik, amelynek 75%-a szénhidrát, de ennek csak 3%-át hasznosítják. Somsák, L.; Vágvölgyiné Tóth, M.: Az
Cukorkémia = Szénhidrátkémia Cukrok fontossága: A Földön évente 200 milliárd tonna biomassza képződik, amelynek 75%-a szénhidrát, de ennek csak 3%-át hasznosítják. Somsák, L.; Vágvölgyiné Tóth, M.: Az
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
2 TULAJDONSÁGOK ANYAGI HALMAZOK SZINTJÉN
 1 Sztereoszelektív szintézisek 2 TULAJDONSÁGOK ANYAGI HALMAZOK SZINTJÉN 2.3 Abszolút konfiguráció Az 1.2.2 fejezetben már tárgyaltuk a sztereokémia alapvető fogalmait, amelyek összefüggésben állnak egy
1 Sztereoszelektív szintézisek 2 TULAJDONSÁGOK ANYAGI HALMAZOK SZINTJÉN 2.3 Abszolút konfiguráció Az 1.2.2 fejezetben már tárgyaltuk a sztereokémia alapvető fogalmait, amelyek összefüggésben állnak egy
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Részletes tematika: I. Félév: 1. Hét (4 óra): 2. hét (4 óra): 3. hét (4 óra): 4. hét (4 óra):
 Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások
 ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
Curie Kémia Emlékverseny 10. évfolyam országos döntő 2018/2019. A feladatok megoldásához csak periódusos rendszer és zsebszámológép használható!
 A feladatokat írta: Kódszám: Horváth Balázs, Szeged Lektorálta: 2019. május 11. Széchenyi Gábor, Budapest Curie Kémia Emlékverseny 10. évfolyam országos döntő 2018/2019. A feladatok megoldásához csak periódusos
A feladatokat írta: Kódszám: Horváth Balázs, Szeged Lektorálta: 2019. május 11. Széchenyi Gábor, Budapest Curie Kémia Emlékverseny 10. évfolyam országos döntő 2018/2019. A feladatok megoldásához csak periódusos
H 3 CH 2 C H 2 N HS CH 3 H CH 3 HO CH 2 CH 3. CHBr 2 CH 2 OH SCH H 3 CH 2 CH 3 H 3 C OH NH 2 OH CH 2CH 3 (R) (R) (S) O CH 3 SCH 3 SCH
 Állapítsa meg az alábbi modellek kiralitáscentrumának konfigurációját! (A megoldások a képletek alatt zárójelben találhatók.) Az első három modellen bemutattuk egy-egy lehetséges ischer-projekció elkészítését.
Állapítsa meg az alábbi modellek kiralitáscentrumának konfigurációját! (A megoldások a képletek alatt zárójelben találhatók.) Az első három modellen bemutattuk egy-egy lehetséges ischer-projekció elkészítését.
Budapest, augusztus 22. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
2. SZÉNHIDRÁTOK 2.1. A legfontosabb D-sorbeli aldózok és ketózok
 2. SZÉNIDRÁTK 2.0. Bevezetés A szénhidrátok a Földön található szerves anyagok közül a legnagyobb mennyiségben fordulnak elı. Szerepük egyrészt az élı szervezetek energiaháztartásában van. A növények a
2. SZÉNIDRÁTK 2.0. Bevezetés A szénhidrátok a Földön található szerves anyagok közül a legnagyobb mennyiségben fordulnak elı. Szerepük egyrészt az élı szervezetek energiaháztartásában van. A növények a
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Kémia fogorvostan hallgatóknak Munkafüzet 13. hét
 Kémia fogorvostan hallgatóknak Munkafüzet 13. hét Szerves anyagok vizsgálata II. (174-176. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás, Nagy Veronika, Radó-Turcsi
Kémia fogorvostan hallgatóknak Munkafüzet 13. hét Szerves anyagok vizsgálata II. (174-176. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás, Nagy Veronika, Radó-Turcsi
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
Cikloalkánok és származékaik konformációja
 1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
Szerves Kémia II. Dr. Patonay Tamás egyetemi tanár E 405 Tel:
 Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
A szén tetraéderes vegyérték-orientációja (van t Hoff, Le Bel, 1874)
 A szén tetraéderes vegyérték-orientációja (van t off, Le Bel, 874) Perspektivikus ábrázolásmód: a központi szénatomtól indulva vonal a papír síkjában halad (ezek az ábrán az egyenletes vastagságúak), egy
A szén tetraéderes vegyérték-orientációja (van t off, Le Bel, 874) Perspektivikus ábrázolásmód: a központi szénatomtól indulva vonal a papír síkjában halad (ezek az ábrán az egyenletes vastagságúak), egy
A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok)
 SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
Szemináriumi feladatok (kiegészítés) I. félév
 Szemináriumi feladatok (kiegészítés) I. félév I. Szeminárium 1. Rajzolja fel az alábbi ion π-molekulapályáit: N ány centrumú a delokalizált rendszer? ány elektron építi fel a delokalizált rendszert? ány
Szemináriumi feladatok (kiegészítés) I. félév I. Szeminárium 1. Rajzolja fel az alábbi ion π-molekulapályáit: N ány centrumú a delokalizált rendszer? ány elektron építi fel a delokalizált rendszert? ány
3. előadás: A víz szerepe az élő szervezetekben
 3. előadás: A víz szerepe az élő szervezetekben A víz a földi élet alapja A víz az élet biológiai közege a Földön Az egyetlen gyakori molekula, mely midhárom halmazállapotban jelen van Minden élő szervezetnek
3. előadás: A víz szerepe az élő szervezetekben A víz a földi élet alapja A víz az élet biológiai közege a Földön Az egyetlen gyakori molekula, mely midhárom halmazállapotban jelen van Minden élő szervezetnek
Sejtek a térben: a sejtközi térben lévő fehérvértestek szolgálat közben. vörösvértest
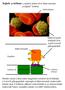 Sejtek a térben: a sejtközi térben lévő fehérvértestek szolgálat közben. vörösvértest fehérvérsejtek fehérvérsejtek felületén lévő szialil LewisX glikopeptidek Kapilláris kapiláris fal endotél sejtek szelektin
Sejtek a térben: a sejtközi térben lévő fehérvértestek szolgálat közben. vörösvértest fehérvérsejtek fehérvérsejtek felületén lévő szialil LewisX glikopeptidek Kapilláris kapiláris fal endotél sejtek szelektin
1. Bevezetés. Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei
 1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
Javítóvizsga feladatok 9.osztály
 Javítóvizsga feladatok 9.osztály 1. Hány darab elemi részecske van 1 db 13 C atomban db p + db n 0 db e - 2. 10 23 db 13 C atomban db p + db n 0 db e - 0,5 mol 13 C atomban db p + db n 0 db e - 3,25 g
Javítóvizsga feladatok 9.osztály 1. Hány darab elemi részecske van 1 db 13 C atomban db p + db n 0 db e - 2. 10 23 db 13 C atomban db p + db n 0 db e - 0,5 mol 13 C atomban db p + db n 0 db e - 3,25 g
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll.
 KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
