Ph.D. értekezés. Készítette: Dr. Halász József
|
|
|
- Hanna Juhászné
- 7 évvel ezelőtt
- Látták:
Átírás
1 A glukokortikoid hipofunkció hatása az agresszióra és a társuló zavarokra - magatartási, neuronális és vegetatív változások Ph.D. értekezés Készítette: Dr. Halász József Témavezeto: Dr. Haller József, Ph.D. Magyar Tudományos Akadémia Kísérleti Orvostudományi Kutatóintézet, 2003 Semmelweis Egyetem Doktori Iskola Idegtudományok Doktori Iskola (Multidiszciplináris orvostudományok) Idegtudományok Program Doktori Iskola vezetoje: Programvezeto: Dr. Réthelyi Miklós, egyetemi tanár Dr. Palkovits Miklós, egyetemi tanár Szigorlati Bizottság: Hivatalos Bírálók: Elnök: Dr. Halász Béla akadémikus Dr. Bárdos György, MTA doktora Tagok: Dr. Bagdy György, MTA doktora Dr. Kabai Péter, kandidátus Dr. Nagy György, MTA doktora 1
2 Tartalomjegyzék Rövidítések jegyzéke 4 1. Bevezetés 5 2. Irodalmi háttér A kóros agresszivitás Az agresszió laboratóriumi vizsgálata Az agresszió centrális szabályozása Az agresszió szabályozásában szerepet játszó agyterületek Az agresszió neurofarmakológiája Neuronális aktiváció agresszióban Az agresszió hormonális szabályozása A glukokortikoid szint szabályozása és hatása az agresszivitásra A glukokortikoid elválasztás szabályozása A glukokortikoidok celluláris hatásmechanizmusa Megváltozott glukokortikoid szintek neurális következményei A glukokortikoidok hatása az agresszióra Alacsony glukokortikoid szintekhez társuló egyéb magatartási zavarok A vegetatív reaktivitás és a patológiás agresszió Célkituzések Anyagok és módszerek Állatok és tartási körülmények A kísérletek során használt anyagok Kortikoszteron pótlás, kortikoszteron kezelés Buspiron A kísérletek során használt egyéb anyagok Mutéti beavatkozások Adrenalektómia és kortikoszteron tabletta beültetés Hipotalamikus elektród beültetése Telemetriás transzmitter beültetése Magatartási tesztek Rezidens-betolakodó teszt Hipotalamikus ingerléssel kiváltott agresszió Szociális interakció teszt Megemelt keresztpalló teszt Szövettani feldolgozás Perfúzió és immuncitokémia c-fos pozitív sejtek analízise Rádiótelemetriás rendszer Hormonmérés Kísérleti protokollok Statisztikai kiértékelés Eredmények Glukokortikoid hipofunkció hatása az agresszív viselkedésre és az agresszív viselkedés szabályozásában részt vevo agyterületek neuronális aktivitására. Patológiás agresszió során fellépo aktivitásmintázat Neuronális aktiváció territoriális agresszió során Neuronális aktiváció hipotalamikus ingerléssel kiváltott agresszió során Neuronális aktiváció glukokortikoid hipofunkció során megjeleno agresszióban Glukokortikoid hipofunkció hatása a szorongásra és a buspiron hatékonyságára Alacsony glukokortikoid szint hatása a szorongásra. 74 2
3 Glukokortikoid hipofunkció hatása a buspiron szorongásoldó hatékonyságára Glukokortikoid hipofunkció hatása a szívfrekvencia és a motilitás ala kulására. Vegetatív paraméterek változása különbözo kihívások során Glukokortikoid hipofunkció hatása a napi ritmus alakulására A magatartási tesztek során mutatott vegetatív változások glukokortikoid hipofunkcióban Megbeszélés A territoriális agresszió során fellépo neuronális aktiváció A hipotalamikus ingerléssel kiváltott agresszió során fellépo neuronális aktiváció A glukokortikoid hipofunkcióban kialakuló agresszió A glukokortikoid hipofunkcióban kialakuló szorongás. A buspiron hatékonyságának megváltozása Glukokortikoid hipofunkció és autonóm aktivitás Köszönetnyilvánítás Irodalomjegyzék Saját közlemények jegyzéke Összefoglalás Summary 131 3
4 Rövidítések jegyzéke ACTH adrenokortikotróp hormon ADX r AVP BNST CC CeA CRH DR GR HAA HPA im. ip. LC LS MD MeA MR PAG PC PVN PTSD mellékvese eltávolítás (adrenalektómia) + kortikoszteron tabletta beültetés arginin-vazopresszin bed nucleus stria terminalis cinguláris kéreg centrális amigdala kortikotropin (ACTH) felszabadulást serkento hormon (corticotropin releasing hormone) dorzális raphe glukokortikoid receptor hipotalamikus támadási zóna (hypothalamic attack area) hipotalamusz-hipofízis-mellékvesekéreg (hypothalamus-pituitary-adrenal) intramuszkuláris intraperitoneális locus coeruleus laterális szeptum mediodorzális talamikus mag mediális amigdala mineralokortikoid receptor középagyi centrális (periakveduktális) szürkeállomány (periaqueductal gray) piriform kéreg hipotalamikus paraventrikuláris mag poszttraumás stressz zavar (posttraumatic stress disorder) 4
5 1. Bevezetés A patológiás agressziót orvos-biológiai értelemben a normális agressziótól elsosorban az adaptivitás hiánya különbözteti meg. A 90-es évek második felétol kezdodoen számos pszichiátriai tanulmány kezdetben még a szukebb szakmai közvélemény számára is meglepo kapcsolatot mutatott ki a glukokortikoid hormonok szintje és a patológiásan agresszív magatartás megjelenése között. A patológiás magatartást mutató populációkban jellegzetesen alacsony alapszinteket és a kihívásokra adott glukokortikoid szint kisebb mértéku emelkedését jelezte párhuzamosan több kutatócsoport, ezt az eltérést nevezzük glukokortikoid hipofunkciónak*. A hipotalamusz-hipofízis-mellékvesekéreg rendszer aktiválódása alapveto jelentoségu az egyed külso és belso kihívásokra adott, a homeosztatikus egyensúly visszaállítására irányuló válaszreakcióiban. A rendszer (a kiváltó ágenstol esetleg független) túlzott mértéku aktiválódása hosszú távú változásokat indukálhat, amelyek az egyed számára súlyosabb következményekkel járhatnak, mint a kiváltó esemény maga (pl. depresszió). A rendszer megváltozott muködése következtében kialakuló alacsony és nem reaktív glukokortikoid szintek, mint a stresszel kapcsolatos önálló kóroki tényezo jelentosége csak az utóbbi években került felismerésre. A glukokortikoidok számos jól ismert endokrin, metabolikus, immunszuppresszív hatásukon túl a kognitív minosítések és különbözo magatartások, köztük az agresszió és a szorongás modulátorai is. Kísérletesen eloidézett glukokortikoid hipofunkcióban patológiás agressziómintázat jelenik meg, mely megszüntetheto a glukokortikoid válasz helyreállításával. Ez a glukokortikoid-függo patológiás agresszió képezi a disszertáció fo elemét. A leírt viselkedésmintázat az elso olyan állatkísérletes modellje a társadalomban számos problémát jelento kóros agresszivitásnak, amely mind fenomenológiai, mind hormonális analógiára épül. Az általunk végzett vizsgálatok megpróbálnak rávilágítani az ilyen endokrin háttérre épülo patológiás magatartás idegrendszeri hátterére, valamint vizsgáltuk viszonyát olyan pszichikai és autonóm rendellenességekkel, amelyeket patológiásan agresszív embereknél megfigyeltek. * A glukokortikoid hipofunkció elnevezés tartósan alacsony nyugalmi glukokortikoid szinteket jelöl, és ezzel egyidejuleg a kihívásokra adott csökkent reaktivitást. Ez a funkcionális eltérés endorin terminológiával nehezen körülírható, humán leírásokban a hipokortizolizmus elnevezést vezették be 2000-ben 121. Ennek megfeleloen laboratóriumi rágcsálókban hipokortikoszteronizmus, illetve az analógia elnevezésére hipoglukokortikoidizmus elnevezést lehetne használni, azonban erre nincs irodalmi utalás, és meglehetosen bonyolult nevezéktannak tunik. A disszertáció során ezt az endokrin eltérést modelleztük, és a glukokortikoid hipofunkció terminológiát végig ilyen értelemben használjuk. 5
6 2. Irodalmi háttér 2.1. A kóros agresszivitás Az agresszió összetett társadalmi-biológiai jelenség, vizsgálatának számos szempontja lehetséges. Az irodalomban fellelheto nagy számú meghatározás közül kiemelünk egy etológiai és egy pszichológiai megközelítést. Egy etológiai szemléletu megfogalmazás szerint az agresszió az azonos fajú egyedek közötti, a korlátozott eroforrások (terület, táplálék, szaporodási lehetoség) megszerzésére irányuló magatartás 66. Bár a fenti megközelítés alapjaiban tökéletesen leírja az emberi társadalomban megjeleno agresszív viselkedést is, az ott megjeleno viselkedés kialakulása motiváció szempontjából lényegesen árnyaltabb lehet. Hárdi pszichológiai jellegu megfogalmazása szerint agresszióról beszélünk támadó jellegu magatartás, ellenséges - legtöbbször feszültséggel járó - belso rezdületek, élmények jelentkezésekor, amelyek irányulhatnak a külvilágra, vagy befelé az átélore magára; lehetnek tudatosak vagy tudattalanok, megmutatkozhatnak közvetlenül vagy közvetve, akár átalakult formában is (például elfojtott agresszióból származó szorongásban, testi tünetekben) 118. A fenti definíciók közül az elso jóval általánosabb és az agresszió lényegét teljesebben tükrözi, a második viszont felhívja a figyelmet az emberi magatartások lényegesen összetettebb mivoltára. A disszertáció során levont párhuzamok és következtetések a neurobiológiai szabályozás közös elemeire kívánják felhívni a figyelmet, nem a teljes, társadalmi környezettol nehezen elvonatkoztatható jelenségekre kívánnak magyarázatot adni. Az agresszivitás alapvetoen adaptív magatartás, a szerepe különösen fontos az egyén túlélése szempontjából a változó környezeti kihívásokkal szemben. Számos olyan emberi agresszióforma létezik, amelyet a társadalom legalizál (valamilyen mértékben mindenkinél megnyilvánulnak) és ezeknek az általános szemlélet pozitív és negatív jelentoséget is tulajdonít (érdekérvényesítés, karrier, sportversenyek és többek között a háború is). A kóros, patológiás agressziót alapvetoen a minden fajra jellemzo normális agressziótól az adaptivitás hiánya különíti el 195. Orvostudományi szempontból a DSM- IV állásfoglalásának megfeleloen kóros agresszivitásról akkor beszélünk, ha az egyénnek és/vagy környezetének életvitelében ez problémát okoz 9. Számos pszichiátriai-neurológiai betegségben jelenik meg a kóros agresszivitás, ezek egyrészt az agresszió szempontjából kulcsfontosságú területekre lokalizálódó elváltozások 6
7 következményei lehetnek (pl. a frontális kéregben megjeleno sérülés, vagy a temporális lebenyt érinto fokális epileptiform elváltozás), de lehetnek kevésbé lokalizáltak is (pl. egyéb pszichiátriai eltérésekhez társuló - pszichotikus, mániás állapotok; esetleg súlyos anyagcserezavarok, mint a hipoxia és hipoglikémia) (1. táblázat) 11,135, táblázat. Kóros agresszivitással járó állapotok. Az agresszió fokális okai Hipotalamusz Craniopharingeoma Astrocytoma Temporális lebeny / amigdala Temporális lebeny epilepszia Meziális temporális szklerózis Vaszkuláris malformáció Glioma Traumatikus sérülés Orbitofrontális kéreg / szeptum Traumatikus sérülés Arteria comm. ant. aneurizma Meningeoma Herpes simplex encephalitis Az agresszió multifokális / kevéssé lokalizált okai Pszichiátriai állapotok (szorongás, mánia, pszichózis) Endokrin zavarok (gonadok, mellékvesekéreg, pajzsmirigy, hipoglikémia) Demencia (Alzheimer, Pick, vaszkuláris) Mozgászavarok (Gilles de la Tourette szindróma, Wilson betegség, Huntington kór) Alvászavarok (paraszomniák) Elektrolit zavarok (elsosorban hiper, hiponatrémia) Hipoxia (elektrolit zavarokhoz hasonlóan delíriumot okozhat) Gyógyszerek és kábítószerek (alkohol, kokain, amfetamin, antidepresszánsok, opiátok, anxiolitikumok) Táplálkozási faktorok (B1, B6, B12, fólsav hiány) Mérgezések (higany, ólom, mangán, arzén, organofoszfát) A DSM-IV azonban számon tart olyan elváltozásokat is, amelyeknél ismert organikus eltérés nélkül, a kóros agresszivitás vezeto tünetként szerepel. Ide sorolhatóak a felnott korban diagnosztizálandó antiszociális személyiségzavar, ismétlodo explozív zavar, a gyermek-tinédzser korban megjeleno viselkedési, oppozíciós és diszruptív zavarok. Ezekben a betegségekben megváltozik a hipotalamusz-hipofízis-mellékvesekéreg rendszer aktivitása 186,290,293, a keringésben levo szabad glukokortikoid szint alacsonyabb, a különbözo kihívásokra adott reaktivitása lecsökken; ráadásul a fennálló agresszivitással fordított korrelációt mutat. Az alacsony glukokortikoid szint és a kóros agresszivitás kapcsolatának megértése érdekében egy állatkísérletes modellrendszerben, hím Wistar patkányokon vizsgáltuk a glukokortikoidok és az agresszió kapcsolatát. Eloször ismertetjük az agresszió vizsgálatának lehetséges állatkísérletes laboratóriumi módszereit, az agresszív viselkedés agyi szervezodését, majd a glukokortikoidok elválasztásának szabályozását. 7
8 2.2. Az agresszió laboratóriumi vizsgálata A kórosan agresszív magatartás laboratóriumi modellezése során két szempontnak kiemelt jelentosége van. Eloször is, a humán agresszió megjelenési formái számos esetben nem jelentkeznek laboratóriumi rágcsálókban (és egyéb állatokban sem), így azokat modellezni sem lehetséges (pl. a verbális agresszió) 111,281. Másodszor, az állati és humán agresszió összehasonlításakor a direkt fizikai sérülés okozása embereknél már patológiásnak számíthat, míg az állati szocializáció természetes eleme 6. Az agresszió megjelenése idoben elszórt, az állatok viselkedésének 2-10%-át teszi ki. A laboratóriumban alkalmazott vizsgálómódszerek mindegyike szinkronizálja az agresszív magatartást, és a viszonylag rövid (5 perces 1 órás) vizsgálati periódusban nagy valószínuséguvé teszi az agresszív viselkedés megjelenését. Az alábbiakban megemlítjük azokat a modelleket, amelyek a leginkább használatosak a laboratóriumi agressziókutatásban 39,195, Territoriális agresszió (egyedül vagy nosténnyel tartott hím saját területére egy idegen hím behelyezése). 2. Ragadozói agresszió (patkány vizsgálata esetén az egér, illetve béka megtámadása, amit szukebb értelemben nem tekintünk agressziónak). 3. Kompetíciós agresszió (éheztetés után a közös területre helyezett állatok étel behelyezésére mutatott versengo-agresszív magatartása). 4. Elektromos sokk indukálta agresszió (fájdalmas elektromos ingerekre fellépo, speciális agresszióforma). 5. Anyai agresszió (laktációs periódusban az utódok védelme idegen hímmel vagy nosténnyel szemben). 6. Defenzív agresszió (élet védelme ragadozóval, vagy jelentos túlerovel szemben mind nosténynél, mind hímnél), egyes szerzok az anyai agressziót a defenzív agresszióhoz sorolják. 7. Hipotalamikus agresszió (a hipotalamikus támadási zóna elektromos ingerlésével kiváltott agresszió). 8. Agyi lézióval kiváltott agresszió (pl. a szeptum roncsolásával). 8
9 9. Farmakonok (pl. apomorfin) indukálta agresszió (rendszerint territoriális környezetben). A ragadozói, kompetíciós, illetve sokk indukálta agresszió vizsgálata patkányban már csak elvétve fordul elo; az agyi lézióval kiváltott agresszió és farmakonok indukálta agresszió vizsgálata is kevéssé elterjedt. A defenzív agresszió vizsgálata elsosorban a szociális stressz következtében kialakuló magatartási rendellenességeknek (szorongás, depresszió) vizsgálatához társul 36,40,85. Kísérleteinkben elsodlegesen a territoriális agresszió során mutatott viselkedést vizsgáltuk. Az agresszióval kapcsolatos agyi struktúrák aktivitásának elemzése során lehetoségünk nyílt technikailag viszonylag nehezen kivitelezheto kísérletek elvégzésére (a hipotalamikus stimulációval kiváltott agresszió vizsgálatára a világon csak néhány laboratóriumban van lehetoség). A hipotalamikus támadási zóna elektromos ingerlésével kiváltott agresszió neurofarmakológiai háttere a territoriális agresszióhoz meglehetosen hasonló 270. A továbbiakban ismertetett irodalmi adatok a territoriális (és a hipotalamikus) agresszió szabályozására vonatkoznak, és nem feltétlenül egyeznek meg más agresszióformák (pl. anyai agresszió, elektromos sokk indukálta agresszió) szabályozó mechanizmusaival Az agresszió centrális szabályozása Az agresszív magatartás szabályozása a központi idegrendszerben alapvetoen három szinten zajlik, és különbözo neurofarmakológiai manipulációk is ezeken a szinteken tudnak beavatkozni: (1) agressziót provokáló jelzések szenzoros feldolgozása, (2) a különbözo magatartási elemek motoros végrehajtása, (3) központi szabályozás az agresszív magatartáselemek kifejezésének beindítására, kivitelezésére, és leállítására 193. Ebben a fejezetben elsosorban a harmadik pontról lesz szó Az agresszió szabályozásában szerepet játszó agyterületek Az agresszív magatartás szabályozását egy kissé sematikus, de az irodalmi álláspontok többségét tükrözo vezérelv mentén ismertetjük. Az agresszió szabályozásának központi eleme egy döntoen egyirányú információ-áramlást közvetíto rendszer, melynek elemei a mediális amigdala, a hipotalamikus támadási zóna és a középagyi centrális szürkeállomány. A rendszer elemeinek muködését a limbikus rendszerhez tartozó számos más (elsosorban gátló) agyterület modulálja. 9
10 Mediális amigdala A mediális amigdala elsodleges szerepe a szociális kontaktusokban alapveto szerepet játszó szenzoros modalitások (legfoképpen az olfaktorikus bemenetek) integrálása és a hipotalamusz felé továbbítása 7,51,220,255. A mediális amigdala a centrális amigdala magot leszámítva az összes azonos oldali amigdala magból (elsosorban anterior, poszterior kortikális; laterális; bazális; periamigdaloid kéreg; elülso amigdaloid terület) kap rostokat, és az ellenoldali mediális amigdala is beidegzi 51,223. Direkt bemenetet kap az olfaktoros rendszerbol, illetve a frontális és temporo-parietális kérgi területekrol 7,255. A boséges feldolgozott szenzoros információ a komplex szociális magatartások organizációjában játszik kulcsfontosságú szerepet. Patkányban a mediális amigdala az egyetlen olyan amigdaláris régió, amely a hipotalamikus támadási zónával bizonyítottan reciprok kapcsolatot tart fenn 174. A terület léziója károsodást okoz a szociális folyamatokkal kapcsolatos tanulás kivitelezésében, és irtása hatékonyan csökkenti az agressziót 58,267,294. Hörcsögöknél a mediális amigdala nagy mennyiségu vazopresszint tartalmaz, amely ebben a fajban a támadási zónával analóg elülso hipotalamuszba vetülve facilitálja az agresszív magatartást 90. A mediális amigdala elektromos ingerlése megnöveli az ingerlést követo idoszakban az agresszív interakciók gyakoriságát 226. Macskában a mediális amigdalából eredo, a mediális hipotalamusz támadási zónájának megfelelo területére vetülo P anyag tartalmú idegsejtek az 1-es neurokinin receptoron keresztül serkentik az affektív agressziót 105,270. Az emberi pszichosebészet is számos adatot szolgáltat az amigdala agresszióban játszott szerepére. Gyakori, hogy a temporális kéreg amigdalát is érinto epileptiform aktivitás fokozódása impulzív agresszív viselkedést hoz létre 6. A kétoldali amigdalotómiát sikerrel használták terápia-rezisztens agresszív betegek kezelésére 233,245. Kombinált PET és fmri vizsgálatokkal bebizonyosodott, hogy egészséges egyéneknél verbális agresszióval párhuzamosan az amigdala aktivitása megemelkedik 136. Humán képalkotó eljárásokkal az egyes amigdaláris magok elkülönítése nem lehetséges, ezért az utóbbi esetben csak közvetett módon lehet következtetni a mediális amigdala érintettségére. 10
11 A hipotalamikus támadási zóna A hipotalamusz szerepét a magatartás, köztük az agresszió szabályozásában Hess svájci elektrofiziológus vetette fel macskán végzett kísérletei kapcsán 129. Az agresszióra vonatkozó, hipotalamikus stimulációt magába foglaló adatait egy nagy összefoglaló muben közölte 130. Azóta gyakorlatilag minden vizsgált fajban (emberben is) ki tudtak váltani agresszív magatartást a hipotalamusz medio-laterális átmenetében elhelyezkedo bazális hipotalamikus terület stimulációjával (összefoglaló: 270,285 ). Egy több mint 600 esetet magába foglaló, a gyógyszeres kezelésre nem reagáló agresszív magatartás sebészi kezelését ismerteto tanulmány adatai szerint az általuk elsodlegesen választott beavatkozás az amigdalotómia volt, amely az esetek 67%-ban javulást okozott; azonban erre a beavatkozásra nem reagáló betegeknél (33%) végzett másodlagos poszterior hipotalamotómia 60%-ban megszüntette a fennálló agresszivitást 233. A terület jelentoségét jelzi, hogy patkányban ez az egyedüli agyterület, ahonnan elektromos ingerléssel agresszív magatartás megbízhatóan kiváltható 159,161 (1. ábra). f 1. ábra. A hipotalamikus támadási zóna elhelyezkedése a frontális síkban (árnyékolt rész). A kettos szaggatott vonal az elektród optimális elhelyezkedését jelzi. Az ábrázolt reprezentatív sík az intraaurális sík elott 6,7 mm-re van. Arc= hipotalamikus arkuátusz mag (D-dorzális, M-mediális, L-laterális rész); f= fornix; LH= laterális hipotalamusz; ME=eminencia mediana (I- pars interna, E-pars externa); SOR= szupraoptikus hipotalamikus mag, retrochiazmatikus rész; VMH= hipotalamikus ventromediális mag (C-centrális; DM-dorzomediális; VL-ventrolaterális rész). 11
12 A terület elektrofiziológusok által használt elnevezése a hipotalamikus támadási zóna, amelynek elhelyezkedését patkányban két nagyon részletes, egymástól függetlenül készült diszkriminancia-analízis alapján határozták meg 161,168. Ez a régió átfedést mutat az intermedier hipotalamikus területtel, frontálisan elsosorban az eminencia mediana elülso részének szintjében, szagittálisan a fornixtól a hipotalamusz bázisa felé eso részen helyezkedik el. A részletes szövettani elemzés szerint a hipotalamusz mediális részén elhelyezkedo magokhoz, pl. a stresszválasz organizációjában központi szerepet játszó paraventrikuláris maghoz képest egy sejtszegény területrol van szó, amely arányaiban nagy számú szinaptikus kapcsolatot képez 1. Mozgatható elektródok segítségével megbecsülték, hogy mindössze néhány száz sejt ingerlése elegendo az agresszív viselkedés kiváltásához 1,168, és az ingerlés hatósugara sem nagyobb 100? m- nél. A támadási zóna neuronjai feltehetoleg eros GABA-erg gátlás alatt állnak, hiszen az ide adott GABA antagonista mikroinjekciókkal (pikrotoxin, illetve bikukullin) 3,240, illetve mikrodialízissel a glutamát agonista kainát és bikukullin keverék alkalmazásakor agresszív magatartás váltható ki 112. Mindezek azt is jelzik, hogy nem az átmeno rostok, hanem az itt elhelyezkedo neuronok felelosek a kialakult válaszért. A hipotalamikus támadási zóna kiterjedt kapcsolatrendszerrel rendelkezik, közel 30 agyterületre küld rostokat 241. Az agytörzsbe irányuló vetülések (pl. középagyi centrális szürkeállomány, locus coeruleus) könnyen értelmezhetoek, azonban számos eloagyi területre futó rost (pl. a BNST, laterális szeptum, mediodorzális talamusz mag vagy a mediális amigdala területére futó rostok) funkcionális jelentosége nem ismert. A kiterjedt eloagy felé irányuló kapcsolatrendszer felveti a támadási zónából a limbikus és kérgi területek felé történo visszajelzés fontosságát az agresszív viselkedés szabályozásában, azonban ennek célzott vizsgálatára nincs irodalmi adat. Általánosan elfogadott szerepe szerint a támadási zóna az agresszió szabályozásában központi elemként szerepel; a stresszválasszal, a szituáció kognitív felmérésével és a fiziológiás állapottal egyeztetve itt dol el, vajon támadó magatartást mutasson-e az egyed, vagy sem 73,160,163. A hipotalamikus támadási zónában bipoláris elektródával kiváltott egyoldali ingerlés környezettol független támadást vált ki 161,162. A támadás kizárólag ellenfél jelenlétében, de számos szokatlan támadási partner, pl. nostény, domináns állat, vagy altatott ellenféllel szemben is megjelenik. A vizsgálati arénában spontán agresszív viselkedés 12
13 nem jelenik meg, és a támadások kizárólag az ingerlés idejére korlátozódnak. Ha az ingerlésnél alkalmazott áramerosség eléri az ún. támadási küszöböt, az ingerlés kezdete után néhány másodperccel harapással járó támadó magatartás figyelheto meg. Az ingerlések közötti szünetekben agresszív viselkedés nem jelenik meg. Ez a ki-be kapcsolható, szokatlan ellenfelek ellen is megjeleno agresszív magatartás elemeiben kórosnak tekintheto és az agresszív viselkedés szabályozásának megértésében nagy jelentoséggel bír. A kiváltott válaszban nem jelenik meg az agresszív viselkedésre jellemzo összes magatartási elem, a territoriális agresszió során nagy számban megfigyelheto fenyegeto magatartások ebben a modellben egyáltalán nincsenek. Ez a kísérleti felállás az agresszív viselkedés legnagyobb jelentoséggel bíró eleme, a harapással járó támadás vizsgálatára ad lehetoséget A középagyi centrális szürkeállomány A középagyi centrális szürkeállomány (periaqueductal gray, PAG) a rendszer harmadik eleme. Szerepe az agresszív viselkedés szabályozásában macskában egyértelmubb, mint rágcsálókban, embereknél gyakorlatilag nem ismert. Feladata elsosorban a fájdalomérzés (a ventrolaterális részen elhelyezkedo neuronok központi szereppel bírnak a stressz-analgéziában), menekülés és agresszió felsobb organizációja és a vegetatív reakciók közötti kapcsolat összehangolása 27,32. A hipotalamikus támadási zóna direkt vetít mind macskában, mind patkányban a PAG dorzolaterális-laterális részéhez (macska: 25,26 ; patkány: 201,241 ). Macskában a PAG elektromos/kémiai ingerlésével az ebben a fajban megfigyelt jellegzetes kétfajta agresszív viselkedés (affektív agresszió és a ragadozói magatartás) konzisztensen kiváltható. Az affektív agresszió a PAG dorzolaterális részérol, míg a ragadozói magatartás a ventrolaterális rész elektromos/kémiai ingerlését követoen jelenik meg 105. Ezeknek a területeknek diszkrét léziói meggátolják a felsobb központok ingerlésével kiváltható agresszív válasz kifejezodését is 105,270. Patkányban ezzel ellentétben már kevésbé egyértelmu a PAG szerepe. A PAG léziója megemeli a hipotalamikus támadási zóna ingerlésével kiváltott agresszió küszöbét, és kismértékben gátolja a territoriális agresszió kifejezodését 202. Elektromos stimulációja patkányban csak bizonytalan agresszív válaszokat hoz létre, ismételten és stabilan agresszió innen nem váltható ki
14 A rendszer modulátorai A fent ismertetett területeken kívül az agresszió szabályozásában fontos szerepet játszó agyterületek közül kiemelendo a laterális szeptum, a BNST, frontális és temporális kortikális területek, valamint a mediodorzális talamikus mag 5,6,28,101,269. A laterális szeptum gátló szerepe mind állatkísérletesen, mind embereknél jól dokumentált: a terület roncsolása, vagy a hipotalamusz felé haladó rostok átvágása agresszív magatartást eredményez, míg a terület stimulációjával az agresszív válasz elnyomható 5,6. A kérgi területek (elsosorban orbitofrontális, kisebb mértékben temporális) agresszióval kapcsolatos gátló szerepe jól dokumentált humán esetleírásokban, azonban szerepük állatkísérletekben nincs alátámasztva 101, Az agresszió neurofarmakológiája Az egyes neuroncsoportok által használt fo neurotranszmitterek az agresszív viselkedés rendszerének szabályozásában az excitátoros aminosavak, GABA, P-anyag, melyet a monoaminerg rendszerek modulálnak (2. ábra); patkányban csak a modulatorikus elemek jelentosége ismert 105,270. MeA SP (NK1) + NA (α2) DA (D2) + MH - GABA (GABA A ) - LH EAA (NMDA) + 5-HT (1 A ) PAG - affektív agresszió ragadozói magatartás 2. ábra. Az agresszív viselkedés szabályozásának központi elemei macskában. A mediális hipotalamuszban elhelyezkedo támadási zóna az agresszív viselkedés központi eleme. MeA: mediális amigdala; MH= mediális hipotalamusz; LH= laterális hipotalamusz; PAG= középagyi centrális szürkeállomány. DA= dopamin; EAA= excitátoros aminosavak; NA= noradrenalin; 5-HT= szerotonin; SP= P anyag. 14
15 Az agresszív viselkedést leghatékonyabban moduláló szerek hatásmechanizmusa a szerotoninerg, a dopaminerg, illetve a GABA-erg rendszerhez kötodik. A célzottan ezekre a rendszerekre ható farmakonok állatkísérletesen és a klinikumban is az agresszió hatékony modulátorai, azonban nem szelektíven hatnak az agresszív magatartásra és számos mellékhatással rendelkeznek 193. Ezen kívül a noradrenerg rendszer szerepét támasztja alá sok kísérleti adat 115. A klinikumban az agresszió kezelésére használt gyógyszeres stratégia attól függ, hogy az agresszió megjelenése egy meglevo pszichiátriai / neurológiai betegségre épül, vagy mint elsodleges, vezeto tünet jelentkezik. Ennek megfeleloen az alapbetegségtol függoen használatos a lítium (hangulatstabilizátor), carbamazepin, valproát (antiepileptikumok), és a már említett rendszerekre ható antipszichotikumok, triciklikus antidepresszánsok, illetve a szerotoninerg transzmissziót moduláló egyéb szerek 62. A szerotoninerg rendszer hatását részletesebben ismertetjük, mert az említett modulátor rendszerek közül ennek nagyon jelentos kétirányú kapcsolata van a hipotalamuszhipofízis-mellékvesekéreg rendszer muködésével. Az egyes neurotranszmitter rendszerek muködésének megváltozása közül kiemelt jelentoségu a szerotoninerg rendszer megváltozott aktivitása, amely szerepet játszhat patológiás humán agresszióformák kialakulásában Dopamin A pszichotikus kórképekben gyakran megjeleno agresszív viselkedés D 2 antagonista antipszichotikumok (pl. haloperidol) alkalmazásával hatékonyan gátolható, az akut gyógyszeres kezelést igénylo agresszióval társuló pszichiátriai állapotok esetében ez a gyógyszercsoport az elsodlegesen választandó szer 11,252. Macskában a dopamin D 2 receptoron keresztül facilitálja a támadási zónában az affektív agressziót 277. Haloperidollal patkányban a hipotalamikus agresszió hatékonyan gátolható 159,270. A dopaminerg rendszeren kifejtett hatás elsosorban a mezokortikolimbikus dopaminerg pályákon keresztül történik, azonban a számos kísérleti adat mellett nem elfelejtheto, hogy a motivációra, jutalmazásra és a magatartási mintázatok motoros kontrolljára eroteljesen ható transzmisszióról van szó
16 GABA Akut agresszív viselkedés esetén a klinikumban második sorban választandó szerek a benzodiazepinek, azonban az agressziót hatékonyan csökkento hatásuk már nem specifikus, szedatív dózisban lép fel 11,252. A benzodiazepinek GABA A receptoron való hatása kis dózisokban még fokozhatja is az agressziót, ezzel bifáziskus hatást mutatva. Ráadásul, az alkohol agressziót fokozó hatását is a megváltozott GABA-erg transzmisszióval magyarázzák 193. A benzodiazepinek közül a klórdiazepoxid csak az alkalmazott legnagyobb dózisban (20 mg/kg), míg az oxazepam csak kis mértékben gátolta patkányban a hipotalamikus agresszió kiválthatóságát 159,270. A hipotalamikus támadási zóna GABA-erg kontrolljára patkányban már korábban utaltunk. Macskában a támadási zónában jelen levo GABA-erg kontroll kulcseleme egy reciprok gátlás folyamatnak, amely biztosítja, hogy a lehetséges kétféle agresszív válasz (az affektív agresszió és a ragadozói magatartás) egyszerre ne jelenjen meg 105. A mediális amigdala SP sejtjei NK 1 receptoron keresztül beidegzik a támadási zónát, ott glutamát sejteket facilitálva serkentik az affektív agressziót. Ezeknek a sejteknek kollaterálisai a laterális hipotalamuszba vetülo GABA-erg sejtek muködését serkentik, így gátolják a ragadozói válasz megjelenését 105, Noradrenalin Klinikumban az akutan fellépo agresszió kezelésére nem alkalmaznak a noradrenerg transzmisszióra ható szereket, de krónikus esetekben kiegészíto szerként alkalmazásuk gyakori (? antagonista szereké) 252. A ß receptor antagonista propranolol patkányban megemeli a hipotalamikus agresszió küszöbét 159. Macskában a támadási zónában a noradrenalin az a 2 receptorokon keresztül fokozza az affektív agressziót 30,31. Egy részletes összefoglaló hipotézisére utalva kiemeljük, hogy a posztszinaptikus a 2 és ß receptorokon keresztül az agressziót fokozza a felszálló noradrenerg rendszer aktivitásának emelkedése (ahol az említett receptorok az agresszív viselkedés különbözo elemeire hatnak); azonban túlzott aktiváció a preszinaptikus a 2 receptorok kontrollja következtében ezt a hatást csökkentheti 115. A noradrenerg rendszer egyes hatásait az agresszív viselkedéssel szorosan összefüggo, azt elosegíto, de szigorúan nem annak mechanizmusát befolyásoló tényezokre fejti ki (mint pl. a figyelem fokozása, memória és szaglás stimulálása, fájdalomérzés csökkentése) 115. A noradrenerg rendszer 16
17 fontosságára utalnak genetikai vizsgálatok is. Az elsosorban noradrenalint és szerotonint bontó MAO A enzim hiánya X kromószómához kötötten egy holland család tagjaiban visszatéroen súlyos eroszakos cselekményeket eredményezo patológiás agresszióval járt együtt 46. Késobb igazolták, hogy a MAO A génkiütött egér hiperagresszív, és ez felnott korban megnövekedett noradrenalin szintekkel társult 53. Egy közelmúltban megjelent cikk adatai szerint a gyermekkori bántalmazást követoen azok a gyermekek váltak felnottkorban agresszív bántalmazókká, akik a gén polimorfizmusa kapcsán csökkent MAO A enzimaktivitást mutattak Szerotonin A 60-as évek végén figyeltek fel eredetileg a szerotonin lehetséges gátló szerepére az agresszív viselkedés szabályozásában. Agresszív egerek agytörzsében kevesebb 5-HT és metabolitja, 5-HIAA volt, mint a kevésbé agresszív kontrollokban 99. A 70-es évekbol származó elso leírás szerint súlyos agresszív cselekményeket magába foglaló sorozatos magatartási problémákkal küzdo tengerészgyalogosok liquorában az 5-HIAA szintje fordítottan arányos volt a korábban mutatott agresszív magatartással 45. A szerotoninerg hiányt elsosorban olyan jól körülírt csoportokban regisztrálják rendszeresen, akik kifejezett impulzív agresszív magatartást mutatnak (nem törodve annak a következményeivel), míg más agresszív típusoknál ez kevésbé jelentos 59. Ezt foemlosökön végzett vizsgálatok is megerosítették 189. A szerotoninerg rendszer megváltozott muködése, mint közös mechanizmus szerepelhet számos génkiütött állat agresszivitásának megváltozásában (pl. nnos, béta ösztrogén receptor esetében) 204. A szerotoninerg rendszer rendkívül bonyolult, az egyik legösszetettebb receptorarzenállal rendelkezik: eddig 14 receptor-altípust klónoztak, de újabbak létezését is feltételezik 29. Az agresszió szabályozásában két receptornak, az 5-HT 1A és 5HT 1B receptoroknak tulajdonítanak elsodleges jelentoséget, ezek mind pre, mind posztszinaptikusan helyezkednek el 19,109. Mindkét receptor Gi fehérjék közvetítésével az adenilát-cikláz aktivitást gátolja 29,78. Laboratóriumi tanulmányok szerint az 5-HT 1A agonisták jelentosen és hatékonyan képesek gátolni az agresszív magatartást számos fajban 38,70,71,143,289, az antagonista WAY elokezelés felfüggeszti ezt a hatást 71,194. A hatásmechanizmus pontosan nem ismert, hiszen az autoreceptorokon keresztül a raphe szerotoninerg neuronok 17
18 tüzelését gátolja, ezzel csökkent szerotoninerg transzmissziót idézve elo 78,222. A dorzális raphe-ba injektált agonisták csökkentik az agresszív magatartást 71,289, azonban a posztszinaptikus receptor agresszió csökkentését mediáló hatása is jól dokumentált 193 ; így valószínuleg mind a pre, mind a posztszinaptikus receptorok szerepet játszanak az agressziót csökkento hatás közvetítésében. Macskában az 5-HT 1A receptorok a PAGban gátolják a támadási zóna stimulációjával kiváltott affektív agressziót 263. Hörcsögben a szerotonin agresszív viselkedést csökkento hatásában központi elemnek az elülso hipotalamuszban végbemeno, a mediális amigdala neuronjaiból ide vetülo vazopresszin felszabadulásának gátlását tekintik, amely az 5-HT 1A és 1B receptorokon keresztül mediált 90. Az 5-HT 1A és 5-HT 1B kevert agonista eltoprazin hatékonyan gátolja az agresszív magatartást 271,272. Az 5-HT 1B génkiütött egér agresszivitása jelentosen magasabb 251. Ezt az agresszív magatartást az eltoprazin csökkenti az 5-HT 1B génkiütött egerekben, ez tovább erosíti az 5-HT 1A receptorok szerepére vonatkozó hipotéziseket 42. Ezzel látszólag ellentmondásban áll, hogy az 5-HT 1A génkiütött állatok agresszivitása csökkent 306, ezt az irodalmi álláspontok ismeretében a szerzok a kiindulási törzsek szokatlan viselkedésével magyarázták. Szerotonin transzporter génkiütött állatokban az agresszivitás jelentosen lecsökken (amelyekben a szerotonin szinaptikus eltávolítása lassabban történik) 133. A MAO A génkiütött egér viselkedése a fenti információkkal párhuzamba állítva nehezen értelmezheto, de a génkiütött egereknél fiatal korban jelentos szerotonin többlet lép fel, ami felnottkorra normalizálódik, a kialakuló hiperagresszivitást a noradrenerg többlet, illetve egy relatív szerotoninerg hiány magyarázhatja 53. A szerotoninerg rendszer differenciációjában kulcsfontosságú szerepet játszó Pet-1 gén hiánya a szerotoninerg rendszer kifejlodésének zavarával társul, gyakorlatilag nem alakulnak ki normálisan muködo szerotoninerg sejtek 123. Ezekben az állatokban a bazális és a kihívásokra adott szerotonin és HIAA szintek mind a kéregben, mind a hippokampuszban a vad típushoz képest jelentosen alacsonyabbak; a génkiütött állatok jellemzo magatartási eltérése a hiperagresszivitás és a szorongás. Klinikailag a szerotoninerg rendszerre ható szerek az agresszivitás szempontjából kettos jelentoséggel bírnak: (1) a szerotoninerg transzmissziót fokozó szerek direkt csökkentik az agresszív magatartást, (2) endokrin (mellék)hatásaik (a HPA axisra és a prolaktinra) diagnosztikus jelentoséggel bírhatnak. Ebbol a szempontból legjelentosebbek az 5-HT 1A receptor parciális agonisták (közülük a klinikumban Magyarországon csak a buspiron 18
19 van forgalomban, a generalizált szorongás terápiájában ez az elsoként választandó kezelés 279 ). A buspiron a klinikai gyakorlatban is csökkenti az agressziót, az antipszichotikumokkal és benzodiazepinekkel ellentétben a szerzok kevesebb mellékhatásról számoltak be 235. Akut buspiron adás megemeli a glukokortikoidok és a prolaktin szekrécióját 10,63,192. Személyiség-zavarban szenvedo betegek buspironra adott prolaktin válasza az irritábilitással fordítottan korrelált 60. A buspironhoz nagyon hasonló receptor-kötéssel és endokrin hatásokkal rendelkezo ipsapiron prolaktin elválasztást fokozó hatását vizsgálták egészséges egyénekben; a prolaktin válaszok az agresszióval fordított arányosságot mutattak 196. Mindkét munkacsoport a megváltozott 5-HT 1A receptor érzékenységet az impulzivitással hozta kapcsolatba, azonban az még nyitott kérdés, vajon ezek a szerek alkalmasak-e bizonyos típusú agresszióformák kezelésére, valamint diagnosztikus vagy prediktív tesztként alkalmazásuk beváltja-e a hozzájuk fuzött reményt Neuronális aktiváció agresszióban Az agresszió centrális szabályozásának vizsgálatának eddig ismertetett adatai elektromos/kémiai stimuláció, illetve lézió kapcsán levont kísérleti következtetések voltak. A 90-es évektol kezdododen lehetové vált az agyi neuronális aktivitás térbeli eloszlásának, illetve funkcionális pályarendszereknek leírása az ún. korai átíródású gének vizsgálatával. Ezzel a megközelítéssel számos új megfigyelés született a stresszkutatásban, különféle neurokémiai anyagok hatásmechanizmusának megértésében, és többek között egyes magatartások centrális szabályozásának vizsgálatában A korai átíródású gének Néhány virális onkogén emlos sejtekben megtalálható analóg génterméke központi szerepet játszik a transzkripcionális szabályozásban, és indikátorként a neuronális aktivitás megbecslésére használható. A virális fos gén (a Finkel-Biskis-Jinkins egér oszteogén sarcoma vírus onkogénje) emlos sejtben meglevo analógjának, a c-fos génnek szerkezetét 1984-ben közölték (összefoglaló: 125 ). A korai átíródású gének de novo protein szintézis nélkül gyorsan átíródnak a sejtet ért különbözo ingerek hatására (elsodlegesen válaszoló gének). Mivel sok egyéb más funkcionálisan nagy jelentoségu gén átíródását szabályozzák, a másodlagos hírvivokkel képezett analógia alapján (több 19
20 másodlagos hírvivo rendszer képes aktiválni) harmadlagos hírvivo rendszernek tekintik ezeket a géneket, illetve átíródott fehérjéiket tol kezdve közölték, hogy a c-fos gén gyorsan aktiválódik in vitro rendszerekben alkalmazott különféle stimulusok hatására 65,104. A c-fos gén átíródás a neuronális aktivitás jó indikátorának mutatkozott, és bizonyították használhatóságát funkcionális központi idegrendszeri pályarendszerek leírására 246. Az agresszióval kapcsolatos pályarendszerek leírására a 90-es évek közepétol kezdodoen használják. A Fos a korai átíródású gének egy fehérje családja, amely a már említett c-fos gén termék c-fos fehérjén kívüli tagjai a Fos B 304, a Fra1 (Fos-related antigén) 61, és a Fra A c-fos gén bazális aktivitása nagyon alacsony, csak a neuronokat ért aktiváció alkalmával mutat gyors átíródási választ, ekkor szintjük többszörösére emelkedik. Az mrns kimutatásakor a maximális válasz perc, míg a c-fos protein kimutatásakor 1-3 órával a behatás után jelenik meg (összefoglaló: 155 ). A Fos család tagjainak elsodleges hatásmechanizmusa a Jun-család valamely tagjával (c-jun, Jun-B, Jun-D) történo heterodimerizáció, amely heterodimer az AP-1 (aktivátor-protein) komplexet képezi. Az AP-1 számos gén regulációs faktora, és direkt interakcióba is léphet egyéb szolubilis citoplazmatikus fehérjékkel 125. A Fos család többi tagjának említése azért fontos, mert idobeli aktivitásuk és alap átíródásuk a c-fos fehérjétol lényegesen eltéro dinamikát mutat (nagyobb alap-aktivitás, lassúbb lebomlás stb.) 125. A korai c-fos tanulmányok nem minden esetben használtak specifikus antitestet, hanem esetenként a c-fos mellett a család több tagját is detektálhatták. Ez az esetenként eltéro Fos-szeru immunreaktivitás szerepet játszhat egyes tanulmányok eredményeinek különbözoségében. A neuronális aktivitás korai átíródású génekkel történo felbecslésére jelenleg nincs a c- Fos-nál pontosabb metodika, és az agresszió vonatkozásában gyakorlatilag csak erre vannak irodalmi adatok, amelyeket az alábbiakban ismertetünk. A módszer elonye, hogy (1) utólag, nem-invazív módon, (2) nagy területekre vonatkozó (akár az egész eloagy, agytörzs stb), (3) sejtszintu térbeli eloszlás-vizsgálat végezheto, (4) az aktiválódott sejt morfológiai tulajdonságai meghatározhatóak. Mindezekre korábban egyáltalán nem volt lehetoség. A módszer hátránya, hogy nem határozható meg (1) a viselkedés egy adott pillanatában megjeleno neuronális aktivitás (egy összesített képet 20
21 kapunk), (2) az aktiválódott sejtekre érkezo inger nagysága, (3) mekkora az esetlegesen ál-negatív sejtek aránya Agresszió és c-fos A c-fos tanulmányok megerosítették és tovább finomították az agresszió szabályozásáról alkotott, stimulációval / lézióval kapott eredményeket. Legrészletesebb vizsgálatok hörcsögben, kevésbé részletes vizsgálatok egérben és patkányban vannak jelen az irodalomban. Az elsoként közölt tanulmányok nostény 142 és hím 148 hörcsögökben hasonlították össze az agresszív és a szexuális kontaktus során bekövetkezo c-fos aktivációt. Bár a mediális amigdala aktiválódása mindkét viselkedés során megjelent, az anterior hipotalamikus régió (hörcsögökben analóg a hipotalamikus támadási zónával) és a PAG dorzolaterális részének specifikus aktiválódását jelezték hímek agresszív viselkedése során 148. Hörcsögökben továbbá részletes vizsgálatokat végeztek domináns és alárendelt állatokon is, mindkét csoportban a kontrollhoz képest jelentos aktivációt találtak a mediális amigdala, támadási zóna, PAG, valamint többek között a laterális szeptum és a BNST területén is 149. A domináns és alárendelt állatok között ez a szerzocsoport korábbi közleményük adatai szerint 148 nem talált különbséget, ebben a közleményükben az alárendelt egyedeknél nagyobb aktivációt találtak a cinguláris kéreg, centrális amigdala, dorzolaterális PAG és locus coeruleus területén 149. A szerzocsoport harmadik, szintén nagyon alapos analízisben az akut és krónikus vereség után megjeleno aktivációt vizsgálta hörcsögökben 147, melynek elsodleges célja a vereség stressz hatására fellépo neuronális aktiváció adaptációjának vizsgálata volt, az akut vereség során megjeleno c-fos mrns aktiváció nagyfokú egyezést mutatott a korábbi tanulmányukban 149 közölttel. Hörcsögöknél közvetlenül az agresszív interakció elotti másik agresszív kontaktus megnöveli az agresszív interakció intenzitását, ez a jelenség a kortikomediális amigdalában megjeleno intenzívebb c-fos aktivitással társult 225,226. Szintén hörcsögökben végzett tanulmány adatai szerint a betolakodó szagával átitatott tárggyal összehasonlítva (amely élénk vizsgálódást vált ki a rezidensben) az agresszív interakció során szignifikánsan magasabb aktiváció volt a mediális amigdala, támadási zóna, PAG, és a BNST területén, ezek a területek reciprok kapcsolatban vannak a támadási zónával
22 Egerekben az agresszív interakció során megjeleno neuronális aktiváció vizsgálata csak néhány tanulmányban történt meg 184,295. Az akut és krónikus vereség összehasonlítása a hörcsögöktol eltéro képet mutatott: az akut vereség hatása nagyjából megegyezett, azonban krónikusan nem habituációt, hanem szenzitizációt mutatott néhány terület (laterális szeptum, amigdaloid magvak) még 24 órával a vereség után is, ami nem illik a c-fos dinamika ismert rendszerébe 184. Ennek egy lehetséges magyarázata, hogy a kísérletet közlok nem specifikus (hanem a Fos család többi tagjával is reagáló) antitestet használtak. Mind hím, mind nostény betolakodó ellen mutatott agresszió során jelentosen megemelkedett a mediális amigdalában található c-fos pozitív sejtek száma, a vizsgált területek csak a BNST-szeptum, amigdala és preoptikus areára korlátozódtak 295. Patkányokban vereséget szenvedett állatok c-fos expresszióját vizsgálták, ahol a vizsgált területek közül aktivitás-növekedést jeleztek a mediális és centrális amigdala, laterális hipotalamusz, PAG, laterális szeptum, BNST, locus coeruleus területén 181. A fentiekben leírt eredmények jól mutatják, hogy a c-fos vizsgálatok eredményei nagymértékben átfedést mutatnak a stimulációs / léziós technikákkal kapott eredményekkel, megerosítik az agresszió centrális szabályozásánál leírt területek szerepét. Azonban a fenti kísérleti szituációkban mindig természetes helyzetükbol adódó, normális magatartási repertoárjukból 'prezentáló' állatok neuronális aktivációjának vizsgálatát végezték. Az irodalomban nincs adat arról, milyen neuronális aktivitás lép fel patológiás agresszióban. Ráadásul, az általunk szolgáltatott kísérleti adatok megjelenése elott tudomásunk szerint senki sem közölt kísérleti adatokat territoriális agresszió során kialakult aktivációról patkány rezidensekben. Patkány rezidensek a ketrecükbe helyezett kisebb hím betolakodóval szemben az esetek dönto többségében az agresszióval kapcsolatos támadó magatartáselemek kezdeményezoi, a kialakult küzdelem gyoztesei 39. A patológiás agresszió modellekben megjeleno c-fos aktiváció megértéséhez vizsgálat tárgyává szükséges tenni a territoriális agresszió során megjeleno aktivitásmintázatot is. Tudomásunk szerint eddig nem történt semmilyen fajban hipotalamikus ingerléssel kiváltott agresszív magatartás során megjeleno c-fos aktiváció feltérképezése. A hipotalamikus stimuláció a humán analógiákat tekintve nem 22
23 a legszerencsésebb, de kétségtelenül az agresszió szabályozási elemei kapcsolatának megértésében eddig egyedülálló vizsgálati lehetoséget biztosít. A hipotalamikus stimulációnál még értékesebb adatokat szolgáltathat a humán patológiás agresszóval kapcsolatba hozható hormonális analógiákon alapuló modell vizsgálata. A különbözo patológiás agressziómodellek során megjeleno aktivitástérképek elemzése elosegíti a patológiás agresszió közös elemeinek megértését, és hosszú távon a viselkedés célzott befolyásolására nyújthat lehetoséget Az agresszió hormonális szabályozása Az anyagcserében központi jelentoséggel bíró hormonális szignálok egyrészt az agresszió energetikai hátterét biztosítják, másrészt összetett központi idegrendszeri hatásokat fejtenek ki. A központi idegrendszerre kifejtett hatások (a metabolikus szignálok mellett) megjelenhetnek egyes agyterületeken közvetlenül receptoriális mechanizmusokon keresztül, illetve befolyásol(hat)ják neurotranszmitter rendszerek muködését (köztük az aminerg rendszereket), ezáltal egyéb agyterületek muködését modulálhatják. Az agresszió szabályozásában számos hormonnak (pl. inzulin, pajzsmirigyhormonok) tulajdonítanak jelentoséget, azonban a nemi hormonok és a mellékvesekéreg glukokortikoid hormonjainak a hatása a legkifejezettebb és legjobban dokumentált. Az agresszió szabályozásában korábban kulcsfontosságúnak ítélt adrenalin 50 nem jut át a vér-agy gáton, az agresszív viselkedés megjelenésében nagyobb szerepe lehet az agytörzsi noradrenerg rendszernek 115. A tesztoszteron a születés körüli idoszakban feltétlenül szükséges ahhoz, hogy felnott korban kifejthesse jól ismert agresszió fokozó hatását (ezzel mintegy érzékenyíti az agyat késobbi hatásokra). A tesztoszteron hatását felnott korban egyes agyterületeken nem tesztoszteronként, hanem dihidrotesztoszteronként vagy (lokális aromatizációval képzodo) ösztradiolként fejti ki; az agresszió facilitáló hatása elsodlegesen a szerotoninerg rendszer és a vazopresszin modulálásán keresztül érvényesül (összefoglaló: 273 ). A tesztoszteron szintek és a kóros emberi agresszivitás kapcsolatát nagy számú tanulmányban vizsgálták, és a közlemények többsége elfogadja a magas tesztoszteron szint és az agresszivitás közötti összefüggést 6. 23
24 A disszertáció szempontjából számunkra elsodleges jelentoséggel a glukokortikoidok bírnak, így az elválasztás szabályozását és az agresszív viselkedésre való hatásokat részletesen ismertetjük A glukokortikoid szint szabályozása és hatása az agresszivitásra A glukokortikoid elválasztás szabályozása A glukokortikoidokat (emberben kortizolt, laboratóriumi rágcsálókban kortikoszteront) a mellékvesekéreg zona fasciculata sejtjei szintetizálják és szekretálják a keringésbe. A keringo glukokortikoid szint jellegzetes napi ingadozást mutat, a legmagasabb szintet az aktív periódus kezdete elott éri el (a világos periódus kezdete elott emberben, míg a sötét periódus kezdete elott rágcsálókban). A szervezetet ért kihívásra a szimpatikus idegrendszerrel együttesen a hipotalamusz-hipofízis-mellékvesekéreg rendszer gyors és nagyfokú aktiválódása következik be. A glukokortikoidok egyrészt gátolják a rendszer további és túlzott aktiválódását, másrészt részt vesznek a magasabb rendu idegi muködések (tanulás, hangulati élet, agresszív magatartás) szabályozásában, fontos perifériás hatásaik kifejtése mellett (anyagcsere, immunrendszer modulálása stb.) 75,77,250. A hipotalamusz paraventrikuláris magja (PVN) tekintheto a glukokortikoid elválasztás és a stresszre adott reakció központi elemének. A mediális parvocelluláris részben található hipofizeotróp CRH/vazopresszin tartalmú neuronok mindkét mediátor révén a portális keringésen keresztül fokozzák a hipofízis elülso lebenyében az ACTH elválasztását (CRHR 1 és V 1b receptoron keresztül) 12,13,57,284. A keringésbe kerülo ACTH a mellékvesekéregben 2-es melanokortin receptoron keresztül a glukokortikoidok termelésének és elválasztásának legfobb induktora 203,298, a direkt neurális beidegzés szerepe a glukokortikoidok elválasztásában kevésbé jelentos 97. A paraventrikuláris mag léziójával a kihívásokra adott ACTH- és glukokortikoid- válasz gátolható, az eminencia mediána CRH tartalma is jelentosen csökken 178. A paraventrikuláris mag bonyolult afferentációval rendelkezik, amely magába foglalja az aminerg rendszereket, a hippokampuszt, amigdalát, számos egyéb eloagyi limbikus területet (laterális szeptum, BNST) és kortikális struktúrákat (asszociatív, prefrontális kéreg) 126,171. Ezek a területek (1) közvetítik a stresszorok hatásait (kérgi területek vagy felszálló rendszerek aktiválódásán keresztül aktiválódik a PVN), (2) képezhetik a 24
25 glukokortikoid feedback hatás célpontjait, (3) glukokortikoidok központi idegrendszeri hatásait mediálhatják. A glukokortikoidok két ismert intracelluláris receptora a mineralokortikoid (MR) és a glukokortikoid receptor (GR) 17,132, ezek affinitása és elhelyezkedése egymástól lényegesen különbözik (2. táblázat). 2. táblázat. Az agyban levo két intracelluláris kortikoszteron receptor. Mineralokortikoid receptor (MR) Nagy affinitású a kortikoszteronra (K D 0,5nM) Limbikus agyi területeken Agonista: kortikoszteron, kortizol, aldoszteron Antagonista: RU26752, spironolakton Glukokortikoid receptor (GR) Alacsonyabb affinitású a kortikoszteronra (K D 5,0nM) Számos agyterületen Agonista: kortikoszteron, kortizol, dexametazon, RU Antagonista: RU A MR expresszió az agyban elsosorban a limbikus területekre korlátozódik, mint a hippokampusz, amigdala és szeptum 16,56 ; és nem található meg a PVN-ben, illetve az elülso hipofízisben. A GR expresszió majdnem minden agyi régióban megtalálható, de különösen nagy mennyiségben van jelen a stresszválasszal szoros kapcsolatban álló területeken, mint a hipotalamikus paraventrikuláris mag, hippokampusz, amigdala, az agytörzs noradrenerg és szerotoninerg sejtjei 15,56. A tényleges glukokortikoid hatásokért nem a teljes, hanem a szállítófehérjékhez (elsosorban a kortikoszteroid-köto fehérjéhez) nem kötött szabad frakció a felelos, ami a keringésben levo mennyiség (emberben a diurnális ingadozást tekintve kb nmol/l) csak néhány százaléka, így értheto a receptorok affinitásának kritikus jelentosége 67. A MR receptorok nagyobb affinitással kötik a kortikoszteront, mint a GR, a körülbelüli K d értékek 0,5 nm, illetve 5 nm a két receptor esetében, ennek a napi ingadozás és stressz során is jelentos szerepe van 237. Az inaktív periódus nyugalmi kortikoszteron értékeinél a MR már jelentosen telítodik, kb %-ban 237. A GR-ok többsége akkor kezd telítodni, amikor a kortikoszteron napi ritmusa eléri a csúcsát, vagy még kifejezettebben stresszhatást követoen, ráadásul a GR szintje a MR szintjével ellentétben napi ingadozást mutat
26 PFC GR MR/GR +/- GR - hippokampusz PVN + MR/GR AMI + HF CRH AVP + LS BNST MR/GR DR LC GR + ACTH + kortikoszteron perifériás szervek 3. ábra. A kortikoszteron szekréció szabályozása. A feedback központi elemei a bal oldalon, míg a moduláló elemek a jobb oldalon vannak feltüntetve. MR: mineralokortikoid receptor; GR: glukokortikoid receptor; AMI: amigdala; BNST: bed nucleus stria terminalis; DR: dorzális raphe; HF: hipofízis; LC: locus coeruleus; LS: laterális szeptum; PFC: prefrontális kéreg; PVN: paraventrikuláris mag. A feedback elsodleges helye a PVN 154,157, illetve a hipofízis 67, a glukokortikoid gátlás itt csak GR-on keresztül érvényesülhet (3. ábra). A feedback második legfontosabb eleme a hippokampusz, itt a legmagasabb a MR és GR receptorok denzitása, és bár a két receptorrendszer a hippokampuszban a PVN felé irányuló kimenetet tekintve eltéro hatásokat közvetít, összességében a gátlás dominál 137. Az agytörzsi noradrenerg és szerotoninerg rendszerek fokozzák a rendszer aktivitását, az amigdalához (mediális és centrális) hasonlóan 126. A prefrontális kortex a PVN aktivitás gátlásának egyik fontos eleme 276, a laterális szeptum és a BNST szerepe kevésbé tisztázott 126. Ezek a területek, mint korábban említettük, az agresszió szabályozásában is kiemelt fontossággal bírnak, 26
27 elsosorban a mediális amigdala, támadási zóna és központi szürkeállomány aktivitásának modulálása révén. A PVN közvetlen szomszédságában levo perinukleáris GABA-erg zóna jelen adatok szerint központi jelentoséggel bír a PVN-be érkezo gátlás/serkentés közvetítésében A glukokortikoidok celluláris hatásmechanizmusa A glukokortikoid hatás receptoriális mechanizmusai Az eddigiekben említett MR és GR receptorok a nukleáris receptorok szupercsaládjába tartoznak 14. Három doménbol állnak: 1. N-terminális domén (transzaktiváció); 2. DNSköto domén (a receptor dimerizációért és a nukleáris transzlokációért is felelos); 3. C- terminális domén (szteroid kötohely, ho-sokk fehérjék kötohelyei; valamint a nukleáris transzlokációban, dimerizációban és transzaktivációban szerepet játszó szekvenciák). A szteroidhoz nem kötött szabad GR és MR receptor egy több fehérjébol álló konglomerátum része (a receptoron kívül két hsp90, hsp70, immunofilin és p23 molekula); a receptor szteroidhoz kötésekor ezek disszociálnak a komplexrol, ezáltal szabaddá válnak a DNS köto és a dimerizációs helyek (összefoglaló: 227 ). A receptor dimerizálódik, foszforilálódik, transzlokálódik és a megfelelo DNS regulátoros elemhez köt (pozitív vagy negatív glukokortikoid reszponzív elemhez), azonban ezt befolyásolja még koregulátor elemek kötodése 239, illetve heterodimerizáció megjelenése 282. A ligandkötött glukokortikoid receptor direkt interakcióba léphet celluláris transzkripciós faktorokkal, mint az AP-1, Nf-?B és a CREB, anélkül, hogy a glukokortikoid reszponzív elemekhez kötodne 187,221,236. A glukokortikoidok adott szövetben kifejtett hatását még a receptorok izoformái is módosíthatják. A GR két izoformában létezik, amelyek alternatív átíródás révén jönnek létre. A GRa a normál receptor, míg a GRß C- terminálisa nem képes megfelelo aktivitású hormonkötésre és transzaktivációs hatás kifejtésére; ezáltal modulálhatja a GRa hatását 207. A MR-nak emberben két, patkányban három mrns izoformája került leírásra (a, ß,?), melyek funkcionális jelentosége nem ismert A glukokortikoidok nem klasszikus receptorain kifejtett hatásai Egyre több kísérleti adat támasztja alá, hogy az agyban a glukokortikoid hormonok nem csak klasszikus receptoraikon fejthetik ki hatásukat. A hatások széles spektrumának 27
28 áttekintésére nincs módunk, de ezek a hatások általában gyorsak (néhány percen belüliek), szerepet játszhatnak a korai feedback, neuronális excitábilitás, sot a magatartás szabályozásában is (összefoglaló: 177 ). Támadáspontja lehet nem konvencionális glukokortikoid receptor (nagy affinitású glukokortikoid kötohelyet már leírtak neuronális membránban, ennek szerkezete nem egyezik meg a klasszikus GRral 208 ), de képesek allosztérikusan modulálni egyes G-fehérje kapcsolt receptorok (pl.?- opioid receptor), illetve ioncsatornák (acetilkolin receptor (N M acetilkolin receptor), GABA A receptor, L-típusú Ca csatorna) muködését is 177. Ezek a hatások elméleti jelentoségükön túl is fontosak a magatartás vizsgálatában, mert szerepet játszanak a goték szexuális magatartásának gyors szabályozásában 200, patkány lokomotoros aktivitásának megváltozásában 248, és csoportunk adatai szerint az agresszió szabályozásában is Megváltozott glukokortikoid szintek neurális következményei Teljes glukokortikoid hiány mellékveseírtást (adrenalektómia, ADX) követoen markáns változásokat okoz a központi idegrendszerben és a magatartásban. A hippokampusz gyrus dentatus szemcsesejtjeinek elhalása következik be teljes hiányban, ami már a MR receptorokon ható pótlással kivédheto 175. Az agyi GR receptorok denzitása és expressziója fokozódik, azonban nagyon érzékenyen reagál kis mennyiségu glukokortikoid adására 175. A hipotalamusz-hipofízis-mellékvesekéreg szabályozásának feedback alól felszabaduló elemeinek aktivitása megemelkedik, így a CRH, AVP és hipofízeális POMC szintje no (összefoglaló: 77,250 ). Ezek a gének a glukokortikoidok által szabályozott negatív glukokortikoid reszponzív elemeket is tartalmaznak 87,146,180. Glukokortikoid hiányban a PVN-ben elsosorban a parvocelluláris vazopresszin tartalom emelkedik, ez a CRH-val kolokalizáltan található 253,254. Érdekes módon, ezzel ellentétben a legnagyobb extrahipotalamikus CRH neuronpopuláció (a centrális amigdalában) CRH tartalma a glukokortikoidok hiányában csökken, és alacsony kortikoszteron szinteket biztosító szubsztitúció visszaállítja az eredeti szintet 179,213,266. A glukokortikoidok befolyásolják számos neurotranszmitter rendszer (szerotoninerg, noradrenerg, glutamaterg, GABA-erg, kolinerg transzmisszió) muködését 77,140,141. Glukokortikoid hiány legjelentosebb változást a szerotoninerg transzmisszióban okoz, a glukokortikoidok és a szerotoninerg transzmisszió között kétirányú kapcsolat áll fenn. 28
29 Már a feedback elemzésénél is említettük, hogy a glukokortikoidok facilitálják a felszálló (elsosorban dorzális raphe) magból kiinduló szerotoninerg sejtek muködését 18, és ez a glukokortikoid szekréció szempontjából egy pozitív visszacsatolást jelent. A szerotoninerg rendszer beidegzi a CRH neuronokat 172, és számos receptorán - elsosorban az 1A és 2C receptorokon- keresztül serkenti a CRH szekréciót, és emeli a glukokortikoid szintet 95. PVN lézióval az 5-HT 1A és 5-HT 2 receptorokon ható szerotoninerg agonisták által indukált glukokortikoid szekréció fokozódás nagymértékben gátolható 23. A szerotoninerg rendszer diszfunkciója tehát csökkent glukokortikoid szekrécióval társulhat. További kapcsolóelem a két rendszer között, hogy a szerotonin szintézis sebességének meghatározó enzime a triptofán-hidroxiláz, amelynek szintje csökken ADX után és dexametazon adás után megno Továbbá, a szerotonin felszabadulás és metabolitjainak szintje lecsökken ADX után 74. A szerotonin transzporter funkcionális kapacitása csökken magas glukokortikoid szintek esetén 176,274, a transzporter átíródása feltehetoleg direkt glukokortikoid kontroll alatt áll 33. A legtöbb szerzo szerint az 5- HT 1A receptorok képezik a legjelentosebb kapcsolatot a HPA rendszer és a szerotoninerg rendszer között 95,191. A legjellegzetesebb elváltozás ADX után az 5-HT 1A receptorok fokozott posztszinaptikus (elsosorban hippokampális) expressziója 55,165,191, az egyedi sejtek 5-HT 1A receptor tartalma is fokozódik 305. Az 5-HT 1A receptorra jellemzo upreguláció nem áll fenn általánosan a szerotoninerg autoreceptorok között, hiszen pl. az 5-HT 1B receptorok nem érintettek 205. A direkt glukokortikoid hatást (és nem a csökkent szerotoninerg transzmisszió miatt kialakuló upregulációt) támasztja alá az, hogy a közelmúltban került leírásra egy, a MR/GR heterodimerizációt igénylo negatív glukokortikoid reszponzív elem az 5-HT 1A receptorát kódoló gén promoterén 209. Az 5-HT 1A receptorok glukokortikoid szuppressziója mind a MR, mind a GR receptorokon keresztül érvényesül 190. Mint korábban említettük, a szerotoninerg rendszer aktivitásának megváltozása jelentosen befolyásolja az agresszív viselkedést, ezért nem meglepo, hogy a szerotoninerg rendszer aktivitását befolyásoló glukokortikoidok fontos szerepet játszanak az agresszió szabályozásában. 29
30 A glukokortikoidok hatása az agresszióra Az agresszió és a HPA rendszer szoros, kétirányú kapcsolatban van egymással: az agresszív kontaktus önmagában stressz-tényezo, míg a HPA axis aktivitása jelentosen modulálja az agresszív magatartás megjelenését. Az agresszív interakció a legerosebb stresszorok egyike 151, és az agresszív interakció során megjeleno glukokortikoid szekréció változás befolyásolhatja az interakció következo fázisaiban az agresszivitást. Más a hatása az akut és krónikus módon megváltozott glukokortikoid szinteknek, egy mechanizmussal az összetett hatás nem magyarázható Akut hatások Az akut hatások gyorsan (néhány percen belül) jelentkeznek, feltehetoleg nem csak a klasszikus receptor-mediált, hanem nem-genomiális úton is modulálják az agresszivitást. Hörcsögökben 5 perccel az agresszív kontaktust megelozoen az elülso hipotalamuszba injektált kortikoszteron (1000 nmol/l) megnövelte az agresszív kontaktusok számát a rezidensekben vizsgált 15 perces idoszakban, érdekes módon a betolakodókban az alárendelt magatartásminták gyakoriságát fokozta; ezt a hatást más vizsgált szteroid (tesztoszteron, dihidrotesztoszteron, progeszteron, béta-ösztradiol, dezoxikortikoszteron) nem mutatta 120. Az agresszív interakció elott 10 perccel adott kortikoszteron (0,5 mg/kg) más hatásokat fejtett ki naív állatokban, mint az agresszív tapasztalattal rendelkezo, de egyedül tartott hímekben, vagy nosténnyel tartott, agresszív tapasztalattal rendelkezo hímekben 113. Az elso esetben a kortikoszteron lokomotoros hatásokat fejtett ki, míg a másik két esetben hatékonyan növelte az agresszív interakciók gyakoriságát. A glukokortikoid szintek a napszakos ritmusnak megfelelo ingadozást mutatnak, az agresszív magatartásban és a napi aktivitásban is hasonló ingadozás játszódik le. A glukokortikoid szintek már egy órával az aktív periódus (sötétség) kezdete elott megemelkednek, az agresszivitás szintje ezzel párhuzamosan változik; az agresszív magatartásokra fordított idot ebben az idoszakban a mineralokortikoid receptor antagonista spironolakton szignifikánsan csökkenti 116. A napi ingadozásra rátevodik egy gyors, ultradián ingadozás, amit számos faj mellett patkányban is leírtak 114,299. A gyors kortikoszteron ingadozások pontos jelentosége nem ismert, azonban az ilyen nagy amplitúdójú oszcilláció különbözo pillanataiban mért hormonhatások vagy viselkedések 30
31 nem függetleníthetok az ultradián oszcilláció jelenlététol. A stresszválasz intenzitása nostény patkányokban 10 perces zajstresszre nagyfokú változékonyságot mutatott az ultradián oszcilláció szerint (az általuk mért ciklusido kb. 100 perc, egy automatizált rendszerrel 10 percenként vett vérminták alapján utólag azonosítva); nevezetesen ha a stresszor megjelenésének pillanatában az állatokban a kortikoszteron szintek éppen a felszálló ágban voltak, a kortikoszteron válasz szignifikánsan nagyobb volt, mint a leszálló periódusban levo állatoknál 299. Az ultradián oszcilláció adataink szerint az agresszió szabályozásában is jelentoséggel bírhat, és a hatások gyors megjelenése miatt feltehetoleg nem-genomiális hatásokban játszik szerepet. A fenyegeto magatartások gyakorisága a vizsgált 5 perces periódusban szignifikánsan magasabb volt a növekvo, mint a csökkeno kortikoszteron szinteket mutató állatok esetében 114. Amennyiben az endogén glukokortikoid szintézis a 11ß-hidroxiláz gátló metiraponnal gátlásra került, a fenyegetések idotartama szignifikánsan csökkent, míg a kortikoszteron kezelés ezt normalizálta 114. Mindezek azt bizonyítják, hogy territoriális agresszióban akutan a glukokortikoidok hatékonyan stimulálják az agressziót, illetve annak egy elemét, a fenyegeto magatartást. Ezzel egy önerosíto kör jöhet létre, hiszen mint említettük, az ellenfél megjelenése, illetve az agresszív interakció maga is fokozza a kortikoszteron szintézist, ezzel pedig elosegíti a további agresszív magatartást. Az akut hatások tekintetében így viszonylag tiszta a kép, az ép hipotalamusz-hipofízis-mellékvesekéreg rendszer esetében az akut glukokortikoid emelkedés serkenti, míg az emelkedés elmaradása csökkenti az agressziót. Ezeket az adatokat egészséges önkénteseken végzett humán vizsgálatok adatai is alátámasztják. Egészséges önkénteseket tesztszituációba kitéve pozitív korrelációt mutattak ki a glukokortikoid szintek és az irritábilis ingerre kiváltott hangsúlyozottan 'normális' agresszivitás között 98. Egészséges sportolók cselgáncs versenyen mutatott agresszivitása (a küzdotéren, a bírók által felügyelt szignálokra indított, kontrollált, a szabályoknak megfelelo viselkedés) és kortizol válaszuk között pozitív korrelációt találtak 247. Mindkét kiemelt példában az itt adott reakciók a feladatra adott, adaptív válaszok voltak, és az itt megjeleno agresszív magatartás sem minoségében, sem súlyában nem tekintheto ekvivalensnek a patológiás agresszivitással. 31
32 Krónikus hatások Tartósan magas glukokortikoid szint hatása az agresszivitásra A krónikus stressz hatására egerekben az agresszivitás csökken, és ugyanezt eredményezi a krónikus glukokortikoid kezelés is 170,224. Patkányokban a vereség a gyozelemmel ellentétben tartósan glukokortikoid szint emelkedést eredményez, és ezzel párhuzamosan a vereséget szenvedett egyedek viselkedése alárendeltté válik, és agresszivitásuk csökken 256. Páviánoknál a tartósan alárendeltségben élo egyedek rendelkeznek a legmagasabb nyugalmi kortikoszteron szintekkel, és ez együtt jár nem csak az agresszív viselkedés, de a szexuális funkciók és táplálékkereso magatartás csökkenésével is, egyfajta általános viselkedési gátlást eredményezve 249. Úgy tunik, tartósan magas glukokortikoid szintek az agresszió csökkenését idézik elo, az akut agresszió facilitáló hatással ellentétben. Tartósan alacsony glukokortikoid szint hatása az agresszivitásra A krónikusan alacsony és a kihívásokra kevésbé reagáló glukokortikoid szinteknek az agresszió kutatásában sokkal nagyobb lehet a jelentosége, mint korábban feltételezték. Egy finn pszichiáter a szukebb szakmai közvélemény számára is meglepo eredményt közölt 1985-ben: szignifikánsan alacsonyabb kortizol ürítést találtak (kb. 50%) a visszatéroen eroszakos cselekményeket végrehajtó antiszociális elítélteknél a többi csoporthoz képest 293. A többi vizsgált csoport kortizol ürítése egymáshoz nagyon hasonló volt, ezek magukba foglalták (1) intermittáló explozív magatartás, (2) egyéb bunözok, (3) kóros gyújtogatók, (4) pszichiátriai személyzet, (5) eroszakos cselekedeteket végre nem hajtó antiszociális személyiségzavar kategóriákat. Ez a tanulmány azt sugallja, hogy nem általánosan az antiszociális személyiségzavarban szenvedok, hanem egy alcsoport, a visszatéroen eroszakos buncselekményeket elköveto antiszociális személyek rendelkeznek alacsony glukokortikoid szintekkel. A tanulmány egy második analízisben a már serdülokorban fennálló magatartási elváltozásokat korreláltatta a felnottkori glukokortikoid szintekkel. Az alulszocializált agresszív viselkedési zavar (DSM-III diagnózis, DSM-IV eltörölte) serdülokori jelenlétét alacsony glukokortikoid szintek jellemezték, míg hasonló kapcsolatot nem találtak az eroszakos öngyilkosságra való hajlam között 293. Viselkedési zavarban szenvedo 32
33 gyermekek agresszív tüneteinek gyakorisága és az elso agresszív tünetek megjelenése fordított arányosságot mutatott a nyálban mért kortizol szintekkel 185, alacsony kortizol szintek a két év múlva bekövetkezo agresszív viselkedések gyakoriságát nagy pontossággal elore jelezték. Diszruptív viselkedési zavarral diagnosztizált gyermekeknél és serdüloknél mért alacsony kortizol szintek állandósult és fiatalabb korban kezdodo agresszióval társultak, az alacsony kortizol szintekkel rendelkezo egyedek agresszivitása (agresszív viselkedéssel kapcsolatos tünetek, cselekedetek száma és súlyossága) jelentosen felülmúlta a magas kortizol szintekkel rendelkezo, viselkedési zavarral diagnosztizált társaik agresszivitását 186. Oppozícionális viselkedési zavararral diagnosztizált agresszív gyermekek bazális és stresszre adott kortizol szintje szignifikánsan alacsonyabb volt, mint normál kontrollok esetében 290. Ebben a tanulmányban a viselkedési zavar jelenléte fokozott szorongással társult, a kortizol szintek egyenes arányosságot mutattak a szorongásos tünetek gyakoriságával az összes vizsgálati alanyt tekintve 290. Agresszivitást magába foglaló viselkedési zavarral diagnosztizált serdülo lányok reggeli plazma kortizol szintjei a normál kontrollokhoz képest szignifikánsan alacsonyabbak voltak 211. Hasonló változásokat mutattak ki komorbid diagnózisú figyelemhiányos-hiperaktív / oppozícionális viselkedési zavarral rendelkezo gyermekeknél 144. A gyermek-serdülokori viselkedési zavarok átmehetnek antiszociális személyiségzavarba 18 éves kor felett, a szülok antiszociális agresszív tüneteinek gyakorisága egyenes arányosságot mutatott a gyermekkori viselkedési zavar tüneteinek gyakoriságával, ráadásul a viselkedési zavarban szenvedo gyermekek kortizol szintje a kontrollokhoz képest szignifikánsan alacsonyabb volt 291. A fenti adatok meggyozoen bizonyítják, hogy a visszatéro agresszivitás / viselkedési zavar / antiszociális magatartás alacsony glukokortikoid szintekkel és reaktivitással, egyes esetekben szorongással is társul, ez megjelenik felnott és gyermek, férfi és no populációban. Ezeket az eredményeket néhány állatkísérletes adat támasztja alá. Kutyamenhelyen a késobb megjeleno agresszivitással társuló magatartási problémákat az alacsony glukokortikoid szintek elore jelezték 124. Csoportunk által került leírásra a kísérletesen eloidézett alacsony, magatartási kihívásokra nem reagáló glukokortikoid szintek hatása az agresszív viselkedés idobeli alakulására 117. Az eloidézett glukokortikoid hipofunkció drámai változást idézett elo az állatok agresszív viselkedésében: a támadások száma 33
34 nem változott, de a sérülékeny területekre (fej, torok, has) adott támadások aránya jelentosen megemelkedett, és a támadásokat kevesebb fenyegetés kísérte. Patkány és egyéb laboratóriumi rágcsálók territoriális agresszív viselkedése során a támadások az esetek jelentos többségében a nem sérülékeny, háti területek felé történnek, sérülékeny területekre irányuló támadások megjelenése kizárólag életveszélyes szituációban történik 37,39,214,215. Ezek az állatok azonban saját területen, egy kisebb ellenfél behelyezésekor mutattak a sérülékeny területekre irányuló támadásokat, amelyeket csökkent fenyegeto magatartások kísértek. A fenyegeto magatartások felkészítik az ellenfelet a támadás megjelenésére, jelzésük ezért fontos szereppel bír 39. Az alacsony glukokortikoid szintek tehát állatkísérletesen egy újonnan leírt, patológiás magatartással járnak együtt, és hormonálisan analógiát képeznek a humán patológiás agresszióban látható elváltozással Alacsony glukokortikoid szintekhez társuló egyéb magatartási zavarok A Selye által megalkotott stressz fogalom tudományos köztudatba kerülése óta 261 az orvosbiológiai kutatások egy jelentos részét a hipotalamusz-hipofízis-mellékvesekéreg rendszer aktivitásának megváltozását eloidézo és annak következtében fellépo változások vizsgálata képezi. Az ide vonatkozó irodalomban döntoen a különbözo stresszorok hatására kialakuló kórosan magas glukokortikoid szintek hatásának leírása található. Tudományos közlemények hada bizonyítja, hogy a rendszer túlmuködése számos nem adaptív elváltozás megjelenéséhez vezethet, mint a neuronális degeneráció (és ehhez tartozó dementiform elváltozások), hipertónia, fertozésre való hajlam és így tovább, amelyet mind humán adatok, mind állatkísérletes eredmények jól dokumentáltan alátámasztanak. Magatartási szempontból legjobban dokumentált a kórosan emelkedett glukokortikoid szintek és a depresszió kapcsolata 76,77,145. Ennek bizonyos értelemben ellenpólusát képezik azok a betegségek, melyeket szintén a stresszel hoznak kapcsolatba, azonban alacsony glukokortikoid szintekkel járnak; felvetodött az alacsony glukokortikoid szintek önálló pszichopatológiai jelentosége 121. Három olyan betegség biztosan van, amit a stresszrendszer funkcionális zavarával hoznak összefüggésbe, és alacsony glukokortikoid szintekkel járnak: a poszttraumatikus stressz zavar, a krónikus fáradtság szindróma és a fibromialgia szindróma. 34
35 Ezekkel az állapotokkal glukokortikoid szintek tekintetében nem összemérheto a teljes glukokortikoid hiány, amely a mellékvesekéreg destrukciója következtében áll fenn (Addison kór). Glukokortikoid szubsztitúció nélkül ez a kórkép rövid idon belül halálhoz vezet 216. Bár ebben a kórképben glukokortikoid szintek tekintetében egy extrém állapotról van szó, ahol súlyos metabolikus és ioneltérések állnak fenn, amelyek a kezelést elsodlegesen igénylo állapotok, megjelennek jól dokumentált magatartási eltérések is. Ezek elsodlegesen az impulzivitás-irritábilitás, mely szorongással is társulhat 199,216. A poszttraumás stressz zavar (PTSD, posttraumatic stress disorder) dokumentált szorongással kapcsolatos zavar, amely diagnosztikus kritériumaiban az agresszivitás is szerepel 9. Ebben az esetben a diagnózis alapköve egy korábbi rendkívül súlyos trauma jelenléte, amely többféle eredetu lehet (háború, földrengés, nemi eroszak). Ezért megleponek tunhet, hogy ebben a kórképben nem magas, hanem tartósan alacsony glukokortikoid szinteket jelentenek. Bár vannak tanulmányok, amelyek szerint a PTSDben nem változott, vagy magas kortizol szintek vannak 52, az irodalmi adatok szerint összességében nagyon meggyozo alacsony glukokortikoid szintek megjelenése PTSDben. PTSD-ben szenvedo vietnámi veteránok 24 órás ürített kortizol szintje szignifikánsan alacsonyabb egészséges kontrollokhoz és más pszichiátriai betegségben szenvedokhöz viszonyítva 182,302. Ez a változás holokauszt túléloknél is megjelenik, ahol az alacsony kortizol szintek a PTSD-vel korrelálva évtizedekig álltak fenn 301. Nagy populációt vizsgálva (valamivel több, mint 4000 embert magában foglaló tanulmány) a vietnámi háború aktuálisan PTSD szimptómában szenvedo veteránjainak plazmájában mutattak alacsony reggeli kortizol szinteket a megfelelo kontrollokkal összehasonlítva; legalacsonyabb kortizol szinteket a legnagyobb traumának kitett katonákban mértek 41. Szubklinikai PTSD-ben a tünetek fordítottan korreláltak a glukokortikoid szintekkel (amelyek reggel alacsonyabbak, este magasabbak voltak, jelezve a reguláris napi ingadozás zavarát is), a tünetek javulásával a kortizol szintek emelkedtek 2. Alacsony glukokortikoid szintek és fokozott dexametazon szupresszió jelen volt PTSD-ben szenvedo szexuálisan zaklatott noknél 275, de örmény gyermekeknél is évekkel a földrengés után 100. A másik két említett kórképben, a fibromialgia és krónikus fáradtság esetében szintén megjelenik az alacsony kortizol szintek mellett az irritábilitás és a szorongás. Az 35
36 irritábilitás a krónikus fáradtság szindróma egyik diagnosztikus kritériuma, és az újonnan felállított közös krónikus fáradtság - fibromialgia skálán is szerepel 303. Krónikus fáradtság szindrómában irritábilitáshoz társul defenzív beállítottság is 64. A szorongással kapcsolatos tünetek illetve a komorbid szorongás gyakorisága megemelkedett krónikus fáradtság szindrómában 96,244,280 (együttes fennállás rosszabb prognózist képez 34 ), és fibromialgia szindrómában is 89,296. A fibromialgia szindrómában megjeleno szorongás és az irritábilitás nem magyarázható a fájdalom jelenlétével, hiszen hasonló izomfájdalmakkal küzdo, de nem fibromialgiás embereknél ez nem mutatkozik 110. Mindkét kórkép alacsony glukokortikoid szintekkel társul (krónikus fáradtság: 82,83,257,258 ; fibromialgia: 106,169 ). Krónikus fáradtságban a mellékvesék méretének csökkenését is kimutatták 259. Ebbol az a következtetés szurheto le, hogy alacsony glukokortikoid szintekkel járó betegségekben szenvedok egy spektrumot képeznek, amelyben az agresszivitás valamilyen mértékben jelen van, és szorongással is társulhat. A korábbi stresszor jelenléte PTSD esetén egyértelmu, azonban patológiás agresszió esetén a glukokortikoid szintekkel kapcsolatban nem bizonyított. A korábbi agresszív interakcióban való részvétel, korai traumatikus bántalmazás fokozza a késobbi agresszivitást, de nem teszi szükségszeruvé 86,297. A kóros agresszivitás és a glukokortikoid szintek kapcsolatánál említett tanulmányokban sajnos nem vizsgálták, vajon az alacsony glukokortikoid szintekkel kapcsolatban korábban megelozo traumatikus élmény(ek) szerepeltek-e, és lehet-e szerepük a kóros agresszivitás kialakulásában. Állatkísérletesen a krónikus, nagy traumákat követo stressznek részletes irodalma van 40,85, azonban trauma hatására alacsony glukokortikoid szinteket konzisztensen eloidézo eljárást nem közöltek az irodalomban. Nem ismert annak a magyarázata, hogyan lehetséges bizonyos embereknél egy centrális hiperszenzitivitás kialakulása, és állatkísérletesen ez miért nem alakul ki. Az alacsony glukokortikoid szintek hatása az agresszivitásra a korábbi stresszfaktortól függetlenül is érdekes kérdés, és segítséget nyújthat a patológiásan agresszív magatartás megértéséhez A vegetatív reaktivitás és a patológiás agresszió A bazálisan és kihívásokra adott alacsony glukokortikoid szintek társulnak humán patológiás agresszióval, amint ezt az eddigiekben részletesen kifejtettük. A patológiás 36
37 agresszió során nem csak a hipotalamusz-hipofízis-mellékvesekéreg rendszerre, hanem a vegetatív aktivációra is jellemzo a kihívásokra megjeleno csökkent reaktivitás. Agresszív, börtönben levo kriminális pszichopaták félelemkelto szituációban szignifikánsan alacsonyabb vegetatív reaktivitást mutatnak, és a válasz elmaradása jól korrelál az antiszociális személyiségzavarral 217. Viselkedési zavarban szenvedo gyermekek mind orientáló, mind averzív stimulusokra csökkent kardiovaszkuláris reaktivitást mutatnak 128. Antiszociális személyiségzavarban a visszatéro agresszív cselekményeket elkövetoknél kisebb a vegetatív autonóm aktivitás 228,229,231 ; ez társulhat frontális lebeny elváltozásokkal 230, ráadásául a magas autonóm aktivitás antiszociális személyiségzavar esetében 'védo faktornak' tunik a késobbi kriminális agresszivitással kapcsolatban 43,232. Az alacsony autonóm arousal tehát társul az antiszociális, kriminálisan agresszív viselkedéshez, azonban ennek a glukokortikoid szekrécióhoz való viszonyát nem elemezték. 37
38 3. Célkituzések A fentiekben részletesen bemutatásra került, hogy a humán patológiás agresszió tartósan alacsony és nem reaktív glukokortikoid szintekkel társul, és az alacsony glukokortikoid szintek ezzel egyidejuleg szorongással kapcsolatos magatartással járhatnak. Továbbá, humán patológiás agresszióban nem csak a hipotalamusz-hipofízis-mellékvesekéreg rendszer underarousal áll fenn, hanem jellegzetes vegetatív eltérések is megjelennek. A kísérleteink tárgyát ennek a humán populációban is megjeleno endokrin analógiának hím Wistar patkányokon történo modellezése és részletes vizsgálata képezte. Az értekezés alapját négy megjelent közlemény képezi, továbbá tartalmazza egy közlésre elokészített kézirat adatait is. A kísérletek során a következo kérdésekre kerestük a választ: I. Kimutatható-e a normális territoriális agresszióhoz képest a glukokortikoid hipofunkcióban megjeleno patológiás agresszív magatartás során egy megváltozott agyi neuronális aktivációs mintázat, és ez mennyiben mutat átfedést más úton létrehozott patológiás agresszió által kiváltott neuronális aktivációs mintázattal? Ezt a kérdést három lépcsoben, a neuronális aktiváció egyik szövettani markerével, a korai átíródású géntermék c-fos fehérje expressziójának részletes agyi eloszlásának immuncitokémiai elemzésével vizsgáltuk. 1. Milyen a normális territoriális agresszív interakció során megjeleno térbeli c-fos eloszlás hím Wistar rezidensekben? Territoriális agresszió során a rezidens állatok az agresszív magatartáselemek kezdeményezoi és fo kifejezoi. Az agresszió centrális szabályozásának megértésében az utóbbi években kulcsszerepet játszó c- Fos aktiváció leírása patkány rezidensekben korábban nem történt meg, ezért leírása elengedhetetlen a patológiás agresszió során megjeleno aktiváció megértéséhez. 2. Milyen neuronális aktiváció jelenik meg a hipotalamikus támadási zóna ingerlésével kiváltott agresszió során? A hipotalamikus támadási zóna elektromos ingerlésével környezettol független agresszív magatartás váltható ki, amely patológiásnak tekintheto. Az alkalmazott kísérleti elrendezés lehetové teszi az agresszió kialakulásának specifikus, lépésenkénti nyomonkövetését. Patológiás agresszió során c-fos aktiváció térképezése nem történt meg, így ez a modell a mechanizmus 38
39 megvilágításán túl a fo kísérleti cél, az alacsony glukokortikoid szint következtében kialakuló patológiás agresszió teljesebb megértését is szolgálja. 3. Kialakul-e a glukokortikoid hipofunkcióval társuló patológiás agresszióban a normális territoriális agressziótól eltéro c-fos aktivációs mintázat, és ez változtatható-e glukokortikoid kezeléssel? Az aktivációs mintázat megváltozása utal azokra a neuronpopulációkra, amelyek muködése elsodlegesen eltér a normális agresszió során tapasztaltaktól, és rávilágít ezen területek célzott vizsgálatának fontosságára. Az ilyen területek kiszurése más metodikával csak rendkívül nehezen lehetséges. A glukokortikoid hipofunkcióban megjeleno eltéréseken túl a másik patológiás agressziómodellel való összehasonlítás lehetové teszi a patológiás agresszió közös elemeinek a leírását. II. Az agresszív interakció során a glukokortikoid hipofunkciós kísérleti állatok olyan magatartásmintázatot mutattak, melyek irodalmi adatok tanulsága szerint kizárólag életveszélyes szituációkban fordulhatnak elo. Ráadásul, a neuronális aktiváció feltérképezése során patológiás agresszióban a szorongással kapcsolatos agyterületek fokozott aktivitását tapasztaltuk. 4. Változik-e a szorongással kapcsolatos magatartás különbözo szorongástesztekben? A szorongással kapcsolatos magatartás megváltozása glukokortikoid hiányban és a patológiás agresszióban is felmerült. A kialakuló megváltozott szorongással kapcsolatba hozható a szerotoninerg rendszer érintettsége, amely a kóros agresszivitás esetében is jelentoséggel bírhat. 5. Megváltozik-e alacsony glukokortikoid szintek mellett a klinikumban is használatos 5-HT 1A parciális agonista buspiron hatékonysága szorongástesztekben? A glukokortikoid hiány eroteljesen befolyásolja a szerotoninerg rendszer muködését, és elsodlegesen az 5-HT 1A receptorok számát és funkcionalitását. Már korábban felmerült a glukokortikoid moduláció lehetosége ezen a receptoron ható vegyületek szorongásoldó hatásának vizsgálata kapcsán, de kísérletes bizonyítékot még nem írtak le az irodalomban. Humán patológiás agresszióban felmerült az 5-HT 1A receptorok megváltozott érzékenységének szerepe. III. Humán irodalmi adatok arra utalnak, hogy patológiásan agresszív egyéneknél jellemzo vegetatív eltérések (vészhelyzetben kontroll csoporthoz képest alacsonyabb 39
40 szívfrekvencia emelkedés, kisebb borellenállás-növekedés, ún. alacsony autonóm aktivációs szint) jelennek meg. A szívfrekvencia változását használtuk, mint a vegetatív aktivitás indikátorát. 6. Hogyan módosul a szívfrekvencia glukokortikoid hipofunkcióban a napi aktivitás és különbözo kihívások során? A vizsgált szituációk magukba foglalták a részletes nyomonkövetést teljes 24 órás nyugalmi ciklus, rezidens-betolakodó teszt (patológiás agresszió megjelenésekor), valamint különbözo szorongástesztek alatt. 40
41 4. Anyagok és módszerek 4.1. Állatok és tartási körülmények A kísérletek során használt állatok g súlyú Wistar hímek voltak (Charles River Laboratories). Általános laboratóriumi táp és ivóvíz szabadon az állatok rendelkezésére állt, a homérséklet (22±2 C) és a páratartalom (60±10%) állandó szinten tartását klimatikus berendezés biztosította. Mindegyik kísérlet magatartási elemek vizsgálatát is magába foglalta, melyek az irodalmi adatokkal összhangban az állatok aktív (sötét) periódusában kerültek végrehajtásra. Az állatokat fordított napszakos ritmusú szobában tartottuk, 12 órás váltakozó sötét / világos ciklusokkal (a sötét periódus kezdete az idoszámítástól függoen délelott 10, illetve 11 óra volt). A fordított napszakos ritmushoz az állatok legalább két hétig csoportosan (5-6 állat / ketrec) alkalmazkodtak. A magatartási kísérletek végrehajtására a sötét periódus elso óráiban került sor (12 és 14 óra között). Az általunk alkalmazott magatartási paradigmák megkövetelték az állatok egyedül tartását, ezért az adaptációs periódust követoen az állatokat izoláltuk (az alkalmazott mutétek után, illetve a magatartás vizsgálata elott egy héttel). Amennyiben két mutétre is sor került, a két mutét között egy hét telt el. A magatartási vizsgálatokat egy héttel a mutét után végeztük. Az agresszív magatartást vizsgáló kísérletekben (mind a territoriális, mind a hipotalamikus ingerléssel kiváltott agresszió során) ellenfeleket is használtunk, ezek súlya kisebb volt a vizsgálatunk tárgyát képezo állatoknál ( g). Ezeket az állatokat a fentieknek megfeleloen teljesen azonos laboratóriumi körülmények között tartottuk, de végig csoportosan. Mindegyik ellenfél a kísérletek során csak egyszer került felhasználásra. Mind a kísérleti állatok, mind az ellenfelek a kísérlet megkezdéséig semmilyen kezelésben vagy tesztben nem vettek részt. Az itt leírásra kerülo kísérletek végrehajtása az Európai Közösségi Tudományos Tanács eloírásának (86/609/EEC) megfeleloen, a Magyar Tudományos Akadémia Kísérleti Orvostudományi Kutatóintézet Állatjóléti Bizottságának felügyeletével és jóváhagyásával történt. 41
42 4.2. A kísérletek során használt anyagok Kortikoszteron pótlás, kortikoszteron kezelés A mellékvesék kétoldali eltávolítása után a teljes glukokortikoid hiány következtében kialakuló neuronális degeneráció megelozésére egy 25% kortikoszteront és 75% koleszterint (Sigma) tartalmazó 100 mg-os tablettát ültettünk be az állatok bore alá interscapularisan. Ilyen tabletták legalább három hétig stabilan 100 nmol/l körüli plazma kortikoszteron szintet eredményeznek 117. Ez a kortikoszteron szint nagyjából megegyezik az inaktív periódus során mért értékek átlagával. Akut kortikoszteron kezelések esetén, amikor kísérletesen próbáltuk helyreállítani a mesterségesen létrehozott gátolt reaktivitást, kortikoszteron-2-hidroxipropil-ßciklodextrin (kortikoszteron-hbc, Sigma-RBI) komplexet adtunk (0,25 illetve 0,5 kortikoszteron mg/kg dózisokban) ip. 10 perccel a magatartási teszt elott. A HBC biológiailag közömbös vegyület, amely megnöveli a kortikoszteron oldékonyságát és felszívódását, ezáltal alkalmassá teszi gyors (akár perces) hatások vizsgálatára. A kortikoszteron-hbc ip adást követo idogörbéje csoportunkban már korábban közlésre került 117, az általunk alkalmazott dózisok magas, stressznek megfelelo kortikoszteron szinteket eredményeznek ( nmol/l) (4. ábra). A kontroll állatok a HBC dózisának megfelelo injekciót kaptak. 4. ábra. Kortikoszteron-HBC dózis-ido görbéje. Mellékvese eltávolítása és lassú felszívódású, 25 mg kortikoszteront tartalmazó tabletta beültetése után (n=8) kortikoszteron-hbc komplex ip. beadásakor a plazmában mért kortikoszteron koncentráció. A 0,25 mg/kg kortikoszteron tartalmú dózis az agresszív interakció során megjeleno szintet jól modellezi. A beadás 0 percnél volt, a plazmaminták nyerése farokvérmintavétellel történt. Kortikoszteron (nmol/l) mg/kg kortikoszteron perc 42
43 Buspiron A pirimidinil-piperazinok közé tartozó szerotonin 5-HT 1A receptor agonista (preszinaptikusan teljes agonista, posztszinaptikusan parciális agonista) buspiron jelenleg Magyarországon egyetlen, a klinikumban forgalomban levo képviseloje ennek a szorongásoldó vegyületcsaládnak. A buspiront (Buspirone-HCl, Sigma) fiziológiás sóoldatban oldva 1 órával a magatartási tesztek elott ip. alkalmaztuk mg/kg dózisokban. A kontroll állatok fiziológiás sóoldatot kaptak A kísérletek során használt egyéb anyagok Az altatásnál használatos anyagokat és származási helyüket a mutéti fejezetben ismertetjük. Az immuncitokémiai eljárás során a fixálóhoz, pufferekhez és törzsoldatokhoz szükséges anyagokat az alábbiakban, míg az antitesteket és azok reagenseit az immuncitokémiai eljárásról szóló fejezetben ismertetjük. Foszfát puffer, fiziológiás sóoldatot tartalmazó (PBS, 0,1 M; 420 mosm, ph: 7,4): 1000 ml-re kiegészítve desztillált vízzel a következo anyagok: 1,56 g NaH 2 PO 4 (vízmentes); 15,1 g Na 2 HPO 4 x2h 2 O; 5 g NaCl és 0,2 g MgCl 2. Azidos-PBS esetén 4 g NaCl-t és 1 g Na-azidot használtunk (Spektrum 3D, illetve Fluka). Tris puffer (ph: 7,6): Trizma (Sigma) elokevert kristályokból (Tris-(hidroximetil)- aminometán és Tris HCl) 7,45 g 1000 ml desztillált vízben. Antitest higító oldat: azidos-pbs alapú, 1000 ml-ben 20 ml normál szérumot is tartalmaz. Streptavidin-konjugált tormaperoxidáz higító oldat: PBS alapú, 1000 ml-ben 20 ml normál szérumot és 1 g mertiolát-ot is tartalmaz. Fixáló (4% paraformaldehidet tartalmazó, PBS alapú): az A és B oldat összekeverésével, és ennek desztillált vízzel 1000 ml-re való kiegészítésével készült. A fixálót lehutve, 1 napon belül használtuk. A oldat: 400 ml desztillált vízben 40 g paraformaldehidet (Sigma) állandó keverés mellett fokozatosan 56ºC-ra melegítettük, és 10 N NaOH hozzáadásával feloldottuk, majd leszurtük. B oldat: 400 ml desztillált vízben 1,56 g NaH 2 PO 4 (vízmentes); 15,1 g Na 2 HPO 4 x2h 2 O; 5 g NaCl és 0,2 g MgCl 2 sókat feloldunk (Spektrum 3D, illetve Fluka). 43
44 4.3. Mutéti beavatkozások Adrenalektómia és kortikoszteron tabletta beültetés Mindkét mellékvese eltávolítása (adrenalektómia) elterjedt mutéti beavatkozás a legfontosabb mellékvesekéreg hormonok, a glukokortikoidok hatásainak vizsgálatához. A mutéti eltávolítás hátulsó feltárásból, középvonali hosszanti metszésbol történt ketamin-xylazin-prometazin ( mg/kg ip.) altatásban. A 2,5 cm-es legalsó háti csigolyánál történo bormetszést követoen a sebszéleket oldalra húzva a ferde hasizmokon tompán áthatolva a hasüreget megnyitottuk. A mellékvesét a vese felso pólusánál feltárva a szorosan körülölelo tokkal és zsírszövettel együtt egészben kiemeltük. Mint korábban részletesen elemeztük, kísérleti rendszerünkben célunk nem a teljes glukokortikoid hiány létrehozása volt, hanem stabilan alacsony és nem reaktív kortikoszteron plazma szintek elérése, ezért a mutét utolsó lépéseként egy 100 mg-os (25 mg kortikoszteron és 75 mg koleszterin tartalmú), lassú felszívódású tablettát ültettünk be a hát bore alá interscapularisan. A tabletta legalább 3 hétig stabilan 100 nmol/l körüli kortikoszteron szinteket biztosít 117, ez a kortikoszteron szint nagyjából megfelel patkányoknál a világos periódus, emberekben pedig a sötét periódus (kortizol), vagyis mindkét fajban az alacsonyabb értékeket mutató inaktív periódus átlagának. A bormetszést 4-5, fel nem szívódó, csomós varrattal zártuk. Álmutét során a bormetszést követoen a mellékveséket feltártuk, de nem távolítottuk el azokat. A mellékvesék eltávolítása után az operált állatok a víz mellett szabadon fogyaszthattak 0,9%-os fiziológiás NaCl oldatot is Hipotalamikus elektród beültetése Az itt alkalmazott anesztézia kismértékben különbözött a többi mutét során alkalmazottól, mivel ebben az esetben hosszabb altatást kellett biztosítanunk. Midazolam (5mg/kg, sc) adását követoen fluanizon - fentanylcitrát (10-0,135 mg/kg im.) kombinált altatásban végeztük a mutétet. Az állat fejét leborotváltuk és az állatot a sztereotaxikus készülékbe helyeztük. A mutéti terület gondos fertotlenítése után középvonali bormetszést ejtettünk, majd a galea átmetszése után a csonthártyát oldalra preparáltuk. A mutét során mindkét oldali hipotalamikus támadási központba egy-egy bipoláris elektródot ültettünk. Az elektród két darab helikálisan egymásra tekert 20 mm hosszú, 70 µm átméroju, teflon bevonatú platina-irídium (10%) drótszál (MedWire 44
45 PtIr3T). Az elektródákat a középvonali szinuszokat elkerülve a frontális síkban a középsíkhoz képest 10º-kal megdöntve ültettük be a hipotalamikus támadási központba a Paxinos és Watson atlasz 218 interaurális koordinátáinak (antero-posterior 6,7 mm; medio-lateral 1,02 mm; dorso-ventral 0,68 mm) megfeleloen. Egy indifferens elektródát (70 µm átméroju platina elektród, Johnson Ltd.) helyeztünk az agyfelszínen levo liquor felületéhez. Az elektródákat pillanatragasztóval (Cyanolith) a koponyához rögzítettük, majd egy miniatur konnektorhoz forrasztottuk. Négy rozsdamentes acél csavart rögzítettünk a koponyacsontba a cementsapka stabilizálásához (fogászati cement, Durelon -ESPE, D-8031, Seefeld/Oberbay, Hollandia), amely csak az ingerléshez használt berendezéshez csatlakoztatható konnektor felszínét hagyta szabadon. Az elektródák, a konnektor és az ingerléshez használt rendszer részletes leírását itt mellozzük Telemetriás transzmitter beültetése A rádiótelemetriás transzmitter beültetése elülso feltárásban történt, ketamin- xylazinprometazin ( mg/kg ip) altatásban. A Minimitter (Oregon, USA) transzmitterek 4000-es szériájának szívfrekvencia regisztrálására is alkalmas változatát (HR E-Mitter, PDT-4000) ültettük be (5. ábra) elektródák transzmitter test 5. ábra. A telemetriás adó helyzete. 45
46 A transzmitter teste tartalmazza a cserét nem igénylo (hosszú távú beültetésre is alkalmas) áramforrást, a helyjelzo lokátort, valamint a szívfrekvencia továbbítását végzo integrátort. A szívfrekvencia, lokomotoros aktivitás (és az általunk most nem részletezett testhomérséklet) rádiófrekvenciás jeleit egy, a ketrec alatt elhelyezett vevokészülék regisztrálja (külön minden egyes állatra vonatkozóan). A transzmitter beültetésekor a gyártó cég által javasolt beültetési eljárást kismértékben módosítottuk. Az általunk alkalmazott módszer mutéti felépülés és jeldetektálás tekintetében minoségileg hatékonyabbnak bizonyult. A gondosan szortelenített mutéti területet alkoholos fertotlenítést követoen a processus xyphoideus kitapintásával azt középpontnak tekintve kb. 3 cm-es hosszanti középvonali bormetszést ejtettünk. A hasüreg a középvonali bormetszést mélyre kiterjesztve megnyitásra került. A transzmitter testét a szabad hasüregbe behelyezve, az átvágott abdominális izomzat cranialis részén az izomban a sebszélektol 2 mm-re a negatív elektródot tartalmazó szárat jobb oldalon, míg a pozitív szárat a metszés bal oldalán az izmon átvezettük. Ezután az eredetileg alkalmazott bormetszés cranialis részén (a mellkas felett) a laza trabecularis bor alatti kötoszövetet lateralisan és cranialisan felpreparáltuk. A két elektródát úgy rögzítettük, hogy vékony fémszál segítségével az elektróda végén levo ferritgyurut a musculus pectoralis major-hoz erosítettük, a kívánt optimális lokalizációnak megfeleloen. A hasfalat ezek után két csomós öltéssel, majd a bormetszést 6-7 fel nem szívódó csomós öltéssel zártuk Magatartási tesztek Rezidens-betolakodó teszt Az általunk használt rezidens-betolakodó tesztet korábbi leírás alapján végeztük 103. A vizsgálat során használt dobozok mérete 60x40x50cm, az elülso átlátszó fal kivételével át nem látszó muanyag falakkal. A teszt idotartama 20 perc, erre az idore a betolakodókat a rezidens mellé helyeztük, és kamerával rögzítettük a magatartást (6.?ábra). A felvételeket utólag értékeltük ki a laborunkban kifejlesztett eseményregisztráló program (H77) segítségével. 46
47 6. ábra. A rezidens betolakodó teszt. 3. táblázat. A rezidens-betolakodó teszt során vizsgált magatartási elemek. Ellenfél jelenlététol függo magatartások Szociális magatartások szociális vizsgálódás (az ellenfél szagolgatása) kurkászás követés (a másik állat folyamatos lassú követése, szociális magatartáselem kiséretében) aláfurakodás rámászás Fenyegeto (támadásokat bevezeto) magatartások oldalfenyegetés (taszigálás, megközelítés, vagy mozgás borzolt szorrel, ívelt háttal a másik állat felé) agresszív kurkászás (durva, hirtelen kurkászás, az ellenfél lenyomása mellett) felegyenesedés (egyik / mindkét állat felegyenesedik, mellso végtaggal bokszolnak) üldözés (gyors mozgás a menekülo ellenfél irányába) rúgás (hátsó végtaggal a másik állat felé) Támadással kapcsolatos magatartások birkózó támadás (harapással járó, intenzív bírkózással járó támadás) egyszeru harapás (harapás, bírkózás jelenléte nélkül) Dominanciára / alárendeltségre utaló magatartások leszorítás aláfekvés Védekezo magatartások menekülés (gyors eltávolodó mozgás a másik állattól) aktív védekezés (felegyenesedéssel társul) dermedés (mozdulatlanul gubbaszt) Ellenfél jelenlététol független magatartások Exploráció (a környezet felderítése, vizsgálata) Pihenés (fekvés, látható nagyobb mozgások hiánya) Tisztálkodás (mosakodás, vakarózás) 47
48 Az agresszív interakció során megjeleno, általunk is regisztrált magatartási elemeket a 3. táblázat mutatja. Az alkalmazott paradigma szerint a rezidens gyozelmi esélyei a betolakodóval szemben nagyon magasak, mert saját területen vannak (legalább három nappal a teszt elott ezekbe a dobozokba kerülnek), és a súlyuk kb. 30%-kal meghaladja a betolakodók súlyát 39. A leírt feltételek mellett gyakorlatilag mindig a rezidensek kezdeményeznek agresszív magatartást és megverik a náluk kisebb betolakodót. Általánosságban egy rezidens annál agresszívebb, minél többet támad (harap), illetve minél több idot tölt el agresszív jellegu magatartásokkal. A feltüntetett paraméterek esetén mind az esemény gyakoriságát (frekvencia), mind a hosszát (az eltöltött ido az összes ido százalékában) regisztráltuk. A terjedelmes adatsor könnyebb áttekintése érdekében a fontosabb idotartamot tüntettük fel, ha a frekvencia irányultsága ettol eltért, akkor ezt is jeleztük. Egyetlen kivétel a harapás, amely olyan gyorsan zajlik, hogy frekvenciával célszerubb a jellemzése. Az agresszív magatartások közül a legeroteljesebb és legnagyobb sérülés okozására képes magatartási elem a harapással járó támadás. A fenyegeto magatartások jelzés értékuek, néha elengedoek az agresszív interakció kimenetelének eldöntéséhez, azonban a harapások jelentik a tényleges fizikai kényszerítést egy adott alárendeltségi helyzet elfogadására. A támadások irányultsága dönto jelentoségu, és csoportunk korábbi adatai szerint kiemelten fontos az alacsony glukokortikoid szintekhez társuló agresszióban (7.?ábra). fej nyak hát has 7. ábra. A betolakodó testfelületén a harapások irányultságának elkülönítése. Territoriális agresszió során a rezidensek az esetek túlnyomó részében a nem sérülékeny háti régiót támadják. A fejre, nyak ventrális részére, illetve hasra irányuló harapásokat veszélyes testfelületre irányuló támadásoknak tekintettük. 48
49 Megjegyezzük, hogy normális territoriális agresszióban a támadások irányultsága az esetek dönto többségében a háti területekre irányul, ahol a bor a legvastagabb, és ritkán alakul ki még eroteljes harapások után is sérülés 39. Azonban életveszélyes helyzetben, amikor 'már az etológiai konszenzus erejét veszti', a sérülékeny területekre irányuló támadások aránya megemelkedik, így fokozva az esélytelen számára a túlélés esélyét a nem túl sok jóval kecsegteto helyzetben 39,215. A harapás irányultságának meghatározásához a felvételeken lassítva, kockáról-kockára haladtunk. A következo célpontokat azonosítottuk: fej; nyak (fülek alatti ventrális terület); hát (fül mögötti dorzális terület), és has (végtagok közötti ventrális terület). A fejre, nyakra, és hasra irányuló támadásokat veszélyes, sérülékeny területre irányuló támadásoknak tekintettük Hipotalamikus ingerléssel kiváltott agresszió Az ingerlés 60 cm átméroju, átlátszó Perspex hengerekben történt, az állatoknak addig ismeretlen tesztszobában. A részletes eljárást itt csak rövidítve mutatjuk be 159,161. Az állatok fején cementtel rögzített miniatur konnektorhoz csatlakoztattuk az ingerléshez használt rendszert, majd közvetlenül ezután egy kisebb méretu ellenfelet helyeztünk a vizsgált egyedekhez. Ilyen körülmények között nincs spontán agresszív magatartás a két állat között. A 60 másodperces stimulációs periódusokat 60 másodperces szünetek követték. A bifázikus 40 Hz-es négyszögimpulzusokat (fázis tartam: 0,2 msec, fázis szünet: 12,5 msec) két izolált egyenáramforrás hozta létre (Grass PSIU6), amelyek a stimulátorhoz (Grass S88) kapcsolódtak; az indifferens elektródát földeltük. Az egymást követo ingerlések során az állat viselkedését a tesztszobában regisztráltuk. A kiváltott magatartástól függoen az ingerlés intenzitása is változott. Az egymást követo ingerlések során a kezdeti 20 µa áramerosséget 20 µa-es lépésekkel növelte a rendszer, egészen az elso harapás (támadás) megjelenéséig. A támadás regisztrálása után, a számítógéphez csatlakoztatott berendezés 20 µa-es lépésekben csökkentette az áramerosséget addig, míg a támadás elmaradt a 60 másodperces ingerlés során. Ettol kezdve a rendszer ismét emelte az áramerosséget egy újabb támadás megjelenéséig. Az ingerlés addig folytatódott, amíg a válaszkészségben (volt-e támadás vagy sem) hat változást nem detektált a rendszer, illetve ha támadás egyáltalán nem jelent meg, akkor 300 µa-es áramerosség eléréséig. Az ingerlésnél alkalmazott eljárás a válaszkészségtol függetlenül kb. 30 percig tartott. 49
50 Szociális interakció teszt Ez a teszt új környezeti kihíváson alapuló, szociális komponenst is magába foglaló (jelenleg az általánosan elfogadott tesztek közül az egyetlen, amely a szociális kapcsolatok természetét is vizsgálja), elterjedten alkalmazott szorongásteszt 92,108. A tesztben használt vizsgálati dobozok mérete megegyezik a rezidens-betolakodó tesztben leírtakkal. A teszt idotartama 10 perc, párhuzamosan hat kísérleti dobozban történik. A rezidens-betolakodó teszttel összehasonlítva a fo különbségek a következok: (1) a partnerek súlykülönbsége kisebb, mint 10%; (2) a partnerek ugyanolyan kezelést kapnak (pl. két alacsony glukokortikoid szinttel rendelkezo állat, vagy két 3 mg/kg buspiront kapott állat kerül össze egy dobozban egyidejuleg); (3) a tesztarénát idegen területként értékelo állatok vizsgálata történik. A tesztben párba kerülo állatok egymásnak ismeretlenek. A teszt alatt mutatott magatartást kamerával rögzítettük, és utólag a H77 programmal kiértékeltük. A rezidens-betolakodó tesztben leírt magatartási mintázatokat értékeltük a szociális interakció tesztben is. A teszt ideje alatt az agresszív viselkedés megjelenésének gyakorisága lényegesen kisebb, mint a rezidens-betolakodó tesztben, támadások ritkán vagy egyáltalán nem fordulnak elo, az agresszióval kapcsolatos magatartásokat egy összevont adattal szokták jellemezni. A szociális magatartásokkal töltött ido növekedése és az agresszióval kapcsolatos magatartásokra fordított ido csökkenése jellemzo a szorongásoldó hatásra, a pihenéssel töltött idotartam változása utal az esetleges szedatív hatásra 92, Megemelt keresztpalló teszt A megemelt keresztpalló (elevated plus-maze) 219 az egyik legelterjedtebb, újdonságon alapuló szorongásteszt. A megemelt középso platform két-két szemben levo nyílt (oldalfalakkal nem rendelkezo) illetve zárt (oldalfalakkal rendelkezo) karban végzodik (8. ábra). Kísérleteink során alkalmazott berendezés fából készült, sötétszürke nem tükrözodo festékbevonatú (kar hossz: 50 cm, kar szélesség: 20 cm, középso platform: 20x20 cm, zárt karokban a falmagasság: 30 cm, platform magasság: 80 cm). A teszt során a vizsgálati ido 5 perc, mely alatt a palló tompa vörös fénnyel van megvilágítva. Az egyes állatok között a pallót gondosan letisztítottuk. A kísérletek során az állatokat a középso platformra helyeztük, arccal a zárt karok felé. Az állatok magatartása az apparátus felett elhelyezett fényérzékeny kamera továbbított jelén 50
51 keresztül számítógépen rögzítésre és párhuzamosan értékelésre került egy erre a célra kifejlesztett, fényintenzitás különbség meghatározásán alapuló programcsomag segítségével (EthoVision, Noldus Inc.). 8. Ábra. Megemelt keresztpalló teszt. Az automatikusan detektált paraméterek a következok voltak: a nyílt és zárt karokba történo belépések száma, a nyílt és zárt karokban illetve középso platformon eltöltött ido (a teljes ido százalékában kifejezve). A nyílt kari preferenciát utólagosan számítottuk (a nyílt kari belépések százalékos aránya a karokba való összesített belépések számából). A teszt során a kezeletlen kísérleti állatok a nyílt tértol való félelem miatt elsosorban a zárt karokban tartózkodnak. A szorongás csökkenésével párhuzamosan a nyílt kari aktivitás fokozódik, szorongásoldó vegyületek fokozzák a nyílt kari aktivitást, míg szorongáskeltok csökkentik azt. A teszt kritikus változója szorongás tekintetében a nyílt karban töltött ido (másodlagos jelentoséggel bír a nyílt kari belépések száma és nyílt kari preferencia) 219. A lokomotoros aktivitás legjobb indikátora a zárt kari belépések száma Szövettani feldolgozás Perfúzió és immuncitokémia Az állatokat nátrium-pentobarbital (Nembutal, Sanofi, 50 mg/kg ip.) anesztézia után a mellkasfal gyors megnyitását követoen a bal kamra csúcsi részén ejtett kisméretu nyíláson keresztül a felszálló aortába vezetett kanülön keresztül perfundáltuk. Az ereket 51
52 átmosástuk eloször 150 ml 4 C-os fiziológiás sóoldat alapú 0,1M-os foszfát puffer segítségével (PBS), majd ~300 ml 4%-os paraformaldehidet (PBS alapú) áramoltattunk az érpályába. Az agyakat eltávolítottuk, ugyanilyen oldatban még 3 órát utófixáltuk. Az agyakat 15 óráig 20%-os szacharóz-pbs oldatba helyeztük, a fagyasztásos metszés során keletkezo szöveti roncsolódás elkerülése érdekében. Hat sorozat 30 µm vastag fagyasztott metszetet készítettünk frontális síkban Reichert mikrotómon. A metszeteket 0,1% Na-azidot tartalmazó PBS-ben tároltuk. Az immuncitokémiai protokoll alapja korábban publikálásra került 173. A c-fos p62 protein N terminálisát specifikusan felismero antitestet (nyúl, poliklonális, sc-52, Santa Cruz Biotechnology, USA) használtunk. Ez az antitest nem lép keresztreakcióba a Fos protein család többi tagjával. Röviden, az egyes lépések között 4x15 perces PBS öblítést alkalmaztunk. Az úsztatott metszeteket Triton-X-100 (0,2% PBS-ben, 20 perc) és normál szérum (2%, ló, 20 perc) kezelésnek vetettük alá. Az elsodleges antitesthez (1:10000, 48h) biotin-konjugált F AB láncot (kecskében termelt, nyúl ellen; 1:1000, 1h, Jackson Laboratories), majd streptavidin-konjugált tormaperoxidázt (1:1000, 1h, Jackson Laboratories) kapcsoltunk. A peroxidáz reakció Tris pufferben oldott diaminobenzidin tetrahidroklorid (0,2mg/ml), nikkel-ammónium szulfát (0,1%) és hidrogén-peroxid (0,003%) jelenlétében zajlott. A metszeteket tárgylemezre felhúztuk, és Depex segítségével fedtük c-fos pozitív sejtek analízise A metszeteket Paxinos és Watson atlasznak 218 megfeleloen vizsgáltuk. A kvalitatív analízis során a következo skálát használtuk: +++, nagyon eros; ++, eros; +, közepes; ±, gyenge,?, nincs reakció. A kvantitatív analízist ott végeztük, ahol a kvalitatív analízis különbségeket mutatott, illetve az agresszió szabályozásában kiemelt jelentoséggel bíró területeknél. A mikroszkópos képeket egy SONY CCD kamera segítségével digitalizáltuk, és a c-fos pozitív sejtek számát NIH-IMAGE (v1.66, Power Macintosh) programmal számítattuk. Egységes háttérküszöb használata mellett a pozitív elemek minimális méretét 5 pixelben határoztuk meg (240x-es nagyításnál). Minden vizsgált területre egy, az adott területre jellemzo standard keretet illesztettünk. A területeket két párhuzamos metszeten, bilaterálisan analizáltuk. Ez alól kivétel volt a hipotalamikus 52
53 támadási zóna ingerlésével kiváltott agresszió, ahol a stimulált és ellenoldal területeit külön értékeltük. A részletesen elemzett területek vizsgálati adatait a 4. táblázat mutatja. 4. táblázat. A c-fos analízis során használt vizsgálati adatok. Terület megnevezése Keret nagysága (mm 2 ) Vizsgálati sik (interaurálisan, mm) Piriform kéreg 0,068 9,70 Cinguláris kéreg 0,274 9,70 Laterális szeptum 0,257 9,20 Bed nucleus stria terminalis 0,127 9,20 Paraventrikuláris mag 0,068 7,20 Hipotalamikus támadási zóna 0,647 6,44 Centrális amigdala 0,337 6,44 Mediális amigdala 0,065 6,44 Mediodorzális talamikus mag 0,154 6,44 Középagyi centrális szürkeállomány 0,549 1,36 Dorzális raphe 0,404 1,36 Locus coeruleus 0,052-0, Rádiótelemetriás rendszer A szívfrekvencia és a saját-ketrec aktivitás mérése a VitalView adatgyujto és elemzo rendszer segítségével történt (MiniMitter, USA). A beültetett transzmitterek jelei egy elsodleges adatgyujto rendszeren keresztül a számítógépbe kerültek. A beérkezo adatok gyujtését és vizsgálatát a VitalView programmal végeztük. Az adatgyujtés során a mintavételezés gyakoriságát 1 percre állítottuk be, ez alól a magatartási tesztek ideje volt kivétel, ahol 1 másodpercre állítottuk a gyakoriságot. A napszakos ritmus analízisénél 1 órás összesített idoszakokat vizsgáltunk, míg a magatartási tesztekkel párhuzamosan végzett adatgyujtés során 1 perces lebontásban végeztük az analízist. A számítógépes értékelés során a program a szívfrekvencia detektálásakor a felületi, indifferens elektródot nem tartalmazó elvezetés R hullám-szeru pozitív hullámát regisztrálta, és az adatok a vizsgálati idotartamra vonatkozó összehúzódás/perc egységben kerültek megadásra. A motilitás értékét egy a VitalView által eloállított mesterséges egység alapján számoltuk, amit 1 perces idotartamra korrigáltunk. Abban az esetben, ha az adatgyujtés kritikus idotartama (a magatartási teszt) nem a saját ketrecben zajlott (pl. a szorongástesztek esetében), a kísérletek leírásánál ismertetett mintavételezési stratégiát követtük. 53
54 4.7. Hormonmérés A dekapitációval vagy farok metszéssel 94 nyert, EDTA tartalmú eppendorf csövekbe gyujtött, hidegen tartott vérmintákat 2500-as fordulatszámon 25 percig centrifugáltuk, a plazmamintákat -20 C-on tartottuk az analízisig. A radioimmunesszé (RIA) több sorozatban zajlott, de az egy kísérlethez tartozó összes mintát együtt analizáltuk. A mérés extrakció nélkül történt. A kortikoszteron antiszérumot kortikoszteronkarboximetilamin bovin szérum albumin ellen nyúlban termeltették. 125 I-dal kapcsolt kortikoszteron-karboximetilamin-tirozin-metilésztert használtunk jelöloanyagként. A plazma transzkortinnal való interferenciát a transzkortin alacsony ph-n történo inaktiválásával zártuk ki. Az esszé érzékenysége 1 pmol/ml volt Kísérleti protokollok 1. Territoriális agresszió (rezidens-betolakodó teszt) során kialakuló neuronális aktiváció meghatározása. Hím Wistar patkányokat ( g, n=10) egy héttel a tényleges kísérletet megelozoen a rezidensek számára fenntartott vizsgálati dobozokba helyeztük, ami biztosította a territórium kialakulását. A sötét periódus kezdete után két órával egy kisebb súlyú hímet ( g) helyeztünk az állatok feléhez (n=5, verekedésnek kitett) 20 perces idotartamra, míg az állatok másik fele (n=5, kontroll) nem kapott ellenfelet. Az agresszív interakció 20 percét videókamerával rögzítettük, és a késobbiekben egy eseményelemzo program (H77) segítségével részletesen kiértékeltük. A magatartási interakció során az összes állat ketrecében tompa vörös fényu (2X40W) megvilágítást alkalmaztunk, így a kontrollok ténylegesen csak az ellenfél behelyezését tekintve különböztek a másik csoporttól. Az agresszív interakció 20 percét követoen az ellenfeleket eltávolítottuk. Az agresszív interakció kezdetét követoen két órával az állatokat elaltattuk, perfundáltuk, az agyukat eltávolítottuk. Az agyakat az ismertetett protokoll szerint szövettanilag feldolgoztuk. Részletes, az eloagyra és az agytörzsre kiterjedo c-fos immuncitokémiai analízist végeztünk. 2. A hipotalamikus ingerléssel kiváltott agresszió során fellépo neuronális aktiváció meghatározása. Hím Wistar patkányok ( g) támadási zónájába bilaterálisan bipoláris elektródákat ültettünk. A beültetés után 1 héttel a sötét periódus kezdetén az állatokat a számukra ismeretlen, ingerléshez használt szobába vittük (n=14), ahol az ingerlés vizsgálatánál használt Perspex hengerekbe kerültek. A vizsgált állatok cementsapkájába beépített miniatur konnektoron keresztül az elektródákat az 54
55 ingerléshez használt rendszerhez csatlakoztattuk, és ezzel egyidejuleg egy kisebb súlyú ellenfelet ( g) helyeztünk az arénában levo állat mellé (a csatlakoztatás kb. 30 másodpercet vesz igénybe). Az állatok egy része az ellenfél behelyezését követoen a leírt protokollnak megfeleloen a támadási zónába irányuló impulzusokat kapott (n=9), míg a többi állat nem kapott elektromos ingerlést (n=5). A magatartást kamerával rögzítettük, de egyidejuleg a számítógép billentyuzetén keresztül is jeleztük a stimulációs programnak az agresszív, harapással járó támadás megjelenését. Ez vezényelte az áramerosség lépésenkénti emelkedését, illetve csökkenését. Az ingerlés eredményétol függetlenül az eljárás kb. 30 percig tartott, a nem stimulált kontrollok esetében is ennyit vártunk. A vizsgálati arénában eltöltött ido után az ellenfeleket eltávolítottuk, és a kísérlet alanyai visszakerültek a saját ketreceikbe. A kísérlet kezdetete után két órával az állatokat perfundáltuk, és az agyakat szövettanilag feldolgoztuk. 3. Tartósan alacsony és nem reaktív glukokortikoid szintek hatására kialakuló agresszió és neuronális aktiváció együttes leírása. Az addig csoportosan tartott állatokon ( g súlyú Wistar hímek, n=36) vagy álmutétet, vagy kétoldali mellékvese eltávolítást és alacsony kortikoszteron tartalmú tabletta beültetését végeztük. Ilyen kortikoszteron tabletta beültetése mellékvese eltávolítás után stabil, kihívásokra nem reagáló 100?nmol/l körüli kortikoszteron szinteket eredményez 117. A mutét után az állatok egyesével az agresszív interakció monitorozására alkalmas kísérleti dobozokba kerültek. A kísérlet során hat csoportra osztottuk az állatokat, a következo protokoll szerint. Az agresszív interakciót megelozoen tíz perccel 0,25 mg/kg kortikoszteron, illetve vehikulum injekciót adtunk az állatoknak, hogy az ellenfél megjelenésekor kialakuló kortikoszteron választ modellezzük kortikoszteron szekréciót nem mutató állatoknál. Az agresszív interakció az injekciót követoen 10 perccel kezdodött, és 20 percig tartott. A csoportok könnyebb átláthatósága miatt ezt külön tüntettük fel (5. táblázat). A rezidens-betolakodó teszt ideje alatt tompa vörös fényu megvilágítást használtunk, a teszt végén a betolakodókat eltávolítottuk. A rezidens-betolakodó teszt alatt mutatott magatartás kamerával rögzítettük, és késobb a H77 eseményelemzo program segítségével értékeltük. A korábban leírtakhoz hasonlóan az állatokat perfundáltuk, az agyakat eltávolítottuk, és részletes szövettani feldolgozást végeztünk. 55
56 5. táblázat. Az alkalmazott kezelések glukokortikoid hipofunkció kapcsán. Csoport Adrenalektómia Akut kezelés Ellenfél Kontroll? HBC? ADX r + HBC? ADX r + B + Kortikoszteron-HBC? Kontroll -agresszív? HBC + ADX r -agresszív + HBC + ADX r + B -agresszív + Kortikoszteron-HBC + Adrenalektómia esetén 25 mg kortikoszteront tartalmazó lassú felszívódású tablettát ültettünk be, a kontrolloknál álmutétet végeztünk. Az akut kezelést 10 perccel az interakció elott, 0,25 mg/kg kortikoszteron-hbc ip injekció formájában végeztük. 4. Tartósan alacsony és nem reaktív glukokortikoid szintek hatása a szorongásra megemelt keresztpalló és szociális interakció tesztekben. Az alacsony glukokortikoid szint esetén kialakuló patológiás magatartásmintázat megjelenése ép glukokortikoid szekrécióval rendelkezo állatok esetében kizárólag életveszélyben fordul elo. Ez a tény, valamint a részletes szövettani elemzés adatai arra utaltak, hogy a szorongással kapcsolatos magatartás jelentoséggel bírhat a patológiás agresszió megjelenésében. Ezekben a kísérletekben g súlyú Wistar hímeket használtunk. Az addig csoportosan tartott állatokon (n=20) álmutétet, illetve mellékvese eltávolítást és kortikoszteron tabletta beültetést végeztünk. A kísérletben két csoportot használtunk, a kontroll (álmutött, n=10) és az alacsony glukokortikoid szintekkel rendelkezo (ADX r, n=10) csoportokat. A mutét után az állatokat izoláltuk. Egy hét felépülési idoszakot követoen tompa vörös megvilágítás mellett a sötét periódus elso óráiban az állatok 5 perces megemelt keresztpalló tesztben vettek részt, mely után közvetlenül és egy nap elteltével a kortikoszteron szintek meghatározására farokmetszéssel vérmintát nyertünk. A megemelt keresztpalló teszt után egy héttel az állatok szociális interakció tesztben vettek részt. A megemelt keresztpalló tesztben mutatott magatartást az EthoVision analizáló rendszer segítségével, míg a szociális interakció tesztet a H77 program segítségével utólag értékeltük. 56
57 5. Buspiron hatása a szorongásra megemelt keresztpalló és szociális interakció tesztben. Az irodalmi háttérben részletesen tárgyaltaknak megfeleloen vizsgáltuk az 5- HT 1A receptorok muködésének lehetséges funkcionális eltéréseit a glukokortikoid szintekkel összefüggésben, amely a megváltozott szorongással és patológiás agresszióval kapcsolatba hozható. Párhuzamosan vizsgáltuk Wistar hímekben ( g) a buspiron (parciális 5-HT 1A agonista) hatását a szorongásra ép glukokortikoid szekréció mellett ( mg/kg dózisokban ip., 1 órával a tesztet megelozoen) megemelt keresztpalló (n=12-9-9) és szociális interakció tesztekben (n= ). A tesztet követoen dekapitációval nyert vérbol kortikoszteron szint meghatározást végeztünk. A megemelt keresztpalló tesztben mutatott magatartást az EthoVision analizáló rendszer segítségével, míg a szociális interakció tesztet a H77 program segítségével utólag értékeltük. 6. Buspiron hatása a szorongásra tartósan alacsony glukokortikoid szintek esetében. Wistar hímekbol ( g) a mellékveséket eltávolítottuk, és a borük alá kortikoszteron tablettát ültettünk (n=72). Eloször 36 állattal szociális interakció tesztet végeztünk, melyben a buspiron hatását (ip mg/kg, 1 órával a teszt elott; n= ) teszteltük. A tesztet követoen farokmetszéssel nyertünk vért kortikoszteron meghatározás céljából. A másik 36 állattal vizsgáltuk a kortikoszteron moduláló szerepét. Ebben a kísérletben az adrenalektomizált állatok 0 vagy 10 mg/kg buspiront kaptak (ip, 1 órával a szociális interakció teszt elott). Ezután 50 perccel (10 perccel a teszt elott) a kontroll állatok HBC injekciót kaptak. A nagyobb buspiron dózisban (10 mg/kg ip.) intakt állatoknál megjeleno kortikoszteron szint emelkedést 10 perccel a teszt kezdete elott adott 0,5 mg/kg kortikoszteron-hbc injekcióval modelleztük az egyik csoportban, míg HBC injekciót kapott a másik 10 mg/kg buspiront kapott csoport (n=12 mindhárom csoportban). A tesztet követoen farokmetszéssel nyertünk vért késobbi kortikoszteron meghatározáshoz. A tesztben mutatott magatartást utólag értékeltük a H77 program segítségével. 7. Tartósan alacsony glukokortikoid szint hatása a vegetatív paraméterek napszakos ingadozására. A vegetatív paraméterek alakulása glukokortikoid hipofunkció indukálta patológiás agresszió és szorongás során. Ezekben a kísérletekben az állatokon két mutétet végeztünk. Az elso mutét a mellékvesék eltávolítása és glukokortikoid tabletta beültetése volt, míg a második mutétre egy héttel késobb került sor, ekkor a 57
58 rádiótelemetriás transzmitterek kerültek beültetésre. A második mutét után egy héttel végeztük a magatartási kísérleteket. Az egyik kísérletsorozatban végzett mérésekbol (n=12, az álmutött és az ADX r csoportban) a napi ingadozást és a szorongástesztekben mutatott magatartás során megjeleno szívfrekvencia választ, valamint a motilitást határoztuk meg, a magatartást kamerával rögzítettük. A napi ingadozás meghatározására a második mutétet követo ötödik napot használtuk, a mutétet követo hetedik napon került sor a megemelt keresztpalló tesztre, míg újabb öt napot követoen végeztük el a szociális interakció tesztet. Ebben a kísérletsorozatban technikailag nem tudtuk megoldani a teszt elotti, alatti és utáni közvetlen regisztrációt (pl. a megemelt keresztpalló teszthez a vevokészülékeket a megemelt keresztpalló karjai alá kellett helyezni, amelynek beállítása idoigényes -több órás- muvelet). Így ebben a kísérletsorozatban a reaktivitás meghatározása érdekében elozoleg kísérletmentes napon gondosan regisztráltuk a szívfrekvencia változását, és a tesztmentes napon ebben az idoben vett értékekbol képzett stabil átlagot tekintettük az ún. alapértéknek. A megemelt keresztpalló tesztben csoportonként állatot vizsgáltunk, de csak azoknak az állatoknak az eredményeit értékeltük, akik mind a nyílt, mind a zárt karban jelen voltak a teszt 5 perces idotartama alatt (ez álmutött kontroll esetében n=8, míg ADX r csoportban n=7 volt). Ezzel lehetové vált a nyílt és zárt karban megjeleno szívfrekvencia értékekre vonatkozó összehasonlító analízis elvégzése. Egy másik kísérletsorozatban hasonlóan a két mutét után a saját ketrecben lezajló rezidensbetolakodó tesztben mutatott aktivitást határoztuk meg, erre a mutétet követo hetedik napon került sor (n=14, az álmutött és az ADX r csoportban). Az utóbbi kísérleti felállásban folyamatosan és a teszt ideje alatt is a vevokészülékek az állatok saját ketrece alatt helyezkedtek el, így lehetoségünk volt az aktivitás változások folyamatos regisztrálására (a magatartási tesztet közvetlenül megelozo és az azt követo idoszakban). Mindkét kísérletsorozatban az utolsó magatartási kísérletet követo napon farokmetszéssel vért vettünk kortikoszteron meghatározás céljából. A magatartási tesztek a korábbiakban említetteknek (és az irodalmi ajánlásoknak) megfeleloen megemelt keresztpalló teszt esetén 5 perc, szociális interakcióban 10 perc, míg rezidensbetolakodó tesztnél 20 percig tartott. 58
59 4.9. Statisztikai kiértékelés Az egyes csoportokra jellemzo adatokat átlag±se formában jelöltük, a statisztikai elemzéseket a STATISTICA program (Statistica Inc., Tulsa, USA) használatával végeztük. A magatartási tesztek adatainak értékelésénél a nem paraméteres változók elemzésére alkalmas Kruskal-Wallis tesztet használtuk. A hormonmérések, a c-fos adatok és a telemetriás rendszerbol származó adatok értékelésénél variancia analízist (ANOVA) használtunk (egy-, illetve két-utas ANOVA, ismételt mérésekre kidolgozott ANOVA, két-utas ANOVA függo kontroll csoporttal). A csoportok közötti páros összehasonlítások során nem paraméteres változók esetében Mann-Whitney féle U tesztet, míg paraméteres változóknál Newman-Keuls tesztet használtunk. Szignifikánsnak a p<0,05 értékeket tekintettük, többszörös összehasonlítás után Holmféle korrekciót alkalmaztunk. 59
60 5. Eredmények 5.1. Glukokortikoid hipofunkció hatása az agresszív viselkedésre és az agresszív viselkedés szabályozásában részt vevo agyterületek neuronális aktivitására. Patológiás agresszió során fellépo aktivitásmintázat Neuronális aktiváció territoriális agresszió során. A rezidens-betolakodó tesztben mindegyik kísérleti állat agresszív magatartást mutatott, átlagosan 8,0±2,5 esetben támadták meg a kisebb betolakodót. A támadások nagy része nem sérülékeny (háti) területekre irányult (7,2±2,0). A hasi régió volt az egyedüli sérülékeny terület, ahova kis számban ugyan, de irányult támadás (0,8±0,5). Így a sérülékeny támadások aránya az összes támadásból egyedi átlagra vonatkoztatva alacsonynak (0,06±0,04) mutatkozott. A teszt 20 perce alatt mutatott magatartás egyéb adatait a 6.?táblázat mutatja. 6. táblázat. Rezidens-betolakodó tesztben az egyes magatartásokkal töltött ido (a teljes ido %-a). Felderíto Piheno Tisztálkodó Szociális Fenyegeto Védekezo Domináns Alárendelt 45,8±1,8 17,5±1,2 17,1±3,9 7,5±0,7 4,3±0,8 0,7±0,7 5,5±1,1 0,1±0,1 A c-fos immuncitokémia kiértékelése során minden állatból egyedi kvalitatív térképet készítettünk, amelynek reprezentatív adatait a 7. táblázat mutatja. Részletes analízist az agresszív viselkedés szabályozásában kulcsfontosságú, illetve a jelentos különbségeket mutató területeken végeztünk. A kvantitatív analízis során az aktiválódott sejtek számának nagyfokú növekedését figyeltük meg (9. ábra) a cinguláris kéreg (F (1,8) =21,37; p<0,002), piriform kéreg (F (1,8) =44,22; p<0,001), laterális szeptum (F (1,8) =16,89; p<0,003), BNST (F (1,8) =54,37; p<0,001), mediodorzális talamikus mag (F (1,8) =44,62; p<0,001), mediális amigdala (F (1,8) =83,31; p<0,001), támadási zóna (F (1,8) =243,03; p<0,001), a PAG laterális részén (F (1,8) =103,26; p<0,001) és a locus coeruleus területén (F (1,8) =19,84; p<0,002). Kisebb, de szignifikáns különbség mutatkozott a centrális amigdala (F (1,8) =15,60; p<0,02) területén. Nem volt különbség a PVN (F (1,8) =1,23; p=0,29) és a dorzális raphe (F (1,8) =0,01; p=0,94) aktivációjában. 60
61 7. táblázat. Kvalitatív c-fos térkép territoriális és hipotalamikus agresszióban. Terület Territoriális Hipotalamikus agresszió Stimulált Kontroll Agresszív Kontroll Agresszív Nem-agresszív Ipszi Kontra Ipszi Kontra Kéreg Cinguláris Piriform Bazális ganglionok Caudatoputamen??????? Szeptális régió Mediális szeptum ± Laterális szeptum ± Bed nucleus stria terminalis ± Preoptikus terület Medián preoptikus mag Mediális preoptikus terület Laterális preoptikus terület ± Hipotalamusz Szuprakiazmatikus mag Szupraoptikus mag ± +? Elülso hipotalamikus terület ± ++? / Laterális hipotalamikus terület ± +? Periventrikuláris mag ± ±? Paraventrikuláris mag (magno) ± ±? + +?? Paraventrikuláris mag (parvo) Arkuátusz mag Dorzomediális mag ± ++? Ventromediális mag? +? Hipotalamikus támadási zóna ± ++/ Talamusz Paraventrikuláris mag Mediodorzális mag? Hippokampusz CA1/CA2/CA3/CA4? ±? + +?? Dentate gyrus? ±????? Amigdala Mediális mag ± ++/ /+++ + Kortikális mag ± Centrális mag ± +? ++/+++??? Laterális mag ± +? ++? + + Agytörzs Centrális szürkeállomány ± ++/ / / Dorzális raphe ± ± Medián raphe ± ±??? Paramedián raphe ± ±????? Raphe magnus??????? Raphe interpositus??????? Locus coeruleus ± +? A territoriális és hipotalamikus agresszió során megjeleno aktiváció az agresszió szempontjából kulcsfontossággal bíró, illetve az eros aktivációt mutató területeken. Ipszi/Kontra= ipszi-vagy kontralateálisan az elektromos stimulációhoz képest. Aktivitási skála: +++= nagyon eros; ++= eros; += közepes; ±= gyenge;?= nincs c-fos reakció. 61
62 120 * c-fos pozitív sejtmagok / terület * * * * * # * * * 0 PC CC LS BNST MD PVN CeA MeA HAA PAG DR LC Kontroll Verekedésnek kitett 9. ábra. Territoriális agresszió során (20 perces rezidens-betolakodó teszt) kialakuló aktiváció egyes agyterületeken. Az adatok átlag ± SE értékben vannak megadva. Az értékelés során ANOVA tesztet használtunk, a jelölések a csoportok között megjeleno szignifikáns különbségeket mutatják (*-p<0,01; #-p<0,05). BNST= bed nucleus stria terminalis; CeA= centrális amigdala; CC= cinguláris kéreg; DR= dorzális raphe; HAA= hipotalamikus támadási zóna (attack area); LC= locus coeruleus; LS= laterális szeptum; MD= mediodorzális talamikus mag; MeA= mediális amigdala; PAG= centrális szürkeállomány; PC= piriform kéreg; PVN= paraventrikuláris hipotalamikus mag (parvocelluláris rész). 62
63 Neuronális aktiváció hipotalamikus ingerléssel kiváltott agresszió során. Az állatokat az ingerlés alatt mutatott viselkedésüknek megfeleloen utólag további csoportokra osztottuk, az állatok a hipotalamikus támadási zóna stimulációját követoen nem szükségszeruen mutattak támadó magatartást (8. táblázat). 8. táblázat. A hipotalamikus támadási zóna ingerlése után kialakult csoportok (n). Csoport Elektróda Ellenfél Ingerlés Harapás Hipotalamikus kontroll (5) + +?? Stimulált nem támadó (4) + + +? Stimulált támadó (5) A kísérlet során a kontroll állatok elsosorban a teszt-ketrecet explorálták és nemagresszív szociális kontaktusokat létesítettek a partnerekkel. A stimulált állatok az ingerlések közötti szünetekben a nem-stimulált állatokkal megegyezo magatartást mutattak. A stimulált állatok közül öt az ingerlés alatt megtámadta az ellenfelét (10,50±1,55 támadás, ez a territoriális agresszió során mutatott támadások számától nem különbözik), míg négy stimulált állat nem mutatott agresszív magatartást. A beültetett és ingerlésre használt elektródák helyzete nem mutatott különbséget a stimulált és támadó, illetve nem támadó állatok között. Az interaurális referencia ponthoz képest az elektródák helyzete a következo volt: 1. támadó állatok: anterioposzterior (A-P) 6,65±0,05 mm; medio-lateral (M-L) 1,08±0,06 mm; dorzo-ventral (D- V) 0,34±0,02 mm; 2. nem támadó állatok: A-P 6,69±0,15 mm; M-L 0,95±0,09 mm; D- V 0,40±0,07 mm. Ezen elektródok mindegyike elérte a támadási zóna területét 168. Az immuncitokémiai reprezentatív kvalitatív analízis eredményét a 7. táblázat mutatja. A kvantitatív analízis eredménye a 9. táblázatban, reprezentatív metszetek a 10. ábrán láthatóak. A statisztikai analízis során két utas ANOVA tesztet (támadás megjelenése, illetve stimulált oldal) végeztünk függo kontroll csoporttal való összehasonlítással (hipotalamikus kontroll). A territoriális agresszióval való összehasonlíthatóság kedvéért az egyes területeket külön is feltüntettük (11. és 12. ábra). 63
64 9. táblázat. Neuronális aktiváció (c-fos pozitív sejtmagok/terület) és részletes statisztikai adatok hipotalamikus ingerlés során. Terület Kontroll Agresszív Nem-agresszív F 1(p) F 2(p) F i(p) ipszilaterális kontralaterális ipszilaterális kontralaterális Cinguláris kéreg 60.1± ±12.0 ab 100.4±9.0 ab 66.0± ± (0.01) 0.89(0.36) 0.23(0.64) Piriform kéreg 30.8± ±3.0 ab 56.7±2.9 ab 28.5± ± (0.0001) 1.03(0.32) 0.20(0.66) Laterális szeptum 31.2± ±26.9 a 113.7± ±49.2 a 94.0± (0.13) 7.00(0.02) 0.90(0.36) Bed nucleus stria terminalis 12.9± ±9.8 abc 48.6±4.2 a 93.7±10.7 ac 57.4±9.4 a 7.92(0.01) 73.59(0.0001) 15.48(0.001) Paraventrikuláris mag 21.4± ±8.4 ab 95.1±6.7 ab 59.4±13.3 a 52.9±16.2 a 16.68(0.0007) 0.50(0.49) 0.01(0.93) Centrális amigdala 7.6± ±22.7 abc 12.6± ± ± (0.0008) 12.86(0.002) 12.03(0.003) Mediális amigdala 12.4± ±11.2 abc 56.4±2.0 a 73.0±13.6 ac 35.6± (0.0003) 40.65(0.0001) 3.78(0.07) Hipotalamikus támadási zóna 42.4± ±31.6 abc 127.7±13.3 a 235.6±42.1 ac 73.2± (0.0002) 82.93(0.0001) 6.24(0.02) Mediodorzális talamikus mag 56.3± ±12.3 ab 121.1±13.5 ab 75.5± ± (0.0002) 1.73(0.21) 0.27(0.61) Középagyi szürkeállomány 19.2± ±7.0 ac 45.8± ±22.9 ac 44.0± (0.84) 18.32(0.001) 0.01(0.96) Locus coeruleus 5.5± ±9.3 a 39.2±12.2 a 68.6±16.9 a 51.7±16.8 a 0.27(0.61) 3.48(0.08) 0.25(0.63) Az adatok átlag? SE értékben vannak kifejezve. F 1 : ANOVA F az agresszivitás; F 2 : agyi oldal; Fi: interakcióval kapcsolatban. A betujelek szignifikáns különbséget jeleznek post hoc tesztben a =kontroll; b =nem-agresszív; c =ellenkezo oldal szerinti összehasonlításban. 64
65 10. ábra. Reprezentatív metszetek hipotalamikus agresszió során megjeleno aktivációból. A metszetek a mediális amigdala (A-C-E) és a hipotalamikus támadási zóna (B-D-F) területérol hipotalamikusan stimulált és támadó állat stimulált (A-B) és nem stimulált oldaláról (C-D), illetve ellenfélnek kitett, de nem stimulált (és nem támadó) hipotalamikus kontroll csoportból (E-F) származnak. A stimulált és támadó állatok ellenoldalán mutatott c-fos jelintenzitás és mintázat nagymértékben megegyezik a territoriális agresszió során látott aktivációval. A nyíl az ingerléshez használt elektróda végének helyét jelzi. AN= hipotalamikus arkuátusz mag; CoA= kortikális amigdala; HAA= hipotalamikus támadási zóna (attack area); OT= tractus opticus; VMH= ventromediális hipotalamikus mag. Lépték: 200? m. 65
66 * Piriform kéreg ab ab * Cinguláris kéreg ab ab c-fos pozitív sejtmagok * BNST abc a ac a * Laterális szeptum a a Mediodorzális talamikus mag ab ab * Kontroll (territoriális) Agresszív (territoriális) Hipotalamikus kontroll Hipotalamikus agresszív -stimulált oldal Hipotalamikus agresszív -nem stimulált oldal Hipotalamikus nem agresszív -stimulált oldal Hipotalamikus nem agresszív -nem stimulált oldal 11. ábra. Területenkénti lebontásban c-fos aktiváció territoriális és hipotalamikus agresszióban. Az adatok átlag? SE értékben vannak megadva, a könnyebb összehasonlíthatóság miatt ismételten ábrázolva. *-p<0,05 territoriális agresszióban. A betujelek szignifikáns különbséget jeleznek (p<0,05) post hoc tesztben a = kontroll; b = nem-agresszív; c = ellenkezo oldal szerinti összehasonlításban. A stimuláció önmagában (támadás nélkül) szignifikáns emelkedést okozott az ipszilaterális laterális szeptum, BNST, parvocelluláris PVN, mediális amigdala, hipotalamikus támadási zóna, periakveduktális szürkeállomány és a locus coeruleus területén. Az aktiváció kétoldali volt a BNST, PVN és a locus coeruleus esetében. A BNST aktivációja az ipszilaterális oldalon erosebb volt, mint az ellenkezo oldalon. A támadó állatokban (a nem támadó állatokhoz képest is) az aktiváció tovább fokozódott a BNST, PVN, mediális amigdala és hipotalamikus támadási zóna területén. A centrális amigdala kizárólag a támadó állatokban mutatott nagyfokú aktivitásfokozódást. A cinguláris kéreg, piriform kéreg és a mediodorzális talamusz mag aktivációja bilaterálisan, oldalkülönbség nélkül fokozódott a támadó állatokban (az aktivitás szintje ezekben a magokban megegyezett a másik két hipotalamikus csoportban, és nagyságrendileg a territoriális agresszióban mutatott aktivitással). 66
67 Oldalkülönbség nélküli kétoldali aktiváció volt jelen a PVN-ben és a locus coeruleusban. Kétoldali fokozott aktivációt mutatott a stimulált oldal dominanciájával a BNST, mediális amigdala és a hipotalamikus támadási zóna * Mediális amigdala abc a ac * Centrális amigdala abc c-fos pozitív sejtmagok Hipotalamikus támadási zóna abc ac a * Hipotalamikus paraventrikuláris mag ab ab a a Központi szürkeállomány Locus coeruleus ac 100 ac a 80 a * * 20 0 a a 12. ábra. Területenkénti lebontásban c-fos aktiváció territoriális és hipotalamikus agresszióban. Az adatok átlag? SE értékben vannak megadva, a könnyebb összehasonlíthatóság miatt ismételten ábrázolva. *-p<0,05 territoriális agresszióban. A betujelek szignifikáns különbséget jeleznek (p<0,05) post hoc tesztben a = kontroll; b = nem-agresszív; c = ellenkezo oldal szerinti összehasonlításban. Jelöléseket lásd a 11. ábránál Neuronális aktiváció glukokortikoid hipofunkció során megjeleno agresszióban. Mindegyik ellenfelet kapott kísérleti állat megtámadta a betolakodót. A támadások összesített száma nem változott az egyes csoportok között, azonban a sérülékeny testfelületre irányuló támadások aránya az ADX r -es csoportokban mintegy tízszeresére megemelkedett. A fejre irányuló támadások száma szignifikánsan megemelkedett (álmutött állatoknál nem fordult elo, H=7,62, p<0,02); az egyéb területekre irányuló, illetve összesített támadások száma nem mutatott szignifikáns különbséget. Akut kortikoszteron injekció (0,25 mg/kg) visszaállította a sérülékeny testrészekre irányuló támadások arányát. A támadások számát és irányultságát a 10. táblázat mutatja. 67
68 10. táblázat. A harapások irányultsága glukokortikoid hipofunkcióban. Csoport Támadási célpontok Fej* Nyak Has Hát Összes harapás Sérülékeny / összes harapások* Kontroll 0.00 ± ± ± ± ± ± 0.07 ADX r 2.50 ± 0.84* 1.25 ± ± ± ± ± 0.06* ADX r +B 0.29 ± ± ± ± ± ± 0.05 H(2) p< 0.03* * Az értékek átlag ± SE -ként kerültek bemutatásra. Kontroll: álmutött + 10 perccel a teszt elott HBC injekciót kapott; ADX r : adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott HBC injekciót kapott; ADX r +B: adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott kortikoszteron-hbc injekciót kapott (0,25 mg/kg kortikoszteron). H(2), p = Kruskal-Wallis koefficiens, illetve p érték. *-szignifikánsan különbözik a kontrolltól Mann-Whitney post hoc tesztben (p<0,025). A többi magatartással töltött idotartamot (a teljes idotartam %-a) a 11. táblázat mutatja. 11. táblázat. Rezidens-betolakodó tesztben mutatott magatartások glukokortikoid hipofunkcióban. Csoport Felderíto Piheno Tisztálkodó Szociális Támadó Védekezo Domináns Alárendelt Kontroll 60,0±3,8 0,6±0,3 16,1±5,9 6,0±1,1 10,4±1,8 ab 1,9±1,3 1,4±0,8 0,3±0,3 ADX r 54,6±3,1 0,9±0,3 17,4±4,3 4,7±0,7 7,0±1,3 a 5,23±1,4 5,6±2,5 1,4±0,6 ADX r +B 53,2±3,1 2,3±0,9 14,6±2,7 5,7±1,0 13,9±2,0 b 3,7±1,5 1,5±0,8 0,9±0,7 H(2) 1,61 3,96 0,06 0,72 7,78 1,69 0,36 1,95 p< 0,45 0,14 0,97 0,70 0,02* 0,43 0,83 0,38 Az értékek átlag ± SE -ként kerültek bemutatásra. Kontroll: álmutött + 10 perccel a teszt elott HBC injekciót kapott; ADX r : adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott HBC injekciót kapott; ADX r +B: adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott kortikoszteron-hbc injekciót kapott (0,25 mg/kg kortikoszteron). H(2), p = Kruskal-Wallis koefficiens, illetve p érték. A különbözo betujellel ellátott csoportok a post hoc tesztben mutatott szignifikáns különbséget jelzik. A fenyegeto magatartások idotartama szignifikáns emelkedést mutatott kortikoszteron kezelés hatására, a többi agresszióval kapcsolatos paraméter nem mutatott szignifikáns különbséget. Nem mutatkozott különbség a szociális, illetve az ellenfél jelenlététol független változókban. Az agresszív viselkedés során megjeleno c-fos mintázat az áloperált és HBC injektált állatokban mind a verekedésnek kitett, mind az ellenfelet nem kapó állatokban megfelelt a korábbi kísérletekben territoriális agresszióban részt vevo normál (nem operált) 68
69 állatoknál látott mintázatnak. A kvalitatív térképet a 12. táblázat mutatja. A kvantitatív analízis során két utas ANOVA tesztet használtunk (agresszió teszt(f agr ) és glukokortikoid háttér (F Cort )) (13. ábra). A c-fos aktiváció szignifikánsan megemelkedett verekedés hatására a mediális amigdala, támadási zóna és PAG területén (F agr (1,30)=152,33; p agr <0,001; F agr (1,30)=109,18, p agr <0,001; F agr (1,30)=31,22; p agr <0,001). Sem az ADX r, sem az akut kortikoszteron kezelés nem befolyásolta az aktivációt ezeken a területeken (F Cort (2,30)=0,81; p Cort =0,50; F Cort (2,30)=0,01; p Cort =0,90; F Cort (2,30)=1,41; p Cort =0,26). Ezzel ellentétben, mind a PVN, mind a centrális amigdala aktivációját befolyásolta a kortikoszteron háttér. A c-fos aktiváció a parvocelluláris PVN-ben nem függött az agresszív interakciótól (F agr (1,30)=0,05; p agr =0,80), de a kortikoszteron háttértol igen (F Cort (2,30)=10,56; p Cort <0,001), a faktorok között nem volt statisztikai interakció. Úgy tunik, a kísérleti körülmények között az ADX r önmagában megnövelte a PVN aktivitását, amelyet a verekedés nem befolyásolt, de az akut kortikoszteron injekció az álmutött kontroll állatok szintjére csökkentett. A centrális amigdalában szignifikánsan megemelkedett a c-fos pozitív sejtek száma verekedés hatására (F agr (1,30)=5,63; p agr <0,02). Az itt megjeleno aktivációt a kortikoszteron háttér is befolyásolta (F Cort (2,30)=27,16; p Cort <0,001), valamint a két faktor között szignifikáns interakció lépett fel (F INT (2,30)=3,68; p INT <0,04). Az ADX r megnövelte a centrális amigdala aktivációját azokban a rezidensekben is, amelyek nem kaptak ellenfelet, és ez az aktiváció tovább erosödött verekedés hatására. Akut kortikoszteron injekció az álmutött állatokkal megegyezové tette az aktivitást a centrális amigdala területén. A 14. és 15. ábrák mutatják be a PVN, centrális és mediális amigdala területén bekövetkezo változásokat. 69
70 11. táblázat. Glukokortikoid hipofunkcióban mutatott agresszió során kialakuló c-fos aktiváció. Terület Nem-agresszív Agresszív Kontroll ADX r ADX r +B Kontroll ADX r ADX r +B Kéreg Cinguláris Piriform Bazális ganglionok Caudatoputamen?????? Szeptális régió Mediális szeptum??? Laterális szeptum??? Bed nucleus stria terminalis??? Preoptikus terület Medián preoptikus mag Mediális preoptikus terület Laterális preoptikus terület??? Hipotalamusz Szuprakiazmatikus mag Szupraoptikus mag??? Elülso hipotalamikus terület??? Laterális hipotalamikus terület??? Periventrikuláris mag??? Paraventrikuláris mag (magno)?????? Paraventrikuláris mag (parvo) Arkuátusz mag Dorzomediális mag??? Ventromediális mag??? Hipotalamikus támadási zóna??? ++/+++ ++/+++ ++/+++ Talamusz Paraventrikuláris mag Mediodorzális mag??? Hippokampusz CA1/CA2/CA3/CA4?????? Dentate gyrus?????? Amigdala Mediális mag??? ++/+++ ++/+++ ++/+++ Kortikális mag??? Centrális mag? +?? ++? Laterális mag??? Agytörzs Középagyi centrális szürkeállomány??? Dorzális raphe?????? Locus coeruleus??? A rezidens-betolakodó teszt 20 percig tartott, a teszt során a rezidensek viselkedését és agyi aktivitását elemeztük. Kontroll: álmutött + 10 perccel a teszt elott HBC injekciót kapott; ADX r : adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott HBC injekciót kapott; ADX r +B: adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott kortikoszteron-hbc injekciót kapott (0,25 mg/kg kortikoszteron). Aktivitási skála: +++= nagyon eros; ++= eros; += közepes; ±= gyenge;?= nincs c-fos reakció. 70
71 120 * c-fos pozitív sejtmagok / terület * * * # * * 0 MeA HAA PAG CeA PVN Kontroll ADX r ADX r + B Kontroll ADX r ADX r + B Kontroll Agresszív (verekedésnek kitett) 13. ábra. Territoriális agresszió során kialakuló aktiváció egyes agyterületeken glukokortikoid hipofunkcióban. Az értékek átlag ± SE -ként kerültek bemutatásra. Az értékelés során két utas ANOVA tesztet használtunk (agresszív interakció és glukokortikoid háttér). *-p<0,05 a két utas ANOVA tesztet követo Newman-Keuls teszt eredményeként; #-p<0,05 post hoc az összes többi csoporthoz képest. Kontroll: álmutött + 10 perccel a teszt elott HBC injekciót kapott; ADX r : adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott HBC injekciót kapott; ADX r +B: adrenalektomizált és lassú felszívódású kortikoszteron tabletta került beültetésre + 10 perccel a teszt elott kortikoszteron-hbc injekciót kapott (0,25 mg/kg kortikoszteron). Rövidítések: CeA- centralis amigdala; HAA- hipotalamikus támadási zóna (attack area); MeA- mediális amigdala; PAG- periakveduktális szürkeállomány; PVN- hipotalamikus paraventrikularis mag (parvocelluláris rész). 71
72 14. ábra. A mediális és centrális amigdalában megjeleno c-fos aktiváció territoriális agresszió során különbözo glukokortikoid háttérrel rendelkezo állatokból származó reprezentatív metszeteken. A-B-C : ellenfelet nem kapott (A: kontroll; B: ADXr; C: ADXr + B), D-E-F: verekedésnek kitett (agresszív) (D: kontroll; E: ADXr; F: ADXr + B), CeA= centrális amigdala; MeA= mediális amigdala; OT= optikus traktus. Lépték: 100? m. 72
73 15. ábra. A paraventrikuláris mag parvocelluláris részében megjeleno c-fos aktiváció territoriális agresszió során különbözo glukokortikoid háttérrel rendelkezo állatokból származó reprezentatív metszeteken. A-B-C : ellenfelet nem kapott (A: kontroll; B: ADXr; C : ADXr + B), D-E-F: verekedésnek kitett (agresszív) (D: kontroll; E: ADXr; F: ADXr?+?B). Lépték: 100? m. 73
A magatartás szabályozása A vegetatív idegrendszer
 A magatartás szabályozása A vegetatív idegrendszer A magatartási válasz A külső vagy belső környezetből származó ingerekre adott komplex (szomatikus, vegetatív, endokrin) válaszreakció A magatartási választ
A magatartás szabályozása A vegetatív idegrendszer A magatartási válasz A külső vagy belső környezetből származó ingerekre adott komplex (szomatikus, vegetatív, endokrin) válaszreakció A magatartási választ
MAGYAR NYELVŰ ÖSSZEFOGLALÁS
 MAGYAR NYELVŰ ÖSSZEFOGLALÁS Bevezetés Ph.D. munkám során az agynak a neurodegeneratív folyamatok iránti érzékenységét vizsgáltam, különös tekintettel a korai neonatális fejlődést befolyásoló különböző
MAGYAR NYELVŰ ÖSSZEFOGLALÁS Bevezetés Ph.D. munkám során az agynak a neurodegeneratív folyamatok iránti érzékenységét vizsgáltam, különös tekintettel a korai neonatális fejlődést befolyásoló különböző
Az idegrendszer és a hormonális rednszer szabályozó működése
 Az idegrendszer és a hormonális rednszer szabályozó működése Az idegrendszer szerveződése érző idegsejt receptor érző idegsejt inger inger átkapcsoló sejt végrehajtó sejt végrehajtó sejt központi idegrendszer
Az idegrendszer és a hormonális rednszer szabályozó működése Az idegrendszer szerveződése érző idegsejt receptor érző idegsejt inger inger átkapcsoló sejt végrehajtó sejt végrehajtó sejt központi idegrendszer
Sejtek közötti kommunikáció:
 Sejtek közötti kommunikáció: Mi a sejtek közötti kommunikáció célja? Mi jellemző az endokrin kommunikációra? Mi jellemző a neurokrin kommunikációra? Melyek a közvetlen kommunikáció lépései és mi az egyes
Sejtek közötti kommunikáció: Mi a sejtek közötti kommunikáció célja? Mi jellemző az endokrin kommunikációra? Mi jellemző a neurokrin kommunikációra? Melyek a közvetlen kommunikáció lépései és mi az egyes
Központi idegrendszeri vizsgálatok.
 Központi idegrendszeri vizsgálatok. Újszülött patkány endorfin imprintingje után, felnőtt állatban a szexuális magatartást, szteroid hormon kötést és az agyi szerotonin szinteket vizsgáltuk. A nőstények
Központi idegrendszeri vizsgálatok. Újszülött patkány endorfin imprintingje után, felnőtt állatban a szexuális magatartást, szteroid hormon kötést és az agyi szerotonin szinteket vizsgáltuk. A nőstények
AZ ÖSZTROGÉN ÉS A DEHIDROEPIANDROSZTERON SZEREPE A SZINAPTIKUS ÁTRENDEZŐDÉSBEN
 AZ ÖSZTROGÉN ÉS A DEHIDROEPIANDROSZTERON SZEREPE A SZINAPTIKUS ÁTRENDEZŐDÉSBEN c. PhD-értekezés magyar nyelvű összefoglalója Csákvári Eszter Témavezető: Dr. Párducz Árpád Magyar Tudományos Akadémia Szegedi
AZ ÖSZTROGÉN ÉS A DEHIDROEPIANDROSZTERON SZEREPE A SZINAPTIKUS ÁTRENDEZŐDÉSBEN c. PhD-értekezés magyar nyelvű összefoglalója Csákvári Eszter Témavezető: Dr. Párducz Árpád Magyar Tudományos Akadémia Szegedi
Az endokrin szabályozás általános törvényszerűségei
 Az endokrin szabályozás általános törvényszerűségei a kémiai és idegi szabályozás alapelvei hormonok szerkezete, szintézise, tárolása, szekréciója hormonszintet meghatározó tényezők hormonszekréció szabályozása
Az endokrin szabályozás általános törvényszerűségei a kémiai és idegi szabályozás alapelvei hormonok szerkezete, szintézise, tárolása, szekréciója hormonszintet meghatározó tényezők hormonszekréció szabályozása
2006 1. Nemszinaptikus receptorok és szubmikronos Ca2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra.
 2006 1. Nemszinaptikus receptorok és szubmikronos Ca 2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra. A kutatócsoportunkban Közép Európában elsőként bevezetett két-foton
2006 1. Nemszinaptikus receptorok és szubmikronos Ca 2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra. A kutatócsoportunkban Közép Európában elsőként bevezetett két-foton
Az agy betegségeinek molekuláris biológiája. 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5.
 Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
Az elért eredmények. a) A jobb- és baloldali petefészek supraspinális beidegzése
 Az elért eredmények A perifériás belsőelválasztású mirigyek működésének szabályozásában a hypothalamushypophysis-célszerv rendszer döntő szerepet játszik. Közvetett, élettani megfigyelések arra utaltak,
Az elért eredmények A perifériás belsőelválasztású mirigyek működésének szabályozásában a hypothalamushypophysis-célszerv rendszer döntő szerepet játszik. Közvetett, élettani megfigyelések arra utaltak,
ISMÉTLŐDŐ STRESSZ HATÁSAINAK VIZSGÁLATA ZEBRADÁNIÓN (DANIO RERIO)
 ISMÉTLŐDŐ STRESSZ HATÁSAINAK VIZSGÁLATA ZEBRADÁNIÓN (DANIO RERIO) Buza Eszter, Váradi László, Csenki Zsolt, Müller Tamás, Jeney Zsigmond, Mézes Miklós Szent István Egyetem Mezőgazdaság-és Környezettudományi
ISMÉTLŐDŐ STRESSZ HATÁSAINAK VIZSGÁLATA ZEBRADÁNIÓN (DANIO RERIO) Buza Eszter, Váradi László, Csenki Zsolt, Müller Tamás, Jeney Zsigmond, Mézes Miklós Szent István Egyetem Mezőgazdaság-és Környezettudományi
Homeosztázis és idegrendszer
 Homeosztázis és idegrendszer Magatartás és homeosztázis a hipotalamusz és a limbikus rendszer ingerlése összehangolt motoros-vegetatívendokrin változásokat indít ezek a reakciók a homeosztázis fenntartására,
Homeosztázis és idegrendszer Magatartás és homeosztázis a hipotalamusz és a limbikus rendszer ingerlése összehangolt motoros-vegetatívendokrin változásokat indít ezek a reakciók a homeosztázis fenntartására,
OTKA nyilvántartási szám: T 046785 1 Haller J. és mtsai: Glukokortikodok és magatartási rendellenességek...
 OTKA nyilvántartási szám: T 046785 1 ZÁRÓJELENTÉS A projekt célja az volt, hogy tisztázzuk a glukokortikoidok integráló szerepét három fő magatartási zavar kialakulásában, illetve azokat az idegrendszeri
OTKA nyilvántartási szám: T 046785 1 ZÁRÓJELENTÉS A projekt célja az volt, hogy tisztázzuk a glukokortikoidok integráló szerepét három fő magatartási zavar kialakulásában, illetve azokat az idegrendszeri
Korai stressz és sérülékenység. Tóth Máté, PhD MTA KOKI Magatartás Neurobiológia Osztály
 Korai stressz és sérülékenység Tóth Máté, PhD MTA KOKI Magatartás Neurobiológia Osztály Korai stressz és sérülékenység + = Biológiai dinamika folyamatos kölcsöhatásban akörnyezettel Pszichiátriai zavarok
Korai stressz és sérülékenység Tóth Máté, PhD MTA KOKI Magatartás Neurobiológia Osztály Korai stressz és sérülékenység + = Biológiai dinamika folyamatos kölcsöhatásban akörnyezettel Pszichiátriai zavarok
PhD vizsgakérdések április 11. Próbálja meg funkcionális szempontból leírni és példákon bemutatni az intralimbikus kapcsolatok jelentőségét.
 PhD vizsgakérdések 2012. április 11 1 Mi a szerepe a corpus geniculatum lateralé-nak a látásban? Próbálja meg funkcionális szempontból leírni és példákon bemutatni az intralimbikus kapcsolatok jelentőségét.
PhD vizsgakérdések 2012. április 11 1 Mi a szerepe a corpus geniculatum lateralé-nak a látásban? Próbálja meg funkcionális szempontból leírni és példákon bemutatni az intralimbikus kapcsolatok jelentőségét.
A beszéd lateralizáció reorganizációjának nyomonkövetésea fmri-velaneurorehabilitációsorán
 A beszéd lateralizáció reorganizációjának nyomonkövetésea fmri-velaneurorehabilitációsorán (klinikai tanulmány terv) Péley Iván, Janszky József PTE KK Neurológiai Klinika Az (emberi) agy egyik meghatározó
A beszéd lateralizáció reorganizációjának nyomonkövetésea fmri-velaneurorehabilitációsorán (klinikai tanulmány terv) Péley Iván, Janszky József PTE KK Neurológiai Klinika Az (emberi) agy egyik meghatározó
Az adenohipofizis. Az endokrin szabályozás eddig olyan hormonokkal találkoztunk, amelyek közvetlen szabályozás alatt álltak:
 Az adenohipofizis 2/10 Az endokrin szabályozás eddig olyan hormonokkal találkoztunk, amelyek közvetlen szabályozás alatt álltak: ADH, aldoszteron, ANP inzulin, glukagon szekretin, gasztrin, CCK, GIP eritropoetin
Az adenohipofizis 2/10 Az endokrin szabályozás eddig olyan hormonokkal találkoztunk, amelyek közvetlen szabályozás alatt álltak: ADH, aldoszteron, ANP inzulin, glukagon szekretin, gasztrin, CCK, GIP eritropoetin
A somatomotoros rendszer
 A somatomotoros rendszer Motoneuron 1 Neuromuscularis junctio (NMJ) Vázizom A somatomotoros rendszer 1 Neurotranszmitter: Acetil-kolin Mire hat: Nikotinos kolinerg-receptor (nachr) Izom altípus A parasympathicus
A somatomotoros rendszer Motoneuron 1 Neuromuscularis junctio (NMJ) Vázizom A somatomotoros rendszer 1 Neurotranszmitter: Acetil-kolin Mire hat: Nikotinos kolinerg-receptor (nachr) Izom altípus A parasympathicus
Zárójelentés. A) A cervix nyújthatóságának (rezisztencia) állatkísérletes meghatározása terhes és nem terhes patkányban.
 Zárójelentés A kutatás fő célkitűzése a β 2 agonisták és altípus szelektív α 1 antagonisták hatásának vizsgálata a terhesség során a patkány cervix érésére összehasonlítva a corpusra gyakorolt hatásokkal.
Zárójelentés A kutatás fő célkitűzése a β 2 agonisták és altípus szelektív α 1 antagonisták hatásának vizsgálata a terhesség során a patkány cervix érésére összehasonlítva a corpusra gyakorolt hatásokkal.
ÖNINGERLÉS PRANCZ ÁDÁM
 ÖNINGERLÉS PRANCZ ÁDÁM Az agyi jutalmazási ( revard ) rendszere: Egyes fiziológiai tevékenységek, mint az evés, ivás, nemi kontaktus 2jutalmazottak, örömmel, gyönyörrel, kellemes érzéssel vagy kielégüléssel
ÖNINGERLÉS PRANCZ ÁDÁM Az agyi jutalmazási ( revard ) rendszere: Egyes fiziológiai tevékenységek, mint az evés, ivás, nemi kontaktus 2jutalmazottak, örömmel, gyönyörrel, kellemes érzéssel vagy kielégüléssel
Alkohollal kapcsolatos zavarok. Az alkoholbetegség. Általános jellegzetességek
 Alkohollal kapcsolatos zavarok Az alkoholbetegség Az alkoholisták mértéktelen ivók, alkoholfüggőségük olyan szintet ér el, hogy észrevehető mentális zavarokat okoz, károsítja test-lelki egészségüket, interperszonális
Alkohollal kapcsolatos zavarok Az alkoholbetegség Az alkoholisták mértéktelen ivók, alkoholfüggőségük olyan szintet ér el, hogy észrevehető mentális zavarokat okoz, károsítja test-lelki egészségüket, interperszonális
Ápolás Betegellátás Alapszak ADDIKTOLÓGIA 1. Deutsch Krisztina szakoktató PTE ETK
 Ápolás Betegellátás Alapszak ADDIKTOLÓGIA 1. Deutsch Krisztina szakoktató PTE ETK Tárgyleírás A drog és az idegrendszer. A drogok hatásmechanizmusa. Addiktológiai alapfogalmak. A függőség kialakulását
Ápolás Betegellátás Alapszak ADDIKTOLÓGIA 1. Deutsch Krisztina szakoktató PTE ETK Tárgyleírás A drog és az idegrendszer. A drogok hatásmechanizmusa. Addiktológiai alapfogalmak. A függőség kialakulását
Az agykéreg és az agykérgi aktivitás mérése
 Az agykéreg és az agykérgi aktivitás mérése Intrakortikális hálózatok Elektromos aktiváció, sejtszintű integráció Intracelluláris sejtaktivitás mérés Sejten belüli elektromos integráció 70 mv mikroelektrod
Az agykéreg és az agykérgi aktivitás mérése Intrakortikális hálózatok Elektromos aktiváció, sejtszintű integráció Intracelluláris sejtaktivitás mérés Sejten belüli elektromos integráció 70 mv mikroelektrod
A köztiagy (dienchephalon)
 A köztiagy, nagyagy, kisagy Szerk.: Vizkievicz András A köztiagy (dienchephalon) Állománya a III. agykamra körül szerveződik. Részei: Epitalamusz Talamusz Hipotalamusz Legfontosabb kéregalatti érző- és
A köztiagy, nagyagy, kisagy Szerk.: Vizkievicz András A köztiagy (dienchephalon) Állománya a III. agykamra körül szerveződik. Részei: Epitalamusz Talamusz Hipotalamusz Legfontosabb kéregalatti érző- és
SZOCIÁLIS VISELKEDÉSEK
 VISELKEDÉSÉLETTAN 10. ELŐADÁS SZOCIÁLIS VISELKEDÉSEK Dobolyi Árpád ELTE, Élettani és Neurobiológiai Tanszék AZ ELŐADÁS VÁZLATA A szociális viselkedések a társas kapcsolat, mint jutalom Fajtársakkal kapcsolatos
VISELKEDÉSÉLETTAN 10. ELŐADÁS SZOCIÁLIS VISELKEDÉSEK Dobolyi Árpád ELTE, Élettani és Neurobiológiai Tanszék AZ ELŐADÁS VÁZLATA A szociális viselkedések a társas kapcsolat, mint jutalom Fajtársakkal kapcsolatos
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA NOVEMBER
 Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
A központi idegrendszer funkcionális anatómiája
 A központi idegrendszer funkcionális anatómiája Nyakas Csaba Az előadás anyaga kizárólag tanulmányi célra használható (1) Az idegrendszer szerveződése Agykéreg Bazális ganglionok Kisagy Agytörzs Gerincvelő
A központi idegrendszer funkcionális anatómiája Nyakas Csaba Az előadás anyaga kizárólag tanulmányi célra használható (1) Az idegrendszer szerveződése Agykéreg Bazális ganglionok Kisagy Agytörzs Gerincvelő
Endokrinológia. Közös jellemzők: nincs kivezetőcső, nincs végkamra - hámsejt csoportosulások. váladékuk a hormon
 Közös jellemzők: Endokrinológia nincs kivezetőcső, nincs végkamra - hámsejt csoportosulások váladékuk a hormon váladékukat a vér szállítja el - bő vérellátás távoli szervekre fejtik ki hatásukat (legtöbbször)
Közös jellemzők: Endokrinológia nincs kivezetőcső, nincs végkamra - hámsejt csoportosulások váladékuk a hormon váladékukat a vér szállítja el - bő vérellátás távoli szervekre fejtik ki hatásukat (legtöbbször)
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Belső elválasztású mirigyek
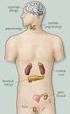 Belső elválasztású mirigyek Szekréciós szervek szövettana A különböző sejtszervecskék fejlettsége utal a szekretált anyag jellemzőire és a szekréciós aktivitás mértékére: Golgi komplex: jelenléte szekrétum
Belső elválasztású mirigyek Szekréciós szervek szövettana A különböző sejtszervecskék fejlettsége utal a szekretált anyag jellemzőire és a szekréciós aktivitás mértékére: Golgi komplex: jelenléte szekrétum
Neuronális hálózatok aktivitás-mérése, biológiai ritmusok
 Neuronális hálózatok aktivitás-mérése, biológiai ritmusok Emlős agykéreg szerkezete patkány agykéreg emberi agykéreg Intrakortikális hálózatok Az agykéreg szerkezeti és működési térképezése szerkezeti
Neuronális hálózatok aktivitás-mérése, biológiai ritmusok Emlős agykéreg szerkezete patkány agykéreg emberi agykéreg Intrakortikális hálózatok Az agykéreg szerkezeti és működési térképezése szerkezeti
Biológiai perspektíva 2: Biológiai folyamatok és személyiség
 Biológiai perspektíva 2: Biológiai folyamatok és személyiség Alapkérdés: milyen mechanizmusok révén gyakorolnak hatást a genetikai tényezők a személyiségre? Kiindulópont: A személyiséget biológiai működések
Biológiai perspektíva 2: Biológiai folyamatok és személyiség Alapkérdés: milyen mechanizmusok révén gyakorolnak hatást a genetikai tényezők a személyiségre? Kiindulópont: A személyiséget biológiai működések
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai
 Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Pszichiátriai zavarok neurobiológiai alapjai
 Pszichiátriai zavarok neurobiológiai alapjai Kéri Szabolcs 1 1. Alapfogalmak: anatómia, fiziológia 2. Funkcionális lokalizáció az agyban 3. Szinapszisok és neurotranszmitterek 4. A neurotranszmisszió molekuláris
Pszichiátriai zavarok neurobiológiai alapjai Kéri Szabolcs 1 1. Alapfogalmak: anatómia, fiziológia 2. Funkcionális lokalizáció az agyban 3. Szinapszisok és neurotranszmitterek 4. A neurotranszmisszió molekuláris
Disszociatív zavarok, traumával és stresszorral összefüggő zavarok. Mi a disszociáció? Az emlékezés, a tudat, a szenzoros és
 Disszociatív zavarok, traumával és stresszorral összefüggő zavarok Pécsi Tudományegyetem Mi a disszociáció? Az emlékezés, a tudat, a szenzoros és motoros működések egységének időszakos szétválása A disszociáció
Disszociatív zavarok, traumával és stresszorral összefüggő zavarok Pécsi Tudományegyetem Mi a disszociáció? Az emlékezés, a tudat, a szenzoros és motoros működések egységének időszakos szétválása A disszociáció
Ember egészségtana és élettana esszé tételsorok 5+1 Esszé kérdések:
 Ember egészségtana és élettana esszé tételsorok 5+1 Esszé kérdések: 1 témát húznak (dőlt betűs címek), azon belül 1 kérdést választanak és azt dolgozzák ki Hormonrendszer: 1. Hogyan történik a növekedési
Ember egészségtana és élettana esszé tételsorok 5+1 Esszé kérdések: 1 témát húznak (dőlt betűs címek), azon belül 1 kérdést választanak és azt dolgozzák ki Hormonrendszer: 1. Hogyan történik a növekedési
Autonóm idegrendszer
 Autonóm idegrendszer Az emberi idegrendszer működésének alapjai Október 26. 2012 őszi félév Vakli Pál vaklip86@gmail.com Web: http://www.cogsci.bme.hu/oraheti.php Szomatikus és autonóm idegrendszer Szomatikus:
Autonóm idegrendszer Az emberi idegrendszer működésének alapjai Október 26. 2012 őszi félév Vakli Pál vaklip86@gmail.com Web: http://www.cogsci.bme.hu/oraheti.php Szomatikus és autonóm idegrendszer Szomatikus:
Bevezetés s a gyermek- pszichofarmakológi
 Bevezetés s a gyermek- pszichofarmakológi giába Gádoros Júlia Vadaskert Kórház Budapest A kezdetek Bradley 1937 benzedrinkezelés ötvenes években megjelent antipszichotikumok és antidepresszívumok 1960-ban
Bevezetés s a gyermek- pszichofarmakológi giába Gádoros Júlia Vadaskert Kórház Budapest A kezdetek Bradley 1937 benzedrinkezelés ötvenes években megjelent antipszichotikumok és antidepresszívumok 1960-ban
A szkizofrénia dopamin elmélete. Gyertyán István. Richter Gedeon NyRt.
 A szkizofrénia dopamin elmélete Az antipszichotikumok kutatása Gyertyán István Richter Gedeon NyRt. Preklinikai és klinikai neuropszichofarmakológia és pszichofarmakogenetika. Dr. Bagdy György Skizofrénia
A szkizofrénia dopamin elmélete Az antipszichotikumok kutatása Gyertyán István Richter Gedeon NyRt. Preklinikai és klinikai neuropszichofarmakológia és pszichofarmakogenetika. Dr. Bagdy György Skizofrénia
AGRESSZÍV, MERT NINCS MÁS ESZKÖZE Magatartászavaros gyerekek megküzdési stratégiáinak vizsgálata a Pszichológiai Immunkompetencia Kérdőív tükrében
 AGRESSZÍV, MERT NINCS MÁS ESZKÖZE Magatartászavaros gyerekek megküzdési stratégiáinak vizsgálata a Pszichológiai Immunkompetencia Kérdőív tükrében Készítette: Uicz Orsolya Lilla 2011. Erőszakos, támadó!
AGRESSZÍV, MERT NINCS MÁS ESZKÖZE Magatartászavaros gyerekek megküzdési stratégiáinak vizsgálata a Pszichológiai Immunkompetencia Kérdőív tükrében Készítette: Uicz Orsolya Lilla 2011. Erőszakos, támadó!
Orvosi élettan. Bevezetés és szabályozáselmélet Tanulási támpontok: 1.
 Orvosi élettan Bevezetés és szabályozáselmélet Tanulási támpontok: 1. Prof. Sáry Gyula 1 anyagcsere hőcsere Az élőlény és környezete nyitott rendszer inger hő kémiai mechanikai válasz mozgás alakváltoztatás
Orvosi élettan Bevezetés és szabályozáselmélet Tanulási támpontok: 1. Prof. Sáry Gyula 1 anyagcsere hőcsere Az élőlény és környezete nyitott rendszer inger hő kémiai mechanikai válasz mozgás alakváltoztatás
Limbikus rendszer Tanulás, memória
 Limbikus rendszer Tanulás, memória Limbikus kéreg Részei: septum, area piriformis, preapiriformis, amygdala, hippocampus, hypothalamus thalamus bizonyos részei. Limbikus rendszer: Funkciója: motiváció,
Limbikus rendszer Tanulás, memória Limbikus kéreg Részei: septum, area piriformis, preapiriformis, amygdala, hippocampus, hypothalamus thalamus bizonyos részei. Limbikus rendszer: Funkciója: motiváció,
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Pszichoszomatikus betegségek. Mi a pszichoszomatikus betegség lényege?
 Pszichoszomatikus betegségek Pécsi Tudományegyetem Mi a pszichoszomatikus betegség lényege? Valódi organikus háttérrel rendelkező kórképek, amelyek kóreredete multifaktoriális A genetikai, immunológiai,
Pszichoszomatikus betegségek Pécsi Tudományegyetem Mi a pszichoszomatikus betegség lényege? Valódi organikus háttérrel rendelkező kórképek, amelyek kóreredete multifaktoriális A genetikai, immunológiai,
Természetgyógyászati Klinikum
 Természetgyógyászati Klinikum A Pszichiátria és a természetgyógyászat kapcsolata Fekete Szabolcs - 2016 pszichiátria A gondolkodás, az érzelmi élet és a viselkedés zavaraival foglalkozó szakterület A terápiák
Természetgyógyászati Klinikum A Pszichiátria és a természetgyógyászat kapcsolata Fekete Szabolcs - 2016 pszichiátria A gondolkodás, az érzelmi élet és a viselkedés zavaraival foglalkozó szakterület A terápiák
Gyógyszerészeti neurobiológia. Idegélettan
 Az idegrendszert felépítő sejtek szerepe Gyógyszerészeti neurobiológia. Idegélettan Neuronok, gliasejtek és a kémiai szinapszisok működési sajátságai Neuronok Információkezelés Felvétel Továbbítás Feldolgozás
Az idegrendszert felépítő sejtek szerepe Gyógyszerészeti neurobiológia. Idegélettan Neuronok, gliasejtek és a kémiai szinapszisok működési sajátságai Neuronok Információkezelés Felvétel Továbbítás Feldolgozás
Nocturia napjaink betegsége Dr. Siller György
 Szegedi úti akadémia 2017 Nocturia napjaink betegsége Dr. Siller György Nocturia Életminőséget jelentősen rontja Életkilátásokat is befolyásolhatja Férfiakat és nőket egyaránt érinti Rendszeres témája
Szegedi úti akadémia 2017 Nocturia napjaink betegsége Dr. Siller György Nocturia Életminőséget jelentősen rontja Életkilátásokat is befolyásolhatja Férfiakat és nőket egyaránt érinti Rendszeres témája
Gyógyszeres kezelések
 Gyógyszeres kezelések Az osteogenesis imperfecta gyógyszeres kezelésében számos szert kipróbáltak az elmúlt évtizedekben, de átütő eredménnyel egyik se szolgált. A fluorid kezelés alkalmazása osteogenesis
Gyógyszeres kezelések Az osteogenesis imperfecta gyógyszeres kezelésében számos szert kipróbáltak az elmúlt évtizedekben, de átütő eredménnyel egyik se szolgált. A fluorid kezelés alkalmazása osteogenesis
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Kutatási beszámoló ( )
 Kutatási beszámoló (2008-2012) A thrombocyták aktivációja alapvető jelentőségű a thrombotikus betegségek kialakulása szempontjából. A pályázat során ezen aktivációs folyamatok mechanizmusait vizsgáltuk.
Kutatási beszámoló (2008-2012) A thrombocyták aktivációja alapvető jelentőségű a thrombotikus betegségek kialakulása szempontjából. A pályázat során ezen aktivációs folyamatok mechanizmusait vizsgáltuk.
Új terápiás lehetőségek (receptorok) a kardiológiában
 Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
A sejtmembrán szabályozó szerepe fiziológiás körülmények között és kóros állapotokban
 A sejtmembrán szabályozó szerepe fiziológiás körülmények között és kóros állapotokban 17. Központi idegrendszeri neuronok ingerületi folyamatai és szinaptikus összeköttetései 18. A kalciumháztartás zavaraira
A sejtmembrán szabályozó szerepe fiziológiás körülmények között és kóros állapotokban 17. Központi idegrendszeri neuronok ingerületi folyamatai és szinaptikus összeköttetései 18. A kalciumháztartás zavaraira
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
SZOCIÁLIS VISELKEDÉSEK 2
 VISELKEDÉSÉLETTAN 11. ELŐADÁS SZOCIÁLIS VISELKEDÉSEK 2 Dobolyi Árpád ELTE, Élettani és Neurobiológiai Tanszék AZ ELŐADÁS VÁZLATA A szociális viselkedések a társas kapcsolat, mint jutalom Fajtársakkal kapcsolatos
VISELKEDÉSÉLETTAN 11. ELŐADÁS SZOCIÁLIS VISELKEDÉSEK 2 Dobolyi Árpád ELTE, Élettani és Neurobiológiai Tanszék AZ ELŐADÁS VÁZLATA A szociális viselkedések a társas kapcsolat, mint jutalom Fajtársakkal kapcsolatos
Az érzelmi felismerés viselkedészavaros lányokban (Emotion recognition in girls with conduct problems)
 Az érzelmi felismerés viselkedészavaros lányokban (Emotion recognition in girls with conduct problems) Christina Schwenck, Angelika Gensthaler Marcel Romanos Christine M. Freitag, Wolfgang Schneider, Regina
Az érzelmi felismerés viselkedészavaros lányokban (Emotion recognition in girls with conduct problems) Christina Schwenck, Angelika Gensthaler Marcel Romanos Christine M. Freitag, Wolfgang Schneider, Regina
A nesfatin-1/nucb2 szerepének vizsgálata a központi idegrendszerben. Doktori tézisek Könczöl Katalin
 A nesfatin-1/nucb2 szerepének vizsgálata a központi idegrendszerben Doktori tézisek Könczöl Katalin Semmelweis Egyetem Szentágothai János Idegtudományi Doktori Iskola Témavezető: Hivatalos bírálók: Szigorlati
A nesfatin-1/nucb2 szerepének vizsgálata a központi idegrendszerben Doktori tézisek Könczöl Katalin Semmelweis Egyetem Szentágothai János Idegtudományi Doktori Iskola Témavezető: Hivatalos bírálók: Szigorlati
Kolin-acetiltranszferáz
 Kolin-acetiltranszferáz Neurotranszmitter-kritériumok: Szintetizáló enzim-készlet ( kulcs-enzimek ) Tároló-rendszer (vezikuláris transzporterek) Felvevő /lebontó rendszer Adagolással posztszinaptikus válasz
Kolin-acetiltranszferáz Neurotranszmitter-kritériumok: Szintetizáló enzim-készlet ( kulcs-enzimek ) Tároló-rendszer (vezikuláris transzporterek) Felvevő /lebontó rendszer Adagolással posztszinaptikus válasz
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Affektív zavarok - hangulatzavarok. Hidasi Zoltán
 Affektív zavarok - hangulatzavarok Hidasi Zoltán Alapfogalmak Érzelem (emóció) Indulat (affektus) Hangulat (-thymia) Közérzet (-phoria) Hangulatzavarok Szindrómák Klasszifikáció Epidemiológia Diagnózis
Affektív zavarok - hangulatzavarok Hidasi Zoltán Alapfogalmak Érzelem (emóció) Indulat (affektus) Hangulat (-thymia) Közérzet (-phoria) Hangulatzavarok Szindrómák Klasszifikáció Epidemiológia Diagnózis
A generalizált szorongás etiológiája és pathomechanismusa
 A generalizált szorongás etiológiája és pathomechanismusa Genetikai vizsgálatok Az egyik ikervizsgálat nem talált a generalizált szorongás (Generalized Anxiety Disorder, a továbbiakban GAD) genetikai átörökítése
A generalizált szorongás etiológiája és pathomechanismusa Genetikai vizsgálatok Az egyik ikervizsgálat nem talált a generalizált szorongás (Generalized Anxiety Disorder, a továbbiakban GAD) genetikai átörökítése
1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil.
 1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil. Magyarországon egyedi gyógyszerrendelés alapján két éve adható (MODASOMIL,
1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil. Magyarországon egyedi gyógyszerrendelés alapján két éve adható (MODASOMIL,
A KÉMIAI KOMMUNIKÁCIÓ ALAPELVEI. - autokrin. -neurokrin. - parakrin. -térátvitel. - endokrin
 A KÉMIAI KOMMUNIKÁCIÓ ALAPELVEI - autokrin -neurokrin - parakrin -térátvitel - endokrin 3.1. ábra: Az immunreakciók főbb típusai és funkciójuk. IMMUNVÁLASZ TERMÉSZETES ADAPTÍV humorális sejtes HUMORÁLIS
A KÉMIAI KOMMUNIKÁCIÓ ALAPELVEI - autokrin -neurokrin - parakrin -térátvitel - endokrin 3.1. ábra: Az immunreakciók főbb típusai és funkciójuk. IMMUNVÁLASZ TERMÉSZETES ADAPTÍV humorális sejtes HUMORÁLIS
VÁLASZ DR. JULOW JENİ TANÁR ÚR, AZ MTA DOKTORA OPPONENSI VÉLEMÉNYÉRE. Tisztelt Julow Jenı Tanár Úr!
 1 VÁLASZ DR. JULOW JENİ TANÁR ÚR, AZ MTA DOKTORA OPPONENSI VÉLEMÉNYÉRE Tisztelt Julow Jenı Tanár Úr! Köszönöm Dr. Julow Jenı Tanár Úr részletes, minden szempontra kiterjedı opponensi véleményezését, megtisztelı,
1 VÁLASZ DR. JULOW JENİ TANÁR ÚR, AZ MTA DOKTORA OPPONENSI VÉLEMÉNYÉRE Tisztelt Julow Jenı Tanár Úr! Köszönöm Dr. Julow Jenı Tanár Úr részletes, minden szempontra kiterjedı opponensi véleményezését, megtisztelı,
Pszichopatológia 2. DISSZOCIATÍV ZAVAROK
 Pszichopatológia 2. DISSZOCIATÍV ZAVAROK Prof. Dr. Perczel - Forintos Dóra Semmelweis Egyetem ÁOK Klinikai Pszichológia Tanszék 2018 szakképzés 1. évfolyam 1 DSM IV DSM V 8. Szomatoform zavarok Szomatikus
Pszichopatológia 2. DISSZOCIATÍV ZAVAROK Prof. Dr. Perczel - Forintos Dóra Semmelweis Egyetem ÁOK Klinikai Pszichológia Tanszék 2018 szakképzés 1. évfolyam 1 DSM IV DSM V 8. Szomatoform zavarok Szomatikus
Az élő szervezetek menedzserei, a hormonok
 rekkel exponálunk a munka végén) és azt utólag kivonjuk digitálisan a képekből. A zajcsökkentés dandárját mindig végezzük a raw-képek digitális előhívása során, mert ez okozza a legkevesebb jelvesztést
rekkel exponálunk a munka végén) és azt utólag kivonjuk digitálisan a képekből. A zajcsökkentés dandárját mindig végezzük a raw-képek digitális előhívása során, mert ez okozza a legkevesebb jelvesztést
A neuroendokrin jelátviteli rendszer
 A neuroendokrin jelátviteli rendszer Hipotalamusz Hipofízis Pajzsmirigy Mellékpajzsmirigy Zsírszövet Mellékvese Hasnyálmirigy Vese Petefészek Here Hormon felszabadulási kaszkád Félelem Fertőzés Vérzés
A neuroendokrin jelátviteli rendszer Hipotalamusz Hipofízis Pajzsmirigy Mellékpajzsmirigy Zsírszövet Mellékvese Hasnyálmirigy Vese Petefészek Here Hormon felszabadulási kaszkád Félelem Fertőzés Vérzés
FUSARIUM TOXINOK IDEGRENDSZERI HATÁSÁNAK ELEMZÉSE
 FUSARIUM TOXINOK IDEGRENDSZERI HATÁSÁNAK ELEMZÉSE Világi Ildikó, Varró Petra, Bódi Vera, Schlett Katalin, Szűcs Attila, Rátkai Erika Anikó, Szentgyörgyi Viktória, Détári László, Tóth Attila, Hajnik Tünde,
FUSARIUM TOXINOK IDEGRENDSZERI HATÁSÁNAK ELEMZÉSE Világi Ildikó, Varró Petra, Bódi Vera, Schlett Katalin, Szűcs Attila, Rátkai Erika Anikó, Szentgyörgyi Viktória, Détári László, Tóth Attila, Hajnik Tünde,
ADHD Attention Deficit Hyperaktivity Disorder
 ADHD Attention Deficit Hyperaktivity Disorder ELİADÁS KIVONAT 2008. november 06. Balázs Judit Vadaskert Gyermekpszichiátriai Kórház és Ambulancia, Budapest ADHD pervalenciája 3-7 %-a az iskolás korú gyermekeknek
ADHD Attention Deficit Hyperaktivity Disorder ELİADÁS KIVONAT 2008. november 06. Balázs Judit Vadaskert Gyermekpszichiátriai Kórház és Ambulancia, Budapest ADHD pervalenciája 3-7 %-a az iskolás korú gyermekeknek
GLÜKOKORTIKOIDOK. A mellékvese funkciója
 GLÜKOKORTIKOIDOK A mellékvese funkciója A mellékvese hormonjai védelmet nyújtanak a szervezetet érő akut és krónikus stressz-el szemben, valamint a táplálék és a víz elhúzódó hiánya esetén. - "kicsi a
GLÜKOKORTIKOIDOK A mellékvese funkciója A mellékvese hormonjai védelmet nyújtanak a szervezetet érő akut és krónikus stressz-el szemben, valamint a táplálék és a víz elhúzódó hiánya esetén. - "kicsi a
DOI: /SE Doktori értekezés. Tulogdi Áron. Semmelweis Egyetem Szentágothai János Idegtudományi Doktori Iskola
 A krónikus glükokortikoid-hiány és a korai szociális izoláció következtében kialakuló abnormális agresszióformák, valamint a ragadozói agresszió idegrendszeri szabályozásának vizsgálata patkányban Doktori
A krónikus glükokortikoid-hiány és a korai szociális izoláció következtében kialakuló abnormális agresszióformák, valamint a ragadozói agresszió idegrendszeri szabályozásának vizsgálata patkányban Doktori
Interdiszciplináris megközelítés és elemzés (anamnézis és diagnózis)
 Interdiszciplináris megközelítés és elemzés (anamnézis és diagnózis) M2 Unit 3 Jövőbeli lehetséges krízishelyzetek előrejelzése az anamnézis és a diagnosztikai jelentések alapján A normál serdülőkori magatartás
Interdiszciplináris megközelítés és elemzés (anamnézis és diagnózis) M2 Unit 3 Jövőbeli lehetséges krízishelyzetek előrejelzése az anamnézis és a diagnosztikai jelentések alapján A normál serdülőkori magatartás
A diabetes hatása a terhes patkány uterus működésére és farmakológiai reaktivitására
 OTKA 62707 A diabetes hatása a terhes patkány uterus működésére és farmakológiai reaktivitására Zárójelentés A gesztációs diabetes mellitus (GDM) egyike a leggyakoribb terhességi komplikációknak, megfelelő
OTKA 62707 A diabetes hatása a terhes patkány uterus működésére és farmakológiai reaktivitására Zárójelentés A gesztációs diabetes mellitus (GDM) egyike a leggyakoribb terhességi komplikációknak, megfelelő
VISELKEDÉSSZABÁLYOZÁS DIMENZIÓI II. Lajkó Károly SZTE Magatartástudományi Intézet
 VISELKEDÉSSZABÁLYOZÁS DIMENZIÓI II. Lajkó Károly SZTE Magatartástudományi Intézet lajko.karoly@med.u-szeged.hu Az emberi viselkedésszabályozás színterei I. Viselkedés és környezet találkozásai (funkcionális
VISELKEDÉSSZABÁLYOZÁS DIMENZIÓI II. Lajkó Károly SZTE Magatartástudományi Intézet lajko.karoly@med.u-szeged.hu Az emberi viselkedésszabályozás színterei I. Viselkedés és környezet találkozásai (funkcionális
Etológia/BSc. Etológiai alapvetések: Történet és módszer. Miklósi Ádám Pongrácz Péter
 Etológia/BSc Etológiai alapvetések: Történet és módszer Miklósi Ádám Pongrácz Péter 2018 KÖVETELMÉNY (!) - Előadások anyaga (ppt-pdf: honlapról) - Csányi Vilmos Etológia Számonkérés: - írásbeli vizsga
Etológia/BSc Etológiai alapvetések: Történet és módszer Miklósi Ádám Pongrácz Péter 2018 KÖVETELMÉNY (!) - Előadások anyaga (ppt-pdf: honlapról) - Csányi Vilmos Etológia Számonkérés: - írásbeli vizsga
Tamás László: Fülben végbemenő folyamatok nagy hangosságú zajok, zenei események tartós behatásakor. László Tamás MD
 Tamás László: Fülben végbemenő folyamatok nagy hangosságú zajok, zenei események tartós behatásakor László Tamás MD A hang, intenzitásától függően előidézhet Adaptációt, élettani jelenség a 70dB és annál
Tamás László: Fülben végbemenő folyamatok nagy hangosságú zajok, zenei események tartós behatásakor László Tamás MD A hang, intenzitásától függően előidézhet Adaptációt, élettani jelenség a 70dB és annál
SUMMARY IN HUNGARIAN MAGYAR NYELVŰ ÖSSZEFOGLALÓ
 Summary in Hungarian SUMMARY IN HUNGARIAN MAGYAR NYELVŰ ÖSSZEFOGLALÓ Naponta hozzávetőlegesen nyolc órát töltünk alvással, vagyis életünk egy-harmadát átalusszuk. Magában a tény, hogy ilyen sok időt szentelünk
Summary in Hungarian SUMMARY IN HUNGARIAN MAGYAR NYELVŰ ÖSSZEFOGLALÓ Naponta hozzávetőlegesen nyolc órát töltünk alvással, vagyis életünk egy-harmadát átalusszuk. Magában a tény, hogy ilyen sok időt szentelünk
Szorongás, szorongásos zavarok, szomatoform zavarok. Hidasi Zoltán
 Szorongás, szorongásos zavarok, szomatoform zavarok Hidasi Zoltán Szorongás Meghatározás Fiziológiás szorongás Tünetek Szorongásos zavarok Terápia Fogászati vonatkozások Félelem v. szorongás Szorongás:
Szorongás, szorongásos zavarok, szomatoform zavarok Hidasi Zoltán Szorongás Meghatározás Fiziológiás szorongás Tünetek Szorongásos zavarok Terápia Fogászati vonatkozások Félelem v. szorongás Szorongás:
HORMONOK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 HORMONOK BIOTECHNOLÓGIAI
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 HORMONOK BIOTECHNOLÓGIAI
Szomatoform (szomatikus tünet) zavarok, kényszerbetegség és kapcsolódó zavarok. A szomatoform (szomatikus tünet) zavarok általános jellemzők
 Szomatoform (szomatikus tünet), kényszerbetegség és kapcsolódó Pécsi Tudományegyetem A szomatoform (szomatikus tünet) általános jellemzők A hisztéria és a hipochondria az ókortól ismertek Paul Briquet
Szomatoform (szomatikus tünet), kényszerbetegség és kapcsolódó Pécsi Tudományegyetem A szomatoform (szomatikus tünet) általános jellemzők A hisztéria és a hipochondria az ókortól ismertek Paul Briquet
Gyógyszerészeti neurobiológia Idegélettan 3. A gerincvelő szerepe az izomműködés szabályozásában
 Gyógyszerészeti neurobiológia Idegélettan 3. A gerincvelő szerepe az izomműködés szabályozásában A szomatomotoros szabályozási központok hierarchiája A hierarchikus jelleg az evolúciós adaptáció következménye
Gyógyszerészeti neurobiológia Idegélettan 3. A gerincvelő szerepe az izomműködés szabályozásában A szomatomotoros szabályozási központok hierarchiája A hierarchikus jelleg az evolúciós adaptáció következménye
Szexuális izgalom (arousal) Szexuális izgalom Sexual Arousal A SZEXUÁLIS AROUSAL 3 NAGY RENDSZERE:
 Szexuális izgalom (arousal) Szexuális izgalom Sexual Arousal Humán szexuális válasz: interperszonális, vallási, szociális, pszichológiai és biológiai tényezők Szexuális izgalom (arousal): egy emelkedett
Szexuális izgalom (arousal) Szexuális izgalom Sexual Arousal Humán szexuális válasz: interperszonális, vallási, szociális, pszichológiai és biológiai tényezők Szexuális izgalom (arousal): egy emelkedett
A korai magömlés diagnózisa és terápiája (ISSM 2014-es ajánlása alapján) Dr. Rosta Gábor Soproni Gyógyközpont
 A korai magömlés diagnózisa és terápiája (ISSM 2014-es ajánlása alapján) Dr. Rosta Gábor Soproni Gyógyközpont ISSM definíció- 2014 Szexuális aktivitás során az ejakuláció állandóan vagy visszatérően bekövetkezik
A korai magömlés diagnózisa és terápiája (ISSM 2014-es ajánlása alapján) Dr. Rosta Gábor Soproni Gyógyközpont ISSM definíció- 2014 Szexuális aktivitás során az ejakuláció állandóan vagy visszatérően bekövetkezik
Tények a Goji bogyóról:
 Tények a Goji bogyóról: 19 aminosavat (a fehérjék építőkövei) tartalmaz, melyek közül 8 esszenciális, azaz nélkülözhetelen az élethez. 21 nyomelemet tartalmaz, köztük germániumot, amely ritkán fordul elő
Tények a Goji bogyóról: 19 aminosavat (a fehérjék építőkövei) tartalmaz, melyek közül 8 esszenciális, azaz nélkülözhetelen az élethez. 21 nyomelemet tartalmaz, köztük germániumot, amely ritkán fordul elő
Genetikai vizsgálatok
 Genetikai vizsgálatok Családvizsgálatok Bottom-up Top-down Ikertanulmányok Adoptációs vizsgálatok Molekuláris genetikai vizsgálatok 1 Depresszió-Családvizsgálatok Bottom-up tanulmányok (MDD-s gyermek proband
Genetikai vizsgálatok Családvizsgálatok Bottom-up Top-down Ikertanulmányok Adoptációs vizsgálatok Molekuláris genetikai vizsgálatok 1 Depresszió-Családvizsgálatok Bottom-up tanulmányok (MDD-s gyermek proband
HYPOTHALAMIKUS STRUKTÚRÁK ÉS FAKTOROK JELENTOSÉGE A PROLAKTIN ELVÁLASZTÁS SZABÁLYOZÁSÁBAN. Bodnár Ibolya. Doktori (Ph.D.) értekezés tézisei
 HYPOTHALAMIKUS STRUKTÚRÁK ÉS FAKTOROK JELENTOSÉGE A PROLAKTIN ELVÁLASZTÁS SZABÁLYOZÁSÁBAN Bodnár Ibolya Doktori (Ph.D.) értekezés tézisei Témavezeto: Prof. Dr. Nagy György Semmelweis Egyetem, Doktori Iskola
HYPOTHALAMIKUS STRUKTÚRÁK ÉS FAKTOROK JELENTOSÉGE A PROLAKTIN ELVÁLASZTÁS SZABÁLYOZÁSÁBAN Bodnár Ibolya Doktori (Ph.D.) értekezés tézisei Témavezeto: Prof. Dr. Nagy György Semmelweis Egyetem, Doktori Iskola
Doktori tézisek. Tulogdi Áron. Semmelweis Egyetem Szentágothai János Idegtudományi Doktori Iskola
 A krónikus glükokortikoid-hiány és a korai szociális izoláció következtében kialakuló abnormális agresszióformák, valamint a ragadozói agresszió idegrendszeri szabályozásának vizsgálata patkányban Doktori
A krónikus glükokortikoid-hiány és a korai szociális izoláció következtében kialakuló abnormális agresszióformák, valamint a ragadozói agresszió idegrendszeri szabályozásának vizsgálata patkányban Doktori
Pszichotrauma és disszociatív kapacitás összefüggésének vizsgálata syncopés betegek körében
 Pszichotrauma és disszociatív kapacitás összefüggésének vizsgálata syncopés betegek körében Dávid Tamás, G. Tóth Kinga, Nagy Kálmán, Rónaszéki Aladár Péterfy S. u. Kórház, Kardiológiai Osztály, Budapest
Pszichotrauma és disszociatív kapacitás összefüggésének vizsgálata syncopés betegek körében Dávid Tamás, G. Tóth Kinga, Nagy Kálmán, Rónaszéki Aladár Péterfy S. u. Kórház, Kardiológiai Osztály, Budapest
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Az emésztôrendszer károsodásai. Lonovics János id. Dubecz Sándor Erdôs László Juhász Ferenc Misz Irén Irisz. 17. fejezet
 Az emésztôrendszer károsodásai Lonovics János id. Dubecz Sándor Erdôs László Juhász Ferenc Misz Irén Irisz 17. fejezet Általános rész A fejezet az emésztôrendszer tartós károsodásainak, a károsodások
Az emésztôrendszer károsodásai Lonovics János id. Dubecz Sándor Erdôs László Juhász Ferenc Misz Irén Irisz 17. fejezet Általános rész A fejezet az emésztôrendszer tartós károsodásainak, a károsodások
Droghasználat korai és késői hatásainak észlelése különböző pszichiátriai rendszerekben
 Droghasználat korai és késői hatásainak észlelése különböző pszichiátriai rendszerekben Kezdetben a szenvedély idegen, később vendég, végül úr a házban Ma, amikor addiktológiáról beszélünk, egy olyan tudományterületre
Droghasználat korai és késői hatásainak észlelése különböző pszichiátriai rendszerekben Kezdetben a szenvedély idegen, később vendég, végül úr a házban Ma, amikor addiktológiáról beszélünk, egy olyan tudományterületre
Dr. Péczely László Zoltán. A Grastyán örökség: A játék neurobiológiája
 Dr. Péczely László Zoltán A Grastyán örökség: A játék neurobiológiája A motiváció A motiváció az idegrendszer aspeficikus aktiváltsági állapota, melyet a külső szenzoros információk, és a szervezet belső
Dr. Péczely László Zoltán A Grastyán örökség: A játék neurobiológiája A motiváció A motiváció az idegrendszer aspeficikus aktiváltsági állapota, melyet a külső szenzoros információk, és a szervezet belső
Az idegsejtek kommunikációja. a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
Egyes központi idegrendszeri funkciók agykérgi szabályozása
 Egyes központi idegrendszeri funkciók agykérgi szabályozása Az agykéreg funkciói - Specifikus érző működések hallás látás szomatoszenzoros működés Specifikus mozgató működések szomatomotoros koordináció
Egyes központi idegrendszeri funkciók agykérgi szabályozása Az agykéreg funkciói - Specifikus érző működések hallás látás szomatoszenzoros működés Specifikus mozgató működések szomatomotoros koordináció
Orvosi élettan. Bevezetés és szabályozáselmélet Tanulási támpontok: 1.
 Orvosi élettan Bevezetés és szabályozáselmélet Tanulási támpontok: 1. Prof. Sáry Gyula 1 Orvosi élettan A tárgy Mit adunk? Visszajelzés www.markmyprofessor.com Domoki.Ferenc@med.u-szeged.hu 2 1 Az orvosi
Orvosi élettan Bevezetés és szabályozáselmélet Tanulási támpontok: 1. Prof. Sáry Gyula 1 Orvosi élettan A tárgy Mit adunk? Visszajelzés www.markmyprofessor.com Domoki.Ferenc@med.u-szeged.hu 2 1 Az orvosi
Etológia/BSc. Etológiai alapvetések: Történet és módszer. Miklósi Ádám Pongrácz Péter
 Etológia/BSc Etológiai alapvetések: Történet és módszer Miklósi Ádám Pongrácz Péter 2018 A félév tematikája alkalom Téma előadó 1 Bevezetés az etológia tudománya Pongrácz Péter 2 4 kérdés az etológiai
Etológia/BSc Etológiai alapvetések: Történet és módszer Miklósi Ádám Pongrácz Péter 2018 A félév tematikája alkalom Téma előadó 1 Bevezetés az etológia tudománya Pongrácz Péter 2 4 kérdés az etológiai
Az autonómia és complience, a fogyatékosság elfogadtatásának módszerei
 Az autonómia és complience, a fogyatékosság elfogadtatásának módszerei Dr. Kollár János egyetemi adjunktus Debreceni Egyetem Orvos- és Egészségtudományi Centrum, Népegészségügyi Kar Magatartástudományi
Az autonómia és complience, a fogyatékosság elfogadtatásának módszerei Dr. Kollár János egyetemi adjunktus Debreceni Egyetem Orvos- és Egészségtudományi Centrum, Népegészségügyi Kar Magatartástudományi
Poszt-traumás stressz zavar: a vietnámi háborútól a orvosbiológiáig
 MTA, Kísérleti Orvostudományi Kutatóintézet Poszt-traumás stressz zavar: a vietnámi háborútól a orvosbiológiáig Haller József Mi idézi elı? háború (katona, áldozat, passzív résztvevı) terrortámadás természeti
MTA, Kísérleti Orvostudományi Kutatóintézet Poszt-traumás stressz zavar: a vietnámi háborútól a orvosbiológiáig Haller József Mi idézi elı? háború (katona, áldozat, passzív résztvevı) terrortámadás természeti
Sav-bázis egyensúly. Dr. Miseta Attila
 Sav-bázis egyensúly Dr. Miseta Attila A szervezet és a ph A ph egyensúly szorosan kontrollált A vérben a referencia tartomány: ph = 7.35 7.45 (35-45 nmol/l) < 6.8 vagy > 8.0 halálozáshoz vezet Acidózis
Sav-bázis egyensúly Dr. Miseta Attila A szervezet és a ph A ph egyensúly szorosan kontrollált A vérben a referencia tartomány: ph = 7.35 7.45 (35-45 nmol/l) < 6.8 vagy > 8.0 halálozáshoz vezet Acidózis
Alsó és felső részén fehér, átlátszatlan, 4-es méretű, kemény zselatin kapszula, amely 155 mg fehér színű, szagtalan port tartalmaz.
 1. A GYÓGYSZER NEVE Tramalgic 50 mg kemény kapszula 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag: 50 mg tramadol-hidroklorid kapszulánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA
1. A GYÓGYSZER NEVE Tramalgic 50 mg kemény kapszula 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag: 50 mg tramadol-hidroklorid kapszulánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA
