Fizikai kémia. Tantárgy neve Fizikai kémia 1.
|
|
|
- Antal Somogyi
- 7 évvel ezelőtt
- Látták:
Átírás
1 Fizikai kémia A tárgy a kémia alapszak (BSC ) szakmai törzsanyagának fontos része. A három féléves anyag teljesítésével 20 kreditet (előadások:12, szeminárium jellegű számítási gyakorlatok:3, laboratóriumi gyakorlatok:5) lehet összegyűjteni, az összes órák száma 18. Az előadások összes óra száma: 9, a gyakorlatoké (szeminárium jellegű számítási gyakorlatok): 3, a laboratóriumi gyakorlatoké: 6. Tantárgy neve Fizikai kémia 1. KEB1401 Meghirdetés féléve 3 Kreditpont 4 Összóraszám (elm+gyak) Számonkérés módja kollokvium Előfeltétel (tantárgyi kód) KEB1003 Alapvető fizikai, kémiai jelenségek, törvényszerűségek ismertetése, elméletté fejlesztése, az anyag makroszkopikus és mikroszkopikus szervezettségi szintjén megjelenő tulajdonságainak, változásainak leírása a matematika eszközrendszerének felhasználásával. A termodinamika oktatásának célja annak megértetése, hogyan lehet az anyagi rendszerek tulajdonságait, változásait leírni általános érvényességű törvényekkel, pusztán csak makroszkopikus paraméterek segítségével, figyelmen kívül hagyva az individuális atomi tulajdonságokat. A hallgatók ismerjék a reverzibilitás és irreverzibilitás meghatározó jegyeit. TERMODINAMIKA A gázok tulajdonságai. A tökéletes gáz. A gáz állapot, gáztörvények. Reális gázok. Molekuláris kölcsönhatások. A van der Waals egyenlet. Kritikus állapot. A megfelelő állapotok tétele. A termodinamika első főtétele. A munka, hő és energia közti kapcsolat. A termodinamika első főtétele. A belső energia. Mechanikai munka. Térfogati munka. Az entalpia. Termokémia. (Standardentalpia-változás. Fizikai változások entalpiája. A képződési entalpia. Kémiai változások entalpiája. Hess-tétel. Born-Haber ciklus.) Az anyagok hőkapacitása. Kirchoff törvénye. A belsőenergia-változást és az entalpiaváltozást befolyásoló tényezők. A Joule kísérlet. A Joule-Thomson hatás. A C v és C p kapcsolata. Az adiabatikus kiterjesztés munkája. A kinetikus gázelmélet alapjai. A termodinamika második főtétele. Az önként végbemenő (spontán) változások. Az entrópia termodinamikai és statisztikus mechanikai értelmezése. A Clausius-féle egyenlőtlenség. Néhány fontos folyamat entrópiaváltozása. A termodinamika harmadik főtétele. Termikus folyamatok hatásfoka. (A hőerőgépek hatásfoka. A Carnot ciklus. A hűtés energetikája.). A Helmholtz- és Gibbs-függvény, szabadenergia, szabadentalpia. A standard reakciószabadentalpia. Az első és második főtétel egyesítése. Nyílt rendszerek és az összetétel változásai. A kémiai potenciál és tágabb jelentése, fugacitás.
2 Tiszta anyagok fizikai átalakulásai. Fázisdiagramok. (Fázishatárok. Egykomponensű rendszerek fázisdiagramjai.) Fázisstabilitás és fázisátmenet. (A hőmérséklet és nyomás hatása a fázisstabilitásra. A fázishatások elhelyezkedése a fázisátmenetek osztályozása.). Egyszerű elegyek fizikai változásai. Az elegyek termodinamikai leírása. (Parciális moláris mennyiségek. Az elegyedés termodinamikája. Folyadékok kémiai potenciálja. Folyadékelegyek. Kolligatív tulajdonságok.) Illékony folyadékok elegyei. (Gőznyomásdiagramok. Hőmérséklet-összetétel diagramok. Elegyek desztillálása.) Reális elegyek és oldatok. (Az oldószer aktivitása. Az oldott anyag aktivitása.). Fázisok, komponensek és szabadsági fokok. A fázistörvény. Kétkomponensű rendszerek. (Folyadékfolyadék fázisdiagramok. Korlátozottan elegyedő folyadékok desztillációja. Folyadék-szilárd fázisdiagramok.) Kémiai reakciók. Spontán kémiai reakciók. (A szabadentalpia minimuma. Reakciók egyensúly összetétele). A termodinamikai és a gyakorlati egyensúlyi állandó kapcsolata. A körülmények hatása az egyensúlyra. A Le Chatelier elv. A nyomás hatása az egyensúlyra. Néhány fontos reakció jellemzése. (Fémek előállítása oxidjaikból, sav-bázis egyensúlyok, az ATP termodinamikája.) 3.Évközi ellenőrzés módja A hallgató feladatmegoldó, ismereteket értelmező, rendszerező, vitákban résztvevő teljesítményének szóbeli értékelése a szeminárium-jellegű gyakorlatokon történik. Az otthoni feldolgozásra kiadott számítási feladatok elkészítésének ellenőrzése. Az előadás anyagából meghatározott számú (általában három) zárthelyi dolgozat írása. 4. A tárgy előírt külső szakmai gyakorlatai - 5. Kötelező és ajánlott irodalom P. W Atkins: Fizikai kémia I-II-III. Tankönyvkiadó. Budapest, Országh I.: Termodinamika: KLTE jegyzete. Debrecen, Liszi J., Schiller R., Ruff I., Varsányi Gy.: Bevezetés a fizikai kémiába. Műszaki Könyvkiadó. Budapest, C. Dillard és D. Goldberg: Kémia. Reakciók, szerkezetek, tulajdonságok. Gondolatkiadó. Budapest, Berecz E.: Fizikai kémia. Tankönyvkiadó. Budapest Riedel M.: Fizikai kémia, Budapest, Szabó K.: Fizikai kémia. Semmelweis Kiadó és Multimédia Stúdió A tantárgy tárgyi szükségletei Az előadásokat audiovizuális eszközökkel ellátott, légkondicionált előadóteremben tartjuk.
3 Tantárgy neve Fizikai kémia 2. KEB1403 Meghirdetés féléve 4 Kreditpont 4 Összóraszám (elm+gyak) Számonkérés módja kollokvium Előfeltétel (tantárgyi kód) KEB1401 Alapvető fizikai, kémiai jelenségek, törvényszerűségek ismertetése, elméletté fejlesztése, az anyag makroszkopikus és mikroszkopikus szervezettségi szintjén megjelenő tulajdonságainak leírása a matematika eszközrendszerének felhasználásával. A hallgatók legyenek képesek a termodinamikai ismereteket alkalmazni az elektrokémiai cellákban lejátszódó folyamatokra. Ismerjék meg, hogy bizonyos külső tényezők (hőmérséklet, koncentráció, elektromos potenciál, stb.), hogyan befolyásolják a transzport folyamatokat, vagyis a részecskék mozgását a gáz- és folyadék fázisban. A hallgatók tudják értelmezni a reakciósebesség fogalmát, legyenek képesek egyszerűbb sebességi egyenleteket megoldani, ismerjék az elemi lépések szerepét a bruttó folyamatokban. Tudják reakció-kinetikai alapokat felhasználni az összetett reakciók kinetikai jellemzésénél. Ismerjék meg milyen szerkezeti és energetikai változások történnek a reakció pillanatában, tudják alkalmazni erre a pillanatra termodinamikai és reakciókinetikai ismereteiket. Legyenek képesek szintetizálni termodinamikai, egyensúlyi elektrokémiai, anyag-transzporttal kapcsolatos és reakciókinetikai fogalom-rendszerüket az elektrolizáló és áramtermelő cellák szerkezetének, működésének elsajátításánál. ELEKTROKÉMIA. Egyensúlyi elektrokémia. Ionok termodinamikai sajátságai oldatokban. Ionaktivitások, Debye-Hückel elmélet. Elektrokémiai cellák. Elektródok típusai, redoxi-félreakciók. Standard-elektródpotenciálok, elektromotoros erő. Az elektródpotenciál felhasználása gyakorlati problémák megoldására. TRANSZPORT FOLYAMATOK. A transzport folyamatok általános jellemzése. A hővezetés. Diffúzió (Fick I. törvénye, kristályos sók oldódása, Fick II. törvénye). A viszkozitás. Elektrolitok áramvezetése (alapfogalmak, Kohlrausch törvénye, Ostwald-féle higítási törvény, vándorlási sebesség, mozgékonyság, átviteli szám). REAKCIÓKINETIKA. A kémiai reakciók sebessége. Tapasztalati reakciókinetika. Kísérleti módszerek a sebességi egyenlet meghatározására. Integrált sebességi egyenletek. Egyensúly közeli reakciók. A sebességi állandó hőmérséklet függése. A sebességi egyenlet értelmezése. Elemi reakciók. Egymást követő elemi reakciók, sebességmeghatározólépés. Steady-state közelítés. Előegyensúly. Michaelis-Menten mechanizmus. Unimolekuláris reakciók.
4 Az összetett reakciók kinetikája. Láncreakciók, robbanások. Fotokémiai reakciók. Polimerizáció. A katalitikus reakciók típusai. Az oszcilláló reakciók és a bistabilitás alapjai. REAKCIÓK MOLEKULÁRIS DINAMIKÁJA. Ütközési elmélet. Diffúziógátolt és energiagátolt reakciók. Anyagmérleg egyenlet. Az aktivált komplex elmélete. Potenciális energiafelületek. DINAMIKUS ELEKTROKÉMIA. Elekrtódfolyamatok. Elektromos kettősréteg és modelljei, Galvani-féle potenciál. Az elektródfolyamatok kinetikája. Az elektrokémiai polarizáció, a túlfeszültség és típusai (átlépési túlfeszültség, Tafel-egyenlet, diffúziós túlfeszültség.) Az elektrokémiai folyamatok. Elektrolízis. Áramtermelő galváncellák. Akkumulátorok. Tüzelőanyag-cellák. Korrózió, korrózióvédelem. A hallgató feladatmegoldó, ismereteket értelmező, rendszerező, vitákban résztvevő teljesítményének szóbeli értékelése a szeminárium-jellegű gyakorlatokon történik. Az otthoni feldolgozásra kiadott számítási feladatok elkészítésének ellenőrzése. Az előadás anyagából meghatározott számú (általában három) zárthelyi dolgozatot írnak. 4. A tárgy előírt külső szakmai gyakorlatai - 5. Kötelező és ajánlott irodalom P. W Atkins: Fizikai kémia I-II-III. Tankönyvkiadó. Budapest Országh I.: Termodinamika: KLTE jegyzete. Debrecen, M. J. Pilling, P. W. Seakins: Reakciókinetika. Nemzeti Tankönyvkiadó. Budapest, Liszi J., Schiller R., Ruff I., Varsányi Gy.: Bevezetés a fizikai kémiába. Műszaki Könyvkiadó. Budapest C. Dillard és D. Goldberg: Kémia. Reakciók, szerkezetek, tulajdonságok. Gondolatkiadó. Budapest, Kiss L.: Bevezetés az elektrokémiába. Nemzeti Tankönyvkiadó: Inzelt Gy.: Az elektrokémia korszerű elmélete és módszerei. I. II. Tankönyvkiadó, Berecz E.: Fizikai kémia. Tankönyvkiadó. Budapest Szabó K.: Fizikai kémia. Semmelweis Kiadó és Multimédia Stúdió A tantárgy tárgyi szükségletei Az előadásokat audiovizuális eszközökkel ellátott, légkondicionált előadóteremben tartjuk
5 Tantárgy neve Fizikai kémia 3. KEB1406 Meghirdetés féléve 5 Kreditpont 4 Összóraszám (elm+gyak) Számonkérés módja kollokvium Előfeltétel (tantárgyi kód) KEB1403 Alapvető fizikai, kémiai jelenségek, törvényszerűségek ismertetése, elméletté fejlesztése, az anyag makroszkopikus és mikroszkopikus szervezettségi szintjén megjelenő tulajdonságainak leírása a matematika eszközrendszerének felhasználásával. A hallgató ismerje meg az anyag egyik különlegesen fontos szerveződési szintjének, a nanoméretű kolloid részecskék világának szerkezetét, tulajdonságait, szerepét az iparban, a környezetben, a mindennapi életben. Értelmezésükhöz alkotó módon alkalmazza a termodinamikai, reakció-kinetikai, elektrokémiai ismereteit. Ismerje meg a radioaktív sugarak keletkezésének lehetőségeit, a sugárzás törvényszerűségeit, energetikai vonatkozásait, a maghasadás szerepét az energia termelésében. Az előadások további célja az atomenergiával kapcsolatos reális kép kialakítása. KOLLOIDKÉMIA. Kolloid állapot általános jellemzése. Inkoherens rendszerek. A diszperz rendszerek. Diszperz rendszerek jellemzése (diszperzitásfok, alak, eloszlás). A kolloid rendszerek állandósága. Kolloid rendszerek előállítása. Aeroszolok. Habok. Emulziók (előállításuk, emulgeátorok, stabilitásuk, gyakorlati alkalmazásuk). Szolok, szuszpenziók (előállításuk, stabilitásuk, a DLVO elmélet alapjai, a koaguláció, a szolok és szuszpenziók tulajdonságai). Asszociációs kolloidok, (fogalmuk, csoportosításuk, tulajdonságaik, kritikus micelláris koncentráció, az asszociáció elméleti értelmezése, a micellák szerkezete, mérete az asszociációs kolloidok gyakorlati jelentősége). Makromolekuláris kolloidok /polimerek/ (fogalmuk, méretük, alakjuk, moláris tömeg szerinti eloszlásuk, moláris tömegük meghatározása, ülepedésük, viszkozitásuk). Koherens rendszerek. A gélek fogalma, tulajdonságai, szerkezetük. Pórusos testek. Határfelületi jelenségek. Gázok és gőzök adszorpciója szilárd felületen. Fiziszorpció, kemiszorpció, adszorpciós izotermák. Adszorpció szilárd-folyadék felületen. Adszorpció nemelektrolit oldatokból. Adszorpció elektrolit-oldatokból. Az elektromos kettősréteg jellemzői. Az ioncsere-adszorpció. RADIOKÉMIA. Az atommag szerkezete, tulajdonságai. A radioaktivitás, az atommag bomlásának típusai., kinetikája. A sugárzás kölcsönhatása az anyaggal. Fúziós reakciók. Nukleogenezis. Hasadásos magreakciók. Atomreaktorok típusai, működése és radioaktív hulladékai. A radioaktivitás környezeti vonatkozásai. A radioaktív izotópok alkalmazásai.
6 A hallgató feladatmegoldó, ismereteket értelmező, rendszerező, vitákban résztvevő teljesítményének értékelése a szeminárium-jellegű gyakorlatokon történik. Az otthoni feldolgozásra kiadott számítási feladatok elkészítésének ellenőrzése. Az előadás anyagából meghatározott számú (általában három) zárthelyi dolgozat írnak. 4. A tárgy előírt külső szakmai gyakorlatai: - 5. Kötelező és ajánlott irodalom P. W Atkins: Fizikai kémia I-II-III. Tankönyvkiadó. Budapest Berecz E.: Fizikai kémia. Tankönyvkiadó. Budapest Fejes P., Hajdu É., Kókai M.: Radiokémia, Tankönyvkiadó, Budapest, Nagy Lajos Gy.: Radiokémia és izotóptechnika. Tankönyvkiadó, Budapest, Kiss I. Vértes A.: Magkémia. Akadémiai Kiadó, Budapest, Rohrsetzer S.: Kolloidika. Tankönyvkiadó, Budapest, Shaw, D. J.: Bevezetés a kolloid- és felületi kémiába. Műszaki Könyvkiadó, Szántó F.: A kolloidkémia alapjai. Gondolat Kiadó, Budapest, Patzkó Á.: Kolloidika alapjai, JATE Szakképzés, Phare, A tantárgy tárgyi szükségletei Az előadásokat audiovizuális eszközökkel ellátott, légkondicionált előadóteremben tartjuk. Tantárgy neve Fizikai kémia gyakorlat 1. KEB1402 Meghirdetés féléve 3 Kreditpont 1 Összóraszám (elm+gyak) Számonkérés módja gyakorlati jegy Előfeltétel (tantárgyi kód) KEB1401(E) A szeminárium jellegű gyakorlat feladata a fizikai kémiai ismeretek gyakorlása, reproduktív és produktív alkalmazása, az ellenőrzés és értékelés. A számítási feladatok szorosan kapcsolódnak az előadások anyagához, segítik annak megértését. A számítási feladatok célja a logikus gondolkodás, a matematikai készségek, a grafikus értékelés képességének fejlesztése. Feladatok az ideális gáztörvényekre, a Dalton törvényre és a van der Waals egyenlet alkalmazására, a kritikus állapot vizsgálatára. A differenciál-számítás gyakorlása. Integrálszámítás gyakorlása. Feladatmegoldások a termokémia első főtételére. Feladatok a második főtételre. Tiszta anyagok és elegyek halmazállapot-változásaira vonatkozó feladatok. Feladatok a sav-bázis egyensúlyokra. A hallgató feladatmegoldó, nehezebb ismereteket értelmező, rendszerező, vitákban résztvevő teljesítményének szóbeli értékelése a szeminárium-jellegű gyakorlatokon történik. Az otthoni
7 feldolgozásra kiadott számítási feladatok elkészítésének ellenőrzése. Az előadás anyagából meghatározott számú (általában három) zárthelyi dolgozatot írnak. A hallgatók a szemináriumon nyújtott problémamegoldó teljesítménye egyfajta visszajelzést ad a tananyag évközi elsajátításáról és felkészültségük szintjéről. 4. A tárgy előírt külső szakmai gyakorlatai - 5. A kötelező ill. ajánlott irodalom P. W Atkins: Fizikai kémiai feladatok és megoldásuk. Tankönyvkiadó. Budapest Maleczkiné Szenes Márta: Kémiai számítások, kémiai gondolatok. Veszprémi Egyetem sokszorosítója A tantárgy tárgyi szükségletei és ellátása Audiovizuális és szemléltető eszközökkel ellátott előadóteremben. Tantárgy neve Fizikai kémia gyakorlat 2. KEB1405 Meghirdetés féléve 4 Kreditpont 1 Összóraszám (elm+gyak) Számonkérés módja gyakorlati jegy Előfeltétel (tantárgyi kód) KEB1403(E) A szeminárium jellegű gyakorlat feladata a fizikai kémiai ismeretek gyakorlása, reproduktív és produktív alkalmazása, az ellenőrzés és értékelés. A számítási feladatok szorosan kapcsolódnak az előadások anyagához, segítik annak megértését. A számítási feladatok célja a logikus gondolkodás, a matematikai készségek, a grafikus értékelés képességének fejlesztése. Ionerősség, aktivitási koefficiens számítása. Az elektropotenciállal, elektromotoros erővel, elektrolízissel kapcsolatos feladatok. Feladatok az oldhatósági szorzatra. Reakciókinetikai feladatok megoldása. A hallgató feladatmegoldó, nehezebb ismereteket értelmező, rendszerező, vitákban résztvevő teljesítményének szóbeli értékelése a szeminárium-jellegű gyakorlatokon történik. Az otthoni feldolgozásra kiadott számítási feladatok elkészítésének ellenőrzése. Az előadás anyagából meghatározott számú (általában három) zárthelyi dolgozatot írnak. A hallgatók a szemináriumon nyújtott problémamegoldó teljesítménye egyfajta visszajelzést ad a tananyag évközi elsajátításáról és felkészültségük szintjéről 4. A tárgy előírt külső szakmai gyakorlatai - 5. A kötelező és ajánlott irodalom P. W Atkins: Fizikai kémiai feladatok és megoldásuk. Tankönyvkiadó. Budapest
8 Maleczkiné Szenes Márta: Kémiai számítások, kémiai gondolatok. Veszprémi Egyetem sokszorosítója A tantárgy tárgyi szükségletei és ellátása Audiovizuális és szemléltető eszközökkel ellátott előadóteremben. Tantárgy neve Fizikai kémia gyakorlat 3. KEB1407 Meghirdetés féléve 5 Kreditpont 1 Összóraszám (elm+gyak) Számonkérés módja gyakorlati jegy Előfeltétel (tantárgyi kód) KEB1406(E) 2. A tantárgy általános célja és specifikus célkitűzései A szeminárium jellegű gyakorlat feladata a fizikai kémiai ismeretek gyakorlása, reproduktív és produktív alkalmazása, az ellenőrzés és értékelés. A feladatok szorosan kapcsolódnak az előadások anyagához, segítik annak megértését. A számítási feladatok célja a logikus gondolkodás, a matematikai készségek, a grafikus értékelés képességének fejlesztése. 3. A tantárgy tartalma A kolloidok típusaira vonatkozó feladatok. Adszorpcióra vonatkozó feladatok. Részecskeméret-eloszlás meghatározása. Ülepedési sebesség meghatározás. Radioaktivitással és magreakciókkal kapcsolatos feladatok megoldása. 4. Évközi ellenőrzés módja A hallgató feladatmegoldó, nehezebb ismereteket értelmező, rendszerező, vitákban résztvevő teljesítményének szóbeli értékelése a szeminárium-jellegű gyakorlatokon történik. Az otthoni feldolgozásra kiadott számítási feladatok elkészítésének ellenőrzése. Az előadás anyagából meghatározott számú (általában három) zárthelyi dolgozatot írnak. A hallgatók a szemináriumon nyújtott problémamegoldó teljesítménye egyfajta visszajelzést ad a tananyag évközi elsajátításáról és felkészültségük szintjéről 5. A tárgy előírt külső szakmai gyakorlatai - 6. A kötelező és ajánlott irodalom Rohrsetzer S.: Kolloidika. Tankönyvkiadó, Budapest, Kiss I. Vértes A.: Magkémia, Akadémiai Könyvkiadó, Nagy Lajos György, Nagyné László Krisztina: Radiokémia és izotóptechnika, Műegyetemi Kiadó, Budapest, A tantárgy tárgyi szükségletei és ellátása Audiovizuális és szemléltető eszközökkel ellátott tanterem.
9 Tantárgy neve Bevezetés a fizikai kémiai mérésekbe KEB1408 Meghirdetés féléve 4 Kreditpont 2 Összóraszám (elm+gyak) Számonkérés módja gyakorlati jegy Előfeltétel (tantárgyi kód) KEB1401 Tantárgyfelelős neve Sarka Lajos Tantárgyfelelős beosztása Főiskolai docens A gyakorlat célja, hogy a hallgatók elsajátítsák az alapvető mérési módszereket, az egyszerűbb eszközöket készségszintjén tudják használni. Megtanulják a hibatényezők mérlegelését, a hibaszámítás alapjait. A gyakorlat munkafegyelemre, a munkaidő átgondolt, célszerű kihasználására, a balesetvédelmi előírások betartására ösztönöz. A mérési hibák. A hibaszámítás alapjai. Tömegmérés. Sűrűségmérés Mohr-Westphal-féle mérleggel. Sűrűségmérés piknométerrel. Fagyáspont-csökkenés mérése. Viszkozitás mérés Ostwald-féle viszkoziméterrel. Áram- és feszültségmérő használata. Elektromos vezetés mérése konduktométerrel. ph-mérés mérőműszerrel. Mérés spektrofotométerrel. Optikai forgatóképesség mérése polariméterrel. Törésmutató mérése refraktométerrel. Zárthelyi dolgozatok iratása, a laboratóriumi jegyzőkönyv ellenőrzése. Az osztályzat alapját a mérési eredmények pontossága, azok bemutatása, a diszkusszió, a jegyzőkönyv formai kivitelezésének színvonalat és a zárthelyi dolgozatokra kapott érdemjegy képzi. 4. A tárgy előírt külső szakmai gyakorlatai: - 5. Kötelező és ajánlott irodalom Bevezetés a fizikai kémiai mérésekbe. Debreceni Egyetem, Fizikai Kémiai Tanszék. Baltazárné Vass Katalin: Fizikai kémiai gyakorlatok. ELTE Kovács Barna, Kunsági Máté Sándor: Fizikai kémiai gyakorlatok. Janus Pannonius Tudományegyetem, Pécs, A tantárgy tárgyi szükségletei A gyakorlatot 12 személyes, a gyakorlatokhoz szükséges műszerekkel, eszközökkel vegyszerekkel felszerelt laboratóriumban tartjuk.
10 Tantárgy neve Fizikai kémia labor KEB1404 Meghirdetés féléve 5 Kreditpont 3 Összóraszám (elm+gyak) Számonkérés módja gyakorlati jegy Előfeltétel (tantárgyi kód) KEB1403 A gyakorlat célja az, hogy a hallgatók az előadásokon elhangzott ismereteket, törvényszerűségeket elmélyítsék, kísérletileg igazolják és a gyakorlatban alkalmazzák. A gyakorlat új, önálló ismeretszerzésre is ösztönöz. A gyakorlat további célja az, hogy több oldalról rávilágítson arra, hogy egy konkrét elméleti probléma milyen mérési módszerekkel közelíthető meg, a mérésekből az adatok feldolgozása és értékelése után milyen információk nyerhetők. A gyakorlat a körülmények gondos figyelembe vételére, a hibatényezők mérlegelésére, a munkafegyelem és a balesetvédelmi előírások betartására, a munkaidő átgondolt, célszerű kihasználására ösztönöz. Fejleszti az anyagismeretet és a kísérletező készséget. Disszociációhő meghatározása semlegesítési hő mérésével, kalorimetriásan. Kevéssé oldódó só oldhatóságának meghatározása vezetőképesség mérés alapján. Indikátor pk illetve protonállódási állandó meghatározása spektrofotometriásan. Gyenge sav disszociációs fokának és disszociáció-állandójának meghatározása konduktometriásan. Egyensúlyi állandó meghatározása extrakciós módszerrel. Ezüstamminkomplex összetételének és stabilitási állandójának meghatározása. Jodid-perszulfát reakció tanulmányozása. Savkatalízis vizsgálata cukorinverzió kinetikájában. Etil-acetát hidrolízisének kinetikája. Oszcillációs reakció vizsgálata. Redoxi potenciál mérése. Kritikus micellaképződési koncentráció meghatározása. Ioncserés adszorpció vizsgálata. Radioaktív sugárzás és az anyag kölcsönhatásának vizsgálata. A gyakorlat anyagából a hallgatók zárthelyi dolgozatokat írnak. Az osztályzat alapját a mérési eredmények pontossága, azok feldolgozása és tárgyilagos, reális diszkussziója, a jegyzőkönyv formai kivitelezésének színvonala és a zárthelyi dolgozatokra kapott érdemjegy képezi. 4. A tárgy előírt külső szakmai gyakorlatai: - 5. A kötelező és ajánlott irodalom Debreceni egyetem TTK Munkaközösség: Fizikai kémiai laboratóriumi gyakorlatok. Nemzeti Tankönyvkiadó, Hargitainé Tóth Ágnes: Fizikai kémiai mérések. Oktatási segédanyag. Nyíregyházi Főiskola, Kaposi Olivér.: Bevezetés a fizikai kémiai mérésekbe. Tankönyvkiadó, Budapest, Kovács Barna, Kunsági Máté Sándor: Fizikai kémiai gyakorlatok. Janus Pannonius Tudományegyetem, Pécs, 1997.
11 Peintler Gábor (szerkesztő): Fizikai kémiai laboratóriumi gyakorlatok. Szegedi Egyetem, Szeged, A tantárgy tárgyi szükségletei és ellátása A gyakorlatokat 12 személyes, a mérési gyakorlatokhoz szükséges műszerekkel és eszközökkel, vegyszerekkel felszerelt laboratóriumban végzik.
SZBN Fizikai kémia 2017/18/2
 4 kredit vizsga Alapozó modul tavasszal Foglalkozás/félév: 28 óra előadás + 0 óra gyakorlat + 0 óra szeminárium = összesen 28 óra Kurzus létszámkorlát: min. 1 fő max. 100 fő Tematika 1. hét: Tökéletes
4 kredit vizsga Alapozó modul tavasszal Foglalkozás/félév: 28 óra előadás + 0 óra gyakorlat + 0 óra szeminárium = összesen 28 óra Kurzus létszámkorlát: min. 1 fő max. 100 fő Tematika 1. hét: Tökéletes
OGA-FZ1-T Fizikai kémia /18/2
 2 kredit vizsga Alapozó modul tavasszal ajánlott félév: 2. Foglalkozás/félév: 28 óra előadás + 0 óra gyakorlat + 0 óra szeminárium = összesen 28 óra Kurzus létszámkorlát: min. 1 fő max. 100 fő Előfeltételek:
2 kredit vizsga Alapozó modul tavasszal ajánlott félév: 2. Foglalkozás/félév: 28 óra előadás + 0 óra gyakorlat + 0 óra szeminárium = összesen 28 óra Kurzus létszámkorlát: min. 1 fő max. 100 fő Előfeltételek:
Elektrokémia kommunikációs dosszié ELEKTROKÉMIA. ANYAGMÉRNÖK NAPPALI MSc KÉPZÉS, SZABADON VÁLASZTHATÓ TÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 ELEKTROKÉMIA ANYAGMÉRNÖK NAPPALI MSc KÉPZÉS, SZABADON VÁLASZTHATÓ TÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014. Tartalom jegyzék 1. Tantárgyleírás,
ELEKTROKÉMIA ANYAGMÉRNÖK NAPPALI MSc KÉPZÉS, SZABADON VÁLASZTHATÓ TÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014. Tartalom jegyzék 1. Tantárgyleírás,
Általános kémia képletgyűjtemény. Atomszerkezet Tömegszám (A) A = Z + N Rendszám (Z) Neutronok száma (N) Mólok száma (n)
 Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
ÁLTALÁNOS ÉS SZERVETLEN KÉMIA SZIGORLATI VIZSGAKÉRDÉSEK 2010/2011 TANÉVBEN ÁLTALÁNOS KÉMIA
 ÁLTALÁNOS ÉS SZERVETLEN KÉMIA SZIGORLATI VIZSGAKÉRDÉSEK 2010/2011 TANÉVBEN ÁLTALÁNOS KÉMIA 1. Kémiai alapfogalmak: - A kémia alaptörvényei ( a tömegmegmaradás törvénye, állandó tömegarányok törvénye) -
ÁLTALÁNOS ÉS SZERVETLEN KÉMIA SZIGORLATI VIZSGAKÉRDÉSEK 2010/2011 TANÉVBEN ÁLTALÁNOS KÉMIA 1. Kémiai alapfogalmak: - A kémia alaptörvényei ( a tömegmegmaradás törvénye, állandó tömegarányok törvénye) -
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
Kiss László Láng Győző ELEKTROKÉMIA
 Kiss László Láng Győző ELEKTROKÉMIA A könyv megjelenését támogatta a Magyar Tudományos Akadémia Kémiai Tudományok Osztálya Dr. Kiss László, Dr. Láng Gőző, 2011 ISBN 978 963 331 148 6 A könyv és adathordozó
Kiss László Láng Győző ELEKTROKÉMIA A könyv megjelenését támogatta a Magyar Tudományos Akadémia Kémiai Tudományok Osztálya Dr. Kiss László, Dr. Láng Gőző, 2011 ISBN 978 963 331 148 6 A könyv és adathordozó
PHYWE Fizikai kémia és az anyagok tulajdonságai
 PHYWE Fizikai kémia és az anyagok tulajdonságai Témakörök: Gázok és gáztörvények Felületi feszültség Viszkozitás Sűrűség és hőtágulás Olvadáspont, forráspont, lobbanáspont Hőtan és kalorimetria Mágneses
PHYWE Fizikai kémia és az anyagok tulajdonságai Témakörök: Gázok és gáztörvények Felületi feszültség Viszkozitás Sűrűség és hőtágulás Olvadáspont, forráspont, lobbanáspont Hőtan és kalorimetria Mágneses
Visy Csaba Kredit 4 Heti óraszám 3 típus AJÁNLOTT IRODALOM. P. W. Atkins: Fizikai kémia I.
 A tárgy neve FIZIKAI KÉMIA 1. Meghirdető tanszék(csoport) SZTE TTK FIZIKAI KÉMIAI TANSZÉK Felelős oktató: Visy Csaba Kredit 4 Heti óraszám 3 típus Előadás Számonkérés Kollokvium Teljesíthetőség feltétele
A tárgy neve FIZIKAI KÉMIA 1. Meghirdető tanszék(csoport) SZTE TTK FIZIKAI KÉMIAI TANSZÉK Felelős oktató: Visy Csaba Kredit 4 Heti óraszám 3 típus Előadás Számonkérés Kollokvium Teljesíthetőség feltétele
Tantárgy neve. Környezetfizika. Meghirdetés féléve 6 Kreditpont 2 Összóraszám (elm+gyak) 2+0
 Tantárgy neve Környezetfizika Tantárgy kódja FIB2402 Meghirdetés féléve 6 Kreditpont 2 Összóraszám (elm+gyak) 2+0 Számonkérés módja Kollokvium Előfeltétel (tantárgyi kód) - Tantárgyfelelős neve Dr. Varga
Tantárgy neve Környezetfizika Tantárgy kódja FIB2402 Meghirdetés féléve 6 Kreditpont 2 Összóraszám (elm+gyak) 2+0 Számonkérés módja Kollokvium Előfeltétel (tantárgyi kód) - Tantárgyfelelős neve Dr. Varga
Gergely Pál - Erdőd! Ferenc ALTALANOS KÉMIA
 Gergely Pál - Erdőd! Ferenc ALTALANOS KÉMIA TARTALOM KÉMIAI ALAPFOGALMAK 1 Sí rendszer 1 Atomok és elemek 2 Tiszta anyagok és keverékek 3 Az atomok szerkezete 4 Az atom alkotórészei 4 Az atommag felépítése
Gergely Pál - Erdőd! Ferenc ALTALANOS KÉMIA TARTALOM KÉMIAI ALAPFOGALMAK 1 Sí rendszer 1 Atomok és elemek 2 Tiszta anyagok és keverékek 3 Az atomok szerkezete 4 Az atom alkotórészei 4 Az atommag felépítése
Általános kémia gyakorlat vegyészmérnököknek. 2015/2016. őszi félév
 Általános kémia gyakorlat vegyészmérnököknek 2015/2016. őszi félév Zárthelyik A zárthelyik időpontja az kari zh-időpont: 17 00 19 00. A zárthelyik időtartama 90 perc. Mindkét zárthelyin legalább 50%-ot
Általános kémia gyakorlat vegyészmérnököknek 2015/2016. őszi félév Zárthelyik A zárthelyik időpontja az kari zh-időpont: 17 00 19 00. A zárthelyik időtartama 90 perc. Mindkét zárthelyin legalább 50%-ot
T E M A T I K A. Óvó- és Tanítóképző Intézet
 Óvó- és Tanítóképző Intézet T E M A T I K A a tanító szakos hallgatók számára TERMÉSZETTUDOMÁNY A HÉTKÖZNAPOKBAN (CB3313) oktatáshoz 2018/2019. tanév I. félév Heti óraszám: 0 óra előadás 1 óra szeminárium
Óvó- és Tanítóképző Intézet T E M A T I K A a tanító szakos hallgatók számára TERMÉSZETTUDOMÁNY A HÉTKÖZNAPOKBAN (CB3313) oktatáshoz 2018/2019. tanév I. félév Heti óraszám: 0 óra előadás 1 óra szeminárium
TÁJÉKOZTATÓ. I. évf. állatorvostan-hallgatók részére KÉMIA. 2013/14 tanév, 1. félév
 TÁJÉKOZTATÓ I. évf. állatorvostan-hallgatók részére KÉMIA 2013/14 tanév, 1. félév A KÉMIAI TANSZÉK OKTATÓI DR. NEMES PÉTER DR. SCHEIBER PÁL DR. VARGA TAMÁS DR. VINCZE ZOLTÁN DR. PILIPECZ MIHÁLY tanszékvezető,
TÁJÉKOZTATÓ I. évf. állatorvostan-hallgatók részére KÉMIA 2013/14 tanév, 1. félév A KÉMIAI TANSZÉK OKTATÓI DR. NEMES PÉTER DR. SCHEIBER PÁL DR. VARGA TAMÁS DR. VINCZE ZOLTÁN DR. PILIPECZ MIHÁLY tanszékvezető,
KÉMIAI ALAPFOGALMAK, SZTÖCHIOMETRIA
 Általános kémia A tárgy a kémia alapszak (BSC) szakmai törzsanyagának első, alapozó része, melynek teljesítésével 8 kreditet (előadás: 4, szeminárium jellegű számítási gyakorlat:1, laboratóriumi gyakorlat:
Általános kémia A tárgy a kémia alapszak (BSC) szakmai törzsanyagának első, alapozó része, melynek teljesítésével 8 kreditet (előadás: 4, szeminárium jellegű számítási gyakorlat:1, laboratóriumi gyakorlat:
FIZIKAI KÉMIA ANYAGMÉRNÖKI KAR ENERGETIKAI MÉRNÖKASSZISZTENS FELSŐFOKÚ SZAKKÉPZÉS
 ENERGETIKAI MÉRNÖKASSZISZTENS FIZIKAI KÉMIA ANYAGMÉRNÖKI KAR ENERGETIKAI MÉRNÖKASSZISZTENS FELSŐFOKÚ SZAKKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET
ENERGETIKAI MÉRNÖKASSZISZTENS FIZIKAI KÉMIA ANYAGMÉRNÖKI KAR ENERGETIKAI MÉRNÖKASSZISZTENS FELSŐFOKÚ SZAKKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET
KOLLOIDKÉMIA ANYAGMÉRNÖK BSc. NAPPALI TÖRZSANYAG
 KOLLOIDKÉMIA ANYAGMÉRNÖK BSc. NAPPALI TÖRZSANYAG TANTÁRGYI MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2018/19. tanév I. félév 1 Tartalomjegyzék 1. Tantárgyleírás,tárgyjegyző, óraszám,
KOLLOIDKÉMIA ANYAGMÉRNÖK BSc. NAPPALI TÖRZSANYAG TANTÁRGYI MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2018/19. tanév I. félév 1 Tartalomjegyzék 1. Tantárgyleírás,tárgyjegyző, óraszám,
A kémiatanári zárószigorlat tételsora
 1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
Általános kémia gyakorlat biomérnököknek
 Általános kémia gyakorlat biomérnököknek Zárthelyi követelmények A zárthelyik időtartama 90 perc. Mindkét zárthelyin legalább 50%-ot kell teljesíteni az elégséges jegyért. Akinek nincs meg az 50%-os eredménye,
Általános kémia gyakorlat biomérnököknek Zárthelyi követelmények A zárthelyik időtartama 90 perc. Mindkét zárthelyin legalább 50%-ot kell teljesíteni az elégséges jegyért. Akinek nincs meg az 50%-os eredménye,
5. előadás 12-09-16 1
 5. előadás 12-09-16 1 H = U + PV; U=Q-PV H = U + (PV); P= áll H = U + P V; U=Q-P V; U=Q-P V H = Q U= Q V= áll P= áll H = G + T S Munkává nem alakítható Hátalakulás = G + T S 2 3 4 5 6 7 Szilárd halmazállapot
5. előadás 12-09-16 1 H = U + PV; U=Q-PV H = U + (PV); P= áll H = U + P V; U=Q-P V; U=Q-P V H = Q U= Q V= áll P= áll H = G + T S Munkává nem alakítható Hátalakulás = G + T S 2 3 4 5 6 7 Szilárd halmazállapot
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
Fizikai Kémia törzsmodul
 Fizikai Kémia törzsmodul Bevezetés a fizikai kémiai mérésekbe (óraszám: 0+0+4, kreditszám: 0+0+3) Fizikai Kémia I. (óraszám: 2+2+0, kreditszám: 3+1+0) Fizikai kémia II. (óraszám: 3+2+4, kreditszám: 4+1+3)
Fizikai Kémia törzsmodul Bevezetés a fizikai kémiai mérésekbe (óraszám: 0+0+4, kreditszám: 0+0+3) Fizikai Kémia I. (óraszám: 2+2+0, kreditszám: 3+1+0) Fizikai kémia II. (óraszám: 3+2+4, kreditszám: 4+1+3)
VÍZKÉMIA TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 KÖRNYEZETMÉRNÖKI MESTERKÉPZÉS TÖRZSANYAG TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014 1 Tartalomjegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
KÖRNYEZETMÉRNÖKI MESTERKÉPZÉS TÖRZSANYAG TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014 1 Tartalomjegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
Kolloidkémia 1. előadás Első- és másodrendű kémiai kötések és szerepük a kolloid rendszerek kialakulásában. Szőri Milán: Kolloidkémia
 Kolloidkémia 1. előadás Első- és másodrendű kémiai kötések és szerepük a kolloid rendszerek kialakulásában 1 Órarend 2 Kurzussal kapcsolatos emlékeztető Kurzus: Az előadás látogatása ajánlott Gyakorlat
Kolloidkémia 1. előadás Első- és másodrendű kémiai kötések és szerepük a kolloid rendszerek kialakulásában 1 Órarend 2 Kurzussal kapcsolatos emlékeztető Kurzus: Az előadás látogatása ajánlott Gyakorlat
FIZIKAI KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG
 FIZIKAI KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2013. Tartalomjegyzék 1 1. Tantárgyleírás, tárgyjegyző,
FIZIKAI KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2013. Tartalomjegyzék 1 1. Tantárgyleírás, tárgyjegyző,
Követelmények: f - részvétel az előadások 67 %-án - 3 db érvényes ZH (min. 50%) - 4 elfogadott laborjegyzőkönyv
 Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Az elektromos kettősréteg. Az elektromos potenciálkülönbség eredete, értéke és az azt befolyásoló tényezők. Kolloidok stabilitása.
 Az elektromos kettősréteg. Az elektromos potenciálkülönbség eredete, értéke és az azt befolyásoló tényezők. Kolloidok stabilitása. Adszorpció oldatból szilárd felületre Adszorpció oldatból Nem-elektrolitok
Az elektromos kettősréteg. Az elektromos potenciálkülönbség eredete, értéke és az azt befolyásoló tényezők. Kolloidok stabilitása. Adszorpció oldatból szilárd felületre Adszorpció oldatból Nem-elektrolitok
Általános kémia gyakorlat biomérnököknek
 Általános kémia gyakorlat biomérnököknek Zárthelyi követelmények A zárthelyik időtartama 90 perc. Mindkét zárthelyin legalább 50%-ot kell teljesíteni az elégséges jegyért. Akinek nincs meg az 50%-os eredménye,
Általános kémia gyakorlat biomérnököknek Zárthelyi követelmények A zárthelyik időtartama 90 perc. Mindkét zárthelyin legalább 50%-ot kell teljesíteni az elégséges jegyért. Akinek nincs meg az 50%-os eredménye,
Kémiai metallurgia-ii (Fémelőállítási folyamatok elméleti alapjai)
 MISKOLCI EGYETEM Műszaki Anyagtudományi Kar Kerpely Antal Anyagtudományok és Technológiák Doktori Iskola Kémiai metallurgia-ii (Fémelőállítási folyamatok elméleti alapjai) Dr. Kékesi Tamás TANTÁRGYLEÍRÁS
MISKOLCI EGYETEM Műszaki Anyagtudományi Kar Kerpely Antal Anyagtudományok és Technológiák Doktori Iskola Kémiai metallurgia-ii (Fémelőállítási folyamatok elméleti alapjai) Dr. Kékesi Tamás TANTÁRGYLEÍRÁS
Kémia. (állatorvos szak)
 Kémia Helye: 1. év 1. félév Előadás: 45 óra Gyakorlat: 45 óra Kredit: 6 Értékelés: vizsga (kollokvium) (állatorvos szak) Kémiai Tanszék Előadó Előadó: Dr. Scheiber Pál tanszékvezető egyetemi tanár Elérhető:
Kémia Helye: 1. év 1. félév Előadás: 45 óra Gyakorlat: 45 óra Kredit: 6 Értékelés: vizsga (kollokvium) (állatorvos szak) Kémiai Tanszék Előadó Előadó: Dr. Scheiber Pál tanszékvezető egyetemi tanár Elérhető:
Korrózió kommunikációs dosszié KORRÓZIÓ. ANYAGMÉRNÖK NAPPALI BSc KÉPZÉS, SZABADON VÁLASZTHATÓ TÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 KORRÓZIÓ ANYAGMÉRNÖK NAPPALI BSc KÉPZÉS, SZABADON VÁLASZTHATÓ TÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014. Tartalom jegyzék 1. Tantárgyleírás,
KORRÓZIÓ ANYAGMÉRNÖK NAPPALI BSc KÉPZÉS, SZABADON VÁLASZTHATÓ TÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014. Tartalom jegyzék 1. Tantárgyleírás,
KÉMIATANÁRI SZAK. NAPPALI TAGOZAT
 Általános kémia előadás KE1007 Meghirdetés féléve 1 Összóraszám (elm+gyak) 2+0 kollokvium KE1009(E) Hargitainé dr. Tóth Ágnes habilitált főiskolai tanár A kémia alapvető fogalmainak, törvényszerűségeinek
Általános kémia előadás KE1007 Meghirdetés féléve 1 Összóraszám (elm+gyak) 2+0 kollokvium KE1009(E) Hargitainé dr. Tóth Ágnes habilitált főiskolai tanár A kémia alapvető fogalmainak, törvényszerűségeinek
Általános és szervetlen kémia Laborelıkészítı elıadás I.
 Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
TANTÁRGYI TEMATIKA ÉS FÉLÉVI KÖVETELMÉNYRENDSZER
 TANTÁRGYI TEMATIKA ÉS FÉLÉVI KÖVETELMÉNYRENDSZER Tantárgy neve Természetismeret ttp. Tantárgy kódja BTA1224 Meghirdetés féléve II.évf. 2.félév Kreditpont: 4 Heti kontaktóraszám (elm.+gyak.) 1+2 Félévi
TANTÁRGYI TEMATIKA ÉS FÉLÉVI KÖVETELMÉNYRENDSZER Tantárgy neve Természetismeret ttp. Tantárgy kódja BTA1224 Meghirdetés féléve II.évf. 2.félév Kreditpont: 4 Heti kontaktóraszám (elm.+gyak.) 1+2 Félévi
Kolloidkémia 5. Előadás Kolloidstabilitás. Szőri Milán: Kolloidkémia
 Kolloidkémia 5. Előadás Kolloidstabilitás Szőri Milán: Kolloidkémia 1 Kolloidok stabilitása Termodinamikailag lehetnek stabilisak (valódi oldatok) Liofil kolloidok G oldat
Kolloidkémia 5. Előadás Kolloidstabilitás Szőri Milán: Kolloidkémia 1 Kolloidok stabilitása Termodinamikailag lehetnek stabilisak (valódi oldatok) Liofil kolloidok G oldat
Az energia bevezetése az iskolába. Készítette: Rimai Anasztázia
 Az energia bevezetése az iskolába Készítette: Rimai Anasztázia Bevezetés Fizika oktatása Energia probléma Termodinamika a tankönyvekben A termodinamikai fogalmak kialakulása Az energia fogalom története
Az energia bevezetése az iskolába Készítette: Rimai Anasztázia Bevezetés Fizika oktatása Energia probléma Termodinamika a tankönyvekben A termodinamikai fogalmak kialakulása Az energia fogalom története
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
Főkérdések fizikai-kémia kollokviumra gyógyszerész hallgatók számára, tanév, I. félév.
 1. Gáztörvények. Az ideális gáztörvény érvényességének feltételei. A termodinamikai hőmérséklet. 2. A termodinamika alapfogalmainak definíciói. 3. A termodinamika első főtétele. A belső energia, a munka
1. Gáztörvények. Az ideális gáztörvény érvényességének feltételei. A termodinamikai hőmérséklet. 2. A termodinamika alapfogalmainak definíciói. 3. A termodinamika első főtétele. A belső energia, a munka
Tantárgy kódja Tantárgy neve Óraszám Kredit Szemeszter Előadás Gyakorlat Otthoni SMKKB2031XN. Mérőné Dr. Nótás Erika egyetemi docens
 Tantárgy kódja Tantárgy neve Óraszám Kredit Szemeszter Előadás Gyakorlat Otthoni SMKKB2031XN Mezőgazdasági 2 2 4 4 1 kémia Tárgyfelelős: Mérőné Dr. Nótás Erika egyetemi docens Ötsoros összefoglaló A tantárgy
Tantárgy kódja Tantárgy neve Óraszám Kredit Szemeszter Előadás Gyakorlat Otthoni SMKKB2031XN Mezőgazdasági 2 2 4 4 1 kémia Tárgyfelelős: Mérőné Dr. Nótás Erika egyetemi docens Ötsoros összefoglaló A tantárgy
Bevezetés a laboratóriumi gyakorlatokba
 A fizika matematikai alapjai I. MT4008L Meghirdetés féléve 1 Összóraszám (elm+gyak) 6+12 Gyakorlati jegy Tantárgyfelelős neve Dr. Rozgonyi Tibor A részletes tantárgyleírást lásd: MT1008 Mechanika 1. FI4101L
A fizika matematikai alapjai I. MT4008L Meghirdetés féléve 1 Összóraszám (elm+gyak) 6+12 Gyakorlati jegy Tantárgyfelelős neve Dr. Rozgonyi Tibor A részletes tantárgyleírást lásd: MT1008 Mechanika 1. FI4101L
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Reakciókinetika és katalízis
 Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Meghirdetés féléve 2. Kreditpont 4. Összóraszám (elm+gyak) A részletes tantárgyleírást lásd:ke1101. Kreditpont 4.
 Általános kémia előadás KE4007L KE4009L(E) A részletes tantárgyleírást lásd:ke1007 Általános kémia laboratóriumi gyakorlat KE4009L KE4007L(E) A részletes tantárgyleírást lásd:ke1009 Anyagszerkezet alapjai
Általános kémia előadás KE4007L KE4009L(E) A részletes tantárgyleírást lásd:ke1007 Általános kémia laboratóriumi gyakorlat KE4009L KE4007L(E) A részletes tantárgyleírást lásd:ke1009 Anyagszerkezet alapjai
KÖVETELMÉNYEK 2017/ félév. Informatika II.
 Tantárgy neve Informatika II. Tantárgy kódja TAB1110 Meghirdetés féléve 4. Kreditpont 1 Heti kontakt óraszám (elm. + gyak.) 0 + 1 Félévi követelmény Előfeltétel (tantárgyi kód) TAB1109 Tantárgyfelelős
Tantárgy neve Informatika II. Tantárgy kódja TAB1110 Meghirdetés féléve 4. Kreditpont 1 Heti kontakt óraszám (elm. + gyak.) 0 + 1 Félévi követelmény Előfeltétel (tantárgyi kód) TAB1109 Tantárgyfelelős
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
TANTÁRGYI ADATLAP. Mechatronika/Mechatronikus mérnök Végzettség
 TANTÁRGYI ADATLAP 1. A tanulmányi program jellemzői 1.1 A felsőoktatási intézmény Sapientia Erdélyi Magyar Tudományegyetem 1.2 Kar Marosvásárhelyi Műszaki és Humán Tudományok Kar 1.3 Tanszék Gépészmérnöki
TANTÁRGYI ADATLAP 1. A tanulmányi program jellemzői 1.1 A felsőoktatási intézmény Sapientia Erdélyi Magyar Tudományegyetem 1.2 Kar Marosvásárhelyi Műszaki és Humán Tudományok Kar 1.3 Tanszék Gépészmérnöki
1. Mi a folytonos anyagelmélet négy eleme? 2. Mi a Dalton-féle atomelmélet négy alaptétele (posztulátuma)? 3. Mi az SI mértékegység rendszer 7
 1. Mi a folytonos anyagelmélet négy eleme? 2. Mi a Dalton-féle atomelmélet négy alaptétele (posztulátuma)? 3. Mi az SI mértékegység rendszer 7 alapmennyisége, mi ezek jele? 4. Mi az SI mértékegység rendszer
1. Mi a folytonos anyagelmélet négy eleme? 2. Mi a Dalton-féle atomelmélet négy alaptétele (posztulátuma)? 3. Mi az SI mértékegység rendszer 7 alapmennyisége, mi ezek jele? 4. Mi az SI mértékegység rendszer
SZÁMÍTÓGÉPES KÉMIA ALAPJAI VEGYÉSZMÉRNÖK BSc. NAPPALI TÖRZSANYAG
 SZÁMÍTÓGÉPES KÉMIA ALAPJAI VEGYÉSZMÉRNÖK BSc. NAPPALI TÖRZSANYAG TANTÁRGYI MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2019/20. tanév I. félév 1 Tartalomjegyzék 1. Tantárgyleírás
SZÁMÍTÓGÉPES KÉMIA ALAPJAI VEGYÉSZMÉRNÖK BSc. NAPPALI TÖRZSANYAG TANTÁRGYI MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2019/20. tanév I. félév 1 Tartalomjegyzék 1. Tantárgyleírás
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Általános kémia vizsgakérdések
 Általános kémia vizsgakérdések 1. Mutassa be egy atom felépítését! 2. Mivel magyarázza egy atom semlegességét? 3. Adja meg a rendszám és a tömegszám fogalmát! 4. Mit nevezünk elemnek és vegyületnek? 5.
Általános kémia vizsgakérdések 1. Mutassa be egy atom felépítését! 2. Mivel magyarázza egy atom semlegességét? 3. Adja meg a rendszám és a tömegszám fogalmát! 4. Mit nevezünk elemnek és vegyületnek? 5.
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Előszó.. Bevezetés. 1. A fizikai megismerés alapjai Tér is idő. Hosszúság- és időmérés.
 SZABÓ JÁNOS: Fizika (Mechanika, hőtan) I. TARTALOMJEGYZÉK Előszó.. Bevezetés. 1. A fizikai megismerés alapjai... 2. Tér is idő. Hosszúság- és időmérés. MECHANIKA I. Az anyagi pont mechanikája 1. Az anyagi
SZABÓ JÁNOS: Fizika (Mechanika, hőtan) I. TARTALOMJEGYZÉK Előszó.. Bevezetés. 1. A fizikai megismerés alapjai... 2. Tér is idő. Hosszúság- és időmérés. MECHANIKA I. Az anyagi pont mechanikája 1. Az anyagi
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
A kémiai és az elektrokémiai potenciál
 Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
REAKCIÓKINETIKA ÉS KATALÍZIS
 REAKCIÓKINETIKA ÉS KATALÍZIS ANYAGMÉRNÖK MESTERKÉPZÉS VEGYIPARI TECHNOLÓGIAI SZAKIRÁNY MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET PETROLKÉMIAI KIHELYEZETT (TVK) INTÉZETI TANSZÉK Miskolc,
REAKCIÓKINETIKA ÉS KATALÍZIS ANYAGMÉRNÖK MESTERKÉPZÉS VEGYIPARI TECHNOLÓGIAI SZAKIRÁNY MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET PETROLKÉMIAI KIHELYEZETT (TVK) INTÉZETI TANSZÉK Miskolc,
Alkalmazott matematika és módszerei I Tantárgy kódja
 Tantárgy neve Alkalmazott matematika és módszerei I Tantárgy kódja MTB1901 Meghirdetés féléve Kreditpont 4 Összóraszám (elm+gyak) + Számonkérés módja G Előfeltétel (tantárgyi kód) - Tantárgyfelelős neve
Tantárgy neve Alkalmazott matematika és módszerei I Tantárgy kódja MTB1901 Meghirdetés féléve Kreditpont 4 Összóraszám (elm+gyak) + Számonkérés módja G Előfeltétel (tantárgyi kód) - Tantárgyfelelős neve
A kémia alapképzés (BSc) képzési terve
 A kémia alapképzés (BSc) képzési terve A: Alapképzés: 128 kredit I: Szakmai alapozó képzés 109 kredit I.1. Természettudományos alapozó képzés 17 kredit Kurzus Krediszkelés Óra- Érté- Felelős Felelős oktató
A kémia alapképzés (BSc) képzési terve A: Alapképzés: 128 kredit I: Szakmai alapozó képzés 109 kredit I.1. Természettudományos alapozó képzés 17 kredit Kurzus Krediszkelés Óra- Érté- Felelős Felelős oktató
Általános Kémia, 2008 tavasz
 9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
Alkalmazott kémia. Tantárgy neve Alkalmazott kémia 1.
 Alkalmazott kémia A tárgy a kémia alapszak (BSC) szakmai törzsanyagának része, melynek teljesítésével két szemeszter alatt 8 kreditet lehet összegyűjteni. Az előadások száma 8. Tantárgy neve Alkalmazott
Alkalmazott kémia A tárgy a kémia alapszak (BSC) szakmai törzsanyagának része, melynek teljesítésével két szemeszter alatt 8 kreditet lehet összegyűjteni. Az előadások száma 8. Tantárgy neve Alkalmazott
MŐSZAKI KÉMIA. Anyagmérnök MSc képzés. Tantárgyi Kommunikációs Dosszié MISKOLCI EGYETEM MŐSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET
 MŐSZAKI KÉMIA Anyagmérnök MSc képzés Tantárgyi Kommunikációs Dosszié MISKOLCI EGYETEM MŐSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2009 Tartalomjegyzék 1. Tantárgyleírás, tantárgyjegyzı, óraszám,
MŐSZAKI KÉMIA Anyagmérnök MSc képzés Tantárgyi Kommunikációs Dosszié MISKOLCI EGYETEM MŐSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2009 Tartalomjegyzék 1. Tantárgyleírás, tantárgyjegyzı, óraszám,
KÖVETELMÉNYEK II. félév
 KÖVETELMÉNYEK 2016-2017. II. félév Tantárgy neve Multikulturális nevelés Tantárgy kódja SPB2102 Meghirdetés féléve 6 Kreditpont: 3 Félévi óraszám (elm.+gyak.) 1+1 Félévi követelmény Kollokvium Előfeltétel
KÖVETELMÉNYEK 2016-2017. II. félév Tantárgy neve Multikulturális nevelés Tantárgy kódja SPB2102 Meghirdetés féléve 6 Kreditpont: 3 Félévi óraszám (elm.+gyak.) 1+1 Félévi követelmény Kollokvium Előfeltétel
ALKALMAZOTT KÉMIA ÉS TRANSZPORTFOLYAMATOK
 ALKALMAZOTT KÉMIA ÉS TRANSZPORTFOLYAMATOK Anyagmérnök/Kohómérnők MSc képzés Tantárgyi Kommunikációs Dosszié MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014 Tartalomjegyzék 1. Tantárgyleírás,
ALKALMAZOTT KÉMIA ÉS TRANSZPORTFOLYAMATOK Anyagmérnök/Kohómérnők MSc képzés Tantárgyi Kommunikációs Dosszié MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014 Tartalomjegyzék 1. Tantárgyleírás,
TANTÁRGYI KÖVETELMÉNYRENDSZER Mezőgazdasági és élelmiszeripari gépészmérnök szak III. évf. 2010/2011. tanév II. félév
 TANTÁRGYI KÖVETELMÉNYRENDSZER Mezőgazdasági és élelmiszeripari gépészmérnök szak III. évf. 2010/2011. tanév II. félév 1. TANTÁRGY CÍME: ÉLELMISZERIPARI MŰVELETEK 2. TANTÁRGY KÓDJA, ÓRASZÁMA: NMGAG013 ELMÉLET
TANTÁRGYI KÖVETELMÉNYRENDSZER Mezőgazdasági és élelmiszeripari gépészmérnök szak III. évf. 2010/2011. tanév II. félév 1. TANTÁRGY CÍME: ÉLELMISZERIPARI MŰVELETEK 2. TANTÁRGY KÓDJA, ÓRASZÁMA: NMGAG013 ELMÉLET
ACÉLMETALLURGIA ALAPJAI. Anyagmérnök BSc-képzés. Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ. Miskolc, 2014.
 MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR METALLURGIAI ÉS ÖNTÉSZETI INTÉZET ACÉLMETALLURGIA ALAPJAI Anyagmérnök BSc-képzés Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS
MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR METALLURGIAI ÉS ÖNTÉSZETI INTÉZET ACÉLMETALLURGIA ALAPJAI Anyagmérnök BSc-képzés Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS
ÖNTÖTT ÖTVÖZETEK FÉMTANA
 ÖNTÖTT ÖTVÖZETEK FÉMTANA ANYAGMÉRNÖK BSC KÉPZÉS JÁRMŰIPARI ÖNTÉSZETI SZAKIRÁNY (nappali munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR JÁRMŰIPARI ÖNTÉSZETI INTÉZETI
ÖNTÖTT ÖTVÖZETEK FÉMTANA ANYAGMÉRNÖK BSC KÉPZÉS JÁRMŰIPARI ÖNTÉSZETI SZAKIRÁNY (nappali munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR JÁRMŰIPARI ÖNTÉSZETI INTÉZETI
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
TANMENET FIZIKA. 10. osztály. Hőtan, elektromosságtan. Heti 2 óra
 TANMENET FIZIKA 10. osztály Hőtan, elektromosságtan Heti 2 óra 2012-2013 I. Hőtan 1. Bevezetés Hőtani alapjelenségek 1.1. Emlékeztető 2. 1.2. A szilárd testek hőtágulásának törvényszerűségei. A szilárd
TANMENET FIZIKA 10. osztály Hőtan, elektromosságtan Heti 2 óra 2012-2013 I. Hőtan 1. Bevezetés Hőtani alapjelenségek 1.1. Emlékeztető 2. 1.2. A szilárd testek hőtágulásának törvényszerűségei. A szilárd
FIZIKAI KÉMIA ANYAGMÉRNÖKI LEVELEZŐ MSc. KOMPENZÁCIÓS TANTÁRGY
 FIZIKAI KÉMIA ANYAGMÉRNÖKI LEVELEZŐ MSc. KOMPENZÁCIÓS TANTÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2013/14. II. félév 1 Tartalomjegyzék 1.
FIZIKAI KÉMIA ANYAGMÉRNÖKI LEVELEZŐ MSc. KOMPENZÁCIÓS TANTÁRGY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2013/14. II. félév 1 Tartalomjegyzék 1.
A csoport B csoport C csoport D csoport E csoport Sebestyén Timári Sarolta / Lihi Norbert Várnagy Katalin Nagy Zoltán Tóth Zoltán vegyészmérnök,
 oktató szak 09.09-13. napi 2x2 óra 1-10 szem. 8-10 D404 hétfő 16-18 K/6 A csoport B csoport C csoport D csoport E csoport Sebestyén Timári Sarolta / Lihi Annamária Norbert Várnagy Katalin Nagy Zoltán Tóth
oktató szak 09.09-13. napi 2x2 óra 1-10 szem. 8-10 D404 hétfő 16-18 K/6 A csoport B csoport C csoport D csoport E csoport Sebestyén Timári Sarolta / Lihi Annamária Norbert Várnagy Katalin Nagy Zoltán Tóth
9. évfolyam. Osztályozóvizsga tananyaga FIZIKA
 9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
ELEKTROKÉMIA. - elektrolitokban: ionok irányított mozgása. Elektrolízis: elektromos áram által előidézett kémiai átalakulás
 ELEKTROKÉMIA 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
ELEKTROKÉMIA 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
KÖVETELMÉNYEK 2018/ FÉLÉV. 1. hét Szervezési feladatok. Tematika, követelmények.
 KÖVETELMÉNYEK 2018/19. 1. FÉLÉV A tantárgy kódja: BOV1114 A tantárgy neve: Matematikai nevelés és módszertana II. Kredit: 3 Kontakt óraszám: 2 óra/hét Féléves tematika: 1. hét Szervezési feladatok. Tematika,
KÖVETELMÉNYEK 2018/19. 1. FÉLÉV A tantárgy kódja: BOV1114 A tantárgy neve: Matematikai nevelés és módszertana II. Kredit: 3 Kontakt óraszám: 2 óra/hét Féléves tematika: 1. hét Szervezési feladatok. Tematika,
A kémia alapképzés (BSc) képzési terve
 A kémia alapképzés (BSc) képzési terve A: Alapképzés: 128 kredit I: Szakmai alapozó képzés 109 kredit I.1. Természettudományos alapozó képzés 17 kredit Kurzus Krediszkelés Óra- Érté- Felelős Felelős oktató
A kémia alapképzés (BSc) képzési terve A: Alapképzés: 128 kredit I: Szakmai alapozó képzés 109 kredit I.1. Természettudományos alapozó képzés 17 kredit Kurzus Krediszkelés Óra- Érté- Felelős Felelős oktató
Kolloidkémia 8. Előadás Kolloidstabilitás. Szőri Milán: Kolloidkémia
 Kolloidkémia 8. Előadás Kolloidstabilitás Szőri Milán: Kolloidkémia 1 Kolloidok stabilitása Termodinamikailag lehetnek stabilisak (valódi oldatok) Liofil kolloidok G oldat
Kolloidkémia 8. Előadás Kolloidstabilitás Szőri Milán: Kolloidkémia 1 Kolloidok stabilitása Termodinamikailag lehetnek stabilisak (valódi oldatok) Liofil kolloidok G oldat
A KÉMIA ÉRETTSÉGI VIZSGA ÁLTALÁNOS KÖVETELMÉNYEI
 A KÉMIA ÉRETTSÉGI VIZSGA ÁLTALÁNOS KÖVETELMÉNYEI A vizsga formája Középszinten: írásbeli vagy szóbeli Emelt szinten: írásbeli és szóbeli A kémia érettségi vizsga célja A középszintû érettségi vizsgán elsõsorban
A KÉMIA ÉRETTSÉGI VIZSGA ÁLTALÁNOS KÖVETELMÉNYEI A vizsga formája Középszinten: írásbeli vagy szóbeli Emelt szinten: írásbeli és szóbeli A kémia érettségi vizsga célja A középszintû érettségi vizsgán elsõsorban
Diffúzió. Diffúzió. Diffúzió. Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
 Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Az elektrokémia áttekintése
 Az elektrokémia áttekintése 1 Homogén Heterogén Egyensúlyi elektrokémia (árammentes rendszerek) Elektrolitoldatok termodinamikája: elektrolitos disszociáció ionok termodinamikája és aktivitása Galvánelemek/galváncellák
Az elektrokémia áttekintése 1 Homogén Heterogén Egyensúlyi elektrokémia (árammentes rendszerek) Elektrolitoldatok termodinamikája: elektrolitos disszociáció ionok termodinamikája és aktivitása Galvánelemek/galváncellák
Az elektrokémia áttekintése
 1 Az elektrokémia áttekintése 2 Elektródfolyamatok kinetikája (heterogén dinamikus elektrokémia) Homogén Heterogén Egyensúlyi elektrokémia (árammentes rendszerek) Elektrolitoldatok termodinamikája: elektrolitos
1 Az elektrokémia áttekintése 2 Elektródfolyamatok kinetikája (heterogén dinamikus elektrokémia) Homogén Heterogén Egyensúlyi elektrokémia (árammentes rendszerek) Elektrolitoldatok termodinamikája: elektrolitos
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI II. Ismerjük fel, hogy többkomponens fázisegyensúlyokban a folyadék fázisnak kitüntetett szerepe van!
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
Korrózió kommunikációs dosszié KORRÓZIÓ. ANYAGMÉRNÖK LEVELEZŐ BSc KÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 KORRÓZIÓ ANYAGMÉRNÖK LEVELEZŐ BSc KÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI TANSZÉK Miskolc, 2008. Tartalom jegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
KORRÓZIÓ ANYAGMÉRNÖK LEVELEZŐ BSc KÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI TANSZÉK Miskolc, 2008. Tartalom jegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
TANTÁRGYI KÖVETELMÉNYRENDSZER Élelmiszermérnök szak III. évf. 2010/2011. tanév I. félév
 TANTÁRGYI KÖVETELMÉNYRENDSZER Élelmiszermérnök szak III. évf. 2010/2011. tanév I. félév 1. TANTÁRGY CÍME: ÉLELMISZERIPARI MŰVELETEK 3. TANTÁRGY KÓDJA: NEMAT205/1 ELMÉLET 3+0 NEMAT206/1-2 GYAKORLAT 0+2
TANTÁRGYI KÖVETELMÉNYRENDSZER Élelmiszermérnök szak III. évf. 2010/2011. tanév I. félév 1. TANTÁRGY CÍME: ÉLELMISZERIPARI MŰVELETEK 3. TANTÁRGY KÓDJA: NEMAT205/1 ELMÉLET 3+0 NEMAT206/1-2 GYAKORLAT 0+2
Kémia alapszak (BSc)
 Kémia alapszak (BSc) A Kémia alapszak (BSc) záróvizsga tételei tárgycsoportonként 1) Elemi anyagszerkezet. Az anyag atomos szerkezete, a Bohr és a kvantummechanikai atommodell alapfeltevései. Kvantumszámok
Kémia alapszak (BSc) A Kémia alapszak (BSc) záróvizsga tételei tárgycsoportonként 1) Elemi anyagszerkezet. Az anyag atomos szerkezete, a Bohr és a kvantummechanikai atommodell alapfeltevései. Kvantumszámok
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Dinamikus modellek felállítása mérnöki alapelvek segítségével
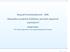 IgyR - 3/1 p. 1/20 Integrált Gyártórendszerek - MSc Dinamikus modellek felállítása mérnöki alapelvek segítségével Hangos Katalin PE Villamosmérnöki és Információs Rendszerek Tanszék IgyR - 3/1 p. 2/20
IgyR - 3/1 p. 1/20 Integrált Gyártórendszerek - MSc Dinamikus modellek felállítása mérnöki alapelvek segítségével Hangos Katalin PE Villamosmérnöki és Információs Rendszerek Tanszék IgyR - 3/1 p. 2/20
Többkomponensű rendszerek. Diszperz rendszerek. Kolloid rendszerek tulajdonságai. Folytonos közegben eloszlatott részecskék - diszperz rendszerek
 Többkomponensű rendszerek 7. hét Folytonos közegben eloszlatott részecskék - diszperz rendszerek homogén - kolloid - heterogén rendszerek - a részecskék mérete alapján Diszperz rendszerek Homogén rendszerek
Többkomponensű rendszerek 7. hét Folytonos közegben eloszlatott részecskék - diszperz rendszerek homogén - kolloid - heterogén rendszerek - a részecskék mérete alapján Diszperz rendszerek Homogén rendszerek
Statisztika 1. Tantárgyi útmutató
 Módszertani Intézeti Tanszék Nappali tagozat Statisztika 1. Tantárgyi útmutató 2015/16 tanév II. félév 1/6 Tantárgy megnevezése: Statisztika 1. Tantárgy kódja: STAT1KAMEMM Tanterv szerinti óraszám: 2+2
Módszertani Intézeti Tanszék Nappali tagozat Statisztika 1. Tantárgyi útmutató 2015/16 tanév II. félév 1/6 Tantárgy megnevezése: Statisztika 1. Tantárgy kódja: STAT1KAMEMM Tanterv szerinti óraszám: 2+2
ÁLTALÁNOS KÉMIA SZEMINÁRIUM (TTKBG0101) I. ÉVES KÉMIA, VEGYÉSZMÉRNÖK ÉS BIOMÉRNÖK BSC SZAKOS HALLGATÓK SZÁMÁRA (2017/18. I. félév)
 1 ÁLTALÁNOS KÉMIA SZEMINÁRIUM (TTKBG0101) I. ÉVES KÉMIA, VEGYÉSZMÉRNÖK ÉS BIOMÉRNÖK BSC SZAKOS HALLGATÓK SZÁMÁRA (2017/18. I. félév) oktató szak A csoport B csoport C csoport D csoport Sebestyén Annamária
1 ÁLTALÁNOS KÉMIA SZEMINÁRIUM (TTKBG0101) I. ÉVES KÉMIA, VEGYÉSZMÉRNÖK ÉS BIOMÉRNÖK BSC SZAKOS HALLGATÓK SZÁMÁRA (2017/18. I. félév) oktató szak A csoport B csoport C csoport D csoport Sebestyén Annamária
Kémiai reakciók mechanizmusa számítógépes szimulációval
 Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly
 Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
Molekulák mozgásban a kémiai kinetika a környezetben
 Energiatartalék Molekulák mozgásban a kémiai kinetika a környezetben A termodinamika és a kinetika A termodinamika a lehetőség θ θ θ G = H T S A kinetika a valóság: 1. A fizikai rész: - a reaktánsoknak
Energiatartalék Molekulák mozgásban a kémiai kinetika a környezetben A termodinamika és a kinetika A termodinamika a lehetőség θ θ θ G = H T S A kinetika a valóság: 1. A fizikai rész: - a reaktánsoknak
13 Elektrokémia. Elektrokémia Dia 1 /52
 13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
Helyi tanterv a kémia. tantárgy oktatásához
 Helyi tanterv a kémia. tantárgy oktatásához 1. A tanterv szerzıi: Név szerint ki, vagy kik készítették 2. Óraszámok: 9. osztály 36.. óra (humán) 10. osztály óra 11. osztály -.óra 12. osztály -.óra SZAKKÖZÉPISKOLA
Helyi tanterv a kémia. tantárgy oktatásához 1. A tanterv szerzıi: Név szerint ki, vagy kik készítették 2. Óraszámok: 9. osztály 36.. óra (humán) 10. osztály óra 11. osztály -.óra 12. osztály -.óra SZAKKÖZÉPISKOLA
ÁLTALÁNOS KÉMIA SZEMINÁRIUM (TTKBG0101) I. ÉVES KÉMIA, VEGYÉSZMÉRNÖK BSC ÉS KÉMIA TANÁR SZAKOS HALLGATÓK SZÁMÁRA (2019/20. I.
 1 ÁLTALÁNOS KÉMIA SZEMINÁRIUM (TTKBG0101) I. ÉVES KÉMIA, VEGYÉSZMÉRNÖK BSC ÉS KÉMIA TANÁR SZAKOS HALLGATÓK SZÁMÁRA (2019/20. I. félév) A csoport B csoport C csoport D csoport oktató Kánya Nándor Homolya
1 ÁLTALÁNOS KÉMIA SZEMINÁRIUM (TTKBG0101) I. ÉVES KÉMIA, VEGYÉSZMÉRNÖK BSC ÉS KÉMIA TANÁR SZAKOS HALLGATÓK SZÁMÁRA (2019/20. I. félév) A csoport B csoport C csoport D csoport oktató Kánya Nándor Homolya
KÖVETELMÉNYEK. Előfeltétel (tantárgyi kód) - Tantárgyfelelős neve és beosztása Dr. Pauwlik Zsuzsa Orsika főiskolai docens
 Az iskola mentálhigiénéje PSX 1211L Meghirdetés féléve 2. Kreditpont: 3 Konzultációs óraszám 10 Gyakorlati jegy TK Zárthelyi dolgozat írása az előadás és a kötelező irodalom alapján a vizsgaidőszak első
Az iskola mentálhigiénéje PSX 1211L Meghirdetés féléve 2. Kreditpont: 3 Konzultációs óraszám 10 Gyakorlati jegy TK Zárthelyi dolgozat írása az előadás és a kötelező irodalom alapján a vizsgaidőszak első
FIZIKA KÖZÉPSZINTŐ SZÓBELI FIZIKA ÉRETTSÉGI TÉTELEK Premontrei Szent Norbert Gimnázium, Gödöllı, 2012. május-június
 1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
Az anyagi rendszerek csoportosítása
 Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
ORVOSI KÉMIA GYAKORLATOK 2014/2015, ÁOK, FOK, OLKDA 1.év/1. félév CSOPORT A GYAKORLATI TEREM CSOPORT B GYAKORLATI TEREM
 TAN. HÉT 1., 8-14. 2., 15-21. 3., 22-28. ORVOSI KÉMIA GYAKORLATOK 2014/2015, ÁOK, FOK, OLKDA 1.év/1. félév CSOPORT A GYAKORLATI TEREM CSOPORT B GYAKORLATI TEREM Balesetvédelmi és tűzvédelmi oktatás. Alapvető
TAN. HÉT 1., 8-14. 2., 15-21. 3., 22-28. ORVOSI KÉMIA GYAKORLATOK 2014/2015, ÁOK, FOK, OLKDA 1.év/1. félév CSOPORT A GYAKORLATI TEREM CSOPORT B GYAKORLATI TEREM Balesetvédelmi és tűzvédelmi oktatás. Alapvető
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont)
 Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
