Szakmai protokoll a varicella kezeléséhez és megelőzéséhez Infektológiai Szakmai Kollégium Aktualizált változat (2009)
|
|
|
- Ervin Lukács
- 9 évvel ezelőtt
- Látták:
Átírás
1 1 Szakmai protokoll a varicella kezeléséhez és megelőzéséhez Infektológiai Szakmai Kollégium Aktualizált változat (2009) Az irányelv érvényessége a kihirdetéstől számított 3 év, amennyiben a témakörrel kapcsolatosan a jelen irányelv módosítását szükségessé tevő új tudományos eredmény a változtatást nem teszi korábban szükségessé. I. Alapvető megfontolások 1. A protokoll érvényességi területe: minden ellátási szint. 2. A protokoll feltétel nélkül bevezethető. 3. Definíció. A bárányhimlő nagy kontagiozitású vírusfertőzés, amely a klinikai kép alapján csaknem minden esetben kórismézhető. Az átvészeltség szerokonverzióval jár és ép immunitás esetén életre szóló védettséget jelent. A gyermekkori megbetegedések általában enyhe lefolyásúak. Adoleszcens kortól lényegesen gyakoribbak a szövődmények. Immunkompromittált egyénben kezeletlenül halálos kimenetelű lehet. 4. Panaszok és tünettan. Heveny fertőzéses megbetegedés jellegzetes, viszkető hólyagos kiütéssel és többnyire lázzal. 5. A betegség leírása. A kórokozó a légutak nyálkahártyáját fertőzi meg, majd a nyirokrendszerbe kerülvén hét nappal a fertőződés után primér virémiát okoz és a szövetekben replikálódik. Többnyire két héttel a fertőződés után, a szekunder virémia nyomán jelentkeznek a betegség tünetei papulákkal, majd a jól ismert hólyagokkal. Újabb erupciók megjelenésére öt-hét napig lehet számítani. A bőr és a garatnyálkahártya után a leggyakrabban érintett szervek a tüdők, a belek, a mononukleáris-makrofág rendszer, ritkábban az agy, a retina és az izületek. A betegek többsége kisgyermek, ill. kisiskolás korú ben hazánkban esetet jelentettek (incidencia: 480/100 ezer lakos). Ennél minden bizonnyal több eset fordult elő. 6. Kóreredet. Az alfa-herpeszvírusok alcsaládjába sorolt varicellovírus (korábbi elnevezése: varicella-zostervírus) okozza. 7. Epidemiológiai megfontolások Átvészeltséget jelent: az anamnesztikus bárányhimlő vagy a specifikus IgG osztályú
2 2 antitest kimutathatósága 7.2. Szignifikáns expozició: fertőző egyén azonos háztartásban, szoros kontaktus legalább öt percig, azonos légtérben tartózkodás legalább egy órán keresztül. A fertőzés forrása lehet: bárányhimlős beteg, disszeminált övsömörben szenvedő beteg, fedetlen testtájon zostert hordozó beteg, immunkompromittált övsömörös beteg (virémia!) Lappangási idő: , az esetek döntő többségében nap. Immun-szupprimált állapotban rövidebb, hiperimmunglobulin alkalmazása után hosszabb (28 nap) lehet A fertőzőképesség: a kiütés előtt két nappal kezdődik és a teljes pörkösödésig (általában 4-5 napig) tart (IV. szintű evidencia) Elkülönités: a kiütés megjelenésétől legalább 5 napig, ill. az erupciók pörkösödéséig indokolt A szövődmények szempontjából magasabb kockázatú (nem immunszupprimált) populációk: felnőtt: terhes, erős dohányos, súlyos idült tüdőbeteg gyermek: súlyos idült tüdőbeteg, tartós salicylkezelésben részesülő, súlyos idült bőrbetegségben-, az intermedier anyagcsere zavarában szenvedő II. Diagnózis. A klinikai kép ismeretén alapszik. 1. Az anamnézis az átvészeltség / szignifikáns expozíció megítélésével adhat segítséget a kórisme megállapításához. 2. A belszervi vizsgálat típusos kórkép esetében a kórisme megállapításához elegendő. 3. Egyéb vizsgálatok kezdeményezése csak szövődményes esetekben (ld. később) indokolt. 4. Differenciáldiagnózis. Kizárólag a kiütések morfológiája alapján olykor nehézséget okozhat az atypusos erupciók felismerése immunkompromittált betegben, továbbá egyéb infekciózus kórképektől (herpes simplex vírus, enterovírusok, Staphylococcus aureus okozta fertőzés), ill. nem fertőzéses, főleg allergiás patomechanizmusú betegségektől (gyógyszer-dermatózis, strofulus stb.) való elkülönítése. A klinikai kép alapján kétséges esetekben indokolt lehet a virológiai vizsgálat. A betegség első öt napján megkísérelhető a direkt víruskimutatás monoklonális fluoreszcens jelölésű monokolonális antitest segítségével a hólyagbennékből. A mintát torokváladék vételére alkalmas pálcával a hólyagalap széli részének erőteljes törlésével célszerű venni, hogy a morfológiai diagnózis megállapításához elegendő vírustartalmú sejt kerüljön a pálcára. Több, mint tíz napja zajló kórkép esetében a specifikus IgM kimutatása igazolja a kórismét.
3 3 III. Kezelés A/ Nem gyógyszeres kezelés 1. Immunkompetens beteg típusos bárányhimlővel az alapellátás keretei között kezelendő. 2. A hospitalizáció javallatai: súlyosabb bőr-lágyrészfertőzés toxikus állapot mellkasi panasz / tünet idegrendszeri panasz / tünet atipusos kiütések vérzés hasi vagy mellkasi fájdalom elhúzódó / megújuló láz 6 nap után újabb erupciók jelentkezése 6 napon túl magas kockázatú egyén esetében megfontolandó 3. A betegség bejelentendő. 4. Betegápolás A viszketést enyhitheti a bőrt hűsitő zuhanyozás, hintőporok alkalmazása. Gyermekkorban célszerű a körmöket rövidre vágni. Fontos a megfelelő folyadékbevitel biztositása. B/ Gyógyszeres kezelés 1. Oki terápia: acyclovir (ACV) Posztexpoziciós állapotban megelőzésre, továbbá lokális alkalmazása nem javasolható. Nem bizonyított, hogy a szövődmények megelőzésére alkalmas. Az allergiától eltekintve az ACV kezelésnek ellenjavallata nincsen. Jelentős gyógyszerkölcsönhatással nem kell számolni. A vesefunkció beszűkülése esetén csökkentendő a dózis. Egyéb antivirális szer nem jön szóba a bárányhimlő kezelésében. Gyógyszerrezisztenciával csak AIDS betegnél kell számolni. (Terhesség alatti varicella antivirális kezelésre a 4. pontban van ajánlás.) 1.1. Az intravénás kezelés javallatai progressiv varicella / immunszupprimált egyén atipusos kiütéssel járó betegsége / generalizálódott zostere újszülött perinatális betegsége (ha az anyai varicella a születés előtt 5 napon belül, ill. azt követően 2 napon belül manifesztálódott) (Megjegyzés: a terhes anya övsömöre nem érinti
4 4 a magzatot; III. szintű evidencia) virus-mediálta szövődmények (pneumonitis, meningoencephalitis) Adagolás: 3 hónaposnál fiatalabb csecsemőnek és felnőttnek 10(-15) mg/ttkg/dosi, 3 hónap és 12 év között 500 mg/m 2 /dosi 8 óránként infúzióban. A terápia tartama 5-10 nap (súlyos kórképben, ill. elhúzódó javulás esetén, pl. encephalitisben hosszabb) Az orális kezelés javallatai Az iniciális per os terápiának csak a kiütés megjelenését követően órán belül elkezdve van értelme! Immunkompetens felnőtt szövődménymentes bárányhimlője esetén a kórlefolyást lerövidíti (Ib szintű evidencia). 13 évesnél idősebbek tipusos varicellája (opcionális; családban akvirált megbetegedés esetében indokolt) immunkompetens, de rizikócsoportba tartozó egyén tipusos varicellája immunszupprimált betegek tipusos varicellája (folyamatos megfigyelés mellett) a parenteralisan megkezdett terápia folytatása Adagolás: 13 év fölött 5 x 800 mg naponta öt-hét napig 3 hó 12 év: 4 x 20 mg/ttkg naponta öt-hét napig (max. 800 mg/dosi) alternativa: 3 hó 2 év: 4 x 200 mg naponta öt-hét napig 2-5 év: 4 x 400 mg naponta öt-hét napig 6-12 év: 4 x 800 mg naponta öt-hét napig Háromhónaposnál fiatalabb csecsemő orális kezelésére vonatkozóan nincs elegendő tapasztalat. Immunkompromittált betegek kezelését a megfelelő ellenanyag szint kialakulásáig folytatni kell. Kétévesnél idősebb immunkompromittált gyermeknél a disszemináció megelőzésére a felnőtt adag alkalmazható. 2. Tüneti kezelés a szövődmények megelőzése érdekében. Lázcsillapitásra ne salicyltartalmú készitményt használjunk! A bőr öntisztulását akadályozó, arról nehezen eltávolitható rázókeverék (Susp. Zinci aquosa) kerülendő. Megkisérelhető antihistamin hatású szer szisztémás -nem lokális!- használata, bár erre vonatkozóan nincsenek az irodalomban evidencia szintek megállapításához klinikai vizsgálatok.
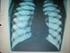
5 5 IV. Szövődmények, prevenció és prophylaxis 1. Szövődmények; komplikált varicella Komplikált bárányhimlős beteg ellátásához infektológiai konzílium szükséges. Bakteriális felülfertőzés A 6. nap után, ill. újabb erupciók megjelenése nélkül észlelt láz avagy láztalan állapotot követő újabb láz esetén bakteriális szövődményt kell feltételezni. A bakterialis szuperinfekció többnyire az erupciók fertőződését jelenti (impetigo, cellulitis) és S. pyogenes, ill. S. aureus idézi elő. Invaziv Streptococcus betegség (véráram-fertőzés, toxicus shock syndroma) lehet a következménye. A mikrobiológiai diagnózishoz hemokultúra vizsgálat, ill. a felülfertőzés területéből vett minta (hólyagbennék, szövetnedv stb.) bakteriológiai vizsgálata szükséges. A felülfertőzést penicillinnel, S. aureus kóroki szerepe esetén antistaphylococcalis szerrel kell kezelni. A gyermekkori Streptococcalis Toxicus Shock Syndroma első kockázati tényezője a bárányhimlő. Pneumonitis Egészséges adoleszcensek és felnőttek esetében leggyakoribb szövődmény a pneumonitis. A kiütések megjelenését 1-3 nappal követően légúti panaszok utalnak a tüdő érintettségére. A diagnózist mellkasröntgen felvétel igazolja. Neuroinfekció (cerebelláris ataxia, meningitis, meningoencephalitis) Hematológiai rendellenességek (thrombocytopenia, leukopenia) A neurológiai és hematológiai komplikációk kórházi szakellátást igényelnek. Progresszív varicella A folyamat a parenchymás szerveket is érinti és erre az erupciók atipusos volta utalhat. Kezeletlenül többnyire fatális. Reye syndroma A salicylkészitmények és a Reye syndroma összefüggése miatt ezen szerek alkalmazása varicella esetében tilos. Csillapithatatlan hányás -esetleg tudatzavarral társulva- föl kell vesse a betegség gyanúját. 2. Prevenció A bárányhimlő megelőzősének hatékony eszköze az aktív immunizáció, élő, attenuált kórokozó tartalmú védőoltással. Az immunizáció globális járványügyi hatását, a bárányhimlő megbetegedés előfordulásának 85%-os csökkenését, igen magas 98-99%-os
6 6 átoltottságnál észlelhetjük. Több mint 10 éves tapasztalat alapján az egyén leghatékonyabb védelmét fertőzést hosszútávon kivédő humorális ellenanyagszintet, T sejtes immunválaszt és boosterelhető immunmemóriát -, minden életkorban 2 oltás után érhetjük el. Javallat: Fogékonyak alapimmunizálása: 2 oltás minimum 4-6 hét különbséggel * Korábban oltottak felzárkózó oltása** *Alapimmunizálást javasolt 15 hónapos korban, az MMR oltással egy időben, és 18 hónaposan, az esedékes DPaT-IPV-HIB oltással egy időben elvégezni. ** Alapimmunizált egyént, - amennyiben oltás után áttöréses fertőzése nem volt - bármely időpontban (legkorábban 4-6 héttel az első oltás után), de legkésőbb egy újabb közösségbe kerülés előtt, második oltásban kell részesíteni. Második oltás csökkenti az egyetlen adag után kialakuló elégtelen védettség előfordulását, és mind a humorális, mind a T sejtes immunválaszt a természetes immunválasznak megfelelő szintűre erősíti, ezáltal jelentően csökkenti az oltás után előforduló áttöréses fertőzés létrejöttét. 3. Posztexpoziciós profilaxis (fogékony egyén szignifikáns expoziciója esetén) 3/A Hyperimmunglobulin (Varicella-Zoster-Immunglobulin, VZIG) Javallat: immunszupprimált egyén terhes újszülött súlyos alapbetegségben szenvedő (opcionális) Adagja: 0,2-1 (5-25 NE) ml/ttkg A VZIG-et 72 órán belül célszerű beadni. Tiz napon belül alkalmazva is mérsékli a kórkép súlyosságát. Átvészeltség esetén, ill. a betegség jelentkezésekor a VZIG alkalmazása már fölösleges.
7 7 3/B Oltás (aktiv immunizálás) 72 órán -legföljebb öt napon- belül ellenjavallat hiányában az élő, attenuált virust tartalmazó vakcinával védettség érhető el. Amennyiben az oltott személy egy oltás után a fertőzést nem aquirálta, 4-6 héttel az első dózis után, 2. oltás szükséges. Az immunizáció után 7-10 nappal ( maximum 21 nappal) varicellára emlékeztető kiütés jelentkezhet, ez az oltási betegség tünete. Amennyiben ez immunszupprimált egyénben fordul elő, az illetőt antivirális kezelésben kell részesíteni. Az oltás után 1 héten belül észlelt kiütés vad virus, azaz VZV fertőzés következménye. 4. Profilaxis és antivirális kezelés az egyes fogékony betegpopulációkban Immunkompetens, nem terhes egyén (egyhónaposnál idősebbek)* Posztexpoziciós prophylaxis: a VZIG alkalmazása fölösleges. Az egyévesnél idősebbek posztexpoziciós vakcinációja elfogadott. Terápia: órán belül -rizikócsoportba nem tartozó egyén: antivirális kezelést nem igényel (11 év fölött opcionális-, családi kontaktus esetén javasolt az ACV terápia.) -rizikócsoportba tartozó egyén: orális ACV kezelés 48 órán túl az orális terápia nem jön szóba. Terhes* A terhesség előrehaladtával nő a pneumonitis kockázata. A terhes bárányhimlője az első trimeszterben a fetalis varicella szindrómát okozhatja. Ez a varicellás terhes anyák magzatainak kevesebb, mint 2 %-ában fordul elő. A terhesség megszakítása az első trimeszterben varicella fertőzés miatt nem indokolt. A kórisme a magzat ultrahangvizsgálatával állapítható meg (III szintű evidencia). A magzatvíz vírus DNS irányú vizsgálata fölösleges. A magzati elhalás kockázatát a terhes varicellája nem növeli (IIb szintű evidencia). Posztexpoziciós profilaxis: VZIG a terhesség bármelyik szakaszában (III szintű evidencia). A foetalis varicella szindróma kialakulására vonatkozó effektusa nem ismert. Az aktiv immunizáció tilos. Terápia Az ACV embriopatogén hatására semmiféle adat nem utal. Azonban a 20. terhességi
8 8 hét előtt csak a terhes megfelelő tájékoztatását követően szabad alkalmazni (IV szintű evidencia). Erős dohányos terhesnek, továbbá annak, akin igen sok (> 100) kiütés jelentkezik, fokozottan javasolható. A 20. terhességi hét után a/ órán belül: per os ACV egy hétig b/ 48 órán túl: ACV iv. Újszülött* A. A születés előtt 5 napon belül, ill. azt követően 2 napon belül jelentkező anyai megbetegedés esetén nagy a kockázata az újszülött progressziv varicellájának (III szintű evidencia). Kielégitő anyai IgG szintre biztosan csak az anya betegségének ötödik napjától lehet számitani. A bárányhimlős gyermekágyas szoptatását nincs értelme megtiltani. magas kockázatú újszülött ( nap ): VZIG profilaxis szükséges; megbetegedés esetén ACV iv. nem magas kockázatú újszülött: súlyosabb kórlefolyás esetén az ACV terápia egyedi elbírálást igényel B. Egyhetes koráig minden fogékony anya (releváns kórelőzmény/pozitiv szerostátusz hiányában) újszülöttje szignifikáns expozíció esetén VZIG profilaxisban kell részesüljön,. C. Újszülöttosztályon: a fogékony anyák újszülöttjei, továbbá minden éretlen újszülött (<30. terhességi hét és/vagy <1 kg születési súly) VZIG profilaxisban kell részesüljön szignifikáns expozíció esetén. D. Súlyos alapbetegségben szenvedő, speciális ellátást igénylő csecsemők szignifikáns expozíció esetén specifikus ellenanyag hiányában VZIG profilaxisban kell részesüljenek. Immunszupprimált egyén* Ide tartoznak a veleszületett vagy szerzett immunhiány-betegségben szenvedők és az immunszuppressziv kezelés alatt álló betegek (Kivéve az izolált antitest hiány szindrómát, mely esetben a varicella normális lefolyású). Az egy hónapon belül alkalmazott szisztémás kortikoszteroid terápia (2 mg/ttkg-ot meghaladó adagban) immunkopromittált állapotot jelent varicella vonatkozásában. Nem jelent viszont veszélyt az inhalációs szteroidok használata és a másodnaponta alkalmazott steroidkezelés. Posztexpoziciós profilaxis: kötelező; ilyen helyzetben a VZIG-nek nincs ellenjavallata. Celluláris immundefektus az oltást ellenjavallja. Humorális immundefektusban elfogadott
9 9 az aktiv immunizálás. A három hónapon belül alkalmazott citosztatikus kezelés és az egy hónapon belül naponta, fenti adagban adott steroidterápia esetén nem szabad aktíve immunizálni. Tünetmentes HIV fertőzött vagy fertőzésük CDC szerinti A1 vagy N1 stádiumában lévő gyermekek megkaphatják az oltást, ha CD4+ limfocita szubpopulációjuk száma a korcsoportuknak megfelelő érték 25 %-át eléri. Terápia: atipusos erupciókkal járó / progressziv kórkép: ACV iv. normális kórlefolyás: órán belül kórházi megfigyelés mellett az orális ACV kezelés megkisérelhető Kórházban megbetegedett egyének (fogékony) kontaktjai* Alapbetegségüktől függően VZIG, ill. oltás egyaránt választható. *Virus-mediálta szövődmény esetén intravénás ACV kezelés kötelező. VI. Melléklet 1. Érintett társszakmák: elsősorban a gyermekgyógyászat, a belgyógyászat, a családorvoslás és a szülészet-nőgyógyászat. 2. Internetes oldalak: aafp.org; neli.org.uk; guideline.gov; aap.org; rcog.org.uk; cdc.gov; ctfphc.org; cd.gov/nip; dh.gov.uk; hpa.org.uk; prodigy.nhs.uk 3. Irodalomjegyzék 1. American Academy of Pediatrics. Committee on Infectious Diseases: Recommendations for the Use of Live Attenuated Varicella Vaccine. Pediatrics 1995;95; American Academy of Pediatrics. Committee on Infectious Diseases: Varicella Vaccine Update. Pediatrics Vol.105. No 1. January British National Formulary Vol49, March Published by the British Medical Association and the Royal Pharmaceutical Society of Great Britain. 4. HPA (2003) Guidelines on the management of communicable disease in schools and nurseries: chickenpox. Health Protection Agency. [Accessed: ]. 5. HPA (2004a) Chickenpox - varicella zoster. Health Protection Agency. [Accessed: ].
10 10 6. HPA (2004b) Immunoglobulin handbook: indications and dosage for normal and specific immunoglobulin preparations issued by the HPA. Health Protection Agency. [Accessed: ]. 7. Klassen, T.P., Belseck, E.M., Wiebe, N., and Hartling, L. (2004) Acyclovir for treating varicella in otherwise healthy children and adolescents (Cochrane Review). The Cochrane Library (Issue 2). Chichester, UK: John Wiley & Sons, Ltd. 8. K. L. Margo, A. F. Shaughnessy,: Antiviral Drugs in Healthy Children. Am Fam Phys Vol 57/No5 (March 1, 1998) 9. Morgan-Capner, P. and Crowcroft, N. (2000) Guidance on the management of, and exposure to, rash illness in pregnancy (including consideration of relevant antibody screening programmes in pregnancy). Report of a PHLS Working Group. Health Prorection Agency. [Accessed: ]. 10. Nathwani, D., Maclean, A., Conway, S., and Carrington, D. (1998) Varicella infections in pregnancy and the newborn: a review prepared for the UK Advisory Group on chickenpox on behalf of the British Society for the Study of Infection. Journal of Infection 36(Suppl 14), Nelson Textbook of Pediatrics. 17th ed. Edited by Behrman RE, Kliegman RM, Jenson HB. Saunders, Elsevier Science. 12. RCOG (2001) Chickenpox in pregnancy. Royal College of Obstetricians & Gynaecologists. [Accessed: ]. 13. Varicella vaccination: Recommendation statement from the Canadian Task Force on Preventive Health Care. CMAJ 2001;164(13): PRODIGY Guidance Cohen & Powderly: Infectious Diseases, 2nd ed., 2004 Mosby 14. Epidemiology and Prevention of Vaccine-Preventable Diseases. The Pink Book. Course Textbook. Updated 8th Edition 2nd Printing (January 2005 ) 15. B. Watson.Humoral and Cell-Mediated Immune Responses in Children and Adults after 1 and 2 Doses of VaricellaVaccine. JID 2008:197 (Suppl 2) S B.Kuter,H.Matthews,H.Shinefield. Ten year follow-up of healthy children who received one or two injections of varicella vaccine. Pediatr Infect Dis J, 2004;23: S.S. Chaves, P.Gargiullo, J. X. Zhang, Loss of Vaccine-Induced Immunity to Varicella over Time N Engl J Med 356;11 march 15, 2007
11 A. Arvin, A. Gershon: Control of Varicella: Why Is a Two-Dose Schedule Necessary? Pediatr Infect Dis J. June 2006Vol:25, No; A. Arvin: Humoral and Cellular Immunity to Varicella-Zoster Virus: An Overview JID 2008: 197 (Suppl). S B. Kuter, F. Schodel F. Second varicella vaccine dose Pediatr Infect Dis J febr Vol:26,No; B.Watson:Humoral and Cell-Mediated Immune Responses in Children and Adults after 1 and 2 Doses of Varicella Vaccine JID2008:197 (Suppl 2) S American Academy of Pediatrics.Committee on Infectious Diseases.Clinical report Guidance for the Clinician in Rendering Pediatric Care Prevention of Varicella: Recommendations for Use of Varicella Vaccines in Children, Including a Recommendation for a Routine Two-Dose Varicella Immunization Schedule Prevention of Varicella Recommendations of the Advisory Committee on Immunization Practices (ACIP) June 22, 2007 / 56(RR04);1-40 Szerzők: Trethon András, Kulcsár Andrea, Mészner Zsófia Az irányelvet összeállítók kinyilvánítják, hogy semmilyen szponzor nem támogatta az irányelv kialakítását, munkájukat külső támogatástól függetlenül végezték.
Irányelv. Szakmai protokoll a varicella kezeléséhez
 Irányelv Szakmai protokoll a varicella kezeléséhez készítette: az Infektológiai Szakmai Kollégium I. Alapvető megfontolások 1. A protokoll érvényességi területe: minden ellátási szint. 2. A protokoll feltétel
Irányelv Szakmai protokoll a varicella kezeléséhez készítette: az Infektológiai Szakmai Kollégium I. Alapvető megfontolások 1. A protokoll érvényességi területe: minden ellátási szint. 2. A protokoll feltétel
Az Egészségügyi Minisztérium szakmai irányelve. A varicella kezelésérõl és megelõzésérõl (1. módosított változat) I. Alapvetõ megfontolások
 21. szám EGÉSZSÉGÜGYI KÖZLÖNY 3119 Az Egészségügyi Minisztérium szakmai irányelve A varicella kezelésérõl és megelõzésérõl (1. módosított változat) Készítette: az Infektológiai Szakmai Kollégium I. Alapvetõ
21. szám EGÉSZSÉGÜGYI KÖZLÖNY 3119 Az Egészségügyi Minisztérium szakmai irányelve A varicella kezelésérõl és megelõzésérõl (1. módosított változat) Készítette: az Infektológiai Szakmai Kollégium I. Alapvetõ
SZAKMAI PROTOKOLL A VARICELLA KEZELÉSÉHEZ ÉS MEGELÕZÉSÉHEZ
 SZAKMAI PROTOKOLL A VARICELLA KEZELÉSÉHEZ ÉS MEGELÕZÉSÉHEZ Infektológiai Szakmai Kollégium Az irányelv érvényessége A kihirdetéstõl számított 3 év, amennyiben a témakörrel kapcsolatosan a jelen irányelv
SZAKMAI PROTOKOLL A VARICELLA KEZELÉSÉHEZ ÉS MEGELÕZÉSÉHEZ Infektológiai Szakmai Kollégium Az irányelv érvényessége A kihirdetéstõl számított 3 év, amennyiben a témakörrel kapcsolatosan a jelen irányelv
Útmutató a varicella kezeléséhez
 ÚJ Útmutató a varicella kezeléséhez Szerkesztõségi irányelv Bevezetés A bárányhimlõ az esetek többségében a klinikai kép alapján kórismézhetõ, nagy contagiositasú, kizárólag humán herpeszvírus okozta fertõzés.
ÚJ Útmutató a varicella kezeléséhez Szerkesztõségi irányelv Bevezetés A bárányhimlõ az esetek többségében a klinikai kép alapján kórismézhetõ, nagy contagiositasú, kizárólag humán herpeszvírus okozta fertõzés.
Ismerni életmentô, oltani ajánlott!
 Ismerni életmentô, oltani ajánlott! Széleskörû védelem a meningococcus betegség ellen Már 2 hónapos kortól Minden korosztálynak. A meningococcus baktérium leggyakoribb, betegséget okozó típusai ellen.
Ismerni életmentô, oltani ajánlott! Széleskörû védelem a meningococcus betegség ellen Már 2 hónapos kortól Minden korosztálynak. A meningococcus baktérium leggyakoribb, betegséget okozó típusai ellen.
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Tetanol pur betegtájékoztató - PIL alapján.doc BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Tetanol pur betegtájékoztató - PIL alapján.doc BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
A Varilrix megfelel az Egészségügyi Világszervezet (WHO) biológiai anyagokra és a varicella vakcinákra előírt követelményeinek.
 1. A GYÓGYSZER NEVE Varilrix por és oldószer oldatos injekcióhoz Élő, attenuált varicella-zoster vírus (OKA törzs) vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A Varilrix a varicella-zoster vírus élő,
1. A GYÓGYSZER NEVE Varilrix por és oldószer oldatos injekcióhoz Élő, attenuált varicella-zoster vírus (OKA törzs) vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A Varilrix a varicella-zoster vírus élő,
40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban).
 1. A GYÓGYSZER NEVE Zovirax 40 mg/ml belsőleges szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban). Ismert hatású segédanyagok:
1. A GYÓGYSZER NEVE Zovirax 40 mg/ml belsőleges szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban). Ismert hatású segédanyagok:
A Havrix megfelel az Egészségügyi Világszervezet (WHO) biológiai anyagokra előírt követelményeinek.
 1. A GYÓGYSZER MEGNEVEZÉSE Havrix 1440 Elisa Egység szuszpenziós injekció előretöltött fecskendőben Havrix 720 Elisa Egység Junior szuszpenziós injekció előretöltött fecskendőben Hepatitis A vakcina antigén
1. A GYÓGYSZER MEGNEVEZÉSE Havrix 1440 Elisa Egység szuszpenziós injekció előretöltött fecskendőben Havrix 720 Elisa Egység Junior szuszpenziós injekció előretöltött fecskendőben Hepatitis A vakcina antigén
Szelektív és univerzális oltási stratégiák
 A közösségi immunitás paradoxonai avagy amikor a vakcináció többet árt(hat) mint használ Ferenci Tamás vedooltas@medstat.hu http://vedooltas.blog.hu 2015. március 19. Tartalom 1 Általános megfontolások
A közösségi immunitás paradoxonai avagy amikor a vakcináció többet árt(hat) mint használ Ferenci Tamás vedooltas@medstat.hu http://vedooltas.blog.hu 2015. március 19. Tartalom 1 Általános megfontolások
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 1 adag (1 ml) tartalma: Hepatitisz B felszíni antigén 1,2. 20 mikrogramm
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
Légzőszervi megbetegedések
 Orrmelléküreg-gyulladás (sinusitis) Légzőszervi megbetegedések Az orr melléküregeinek gyulladása, melyet leggyakrabban baktériumok okoznak. Orrnyálkahártya-gyulladás (rhinitis) Különböző típusú gyulladások
Orrmelléküreg-gyulladás (sinusitis) Légzőszervi megbetegedések Az orr melléküregeinek gyulladása, melyet leggyakrabban baktériumok okoznak. Orrnyálkahártya-gyulladás (rhinitis) Különböző típusú gyulladások
A Mencevax ACWY megfelel a WHO biológiai készítményekre és a meningococcus meningitis vakcinákra vonatkozó előírásainak.
 1. A GYÓGYSZERKÉSZÍTMÉNY MEGNEVEZÉSE MENCEVAX ACWY135 Y egy adagos vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Összetétel dózisonként: Neisseria meningitidis poliszacharid A típusú, tisztított 50,0 μg
1. A GYÓGYSZERKÉSZÍTMÉNY MEGNEVEZÉSE MENCEVAX ACWY135 Y egy adagos vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Összetétel dózisonként: Neisseria meningitidis poliszacharid A típusú, tisztított 50,0 μg
Priorix por és oldószer oldatos injekcióhoz előretöltött fecskendőben Kanyaró, mumpsz és rubeola vakcina (élő)
 1. A GYÓGYSZER NEVE Priorix por és oldószer oldatos injekcióhoz előretöltött fecskendőben Kanyaró, mumpsz és rubeola vakcina (élő) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Feloldást követően 1 adag (0,5 ml)
1. A GYÓGYSZER NEVE Priorix por és oldószer oldatos injekcióhoz előretöltött fecskendőben Kanyaró, mumpsz és rubeola vakcina (élő) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Feloldást követően 1 adag (0,5 ml)
A Boostrix Polio diphtheria, tetanus, pertussis és poliomyelitis elleni emlékeztető oltásra javasolt 4 éves kortól (lásd 4.2 pont).
 1. A GYÓGYSZER NEVE Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett
1. A GYÓGYSZER NEVE Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
Egy immunizáló dózis (0,5 ml) 1,5 μg inaktivált kullancsencephalitis-vírust (törzs K23; csirkeembrio fibroblast sejtkultúrán tenyésztett) tartalmaz.
 1. A GYÓGYSZER NEVE ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy immunizáló dózis (0,5 ml) 1,5 μg inaktivált
1. A GYÓGYSZER NEVE ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy immunizáló dózis (0,5 ml) 1,5 μg inaktivált
Betegtájékoztató: Információk a felhasználó számára. Zovirax 40 mg/ml belsőleges szuszpenzió aciklovir
 Betegtájékoztató: Információk a felhasználó számára Zovirax 40 mg/ml belsőleges szuszpenzió aciklovir Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert
Betegtájékoztató: Információk a felhasználó számára Zovirax 40 mg/ml belsőleges szuszpenzió aciklovir Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert
Betegtájékoztató: Információk a felhasználó számára. Rabipur por és oldószer oldatos injekcióhoz Inaktivált veszettség elleni vakcina
 Betegtájékoztató: Információk a felhasználó számára Rabipur por és oldószer oldatos injekcióhoz Inaktivált veszettség elleni vakcina Mielőtt beadnák Önnek vagy gyermekének a Rabipur-t, olvassa el figyelmesen
Betegtájékoztató: Információk a felhasználó számára Rabipur por és oldószer oldatos injekcióhoz Inaktivált veszettség elleni vakcina Mielőtt beadnák Önnek vagy gyermekének a Rabipur-t, olvassa el figyelmesen
22. évfolyam 8. szám 2015. február 27. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 22. évfolyam 8. szám 2015. február 27. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Kanyarójárvány az Egyesült Államokban, 2014-2015 77 Tájékoztatás engedélyezett fertőtlenítőszerekről 83 Fertőző betegségek
22. évfolyam 8. szám 2015. február 27. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Kanyarójárvány az Egyesült Államokban, 2014-2015 77 Tájékoztatás engedélyezett fertőtlenítőszerekről 83 Fertőző betegségek
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Mixtard 30 40 nemzetközi egység/ml szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 injekciós üveg 10 ml-t tartalmaz, ami 400 NE-gel egyenértékű.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Mixtard 30 40 nemzetközi egység/ml szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 injekciós üveg 10 ml-t tartalmaz, ami 400 NE-gel egyenértékű.
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK AZ OLTANDÓK SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK AZ OLTANDÓK SZÁMÁRA Tetanol pur szuszpenziós injekció előretöltött fecskendőben adszorbeált tetanusz toxoid vakcina, tartósítószer nélkül Mielőtt beadnák Önnek ezt a vakcinát,
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK AZ OLTANDÓK SZÁMÁRA Tetanol pur szuszpenziós injekció előretöltött fecskendőben adszorbeált tetanusz toxoid vakcina, tartósítószer nélkül Mielőtt beadnák Önnek ezt a vakcinát,
Más gyógyszerekhez hasonlóan, a homeopátiás gyógyszerek sem szedhetők hosszabb ideig orvosi felügyelet nélkül (lásd 4.4 pont).
 1. A GYÓGYSZER NEVE Mastodynon belsőleges oldatos cseppek Homeopátiás gyógyszer 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 g oldat hatóanyag tartalma: Vitex agnus castus (Agnus castus) D1 20,0 g Iris versicolor
1. A GYÓGYSZER NEVE Mastodynon belsőleges oldatos cseppek Homeopátiás gyógyszer 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 g oldat hatóanyag tartalma: Vitex agnus castus (Agnus castus) D1 20,0 g Iris versicolor
HUNGARIAN Immunisation for babies just after their first birthday. Védőoltások. Csecsemőknek közvetlenül első születésnapjuk után
 HUNGARIAN Immunisation for babies just after their first birthday Védőoltások Csecsemőknek közvetlenül első születésnapjuk után Bevezető Ez a tájékoztató a gyermekének közvetlenül az első születésnapja
HUNGARIAN Immunisation for babies just after their first birthday Védőoltások Csecsemőknek közvetlenül első születésnapjuk után Bevezető Ez a tájékoztató a gyermekének közvetlenül az első születésnapja
Betegtájékoztató: Információk a felhasználó számára. nasic pur 0,5 mg/ml + 50 mg/ml oldatos orrspray kisgyermekeknek
 Betegtájékoztató: Információk a felhasználó számára nasic pur 0,5 mg/ml + 50 mg/ml oldatos orrspray kisgyermekeknek xilometazolin-hidroklorid és dexpantenol Mielőtt elkezdi alkalmazni ezt a gyógyszert,
Betegtájékoztató: Információk a felhasználó számára nasic pur 0,5 mg/ml + 50 mg/ml oldatos orrspray kisgyermekeknek xilometazolin-hidroklorid és dexpantenol Mielőtt elkezdi alkalmazni ezt a gyógyszert,
Flexove 625 mg Tabletta Szájon át történő alkalmazás 1327 Lysaker, Norvégia Belgium - Navamedic ASA Vollsveien 13 C 1327 Lysaker, Norvégia
 I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN 1 Tagállam Forgalomba hozatali engedély
I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN 1 Tagállam Forgalomba hozatali engedély
Convenia 80 mg/ml por és oldószer injekciós oldathoz kutya és macska számára
 . AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Convenia 0 mg/ml por és oldószer injekciós oldathoz kutya és macska számára. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy ampulla liofilizált por tartalma: Hatóanyag: 5 mg
. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Convenia 0 mg/ml por és oldószer injekciós oldathoz kutya és macska számára. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy ampulla liofilizált por tartalma: Hatóanyag: 5 mg
alumínium-hidroxidhoz adszorbeálva 0,3-0,4 mg Al 3+
 1. A GYÓGYSZER NEVE Menjugate 10 mikrogramm por és oldószer szuszpenziós injekcióhoz C-csoportú meningococcus konjugált vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml,előkészített) vakcina
1. A GYÓGYSZER NEVE Menjugate 10 mikrogramm por és oldószer szuszpenziós injekcióhoz C-csoportú meningococcus konjugált vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml,előkészített) vakcina
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE VPRIV 200 egység por oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy injekciós üveg 200 egység* velagluceráz-alfát tartalmaz.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE VPRIV 200 egység por oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy injekciós üveg 200 egység* velagluceráz-alfát tartalmaz.
www.printo.it/pediatric-rheumatology/hu/intro
 www.printo.it/pediatric-rheumatology/hu/intro Behcet-kór Verzió 2016 1. MI A BEHCET-KÓR 1.1 Mi ez? A Behçet-szindróma vagy Behçet-kór (BD) egy szisztémás vaszkulitisz (az egész testre kiterjedő érgyulladás),
www.printo.it/pediatric-rheumatology/hu/intro Behcet-kór Verzió 2016 1. MI A BEHCET-KÓR 1.1 Mi ez? A Behçet-szindróma vagy Behçet-kór (BD) egy szisztémás vaszkulitisz (az egész testre kiterjedő érgyulladás),
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1. A GYÓGYSZER NEVE Synagis 50 mg por és oldószer oldatos injekcióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 50 mg palivizumab* injekciós üvegenként, a javasolt módon történő
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1. A GYÓGYSZER NEVE Synagis 50 mg por és oldószer oldatos injekcióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 50 mg palivizumab* injekciós üvegenként, a javasolt módon történő
Az oldat tartalma milliliterenként: humán plazmaprotein... 200 mg (legalább 98%-os tisztaságú IgG)
 1. A GYÓGYSZER MEGNEVEZÉSE Hizentra 200 mg/ml oldatos injekció bőr alá történő beadásra 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán normál immunglobulin (SCIg). Az oldat tartalma milliliterenként: humán
1. A GYÓGYSZER MEGNEVEZÉSE Hizentra 200 mg/ml oldatos injekció bőr alá történő beadásra 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán normál immunglobulin (SCIg). Az oldat tartalma milliliterenként: humán
14. évfolyam 14. szám 2007. április 13. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 14. évfolyam 14. szám 2007. április 13. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Szerbiai kanyarójárvány 125 Mumpsz járvány Bulgáriában, 2007-ben 127 Fertőző betegségek adatai 128 Epidemiológiai Információs
14. évfolyam 14. szám 2007. április 13. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Szerbiai kanyarójárvány 125 Mumpsz járvány Bulgáriában, 2007-ben 127 Fertőző betegségek adatai 128 Epidemiológiai Információs
1. Milyen típusú gyógyszer az FSME-IMMUN 0,5 ml felnotteknek vakcina és milyen célra alkalmazható?
 Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! 4. sz. melléklete az OGYI-T-20063/01-02 Forgalomba hozatali engedélynek Budapest, 2006.február 23. Szám: 19340/41/05
Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! 4. sz. melléklete az OGYI-T-20063/01-02 Forgalomba hozatali engedélynek Budapest, 2006.február 23. Szám: 19340/41/05
Betegtájékoztató METFOGAMMA 850 MG FILMTABLETTA. Metfogamma 850 mg filmtabletta metformin-hidroklorid
 METFOGAMMA 850 MG FILMTABLETTA Metfogamma 850 mg filmtabletta metformin-hidroklorid HATÓANYAG: Metformin-hidroklorid. 850 mg metformin-hidroklorid filmtablettánként. SEGÉDANYAG: Hipromellóz, polividon,
METFOGAMMA 850 MG FILMTABLETTA Metfogamma 850 mg filmtabletta metformin-hidroklorid HATÓANYAG: Metformin-hidroklorid. 850 mg metformin-hidroklorid filmtablettánként. SEGÉDANYAG: Hipromellóz, polividon,
Vírusok Szerk.: Vizkievicz András
 Vírusok Szerk.: Vizkievicz András A vírusok az élő- és az élettelen világ határán állnak. Önmagukban semmilyen életjelenséget nem mutatnak, nincs anyagcseréjük, önálló szaporodásra képtelenek. Paraziták.
Vírusok Szerk.: Vizkievicz András A vírusok az élő- és az élettelen világ határán állnak. Önmagukban semmilyen életjelenséget nem mutatnak, nincs anyagcseréjük, önálló szaporodásra képtelenek. Paraziták.
Epinfo Epidemiológiai Információs Hetilap
 7. évfolyam 9. szám 00. július 30. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Epidemiológiai Információs Hetilap NEMZETKÖZI INFORMÁCIÓ KÉRDÉSEK ÉS VÁLASZOK A KANYARÓRÓL AZ EURÓPÁBAN ZAJLÓ KANYARÓJÁRVÁNY KAPCSÁN
7. évfolyam 9. szám 00. július 30. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Epidemiológiai Információs Hetilap NEMZETKÖZI INFORMÁCIÓ KÉRDÉSEK ÉS VÁLASZOK A KANYARÓRÓL AZ EURÓPÁBAN ZAJLÓ KANYARÓJÁRVÁNY KAPCSÁN
Irányelv A heveny tonsillopharyngitis antimikróbás kezeléséhez
 Irányelv A heveny tonsillopharyngitis antimikróbás kezeléséhez Szerkesztette: Mészner Zsófia, Ludwig Endre Készítette: Infektológiai, Gyermekgyógyászati és a Fül-Orr-Gégészeti Szakmai Kollégium Bevezetés
Irányelv A heveny tonsillopharyngitis antimikróbás kezeléséhez Szerkesztette: Mészner Zsófia, Ludwig Endre Készítette: Infektológiai, Gyermekgyógyászati és a Fül-Orr-Gégészeti Szakmai Kollégium Bevezetés
11. évfolyam 1. KÜLÖNSZÁM 2004. január 27. JOHAN BÉLA ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT. Epinfo A "JOHAN BÉLA" ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 11. évfolyam 1. KÜLÖNSZÁM 2004. január 27. JOHAN BÉLA ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epidemiológiai Információs Hetilap A "JOHAN BÉLA" ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT MÓDSZERTANI LEVELE A 2004. ÉVI VÉDŐOLTÁSOKRÓL
11. évfolyam 1. KÜLÖNSZÁM 2004. január 27. JOHAN BÉLA ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epidemiológiai Információs Hetilap A "JOHAN BÉLA" ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT MÓDSZERTANI LEVELE A 2004. ÉVI VÉDŐOLTÁSOKRÓL
A szervezet immunválasza a vérátömlesztésre
 A szervezet immunválasza a vérátömlesztésre Prohászka Zoltán III. Sz. Belgyógyászati Klinika, Kutatólaboratórium Semmelweis Egyetem, Budapest prohoz@kut.sote.hu Transzfúziós Tanfolyam Szigorló Orvostanhallgatóknak
A szervezet immunválasza a vérátömlesztésre Prohászka Zoltán III. Sz. Belgyógyászati Klinika, Kutatólaboratórium Semmelweis Egyetem, Budapest prohoz@kut.sote.hu Transzfúziós Tanfolyam Szigorló Orvostanhallgatóknak
Betegtájékoztató ALPRESTIL 20 MIKROGRAMM/ML KONCENTRÁTUM OLDATOS INFÚZIÓHOZ. Alprestil 20 mikrogramm/ml koncentrátum oldatos infúzióhoz alprosztadil
 ALPRESTIL 20 MIKROGRAMM/ML KONCENTRÁTUM OLDATOS INFÚZIÓHOZ Alprestil 20 mikrogramm/ml koncentrátum oldatos infúzióhoz alprosztadil HATÓANYAG: Alprosztadil. SEGÉDANYAG: Vízmentes etanol. JAVALLAT: Az Alprestil
ALPRESTIL 20 MIKROGRAMM/ML KONCENTRÁTUM OLDATOS INFÚZIÓHOZ Alprestil 20 mikrogramm/ml koncentrátum oldatos infúzióhoz alprosztadil HATÓANYAG: Alprosztadil. SEGÉDANYAG: Vízmentes etanol. JAVALLAT: Az Alprestil
Gyermekkori Spondilartritisz/Entezitisszel Összefüggő Artritisz (SPA-ERA)
 www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Spondilartritisz/Entezitisszel Összefüggő Artritisz (SPA-ERA) Verzió 2016 1. MI A GYERMEKKORI SPONDILARTRITISZ/ENTEZITISSZEL ÖSSZEFÜGGŐ ARTRITISZ
www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Spondilartritisz/Entezitisszel Összefüggő Artritisz (SPA-ERA) Verzió 2016 1. MI A GYERMEKKORI SPONDILARTRITISZ/ENTEZITISSZEL ÖSSZEFÜGGŐ ARTRITISZ
14. évfolyam 28. szám 2007. július 20. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 14. évfolyam 28. szám 2007. július 20. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo surveillance rendszere, 265 Fertőző betegségek adatai 273 Epidemiológiai Információs Hetilap HAZAI INFORMÁCIÓ NEMZETI NOSOCOMIALIS
14. évfolyam 28. szám 2007. július 20. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo surveillance rendszere, 265 Fertőző betegségek adatai 273 Epidemiológiai Információs Hetilap HAZAI INFORMÁCIÓ NEMZETI NOSOCOMIALIS
III. melléklet. Az alkalmazási előírás és a betegtájékoztató egyes fejezeteinek módosításai
 III. melléklet Az alkalmazási előírás és a betegtájékoztató egyes fejezeteinek módosításai 49 Metoklopramid-tartalmú termékek Az alábbi szövegrészek a megfelelő módon beillesztendők a forgalomba hozatali
III. melléklet Az alkalmazási előírás és a betegtájékoztató egyes fejezeteinek módosításai 49 Metoklopramid-tartalmú termékek Az alábbi szövegrészek a megfelelő módon beillesztendők a forgalomba hozatali
Kenőcs A kenőcs különösen alkalmas a száraz, lichenifikált és pikkelyesen hámló elváltozásokra.
 1. A GYÓGYSZER NEVE Dermovate krém 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg klobetazol-propionát 1 g 0,05%-os kenőcsben. Dermovate krém 0,5 mg klobetazol-propionát 1 g 0,05%-os krémben. A segédanyagok
1. A GYÓGYSZER NEVE Dermovate krém 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg klobetazol-propionát 1 g 0,05%-os kenőcsben. Dermovate krém 0,5 mg klobetazol-propionát 1 g 0,05%-os krémben. A segédanyagok
Betegtájékoztató: Információk a felhasználó számára. Dermovate kenőcs klobetazol-propionát
 Betegtájékoztató: Információk a felhasználó számára Dermovate kenőcs klobetazol-propionát Mielőtt elkezdené alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, amely az Ön
Betegtájékoztató: Információk a felhasználó számára Dermovate kenőcs klobetazol-propionát Mielőtt elkezdené alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, amely az Ön
Fehér kapszula, felső részén fekete OGT 918, alsó részén fekete 100 jelzéssel.
 1. A GYÓGYSZER MEGNEVEZÉSE Zavesca 100 mg kemény kapszula. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mg miglusztát kapszulánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Kemény
1. A GYÓGYSZER MEGNEVEZÉSE Zavesca 100 mg kemény kapszula. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mg miglusztát kapszulánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Kemény
Megelőzhető RSV fertőzés
 Megelőzhető RSV fertőzés Dr. Nobilis András SE. II. sz. Szülészeti és Nőgyógyászati Klinika Koraszülött Intenzív Osztály Előzmények Az RSV a leggyakoribb légúti kórokozó a kora és újszülöttek, kisgyermekek
Megelőzhető RSV fertőzés Dr. Nobilis András SE. II. sz. Szülészeti és Nőgyógyászati Klinika Koraszülött Intenzív Osztály Előzmények Az RSV a leggyakoribb légúti kórokozó a kora és újszülöttek, kisgyermekek
1. A GYÓGYSZER MEGNEVEZÉSE. Cutivate 0,5 mg/g krém 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
 1. A GYÓGYSZER MEGNEVEZÉSE Cutivate 0,5 mg/g krém 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg flutikazon-propionát (mikronizált) 1 gramm krémben. 7,5 mg flutikazon-propionát (mikronizált) 15 g krémben.
1. A GYÓGYSZER MEGNEVEZÉSE Cutivate 0,5 mg/g krém 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg flutikazon-propionát (mikronizált) 1 gramm krémben. 7,5 mg flutikazon-propionát (mikronizált) 15 g krémben.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1/33 1. A GYÓGYSZER MEGNEVEZÉSE Resolor 1 mg-os filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 mg prukaloprid filmtablettánként (prukaloprid-szukcinát formájában).
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1/33 1. A GYÓGYSZER MEGNEVEZÉSE Resolor 1 mg-os filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 mg prukaloprid filmtablettánként (prukaloprid-szukcinát formájában).
B. BETEGTÁJÉKOZTATÓ 1
 B. BETEGTÁJÉKOZTATÓ 1 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Pandemrix szuszpenzió és emulzió emulziós injekcióhoz Pandémiás influenza (H1N1) vakcina (split virion, inaktivált, adjuvánshoz
B. BETEGTÁJÉKOZTATÓ 1 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Pandemrix szuszpenzió és emulzió emulziós injekcióhoz Pandémiás influenza (H1N1) vakcina (split virion, inaktivált, adjuvánshoz
SEGÉDANYAG: Povidon K-25, magnézium-sztearát, karboxilmetil-keményítõ-nátrium, talkum, kukoricakeményítõ.
 ALGOPYRIN 500 MG TABLETTA Algopyrin 500 mg tabletta metamizol-nátrium HATÓANYAG: 500 mg metamizol-nátrium tablettánként. SEGÉDANYAG: Povidon K-25, magnézium-sztearát, karboxilmetil-keményítõ-nátrium, talkum,
ALGOPYRIN 500 MG TABLETTA Algopyrin 500 mg tabletta metamizol-nátrium HATÓANYAG: 500 mg metamizol-nátrium tablettánként. SEGÉDANYAG: Povidon K-25, magnézium-sztearát, karboxilmetil-keményítõ-nátrium, talkum,
Újabb adatok a H1N1 vírusról. Miért hívják H1N1-nekÍ?
 Újabb adatok a H1N1 vírusról Miért hívják H1N1-nekÍ? Az Influenza vírusnak három nagy csoportja van az A, B és C. típus- Ezek közül az A vírus a veszélyesebb és fordul elő gyakrabban emberekben is. A rezervoire
Újabb adatok a H1N1 vírusról Miért hívják H1N1-nekÍ? Az Influenza vírusnak három nagy csoportja van az A, B és C. típus- Ezek közül az A vírus a veszélyesebb és fordul elő gyakrabban emberekben is. A rezervoire
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
Influenza szezon 2010/2011: gyakran ismételt kérdések és válaszok 1. verzió 2010. szeptember 21.
 ÁNTSZ Országos Tisztifőorvosi Hivatal Országos Tiszti Főorvos 1097 Budapest, Gyáli út 2 6. 1437 Budapest, Pf. 839 Központ: (1) 476-1100 Telefon: (1) 476-1242 Telefax: (1) 215-4492 E-mail: tisztifoorvos@oth.antsz.hu
ÁNTSZ Országos Tisztifőorvosi Hivatal Országos Tiszti Főorvos 1097 Budapest, Gyáli út 2 6. 1437 Budapest, Pf. 839 Központ: (1) 476-1100 Telefon: (1) 476-1242 Telefax: (1) 215-4492 E-mail: tisztifoorvos@oth.antsz.hu
Betegtájékoztató PAMITOR 15 MG/ML KONCENTRÁTUM OLDATOS INFÚZIÓHOZ. Pamitor 15 mg / ml koncentrátum oldatos infúzióhoz dinátrium-pamidronát
 PAMITOR 15 MG/ML KONCENTRÁTUM OLDATOS INFÚZIÓHOZ Pamitor 15 mg / ml koncentrátum oldatos infúzióhoz dinátrium-pamidronát HATÓANYAG: Milliliterenként 15 mg dinátrium-pamidronát (ami megfelel 12,6 mg pamidronsavnak).
PAMITOR 15 MG/ML KONCENTRÁTUM OLDATOS INFÚZIÓHOZ Pamitor 15 mg / ml koncentrátum oldatos infúzióhoz dinátrium-pamidronát HATÓANYAG: Milliliterenként 15 mg dinátrium-pamidronát (ami megfelel 12,6 mg pamidronsavnak).
Az Advocate macskáknak 100 mg/ml imidaklopridot és 10 mg/ml moxidektint tartalmaz.
 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Advocate rácsepegtető oldat kistestű macskáknak és görényeknek Advocate rácsepegtető oldat nagytestű macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az Advocate macskáknak
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Advocate rácsepegtető oldat kistestű macskáknak és görényeknek Advocate rácsepegtető oldat nagytestű macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az Advocate macskáknak
Betegtájékoztató: Információk a felhasználó számára. Algoflex forte filmtabletta ibuprofén
 Betegtájékoztató: Információk a felhasználó számára Algoflex forte filmtabletta ibuprofén Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára
Betegtájékoztató: Információk a felhasználó számára Algoflex forte filmtabletta ibuprofén Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára
JAVALLAT: A Depakine 50 mg/ml szirup hatóanyaga a valproinsav, amit epilepszia kezelésére alkalmaznak.
 DEPAKINE 50 MG/ML SZIRUP Depakine 50 mg/ml szirup valproinsav HATÓANYAG: 50 mg valproinsavat tartalmaz milliliterenként (7,50 g valproinsav 150 ml szirupban). SEGÉDANYAG: Propil-parahidroxi-benzoát, cseresznye
DEPAKINE 50 MG/ML SZIRUP Depakine 50 mg/ml szirup valproinsav HATÓANYAG: 50 mg valproinsavat tartalmaz milliliterenként (7,50 g valproinsav 150 ml szirupban). SEGÉDANYAG: Propil-parahidroxi-benzoát, cseresznye
Betegtájékoztató: Információk a felhasználó számára. Wellbutrin SR 150 mg retard tabletta. bupropion-hidroklorid
 Betegtájékoztató: Információk a felhasználó számára Wellbutrin SR 150 mg retard tabletta bupropion-hidroklorid Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
Betegtájékoztató: Információk a felhasználó számára Wellbutrin SR 150 mg retard tabletta bupropion-hidroklorid Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Td-pur szuszpenziós injekció előretöltött fecskendőben tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 éven felüliek számára Mielőtt beadják
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Td-pur szuszpenziós injekció előretöltött fecskendőben tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 éven felüliek számára Mielőtt beadják
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Fortum 1 g por oldatos injekcióhoz vagy infúzióhoz Fortum 2 g por oldatos injekcióhoz vagy infúzióhoz ceftazidim Mielőtt elkezdi alkalmazni ezt a gyógyszert,
Betegtájékoztató: Információk a felhasználó számára Fortum 1 g por oldatos injekcióhoz vagy infúzióhoz Fortum 2 g por oldatos injekcióhoz vagy infúzióhoz ceftazidim Mielőtt elkezdi alkalmazni ezt a gyógyszert,
17. évfolyam 7. szám 2010. február 26. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 7. évfolyam 7. szám 00. február 6. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Anyatej útján közvetített sárgaláz megbetegedés Brazíliában 8 Tájékoztatás szakmai rendezvényről 8 Szerkesztőségi tájékoztatás
7. évfolyam 7. szám 00. február 6. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Anyatej útján közvetített sárgaláz megbetegedés Brazíliában 8 Tájékoztatás szakmai rendezvényről 8 Szerkesztőségi tájékoztatás
SEGÉDANYAG: Magnézium-sztearát (Ph.Eur.), povidon K25, hipromellóz, makrogol 6000, titán-dioxid (E 171).
 MEFORAL 850 MG FILMTABLETTA Meforal 850 mg filmtabletta metformin-hidroklorid 10 év feletti gyermekek és felnõttek részére HATÓANYAG: 850 mg metformin-hidroklorid (megfelel 662,9 mg metforminnak) filmtablettánként.
MEFORAL 850 MG FILMTABLETTA Meforal 850 mg filmtabletta metformin-hidroklorid 10 év feletti gyermekek és felnõttek részére HATÓANYAG: 850 mg metformin-hidroklorid (megfelel 662,9 mg metforminnak) filmtablettánként.
1. MILYEN TÍPUSÚ GYÓGYSZER A PIRACETAM AL 800 FILMTABLETTA ÉS MILYEN BETEGSÉGEK ESETÉN ALKALMAZHATÓ?
 PIRACETAM AL 800 MG FILMTABLETTA Piracetam AL 800 filmtabletta Hatóanyag: 800 mg piracetám filmtablettánként. Segédanyagok: kolloid szilícium-dioxid, magnézium-sztearát, kroszkarmellóz-nátrium, povidon,
PIRACETAM AL 800 MG FILMTABLETTA Piracetam AL 800 filmtabletta Hatóanyag: 800 mg piracetám filmtablettánként. Segédanyagok: kolloid szilícium-dioxid, magnézium-sztearát, kroszkarmellóz-nátrium, povidon,
B. BETEGTÁJÉKOZTATÓ 1
 B. BETEGTÁJÉKOZTATÓ 1 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Arepanrix szuszpenzió és emulzió emulziós injekcióhoz Pandémiás influenza (H1N1) vakcina (split virion, inaktivált, adjuvánshoz
B. BETEGTÁJÉKOZTATÓ 1 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Arepanrix szuszpenzió és emulzió emulziós injekcióhoz Pandémiás influenza (H1N1) vakcina (split virion, inaktivált, adjuvánshoz
Betegtájékoztató: Információk a felhasználó számára. Imigran oldatos injekció+autoinjektor szumatriptán
 Betegtájékoztató: Információk a felhasználó számára Imigran oldatos injekció+autoinjektor szumatriptán Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert
Betegtájékoztató: Információk a felhasználó számára Imigran oldatos injekció+autoinjektor szumatriptán Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY MEGNEVEZÉSE MASIVET 50 mg-os filmbevonatú tabletta kutyák számára MASIVET 150 mg-os filmbevonatú tabletta kutyák
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY MEGNEVEZÉSE MASIVET 50 mg-os filmbevonatú tabletta kutyák számára MASIVET 150 mg-os filmbevonatú tabletta kutyák
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
 1. A GYÓGYSZER NEVE Metilprednizolon-Teva 40 mg por oldatos injekcióhoz Metilprednizolon-Teva 125 mg por oldatos injekcióhoz Metilprednizolon-Teva 500 mg por oldatos injekcióhoz Metilprednizolon-Teva 1000
1. A GYÓGYSZER NEVE Metilprednizolon-Teva 40 mg por oldatos injekcióhoz Metilprednizolon-Teva 125 mg por oldatos injekcióhoz Metilprednizolon-Teva 500 mg por oldatos injekcióhoz Metilprednizolon-Teva 1000
HÚGYÚTI FERTÕZÉSEK. I. Alapvetõ megfontolások 1.1. DEFINÍCIÓ ÉS KOMPETENCIASZINTEK. EüM
 HÚGYÚTI FERTÕZÉSEK EüM Csecsemõ- és Gyermekgyógyászati Szakmai Kollégium Szerzõk: dr. Reusz György, dr. Tory Kálmán Az Egészségügyi Minisztérium szakmai protokollja I. Alapvetõ megfontolások 1.1. DEFINÍCIÓ
HÚGYÚTI FERTÕZÉSEK EüM Csecsemõ- és Gyermekgyógyászati Szakmai Kollégium Szerzõk: dr. Reusz György, dr. Tory Kálmán Az Egészségügyi Minisztérium szakmai protokollja I. Alapvetõ megfontolások 1.1. DEFINÍCIÓ
Betegtájékoztató CODOXY 10 MG RETARD TABLETTA
 CODOXY 10 MG RETARD TABLETTA Codoxy 5 mg retard tabletta Codoxy 10 mg retard tabletta Codoxy 20 mg retard tabletta Codoxy 40 mg retard tabletta Codoxy 80 mg retard tabletta oxikodon-hidroklorid HATÓANYAG:
CODOXY 10 MG RETARD TABLETTA Codoxy 5 mg retard tabletta Codoxy 10 mg retard tabletta Codoxy 20 mg retard tabletta Codoxy 40 mg retard tabletta Codoxy 80 mg retard tabletta oxikodon-hidroklorid HATÓANYAG:
Betegtájékoztató: Információk a felhasználó számára. Imigran 50 mg tabletta Imigran 100 mg tabletta szumatriptán
 Betegtájékoztató: Információk a felhasználó számára Imigran 50 mg tabletta Imigran 100 mg tabletta szumatriptán Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
Betegtájékoztató: Információk a felhasználó számára Imigran 50 mg tabletta Imigran 100 mg tabletta szumatriptán Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
20. évfolyam 1. KÜLÖNSZÁM 2013. február 12. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT. Epinfo AZ ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT MÓDSZERTANI LEVELE
 20. évfolyam 1. KÜLÖNSZÁM 2013. február 12. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT E p i d e m i o l ó g i a i I n f o r m á c i ó s H e t i l a p AZ ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT MÓDSZERTANI LEVELE A 2013.
20. évfolyam 1. KÜLÖNSZÁM 2013. február 12. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT E p i d e m i o l ó g i a i I n f o r m á c i ó s H e t i l a p AZ ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT MÓDSZERTANI LEVELE A 2013.
Betegtájékoztató DEPAKINE CHRONO 300 MG FILMTABLETTA
 DEPAKINE CHRONO 300 MG FILMTABLETTA Depakine Chrono 300 mg filmtabletta Depakine Chrono 500 mg filmtabletta nátrium-valproát, valproinsav HATÓANYAG: Nátrium-valproát és valproinsav. SEGÉDANYAG: Depakine
DEPAKINE CHRONO 300 MG FILMTABLETTA Depakine Chrono 300 mg filmtabletta Depakine Chrono 500 mg filmtabletta nátrium-valproát, valproinsav HATÓANYAG: Nátrium-valproát és valproinsav. SEGÉDANYAG: Depakine
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Prevenar 13 szuszpenziós injekció Pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Prevenar 13 szuszpenziós injekció Pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy
BETEGTÁJÉKOZTATÓ 1. MILYEN TÍPUSÚ GYÓGYSZER A MAGYTAX INJEKCIÓ ÉS MILYEN BETEGSÉGEK ESETÉN ALKALMAZHATÓ?
 4. sz. melléklete az OGYI-T-8224/01, sz. Forgalomba hozatali engedély módosításának Budapest, 2005. december 7. Szám: 21 126/41/2005 Eloadó: dr. Mészáros Gabriella Melléklet: Tárgy: Betegtájékoztató módosítása
4. sz. melléklete az OGYI-T-8224/01, sz. Forgalomba hozatali engedély módosításának Budapest, 2005. december 7. Szám: 21 126/41/2005 Eloadó: dr. Mészáros Gabriella Melléklet: Tárgy: Betegtájékoztató módosítása
A komplikált intraabdominális infekciók mikrobiológiai diagnosztikája és kezelése felnőtt betegeknél Intézeti protokoll
 A komplikált intraabdominális infekciók mikrobiológiai diagnosztikája és kezelése felnőtt betegeknél Intézeti protokoll Szegedi Tudományegyetem, Aneszteziológiai és Intenzív Terápiás Intézet 2011. Klasszifikáció:
A komplikált intraabdominális infekciók mikrobiológiai diagnosztikája és kezelése felnőtt betegeknél Intézeti protokoll Szegedi Tudományegyetem, Aneszteziológiai és Intenzív Terápiás Intézet 2011. Klasszifikáció:
A tabletta csaknem fehér színű, ovális és UCY 500 kódjelzéssel van ellátva.
 1. A GYÓGYSZER MEGNEVEZÉSE AMMONAPS 500 mg tabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 500 mg nátrium-fenil-butirát tablettánként. Minden AMMONAPS tabletta 62 mg nátriumot tartalmaz. A segédanyagok teljes
1. A GYÓGYSZER MEGNEVEZÉSE AMMONAPS 500 mg tabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 500 mg nátrium-fenil-butirát tablettánként. Minden AMMONAPS tabletta 62 mg nátriumot tartalmaz. A segédanyagok teljes
Betegtájékoztató: Információk a felhasználó számára. Bactroban 20 mg/g kenőcs mupirocin
 Betegtájékoztató: Információk a felhasználó számára Bactroban 20 mg/g kenőcs mupirocin Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára
Betegtájékoztató: Információk a felhasználó számára Bactroban 20 mg/g kenőcs mupirocin Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára
Gyermekkori Idiopátiás Artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Idiopátiás Artritisz Verzió 2016 3. DIAGNÓZIS ÉS TERÁPIA 3.1 Milyen laboratóriumi vizsgálatok szükségesek? A diagnóziskor bizonyos laboratóriumi
www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Idiopátiás Artritisz Verzió 2016 3. DIAGNÓZIS ÉS TERÁPIA 3.1 Milyen laboratóriumi vizsgálatok szükségesek? A diagnóziskor bizonyos laboratóriumi
22. évfolyam 26. szám 2015. július 3. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 22. évfolyam 26. szám 2015. július 3. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Halálos kimenetelű diftéria megbetegedés Spanyolországban 291 Tájékoztatás engedélyezett ferőtlenítőszerekről 296 Fertőző betegségek
22. évfolyam 26. szám 2015. július 3. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Halálos kimenetelű diftéria megbetegedés Spanyolországban 291 Tájékoztatás engedélyezett ferőtlenítőszerekről 296 Fertőző betegségek
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 1 adag (0,5 ml) tartalma: Hepatitisz B felszíni antigén 1,2.
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
Congenitalis adrenalis hyperplasia, 21-hidroxiláz defektus. Szülő- és betegtájékoztató
 Bevezetés Congenitalis adrenalis hyperplasia, 21-hidroxiláz defektus Szülő- és betegtájékoztató Minden szülő azt várja, hogy gyermeke egészséges lesz. Így azután mélyen megrázza őket, ha megtudják, hogy
Bevezetés Congenitalis adrenalis hyperplasia, 21-hidroxiláz defektus Szülő- és betegtájékoztató Minden szülő azt várja, hogy gyermeke egészséges lesz. Így azután mélyen megrázza őket, ha megtudják, hogy
Betegtájékoztató STREPTASE 1 500 000 NE LIOFILIZÁTUM OLDATOS INJEKCIÓHOZ/INFÚZIÓHOZ
 STREPTASE 1 500 000 NE LIOFILIZÁTUM OLDATOS INJEKCIÓHOZ/INFÚZIÓHOZ Streptase 1 500 000 NE liofilizátum oldatos injekcióhoz/infúzióhoz streptokinase HATÓANYAG: Stabilizált tiszta sztreptokináz. A Streptase
STREPTASE 1 500 000 NE LIOFILIZÁTUM OLDATOS INJEKCIÓHOZ/INFÚZIÓHOZ Streptase 1 500 000 NE liofilizátum oldatos injekcióhoz/infúzióhoz streptokinase HATÓANYAG: Stabilizált tiszta sztreptokináz. A Streptase
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA. Ospen 750 000 NE/5 ml belsoleges szuszpenzió. fenoximetilpenicillin
 Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Ospen 400 000 NE/5 ml belsoleges szuszpenzió Ospen 750 000 NE/5
Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Ospen 400 000 NE/5 ml belsoleges szuszpenzió Ospen 750 000 NE/5
Ismeretlen eredetű tüdőgyulladás megjelenése a SARS kórokozó vírusának azonosítása nemzetközi összefogással
 BIOTECHNOLÓGIA AZ EGÉSZSÉGÜGYBEN Ismeretlen eredetű tüdőgyulladás megjelenése a SARS kórokozó vírusának azonosítása nemzetközi összefogással Tárgyszavak: SARS; vírus; koronavírus; vakcina; kutatás; vírusmutáció.
BIOTECHNOLÓGIA AZ EGÉSZSÉGÜGYBEN Ismeretlen eredetű tüdőgyulladás megjelenése a SARS kórokozó vírusának azonosítása nemzetközi összefogással Tárgyszavak: SARS; vírus; koronavírus; vakcina; kutatás; vírusmutáció.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Synflorix szuszpenziós injekció Pneumococcus poliszacharid konjugált vakcina (adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) tartalmaz:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Synflorix szuszpenziós injekció Pneumococcus poliszacharid konjugált vakcina (adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) tartalmaz:
GONDOLJUNK A LISZTÉRZÉKENYSÉGRE Néhány javaslat a betegség korai kimutatására
 GONDOLJUNK A LISZTÉRZÉKENYSÉGRE Néhány javaslat a betegség korai kimutatására www.lq-celiac.com LQ-CELIAC A LISZTÉRZÉKENY BETEGEK ÉLETMINŐSÉGÉNEK JAVÍTÁSA A SZLOVÉN-MAGYAR HATÁR MENTI TÉRSÉGBEN Az egészségügyi
GONDOLJUNK A LISZTÉRZÉKENYSÉGRE Néhány javaslat a betegség korai kimutatására www.lq-celiac.com LQ-CELIAC A LISZTÉRZÉKENY BETEGEK ÉLETMINŐSÉGÉNEK JAVÍTÁSA A SZLOVÉN-MAGYAR HATÁR MENTI TÉRSÉGBEN Az egészségügyi
Az Országos Epidemiológiai Központ módszertani levele a 2016. évi védőoltásokról. 2016. EüK. 4. szám közlemény 3 (hatályos: 2016.02.
 I. BEVEZETÉS Az Országos Epidemiológiai Központ módszertani levele a 2016. évi védőoltásokról 2016. EüK. 4. szám közlemény 3 (hatályos: 2016.02.15 - ) A Védőoltási Módszertani Levél a fertőző betegségek
I. BEVEZETÉS Az Országos Epidemiológiai Központ módszertani levele a 2016. évi védőoltásokról 2016. EüK. 4. szám közlemény 3 (hatályos: 2016.02.15 - ) A Védőoltási Módszertani Levél a fertőző betegségek
Betegtájékoztató NUROFEN 60 MG VÉGBÉLKÚP GYERMEKEKNEK. Nurofen 60 mg végbélkúp gyermekeknek ibuprofén. HATÓANYAG: 60 mg ibuprofén végbélkúponként.
 NUROFEN 60 MG VÉGBÉLKÚP GYERMEKEKNEK Nurofen 60 mg végbélkúp gyermekeknek ibuprofén HATÓANYAG: 60 mg ibuprofén végbélkúponként. SEGÉDANYAG: Szilárd zsír 1: Whitepsol H 15, szilárd zsír 2: Whitepsol W 45.
NUROFEN 60 MG VÉGBÉLKÚP GYERMEKEKNEK Nurofen 60 mg végbélkúp gyermekeknek ibuprofén HATÓANYAG: 60 mg ibuprofén végbélkúponként. SEGÉDANYAG: Szilárd zsír 1: Whitepsol H 15, szilárd zsír 2: Whitepsol W 45.
Betegtájékoztató ARAVA 10 MG FILMTABLETTA. Arava 10 mg filmtabletta (Aventis Pharma)
 ARAVA 10 MG FILMTABLETTA Arava 10 mg filmtabletta (Aventis Pharma) HATÓANYAG: 10 mg leflunomidum filmtablettánként. SEGÉDANYAGOK: Magnézium-sztearát, vízmentes szilicium-dioxid, polividon K-25, kukoricakeményítõ,
ARAVA 10 MG FILMTABLETTA Arava 10 mg filmtabletta (Aventis Pharma) HATÓANYAG: 10 mg leflunomidum filmtablettánként. SEGÉDANYAGOK: Magnézium-sztearát, vízmentes szilicium-dioxid, polividon K-25, kukoricakeményítõ,
21. évfolyam 21. szám 2014. május 30. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT
 21. évfolyam 21. szám 2014. május 30. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Az OEK jelentése a 2014. április hónapban bejelentett fertőző betegségekről 237 Fertőző betegségek adatai 245 E p i d e m i
21. évfolyam 21. szám 2014. május 30. ORSZÁGOS EPIDEMIOLÓGIAI KÖZPONT Epinfo Az OEK jelentése a 2014. április hónapban bejelentett fertőző betegségekről 237 Fertőző betegségek adatai 245 E p i d e m i
I. MELLÉKLET ALKALMAZÁSI ELÕÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELÕÍRÁS 1 1. A GYÓGYSZER NEVE Docetaxel Mylan 20 mg/1 ml koncentrátum oldatos infúzióhoz 2. MINÕSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A koncentrátum oldatos infúzióhoz milliliterenként
I. MELLÉKLET ALKALMAZÁSI ELÕÍRÁS 1 1. A GYÓGYSZER NEVE Docetaxel Mylan 20 mg/1 ml koncentrátum oldatos infúzióhoz 2. MINÕSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A koncentrátum oldatos infúzióhoz milliliterenként
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Varilrix por és oldószer oldatos injekcióhoz Élő, attenuált varicella-zoster vírus (OKA törzs) vakcina Mielőtt Önnél elkezdenék alkalmazni ezt a vakcinát,
Betegtájékoztató: Információk a felhasználó számára Varilrix por és oldószer oldatos injekcióhoz Élő, attenuált varicella-zoster vírus (OKA törzs) vakcina Mielőtt Önnél elkezdenék alkalmazni ezt a vakcinát,
pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált)
 EMA/90006/2015 EMEA/H/C/001104 EPAR-összefoglaló a nyilvánosság számára pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált) Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő
EMA/90006/2015 EMEA/H/C/001104 EPAR-összefoglaló a nyilvánosság számára pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált) Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő
III. melléklet Az Alkalmazási előírás és a Betegtájékoztató egyes fejezeteinek módosításai
 III. melléklet Az Alkalmazási előírás és a Betegtájékoztató egyes fejezeteinek módosításai 34/42 A. Alkalmazási előírás 4.1 Terápiás javallatok [a jelenleg elfogadott indikációk törlendők és a következőkkel
III. melléklet Az Alkalmazási előírás és a Betegtájékoztató egyes fejezeteinek módosításai 34/42 A. Alkalmazási előírás 4.1 Terápiás javallatok [a jelenleg elfogadott indikációk törlendők és a következőkkel
Herpes Vírus fertőzések. A Herpes Vírus csoportnak 8 tagja van
 Herpes Vírus fertőzések A Herpes Vírus csoportnak 8 tagja van Herpes Simplex Vírus (HSV) A herpes vírus csoport tagjai DNS vírusok A vírus ikozaeder alakú (12 oldal) A kapsid 162 kapsomerből áll, melyet
Herpes Vírus fertőzések A Herpes Vírus csoportnak 8 tagja van Herpes Simplex Vírus (HSV) A herpes vírus csoport tagjai DNS vírusok A vírus ikozaeder alakú (12 oldal) A kapsid 162 kapsomerből áll, melyet
100 mikrogramm szalbutamol (szalbutamol-szulfát formájában) adagonként.
 1. A GYÓGYSZER NEVE Ventolin Evohaler túlnyomásos inhalációs szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mikrogramm szalbutamol (szalbutamol-szulfát formájában) adagonként. A segédanyagok teljes
1. A GYÓGYSZER NEVE Ventolin Evohaler túlnyomásos inhalációs szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mikrogramm szalbutamol (szalbutamol-szulfát formájában) adagonként. A segédanyagok teljes
A tényeket többé senki sem hagyhatja figyelmen kívül
 I. A tényeket többé senki sem hagyhatja figyelmen kívül A rák legyőzése - 1. kötet: Az elképzelhetetlen megvalósítható 1. tény: Az iparosodott világban a harmadik leggyakoribb halálozási ok a rák A 21.
I. A tényeket többé senki sem hagyhatja figyelmen kívül A rák legyőzése - 1. kötet: Az elképzelhetetlen megvalósítható 1. tény: Az iparosodott világban a harmadik leggyakoribb halálozási ok a rák A 21.
Összetétel: Hatóanyag: Flebogamma 5% 0,5 g oldatos infúzió 0,5 g intravénás alkalmazásra szánt humán normál immunglobulin
 Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! 4. sz. melléklete az OGYI-T-10 247/01, az OGYI-T-10 248/01, az OGYI-T-10 249/01, és az OGYI-T-10 250/01 sz. forgalomba
Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! 4. sz. melléklete az OGYI-T-10 247/01, az OGYI-T-10 248/01, az OGYI-T-10 249/01, és az OGYI-T-10 250/01 sz. forgalomba
