Gyógyhatású szénhidrátok a véralvadásgátlástól a géncsendesítésig
|
|
|
- Géza Hegedűs
- 8 évvel ezelőtt
- Látták:
Átírás
1 Magyar Kémiai Folyóirat - Előadások 13 Gyógyhatású szénhidrátok a véralvadásgátlástól a géncsendesítésig HERCZEG Mihály, a CSÁVÁS Magdolna, a BERECZKI Ilona, a MEZŐ Erika, a,b ESZENYI Dániel, a,b KICSÁK Máté, a HADHÁZI Ádám, a TOLLAS Szilvia, a VARGA Eszter, a SZILÁGYI Eszter, a MOLNÁR J. Dénes, a BEGE Miklós, a PÉNZES András, a HERCZEGH Pál a és BORBÁS Anikó a,* a Debreceni Egyetem, GYTK, Gyógyszerészi Kémia Tanszék, Egyetem tér 1., 4032 Debrecen, Magyarország b Debreceni Egyetem, TTK, Szerves Kémia Tanszék, Egyetem tér 1., 4032 Debrecen, Magyarország 1. Bevezetés A sejtfelszíni oligoszacharidok kulcsszerepet játszanak a biológiai jelek továbbításában, különböző normális és patológiás felismerési folyamatokban, így például a sejtsejt kommunikációban, az immunválasz kiváltásában, bakteriális és virális fertőzésekben, kardiovaszkuláris és gyulladásos betegségekben, a rákos áttétek kialakulásában. Ezeknek a folyamatoknak a molekuláris részleteit azonban sok esetben nem ismerjük elég pontosan, a bennük résztvevő oligo- és poliszacharidok heterogenitása és lenyűgöző mértékű szerkezeti változatossága ugyanis olyan szintetikus és analitikai problémákat vet fel, amelyek megoldására még mindig nem elégségesek az eszközeink és módszereink. Míg a nukleinsavak és peptidek automatizált szekvenálása és szintézise rég megoldott, a glikokonjugátumok szénhidrát részének szekvenálása és a szilárd fázisú automatizált oligoszacharid-szintézis csak az utóbbi évtizedre vált elérhetővé, és alkalmazhatóságuk erősen korlátozott. Ez az egyik oka annak, hogy a szénhidrátalapú gyógyszerkutatásban kevés a látványos eredmény. A megfelelő hatékonyságú és stabilitású szénhidrát gyógyszerjelöltek kifejlesztésénél további problémát jelent a glikozidos kötések savas és enzimatikus hidrolízissel szembeni érzékenysége, valamint az, hogy a szénhidrátok jellemzően csak kis energiájú kölcsönhatások kialakítására képesek. Mindezek alapján érthető, hogy az intenzív kutatómunka ellenére csak nagyon kevés szénhidrát-tartalmú hatóanyag van jelen a gyógyszerpiacon. 1,2 A szénhidrátokban azonban vitathatatlanul óriási diagnosztikai és terápiás lehetőségek rejlenek, és ezek mind teljesebb felderítése és kiaknázása a glikokémikusok és glikobiológusok egyik legfontosabb feladata. Elsőrendű cél a szintetikus és analitikai eszköztár további fejlesztése, pontosan ismert szerkezetű oligoszacharidok szintézise, illetve biológiai környezetben stabil szénhidrátmimetikumok megtervezése és előállítása, majd ezek felhasználásával a szénhidrátok biológiai szerepének további vizsgálata, a hatásért felelős szerkezetek pontos azonosítása és új terápiás célpontok meghatározása. A Debreceni Egyetemen Bognár Rezső és Lipták András munkássága nyomán nagy hagyományai vannak a szénhidrát- és oligoszacharidkémiai kutatásoknak. Ezen hagyományokból táplálkozva Tanszékünk egyik kiemelt kutatási területe a gyógyhatású szénhidrát-mimetikumok * Tel.: /22475 ; fax: ; borbas.aniko@pharm.unideb.hu szintézise. Célunk a természetes származékoknál stabilabb és erősebb kölcsönhatásokra képes mimetikumok előállítása. Erről a területről az antikoaguláns hatású heparinoid pentaszacharidok szintézise, multivalens szénhidrátligandumok előállítása és új típusú mesterséges nukleozidok kutatása terén elért legújabb eredményeinket mutatjuk be röviden. 2. Véralvadásgátló hatású heparinoid pentaszacharidszulfonsavak szintézise A heparin lineáris láncú, glükózamin és hexuronsav (d-glükuronsav és l-iduronsav) egységekből váltakozva felépülő, nagymértékben szulfatált poliszacharid. Bár elsősorban véralvadásgátló hatásáról ismert, ezen kívül még nagyon sok biológiai folyamatot képes befolyásolni: nagy negatív töltéssűrűsége révén erős Coulombkölcsönhatásokat alakít ki különböző fehérjékkel, jelentősen módosítva működésüket. Több területen is (pl. atheroszklerózis, angiogenezis, Alzheimer-kór) intenzíven vizsgálják a heparin-alapú terápia lehetőségét, ám ezeket a kutatásokat nehezíti a poliszacharid heterogenitása. Mivel az egyes heparin láncokban a d-glükuronsav és l-iduronsav aránya, és a monoszacharid-egységek szulfatációs foka nagy eltéréseket mutat, sokszor már az is komoly nehézséget jelent, hogy a biológiai aktivitásért felelős oligoszacharidszakasz pontos szerkezetét meg tudják határozni. Éppen ezért a változatos szerkezetű heparin-fragmentumok előállítása és széleskörű biológiai vizsgálata nagyon fontos és intenzíven művelt oligoszacharidkémiai kutatási terület. 3 A heparint több mint 30 éven keresztül alkalmazták antitrombotikumként úgy, hogy sem a véralvadásgátló hatás mechanizmusát, sem a hatásért felelős egység szerkezetét nem ismerték. Ma már pontosan tudjuk, hogy a heparin alloszterikusan aktiválja a vérplazma egyik fehérjéjét, az antitrombint (AT), és ez az aktivált fehérje gátolja a véralvadási kaszkád két proteázát, a trombint és a Xa faktort. 4 Az antitrombin aktiválását a poliszacharidnak egy kicsiny, öt monoszacharidból álló egysége végzi, ezt az aktív pentaszacharidot az azonosításnál alkalmazott jelölés miatt DEFGH egységnek nevezi a szakirodalom (1a, 1. Ábra). A hatásmechanizmus ismeretében nyilvánvalóvá vált, hogy a heterogén poliszacharid lánc nagy része közömbös az alvadásgátlás szempontjából,
2 14 Magyar Kémiai Folyóirat - Előadások viszont szerepet játszik a mellékhatások (vérzékenység, súlyosabb esetekben thrombocytopenia) kialakulásában. Így kiemelt gyógyszerfejlesztési cél lett az antitrombin-kötő pentaszacharid kémiai szintézise. Az első szintetikus heparin pentaszacharid gyógyszer, a fondaparinux (1b, Arixtra ) óriási előrelépést jelentett az antitrombotikus terápiában, mert alkalmazásával a heparinnál tapasztalt mellékhatásokat szinte teljesen ki lehetett küszöbölni. 4,5 A vegyület bonyolult szintézise és klinikai hiányosságai (pl. rövid felezési idő, nem dózisfüggő hatás) által indukált további kutatások elvezettek a sokkal egyszerűbb szerkezetű, glükózamin egységet nem tartalmazó szintetikus heparinoidokhoz, amelyek kiemelkedő képviselője, az idraparinux (2) 6 közel kétszer nagyobb antikoaguláns aktivitással rendelkezik, mint a fondaparinux. amellyel a szulfonátometil-csoportok a cukorgyűrű C-2, C-3 és C-6 helyzetében is kialakíthatók. Erre a célra elsőként a szén-szén kettős kötésen végrehajtott gyökös NaHSO 3 addíciót alkalmaztuk (2. Ábra). Az addíciós lépés előtt a megfelelően védett glükozidokon a szabad hidroxilból oxocsoportot képeztünk, majd Wittig-reakcióval kialakítottuk az exometilén-csoportot (8, 10 és 13). Ezután következett a szintézis kulcslépésének számító gyökös addíció, amely minden esetben kiváló regio- és sztereoszelektivitással adta a várt szulfonsav-sókat. Ezt követően felszabadítottuk a glikozilezendő hidroxil-csoportokat, végül a szulfonsavsókból a sav szabaddá tétele után diazometánnal végrehajtott metilezéssel szulfonsav-metilésztereket állítottunk elő (9, 12 és 15) Ábra. Szulfonátometil-csoport kialakítása gyökös NaHSO 3 addícióval. 1. Ábra. A heparin antitrombin-kötő doménje (1a), a belőle kifejlesztett szintetikus véravadásgátló gyógyszer (1b) és a laboratóriumunkban előállított antioaguláns pentaszacharidok (2-6) szerkezete. Kutatócsoportunkban új típusú antikoagulánsok kifejlesztése céljából évek óta foglakozunk az idraparinux szulfonsav-analogonjainak szintézisével. Ennek során a a pentaszacharid-antitrombin kötődésben kulcsszerepet játszó szulfát-félésztereket (-OSO 3- ) szisztematikusan izoszter szulfonátometil-csoportokkal (-CH 2 SO 3- ) helyettesítjük, amelyek ellenállnak a szulfatázok és az észterázok hidrolitikus hatásának, így biológiai környezetben stabilabbak a szulfátésztereknél, ugyanakkor képesek az antikoaguláns aktivitáshoz szükséges erős ionos kötések kialakítására Az elmúlt évek során a primer szulfátészterek helyettesítésével sikeresen előállítottunk egy tri- (3) és két diszulfonsavat (4, 5), egy monoszulfonsav származékot (6), és a referencia molekula (2) szintézisére is kidolgoztunk két új szintetikus útvonalat 7-14 (1. Ábra). A következőkben a szintetikus munka néhány érdekesebb részletét mutatjuk be, és ismertetjük a szerkezet és az antikoaguláns hatás között eddig feltárt összefüggéseket A szulfonsav-tartalmú építőelemek előállítása Az irodalmi előzmények hiánya miatt a szulfonátometilcsoportot tartalmazó monoszacharid-építőelemek előállítása képezte munkánk legnehezebb és legérdekesebb részét. Kezdeti célkitűzésünk az volt, hogy a glükóz egységeken mind primer, mind szekunder helyzetben végrehajtjuk a szulfátészterek cseréjét, ezért olyan módszert kerestünk, A 9, 12 és 15 szulfonsav-észterek kiváló glikozil akceptoroknak bizonyultak, még a kis reaktivitású uronsav-donorokkal is megfelelő afinitással reagáltak. Így előállítottuk a tervezett pentaszacharidok L-iduronsavtartalmú diszacharid- (16-18) és D-glükuronsav-tartalmú triszacharid-fragmentumait (19-21) ezzel elsőként szintetizáltunk olyan oligoszacharidokat, amelyek egyszerre tartalmaznak uronsav egységet és szulfonsav-csoportot is (3. Ábra) Ábra. Uronsav-tartalmú, heparinoid oligoszacharid-szulfonsavak. A magasabb tagszámú oligoszacharidokhoz azonban új, glikozil donorként is használható, szulfonsav-tartalmú építőelemekre volt szükségünk, a metil-glikozidokat ugyanis az anomer csoport túlzott stabilitása miatt nem vagy csak nagyon rossz hozammal lehet glikozil-donorrá alakítani. (Oligoszacharidok szintézise során akceptornak nevezzük azt a reakciópartnert, amely a hidroxilcsoportjával nukleoilként vesz részt a reakcióban, és donornak nevezzük azt a reaktánst, amely a glikozidos szénatomjával elektroilként reagál.) Új építőelemként
3 Magyar Kémiai Folyóirat - Előadások 15 tioglikozidokat kívántunk előállítani, mivel a tioglikozidok stabilak, ezért jó glikozil akceptorok, tioil reagensekkel mégis könnyen távozásra bírható az anomer csoportjuk, így donorként is kiválóan hasznosíthatók. A tioglikozidszulfonsavak képzéséhez azonban a NaHSO 3 -addíciót nem tudtuk alkalmazni, mert a reakciót katalizáló t-butilperbenzoát a tio-aglikont is oxidálta, nehezen izolálható glikozil-szulfoxidok és -szulfonok keverékét eredményezve. Modellreakciók alapján tioglikozidokon is alkalmazható módszernek bizonyult a szulfonátometilén származékot eredményező addíciós-eliminációs mechanizmusú Horner- Wadsworth-Emmons (HWE) reakció. A pentaszacharid közepére beépítendő F-egységhez először a 22 származékot oxidáltuk, majd az így nyert dialdózt dietilfoszfonátometánszulfonsav-etilészterrel 15 reagáltatva (HWE-reakció) előállítottuk a 23 telítetlen szulfonsavetilészter származékot. A kizárólag (E)-izomer formában képződő oleinből katalitikus hidrogénezéssel jutottunk el a 24 molekulához (4. Ábra). b-helyzetű feniltio-csoport nukleoil támadása révén azonnal átalakult szulfónium-ionná (33); ennek az intermediernek a képződését metanol hozzáadásával igazoltuk, melynek hatására a 34 metil-glikozid képződött Ábra. Szulfonátometil-csoport kialakítása nukleoil cserével: hatékony reakció a-o-glikozidon és sikertelen kísérlet b-s-glikozidon. Feltételeztük, hogy az intramolekuláris nukleoil csere csak akkor megy végbe, ha az aglikon b-térhelyzetű, és a-tioglikozidból kiindulva elkerülhető az anomer csoport nem kívánt részvétele a reakcióban. A megfelelő a-tioglikozidokon (35, 38) valóban a kívánt módon játszódott le szulfonátometil-csoport bevitele (6. Ábra). A primer hidroxilokból képezett trilát-észtereket (36, 39) lítiált metánszulfonsav-etilészterrel reagáltatva kiváló hozammal nyertük a két szulfonsav-tartalmú glikozil donort (37, 40). 4. Ábra. Szulfonátometilezés Horner-Wadsworth-Emmons reakcióval. Hasonló módon, de jóval szerényebb összhozammal állítottuk elő a 25 tioglikozidból a D-építőelemként szolgáló 28 glikozol-donort; a gyengébb kitermelés oka az volt, hogy az oxidációs lépésnél nem tudtuk kiküszöbölni a 27-et eredményező eliminációs mellékreakciót. A HWEreakcióval ugyan szekunder helyzetben is ki tudtuk alakítani a szulfonátometilén-csoportot, de a hidrogénezési lépésnél sem a konverzió, sem a sztereoszelektivitás nem volt megfelelő, így a továbbiakban kizárólag a primer helyzetű szulfonsavat tartalmazó pentaszacharidok szintézisével foglalkoztunk. A rendelkezésünkre álló 9, 24 és 28 építőelemek két pentaszacharid-szulfonsav szintéziséhez voltak elegendőek. 11 A munka folytatásához nagy mennyiségben volt szükségünk a szulfonsav-tartalmú monoszacharidokra, ezért az eddigieknél hatékonyabb módszert kerestünk az előállításukra. Primer helyzetű metánszulfonsav-bevitelre leggyorsabb reakcióút a nukleoil-csere, amely a megfelelően védett 6-hidroxi származékból (7) két lépésben végrehajtható (5. Ábra). A hatékonyság szempontjából kulcsfontosságúnak bizonyult a távozó csoport: a 29 6-jód származék csak szerény konverzióval reagált a metánszulfonsav-etilészterből generált karbanionnal, a 6-O-triluormetán-szulfonát (30) intermedieren keresztül viszont kiváló hozammal nyertük a 31 szulfonsav-etilészter származékot, majd ebből a 32 glikozil akceptort. 14,16 Meglepő módon a 22 tioglikozidon ez a szulfonsav-beviteli módszer nem működött. Az első lépésben képződő 6-O-trilát származék ugyanis a Miután sikerült hatékony módszerrel nagy mennyiségben előállítani a 6-dezoxi-6-szulfonátometil tartalmú D-, F- és H-építőelemeket, hozzáláttunk a tervezett pentaszacharid szulfonsavak szintéziséhez. 6. Ábra. Szulfonátometil-csoport kialakítása nukleoil cserével a-sglikozidokon A pentaszacharidok szintézise A pentaszacharidok szintézisére kipróbált többféle reakcióút közül a leghatákonyabbnak azt találtuk, amikor az uronsavak prekurzorait, a D-glükózt és L-idózt használtuk a glikozilezésekben, és a prekurzorokat oligoszacharidszinten oxidáltuk uronsavvá. A pentaszacharid vázat minden esetben [2+3] blokkszintézissel, a megfelelően védett DE diszacharid donorok és FGH triszacharid akceptorok össze-kapcsolásával állítottuk elő. A szintézis során acetil-csoporttal védtük azokat a hidroxilokat, amelyek a végtermékben metil-éter formában vannak, míg a szulfatálandó hidroxilokon benzil-éter védőcsoportokat
4 16 Magyar Kémiai Folyóirat - Előadások alkalmaztunk. Ezek a védőcsoportok egyúttal biztosították a glikozilezési lépések megfelelő sztereoszelektivitását is: a C-2 helyzetű észterek az 1,2-transz-, az éterek pedig az 1,2-cisz-glikozidos kötések kialakulását segítették elő. Időleges hidroxil védőcsoportként 2-naftilmetil-étert alkalmaztunk, amely szelektíven eltávolítható mind az acetil-, mind a benzil-csoportok mellől. A szintézis részleteit a pentaszacharid triszulfonsav (3) előállításán keresztül mutatjuk be. akceptort. A OH származékot a 37 szulfonsav-tartamú F építőelemmel glikozilezve nyertük a 47 triszacharidot, amelyből a 2-naftilmetil-éter (NAP) oxidatív hasításával állítottuk elő a 48 akceptort. A 42 diszacharid és a 48 triszacharid összekapcsolásával jó hozammal és teljes sztereoszelekivitással nyertük a 49 védett pentaszacharidot (9. Ábra). A 41 tioglikozidot használtuk az E-uronsav egység prekurzoraként, amit a 40 tioglikoziddal glikozileztünk. 14 A két tioglikozid közül az éter védőcsoportokat viselő, ezért reaktívabb 40 származék kemoszelektív aktiválásával képeztük a 42 diszacharidot. A 40 vegyület C-2 éter védőcsoportja nem-résztvevő tulajdonságával elősegítette a kívánt 1,2-cisz (a-d konigurációjú) interglikozidos kötés kialakulását (7. ábra). 7. Ábra. A DE diszacharid donor előállítása kemoszelektív glikozilezéssel. A szulfonsavtartalmú 32 glikozil akceptor és a 43 L-idopiranozil-imidát donor reakciójával állítottuk elő a teljesen védett 44 diszacharidot. Ebben az esetben a donor C-2 résztvevő csoportja biztosította a kívánt 1,2-transz (a-l konigurációjú) glikozidos kötés kialakulását a G és H egység között (8. ábra). Ezután az idóz részről eltávolítottuk 9. Ábra. A pentaszacharid triszulfonsav (3) szintézise. Az adott lépésben kialakított/átalakított csoportokat ellipszissel jelöltük. A pentaszacharid vázon kialakítottuk az E glükuronsav egységet ( 50), a szulfonsav- és karbonsav-észtereket sóvá alakítottuk, az acetil csoportokat metilre cseréltük (51), végül eltávolítottuk a benzilétereket, és a felszabaduló hidroxilok szulfatálásával megkaptuk a 3 pentaszacharid triszulfonsavat. 11,14 Hasonló módon állítottuk elő az idraparinuxot (2), 13 és a további szulfonsav származékokat (4-6) is, amelyek közül eddig a 2-4 vegyületekről vannak részletes biológiai és szerkezetvizsgálati eredményeink 2.3. Szerkezet és antikoaguláns aktivitás 8. Ábra. Az FGH tiszacharid akceptor szintézise. a 4,6-benzilidén acetált, majd a 45 diolból TEMPO (tetrametilpiperidin-1-oxil) és BAIB (bisz-acetoxijódbenzol) reagensekkel végzett szelektív gyökös oxidációval képeztük az L-iduronsav-tartalmú 46 diszacharid A pentaszacharid szulfonsavak (3, 4) antikoaguláns hatását humán plazmán végzett in vitro Xa faktorgátlási vizsgálatokkal határoztuk meg, referenciaként az idraparinuxot (2) és a fondaparinux gyógyszermolekulát (1) használtuk (1. Táblázat). A pentaszacharid-diszulfonsav (4) kiváló anti-xa aktivitást mutatott, kétszer aktívabbnak bizonyult mint a forgalomban lévő gyógyszer (1), a 3 triszulfonsav-származéknál viszont nagyon jelentős hatáscsökkenést tapasztaltunk.
5 Magyar Kémiai Folyóirat - Előadások Táblázat. A pentaszacharidok in vitro Xa-gátló hatása Pentaszacharid Anti-Xa aktivitás (U/mg) a fondaparinux (1) 1195±189 idraparinux (2) 1911±193 3 triszulfonsav 384±139 4 diszulfonsav 2153±153 a Egységnyi nemzetközi heparin standard aktivitására vonatkoztatott érték. A véralvadásgátló hatásban mutatkozó óriási különbség okait keresve NMR mérésekkel és molekuladinamikai szimulációval vizsgáltuk a szabad, és az antitrombinhoz kötött 2-4 pentaszacharidok térszerkezetét. Ezek a vizsgálatok azt mutatták, hogy az antitrombinhoz kötött pentaszacharidok térszerkezete gyakorlatilag azonos, ami érthető, hiszen a kötődéshez szükséges konformáció determinált. A 2 és 4 pentaszacharidok szabad állapotban egyetlen kitüntetett konformációt vesznek fel, ami megegyezik a kötött állapotú konformációkkal, ez magyarázza kiváló aktivitásukat. A pentaszacharid triszulfonsavnak viszont szabad állapotban két stabilis konformációja van, és ezek egyike jelentősen eltér a kötött konformációtól. 17 Az eltérő konformer valószínűleg nehezen tud a kötődéshez szükséges biokatív térszerkezetbe átbillenni, ez magyarázhatja a biológiai aktivitás jelentős csökkenését. Eredményeink bizonyítják, hogy a szulfátészterek helyére beépített szulfonsav-csoportok biztosítani tudják a biológiai hatáshoz szükséges erős kötődést, ugyanakkor módosíthatják az oligoszacharid térszerkezetét, ami alapvetően befolyásolja a biológiai aktivitást. Az 5 és 6 pentaszacharid-szulfonsavak jövőbeni vizsgálatai tovább pontosíthatják ismereteinket a szerkezet és antikoaguláns hatás kapcsolatásól. A szerkezethatás összefüggések alaposabb megismerése más terápiás területen is segítheti a hatásos heparin származékok kifejlesztését, és felgyorsíthatja az Alzheimer-kór, a gyulladásgátlás vagy a daganatok terápiájának terén folyó heparin-alapú gyógyszerkutatást is. 3. Önszerveződő multivalens rendszerek szintézise stabil glikomimetikumokból 3.1. Fotokatalizált tioladdíció endociklusos kettőskötést tartalmazó szénhidrát származékokon Az oligoszacharidok in vivo alkalmazása során komoly problémát jelenthet az O-glikozidos kötések hasítása glikozidázok által. Ez a probléma kiküszöbölhető az enzimatikus hidrolízisnek ellenálló szintetikus glikomimetikumokkal ilyenek például a tioglikozidok, amelyekben a glikozidos oxigént egy kénatom helyettesíti. A tioglikozidos kötés kialakítására az utóbbi években egyre elterjedtebben alkalmazzák a terminális alkéneken lejátszódó fotokatalizált, gyökös mechanizmusú tioladdíciót, amely enyhe körülmények között bármilyen oldószerben végrehajtható gyors, regioszelektív és jó hozamú reakció. 18 Ezekben az eljárásokban általában 1-tiocukrokat reagáltatnak alkenil-szubsztituált (többnyire allilezett) szacharidokkal, aminosavakkal vagy peptidekkel, ami alkilszulfanil híddal összekötött mimetikumokat eredményez. 19 Úgy véltük, jelentősen kibővíthető a tioladdíció alkalmazási köre, ha endociklusos kettős kötésű szénhidrátokat használunk alkén partnerként, mert így a cukoregységeket közvetlenül, hídmolekula beiktatása nélkül kapcsolhatjuk egymáshoz vagy más biomolekulához. Ezért megvizsgáltuk a könnyen előállítható endoglikálok és 2,3-telítetlen glikozidok fotokatalizált reakcióját különböző tiolokkal 2,2-dimetoxi- 2-fenil-acetofenon (DPAP) fotoiniciátor jelenlétében. 20,21 Amint az 1-tioglükóz-peracetáttal (57) végzett tioladdíció példáján látható, a reakciók teljes regioszelektivitással mentek végbe (10. Ábra). A D-glükálra (52) történő addíció sajnos nem mutatott sztereoszelektivitást, az 53 és 54 diasztereomerek ~1:1 arányú, nehezen elválasztható elegyét adta. Az 55 2-acetoxi-D-glükál és az 58 2,3-telítetlen glikozid esetében viszont nagyon jó konverziót és teljes sztereoszelektivitást tapasztaltunk, ezzel elsőkén mutattuk be, hogy ezek a telítetlen szénhidrátok kiváló alkén partnerek lehetnek a fotoiniciált tioladdíciós reakciókban Ábra. Gyökös tioladdíció endociklusos kettős kötést tartalmazó szénhidrátokon. Változatos szerkezetű tiolokkal reagáltatva az 55 2-acetoxiglikált megálapítottuk, hogy a reakciónak vannak korlátai: aromás és benzil-helyzetű tiolokkal a láncközi kettős kötés nem, vagy csak kis konverzióval reagál. 21 Ugyanakkor alkil-tiolokkal, cukor-tiolokkal, ciszteinnel, peptidekkel jó konverzióval és mindig teljes sztereoszelektivitással megy végbe az addíció, 1,2-cisz (a-d) tioglikozidok képződését eredményezve (2. Táblázat). 20,22 Ez a módszer gyors, egyszerű és enyhe reakcióutat nyújt oligoszacharidok és glikokonjugátumok stabil tioglikozid mimetikumainak szintézisére. A 2,3-telítetlen glikozidok tioladdíciós reakciói is mindig teljes regio- és sztereoszelektivitással játszódtak le és kizárólag 3-dezoxi-2-S-diszacharidok képződését eredményezték. 21 Ez a szelektivitás lehetővé teszi a-(1 2)- S-kötésű mannobiozid mimetikumok gyors és hatékony szintézisét, amit oligomannozidok multivalens tiomimetikumainak szintézisében hasznosítottunk Multivalens mannobiozid mimetikumok szintézise A human immundeiciencia vírus (HIV) számos más kórokozóhoz (pl. Ebola vírus) hasonlóan a felületén található oligomannozid struktúrák és a gazdasejt mannózkötő lektinjei közötti kölcsönhatás révén képes megfertőzni a szervezetet. A fertőzés megakadályozásának egyik módja lehet a multivalens szénhidrát ligandumokon alapuló
6 18 Magyar Kémiai Folyóirat - Előadások antiadhéziós terápia. Multivalens ligandumok és receptorok kölcsönhatásának átlagos szabadenergia változása gyakran nagyobb, mint a monomerek közötti kölcsönhatás mértéke. Ilyenkor szinergizmus lép fel a megsokszorozott molekulafajták között, ami ellensúlyozhatja a receptorligandum kölcsönhatások jellemzően kis energiáját. ellátott 2,3-telítetlen glikozidot (60) állítottunk elő, amiből 1-tiomannóz-peracetáttal végrehajtott addícióval nyertük a tioglikozid kötésű mannobiozid-mimetikumot (62). Azidképzés és Zemplén dezacetilezés után megkaptuk a lipoil hordozóhoz konjugálható hidroil bioaktív egységet (64). 2. Táblázat. Tioladdíció 2-acetoxi glükálon 11. Ábra. Azid-alkin cikloaddícióra kész mannobiozid mimetikum szintézise tioladdícióval. Lipoil csoportként többek között a fullerén-c 60 származékot választottuk, amelyet 1,3-dipoláris cikloaddícióval kapcsoltunk össze a 64 mannobiozid mimetikummal (12. ábra). A fullerén tetraetilénglikol oldalláncai biztosították a 66 végtermék megfelelő vízoldékonyságát. A 64 vegyület felhasználásával több amiil származékot is előállítottunk, amelyek a fényszórásfotometriás vizsgálatok szerint vízben nm méretű multivalens aggregátumokká szerveződnek. 24 A származékok mannózkötő-lektinekkel való kötődésének vizsgálata folyamatban van. 4. Új típusú peptid-nukleinsavak: ciszteinil-nukleozidok szintézise és oligomerizálása Az utóbbi időben a multivalencia eléréséhez elsősorban nem kovalens felépítésű vázhoz kötik a monomereket, hanem önszerveződő, klaszterképző vegyületeket alkalmaznak, melyek előállítása biológiailag aktív molekulák és amiil szerkezetek összekapcsolásával történik. 23 Mi is ezt az elvet alkalmaztuk potenciálisan HIV-ellenes multivalens szénhidrátok előállítása során, amelyek bioaktív mannobiozid részét tioladdícióval állítottuk elő 24 (11. Ábra) Az 52 glikálból Ferrier-reakcióval egy hídmolekulával A szintetikus nukleozid származékokat széles körben használják gyógyászati célokra daganatellenes és vírusellenes szerként. A módosított nukleotidok egy intenzíven kutatott, óriási gyógyászati potenciállal bíró alkalmazási lehetősége a géncsendesítés. Géncsendesítő terápia során egy hibás vagy rosszul működő fehérje által okozott betegség gyógyítása a cél a fehérjét kódoló gén expressziójának transzkripciós vagy transzlációs szintű, szelektív gátlásával. 26 Erre a célra meghatározott szekvenciájú, az adott génnel vagy az arról átíródó mrns-sel komplementer szintetikus nukleinsav analógok használhatók. Ezekkel a mesterséges nukleinsavakkal szemben alapvető követelmény a nukleáz rezisztencia, ami biztosíthatja a hatás kifejtéséhez szükséges életidejüket. Terápiás szempontból ígéretes származékok a peptid-nukleinsavak (PNS), amelyek különleges szerkezetükből adódóan ellenállnak mind a nukleázok, mind a proteázok litikus hatásának. Az irodalomból ismert peptidnukleinsavakban a természetes nukleinsavak enzimatikusan hasítható cukor-foszfát gerincét egy peptidváz, leggyakrabban poli-aminoetilglicin helyettesíti, és a nukleobázisok közvetlenül ehhez a peptidvázhoz kapcsolódnak 27 vagyis ezek a származékok nem tartalmaznak szénhidrátot.
7 Magyar Kémiai Folyóirat - Előadások 19 N-(luorenil-metoxikarbonil)-cisztein reakciója kizárólag a kívánt 72 terméket adta, de rossz hatékonysággal. Alacsony hőmérsékleten kicsi volt a konverzió, magasabb hőmérséklet vagy erősebb bázis alkalmazása viszont az Fmoc csoport bomlásához vezetett. Végül a szabad ciszteinnel végrehajtott nukleoil szubsztitúció (73), és az Fmoc védőcsoport utólagos kialakítása bizonyult a leghatékonyabb reakcióútnak, így jó összhozammal kaptuk a szilárdfázisú peptidszintézisre alkalmas 72 ciszteinil-uridin monomert. 12. Ábra. Aggregációra képes mannobiozid-fullerén konjugátum szintézise. A fotokatalitikus tioladdíciós reakció felhasználásával olyan peptid nukleinsavak kifejlesztését határoztuk el, amelyek a természetes nukleinsavakban megtalálható cukor komponenst is tartalmazzák, így azoknak közelebbi szerkezeti analógjai, mint a hagyományos PNS származékok. Célunk ciszteinil-nukleozid monomerek előállítása volt, amelyekből a peptid-szintézis eszközeivel oligocisztein gerincet tartalmazó ún. cisztein-nukleinsavak nyerhetők. A ciszteinil-nukleozid monomerek előállításának körülményeit a legkönnyebben kezelhető nukleozidon, az uridinen dolgoztuk ki. A 4 -exometilén uridin (67) és a 68a N-acetilcisztein reakciója a várakozásainkkal ellentétben nem mutatott sztereoszelektivitást, az addíció a D-riboés L-lixo-konigurációjú diasztereomerek 1:1 arányú, szétválaszthatatlan keverékét adta, és ugyanilyen eredményt kaptunk N-terc-butoxikarbonil-ciszteinnel is. (13. Ábra). Megvizsgáltuk, hogy a cukor részen a ciklikus izopropilidén acetál helyett acetil vagy szilil védőcsoportot alkalmazva javítható-e a kívánt D-ribo-izomer hozama, de sajnos nem jártunk sikerrel. 14. Ábra. Peptidszintézisre alkalmas ciszteinil-nukleozid szintézise. A peptidszintézist Wang gyantán hajtottuk végre. Első lépésben a szabad karboxilcsoportot tartalmazó ciszteinilszármazékot észter-kötéssel a szilárd fázishoz kötöttük, majd követtük a peptidszintézis protokollját (15. Ábra). Lehasítottuk a cisztein aminocsoportjáról az Fmoc védőcsoportot, ezután a 72 származék és a megfelelő reagensek hozzáadásával kialakítottuk az első peptidkötést. A rendelkezésünkre álló monomerrel még három kapcsolási ciklust tudtunk végrehajtani, így egy védett pentapeptidet kaptunk, amit vizes triluorecetsavval lehasítottunk a gyantáról. A savas kezelés egyúttal a védőcsoportokat is eltávolította, így megkaptuk az első ciszteinil-nukleozid oligomer végtemékünket (74). 15. Ábra. Pentaciszteinil-nukleinsav előállítása Wang gyantán. 13. Ábra. Cisztein konjugálása uridinhez fotokatalitkust ioladdícióval. Ezt követően nukleoil szubsztitúciós reakcióval kapcsoltuk a ciszteint a ribózhoz (14. Ábra) A jód uridin és az A géncsendesítéshez tagszámú, meghatározott bázisszekvenciájú nukleinsav származék szükséges. Szilárdfázisú vagy automatizált peptidszintézissel ez a lánchosszúság könnyen elérhető, de valamennyi nukleobázisból elő kell állítanunk hozzá a megfelelő ciszteinil-nukleozid monomert.
8 20 Magyar Kémiai Folyóirat - Előadások A szintézist az uridin komplementer nukleozidjával, az adenozinnal folytattuk (16. Ábra). Az uridinre kidolgozott szintézisút és védőcsoport-stratégia sajnos nem működött, az 5 -jód származékból a purinbázis részvételével intramolekuláris ciklizáció történt. Számos kísérlet után a peptidszintézisre alkalmas 78 ciszteinil-konjugátumot végül a következő módon állítottuk elő: a bázis aminocsoportját N,N-dimetilformamidin formában védtük, a ribóz részen szilil védőcsoportokat alkalmaztunk, és a 71 Fmoc-védett ciszteinnel hajtottuk végre a nukleoil szubsztitúciót. 16. Ábra. Ciszteinil-adenozin monomer előállítása Folyamatban van a 78 ciszteinil-adenozinból homooligomer előállítása, amit a 74 származékkal való Watson-Crick hibridizációs vizsgálatokhoz kívánunk felhasználni. Megkezdtük a további ciszteinil-nukleozid monomerek előállítását, hogy megvalósíthassuk távlati célunkat, változatos bázisszekvenciájú, géncsendesítésre alkalmas cisztein-nukleinsavak kifejlesztését. Köszönetnyilvánítás Köszönjük az OTKA pénzügyi támogatását, a K 62802, K és K pályázatok nélkül a kutatások nem valósulhattak volna meg. A kutatás részben a TÁMOP A/ azonosító számú Nemzeti Kiválóság Program Hazai hallgatói, illetve kutatói személyi támogatást biztosító rendszer kidolgozása és működtetése országos program című kiemelt projekt keretében zajlott. A projekt az Európai Unió támogatásával, az Európai Szociális Alap társinanszírozásával valósul meg. Köszönjük a hivatkozási listában szereplő társzerzőink értékes hozzájárulását. Hivatkozások 1. Wong, C-H. Carbohydrate based Drug Discovery1-2, John Wiley-VCH: Weinheim, Seeberger, P. H.; Werz, D. B. Nature, 2007, 446, Miller, G. J.; Hansen, S. U.; Avizienyte, E.; Rushton, G.; Cole, C.; Jayson, G. C.; Gardiner, J. M. Chem. Sci., 2013, 4, van Boeckel, C. A. A.; Petitou, M. Angew. Chem. Int. Ed. 2004, 43, Chang, C.-H.; Lico, L. S.; Huang, T.-Y.; Lin, S.-Y.; Chang, C.-L.; Arco, S. D.; Hung, S.-C. Angew. Chem. Int. Ed. 2014, 53, Westerduin, P.; van Boeckel, C. A. A.; Basten, J. E. M.; Broekhoven, M. A.; Lucas, H.; Rood, A.; van der Heiden, H.; van Amsterdam, R. G. M.; van Dinther, T. G.; Meuleman, D. G.; Visser, A.; Vogel, G. M. T.; Damm, J. B. L.; Overklift, G. T. Bioorg. Med. Chem. 1994, 2, Herczeg, M.; Lázár, L.; Borbás, A.; Lipták, A.; Antus, S. Org. Lett. 2009, 11, Lázár, L.; Herczeg, M.; Fekete, A.; Borbás, A.; Lipták, A.; Antus, S. Tetrahedron Lett. 2010, 51, Herczeg, M.; Lázár, L.; Mándi, A.; Borbás, A.; Komáromi, I.; Lipták, A.; Antus, S. Carbohydr. Res. 2011, 346, Lázár, L.; Mező, E.; Herczeg, M.; Lipták, A.; Antus, S.; Borbás, A. Tetrahedron 2012, 68, Herczeg, M.; Lázár, L.; Bereczky, Zs.; Kövér, K. E.; Timári, I.; Kappelmayer, J.; Lipták, A.; Antus, S.; Borbás, A. Chem. Eur. J. 2012, 18, Herczeg, M.; Mező, E.; Lázár, L.; Fekete, A.; Kövér, K. E.; Antus, S.; Borbás, A. Tetrahedron 2013, 69, Herczeg, M.; Mező, E.; Eszenyi, D.; Antus, S.; Borbás, A. Tetrahedron 2014, 70, Mező, E.; Herczeg, M.; Eszenyi, D.; Borbás, A. Carbohydr. Res. 2014, 388, Carretero, J. C.; Demillequand, M.; Ghosez, L. Tetrahedron 1987, 43, Herczeg, M.; Mező, E.; Eszenyi, D.; Lázár, L.; Csávás, M.; Bereczki, I.; Antus, S.; Borbás, A. Eur. J. Org. Chem. 2013, Kövér Katalin és Komáromi István kutatócsoportjának még nem publikált eredményei. 18. Hoyle, C. E.; Lee, T. Y.; Roper, T. J. Polym. Sci. Part A: Polym. Chem. 2004, 42, Dondoni, A.; Marra, A. Chem. Soc. Rev. 2012, 41, L. Lázár, M. Csávás M. Herczeg, P. Herczegh, A. Borbás, Org. Lett. 2012, 14, Lázár, L.; Csávás, M..; Hadházi, Á.; Herczeg, M.; Tóth, M.; Somsák, L.; Barna, T.; Herczegh, P.; Borbás, A. Org. Biomol. Chem. 2013, 11, Dénès, F., Pichowicz, M., Povie, G., Renaud, P. Chem. Rev., 2014, 114, Barnard, A., Smith, D. K.: Angew. Chem. Int. Ed. 2012, 51, Csávás, M..; Demeter, T.; Herczeg, M.; Timári, I.; Kövér, K. E.; Herczegh, P.; Borbás, A. Tetrahedron Lett. 2014, 55, Tollas, S.; Bereczki, I.; Borbás, A.; Batta, G.; Vanderlinden, E.; Naesens, L.;Herczegh, P. Bioorg. Med. Chem. Lett. 2014, 24, Dallas, A.; Vlassov, A. V.Med Sci Monit 2006; 12, RA Nielsen P. E. In Chemical Synthetic Biology Luisi, P. L.; C Chiarabelli, C. Eds.; John Wiley & Sons, 2011, pp
9 Carbohydrates as potential therapeutics - from anticoagulation to gene-silencing Magyar Kémiai Folyóirat - Előadások 21 Synthesis of carbohydrate mimetics for potential pharmaceutical applications is one of our main research topics in the Department of Pharmaceutical Chemistry at the University of Debrecen. As therapeutical application of glycosides is hampered by their in vivo instability and their low binding afinity towards proteins, we focus on the design and synthesis of unnatural derivatives with an increased stability and with better binding properties. In this article, we summarized our recent results in the following topics: i) synthesis and biological evaluation of heparinoid pentasaccharide sulfonic acids; ii) preparation of thio-linked glycosides by photoinduced free radical hydrothiolation of endocyclic double bond of sugars and application of the thiol addition method in the synthesis of self-assembling multivalent thiomannobioside ligands of mannose-binding lectins; iii) synthesis of a cysteinyl uridine pentapeptide, the irst member of a novel type of peptide nucleic acids.
Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise
 Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise Varga Eszter IV. éves gyógyszerészhallgató DE-GYTK GYÓGYSZERÉSZI KÉMIAI TANSZÉK Témavezető: Dr. Borbás Anikó tanszékvezető, egyetemi
Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise Varga Eszter IV. éves gyógyszerészhallgató DE-GYTK GYÓGYSZERÉSZI KÉMIAI TANSZÉK Témavezető: Dr. Borbás Anikó tanszékvezető, egyetemi
Megemlékezés Lipták András nemzetközileg elismert szénhidrátkémikusról
 Magyar Kémiai Folyóirat 39 Megemlékezés Lipták András nemzetközileg elismert szénhidrátkémikusról Antus sándor * Debreceni Egyetem Szerves Kémiai Tanszék, 4010 Debrecen, Pf.20 A szénhidrátkémia nemzetközileg
Magyar Kémiai Folyóirat 39 Megemlékezés Lipták András nemzetközileg elismert szénhidrátkémikusról Antus sándor * Debreceni Egyetem Szerves Kémiai Tanszék, 4010 Debrecen, Pf.20 A szénhidrátkémia nemzetközileg
VÉRALVADÁSGÁTLÓ HATÁSÚ PENTASZACHARIDOK
 Egyetemi doktori (PhD) értekezés tézisei VÉRALVADÁSGÁTLÓ HATÁSÚ PENTASZACHARIDOK MODULÁRIS SZINTÉZISE Mező Erika Témavezető Dr. Borbás Anikó DEBRECENI EGYETEM Természettudományi Doktori Tanács Kémiai Doktori
Egyetemi doktori (PhD) értekezés tézisei VÉRALVADÁSGÁTLÓ HATÁSÚ PENTASZACHARIDOK MODULÁRIS SZINTÉZISE Mező Erika Témavezető Dr. Borbás Anikó DEBRECENI EGYETEM Természettudományi Doktori Tanács Kémiai Doktori
II. Szintézis és biológiai vizsgálatok
 I. Bevezetés A támogatott kutatások célja a biológiai szabályozási és felismerési folyamatokban fontos szerepet játszó, negatív töltésű szénhidrátok szulfonsav-tartalmú analóg vegyületeinek előállítása
I. Bevezetés A támogatott kutatások célja a biológiai szabályozási és felismerési folyamatokban fontos szerepet játszó, negatív töltésű szénhidrátok szulfonsav-tartalmú analóg vegyületeinek előállítása
Szénhidrát-alapú véralvadásgátlók
 Szénhidrát-alapú véralvadásgátlók A heparin Felfedezés (1916): Jay McLean, Prof. William Howel, Johns Hopkins Egyetem, Baltimore. Emlős szövetekből nyert extraktum, mely meggátolja a vér alvadását. Izolálás
Szénhidrát-alapú véralvadásgátlók A heparin Felfedezés (1916): Jay McLean, Prof. William Howel, Johns Hopkins Egyetem, Baltimore. Emlős szövetekből nyert extraktum, mely meggátolja a vér alvadását. Izolálás
Oligoszacharid-fehérje konjugátumok elöállítása OTKA ny.sz.: 35128
 ligoszacharid-fehérje konjugátumok elöállítása TKA ny.sz.: 35128 A kutatási idöszakban elért eredmények három csoportba sorolhatók: 1. Mikobakteriális eredetü sejtfelszíni oligoszacharidok elöállítása,
ligoszacharid-fehérje konjugátumok elöállítása TKA ny.sz.: 35128 A kutatási idöszakban elért eredmények három csoportba sorolhatók: 1. Mikobakteriális eredetü sejtfelszíni oligoszacharidok elöállítása,
Az antitrombotikus hatású idraparinux pentaszacharid új szintézise és szulfonsav tartalmú analogonjainak előállítása
 DE-TTK 1949 Az antitrombotikus hatású idraparinux pentaszacharid új szintézise és Egyetemi doktori (PhD) értekezés Herczeg Mihály Témavezető: Prof. Dr. Lipták András DEBRECENI EGYETEM Természettudományi
DE-TTK 1949 Az antitrombotikus hatású idraparinux pentaszacharid új szintézise és Egyetemi doktori (PhD) értekezés Herczeg Mihály Témavezető: Prof. Dr. Lipták András DEBRECENI EGYETEM Természettudományi
Májer Gábor (Témavezető: Dr. Borbás Anikó)
 Anionos oligoszacharidok szintézise 1-dezoxi-1-etoxiszulfonil-hept--ulopiranozil építőelemek felhasználásával. Ketopiranozil-glikozidok anomer konfigurációjának vizsgálata doktori (PhD) értekezés tézisei
Anionos oligoszacharidok szintézise 1-dezoxi-1-etoxiszulfonil-hept--ulopiranozil építőelemek felhasználásával. Ketopiranozil-glikozidok anomer konfigurációjának vizsgálata doktori (PhD) értekezés tézisei
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
1.1. Az N-acetil-neuraminsav szulfonsav mimetikumainak szintézise L-fukózból
 Kutatási zárójelentés a Szénhidrátszulfonsav típusú sziálsavmimetikumok szintézise és neuraminidázgátló hatásuk vizsgálata (K 62802) című pályázatról 1. Potenciálisan neuraminidázgátló vegyületek szintézise
Kutatási zárójelentés a Szénhidrátszulfonsav típusú sziálsavmimetikumok szintézise és neuraminidázgátló hatásuk vizsgálata (K 62802) című pályázatról 1. Potenciálisan neuraminidázgátló vegyületek szintézise
Szerves Kémia II. Dr. Patonay Tamás egyetemi tanár E 405 Tel:
 Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
ZÁRÓJELENTÉS. OAc. COOMe. N Br
 ZÁRÓJELETÉS A kutatás előzményeként az L-treoninból kiindulva előállított metil-[(2s,3r, R)-3-( acetoxi)etil-1-(3-bróm-4-metoxifenil)-4-oxoazetidin-2-karboxilát] 1a röntgendiffrakciós vizsgálatával bizonyítottuk,
ZÁRÓJELETÉS A kutatás előzményeként az L-treoninból kiindulva előállított metil-[(2s,3r, R)-3-( acetoxi)etil-1-(3-bróm-4-metoxifenil)-4-oxoazetidin-2-karboxilát] 1a röntgendiffrakciós vizsgálatával bizonyítottuk,
Zárójelentés a Sonogashira reakció vizsgálata című 48657sz. OTKA Posztdoktori pályázathoz. Novák Zoltán, PhD.
 Zárójelentés a Sonogashira reakció vizsgálata című 48657sz. OTKA Posztdoktori pályázathoz Novák Zoltán, PhD. A Sonogashira reakciót széles körben alkalmazzák szerves szintézisekben acetilénszármazékok
Zárójelentés a Sonogashira reakció vizsgálata című 48657sz. OTKA Posztdoktori pályázathoz Novák Zoltán, PhD. A Sonogashira reakciót széles körben alkalmazzák szerves szintézisekben acetilénszármazékok
A citoplazmában előforduló glikoprotein pentaszacharid szénhidrátrészének szintézise doktori (PhD) értekezés tézisei
 citoplazmában előforduló glikoprotein pentaszacharid szénhidrátrészének szintézise doktori (Ph) értekezés tézisei Szabó Zoltán (Témavezető: r. Lipták ndrás) Synthesis of the pentasaccharide-segment of
citoplazmában előforduló glikoprotein pentaszacharid szénhidrátrészének szintézise doktori (Ph) értekezés tézisei Szabó Zoltán (Témavezető: r. Lipták ndrás) Synthesis of the pentasaccharide-segment of
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 5. Szén-szén többszörös kötések kialakítása: alkének Kovács Lajos 1 Alkének el állítása X Y FGI C C C C C C C C = = a d C O + X C X C X = PR 3 P(O)(OR) 2 SiR 3 SO 2 R
Szerves kémiai szintézismódszerek 5. Szén-szén többszörös kötések kialakítása: alkének Kovács Lajos 1 Alkének el állítása X Y FGI C C C C C C C C = = a d C O + X C X C X = PR 3 P(O)(OR) 2 SiR 3 SO 2 R
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
O S O. a konfiguráció nem változik O C CH 3 O
 () ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
() ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
Ortogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM rtogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére Doktori (PhD) értekezés tézisei Készítette: Tatai János Témavezető:
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM rtogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére Doktori (PhD) értekezés tézisei Készítette: Tatai János Témavezető:
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Általános megjegyzések
 ZÁRÓJELENTÉS Általános megjegyzések A T 048713 sz. kutatási pályázat futamideje során az eredeti munkatervhez képest több módosulás / módosítást történt; ezeket túlnyomó részben a külső körülmények előre
ZÁRÓJELENTÉS Általános megjegyzések A T 048713 sz. kutatási pályázat futamideje során az eredeti munkatervhez képest több módosulás / módosítást történt; ezeket túlnyomó részben a külső körülmények előre
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
Biológiailag aktív oligoszacharidok és analogonjaik szintézise
 AKADÉMIAI DOKTORI ÉRTEKEZÉS Biológiailag aktív oligoszacharidok és analogonjaik szintézise Dr. Borbás Anikó Debreceni Egyetem Orvos- és Egészségtudományi Centrum Gyógyszerészi Kémia Tanszék, MTA-DE Szénhidrátkémiai
AKADÉMIAI DOKTORI ÉRTEKEZÉS Biológiailag aktív oligoszacharidok és analogonjaik szintézise Dr. Borbás Anikó Debreceni Egyetem Orvos- és Egészségtudományi Centrum Gyógyszerészi Kémia Tanszék, MTA-DE Szénhidrátkémiai
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
H 3 C H + H 3 C C CH 3 -HX X 2
 1 Gyökös szubsztitúciók (láncreakciók gázfázisban) - 3 2 2 3 2 3-3 3 Szekunder gyök 3 2 2 2 3 2 2 3 3 2 3 3 Szekunder gyök A propánban az azonos strukturális helyzetű hidrogének és a szekunder hidrogének
1 Gyökös szubsztitúciók (láncreakciók gázfázisban) - 3 2 2 3 2 3-3 3 Szekunder gyök 3 2 2 2 3 2 2 3 3 2 3 3 Szekunder gyök A propánban az azonos strukturális helyzetű hidrogének és a szekunder hidrogének
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
Biológiailag aktív oligoszacharidok és analogonjaik szintézise
 AKADÉMIAI DOKTORI ÉRTEKEZÉS TÉZISEI Biológiailag aktív oligoszacharidok és analogonjaik szintézise Dr. Borbás Anikó Debreceni Egyetem Orvos- és Egészségtudományi Centrum Gyógyszerészi Kémia Tanszék, MTA-DE
AKADÉMIAI DOKTORI ÉRTEKEZÉS TÉZISEI Biológiailag aktív oligoszacharidok és analogonjaik szintézise Dr. Borbás Anikó Debreceni Egyetem Orvos- és Egészségtudományi Centrum Gyógyszerészi Kémia Tanszék, MTA-DE
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Név: Pontszám: / 3 pont. 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
 Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
Szénhidrátok I. (Carbohydrates)
 sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
Szakmai Zárójelentés
 Szakmai Zárójelentés Baktériumok és glikoprotein antennák mannózt tartalmazó oligoszacharidjainak szintézise 1. -Mannozidos kötést tartalmazó bakteriális oligoszacharidok szintézise 1.1. Egy, a Bordetella
Szakmai Zárójelentés Baktériumok és glikoprotein antennák mannózt tartalmazó oligoszacharidjainak szintézise 1. -Mannozidos kötést tartalmazó bakteriális oligoszacharidok szintézise 1.1. Egy, a Bordetella
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Ortogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM VEGYÉSZMÉRNÖKI ÉS BIMÉRNÖKI KAR LÁH GYÖRGY DKTRI ISKLA rtogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére Tézisfüzet
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM VEGYÉSZMÉRNÖKI ÉS BIMÉRNÖKI KAR LÁH GYÖRGY DKTRI ISKLA rtogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére Tézisfüzet
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Zárójelentés a PD OTKA pályázathoz
 Zárójelentés a PD 77467 TKA pályázathoz A pályázat keretében a munkatervnek megfelelően három fontosabb témára összpontosítottam, így a beszámolót is ennek megfelelően tagolom. A reakciókhoz minden témában
Zárójelentés a PD 77467 TKA pályázathoz A pályázat keretében a munkatervnek megfelelően három fontosabb témára összpontosítottam, így a beszámolót is ennek megfelelően tagolom. A reakciókhoz minden témában
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
I. Szerves savak és bázisok reszolválása
 A pályázat négy éve alatt a munkatervben csak kisebb módosításokra volt szükség, amelyeket a kutatás során folyamatosan nyert tapasztalatok indokoltak. Az alábbiakban a szerződés szerinti bontásban foglaljuk
A pályázat négy éve alatt a munkatervben csak kisebb módosításokra volt szükség, amelyeket a kutatás során folyamatosan nyert tapasztalatok indokoltak. Az alábbiakban a szerződés szerinti bontásban foglaljuk
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
Heparánáz inhibitorok szintézise
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁYI EGYETEM Heparánáz inhibitorok szintézise ozil csoporttal védett azacukor akceptorok alkalmazása heparin diszacharid analógok szintézisében Doktori (PhD) értekezés Készítette:
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁYI EGYETEM Heparánáz inhibitorok szintézise ozil csoporttal védett azacukor akceptorok alkalmazása heparin diszacharid analógok szintézisében Doktori (PhD) értekezés Készítette:
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
IX. Szénhidrátok - (Polihidroxi-aldehidek és ketonok)
 IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Szerződéses kutatások/contract research
 Szerződéses kutatások/contract research Év/year Cím/subject (témavezető/principle investigator) Partner Összeg/amount Epitópok predikciója és szintézismódszer kidolgozása/ Epitope prediction and development
Szerződéses kutatások/contract research Év/year Cím/subject (témavezető/principle investigator) Partner Összeg/amount Epitópok predikciója és szintézismódszer kidolgozása/ Epitope prediction and development
3. Előadás. Oligo- és poliszacharidok
 3. Előadás ligo- és poliszacharidok Szénhidrátok Legnagyobb mennyiségben előforduló szerves anyagok: szénhidrátok, 100 milliárd tonna, évente újratermelődő biomassza. Egyéb: fehérje, nukleinsav, zsirok
3. Előadás ligo- és poliszacharidok Szénhidrátok Legnagyobb mennyiségben előforduló szerves anyagok: szénhidrátok, 100 milliárd tonna, évente újratermelődő biomassza. Egyéb: fehérje, nukleinsav, zsirok
Polihidroxi-aldehidek vagy -ketonok, vagy ezek származékai. Monoszacharid: polihidroxi-keton vagy -aldehid
 Szénhidrátok Polihidroxi-aldehidek vagy -ketonok, vagy ezek származékai. Általános képletük: ( 2 ) n ahol n 3 Monoszacharid: polihidroxi-keton vagy -aldehid ligoszacharid: 2 10 monoszacharid glikozidkötéssel
Szénhidrátok Polihidroxi-aldehidek vagy -ketonok, vagy ezek származékai. Általános képletük: ( 2 ) n ahol n 3 Monoszacharid: polihidroxi-keton vagy -aldehid ligoszacharid: 2 10 monoszacharid glikozidkötéssel
A GAMMA-VALEROLAKTON ELŐÁLLÍTÁSA
 A GAMMA-VALEROLAKTON ELŐÁLLÍTÁSA A LEVULINSAV KATALITIKUS HIDROGÉNEZÉSÉVEL Strádi Andrea ELTE TTK Környezettudomány MSc II. Témavezető: Mika László Tamás ELTE TTK Kémiai Intézet ELTE TTK, Környezettudományi
A GAMMA-VALEROLAKTON ELŐÁLLÍTÁSA A LEVULINSAV KATALITIKUS HIDROGÉNEZÉSÉVEL Strádi Andrea ELTE TTK Környezettudomány MSc II. Témavezető: Mika László Tamás ELTE TTK Kémiai Intézet ELTE TTK, Környezettudományi
Funkcionalizált, biciklusos heterociklusok átalakításai sztereokontrollált gyűrűnyitó metatézissel
 Funkcionalizált, biciklusos heterociklusok átalakításai sztereokontrollált gyűrűnyitó metatézissel Benke Zsanett, Nonn Melinda, Fülöp Ferenc, Kiss Loránd Szegedi Tudományegyetem, Gyógyszerkémiai Intézet
Funkcionalizált, biciklusos heterociklusok átalakításai sztereokontrollált gyűrűnyitó metatézissel Benke Zsanett, Nonn Melinda, Fülöp Ferenc, Kiss Loránd Szegedi Tudományegyetem, Gyógyszerkémiai Intézet
A kémiatanári zárószigorlat tételsora
 1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
A citoplazmában előforduló glikoprotein pentaszacharid szénhidrátrészének szintézise. doktori (PhD) értekezés. Szabó Zoltán
 A citoplazmában előforduló glikoprotein pentaszacharid szénhidrátrészének szintézise doktori (PhD) értekezés Szabó Zoltán Debreceni Egyetem Természettudományi Doktori Tanács Kémia Doktori Iskola Debrecen,
A citoplazmában előforduló glikoprotein pentaszacharid szénhidrátrészének szintézise doktori (PhD) értekezés Szabó Zoltán Debreceni Egyetem Természettudományi Doktori Tanács Kémia Doktori Iskola Debrecen,
Szénhidrátok. Szénhidrátok. Szénhidrátok. Csoportosítás
 Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
KÉMIA SZEKCIÓ ANALITIKAI- ÉS KOORDINÁCIÓS KÉMIAI VALAMINT REAKCIÓKINETIKAI TAGOZAT. Időpont: november Hely: Kémia Épület K/1 terem
 KÉMIA SZEKCIÓ ANALITIKAI- ÉS KOORDINÁCIÓS KÉMIAI VALAMINT REAKCIÓKINETIKAI TAGOZAT Időpont: 2010. november 25. 14.00 Hely: Kémia Épület K/1 terem A zsűri elnöke: Dr. Bányai István tszv. egyetemi tanár
KÉMIA SZEKCIÓ ANALITIKAI- ÉS KOORDINÁCIÓS KÉMIAI VALAMINT REAKCIÓKINETIKAI TAGOZAT Időpont: 2010. november 25. 14.00 Hely: Kémia Épület K/1 terem A zsűri elnöke: Dr. Bányai István tszv. egyetemi tanár
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK
 POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
Magyar. Kémiai Folyóirat. Kémiai Közlemények 121. ÉVFOLYAM, 2015
 Magyar Kémiai Folyóirat Kémiai Közlemények 121. ÉVFOLYAM, 2015 1 A Magyar Kémikusok Egyesülete tudományos folyóirata A Magyar Tudományos Akadémia Kémiai Osztályának közleményei Magyar Kémiai Folyóirat
Magyar Kémiai Folyóirat Kémiai Közlemények 121. ÉVFOLYAM, 2015 1 A Magyar Kémikusok Egyesülete tudományos folyóirata A Magyar Tudományos Akadémia Kémiai Osztályának közleményei Magyar Kémiai Folyóirat
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit
 SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
Világító molekulák: Új típusú, szolvatokróm fluorofórok előállítása, vizsgálata és alkalmazásaik
 Világító molekulák: Új típusú, szolvatokróm fluorofórok előállítása, vizsgálata és alkalmazásaik Kéki Sándor Alkalmazott Kémiai Tanszék, Debreceni Egyetem MTA Felolvasó Ülés Budapest, 217. január 24. Vázlat
Világító molekulák: Új típusú, szolvatokróm fluorofórok előállítása, vizsgálata és alkalmazásaik Kéki Sándor Alkalmazott Kémiai Tanszék, Debreceni Egyetem MTA Felolvasó Ülés Budapest, 217. január 24. Vázlat
1. feladat. Versenyző rajtszáma: Mely vegyületek aromásak az alábbiak közül?
 1. feladat / 5 pont Mely vegyületek aromásak az alábbiak közül? 2. feladat / 5 pont Egy C 4 H 8 O összegképletű vegyületről a következő 1 H és 13 C NMR spektrumok készültek. Állapítsa meg a vegyület szerkezetét!
1. feladat / 5 pont Mely vegyületek aromásak az alábbiak közül? 2. feladat / 5 pont Egy C 4 H 8 O összegképletű vegyületről a következő 1 H és 13 C NMR spektrumok készültek. Állapítsa meg a vegyület szerkezetét!
R-OH H + O H O H OH H O H H OH O H OH O H OH H H
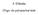 3. Előadás ligo- és poliszacharidok Diszacharidok Definició: Két monoszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésben résztvevő C-atomok
3. Előadás ligo- és poliszacharidok Diszacharidok Definició: Két monoszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésben résztvevő C-atomok
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A természetben előforduló, β-mannozidos kötést tartalmazó szénhidrátok szintézise. doktori (PhD) értekezés. Debreceni Egyetem Debrecen, 2001.
 A természetben előforduló, β-mannozidos kötést tartalmazó szénhidrátok szintézise doktori (PhD) értekezés Rákó János Debreceni Egyetem Debrecen, 2001. Ezen értekezést a Debreceni Egyetem Kémia doktori
A természetben előforduló, β-mannozidos kötést tartalmazó szénhidrátok szintézise doktori (PhD) értekezés Rákó János Debreceni Egyetem Debrecen, 2001. Ezen értekezést a Debreceni Egyetem Kémia doktori
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól
 Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
R R C X C X R R X + C H R CH CH R H + BH 2 + Eliminációs reakciók
 Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
KOVÁCS Anita Kármen PhD hallgató, Dr. HETÉNYI Anasztázia egyetemi tanársegéd, Prof. Dr. TÓTH Gábor egyetemi tanár
 Glikozilált, védett aminosavak szintézise glikozilált biokonjugátumok előállítása céljából Synthesis of Glycosilated, Protected Amino Acids for the Preparation of Glycosilated Bioconjugates Sinteza glicozilaminoacizilor
Glikozilált, védett aminosavak szintézise glikozilált biokonjugátumok előállítása céljából Synthesis of Glycosilated, Protected Amino Acids for the Preparation of Glycosilated Bioconjugates Sinteza glicozilaminoacizilor
Szabó Andrea. Ph.D. értekezés tézisei. Témavezető: Dr. Petneházy Imre Konzulens: Dr. Jászay M. Zsuzsa
 Budapesti Műszaki és Gazdaságtudományi Egyetem Szerves Kémiai Technológia Tanszék α-aminofoszfinsavak és származékaik sztereoszelektív szintézise Szabó Andrea h.d. értekezés tézisei Témavezető: Dr. etneházy
Budapesti Műszaki és Gazdaságtudományi Egyetem Szerves Kémiai Technológia Tanszék α-aminofoszfinsavak és származékaik sztereoszelektív szintézise Szabó Andrea h.d. értekezés tézisei Témavezető: Dr. etneházy
Ortogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM rtogonális védőcsoportstratégia heparin és heparánszulfát oligoszacharidok szintézisére Doktori (PhD) értekezés Készítette: Tatai János Témavezető: Dr. Fügedi
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM rtogonális védőcsoportstratégia heparin és heparánszulfát oligoszacharidok szintézisére Doktori (PhD) értekezés Készítette: Tatai János Témavezető: Dr. Fügedi
Peptidek LC-MS/MS karakterisztikájának javítása fluoros kémiai módosítással, proteomikai alkalmazásokhoz
 Peptidek LC-MS/MS karakterisztikájának javítása fluoros kémiai módosítással, proteomikai alkalmazásokhoz Dr. Schlosser Gitta tudományos munkatárs MTA-ELTE Peptidkémiai Kutatócsoport MedInProt Tavaszi Konferencia
Peptidek LC-MS/MS karakterisztikájának javítása fluoros kémiai módosítással, proteomikai alkalmazásokhoz Dr. Schlosser Gitta tudományos munkatárs MTA-ELTE Peptidkémiai Kutatócsoport MedInProt Tavaszi Konferencia
Heparánáz inhibitorok szintézise
 Ph. D. ÉRTEKEZÉS TÉZISEI Csíki Zsuzsanna Heparánáz inhibitorok szintézise ozil csoporttal védett azacukor akceptorok alkalmazása heparin diszacharid analógok szintézisében Témavezető: Dr. Fügedi Péter
Ph. D. ÉRTEKEZÉS TÉZISEI Csíki Zsuzsanna Heparánáz inhibitorok szintézise ozil csoporttal védett azacukor akceptorok alkalmazása heparin diszacharid analógok szintézisében Témavezető: Dr. Fügedi Péter
12/4/2014. Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció. 1952 Hershey & Chase 1953!!!
 Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Ortogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM rtogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére Doktori (Ph.D.) értekezés Készítette: Daragics Katalin Témavezető:
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁNYI EGYETEM rtogonális védőcsoport-stratégia heparin és heparán-szulfát oligoszacharidok szintézisére Doktori (Ph.D.) értekezés Készítette: Daragics Katalin Témavezető:
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE
 Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
Új oxo-hidas vas(iii)komplexeket állítottunk elő az 1,4-di-(2 -piridil)aminoftalazin (1, PAP) ligandum felhasználásával. 1; PAP
 Új oxo-hidas vas(iii)komplexeket állítottunk elő az 1,4-di-(2 -piridil)aminoftalazin (1, PAP) ligandum felhasználásával. H 1; PAP H FeCl 2 és PAP reakciója metanolban oxigén atmoszférában Fe 2 (PAP)( -OMe)
Új oxo-hidas vas(iii)komplexeket állítottunk elő az 1,4-di-(2 -piridil)aminoftalazin (1, PAP) ligandum felhasználásával. H 1; PAP H FeCl 2 és PAP reakciója metanolban oxigén atmoszférában Fe 2 (PAP)( -OMe)
Biomolekuláris nanotechnológia. Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium
 Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
3. Előadás. Oligo- és poliszacharidok
 3. Előadás ligo- és poliszacharidok Szénhidrátok Legnagyobb mennyiségben előforduló szerves anyagok: szénhidrátok, 100 milliárd tonna, évente újratermelődő biomassza. Egyéb: fehérje, nukleinsav, zsirok
3. Előadás ligo- és poliszacharidok Szénhidrátok Legnagyobb mennyiségben előforduló szerves anyagok: szénhidrátok, 100 milliárd tonna, évente újratermelődő biomassza. Egyéb: fehérje, nukleinsav, zsirok
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
7. évfolyam kémia osztályozó- és pótvizsga követelményei Témakörök: 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2.
 7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
CHO H H H OH H OH OH H CH2OH HC OH HC OH HC OH CH 2
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
A szénhidrátkód. Somsák László az MTA doktora Debreceni Egyetem Szerves Kémiai Tanszék
 A szénhidrátkód Somsák László az MTA doktora Debreceni Egyetem Szerves Kémiai Tanszék somsak@tigris.unideb.hu A Földön évente újratermelődő biomassza mintegy 200 milliárd tonna/év tömegűnek becsülhető
A szénhidrátkód Somsák László az MTA doktora Debreceni Egyetem Szerves Kémiai Tanszék somsak@tigris.unideb.hu A Földön évente újratermelődő biomassza mintegy 200 milliárd tonna/év tömegűnek becsülhető
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
