MULTINUCLEAR NMR SPECTROSCOPY STUDIES OF SOME ALUMINIUM COMPLEXES IN SOLUTION
|
|
|
- Ágoston Csonka
- 8 évvel ezelőtt
- Látták:
Átírás
1 MULTINUCLEAR NMR SPECTROSCOPY STUDIES OF SOME ALUMINIUM COMPLEXES IN SOLUTION PhD thesis Andrea Bodor University of Debrecen Debrecen, 2000
2 I. Bevezetés, célkitűzések Az alumínium a XX század féme. Felfedezése a múlt század közepére esik, nagyobb tételben azonban csak a múlt század végén állították elő. Azidőtájt az ára az ezüstével vetekedett, annak ellenére, hogy a földkéregben előforduló leggyakoribb fém. Jelentősége a vaséval hasonlítható össze és alkalmazása is a vaséval együtt értékelhető. Ha az alumínium oldaláról vizsgálódunk, akkor könnyen észrevehetjük a következő előnyöket. Ötvözetei összevethető szilárdságúak az acélokéval, de jóval kevésbé korrodeálódnak (passziválódás) és jóval könnyebbek (7.8 g cm 3 és 2.7 g cm 3 ). Ahol erős, de könnyű szerkezeti anyagra van szükség, mint pl. repülőgépipar, építőipar, ott az alumíniumot megtaláljuk. Az elektrotechnikai alkalmazás rávilágít az alumínium másik nagy előnyére, nevezetesen arra, hogy kicsi a fajlagos ellenállása, a drága réz helyett így az erősáramú elektrotechnika első számú fémes vezető anyaga. Az alumínium nem alattomos fém, a jelenlegi kutatási eredmények azt mutatják, hogy nem található meg az élő szervezetekben. Sem jelenléte, sem hiánya nem oka betegségeknek, legalábbis egyértelmű bizonyítékok ezt nem támasztják alá. A biokémiai és élettani ciklusban való megjelenése kizárólagosan az emberi tevékenység (ipari termelés) eredménye, következésképpen az élő szervezetekben nem fejlődött ki védekező rendszer ellene. Időről-időre felmerül toxikus volta. Az Alzheimer kór és az alumínium szervezetbeli jelenléte közötti kapcsolat nagyon valószínű, és az élő szervezetek kalcium és magnézium háztartásába való beépülésével is "alaposan gyanúsítható". Az alumínium biológiai szerepe az elmúlt évtizedek aktív kutatómunkája ellenére sem tekinthető tisztázottnak. Az azonban egyértelmű, hogy az Al 3+ ion, hidrolízisre való erős hajlama miatt, csak komplex vegyületei formájában juthat el a "tetthelyre", ahol kedvező (gondoljunk terápiás alkalmazásaira) vagy káros hatását kifejtheti. A komplexképzésben a természetben előforduló fluorid és az oxigéntartalmú kismolekulák, például a citrát (Cit), oxalát (Ox) külön-külön és együttesen is szerepet játszanak, és a vizes oldatban elkerülhetetlenül jelenlévő OH ion hatása sem hanyagolható el. Az alumínium kémiájára vonatkozó ismereteink hiányosságának egyik oka az, hogy az alumínium igen nehezen vizsgálható. Az olcsó és könnyen hozzáférhető műszeres technikák számára rejtőzködő elem. A látható, infravörös és ultraibolya spektrofotometriai és az elektrokémiai módszerek csak igen közvetetten alkalmazhatók. Az NMR 1
3 szempontjából a 27 Al atommag 100 %-os jelenlétével biztató lehetne, de az I=5/2 es értékű magspin és a belőle következő gyors kvadrupólus relaxáció, a széles jelek nem tették az NMR spektroszkópusok kedvelt mérési tárgyává. Így az alumínium komplexek oldatbeli szerkezetéről is keveset tudunk. Egyensúlyi kémiájának vizsgálata sem könnyű az előzőek szerint, amit még tetéz kinetikai inertsége is. Ennek következtében az alumíniumról szóló egyensúlyi tárgyú dolgozatok visszatérő gondja az "egyensúly elérése". Azt mondhatjuk, hogy az alumínium koordinációs kémiai vizsgálata kényszerűen mindig "kinetikával terhelt". A leírtak fényében a munkánk célja az volt, hogy: 1. megvizsgáljuk koordinációs kémiai igényességgel az Al 3+ ion és néhány fémion szállító ligandum (F, OH, oxalát, citrát) vizes oldatait az eddigi eredmények ellenőrzése céljából. 2. eszközként alkalmazva a multinukleáris NMR spektroszkópiát, elsősorban a ligandumok NMR aktív magjainak ( 1 H, 13 C és 19 F) mérésével közvetlen módszerrel igazoljuk az egyensúlyi modellekből következő részecskeeloszlást. 3. felhasználva az utóbbi évtized rohamos fejlődését a kismolekulák NMR spektroszkópiás szerkezetvizsgálatában, szerkezeti információkat gyűjtsünk a képződő komplexek oldatbeli szerkezetéről, és összevessük azt a szilárd komplexekre vonatkozó diffrakciós eredményekkel. 4. a dinamikus NMR teljes eszköztárát felsorakoztatva a gyakorlatilag hiányzó, vagy csak kvalitatív becsléseken alapuló egyensúlyi dinamikai információkat gyűjtsünk az Al 3+ és az előzőekben felsorolt ligandumok vizes oldatbeli egyensúlyairól. 2
4 II. Alkalmazott vizsgálati módszerek Legfontosabb kísérleti eszközünk a magmágneses rezonancia spektroszkópia (NMR) volt. A 1 H, 13 C, 19 F és 27 Al NMR spektrumokat Bruker 360 és 500 MHz es készülékeken vettük fel és a WINNMR program segítségével dolgoztuk fel. Az egyszerű egydimenziós méréseken ( 1 H, 19 F) kívül 13 C NMR esetén a 1 H lecsatoláshoz az "inverse gated" és "power gated"; polarizáció átvitelhez a DEPT impulzusszekvenciákat alkalmaztuk. Szükség esetén a szerves kismolekulák tanulmányozásánál bevált két dimenziós korrelációs módszerekhez folyamodtunk: COSY, NOESY, ROESY, HETCOR, LR HETCOR. Ezek segítségével elvégezhető a jelazonosítás, esetenként a jelek intenzitásából a komplexek stabilitási állandói határozhatók meg. A csatolási séma és a 2 J HH és 3 J CH spin-spin csatolási állandók lehetővé teszik az oldatban lévő komplexek szerkezetének meghatározását. Az egyensúlyi rendszereinkben előforduló kémiai cserefolyamatokat mágnesezettség átviteli módszekkel tanulmányoztuk. A T 1 skálán történő méréseknél szelektív inverzióátvitelt egy dimenzióban a DANTE szekvenciával, két dimenzióban az EXSY impulzusszekvenciával végeztük. Az eredményeket a MATLAB programmal, a Gauss Newton Marquardt féle nem lineáris legkisebb négyzetek módszerével értékeltük. A T 2 skálán a jelszélesség mérése mellett a teljes jelalak analízist is alkalmaztuk. A spektrumokat a Bloch egyenletek mátrix formalizmusa alapján számoltuk ki, a mért és számolt spektrumokat jellegzetes adataik, a jelek szélessége, eltolódása és intenzitása alapján hasonlítottuk össze. Egyensúlyi méréseket az alumínium oxalát fluorid rendszerben potenciometriás módszerrel, fluorid ionszelektív és kinhidron elektród együttes alkalmazásával végeztünk. A stabilitási szorzatokat, amelyek ún. sztöchiometriai állandók, a LETAGROP program alkalmazásával számítottuk ki. Az oldatok ph-ját lehetőség szerint kombinált elektróddal mértük. Savas oldatokban az elektródot tönkretevő HF jelenlétében a F /HF 19 F NMR jelének, illetve nagy, nem állandó elektrolitkoncentráció elkerülhetetlensége folytán, lúgos oldatokban a CN /HCN 13 C NMR jelének kémiai eltolódását mérve in situ határoztuk meg a ph-t. 3
5 III. Új tudományos eredmények Munkánk során az alumínium és néhány fontos ligandum komplexének összetételét, oldatbeli szerkezetét és kinetikai sajátságait határoztuk meg multinukleáris NMR módszerekkel. Eredményeinkkel sikerült a korábban már vizsgált rendszerekre vonatkozó ismereteket kiegészíteni, pontosítani és az ellentmondások egy részét feloldani. Az egyensúlyok dinamikai jellemzésében gyökeresen új eredményeket értünk el. 1. Az alumínium fluorid 19 F NMR vizsgálata során azonosítottuk a törzs komplexeket és a jelintenzitások segítségével kiszámoltuk ezek stabilitási állandóit. Az alkalmazott közegtől függően változott a részecskék száma. Így, 3 M KCl háttérelektrolit mellett az AlF (3 i)+ i, i = 1 3, míg 0.6 M TMACl közegben az AlF (3 i)+ i, i = 1 5 komplexek jelennek meg. Az irodalomban számos utalás történik az AlF 2 5 és AlF 3 6 részecskékre, ám létezésüket vizes oldatban eddig még nem igazolták. Az általunk felvett 19 F NMR spektrumok egyértelműen bizonyítják az AlF komplex képződését, de nem utalnak AlF 6 jelenlétére még nagyon nagy F fölösleg mellett sem. Megállapítottuk, hogy ha ez a komplex mégis létezik vizes közegben, akkor stabilitási állandója, K 6 < 0,5. 2. Az alumínium fluorid rendszerben megjelenő egyes törzskomplexek jelszélessége ph, illetve hőmérsékletfüggő. Teljes jelalak analízissel és mágnesezettség átviteli mérésekkel bizonyítottuk, hogy a rendszer egyensúlyi dinamikáját a F csere jellemzi és nem a komplexképződés. A fluoridcsere valószínűleg asszociatív interchange mechanizmussal írható le. Megállapítottuk, hogy a cseresebességi állandók értéke nagyobb a vízcserére vonatkozó állandókénál, és értékük a szubsztitúció mértékével nő. Alacsony hőmérsékleten az AlF + 2 részecske cisz és transz izomerjei is azonosíthatóak. 3. Az alumínium oxalát rendszerben 13 C NMR segítségével azonosítottuk a törzskomplexeket. Megállapítottuk, hogy szobahőmérsékleten nincs cserefolyamat sem a törzskomplexek, sem pedig ligandumcsere a komplexek és a szabad oxalát között. Az AlOx 2 komplexnek két azonos intenzitású jelét detektáltuk, ez a cisz és transz izomerekhez rendelhető. Vizsgáltuk az izomerizáció hőmérséklet függését, megállapítva, hogy az Al 3+ belső koordinációs szférájában történik az átrendeződés. Az AlOx 3 3 részecske és a szabad oxalát közötti csere csak magasabb hőmérsékleten észlelhető. A 4
6 mágnesezettség átviteli kísérletek eredményeiből számolt aktiválási paraméterek D, vagy I d mechanizmusra utalnak. 4. Az alumínium fluorid oxalát rendszerben négy vegyes ligandumú részecskét találtunk potenciometriásan (AlFOx, AlF 2 Ox, AlFOx 2 2, AlF 2 Ox 3 2 ) és kiszámoltuk a stabilitási állandókat. Összemérhető c F és c Al koncentrációviszonyok mellett a vegyes komplexek képződése meghatározó fontosságú. A komplexeket 13 C és 19 F NMR segítségével is azonosítottuk. Széles NMR jeleik és azok különös viselkedése a hőmérséklet növelésével bonyolult inter és intra molekuláris cserefolyamatok jelenlétére utal. Megállapítható, hogy akár a fluorid, akár az oxalát törzskomplexekhez viszonyítjuk, a vegyes ligandumú komplexekben a ligandumok labilisabbak. 5. Az alumínium citrát rendszerben megjelenő egymagvú és hárommagvú komplexeket egyaránt azonosítottuk 1 H és 13 3 C NMR mérésekkel. Az Al(Cit) 2 és a hárommagvú Al 3 (OH) 4 (H 1 Cit) 7 3 (Sy) részecskék szerkezete oldatban viszonylag szimmetrikus, amint azt a jelszegény NMR spektrumok is alátámasztják. Elvégeztük a hárommagvú Al 3 (OH)(H 1 Cit) 4 3, (As), komplex esetén az igencsak jelgazdag 1 H és 13 C NMR spektrumok teljes hozzárendelését. A csatolási állandók értékeiből megadtuk a három különböző citrát ligandum térbeli elrendeződését. Eredményeinket összevetve az irodalomban közölt szilárd szerkezettel arra a következtetésre jutottunk, hogy vizes oldatban az As komplex megőrizte nem szimmetrikus szerkezetét, és a ligandumok elrendezése igen hasonló a szilárd szerkezethez. 6. Tanulmányoztuk a már szerkezetileg is jellemzett három alumínium citrát részecske kinetikai viselkedését. Az As komplex inert, nem vesz részt sem inter, sem intra molekuláris cserefolyamatokban. Megállapítottuk, hogy az 3 Al(Cit) 2 és Sy részecskék egyaránt fluxionálisak, ez utóbbi esetében kiszámítottuk az intra molekuláris csere aktiválási paramétereit. Mindkét komplex cserekapcsolatban van a szabad citráttal. Az Al(Cit) 3 2 esetén az aktiválási entrópia nagy negatív értéke asszociatív jellegű (I a ) mechanizmusra utal. A Sy komplex esetében a ligandumcsere dinamikáját leíró egyenlet: w= k1[ Sy] + k2[ Sy][ OH ]. Az első tag valószínűleg a víz koncentrációját is tartalmazza. Erre utal az aktiválási entrópia nagy negatív értéke. Az OH kinetikai szerepe magyarázható az egyik Al 3+ hoz való átmeneti koordinálódásával, ami a komplexet labilissá teszi. A komplexek labilitási sorrendje Al(Cit) 3 2 > Sy >> As. A kinetikai sajátság változása jól 5
7 értelmezhető a nem hídhelyzetű protonált háromfogú, illetve a deprotonált háromfogú citrát koordinációval a két első, valamint a négyfogú, hídhelyzetű ligandum jelenlétével a harmadik komplex esetében. Az általunk vizsgált reakciók kinetikai adatait az alábbi táblázatban foglaltuk össze. Cserefolyamat H * (kj mol 1 ) S * (J mol 1 K 1 ) k 298 (s 1 ) Mechanizmus AlOx 2 2 / intra 67 ± 5 6 ± 6 5 ± 0,5 kötés felhasadás AlOx 3 3 / Ox 164 ± ± 51 6, D/I d Al(Cit) 2 3 / Cit 43 ± 1 90 ± 29 1,0 ± 0,1 I a As / Cit <0,03 As / intra <0,03 Sy / intra 70 ± 5 34 ± kötés felhasadás Sy / Cit 65 ± 7 78 ± 21 0,08±0,01 I a 6
8 Közlemények jegyzéke 1. A. Bodor, I. Tóth, I. Bányai, Z. Szabó, G. T. Hefter: 19 F NMR Study of the Equilibria and Dynamics of the Al 3+ /F system; Inorg. Chem., 2000, 39, G. T. Hefter, A. Bodor, Imre Tóth: Does AlF 6 3 exist in solution? (közlésre beküldve) 3. A. Bodor, I. Bányai, I. Tóth: Structural study of the Al(III) citrate system (közlésre előkészítve) 4. A. Bodor, I. Bányai, L. Zékány, I. Tóth: Dynamic study of the Al(III) citrate system (közlésre előkészítve) 5. I. Bányai, A. Bodor: Simple Pulse Sequence for Studying Proton Exchange on Strongly Biased Systems (közlésre előkészítve) 6. A. Bodor, I. Tóth, I. Bányai: Potentiometric and NMR Studies of the Aluminium Fluoride Oxalate System (közlésre előkészítve) 7. M. Gaspar, R. Grazina, A. Bodor, E. Farkas, M. A. Santos: Siderophore analogues: a new macrocyclic tetraamine tris(hidroxamate) ligand; synthesis and solution chemistry of the iron(iii), aluminium(iii) and copper(ii) complexes; Chem. Soc., Dalton Trans, 1999, 799. Előadások és poszterek jegyzéke 1. Bodor A., Bányai I., Tóth I.: Al(III) citrát: szerkezet és dinamika; (Komplex Kémiai Kollokvium, Kecskemét, 1997, június 22 24, előadás) 2. A. Bodor, I. Bányai, I. Tóth, L. Petterson, S. Angus Dunne, M. Hashimoto: H 2 PO 4 - MoO 2 4 -H 2 O 2 System: potentiometric and 31 P NMR study of equilibrium and dynamics; (Inorganic Reaction Mechanisms Meeting 97, Debrecen, 8 10 Jan, 1998, poszter) 3. A. Bodor, I. Tóth, L. Zékány, I. Bányai, Z. Szabó, G.T.Hefter: Al(III) F system: 19 F NMR study of equilibrium and dynamics; (Inorganic Reaction Mechanisms Meeting 97, Debrecen, 8 10 Jan, 1998, poszter) 4. A. Bodor, I. Bányai, I. Tóth: Slow dynamics in Al(III) ligand (fluoride, oxalate, citrate) systems; (COST D8 and ESF WORKSHOP on Biological and Medicinal Aspect of Metal Ion Speciation, József Attila University, Szeged, August, 1998, előadás) 7
9 5. A. Bodor, I. Tóth, I. Bányai: Equilibrium and dynamics of Al 3+ Ox 2 F system: a potentiometric and 19 F NMR study; (XXXIII International Conference on Coordination Chemistry, Florence, Italy, August 30 September 4, 1998, poszter) 6. A. Bodor, I. Bányai, I. Tóth, L. Petterson, S. Angus Dunne, M. Hashimoto: 2 H 2 PO 4 MoO 4 H 2 O 2 System: potentiometric and 31 P NMR study equilibrium and dynamics; (XXXIII International Conference on Coordination Chenmistry, Florence, Italy, August 30 September 4, 1998, poszter) 7. Bodor A., Bányai I., Tóth I.: Multinukleáris NMR alkalmazása Al(III) komplexek vizsgálatában; (EMT konferencia, Kolozsvár, 1998 november 20 21, előadás) 8. Bodor A., Bányai I., Tóth I.: Multinukleáris NMR alkalmazása alumínium fluorid és alumínium citrát rendszerek vizsgálatában; (Komplex Kémiai Munkabizottsági Ülés, Debrecen, 1999 április 16, előadás) 9. Bodor A., Bányai I., Tóth I.: Oldatszerkezet vizsgálata NMR spektroszkópiával; (Komplex Kémiai Kollokvium, Kecskemét, 2000 május 24 26, előadás) 10. A. Bodor, I. Bányai, I. Tóth: Structure Elucidation by NMR Techniques for Trinuclear Al Citrate species; (ICCC34, Edinburgh, 9 14 July, 2000, poszter) 11. I. Tóth, A. Bodor, I. Bányai, L. Zékány: Slow Dynamics in Al(III) Ligand Systems Studied by Multinuclear NMR; (ICCC34, Edinburgh, 9 14 July, 2000) 12. A. Bodor, I. Bányai, J. Glaser: Multinuclear NMR Assignation in Heterobimetallic Pt Tl Complexes; (ICCC34, Edinburgh, 9 14 July, 2000, poszter) 8
ZÁRÓJELENTÉS. A. Fém-fém kötéses vegyületek
 ZÁRÓJELENTÉS A beszámoló szigorúan vett szakmai részletei előtt talán nem felesleges egy szubjektív önértékelést előrebocsátani. A munka (OTKA támogatást is élvező) előzmények után indult, és a mostani
ZÁRÓJELENTÉS A beszámoló szigorúan vett szakmai részletei előtt talán nem felesleges egy szubjektív önértékelést előrebocsátani. A munka (OTKA támogatást is élvező) előzmények után indult, és a mostani
XXXVII. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok gyesülete songrád Megyei soportja és a Magyar Kémikusok gyesülete rendezvénye XXXVII. KÉMII LŐÓI NPOK Program és előadás-összefoglalók Szegedi kadémiai izottság Székháza Szeged, 2014.
Magyar Kémikusok gyesülete songrád Megyei soportja és a Magyar Kémikusok gyesülete rendezvénye XXXVII. KÉMII LŐÓI NPOK Program és előadás-összefoglalók Szegedi kadémiai izottság Székháza Szeged, 2014.
4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel
 4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel A kisméretű peptidek közül az oldalláncban negatív töltésű karboxilcsoportokat tartalmazó AspAsp és AspAspAsp ligandumok komplexképződését
4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel A kisméretű peptidek közül az oldalláncban negatív töltésű karboxilcsoportokat tartalmazó AspAsp és AspAspAsp ligandumok komplexképződését
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 2. előadás: 1/18 Kinetika: Kísérletekkel megállapított sebességi egyenlet(ek). A kémiai reakció makroszkópikus, fenomenológikus jellemzése. 1 Mechanizmus: Az elemi lépések
Reakciókinetika és katalízis 2. előadás: 1/18 Kinetika: Kísérletekkel megállapított sebességi egyenlet(ek). A kémiai reakció makroszkópikus, fenomenológikus jellemzése. 1 Mechanizmus: Az elemi lépések
FÉMIONOKKAL ALKOTOTT FÉM- FÉM KÖTÉST TARTALMAZÓ CIANO KOMPLEXEI SZERKEZETÉNEK ÉS FLUXIONALITÁSÁNAK VIZSGÁLATA NMR SPEKTROSZKÓPIA ALKALMAZÁSÁVAL
 Al(III)- ÉS Tl(III)- AMINO-POLIKARBOXILÁTO ÉS Tl(III) ÁTMENETI FÉMIONOKKAL ALKOTOTT FÉM- FÉM KÖTÉST TARTALMAZÓ CIANO KOMPLEXEI SZERKEZETÉNEK ÉS FLUXIONALITÁSÁNAK VIZSGÁLATA NMR SPEKTROSZKÓPIA ALKALMAZÁSÁVAL
Al(III)- ÉS Tl(III)- AMINO-POLIKARBOXILÁTO ÉS Tl(III) ÁTMENETI FÉMIONOKKAL ALKOTOTT FÉM- FÉM KÖTÉST TARTALMAZÓ CIANO KOMPLEXEI SZERKEZETÉNEK ÉS FLUXIONALITÁSÁNAK VIZSGÁLATA NMR SPEKTROSZKÓPIA ALKALMAZÁSÁVAL
Válasz. A kérdésekre, kritikai megjegyzésekre az alábbiakban válaszolok:
 Válasz Kiss Tamás egyetemi tanárnak Az Imidazolgyűrű szerepe a fémionmegkötésben: oldalláncban több donorcsoportot tartalmazó peptidek és származékaik átmenetifém komplexeinek egyensúlyi és redoxi sajátságai
Válasz Kiss Tamás egyetemi tanárnak Az Imidazolgyűrű szerepe a fémionmegkötésben: oldalláncban több donorcsoportot tartalmazó peptidek és származékaik átmenetifém komplexeinek egyensúlyi és redoxi sajátságai
Kémiai reakciók. Közös elektronpár létrehozása. Általános és szervetlen kémia 10. hét. Elızı héten elsajátítottuk, hogy.
 Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
DOKTORI (PhD) ÉRTEKEZÉS TÉZISEI. Szintay Gergely. Veszprémi Egyetem. Általános és Szervetlen Kémia Tanszék
 A CINK(II)- ÉS A RÉZ(II)- TETRAFENIL- ÉS OKTAETIL- PORFIRINEK FOTOFIZIKAI SAJÁTSÁGAI, KOMPLEXKÉPZÉSÜK ÉS KIOLTÁSUK NITROGÉN- TARTALMÚ DONOR MOLEKULÁKKAL DOKTORI (PhD) ÉRTEKEZÉS TÉZISEI Szintay Gergely
A CINK(II)- ÉS A RÉZ(II)- TETRAFENIL- ÉS OKTAETIL- PORFIRINEK FOTOFIZIKAI SAJÁTSÁGAI, KOMPLEXKÉPZÉSÜK ÉS KIOLTÁSUK NITROGÉN- TARTALMÚ DONOR MOLEKULÁKKAL DOKTORI (PhD) ÉRTEKEZÉS TÉZISEI Szintay Gergely
Eötvös Loránd Tudományegyetem, ELTE, Kémiai Intézet, egyetemi adjunktus. Korábbi munkahelyek
 Tudományos kutatói önéletrajz Személyes adatok Név: Bodor Andrea Születési hely, idő: Kolozsvár, 1972. március 30. Jelenlegi munkahely Eötvös Loránd Tudományegyetem, ELTE, Kémiai Intézet, egyetemi adjunktus.
Tudományos kutatói önéletrajz Személyes adatok Név: Bodor Andrea Születési hely, idő: Kolozsvár, 1972. március 30. Jelenlegi munkahely Eötvös Loránd Tudományegyetem, ELTE, Kémiai Intézet, egyetemi adjunktus.
Anyagvizsgálati módszerek Elektroanalitika. Anyagvizsgálati módszerek
 Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Mágneses módszerek a mőszeres analitikában
 Mágneses módszerek a mőszeres analitikában NMR, ESR: mágneses momentummal rendelkezı anyagok minıségi és mennyiségi meghatározására alkalmas analitikai módszer Atommag spin állapotok közötti energiaátmenetek:
Mágneses módszerek a mőszeres analitikában NMR, ESR: mágneses momentummal rendelkezı anyagok minıségi és mennyiségi meghatározására alkalmas analitikai módszer Atommag spin állapotok közötti energiaátmenetek:
XXXVI. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVI. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVI. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
1D multipulzus NMR kísérletek
 D multipulzus NMR kísérletek Rohonczy János ELTE, Szervetlen Kémia Tanszék Modern szerkezetkutatási módszerek elıadás 202. . Protonlecsatolt heteronukleáris mérések Elv 3 C mag detektálása alatt a protoncsatornán
D multipulzus NMR kísérletek Rohonczy János ELTE, Szervetlen Kémia Tanszék Modern szerkezetkutatási módszerek elıadás 202. . Protonlecsatolt heteronukleáris mérések Elv 3 C mag detektálása alatt a protoncsatornán
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén
 ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
Közös elektronpár létrehozása
 Kémiai reakciók 10. hét a reagáló részecskék között közös elektronpár létrehozása valósul meg sav-bázis reakciók komplexképződés elektronátadás és átvétel történik redoxi reakciók Közös elektronpár létrehozása
Kémiai reakciók 10. hét a reagáló részecskék között közös elektronpár létrehozása valósul meg sav-bázis reakciók komplexképződés elektronátadás és átvétel történik redoxi reakciók Közös elektronpár létrehozása
a) H 3 PO 4 pk a értékeinek meghatározására, b) üdítőital foszfor tartalmának meghatározására, c) pirofoszfát bomlásának követésére Dr.
 31 P NMR spektroszkópia alkalmazása: a) H 3 PO 4 pk a értékeinek meghatározására, b) üdítőital foszfor tartalmának meghatározására, c) pirofoszfát bomlásának követésére Dr. Bodor Andrea Bevezetés: A 31
31 P NMR spektroszkópia alkalmazása: a) H 3 PO 4 pk a értékeinek meghatározására, b) üdítőital foszfor tartalmának meghatározására, c) pirofoszfát bomlásának követésére Dr. Bodor Andrea Bevezetés: A 31
Készítette: NÁDOR JUDIT. Témavezető: Dr. HOMONNAY ZOLTÁN. ELTE TTK, Analitikai Kémia Tanszék 2010
 Készítette: NÁDOR JUDIT Témavezető: Dr. HOMONNAY ZOLTÁN ELTE TTK, Analitikai Kémia Tanszék 2010 Bevezetés, célkitűzés Mössbauer-spektroszkópia Kísérleti előzmények Mérések és eredmények Összefoglalás EDTA
Készítette: NÁDOR JUDIT Témavezető: Dr. HOMONNAY ZOLTÁN ELTE TTK, Analitikai Kémia Tanszék 2010 Bevezetés, célkitűzés Mössbauer-spektroszkópia Kísérleti előzmények Mérések és eredmények Összefoglalás EDTA
Al-Mg-Si háromalkotós egyensúlyi fázisdiagram közelítő számítása
 l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
1) CO 2 hidrolízise a) semleges és b) bázikus körülmények között.
 A 20072011 években az OTKA támogatásával a következő témák indultak el: (A jelen felsorolás eltér attól a csoportosítástól, amit a pályázat megírásakor alkalmaztam, mivel a témák jobban áttekinthetők így.
A 20072011 években az OTKA támogatásával a következő témák indultak el: (A jelen felsorolás eltér attól a csoportosítástól, amit a pályázat megírásakor alkalmaztam, mivel a témák jobban áttekinthetők így.
4.3. Az AcLysSerProValValGluGly heptapeptid Al(III)-kötő sajátságának jellemzése
 4.3. Az AcLysProValValGly heptapeptid Al(III)-kötő sajátságának jellemzése Az Al(III)fehérje kölcsönhatás megismerése céljából olyan neurofilamentum peptidfragmenst vizsgáltunk, mely az oldalláncban oxigén
4.3. Az AcLysProValValGly heptapeptid Al(III)-kötő sajátságának jellemzése Az Al(III)fehérje kölcsönhatás megismerése céljából olyan neurofilamentum peptidfragmenst vizsgáltunk, mely az oldalláncban oxigén
AZ ACETON ÉS AZ ACETONILGYÖK NÉHÁNY LÉGKÖRKÉMIAILAG FONTOS ELEMI REAKCIÓJÁNAK KINETIKAI VIZSGÁLATA
 Budapesti Műszaki és Gazdaságtudományi Egyetem, Fizikai Kémia Tanszék Ph.D. értekezés tézisei AZ ACETON ÉS AZ ACETONILGYÖK NÉHÁNY LÉGKÖRKÉMIAILAG FONTOS ELEMI REAKCIÓJÁNAK KINETIKAI VIZSGÁLATA Készítette
Budapesti Műszaki és Gazdaságtudományi Egyetem, Fizikai Kémia Tanszék Ph.D. értekezés tézisei AZ ACETON ÉS AZ ACETONILGYÖK NÉHÁNY LÉGKÖRKÉMIAILAG FONTOS ELEMI REAKCIÓJÁNAK KINETIKAI VIZSGÁLATA Készítette
Szerkesztették Laufer Noémi SZTE TTIK Alkalmazott és Környezeti Kémiai Tanszék Endrődi Balázs SZTE TTIK Fizikai Kémiai és Anyagtudományi Tanszék
 Szerkesztették Laufer Noémi SZTE TTIK Alkalmazott és Környezeti Kémiai Tanszék Endrődi Balázs SZTE TTIK Fizikai Kémiai és Anyagtudományi Tanszék ISBN 978 963 315 06 7 KALCIUM-HIDROXID OLDHATÓSÁGA LÚGOS
Szerkesztették Laufer Noémi SZTE TTIK Alkalmazott és Környezeti Kémiai Tanszék Endrődi Balázs SZTE TTIK Fizikai Kémiai és Anyagtudományi Tanszék ISBN 978 963 315 06 7 KALCIUM-HIDROXID OLDHATÓSÁGA LÚGOS
XXXVII. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVII. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVII. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Kontakt korrózió vizsgálata
 Kontakt korrózió vizsgálata Haraszti Ferenc 1, Kovács Tünde 1 1 Óbudai Egyetem Bánki Donát Gépész és Biztonságtechnikai Mérnöki Kar, Budapest, Népszínház u. 8, Magyarország Abstract. A korrózió összetett,
Kontakt korrózió vizsgálata Haraszti Ferenc 1, Kovács Tünde 1 1 Óbudai Egyetem Bánki Donát Gépész és Biztonságtechnikai Mérnöki Kar, Budapest, Népszínház u. 8, Magyarország Abstract. A korrózió összetett,
Radioaktív nyomjelzés
 Radioaktív nyomjelzés A radioaktív nyomjelzés alapelve Kémiai indikátorok: ugyanazoknak a követelményeknek kell eleget tenniük, mint az indikátoroknak általában: jelezniük kell valamely elemnek ill. vegyületnek
Radioaktív nyomjelzés A radioaktív nyomjelzés alapelve Kémiai indikátorok: ugyanazoknak a követelményeknek kell eleget tenniük, mint az indikátoroknak általában: jelezniük kell valamely elemnek ill. vegyületnek
Mágneses módszerek a műszeres analitikában
 Mágneses módszerek a műszeres analitikában NMR, ESR: mágneses momentummal rendelkező anyagok minőségi és mennyiségi meghatározására alkalmas Atommag spin állapotok közötti energiaátmenetek: NMR (magmágneses
Mágneses módszerek a műszeres analitikában NMR, ESR: mágneses momentummal rendelkező anyagok minőségi és mennyiségi meghatározására alkalmas Atommag spin állapotok közötti energiaátmenetek: NMR (magmágneses
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Alkalmazott spektroszkópia
 Alkalmazott spektroszkópia 009 Bányai István MR és a fémionok: koordinációs kémiai alkalmazások Bányai István Debreceni Egyetem TEK Kolloid- és Környezetkémiai Tanszék A mágnesség A mágneses erő: F pp
Alkalmazott spektroszkópia 009 Bányai István MR és a fémionok: koordinációs kémiai alkalmazások Bányai István Debreceni Egyetem TEK Kolloid- és Környezetkémiai Tanszék A mágnesség A mágneses erő: F pp
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
Pt Tl fém fém kötést tartalmazó komplexek kinetikai vizsgálata, a Tl(CN) 3 és Tl(CN) 4 reaktánsok szerkezeti jellemzése szilárd fázisban
 Pt Tl fém fém kötést tartalmazó komplexek kinetikai vizsgálata, a Tl(CN) 3 és Tl(CN) 4 reaktánsok szerkezeti jellemzése szilárd fázisban Kinetics and Mechanisms of Platinum Thallium Bonded Complexes and
Pt Tl fém fém kötést tartalmazó komplexek kinetikai vizsgálata, a Tl(CN) 3 és Tl(CN) 4 reaktánsok szerkezeti jellemzése szilárd fázisban Kinetics and Mechanisms of Platinum Thallium Bonded Complexes and
SZAKMAI ÖNÉLETRAJZ Mészáros János Péter
 Születési hely, idő: Szeged, 1993.12.10. Elérhetőség: 6720 Szeged, Dóm tér 7. Telefonszám: +36-62-54-4336 E-mail: meszaros.janos@chem.u-szeged.hu SZAKMAI ÖNÉLETRAJZ Mészáros János Péter MTMT adatbázis:
Születési hely, idő: Szeged, 1993.12.10. Elérhetőség: 6720 Szeged, Dóm tér 7. Telefonszám: +36-62-54-4336 E-mail: meszaros.janos@chem.u-szeged.hu SZAKMAI ÖNÉLETRAJZ Mészáros János Péter MTMT adatbázis:
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján.
 A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
Kémiai reakciók mechanizmusa számítógépes szimulációval
 Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
A SZTE KDI képzési terve
 A SZTE KDI képzési terve (2016. szeptember 1 előtt indult képzésre) Doktori képzési/kutatási programok: 1. Analitikai kémia 2. Bioorganikus kémia 3. Elméleti kémia 4. Fizikai Kémia 5. Katalízis, kolloidika,
A SZTE KDI képzési terve (2016. szeptember 1 előtt indult képzésre) Doktori képzési/kutatási programok: 1. Analitikai kémia 2. Bioorganikus kémia 3. Elméleti kémia 4. Fizikai Kémia 5. Katalízis, kolloidika,
Mi mindenről tanúskodik a Me-OH néhány NMR spektruma
 Mi mindenről tanúskodik a Me-OH néhány NMR spektruma lcélok és fogalmak: l- az NMR-rezonancia frekvencia (jel), a kémiai környezete, a kémiai eltolódás, l- az 1 H-NMR spektrum, l- az -OH és a -CH 3 csoportokban
Mi mindenről tanúskodik a Me-OH néhány NMR spektruma lcélok és fogalmak: l- az NMR-rezonancia frekvencia (jel), a kémiai környezete, a kémiai eltolódás, l- az 1 H-NMR spektrum, l- az -OH és a -CH 3 csoportokban
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
1. feladat Összesen: 15 pont. 2. feladat Összesen: 10 pont
 1. feladat Összesen: 15 pont Vizsgálja meg a hidrogén-klorid (vagy vizes oldata) reakciót különböző szervetlen és szerves anyagokkal! Ha nem játszódik le reakció, akkor ezt írja be! protonátmenettel járó
1. feladat Összesen: 15 pont Vizsgálja meg a hidrogén-klorid (vagy vizes oldata) reakciót különböző szervetlen és szerves anyagokkal! Ha nem játszódik le reakció, akkor ezt írja be! protonátmenettel járó
Kutatási beszámoló 2006
 Kutatási beszámoló 2006 Bevezetés Az energetikai ipar, közlekedés és a gazdaság más területei túlnyomórészt szerves anyagok, általában szénhidrogének elégetésével fedezik energia-szükségleteiket. Ezért
Kutatási beszámoló 2006 Bevezetés Az energetikai ipar, közlekedés és a gazdaság más területei túlnyomórészt szerves anyagok, általában szénhidrogének elégetésével fedezik energia-szükségleteiket. Ezért
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
Platina-alkil-komplexek elemi reakcióinak vizsgálata és alkalmazása hidroformilezési reakciókban. Jánosi László
 latina-alkil-komplexek elemi reakcióinak vizsgálata és alkalmazása hidroformilezési reakciókban hd értekezés tézisei Jánosi László Témavezető: Dr. Kollár László egyetemi tanár écsi Tudományegyetem Természettudományi
latina-alkil-komplexek elemi reakcióinak vizsgálata és alkalmazása hidroformilezési reakciókban hd értekezés tézisei Jánosi László Témavezető: Dr. Kollár László egyetemi tanár écsi Tudományegyetem Természettudományi
Modern Fizika Labor. 12. Infravörös spektroszkópia. Fizika BSc. A mérés dátuma: okt. 04. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
A dinamikai viselkedés hőmérséklet-függése és hőmérséklet-kompenzáció oszcillációs kémiai reakciókban. Doktori (PhD) értekezés tézisei.
 A dinamikai viselkedés hőmérsékletfüggése és hőmérsékletkompenzáció oszcillációs kémiai reakciókban Doktori (PhD) értekezés tézisei Kovács Klára Temperature dependence of the dynamical behavior and temperaturecompensation
A dinamikai viselkedés hőmérsékletfüggése és hőmérsékletkompenzáció oszcillációs kémiai reakciókban Doktori (PhD) értekezés tézisei Kovács Klára Temperature dependence of the dynamical behavior and temperaturecompensation
Kémiai tantárgy középszintű érettségi témakörei
 Kémiai tantárgy középszintű érettségi témakörei Csongrádi Batsányi János Gimnázium, Szakgimnázium és Kollégium Összeállította: Baricsné Kapus Éva, Tábori Levente 1) témakör Mendgyelejev féle periódusos
Kémiai tantárgy középszintű érettségi témakörei Csongrádi Batsányi János Gimnázium, Szakgimnázium és Kollégium Összeállította: Baricsné Kapus Éva, Tábori Levente 1) témakör Mendgyelejev féle periódusos
Vezető kutató: Farkas Viktor OTKA azonosító: 71817 típus: PD
 Vezető kutató: Farkas Viktor TKA azonosító: 71817 típus: PD Szakmai beszámoló A pályázat kutatási tervében kiroptikai-spektroszkópiai mérések illetve kromatográfiás vizsgálatok, ezen belül királis HPLC-oszloptöltet
Vezető kutató: Farkas Viktor TKA azonosító: 71817 típus: PD Szakmai beszámoló A pályázat kutatási tervében kiroptikai-spektroszkópiai mérések illetve kromatográfiás vizsgálatok, ezen belül királis HPLC-oszloptöltet
Szacharóz OH HO O O OH HO O OH HO OH HO 1
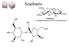 Szacharóz 1 A jelek átfedése miatt oldószer váltás DMS helyett D2 Measured by... Evaluated by... NMR-01 Bruker Avance-500 103.59 92.08 81.28 DEPTq 300K ns=1k D2 115 110 105 100 95 90 85 80 75 70 65 60
Szacharóz 1 A jelek átfedése miatt oldószer váltás DMS helyett D2 Measured by... Evaluated by... NMR-01 Bruker Avance-500 103.59 92.08 81.28 DEPTq 300K ns=1k D2 115 110 105 100 95 90 85 80 75 70 65 60
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Pufferrendszerek vizsgálata
 Pufferrendszerek vizsgálata Ecetsav/nátrium-acetát pufferoldat, ammonia/ammonium-klorid, ill. (nátrium/kálium) dihidrogénfoszfát/hidrogénfoszfát pufferrendszerek vizsgálata. Oldatkészítés: a gyakorlatvezető
Pufferrendszerek vizsgálata Ecetsav/nátrium-acetát pufferoldat, ammonia/ammonium-klorid, ill. (nátrium/kálium) dihidrogénfoszfát/hidrogénfoszfát pufferrendszerek vizsgálata. Oldatkészítés: a gyakorlatvezető
C-Glikozil- és glikozilamino-heterociklusok szintézise
 Egyetemi doktori (Ph.D.) értekezés tézisei C-Glikozil- és glikozilamino-heterociklusok szintézise Szőcs Béla Témavezető: Vágvölgyiné Dr. Tóth Marietta DEBRECENI EGYETEM Kémiai Doktori Iskola Debrecen,
Egyetemi doktori (Ph.D.) értekezés tézisei C-Glikozil- és glikozilamino-heterociklusok szintézise Szőcs Béla Témavezető: Vágvölgyiné Dr. Tóth Marietta DEBRECENI EGYETEM Kémiai Doktori Iskola Debrecen,
CO 2 aktiválás - a hidrogén tárolásban
 CO 2 aktiválás a hidrogén tárolásban PAPP Gábor 1, HORVÁTH Henrietta 1, PURGEL Mihály 1, BARANYI Attila 2, JOÓ Ferenc 1,2 1 MTADE Homogén Katalízis és Reakciómechanizmusok Kutatócsoport, 4032 Debrecen,
CO 2 aktiválás a hidrogén tárolásban PAPP Gábor 1, HORVÁTH Henrietta 1, PURGEL Mihály 1, BARANYI Attila 2, JOÓ Ferenc 1,2 1 MTADE Homogén Katalízis és Reakciómechanizmusok Kutatócsoport, 4032 Debrecen,
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
VILÁGÍTÓ GYÓGYHATÁSÚ ALKALOIDOK
 VILÁGÍTÓ GYÓGYHATÁSÚ ALKALIDK Biczók László, Miskolczy Zsombor, Megyesi Mónika, Harangozó József Gábor MTA Természettudományi Kutatóközpont Anyag- és Környezetkémiai Intézet Hordozóanyaghoz kötődés fluoreszcenciás
VILÁGÍTÓ GYÓGYHATÁSÚ ALKALIDK Biczók László, Miskolczy Zsombor, Megyesi Mónika, Harangozó József Gábor MTA Természettudományi Kutatóközpont Anyag- és Környezetkémiai Intézet Hordozóanyaghoz kötődés fluoreszcenciás
I. Az NMR spektrométer
 I. Az NMR spektrométer I. Az NMR spektrométer fő részei Rádióelektronikai konzol Munkaállomás Mágnes 2 I. Ultra-árnyékolt mágnesek Kettős szupravezető tekerccsel csökkenthető a mágnes szórt tere. Kisebb
I. Az NMR spektrométer I. Az NMR spektrométer fő részei Rádióelektronikai konzol Munkaállomás Mágnes 2 I. Ultra-árnyékolt mágnesek Kettős szupravezető tekerccsel csökkenthető a mágnes szórt tere. Kisebb
XL. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XL. KÉMIAI ELŐADÓI NAPOK Szegedi Akadémiai Bizottság Székháza Szeged, 2017. október 16-18. Szerkesztették:
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XL. KÉMIAI ELŐADÓI NAPOK Szegedi Akadémiai Bizottság Székháza Szeged, 2017. október 16-18. Szerkesztették:
Az SZTE KDI képzési terve
 Az SZTE KDI képzési terve Doktori képzési/kutatási programok: 1. Analitikai kémia 2. Bioorganikus kémia 3. Elméleti kémia 4. Fizikai Kémia 5. Katalízis, kolloidika, felület- és anyagtudomány 6. Komplex
Az SZTE KDI képzési terve Doktori képzési/kutatási programok: 1. Analitikai kémia 2. Bioorganikus kémia 3. Elméleti kémia 4. Fizikai Kémia 5. Katalízis, kolloidika, felület- és anyagtudomány 6. Komplex
FELADATLISTA TÉMAKÖRÖK, ILLETVE KÉPESSÉGEK SZERINT
 FELADATLISTA TÉMAKÖRÖK, ILLETVE KÉPESSÉGEK SZERINT A feladatok kódját a Bevezetésben bemutatott tananyagtartalom- és képességmátrix alapján határoztuk meg. A feladat kódja a következőképpen épül fel: évfolyam/témakör1-témakör2/képesség1-képesség2/sorszám
FELADATLISTA TÉMAKÖRÖK, ILLETVE KÉPESSÉGEK SZERINT A feladatok kódját a Bevezetésben bemutatott tananyagtartalom- és képességmátrix alapján határoztuk meg. A feladat kódja a következőképpen épül fel: évfolyam/témakör1-témakör2/képesség1-képesség2/sorszám
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
ÁLTALÁNOS ÉS SZERVETLEN KÉMIA SZIGORLATI VIZSGAKÉRDÉSEK 2010/2011 TANÉVBEN ÁLTALÁNOS KÉMIA
 ÁLTALÁNOS ÉS SZERVETLEN KÉMIA SZIGORLATI VIZSGAKÉRDÉSEK 2010/2011 TANÉVBEN ÁLTALÁNOS KÉMIA 1. Kémiai alapfogalmak: - A kémia alaptörvényei ( a tömegmegmaradás törvénye, állandó tömegarányok törvénye) -
ÁLTALÁNOS ÉS SZERVETLEN KÉMIA SZIGORLATI VIZSGAKÉRDÉSEK 2010/2011 TANÉVBEN ÁLTALÁNOS KÉMIA 1. Kémiai alapfogalmak: - A kémia alaptörvényei ( a tömegmegmaradás törvénye, állandó tömegarányok törvénye) -
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
Hogyan bírhatjuk szóra a molekulákat, avagy mi is az a spektroszkópia?
 Hogyan bírhatjuk szóra a molekulákat, avagy mi is az a spektroszkópia? Prof. Túri László (ELTE, Kémiai Intézet) turi@chem.elte.hu 2012. november 19. Szent László Gimnázium Önképzőkör 1 Kapcsolódási pontok
Hogyan bírhatjuk szóra a molekulákat, avagy mi is az a spektroszkópia? Prof. Túri László (ELTE, Kémiai Intézet) turi@chem.elte.hu 2012. november 19. Szent László Gimnázium Önképzőkör 1 Kapcsolódási pontok
Elektro-analitikai számítási feladatok 1. Potenciometria
 Elektro-analitikai számítási feladatok 1. Potenciometria 1. Vas-só részlegesen oxidált oldatába Pt elektródot merítettünk. Ennek az elektródnak a potenciálját egy telített kalomel elektródhoz képest mérjük
Elektro-analitikai számítási feladatok 1. Potenciometria 1. Vas-só részlegesen oxidált oldatába Pt elektródot merítettünk. Ennek az elektródnak a potenciálját egy telített kalomel elektródhoz képest mérjük
Koordinációs vegyületek (komplexek)
 Koordinációs vegyületek (komplexek) ML n M: központi ion/atom L: ligandum n: koordinációs szám Komplexek 1. Nevezéktan 2. Csoportosítás 3. A komplexképzıdés ismérvei 4. Koordinációs szám, geometria 5.
Koordinációs vegyületek (komplexek) ML n M: központi ion/atom L: ligandum n: koordinációs szám Komplexek 1. Nevezéktan 2. Csoportosítás 3. A komplexképzıdés ismérvei 4. Koordinációs szám, geometria 5.
Bevezetés és célkitűzések
 Bevezetés és célkitűzések Hosszú időn keresztül az alumínium(iii)iont az emberi szervezet számára ártalmatlannak tekintették, hiszen a természetben rosszul oldódó hidroxidok, szilikátok, foszfátok formájában
Bevezetés és célkitűzések Hosszú időn keresztül az alumínium(iii)iont az emberi szervezet számára ártalmatlannak tekintették, hiszen a természetben rosszul oldódó hidroxidok, szilikátok, foszfátok formájában
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 5. Szén-szén többszörös kötések kialakítása: alkének Kovács Lajos 1 Alkének el állítása X Y FGI C C C C C C C C = = a d C O + X C X C X = PR 3 P(O)(OR) 2 SiR 3 SO 2 R
Szerves kémiai szintézismódszerek 5. Szén-szén többszörös kötések kialakítása: alkének Kovács Lajos 1 Alkének el állítása X Y FGI C C C C C C C C = = a d C O + X C X C X = PR 3 P(O)(OR) 2 SiR 3 SO 2 R
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
b./ Hány gramm szénatomban van ugyanannyi proton, mint 8g oxigénatomban? Hogyan jelöljük ezeket az anyagokat? Egyforma-e minden atom a 8g szénben?
 1. Az atommag. a./ Az atommag és az atom méretének, tömegének és töltésének összehasonlítása, a nukleonok jellemzése, rendszám, tömegszám, izotópok, nuklidok, jelölések. b./ Jelöld a Ca atom 20 neutront
1. Az atommag. a./ Az atommag és az atom méretének, tömegének és töltésének összehasonlítása, a nukleonok jellemzése, rendszám, tömegszám, izotópok, nuklidok, jelölések. b./ Jelöld a Ca atom 20 neutront
Orvosi képalkotásban használt vegyületek szerkezetének és dinamikájának vizsgálata
 Orvosi képalkotásban használt vegyületek szerkezetének és dinamikájának vizsgálata Doktori (PhD) értekezés tézisei Horváthné Csajbók Éva Témavezető: Dr. Bányai István Debreceni Egyetem Debrecen, 2005.
Orvosi képalkotásban használt vegyületek szerkezetének és dinamikájának vizsgálata Doktori (PhD) értekezés tézisei Horváthné Csajbók Éva Témavezető: Dr. Bányai István Debreceni Egyetem Debrecen, 2005.
PANNON EGYETEM. 2,3-DIHIDRO-2,2,2-TRIFENIL-FENANTRO-[9,10-d]-1,3,2λ 5 -OXAZAFOSZFOL KIALAKULÁSA ÉS REAKCIÓJA SZÉN-DIOXIDDAL ÉS DIOXIGÉNNEL
![PANNON EGYETEM. 2,3-DIHIDRO-2,2,2-TRIFENIL-FENANTRO-[9,10-d]-1,3,2λ 5 -OXAZAFOSZFOL KIALAKULÁSA ÉS REAKCIÓJA SZÉN-DIOXIDDAL ÉS DIOXIGÉNNEL PANNON EGYETEM. 2,3-DIHIDRO-2,2,2-TRIFENIL-FENANTRO-[9,10-d]-1,3,2λ 5 -OXAZAFOSZFOL KIALAKULÁSA ÉS REAKCIÓJA SZÉN-DIOXIDDAL ÉS DIOXIGÉNNEL](/thumbs/36/17536851.jpg) PA EGYETEM 2,3-DIHID-2,2,2-TIFEIL-FEAT-[9,10-d]-1,3,2λ 5 -XAZAFSZFL KIALAKULÁSA ÉS EAKCIÓJA SZÉ-DIXIDDAL ÉS DIXIGÉEL Doktori (Ph.D) értekezés tézisei Készítette: Bors István okleveles kémia-környezettan
PA EGYETEM 2,3-DIHID-2,2,2-TIFEIL-FEAT-[9,10-d]-1,3,2λ 5 -XAZAFSZFL KIALAKULÁSA ÉS EAKCIÓJA SZÉ-DIXIDDAL ÉS DIXIGÉEL Doktori (Ph.D) értekezés tézisei Készítette: Bors István okleveles kémia-környezettan
Kinetika. Általános Kémia, kinetika Dia: 1 /53
 Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
6 Ionszelektív elektródok. elektródokat kiterjedten alkalmazzák a klinikai gyakorlatban: az automata analizátorokban
 6. Szelektivitási együttható meghatározása 6.1. Bevezetés Az ionszelektív elektródok olyan potenciometriás érzékelők, melyek valamely ion aktivitásának többé-kevésbé szelektív meghatározását teszik lehetővé.
6. Szelektivitási együttható meghatározása 6.1. Bevezetés Az ionszelektív elektródok olyan potenciometriás érzékelők, melyek valamely ion aktivitásának többé-kevésbé szelektív meghatározását teszik lehetővé.
Név: Pontszám: / 3 pont. 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
 Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
8. osztály 2 Hevesy verseny, megyei forduló, 2008.
 8. osztály 2 Hevesy verseny, megyei forduló, 2008. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
8. osztály 2 Hevesy verseny, megyei forduló, 2008. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
7. Kémia egyenletek rendezése, sztöchiometria
 7. Kémia egyenletek rendezése, sztöchiometria A kémiai egyenletírás szabályai (ajánlott irodalom: Villányi Attila: Ötösöm lesz kémiából, Példatár) 1.tömegmegmaradás, elemek átalakíthatatlansága az egyenlet
7. Kémia egyenletek rendezése, sztöchiometria A kémiai egyenletírás szabályai (ajánlott irodalom: Villányi Attila: Ötösöm lesz kémiából, Példatár) 1.tömegmegmaradás, elemek átalakíthatatlansága az egyenlet
Feladatok haladóknak
 Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Feladatok A formai követelményeknek megfelelő dolgozatokat a nevezési lappal együtt
Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Feladatok A formai követelményeknek megfelelő dolgozatokat a nevezési lappal együtt
9. évfolyam II. félév 2. dolgozat B csoport. a. Arrheneus szerint bázisok azok a vegyületek, amelyek... b. Arrheneus szerint a sók...
 9. évfolyam II. félév 2. dolgozat B csoport 1. Egészítsd ki az alábbi mondatokat! a. Arrheneus szerint bázisok azok a vegyületek, amelyek... b. Arrheneus szerint a sók.... c. Az erős savak vízben........
9. évfolyam II. félév 2. dolgozat B csoport 1. Egészítsd ki az alábbi mondatokat! a. Arrheneus szerint bázisok azok a vegyületek, amelyek... b. Arrheneus szerint a sók.... c. Az erős savak vízben........
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1997
 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1997 JAVÍTÁSI ÚTMUTATÓ I. A HIDROGÉN, A HIDRIDEK 1s 1, EN=2,1; izotópok:,, deutérium,, trícium. Kétatomos molekula, H 2, apoláris. Szobahőmérsékleten
1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1997 JAVÍTÁSI ÚTMUTATÓ I. A HIDROGÉN, A HIDRIDEK 1s 1, EN=2,1; izotópok:,, deutérium,, trícium. Kétatomos molekula, H 2, apoláris. Szobahőmérsékleten
KÉMIA ÍRÁSBELI ÉRETTSÉGI-FELVÉTELI FELADATOK (1997)
 KÉMIA ÍRÁSBELI ÉRETTSÉGI-FELVÉTELI FELADATOK (1997) MEGOLDÁSOK I. 1. A hidrogén, a hidridek 1s 1 EN=2,1 izotópok: 1 1 H, 2 1 H deutérium 1 H trícium, sajátosságai eltérőek A trícium,- atommagja nagy neutrontartalma
KÉMIA ÍRÁSBELI ÉRETTSÉGI-FELVÉTELI FELADATOK (1997) MEGOLDÁSOK I. 1. A hidrogén, a hidridek 1s 1 EN=2,1 izotópok: 1 1 H, 2 1 H deutérium 1 H trícium, sajátosságai eltérőek A trícium,- atommagja nagy neutrontartalma
Modern Fizika Labor Fizika BSC
 Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. május 4. A mérés száma és címe: 9. Röntgen-fluoreszencia analízis Értékelés: A beadás dátuma: 2009. május 13. A mérést végezte: Márton Krisztina Zsigmond
Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. május 4. A mérés száma és címe: 9. Röntgen-fluoreszencia analízis Értékelés: A beadás dátuma: 2009. május 13. A mérést végezte: Márton Krisztina Zsigmond
Általános kémia vizsgakérdések
 Általános kémia vizsgakérdések 1. Mutassa be egy atom felépítését! 2. Mivel magyarázza egy atom semlegességét? 3. Adja meg a rendszám és a tömegszám fogalmát! 4. Mit nevezünk elemnek és vegyületnek? 5.
Általános kémia vizsgakérdések 1. Mutassa be egy atom felépítését! 2. Mivel magyarázza egy atom semlegességét? 3. Adja meg a rendszám és a tömegszám fogalmát! 4. Mit nevezünk elemnek és vegyületnek? 5.
Reakciókinetika és katalízis
 Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Fizikai kémia 2 Reakciókinetika házi feladatok 2016 ősz
 Fizikai kémia 2 Reakciókinetika házi feladatok 2016 ősz A házi feladatok beadhatóak vagy papír alapon (ez a preferált), vagy e-mail formájában is az rkinhazi@gmail.com címre. E-mail esetén ügyeljetek a
Fizikai kémia 2 Reakciókinetika házi feladatok 2016 ősz A házi feladatok beadhatóak vagy papír alapon (ez a preferált), vagy e-mail formájában is az rkinhazi@gmail.com címre. E-mail esetén ügyeljetek a
Többértékű savak és bázisok Többértékű savnak/lúgnak azokat az oldatokat nevezzük, amelyek több protont képesek leadni/felvenni.
 ELEKTROLIT EGYENSÚLYOK : ph SZÁMITÁS Általános ismeretek A savak vizes oldatban protont adnak át a vízmolekuláknak és így megnövelik az oldat H + (pontosabban oxónium - H 3 O + ) ion koncentrációját. Erős
ELEKTROLIT EGYENSÚLYOK : ph SZÁMITÁS Általános ismeretek A savak vizes oldatban protont adnak át a vízmolekuláknak és így megnövelik az oldat H + (pontosabban oxónium - H 3 O + ) ion koncentrációját. Erős
Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása
 Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Etán- és propánvázon szubsztituált oligofoszfonátok és oligofoszfono-karboxilátok protonálódásának és fémkomplexeinek vizsgálata
 Doktori (hd) értekezés tézisei Etán- és propánvázon szubsztituált oligofoszfonátok és oligofoszfono-karboxilátok protonálódásának és fémkomplexeinek vizsgálata Bogdán silla Eötvös Loránd Tudományegyetem,
Doktori (hd) értekezés tézisei Etán- és propánvázon szubsztituált oligofoszfonátok és oligofoszfono-karboxilátok protonálódásának és fémkomplexeinek vizsgálata Bogdán silla Eötvös Loránd Tudományegyetem,
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
TALAJVÉDELEM XI. A szennyezőanyagok terjedését, talaj/talajvízbeli viselkedését befolyásoló paraméterek
 TALAJVÉDELEM XI. A szennyezőanyagok terjedését, talaj/talajvízbeli viselkedését befolyásoló paraméterek A talajszennyezés csökkenése/csökkentése bekövetkezhet Természetes úton Mesterséges úton (kármentesítés,
TALAJVÉDELEM XI. A szennyezőanyagok terjedését, talaj/talajvízbeli viselkedését befolyásoló paraméterek A talajszennyezés csökkenése/csökkentése bekövetkezhet Természetes úton Mesterséges úton (kármentesítés,
évi OTKA jelentés Vezető kutató: Brücher Ernő K-69098
 2007 2010 évi OTKA jelentés Vezető kutató: Brücher Ernő K-69098 LATAIDA(III)-DIETILÉTRIAMI-PETAACETÁT SZÁRMAZÉKOKKAL KÉPZŐDŐ KOMPLEXEK LIGADUMCSERE REAKCIÓIAK KIETIKÁJA: A EMKOVALES KÖLCSÖHATÁSOK SZEREPE
2007 2010 évi OTKA jelentés Vezető kutató: Brücher Ernő K-69098 LATAIDA(III)-DIETILÉTRIAMI-PETAACETÁT SZÁRMAZÉKOKKAL KÉPZŐDŐ KOMPLEXEK LIGADUMCSERE REAKCIÓIAK KIETIKÁJA: A EMKOVALES KÖLCSÖHATÁSOK SZEREPE
Spektroszkópiai módszerek 2.
 Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam
 A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam A feladatok megoldásához csak
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam A feladatok megoldásához csak
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS
 Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
XI. Fémorganikus fotokémia. A cisz-cr(co) 4 (CH 3 CN) 2 előállítása és reaktivitása
 XI. Fémorganikus fotokémia. A cisz-cr(co) 4 (CH 3 CN) 2 előállítása és reaktivitása 1. BEVEZETÉS Az átmenetifémek karbonil komplexeinek egyik legfontosabb reakciója a ligandum-helyettesítési reakció. A
XI. Fémorganikus fotokémia. A cisz-cr(co) 4 (CH 3 CN) 2 előállítása és reaktivitása 1. BEVEZETÉS Az átmenetifémek karbonil komplexeinek egyik legfontosabb reakciója a ligandum-helyettesítési reakció. A
A hőterjedés dinamikája vékony szilikon rétegekben. Gambár Katalin, Márkus Ferenc. Tudomány Napja 2012 Gábor Dénes Főiskola
 A hőterjedés dinamikája vékony szilikon rétegekben Gambár Katalin, Márkus Ferenc Tudomány Napja 2012 Gábor Dénes Főiskola Miről szeretnék beszélni: A kutatás motivációi A fizikai egyenletek (elméleti modellek)
A hőterjedés dinamikája vékony szilikon rétegekben Gambár Katalin, Márkus Ferenc Tudomány Napja 2012 Gábor Dénes Főiskola Miről szeretnék beszélni: A kutatás motivációi A fizikai egyenletek (elméleti modellek)
XXXVII. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVII. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVII. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
8. Egyszerû tesztek sûrûség funkcionál módszerek minõsítésére
 8. Egyszerû tesztek sûrûség funkcionál módszerek minõsítésére XX. Csonka, G. I., Nguyen, N. A., Kolossváry, I., Simple tests for density functionals, J. Comput. Chem. 18 (1997) 1534. XXII. Csonka, G. I.,
8. Egyszerû tesztek sûrûség funkcionál módszerek minõsítésére XX. Csonka, G. I., Nguyen, N. A., Kolossváry, I., Simple tests for density functionals, J. Comput. Chem. 18 (1997) 1534. XXII. Csonka, G. I.,
ELEKTROKÉMIA. - elektrolitokban: ionok irányított mozgása. Elektrolízis: elektromos áram által előidézett kémiai átalakulás
 ELEKTROKÉMIA 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
ELEKTROKÉMIA 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
5. Laboratóriumi gyakorlat
 5. Laboratóriumi gyakorlat HETEROGÉN KÉMIAI REAKCIÓ SEBESSÉGÉNEK VIZSGÁLATA A CO 2 -nak vízben történő oldódása és az azt követő egyensúlyra vezető kémiai reakció az alábbi reakcióegyenlettel írható le:
5. Laboratóriumi gyakorlat HETEROGÉN KÉMIAI REAKCIÓ SEBESSÉGÉNEK VIZSGÁLATA A CO 2 -nak vízben történő oldódása és az azt követő egyensúlyra vezető kémiai reakció az alábbi reakcióegyenlettel írható le:
Oldódás, mint egyensúly
 Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott K
Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott K
NEHÉZFÉMEK ELTÁVOLÍTÁSA IPARI SZENNYVIZEKBŐL Modell kísérletek Cr(VI) alkalmazásával növényi hulladékokból nyert aktív szénen
 NEHÉZFÉMEK ELTÁVOLÍTÁSA IPARI SZENNYVIZEKBŐL Modell kísérletek Cr(VI) alkalmazásával növényi hulladékokból nyert aktív szénen Készítette: Battistig Nóra Környezettudomány mesterszakos hallgató A DOLGOZAT
NEHÉZFÉMEK ELTÁVOLÍTÁSA IPARI SZENNYVIZEKBŐL Modell kísérletek Cr(VI) alkalmazásával növényi hulladékokból nyert aktív szénen Készítette: Battistig Nóra Környezettudomány mesterszakos hallgató A DOLGOZAT
Környezet nehézfém-szennyezésének mérése és terjedésének nyomon követése
 Környezet nehézfém-szennyezésének mérése és terjedésének nyomon követése Krisztán Csaba Témavezető: Csorba Ottó 2012 Vázlat A terület bemutatása Célkitűzés A szennyeződés jellemzése Mintavételezés Módszerek
Környezet nehézfém-szennyezésének mérése és terjedésének nyomon követése Krisztán Csaba Témavezető: Csorba Ottó 2012 Vázlat A terület bemutatása Célkitűzés A szennyeződés jellemzése Mintavételezés Módszerek
