A gyomor- és nyelőcsőrákok világszerte évente több mint egymillió halálesetért tehetők felelőssé. 1 A betegek jelentkezésekor
|
|
|
- Ábel Soós
- 9 évvel ezelőtt
- Látták:
Átírás
1 6. ÉVFOLYAM, 6. SZÁM december Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY Panitumumabbal együtt vagy a nélkül adott epirubicin, oxaliplatin és capecitabin az elôrehaladott nyelôcsôgyomor rák kezelésében: dóziskeresô vizsgálat a több központ bevonásával lefolytatott, prospektív, véletlen besorolásos II/III. fázisú REAL-3 vizsgálathoz Alicia F. C. Okines, Sue E. Ashley, David Cunningham, Jacqueline Oates, Andrea Turner, Janine Webb, Claire Saffery, Yu Jo Chua és Ian Chau A cikkhez kapcsolódó szerkesztôségi kommentár lapunk 341. oldalán olvasható. Közlésre benyújtva: március 17-én; elfogadva: május 13-án; az internetes változat a nyomtatott verziót megelôzôen, augusztus 2-án jelent meg a honlapon. A közlemény elkészítéséhez a Royal Marsden Hospital National Health Service Foundation Trust, valamint az Amgen kutatási ösztöndíja és hozzájárulása nyújtott anyagi támogatást. A National Health Service a National Institute for Health Research Biomedical Research Centre-t támogatta (London, Egyesült Királyság). A közleményben ismertetett adatok részben bemutatásra kerültek: 2010 Gastrointestinal Cancers Symposium (Orlando, FL, január ). Nyilatkozat: Az esetleges anyagi támogatással és a munkamegosztással kapcsolatos szerzôi nyilatkozat a közlemény végén található. A klinikai vizsgálatok regiszterének cikkünkre vonatkozó információi a internetes oldalon megtalálhatók. Levelezési cím: David Cunningham, MD, FRCP, Department of Medicine, Royal Marsden Hospital, Downs Rd, Sutton, Surrey, United Kingdom SM2 5PT; david.cunningham@rmh.nhs.uk American Society of Clinical Oncology X/10/ /$20.00 DOI: /JCO ÖSSZEFOGLALÁS Célkitûzés Az epirubicinbôl, oxaliplatinból és capecitabinból (EOC) álló kombináció az elôrehaladott nyelô csô-gyomor rák standard kezelése. A panitumumab (P) teljesen humán immunglobulin G2 mo no klonális antitest, amely az epidermális növekedési faktor receptora ellen irányul. Az EOC ± panitumumab véletlen besorolásos vizsgálata (REAL-3) az elôrehaladott és lokálisan elô rehaladott nyelôcsô-gyomor rákban azt fogja vizsgálni, hogy a P hozzáadása az EOC-hoz javítja-e a nyelôcsô-gyomor elôrehaladott adenocarcinomájában vagy nem differenciált car ci nomájában szenvedô betegek túlélését. Betegek és módszerek A REAL-3 eredeti felépítésében az EOC standard dózisához (dózisszint [DL] + 1) adtunk hozzá 9 mg/kg P-t. Toxicitás miatt dóziscsökkentést végeztünk EOC + P DL 1 szintre (epirubicin 50 mg/m 2, oxaliplatin 130 mg/m 2, capecitabin 1,000 mg/m 2 /nap + P 9 mg/kg 3 hetente). Miután további toxicitást figyeltünk meg, a vizsgálatot módosítottuk, és két további EOC + P dózisszintet vontunk be. Az 1. ciklus alatt hetente mértük fel a dózislimitáló toxicitásokat (DLT, dose-limiting toxicity) elrendezéssel. A betegeket véletlenszerûen 1:1 arányban soroltuk be az EOC ± P kezelésre. Eredmények Huszonkilenc beteget választottunk ki véletlenszerûen standard dózisú EOC (n = 13) vagy EOC + P kezelésre (n = 16) július és október között. Öt beteget DL + 1 szinten kezeltünk, és a 4. ciklusra ebbôl négy betegnél 3. súlyossági fokú hasmenés jelentkezett. DL 1 szinten egy betegnek volt 3. súlyossági fokú hasmenése és 5. súlyossági fokú fertôzése. Három beteget DL 3 szinten kezeltünk, majd hat beteget DL 2 szinten anélkül, hogy dózislimitáló toxicitás jelentkezett volna. Következtetések Az EOC + P ajánlott dózisa 50 mg/m 2 epirubicin, 100 mg/m 2 oxaliplatin, 1,000 mg/m 2 /nap capecitabin és 9 mg/kg P háromhetente. Ezt a dózist választottuk ki a folyamatban lévô II/ III. fázis REAL-3 vizsgálathoz. J Clin Oncol 28: American Society of Clinical Oncology Bevezetés A gyomor- és nyelőcsőrákok világszerte évente több mint egymillió halálesetért tehetők felelőssé. 1 A betegek jelentkezésekor az esetek többségében a betegség már gyógyíthatatlan, és az átlagos túlélés körülbelül 3 hónap, ha a betegek csak a legjobb szupportív kezelésben részesülnek. 2,3 A palliatív kemoterápia, különösen 344
2 Dóziskeresô vizsgálat a REAL-3 vizsgálathoz elôrehaladott nyelôcsô-gyomor rák kezelésében a fluoropirimidin és platinatartalmú kombinációs sémák javítják a túlélést a legjobb szupportív kezeléshez képest. 4 A Randomized ECF for Advanced and Locally Advanced Esophagogastric Cancer (REAL-2) vizsgálatban arra keresték a választ, hogy egy kemoterápiás tripleten (hármas kombináción) belül a cisplatin és a fluorouracil (FU) infúzió alternatívájaként használható-e az oxaliplatin és a capecitabin nem kezelt előrehaladott nyelőcső-gyomor- (EG, esophagogastric) rákban. A vizsgálat megerősítette mindkét helyettesítő szer egyenértékűségét. Az epirubicin, oxaliplatin és capecitabin (EOC) mellett az átlagos teljes túlélés 11,2 hónap volt, ami szignifikánsan hosszabb, mint az epirubicint, cisplatint és FU-infúziót tartalmazó referenciaséma (ECF) mellett (kockázati arány [HR, hazard ratio], 0,80; 95% CI, 0,66 0,97; p = 0,02). Az EOC mellett ritkábban alakult ki 3/4. súlyossági fokú neutropenia és thromboembolia, de gyakrabban fordult elő 3/4. súlyosságú hasmenés és perifériás neuropathia. 5 Hatékonysága és biztonságossági profilja miatt az EOC-t választottuk a II/III. fázisú REAL-3 vizsgálat kemoterápiás gerinceként. A panitumumab (P) teljesen humán immunglobulin G2 monoklonális antitest, amely az epidermális növekedési faktor receptora (EGFR, epidermal growth factor receptor) ellen irányul. A P-nak monoterápiás aktivitása van kemoterápia-rezisztens metasztatikus colorectalis rákban (mcrc, metastatic colorectal cancer), és a kemoterápiához hozzáadva javítja a progressziómentes túlélést az első vonalbeli 6 és második vonalbeli kezelésben. 7 Hatékonysága csak azokon az mcrc-betegeken mutatkozik meg, akik nem hordoznak mutációt a Kirsten-ras (KRAS) onkogénben. 8 Az EG rákok körülbelül 30 50%-ában számoltak be fokozott EGFR-expresszióról, ami rossz prognózist jelent Az im mun - hisztokémiával mért fokozott EGFR-expressziónak mcrcben nincs jelentősége a P-ra adott tumorválasz tekintetében, 14 de a fluoreszcens in situ hibridizációval mért EGFR-génkópiák száma prediktív biomarker lehet ennél a tumornál. 15 A REAL-3 vizsgálatot a standard dózisú EOC-hez (50 mg/m 2 epirubicin, 130 mg/m 2 oxaliplatin és 1,250 mg/m 2 capecitabin) háromhetente hozzáadott 9 mg/kg P hatásának megítélésére terveztük. Formális dóziskereső vizsgálatot végeztünk, mivel az EOC P mellett elfogadhatatlan toxicitást figyeltünk meg. Betegek és módszerek Betegek Az alkalmas betegeknél szövettanilag igazolt, nem kezelt, metasztatikus vagy lokálisan előrehaladott, inoperábilis adenocarcinoma vagy nem differenciált carcinoma igazolódott a nyelőcsőben, a cardia (EGJ, EG junction) területén vagy a gyomorban. A nyelőcsőrákos betegeket korábbi eredményeink alapján vettük be a vizsgálatba. 16 A betegek életkora > 18 év volt, és betegségük kiterjedése komputertomográfiával (CT, computed tomography) vagy mágnesrezonanciás képalkotással (MRI, magnetic resonance imaging) egy dimenzióban mérhető volt a Response Evaluation Criteria in Solid Tumors kritériumok 17 alapján. A betegek WHO szerint meghatározott általános állapota (PS, performance status) 0 és 2 közé esett, és kardiális, renális (számított kreatinin-clearance > 50 ml/perc), máj- (szérum-bilirubin < 1,5 3 normáltartomány felső határértéke [ULN, upper limit of normal]; ALT/ AST < 2,5 3 ULN vagy májmetasztázisok esetén < 5 3 ULN; alkalikus foszfatáz < 3 3 ULN) és csontvelőfunkciójuk (abszolút neutrofilszám > 1, /l; fehérvérsejtszám > /l; thrombocyta-szám > /l; hemoglobin > 9 g/dl) megfelelő volt. Kizárási kritériumnak számított a radikális kemoradioterápiára vagy műtétre alkalmas betegség, szövettanilag igazolt laphámrák, ismert központi idegrendszeri érintettség, korábbi anti-egfr terápia, klinikailag jelentős szívbetegség vagy más klinikailag jelentős komorbiditás, intersticiális tüdőbetegség, 1. fokúnál súlyosabb perifériás neuropathia, ismert dihidropirimidin-dehidrogenáz-hiány, HIV-fertőzés, hepatitis B vagy C, terhesség, szoptatás vagy korábbi malignus betegség öt éven belül. A vizsgálatot a North West Research Ethics Committee (REC) kutatási etikai bizottság jóváhagyta, és a specifikus szűrővizsgálatok előtt minden beteg írásbeli beleegyezést adott. A központi EGFR-festéshez szövetmintákra volt szükség, és a betegektől újabb beleegyezést kértünk a vérvételhez és a tárolt, paraffinba ágyazott szövetek beszerzéséhez, mely a tervezett transzlációanalízishez kellett. Vizsgálati elrendezés és kezelés A REAL-3 célja, hogy az EOC + P-vel 10%-os javulást érjünk el az 1 éves túlélésben, az EOC-vel elért 45%-ról 5 55%-ra (az EOC + P kockázati hányadosa 0,749 az EOC-hoz képest). Ehhez 509 eseményt (bármilyen okból bekövetkező halált) kell észlelni > 90%-os statisztikai erő és kétoldalas a = 0,05 mellett. Harminchat hónap alatt 730 beteget kell véletlenszerűen besorolni 1:1 arányban EOC, illetve EOC + P kezelésre. Az elemzést az eredeti besorolás szerint (intent-totreat) fogjuk végezni. Mindegyik karban elvégezzük majd a válaszarány előre tervezett, nem komparatív köztes elemzését, ha 200 betegnél van már értékelhető terápiás válasz. Az EOC mellett várható 45%-os válaszarány 5 (p1) alapján előre meghatároztuk a hatástalansági küszöböt (válaszarány < 30%, p0). A KRAS-mutációk gyakoriságát meg fogjuk vizsgálni, és az első köztes elemzésben mindegyik karban párhuzamba állítjuk a terápiás válasszal. A túlélés tervezett köztes elemzését is el fogjuk végezni, ha az események 50%-a már bekövetkezett. A standard dózisú EOC + P ([DL] + 1 dózisszint) toxicitása miatt azonnali hatállyal biztonsági módosítást vezettünk be, és a capecitabin dózisát EOC + P DL 1 szintre csökkentettük, melyet a központi etikai bizottság (REC) és a United Kingdom Medicines and Healthcare Regulatory Agency (MHRA) is jóváhagyott. Mivel az egyik betegnél további súlyos toxicitás lépett fel, a toborzást felfüggesztettük, és a protokoll módosításával az EOC + P két újabb dózisszintjét (DL 2 és DL 3) vettük fel. Miután a REC és az MHRA jóváhagyták a módosítást, a beválasztást folytattuk. A következő betegeket DL 3 szinten 345
3 Okines és mtsai 1. táb lá zat. Dózisszintek, balról jobbra a betegek beválasztásának idôrendjében Kezelés DL + 1 DL 1 DL 3 DL 2 Epirubicin 50 mg/m 2 50 mg/m 2 50 mg/m 2 50 mg/m 2 Oxaliplatin 130 mg/m mg/m mg/m mg/m 2 Capecitabin 1250 mg/ 1000 mg/ 800 mg/ 1000 mg/ m 2 /nap m 2 /nap m 2 /nap m 2 /nap Panitumumab 9 mg/m 2 9 mg/m 2 9 mg/m 2 9 mg/m 2 Megjegyzés: A II. fázisú vizsgálathoz ajánlott dózisszint vastagon kiemelve. Rövidítés: DL, dózisszint. kezeltük. Ha nem észleltünk DLT-t, akkor a beteget DL 2 szinten kezeltük. A dózisszinteket az 1. táblázat foglalja össze. Mindegyik dózisszinten (DL, dose limit) legalább 3 olyan beteg volt, akiknél egy ciklusban értékelhetők voltak a DLT-k, azaz definíció szerint > 3. súlyosságú hasmenés, stomatitis vagy lázas neutropenia. A DL-t 6 betegre bővítettük, ha egy DLT-t észleltünk. A dózist akkor növeltük a következő szintre, ha 3 betegnél egyetlen DLT sem fordult elő, vagy 6 betegnél < 1 DLT jelentkezett. Ha egynél több betegnél észleltünk DLT-t, akkor a dózist egy szinttel csökkentettük. A nemkívánatos eseményeket a National Cancer Institute Common Terminology Criteria for Adverse Events kritériumok 3.0 verziója alapján dokumentáltuk (Cancer Therapy Evaluation program; Bethesda, MD). A betegeket véletlenszerűen 1:1 arányban soroltuk be EOC ± P kezelésre. Amikor egy beteget EOC + P kezelésre soroltunk be, akkor őt egy cikluson át obszerváltuk, mielőtt a toborzást folytattuk. Az EOC dózismódosításai DLT miatt Ha DLT, azaz 3. súlyosságú hasmenés vagy stomatitis fordult elő, akkor a capecitabin adását megszakítottuk, és 25%-os dóziscsökkentéssel folytattuk, ha < 1-es fokra enyhült. Ha a 2. ciklusban ismét 3. fokú toxicitás lépett fel, akkor a capecitabin adását ismét megszakítottuk, és 50%-os dóziscsökkentéssel folytattuk, ha a toxicitás < 1-es fokra enyhült. Lázas neutropenia esetén az egész kemoterápiát elhalasztottuk, amíg a toxicitás meg nem szűnt. A kezelést az epirubicin dózisának 25%-os és az oxaliplatin dózisának 20%-os csökkentésével folytattuk. Az EOC dózismódosításai DLT-n kívüli egyéb ok miatt A nem dózislimitáló hematológiai toxicitások esetén a kezelést addig halasztottuk, amíg az abszolút neutrofilszám nem lett > 1, /l, a thrombocytaszám pedig > /l. Szövődménymentes 3. fokú neutropenia vagy 2. fokú thrombocytopenia esetén az epirubicin dózisát 25%- kal, az oxaliplatin dózisát 20%-kal csökkentettük. Négyes súlyosságú neutropenia vagy 3. fokú thrombocytopenia esetén az epirubicin dózisát 50%-kal, az oxaliplatin adagját pedig 20%-kal csökkentettük. Az epirubicin adását 4. fokú thrombocytopenia esetén leállítottuk, az oxaliplatin dózisát pedig 20%-kal csökkentettük. Hármas súlyossági fokú hányinger/hányás vagy 2 3 fokú kéz-láb szindróma esetén a capecitabin adását megszakítottuk, és 25%-os (2. fokú kéz-láb szindróma esetén 15%-os) dóziscsökkentéssel folytattuk, ha a toxicitás < 1. fokra enyhült. A neurotoxocitást az oxaliplatin 20%-os dóziscsökkentésével kezeltük hideg indukálta paraesthesia, a ciklusok között megmaradó fájdalmatlan paraesthesia, fájdalmas paraesthesia vagy 7 napnál tovább tartó funkcionális károsodás esetén. Tartós fájdalmas paraesthesia vagy funkcionális károsodás esetén az oxaliplatin adását megszakítottuk. A P dózismódosításai A P-t egy ciklusra kihagytuk, ha > 3. fokú toxicitás jelentkezett a tervezett kezelés napján. Amint a toxicitás meg szűnt, az antitest adását 100%-os dózisban újrakezdtük a következő ciklusban. Ha a toxicitás ismét fellépett, akkor a vizsgálatvezető belátása szerint a P-t 100%-os vagy 80%-os dózisban adtuk a következő ciklusokban. Hármas súlyosságú hasmenés esetén a P-t egy ciklusra kihagytuk, és a következő ciklusokban 80%-os dózisban kezdtük újra. A betegek értékelése A véletlenszerűen EOC-re besorolt betegeket, valamint a DL + 1 és DL 1 szinten EOC + P-vel kezelt betegeket a kezelés előtt 21 naponként megvizsgáltuk, ami magában foglalta a toxicitás felmérését, a fizikális vizsgálatot, a teljes vérképet és a biokémiai profilt. Az első három beteget, akiket véletlenszerűen DL 3 és DL 2 szintű EOC + P-re soroltunk be, az első ciklus alatt hetente is értékeltük. A tumorválaszt ismételt komputertomográfiával (CT) vagy mágnesrezonanciás (MR) képalkotással mértük fel négy és nyolc ciklus után. 2. táb lá zat. A betegek kiindulási jellemzôi B kar: EOC + panitumumab A kar: EOC Jellemzô (n = 16) (n = 13) Életkor, év Átlagérték Tartomány Nem Férfi Nô 4 0 Tumor lokalizációja Nyelôcsô 7 3 EGJ 4 6 Gyomor 5 4 PS Tumor kiterjedése Lokálisan elôrehaladott 1 2 Metasztatikus Rövidítések: EOC, epirubicin, oxaliplatin és capecitabin; EGJ, cardia; PS, WHO teljesítménystátus. 346 Journal of Clinical Oncology
4 Dóziskeresô vizsgálat a REAL-3 vizsgálathoz elôrehaladott nyelôcsô-gyomor rák kezelésében Besorolás Követés Elemzés EOC + P kezelésre sorolt (n = 16) EOC + P kezelést kapott (n = 16) Szem elôl tévesztettük (n = 0) Kilépett az EOC + P kezelésbôl Elhalálozás (n = 1) Betegség progressziója (n = 3) Beteg választása (n = 1) Elemzésre kerül (n = 16) Elemzésbôl kizárt (n = 0) Alkalmassági vizsgálat (n = 38) Véletlen besorolásra került (n = 29) Eredmények Kizárásra került (n = 9) Nem felelt meg a beválasztási kritériumoknak (n = 7) Elutasította a részvételt (n = 2) EOC kezelésre sorolt (n = 13) EOC kezelést kapott (n = 13) Szem elôl tévesztettük (n = 0) Kilépett az EOC kezelésbôl Betegség progressziója (n = 3) Elemzésre kerül (n = 13) Elemzésbôl kizárt (n = 0) 1. ábra. CONSORT diagram. EOC, epirubicin, oxaliplatin és capecitabin; P, pani tumumab. Betegpopuláció és dózismódosítások Huszonkilenc beteget választottunk be véletlenszerűen a vizsgálatba 2008 júliusa és 2009 októbere között. Tizenhárom beteget véletlenszerűen EOC, 16-ot pedig EOC + P kezelésre soroltunk be. A betegek kiindulási jellemzői a 2. táblázatban láthatók, a beválasztási és besorolási folyamatot pedig az 1. ábra mutatja. Öt beteget standard dózisú EOC + P-vel (DL + 1) kezeltünk; az 1. ciklus alatt az 5-ből két betegnél észleltünk 3. fokú hasmenést, a 4. ciklusra pedig az 5-ből 4 betegnél lépett fel hasonló jelenség. Ez elfogadhatatlan szintű toxicitás, mely miatt elsőként a capecitabin dózisát csökkentettük (DL 1). DL 1 szinten egy betegnek volt 3. fokú hasmenése 5. súlyosságú septicaemiával és 1. fokú neutropeniával az 1. ciklus alatt. Egy szintén DL 1 szinten kezelt másik betegnél nem alakult ki DLT. Ezután három beteget kezeltünk DL 3, majd DL 2 szinten, és további DLT-ket nem észleltünk. A következő három ugyanezen időszakban DL 2 szintű EOC P-re sorolt beteg és két EOC-re sorolt beteg toxicitási adatait is közöljük. Biztonságosság Az 1. ciklus alatt észlelt gyakori és súlyos toxicitásokat a 3. táblázat foglalja össze. Az EOC + P-vel kezelt 16 beteg közül 6-nak, az EOC-vel kezelt 13 beteg közül egynek volt 3. fokú hasmenése bármelyik ciklus alatt. Az EOC + P-vel kezelt 16 beteg közül 7-nél, az EOC-vel kezelt 13 beteg közül 3-nál alakult ki 3. fokú fáradtság. Az EOC + P-vel kezelt 16 beteg közül 6-nál, az EOC-vel kezelt 13 beteg közül kettőnél lépett fel legalább 3. fokú neutropenia. Egy EOC-vel kezelt betegnél és egy EOC + P-vel kezelt betegnél kétszer alakult ki lázas neutropenia annak ellenére, hogy az első epizód után dóziscsökkentés történt. Egy másik betegnél 5. súlyosságú fertőzés alakult ki 1. fokú neutropeniával (DL 1). A 4. táblázat a bármelyik ciklusban előforduló toxicitásokat mutatja be terápiás kar és DL szerinti bontásban. A II. fázisú vizsgálathoz ajánlott dózis (DL 2) mellett bármelyik ciklusban a következő 3/4. fokú toxicitások jelentkeztek: szövődménymentes 3. fokú neutropenia (egy beteg), 3. fokú hasmenés 3. fokú hypokalaemiával (egy beteg), 3. fokú kéz-láb szindróma (egy beteg), 3. fokú bőrkiütés (egy beteg) és 3. fokú letargia (3 beteg, ami egy betegnél egybeesett a betegség progressziójával). Egy betegnél nem alakult ki 3/4. fokú toxicitás. Kezelés Tizenhat beteg összesen 105 cikluson át (átlagosan 8 ciklusban) EOC + P-t kapott; egy beteg további négy cikluson át P monoterápiában részesült, mivel általános állapota romlott. Öt betegnél nem fejeződött be nyolc ciklus, mivel egy beteg meghalt (1. ciklus), három betegnél a betegség progrediált (a 2., 4., illetve 7. ciklus után), egy beteg pedig a befejezés mellett döntött (a 7. ciklus után). Ugyanezen időszak alatt 13 beteg 84 cikluson át (átlagosan 8 ciklusban) kapott EOC-t. Három betegnél nem fejeződött be nyolc ciklus, mert az 1., 2., illetve 4. ciklus után betegségük progrediált. Négy betegnél hasmenés miatt > 1 ciklusra kihagytuk a P-t, majd 20%-kal csökkentettük a dózist. Egy másik betegnél, akinél az 1. ciklus alatt 3. fokú hasmenés jelentkezett, 3. táb lá zat. Súlyos vagy gyakran elôforduló toxicitások az elsô ciklus alatt szövettani stádium (grade), terápiás kar és dózisszint szerint csoportosítva B kar: EOC + panitumumab A kar: DL 3 DL 2 DL 1 DL + 1 EOC (n = 3) (n = 6) (n = 2) (n = 5) (n = 13) G1/2 G3/4 G1/2 G3/4 G1/2 G3/4 G1/2 G3/4 G1/2 G3/4 Hasmenés Hányinger Hányás Stomatitis Fáradtságérzés Acneszerû kiütés Neutropenia Lázas neutropenia vagy fertôzés normális vagy G1/2 neutrofilokkal 0 0 1* 1 1 Rövidítések: EOC, epirubicin, oxaliplatin és capecitabin; DL, dózisszint; G, szövettani stádium (grade). *5. súlyossági fokú fertôzés G1 neutropeniával
5 Okines és mtsai 4. táb lá zat. Rosszabb toxicitás bármelyik értékelhetô ciklus alatt szövettani stádium (grade), terápiás kar és dózisszint szerint csoportosítva B kar: EOC + panitumumab A kar: DL 3 DL 2 DL 1 DL + 1 EOC (n = 3) (n = 6) (n = 2) (n = 5) (n = 13) G1/2 G3/4 G1/2 G3/4 G1/2 G3/4 G1/2 G3/4 G1/2 G3/4 Anaemia Thrombocytopenia Neutropenia Lázas neutropenia Fertôzés normális vagy G1/2 neutrofilokkal * Thromboembolia Hasmenés Dehidráció Hypokalaemia Hányinger Hányás Stomatitis Fáradtság Kéz-láb szindróma Perifériás neuropathia Bôrkiütés (acneszerû és/vagy hámló) Alopecia Rövidítések: EOC, epirubicin, oxaliplatin és capecitabin; DL, dózisszint; G, szövettani stádium (grade). *5. súlyossági fokú fertôzés G1 neutropeniával. 50%-kal csökkentettük a capecitabin dózisát, de a P-t nem hagytuk ki. E betegnél és egy másiknál a P dózisát csökkenteni kellett, mert a 3. ciklusban 3. fokú bőrkiütések keletkeztek. Az 5. táblázatban látható azon betegek száma, akiknél a kezelés bármelyik komponensének dózisát egyszer vagy többször csökkenteni kellett. Megbeszélés Tudomásunk szerint korábban nem számoltak a P használatáról a nyelőcső-gyomor rák kezelésében, azonban előrehaladott gyomorrák II. fázisú vizsgálataiban a kiméra immunglobulin G1 monoklonális antitest cetuximabot vizsgálták olyan kombinációs sémákban, amelyek FU-t, leucovorint és irinotecant (FOLFIRI), 18 valamint cisplatint és docetaxelt 19 tartalmaztak. Ezekben a vizsgálatokban nem észleltek váratlan toxicitást, és a korai hatékonysági adatok biztatóak voltak. A FOLFIRI + cetuximab kombinációval kezelt betegek 5,3%-ánál, a docetaxel, cisplatin és cetixumab kombinációval kezelt betegek 19,4%-ánál észleltek lázas neutropeniát 20 ; ez a nagyobb gyakoriság sokszor észlelhető a docetaxelalapú sémáknál. 20 Legalább 3. súlyossági fokú hasmenést a FOLFIRI-vel a betegek 4,2%-ánál észleltek. 19 Azonban a közelmúltban egy németországi II. fázisú vizsgálatban, ahol a cetuximabot hetente adott oxaliplatinnal, FU-val és folinsavval kombinálták, a beválasztott 52 beteg 33%-ánál 3/4. fokú hasmenést észleltek. 21 Ez körülbelül a kétszerese volt annak, mint amiről egy korábbi II. fázisú vizsgálatban számoltak be, ahol ugyanezek a szerzők oxaliplatint, FU-t és folinsavat használtak, 22 ami az oxaliplatin és a cetuximab kölcsönhatására utalhat. A 3/4. fokú hasmenések említett gyakorisága azonban meghaladja azt az értéket, melyről a közelmúltban egy mcrc-vizsgálatban számoltak be, ahol kéthetente oxaliplatint, FU-t és leucovorint (OxmdG) adtak cetuximabbal vagy anélkül (20% OxMdG + cetuximab és 11% OxMdG). 23 A 3/4. fokú hasmenéseknek a németországi gyomorrákvizsgálatban tapasztalt gyakoribb előfordulása valószínűleg a cetuximabbal kombinációban, hetente adott oxaliplatin (50 mg/m 2 ) és FU (200 mg/m 2 ) viszonylag nagy dózisával állhat összefüggésben. A 3. fokú hasmenés, a neutropenia és a fáradtság gyakorisága a standard dózisú EOC + P-vel kezelt betegeknél nagyobb volt, mint ami várható lenne a 3 hetente egyszer adott P 8 és EOC 5 összegéből, ami potenciális szinergista toxikus hatásra utal az anti-egfr antitest és a kemoterápiás triplet (hármas kombináció) között. E váratlan eredmény miatt végeztük el a formális dóziskereső vizsgálatot, hogy egy elfogadható toxicitással bíró kombinációt határozzunk meg a folyamatban lévő II/III. fázisú vizsgálathoz. Habár a cetuximab 23,24 és a P6 mcrc-betegeken végzett korábbi vizsgálatainak adatai alapján arra gyanakszunk, hogy a P, az oxaliplatin és a capecitabin között lép fel a kölcsönhatás, nem zárhatjuk ki azt a lehetőséget sem, hogy a kölcsönhatás az epirubicinnel vagy a hármas kombinációval alakul ki. A kombinált EOC + P kezeléshez nem terveztünk I. fázisú vizsgálatot. A REAL-3 vizsgálat előkészítés alatt állt a Panitumumab Advanced Colorectal Cancer Evaluation (PACCE) vizsgálat 25 korai befejezése és adatainak közlése idején, amely kedvezőtlen hatást talált az FU-val, iri no tecan nal vagy oxaliplatinnal és bevacizumabbal és P-vel kezelt mcrc-betegek túlélése tekintetében. Az oxaliplatinnal 5. táb lá zat. Egy vagy több dóziscsökkentést igénylô betegek terápiás kar és gyógyszer szerinti bontásban Az epirubicin Az oxaliplatin A capecitabin A panitumumab dózis- dózis- dózis- dóziscsökkentését csökkentését csökkentését csökkentését igénylô igénylô igénylô igénylô betegek betegek betegek betegek Terápiás kar No. % No. % No. % No. % EOC (n = 12) EOC + panitumumab (n = 15) Rövidítés: EOC, epirubicin, oxaliplatin és capecitabin. 348 Journal of Clinical Oncology
6 Dóziskeresô vizsgálat a REAL-3 vizsgálathoz elôrehaladott nyelôcsô-gyomor rák kezelésében kezelt kohorszban a P hozzáadásakor megnőtt a hasmenések, bőrtoxicitások, fertőzések és thromboemboliák gyakorisága, azonban e betegek mindannyian egy másik monoklonális antitestet (bevacizumab) is kaptak. Ezen adatokkal egy időben közölték a Panitumumab Randomized Trial In Combination With Chemotherapy for Metastatic Colorectal Cancer to Determine Efficacy (PRIME) vizsgálat köztes elemzésének eredményeit (P + FU és oxaliplatin mcrcben), ahol nem észleltek kedvezőtlen jelzéseket a bizton ságossággal kapcsolatban, ezért feltételezték, hogy a két an ti test között lépett fel a negatív kölcsönhatás. Azóta be mutatták a PRIME vizsgálat végleges eredményeit is, amelyek bizonyították, hogy a P biztonságosan hozzáadható az oxa li pla tinhoz és FU-hoz, habár a 3/4. fokú hasmenések gyakorisága körülbelül kétszeresére nő a P hozzáadásakor. 6 A P-t korábban nem kombinálták capecitabinnal, azonban két II. fázisú vizsgálatban a cetuximabot biztonságosan kombinálták a capecitabinnal és oxaliplatinnal az mcrc kezelésében, és a capecitabin napi dózisa nagyobb volt, mint amit a REAL-3-ban terveztünk. 26,27 Hetvenkét, capecitabinnal és oxaliplatinnal (CAPOX; 130 mg/m 2 oxaliplatin és 2000 mg/m 2 /nap capecitabin 2 hétig 21 naponként) kezelt beteg véletlen besorolásos vizsgálatában a cetuximab hozzáadásakor a 3/4. fokú stomatitisek (8% vs. 3%), hasmenések (22% vs. 16%), fáradtság (14% vs. 3%) és bőrtoxicitás (16% vs. 0%) mérsékelt növekedését észlelték. 26 Azóta bemutatták a Continuous Chemotherapy Plus Cetuximab or Intermittent Chemotherapy (COIN) véletlen besorolásos III. fázisú vizsgálat eredményeit, amelyben cetuximabot adtak hozzá egy oxaliplatin/fluoropirimidine doublethez (kettős kombinációhoz). A véletlenszerűen besorolt 1630 beteg 66%-ának capecitabint adtak a vizsgálatvezető belátása szerint. A ce - tu ximab + CAPOX kezelés alatt szignifikánsan gyakoribbak (26%) voltak a 3/4. fokú hasmenések, mint az OxMdG + cetuximab kezelés kapcsán (20%), 23 annak ellenére, hogy egy módosítás során a capecitabin napi dózisát 1700 mg/m 2 -re csökkentették a vizsgálandó karban, miután 804 beteget véletlenszerűen soroltak be, mert a köztes elemzésben túlságosan gyakran észleltek 3/4. fokú hasmenést, hányingert és hányást a CAPOX/cetuximab kezelés alatt. 28 Fontos, hogy a capecitabin dózisának csökkentésekor a gyakori hányingerek és hányások megszűntek. Ez arra utal, hogy a capecitabin 15%-os dóziscsökkentése nem volt megfelelő a hasmenés kezelésére, vagy a hasmenések nagyobb gyakorisága a cetuximab és az oxaliplatin közötti kölcsönhatásnak, vagy a két tényező kombinációjának tudható be. A DL 2 és DL 3 szinten kezelt betegeket hetente monitoroztuk az 1. ciklus alatt, ami e csoportban torzítást okozhat a toxicitási jelentésekben. Azonban a DL 1 és 1 szinten észlelt toxicitások miatt fontosnak tartottuk az intenzívebb monitorozást, és a standard karban lévő betegeknek felesleges kellemetlenséget okoztak volna a járulékos vizitek. Mivel a toxicitás végső elemzése 730 véletlenszerűen kiválasztott beteget fog magába foglalni, nem aggódunk amiatt, hogy e potenciális torzítás befolyásolni fogja az összesített eredményeket. A vizsgálandó kar 10 betegét más capecitabin- és/ vagy oxaliplatindózissal kezeltük, mint a végleges populáció többi tagját, ami feltételezhetően nem lesz hatással a végső biztonságossági és hatékonysági eredményekre. Azonban az adatmonitorozó bizottságot meg fogjuk kérdezni arról, hogy helyettesítsük-e ezeket a betegeket. Potenciális probléma lehet, hogy a P-vel együtt adott mó - dosított dózisú EOC hatékonysága csökkenhet. Azonban a kemoterápiás dózismódosítások mérsékeltek voltak, és a dózisok a várt terápiás indexen belül maradnak. Számos II. fázisú vizsgálatban használtak kombinációs sémákban 1000 mg/m 2 /nap dózisú capecitabint 29 vagy 100 mg/m 2 oxaliplatint az előrehaladott nyelőcső-gyomor rák kezelésében, és 34 48%-os válaszarányokról, 6,3 8,9 hónapos átlagos progressziómentes túlélésről vagy a progresszióig eltelt időről, illetve 10,1 12,1 hónapos átlagos teljes túlélésről számoltak be, ami hasonló, mint a REAL-2 vizsgálat standard dózisú EOC-vel kezelt betegeinél. 5 Dóziskereső vizsgálatunkban nem végeztünk farmakokinetikai elemzést, mivel célunk a kombináció biztonságos dózisának meghatározása volt. A KRAS onkogénben mutációt hordozó mcrc-betegeket már nem kezelik EGFR-antitestekkel, mert ebben az alcsoportban azok hatástalanok. Ha a monoklonális EGFR-antitesteket irinotecan-alapú sémákkal kombinálják a KRAS-mutációt hordozó betegeknél az antitestek hozzáadása nem javítja a hatékonyságot. 7,33 Azoknál a KRAS-mutációt hordozó betegeknél, akiket oxaliplatin-alapú sémával és monoklonális EGFR-antitesttel kezelnek, nemcsak az antitest hozzáadása hatástalan, hanem két vizsgálatban a túlélés rosszabbodását is észlelték, 6,24 ami a nagyobbik vizsgálatban statisztikailag szignifikáns volt. 6 Nyelőcső-gyomor rákban vélhetően ritkábban fordulnak elő KRAS-mutációk, mint mcrc-ben (a közlemények szerint akár 21%-ban 21,34 37 ), bár nagy adatállományok nem állnak rendelkezésre. A cetuximab és kemoterápia II. fázisú vizsgálataiban nem mutattak ki negatív prediktív hatást KRAS-mutációt hordozó előrehaladott gyomorrákban, habár ennek hátterében a vizsgált betegek kis száma is állhat; az egyik elemzésbe bevont 44 beteg közül mindössze 5-nél (11,4%) mutattak ki mutációt. 36 A REAL-3 vizsgálatban az első 200 beteg előre tervezett elemzésében korreláltatni fogjuk a KRAS-mutációs státust és a terápiás választ. A P hozzáadása a standard dózisú EOC-hez váratlan és elfogadhatatlan mértékű toxicitást okozott. Jelen dóziskereső vizsgálatunk alapján az EOC + P ajánlott dózisa 50 mg/m 2 epirubicin, 100 mg/m 2 oxaliplatin, 1000 mg/m 2 /nap capecitabin és 9 mg/kg P háromhetente. Ezt a dózisszintet (DL) építjük be a folyamatban lévő II. fázisú/iii vizsgálatba. ÉRDEKÜTKÖZÉS LEHETôSÉGE MIATT KIZÁRT SZERZôK Noha minden szerző kitöltötte az érdekütközésre vonatkozó nyilatkozatot, az alábbi szerzők vagy családtagjaik esetében felmerült az anyagi motiváció lehetősége. Az U jelzéssel 349
7 Okines és mtsai minősített kapcsolatban a szerző nem részesült díjazásban, a C jelzés pedig a szerző díjazását jelzi. A fenti kategóriák részletes leírása és az ASCO érdekütközéssel kapcsolatos állásfoglalásának további részleteiért, kérjük, olvassa el a kizáró nyilatkozatot (Author Disclosure Declaration) és a szerzőknek szóló útmutatót (Information for Contributors), amely az eredeti folyóirat minden számának elején megtalálható. Alkalmazotti viszony vagy vezető pozíció: N/A Szak tanácsadó: David Cunningham, Roche (C), Amgen (C); Ian Chau, Roche (C) Részvényes: N/A Díjazás: Alicia F.C. Okines, Roche; Ian Chau, sanofi-aventis, Roche Kutatási támogatás: David Cunningham, Roche, sanofi-aventis, Merck Serono, Amgen; Ian Chau, Merck Serono, Roche, Novartis Szakvélemény: N/A Egyéb: Alicia F.C. Okines, Roche HIVATKOZÁSOK 1. Parkin DM, Bray F, Ferlay J, et al: Global cancer statistics, CA Cancer J Clin 55:74-108, Murad AM, Santiago FF, Petroianu A, et al: Modified therapy with 5-fluorouracil, doxorubicin, and methotrexate in advanced gastric cancer. Cancer 72:37-41, Pyrhönen S, Kuitunen T, Nyandoto P, et al: Randomised comparison of fluorouracil, epidoxorubicin and methotrexate (FEMTX) plus supportive care with supportive care alone in patients with non-resectable gastric cancer. Br J Cancer 71: , Wagner AD, Grothe W, Haerting J, et al: Chemotherapy in advanced gastric cancer: A sys tematic review and meta-analysis based on aggregate data. J Clin Oncol 24: , Cunningham D, Starling N, Rao S, et al: Capecitabine and oxaliplatin for advanced esophagogastric cancer. N Engl J Med 358:36-46, Siena S CJ, Tabernero J, Burkes RL, et al: Randomized phase III study of panitumumab (pmab) with FOLFOX4 compared to FOLFOX4 alone as first-line treatment (tx) for metastatic colorectal cancer (mcrc): PRIME trial. Presented at 2010 Gastrointestinal Cancers Symposium, Orlando, FL, January 22-24, Peeters M PTJ, Hotko YS, Cervantes- Ruiperez A, et al: Randomized phase III study of panitumumab (pmab) with FOLFIRI versus FOLFIRI alone as second-line treatment (tx) in patients (pts) with metastatic colorectal cancer (mcrc): Patientreported outcomes (PRO). Presented at 2010 Gastrointestinal Cancers Symposium, Orlando, FL, January 22-24, Amado RG, Wolf M, Peeters M, et al: Wildtype KRAS is required for panitumumab efficacy in patients with metastatic colorectal cancer. J Clin Oncol 26: , Wang KL, Wu TT, Choi IS, et al: Expression of epidermal growth factor receptor in esophageal and esophagogastric junction adenocarcinomas: Association with poor outcome. Cancer 109: , Langer R, Von Rahden BH, Nahrig J, et al: Prognostic significance of expression patterns of c-erbb-2, p53, p16ink4a, p27kip1, cyclin D1 and epidermal growth factor receptor in oesophageal adenocarcinoma: A tissue microarray study. J Clin Pathol 59: , Kim MA, Lee HS, Lee HE, et al: EGFR in gastric carcinomas: Prognostic significance of protein overexpression and high gene copy number. Histopathology 52: , Galizia G, Lieto E, Orditura M, et al: Epidermal growth factor receptor (EGFR) expression is associated with a worse prognosis in gastric cancer patients undergoing curative surgery. World J Surg 31: , Lieto E, Ferraraccio F, Orditura M, et al: Expression of vascular endothelial growth factor (VEGF) and epidermal growth factor receptor (EGFR) is an independent prognostic indicator of worse outcome in gastric cancer patients. Ann Surg Oncol 15:69-79, Hecht JR, Patnaik A, Berlin J, et al: Pani tumumab monotherapy in patients with previously treated metastatic colorectal cancer. Cancer 110: , Sartore-Bianchi A, Moroni M, Veronese S, et al: Epidermal growth factor receptor gene copy number and clinical outcome of metastatic colorectal cancer treated with panitumumab. J Clin Oncol 25: , Chau I, Norman AR, Cunningham D, et al: The impact of primary tumour origins in patients with advanced oesophageal, oesophago-gastric junction and gastric adenocarcinoma: individual patient data from 1775 patients in four randomised controlled trials. Ann Oncol 20: , Therasse P, Arbuck SG, Eisenhauer EA, et al: New guidelines to evaluate the response to treatment in solid tumors: European Organization for Research and Treatment of Cancer, National Cancer Institute of the United States, National Cancer Institute of Canada. J Natl Cancer Inst 92: , Pinto C, Di Fabio F, Siena S, et al: Phase II study of cetuximab in combination with FOLFIRI in patients with untreated advanced gastric or gastroesophageal junction adenocarcinoma (FOLCETUX study). Ann Oncol 18: , Pinto C, Di Fabio F, Barone C, et al: Phase II study of cetuximab in combination with cisplatin and docetaxel in patients with untreated advanced gastric or gastro-oesophageal junction adenocarcinoma (DOCETUX study). Br J Cancer 101: , Van Cutsem E, Moiseyenko VM, Tjulandin S, et al: Phase III study of docetaxel and cisplatin plus fluorouracil compared with cisplatin and fluorouracil as first-line therapy for advanced gastric cancer: A report of the V325 Study Group. J Clin Oncol 24: , Lordick F, Luber B, Lorenzen S, et al: Cetuximab plus oxaliplatin/leucovorin/5-fluorouracil in firstline metastatic gastric cancer: A phase II study of the Arbeitsgemeinschaft Internistische Onkologie (AIO). Br J Cancer 102: , Lordick F, Lorenzen S, Stollfuss J, et al: Phase II study of weekly oxaliplatin plus infusional fluorouracil and folinic acid (FUFOX regimen) as first-line treatment in metastatic gastric cancer. Br J Cancer 93: , Maughan TS AR, Smith C, Seymour M, et al: Oxaliplatin and fluoropyrimidine chemotherapy plus or minus cetuximab: The effect of infusional 5FU or capecitabine on the outcomes of the MRC COIN randomised controlled trial RCT in advanced colorectal cancer ACRC. Presented at 2010 Gastrointestinal Cancers Symposium, Orlando, FL, January 22-24, Bokemeyer C, Bondarenko I, Makhson A, et al: Fluorouracil, leucovorin, and oxaliplatin with and without cetuximab in the first-line treatment of metastatic colorectal cancer. J Clin Oncol 27: , Hecht JR, Mitchell E, Chidiac T, et al: A ran domized phase IIIB trial of chemotherapy, bevacizu mab, and panitumumab compared with chemotherapy and bevacizumab alone for metastatic colorectal cancer. J Clin Oncol 27: , Borner M, Koeberle D, Von Moos R, et al: Adding cetuximab to capecitabine plus oxaliplatin (XELOX) in first-line treatment of metastatic colorectal cancer: A randomized phase II trial of the Swiss Group for Clinical Cancer Research SAKK. Ann Oncol 19: , Souglakos J, Kalykaki A, Vamvakas L, et al: Phase II trial of capecitabine and oxaliplatin (CAPOX) plus cetuximab in patients with metastatic colorectal cancer who progressed after oxaliplatin-based chemotherapy. Ann Oncol 18: , Adams RA, Meade AM, Madi A, et al: Toxicity associated with combination oxaliplatin plus fluoropyrimidine with or without cetuximab in the MRC COIN trial experience. Br J Cancer 100: , Schønnemann KR, Jensen HA, Yilmaz M, et al: Phase II study of short-time oxaliplatin, capecitabine and epirubicin (EXE) as first-line therapy in patients with non-resectable gastric cancer. Br J Cancer 99: , Di Lauro L, Giacinti L, Arena MG, et al: Phase II study of epirubicin, oxaliplatin and docetaxel combination in metastatic gastric or gastroesophageal junction adenocarcinoma. J Exp Clin Cancer Res 28:34, Hejna M, Raderer M, Zacherl J, et al: Phase II study of docetaxel in combination with oxaliplatin in patients with metastatic or locally advanced esophagogastric cancer previously untreated with chemotherapy for advanced disease: Results of the Central European Cooperative Oncology Group Study ESGAS Anticancer Drugs 19: , Neri B, Pantaleo P, Giommoni E, et al: Oxaliplatin, 5-fluorouracil/leucovorin and epirubicin as first-line treatment in advanced gastric carcinoma: A phase II study. Br J Cancer 96: , Van Cutsem E, Ko hne CH, Hitre E, et al: Cetuximab and chemotherapy as initial treatment for metastatic colorectal cancer. N Engl J Med 360: , Arber N, Shapira I, Ratan J, et al: Activation of c-k-ras mutations in human gastrointestinal tumors. Gastroenterology 118: , Sommerer F, Vieth M, Markwarth A, et al: Mutations of BRAF and KRAS2 in the development of Barrett s adenocarcinoma. Oncogene 23: , Stella G RLF, Barone C, Falcone A, et al: KRAS and BRAF mutational status as response biomarkers to cetuximab combination therapy in advanced gastric cancer patients. J Clin Oncol 27, 2009 (suppl; abstr e15503) 37. Yashiro M, Nishioka N, Hirakawa K: K-ras mutation influences macroscopic features of gastric carcinoma. J Surg Res 124:74-78, 2005 nnn 350 Journal of Clinical Oncology
Kétféle antitest egyidejû alkalmazása az elôrehaladott colorectalis rák terápiájában
 5. ÉVFOLYAM, 2. SZÁM 2009. ÁPRILIS JOURNAL OF CLINICAL ONCOLOGY SZERKESZTÔSÉGI KÖZLEMÉNY Kétféle antitest egyidejû alkalmazása az elôrehaladott colorectalis rák terápiájában Charles D. Blanke Division
5. ÉVFOLYAM, 2. SZÁM 2009. ÁPRILIS JOURNAL OF CLINICAL ONCOLOGY SZERKESZTÔSÉGI KÖZLEMÉNY Kétféle antitest egyidejû alkalmazása az elôrehaladott colorectalis rák terápiájában Charles D. Blanke Division
Az angiogenezis gátlásának szerepe a vastagbél- és végbélrák kezelésében
 Az angiogenezis gátlásának szerepe a vastagbél- és végbélrák kezelésében Eredeti közlemény Bodoky György Fôvárosi Szent László és Szent István Kórház, Onkológiai Osztály, Budapest A szolid daganatok korszerû
Az angiogenezis gátlásának szerepe a vastagbél- és végbélrák kezelésében Eredeti közlemény Bodoky György Fôvárosi Szent László és Szent István Kórház, Onkológiai Osztály, Budapest A szolid daganatok korszerû
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Chapter 10 Hungarian Summary. Az onkológiai gyógyszerfejlesztés eredetileg DNS-károsodást indukáló vegyületekre
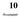 10 Összefoglaló Összefoglaló Az onkológiai gyógyszerfejlesztés eredetileg DNS-károsodást indukáló vegyületekre összpontosított, melyek az osztódó rákos sejteket célozzák meg. Jelenleg, nagy hangsúly fektetődik
10 Összefoglaló Összefoglaló Az onkológiai gyógyszerfejlesztés eredetileg DNS-károsodást indukáló vegyületekre összpontosított, melyek az osztódó rákos sejteket célozzák meg. Jelenleg, nagy hangsúly fektetődik
Minimálisan hormon érzékeny korai emlı daganatos betegcsoport összehasonlító vizsgálata
 Minimálisan hormon érzékeny korai emlı daganatos betegcsoport összehasonlító vizsgálata Rubovszky G. 1, Láng I. 1, Köves I 2, Farkas E. 2,Horváth Zs. 1, Kásler M. 3 1- Országos Onkológiai Intézet, Kemoterápia
Minimálisan hormon érzékeny korai emlı daganatos betegcsoport összehasonlító vizsgálata Rubovszky G. 1, Láng I. 1, Köves I 2, Farkas E. 2,Horváth Zs. 1, Kásler M. 3 1- Országos Onkológiai Intézet, Kemoterápia
VÁLTOZÁSOK A NEM-KISSEJTES TÜDŐRÁK DIAGNOSZTIKUS ÉS TERÁPIÁS STRATÉGIÁJÁBAN
 VÁLTOZÁSOK A NEM-KISSEJTES TÜDŐRÁK DIAGNOSZTIKUS ÉS TERÁPIÁS STRATÉGIÁJÁBAN Ostoros Gyula 1, Döme Balázs 1, Strausz János 1, Tímár József 2 1 Országos Korányi Tbc és Pulmonológiai Intézet, 2 Semmelweis
VÁLTOZÁSOK A NEM-KISSEJTES TÜDŐRÁK DIAGNOSZTIKUS ÉS TERÁPIÁS STRATÉGIÁJÁBAN Ostoros Gyula 1, Döme Balázs 1, Strausz János 1, Tímár József 2 1 Országos Korányi Tbc és Pulmonológiai Intézet, 2 Semmelweis
Krónikus C-vírus hepatitis: Új remények, régi és új nehézségek
 Krónikus C-vírus hepatitis: Új remények, régi és új nehézségek Hunyady Béla Kaposi Mór Oktató Kórház, Kaposvár PTE I.sz. Belgyógyászati Klinika, Pécs A krónikus C-vírus hepatitis lefolyása Gyógyulás Stabilizáció
Krónikus C-vírus hepatitis: Új remények, régi és új nehézségek Hunyady Béla Kaposi Mór Oktató Kórház, Kaposvár PTE I.sz. Belgyógyászati Klinika, Pécs A krónikus C-vírus hepatitis lefolyása Gyógyulás Stabilizáció
M A G Y A R K O N G R E S S Z U S I I R O D A
 Magyar Turizmus Zártkörűen Működő Részvénytársaság Magyar Kongresszusi Iroda 1115 Budapest, Bartók Béla út 105-113. Tel.: (06-1) 488-8640 Fax: (06-1) 488-8641 E-mail: hcb@hungarytourism.hu www.hcb.hu A
Magyar Turizmus Zártkörűen Működő Részvénytársaság Magyar Kongresszusi Iroda 1115 Budapest, Bartók Béla út 105-113. Tel.: (06-1) 488-8640 Fax: (06-1) 488-8641 E-mail: hcb@hungarytourism.hu www.hcb.hu A
A TÁVOLI ÁTTÉTES KOLOREKTÁLIS RÁK (MCRC) ELSŐ VÁLASZTÁSÚ KEZELÉSÉNEK FEJLŐDÉSE
 A TÁVOLI ÁTTÉTES KOLOREKTÁLIS RÁK (MCRC) ELSŐ VÁLASZTÁSÚ KEZELÉSÉNEK FEJLŐDÉSE Landherr László 1, Nagykálnai Tamás 2 1 Fővárosi Önkormányzat Uzsoki utcai Kórháza, Onkoradiológiai Központ, 2 Bajcsy-Zsilinszky
A TÁVOLI ÁTTÉTES KOLOREKTÁLIS RÁK (MCRC) ELSŐ VÁLASZTÁSÚ KEZELÉSÉNEK FEJLŐDÉSE Landherr László 1, Nagykálnai Tamás 2 1 Fővárosi Önkormányzat Uzsoki utcai Kórháza, Onkoradiológiai Központ, 2 Bajcsy-Zsilinszky
Az abortusz a magyar közvéleményben
 Az abortusz a magyar közvéleményben Országos felmérés a egyesület számára Módszer: országos reprezentatív felmérés a 18 éves és idősebb lakosság 1200 fős mintájának személyes megkérdezésével a Medián-Omnibusz
Az abortusz a magyar közvéleményben Országos felmérés a egyesület számára Módszer: országos reprezentatív felmérés a 18 éves és idősebb lakosság 1200 fős mintájának személyes megkérdezésével a Medián-Omnibusz
Radon, Toron és Aeroszol koncentráció viszonyok a Tapolcai Tavas-barlangban
 Radon, Toron és Aeroszol koncentráció viszonyok a Tapolcai Tavas-barlangban Kutatási jelentés Veszprém 29. november 16. Dr. Kávási Norbert ügyvezetı elnök Mérési módszerek, eszközök Légtéri radon és toron
Radon, Toron és Aeroszol koncentráció viszonyok a Tapolcai Tavas-barlangban Kutatási jelentés Veszprém 29. november 16. Dr. Kávási Norbert ügyvezetı elnök Mérési módszerek, eszközök Légtéri radon és toron
Mellékhatások Avastinnal kezelt emlőrákos betegeinknél. Dr Ruzsa Ágnes, Dr. Fekete Ilona MOT Kongresszus, 2009 november 12-14.
 Mellékhatások Avastinnal kezelt emlőrákos betegeinknél Dr Ruzsa Ágnes, Dr. Fekete Ilona MOT Kongresszus, 2009 november 12-14. VEGF gátlás, bevacizumab - Avastin emlőkarcinómában E2100 1 AVADO 2 RIBBON-1
Mellékhatások Avastinnal kezelt emlőrákos betegeinknél Dr Ruzsa Ágnes, Dr. Fekete Ilona MOT Kongresszus, 2009 november 12-14. VEGF gátlás, bevacizumab - Avastin emlőkarcinómában E2100 1 AVADO 2 RIBBON-1
I. melléklet. Tudományos következtetések és a forgalomba hozatali engedélyek feltételeinek a módosításának az indoklása
 I. melléklet Tudományos következtetések és a forgalomba hozatali engedélyek feltételeinek a módosításának az indoklása 1 Tudományos következtetések Figyelembe véve a farmakovigilanciai kockázatértékelő
I. melléklet Tudományos következtetések és a forgalomba hozatali engedélyek feltételeinek a módosításának az indoklása 1 Tudományos következtetések Figyelembe véve a farmakovigilanciai kockázatértékelő
Kiskunmajsa Város Önkormányzatának partnertérképe
 Kiskunmajsa Város Önkormányzatának partnertérképe Kiskunmajsa Város Önkormányzatának potenciális partnerei Helyi vállalkozások Kiskunmajsa Város Önkormányzata számára a lehetséges vállalati partnerek feltérképezéséhez
Kiskunmajsa Város Önkormányzatának partnertérképe Kiskunmajsa Város Önkormányzatának potenciális partnerei Helyi vállalkozások Kiskunmajsa Város Önkormányzata számára a lehetséges vállalati partnerek feltérképezéséhez
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
A bevacizumab javítja a túlélést az áttétes colorectalis carcinoma elsô progressziója után: egy nagy obszervációs kohorszvizsgálat eredményei (BRiTE)
 5. ÉVFOLYAM, 1. SZÁM 2009. FEBRUÁR JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY A bevacizumab javítja a túlélést az áttétes colorectalis carcinoma elsô progressziója után: egy nagy obszervációs kohorszvizsgálat
5. ÉVFOLYAM, 1. SZÁM 2009. FEBRUÁR JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY A bevacizumab javítja a túlélést az áttétes colorectalis carcinoma elsô progressziója után: egy nagy obszervációs kohorszvizsgálat
Az Európai Szabadalmi Egyezmény végrehajtási szabályainak 2010. április 1-étől hatályba lépő lényeges változásai
 DANUBIA Szabadalmi és Védjegy Iroda Kft. Az Európai Szabadalmi Egyezmény végrehajtási szabályainak 2010. április 1-étől hatályba lépő lényeges változásai A Magyar Iparjogvédelmi és Szerzői Jogi Egyesület
DANUBIA Szabadalmi és Védjegy Iroda Kft. Az Európai Szabadalmi Egyezmény végrehajtási szabályainak 2010. április 1-étől hatályba lépő lényeges változásai A Magyar Iparjogvédelmi és Szerzői Jogi Egyesület
Az elôrehaladott gyomorrák gyógyszeres kezelésének lehetôségei 2007-ben
 Az elôrehaladott gyomorrák gyógyszeres kezelésének lehetôségei 2007-ben Eredeti közlemény Dank Magdolna, Torgyík László, Szentmártoni Gyöngyvér Semmelweis Egyetem, Radiológiai és Onkoterápiás Klinika,
Az elôrehaladott gyomorrák gyógyszeres kezelésének lehetôségei 2007-ben Eredeti közlemény Dank Magdolna, Torgyík László, Szentmártoni Gyöngyvér Semmelweis Egyetem, Radiológiai és Onkoterápiás Klinika,
Budapest, 2015. április A beutazó turizmus jellemzői és alakulása 2015-ben A KSH keresletfelmérésének adatai alapján
 Budapest, 2015. április A beutazó jellemzői és alakulása 2015-ben A KSH keresletfelmérésének adatai alapján 2015-ben 20,2 millió külföldi turista látogatott Magyarországra, számuk 17,0%-kal nőtt 2014-hez
Budapest, 2015. április A beutazó jellemzői és alakulása 2015-ben A KSH keresletfelmérésének adatai alapján 2015-ben 20,2 millió külföldi turista látogatott Magyarországra, számuk 17,0%-kal nőtt 2014-hez
Docetaxel kombinációs kezeléssel (TAC) szerzett tapasztalataink az emlôrák adjuváns kemoterápiájában
 Docetaxel kombinációs kezeléssel () szerzett tapasztalataink az emlôrák adjuváns kemoterápiájában BCIRG 001 randomizált, multicentrikus fázis III vizsgálat hazai eredményei Boér Katalin, 1 Láng István,
Docetaxel kombinációs kezeléssel () szerzett tapasztalataink az emlôrák adjuváns kemoterápiájában BCIRG 001 randomizált, multicentrikus fázis III vizsgálat hazai eredményei Boér Katalin, 1 Láng István,
Dr. Erbszt András Szt. János Kh. Idegsebészeti Osztály NEVES BETEGBIZTONSÁGI FÓRUM
 Dr. Erbszt András Szt. János Kh. Idegsebészeti Osztály 2013.10.10. NEVES BETEGBIZTONSÁGI FÓRUM Definíció Szegmentum tévesztésről akkor beszélünk a gerincsebészetben amikor a sebész nem a tervezett magasságban
Dr. Erbszt András Szt. János Kh. Idegsebészeti Osztály 2013.10.10. NEVES BETEGBIZTONSÁGI FÓRUM Definíció Szegmentum tévesztésről akkor beszélünk a gerincsebészetben amikor a sebész nem a tervezett magasságban
tartalmazó becsült értékek. 2 2011. októbertől a lakáscélú és szabad felhasználású jelzáloghitelek új szerződéses összege tartalmazza a
 Grafikonkészlet a háztartási és a nem pénzügyi vállalati kamatlábakról szóló közleményhez 2012. január 1. ábra: A háztartási forint, euro és svájci frank lakáscélú hitelek új szerződéseinek értéke a szezonálisan
Grafikonkészlet a háztartási és a nem pénzügyi vállalati kamatlábakról szóló közleményhez 2012. január 1. ábra: A háztartási forint, euro és svájci frank lakáscélú hitelek új szerződéseinek értéke a szezonálisan
VII. Gyermekszív Központ
 VII. Gyermekszív Központ Dr. Szatmári András Magyarországon évente kb. 75-8 gyermek születik szívhibával, mely adat teljesen megegyezik az európai országok statisztikáival, nevezetesen, hogy 1 millió lakosra
VII. Gyermekszív Központ Dr. Szatmári András Magyarországon évente kb. 75-8 gyermek születik szívhibával, mely adat teljesen megegyezik az európai országok statisztikáival, nevezetesen, hogy 1 millió lakosra
Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY ÖSSZEFOGLALÁS
 6. ÉVFOLYAM, 2. SZÁM 2010. április Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY Gyulladásos vagy lokálisan elôrehaladott emlôrák esetén hasonlóan jó hatású a neoadjuváns kemoterápia,
6. ÉVFOLYAM, 2. SZÁM 2010. április Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY Gyulladásos vagy lokálisan elôrehaladott emlôrák esetén hasonlóan jó hatású a neoadjuváns kemoterápia,
ÖSSZEFOGLALÁS BEVEZETÉS
 5. ÉVFOLYAM, 4. SZÁM 2009. AUGUSZTUS JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az oxaliplatin fluorouracil leucovorin alkotta adjuváns kezelés javítja a II., illetve III. stádiumú vastagbélrákban
5. ÉVFOLYAM, 4. SZÁM 2009. AUGUSZTUS JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az oxaliplatin fluorouracil leucovorin alkotta adjuváns kezelés javítja a II., illetve III. stádiumú vastagbélrákban
A GYÓGYSZERKIBOCSÁTÓ SZTENTEK HATÉKONYSÁGA A HAGYOMÁNYOS SZTENTEK RESZTENÓZISÁNAK KEZELÉSÉBEN SAJÁT REGISZTERÜNK ALAPJÁN
 A GYÓGYSZERKIBOCSÁTÓ SZTENTEK HATÉKONYSÁGA A HAGYOMÁNYOS SZTENTEK RESZTENÓZISÁNAK KEZELÉSÉBEN SAJÁT REGISZTERÜNK ALAPJÁN dr. Fogarassy György, dr. Apró Dezső, dr. Faluközy József, dr. Posgay Balázs, dr.
A GYÓGYSZERKIBOCSÁTÓ SZTENTEK HATÉKONYSÁGA A HAGYOMÁNYOS SZTENTEK RESZTENÓZISÁNAK KEZELÉSÉBEN SAJÁT REGISZTERÜNK ALAPJÁN dr. Fogarassy György, dr. Apró Dezső, dr. Faluközy József, dr. Posgay Balázs, dr.
A HER2-negatív emlőrák kezelési stratégiái
 A HER2-negatív emlőrák kezelési stratégiái Dr. Landherr László Uzsoki Utcai Kórház Magyar Szenológiai Társaság Tudományos Fóruma - 2012 Klinikai igények Az eredetileg rosszabb prognózisú HER2-pozitív emlőrák
A HER2-negatív emlőrák kezelési stratégiái Dr. Landherr László Uzsoki Utcai Kórház Magyar Szenológiai Társaság Tudományos Fóruma - 2012 Klinikai igények Az eredetileg rosszabb prognózisú HER2-pozitív emlőrák
JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY
 5. ÉVFOLYAM, 3. SZÁM 2009. JÚNIUS JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az általános állapot hatása az áttétes colorectalis rák elsô vonalbeli kezelésének kimenetelére összevont hatékonysági és
5. ÉVFOLYAM, 3. SZÁM 2009. JÚNIUS JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az általános állapot hatása az áttétes colorectalis rák elsô vonalbeli kezelésének kimenetelére összevont hatékonysági és
Tájékoztató a szerződés módosításáról_munkaruházati termékek szállítása (5. rész)
 Tájékoztató a szerződés módosításáról_munkaruházati termékek szállítása (5. rész) Közbeszerzési Értesítő száma: 2016/61 Beszerzés tárgya: Árubeszerzés Hirdetmény típusa: Tájékoztató a szerződés módosításáról/2015
Tájékoztató a szerződés módosításáról_munkaruházati termékek szállítása (5. rész) Közbeszerzési Értesítő száma: 2016/61 Beszerzés tárgya: Árubeszerzés Hirdetmény típusa: Tájékoztató a szerződés módosításáról/2015
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Capecitabine medac 150 mg filmtabletta. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 150 mg kapecitabin filmtablettánként. Ismert hatású segédanyag 7 mg vízmentes
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Capecitabine medac 150 mg filmtabletta. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 150 mg kapecitabin filmtablettánként. Ismert hatású segédanyag 7 mg vízmentes
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
xdsl Optika Kábelnet Mért érték (2012. II. félév): SL24: 79,12% SL72: 98,78%
 Minőségi mutatók Kiskereskedelmi mutatók (Internet) Megnevezés: Új hozzáférés létesítési idő Meghatározás: A szolgáltatáshoz létesített új hozzáféréseknek, az esetek 80%ban teljesített határideje. Mérési
Minőségi mutatók Kiskereskedelmi mutatók (Internet) Megnevezés: Új hozzáférés létesítési idő Meghatározás: A szolgáltatáshoz létesített új hozzáféréseknek, az esetek 80%ban teljesített határideje. Mérési
fi) '.MERCK ."" SGS Egészségügyi szakembereknek szóló tájékoztatás a vad tipusú RAS (KRAS és NRAS 2., 3. és 4. exonok)
 '.MERCK Egészségügyi sza kembereknek szóló könetlen tájékozta tás a cet ul.imahról ( Erbitu J.). 2013. december t 8. Egészségügyi szakembereknek szóló tájékoztatás a vad tipusú RAS (KRAS és NRAS 2., 3.
'.MERCK Egészségügyi sza kembereknek szóló könetlen tájékozta tás a cet ul.imahról ( Erbitu J.). 2013. december t 8. Egészségügyi szakembereknek szóló tájékoztatás a vad tipusú RAS (KRAS és NRAS 2., 3.
Bevacizumab kombinációval elért hosszútávú remissziók metasztatikus colorectális carcinomában
 Bevacizumab kombinációval elért hosszútávú remissziók metasztatikus colorectális carcinomában G E LE N C S É R V I K TÓ R I A, B O É R K ATA LI N SZ E N T MA RGIT KÓ RH Á Z, O N KO LÓ GIA MAGYOT, 2016.05.05
Bevacizumab kombinációval elért hosszútávú remissziók metasztatikus colorectális carcinomában G E LE N C S É R V I K TÓ R I A, B O É R K ATA LI N SZ E N T MA RGIT KÓ RH Á Z, O N KO LÓ GIA MAGYOT, 2016.05.05
A sugárterápia változó szerepe és indikációi a mammográfiás szűrés bevezetése óta
 A sugárterápia változó szerepe és indikációi a mammográfiás szűrés bevezetése óta Polgár Cs. Mészáros N. Országos Onkológiai Intézet, Sugárterápiás Centrum Mammográfiás szűrés harmadik szűrési ciklus (2006-2007)
A sugárterápia változó szerepe és indikációi a mammográfiás szűrés bevezetése óta Polgár Cs. Mészáros N. Országos Onkológiai Intézet, Sugárterápiás Centrum Mammográfiás szűrés harmadik szűrési ciklus (2006-2007)
Palliatív mellkasi besugárzás tüdôrákban: szisztematikus áttekintô közlemény
 5. ÉVFOLYAM, 1. SZÁM 2009. FEBRUÁR JOURNAL OF CLINICAL ONCOLOGY ÖSSZEFOGLALÓ KÖZLEMÉNY Palliatív mellkasi besugárzás tüdôrákban: szisztematikus áttekintô közlemény Alysa Fairchild, Kristin Harris, Elizabeth
5. ÉVFOLYAM, 1. SZÁM 2009. FEBRUÁR JOURNAL OF CLINICAL ONCOLOGY ÖSSZEFOGLALÓ KÖZLEMÉNY Palliatív mellkasi besugárzás tüdôrákban: szisztematikus áttekintô közlemény Alysa Fairchild, Kristin Harris, Elizabeth
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Capecitabine Teva 150 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 150 mg kapecitabin filmtablettánként. Ismert hatású segédanyag(ok): 15,6
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Capecitabine Teva 150 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 150 mg kapecitabin filmtablettánként. Ismert hatású segédanyag(ok): 15,6
Biológiai terápia Audit Adatlap
 Biológiai terápia Audit Adatlap Általános adatok A beteg neve:... TAJ száma: Neme: O férfi O nı Születési dátuma: év...hó...nap Munkahely kódja:.. Orvos pecsétszáma:. Beválogatás Diagnózis: Rheumatoid
Biológiai terápia Audit Adatlap Általános adatok A beteg neve:... TAJ száma: Neme: O férfi O nı Születési dátuma: év...hó...nap Munkahely kódja:.. Orvos pecsétszáma:. Beválogatás Diagnózis: Rheumatoid
Kolorektális eredetű májáttétek preoperatív kemoterápiás kezelést követő reszekciós eredményeinek klinikai vizsgálata
 Kolorektális eredetű májáttétek preoperatív kemoterápiás kezelést követő reszekciós eredményeinek klinikai vizsgálata Doktori értekezés Dr. Dede Kristóf Semmelweis Egyetem Klinikai Orvostudományok Doktori
Kolorektális eredetű májáttétek preoperatív kemoterápiás kezelést követő reszekciós eredményeinek klinikai vizsgálata Doktori értekezés Dr. Dede Kristóf Semmelweis Egyetem Klinikai Orvostudományok Doktori
ÖSSZEFOGLALÁS BEVEZETÉS. A kompetitív ösztrogénreceptor- (ER, estrogen-receptor)
 5. ÉVFOLYAM, 1. SZÁM 2009. FEBRUÁR JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az exemestan és a tamoxifen III. fázisú, összehasonlító vizsgálata posztmenopauzában lévô, metasztatikus emlôrákos nôk
5. ÉVFOLYAM, 1. SZÁM 2009. FEBRUÁR JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az exemestan és a tamoxifen III. fázisú, összehasonlító vizsgálata posztmenopauzában lévô, metasztatikus emlôrákos nôk
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Capecitabine SUN 150 mg filmtabletta. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 150 mg kapecitabin filmtablettánként. Ismert hatású segédanyag(ok): 20,69
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Capecitabine SUN 150 mg filmtabletta. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 150 mg kapecitabin filmtablettánként. Ismert hatású segédanyag(ok): 20,69
Fazekas Mihály Fővárosi Gyakorló Általános Iskola és Gimnázium
 26 Fazekas Mihály Fővárosi Gyakorló Általános Iskola és Gimnázium Az Önök telephelyére vonatkozó egyedi adatok táblázatokban és grafikonokon 1. évfolyam gimnázium szövegértés Előállítás ideje: 27.3.. 12:28:21
26 Fazekas Mihály Fővárosi Gyakorló Általános Iskola és Gimnázium Az Önök telephelyére vonatkozó egyedi adatok táblázatokban és grafikonokon 1. évfolyam gimnázium szövegértés Előállítás ideje: 27.3.. 12:28:21
Tapasztalataink súlyos pikkelysömör adalimumab kezelésével* Adalimumab treatment of severe psoriasis
 BÔRGYÓGYÁSZATI ÉS VENEROLÓGIAI SZEMLE 85. ÉVF. 6. 283 288. Szegedi Tudományegyetem, Általános Orvostudományi Kar, Szent-Györgyi Albert Klinikai Központ, Bôrgyógyászati és Allergológiai Klinika (igazgató:
BÔRGYÓGYÁSZATI ÉS VENEROLÓGIAI SZEMLE 85. ÉVF. 6. 283 288. Szegedi Tudományegyetem, Általános Orvostudományi Kar, Szent-Györgyi Albert Klinikai Központ, Bôrgyógyászati és Allergológiai Klinika (igazgató:
A colorectalis carcinoma irinotecan kezelésének legújabb eredményei
 A colorectalis carcinoma irinotecan kezelésének legújabb eredményei (irodalmi összefoglaló) Összefoglaló Láng István, Hitre Erika Országos Onkológiai Intézet B Belgyógyászati Onkológiai Osztály, Budapest
A colorectalis carcinoma irinotecan kezelésének legújabb eredményei (irodalmi összefoglaló) Összefoglaló Láng István, Hitre Erika Országos Onkológiai Intézet B Belgyógyászati Onkológiai Osztály, Budapest
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Vectibix 20 mg/ml koncentrátum oldatos infúzióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A koncentrátum 20 mg panitumumabot tartalmaz milliliterenként.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Vectibix 20 mg/ml koncentrátum oldatos infúzióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A koncentrátum 20 mg panitumumabot tartalmaz milliliterenként.
MAGYAR SZENOLÓGIAI TÁRSASÁG TUDOMÁNYOS FÓRUMA - 2012. Dr. Horváth Zsolt Országos Onkológiai Intézet. A Herceptin kezelés.
 Dr. Horváth Zsolt Országos Onkológiai Intézet A Herceptin kezelés újabb lehetőségei MAGYAR SZENOLÓGIAI TÁRSASÁG TUDOMÁNYOS FÓRUMA - 2012 SC Herceptin kezelés* Herceptin az ebc neoadjuváns kezelésében**
Dr. Horváth Zsolt Országos Onkológiai Intézet A Herceptin kezelés újabb lehetőségei MAGYAR SZENOLÓGIAI TÁRSASÁG TUDOMÁNYOS FÓRUMA - 2012 SC Herceptin kezelés* Herceptin az ebc neoadjuváns kezelésében**
Hidak építése a minőségügy és az egészségügy között
 DEBRECENI EGÉSZSÉGÜGYI MINŐSÉGÜGYI NAPOK () 2016. május 26-28. Hidak építése a minőségügy és az egészségügy között A TOVÁBBKÉPZŐ TANFOLYAM KIADVÁNYA Debreceni Akadémiai Bizottság Székháza (Debrecen, Thomas
DEBRECENI EGÉSZSÉGÜGYI MINŐSÉGÜGYI NAPOK () 2016. május 26-28. Hidak építése a minőségügy és az egészségügy között A TOVÁBBKÉPZŐ TANFOLYAM KIADVÁNYA Debreceni Akadémiai Bizottság Székháza (Debrecen, Thomas
Tájékoztató az önkéntes nyugdíjpénztárak számára a 2012-től érvényes felügyeleti adatszolgáltatási változásokról
 Tájékoztató az önkéntes nyugdíjpénztárak számára a 2012-től érvényes felügyeleti adatszolgáltatási változásokról Szeles Angelika Monitoring szakreferens Adatszolgáltatási és monitoring főosztály Budapest,
Tájékoztató az önkéntes nyugdíjpénztárak számára a 2012-től érvényes felügyeleti adatszolgáltatási változásokról Szeles Angelika Monitoring szakreferens Adatszolgáltatási és monitoring főosztály Budapest,
A rosszindulatú daganatos halálozás változása 1975 és 2001 között Magyarországon
 A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY
 6. ÉVFOLYAM, 3. SZÁM 2010. június Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY A cisplatin/s-1 és a cisplatin/infúziós fluorouracil több központ bevonásával lefolytatott III. fázisú vizsgálata
6. ÉVFOLYAM, 3. SZÁM 2010. június Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY A cisplatin/s-1 és a cisplatin/infúziós fluorouracil több központ bevonásával lefolytatott III. fázisú vizsgálata
Kerékpárlabda kvalifikációs szabályzat
 Kerékpárlabda kvalifikációs szabályzat Érvényesség kezdete: Junior kategória 2016 június 1 Felnőtt kategória 2016 január 1 Tartalom I. Célja... 3 II. Szabályozás... 3 1) A versenyek meghatározása... 3
Kerékpárlabda kvalifikációs szabályzat Érvényesség kezdete: Junior kategória 2016 június 1 Felnőtt kategória 2016 január 1 Tartalom I. Célja... 3 II. Szabályozás... 3 1) A versenyek meghatározása... 3
MEZŐGAZDASÁGI ALAPISMERETEK ÉRETTSÉGI VIZSGA II. A VIZSGA LEÍRÁSA
 A vizsga részei MEZŐGAZDASÁGI ALAPISMERETEK ÉRETTSÉGI VIZSGA II. A VIZSGA LEÍRÁSA Középszint Emelt szint 180 perc 15 perc 240 perc 20 perc 100 pont 50 pont 100 pont 50 pont A vizsgán használható segédeszközök
A vizsga részei MEZŐGAZDASÁGI ALAPISMERETEK ÉRETTSÉGI VIZSGA II. A VIZSGA LEÍRÁSA Középszint Emelt szint 180 perc 15 perc 240 perc 20 perc 100 pont 50 pont 100 pont 50 pont A vizsgán használható segédeszközök
Puskás Tivadar Távközlési Technikum
 27 Puskás Tivadar Távközlési Technikum Az Önök telephelyére vonatkozó egyedi adatok táblázatokban és grafikonokon 1. évfolyam szakközépiskola matematika Előállítás ideje: 28.3.6. 6:48:31 197 Budapest,
27 Puskás Tivadar Távközlési Technikum Az Önök telephelyére vonatkozó egyedi adatok táblázatokban és grafikonokon 1. évfolyam szakközépiskola matematika Előállítás ideje: 28.3.6. 6:48:31 197 Budapest,
HIRDETMÉNY AKCIÓK, KEDVEZMÉNYEK
 HIRDETMÉNY KONDÍCIÓS LISTÁK ÉS ÜGYFÉLTÁJÉKOZTATÓK MÓDOSÍTÁSÁRÓL ÉS VÁLTOZÁSÁRÓL I. A módosítással érintett kondíciós listák és ügyféltájékoztatók A CIB Bank Zrt. (1027 Budapest, Medve u. 4-14.; cégjegyzékszám.:
HIRDETMÉNY KONDÍCIÓS LISTÁK ÉS ÜGYFÉLTÁJÉKOZTATÓK MÓDOSÍTÁSÁRÓL ÉS VÁLTOZÁSÁRÓL I. A módosítással érintett kondíciós listák és ügyféltájékoztatók A CIB Bank Zrt. (1027 Budapest, Medve u. 4-14.; cégjegyzékszám.:
A kemoterápia idôtartama elôrehaladott nem kissejtes tüdôrákban: véletlen besorolásos vizsgálatok áttekintése és metaanalízise
 5. ÉVFOLYAM, 5. SZÁM 2009. OKTÓBER JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY A kemoterápia idôtartama elôrehaladott nem kissejtes tüdôrákban: véletlen besorolásos vizsgálatok áttekintése és metaanalízise
5. ÉVFOLYAM, 5. SZÁM 2009. OKTÓBER JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY A kemoterápia idôtartama elôrehaladott nem kissejtes tüdôrákban: véletlen besorolásos vizsgálatok áttekintése és metaanalízise
A rectum daganatok diagnosztikájának és kezelésének finanszírozási protokollja
 A rectum daganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010. február 15.
A rectum daganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010. február 15.
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ. Orvosi laboratóriumi technikai asszisztens szakképesítés. 2449-06 Mikrobiológiai vizsgálatok modul. 1.
 Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL. (2004. I. negyedév) Budapest, 2004. július
 ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL (2004. I. negyedév) Budapest, 2004. július Évközi minta az egészségügyi bér- és létszámstatisztikából Vezet i összefoglaló Módszertan Táblázatok:
ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL (2004. I. negyedév) Budapest, 2004. július Évközi minta az egészségügyi bér- és létszámstatisztikából Vezet i összefoglaló Módszertan Táblázatok:
Az éves statisztikai összegezés STATISZTIKAI ÖSSZEGEZÉS AZ ÉVES KÖZBESZERZÉSEKRŐL A KLASSZIKUS AJÁNLATKÉRŐK VONATKOZÁSÁBAN
 11. melléklet a 92/2011. (XII.30.) NFM rendelethez Az éves statisztikai összegezés STATISZTIKAI ÖSSZEGEZÉS AZ ÉVES KÖZBESZERZÉSEKRŐL A KLASSZIKUS AJÁNLATKÉRŐK VONATKOZÁSÁBAN I. SZAKASZ: AJÁNLATKÉRŐ I.1)
11. melléklet a 92/2011. (XII.30.) NFM rendelethez Az éves statisztikai összegezés STATISZTIKAI ÖSSZEGEZÉS AZ ÉVES KÖZBESZERZÉSEKRŐL A KLASSZIKUS AJÁNLATKÉRŐK VONATKOZÁSÁBAN I. SZAKASZ: AJÁNLATKÉRŐ I.1)
Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok
 Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok Dr. Lotz Gábor, Dr. Szirtes Ildikó, Dr. Kiss András Prof. Tímár József, Prof. Kulka Janina Semmelweis Egyetem II. Pathologiai Intézet - Exophyticus
Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok Dr. Lotz Gábor, Dr. Szirtes Ildikó, Dr. Kiss András Prof. Tímár József, Prof. Kulka Janina Semmelweis Egyetem II. Pathologiai Intézet - Exophyticus
Homlokzati tűzterjedés vizsgálati módszere
 Homlokzati tűzterjedés vizsgálati módszere Siófok 2008. április 17. Dr. Bánky Tamás Nyílásos homlokzatok esetén a tűzterjedési gát kritériumait nem kielégítő homlokzati megoldásoknál továbbá nyílásos homlokzatokon
Homlokzati tűzterjedés vizsgálati módszere Siófok 2008. április 17. Dr. Bánky Tamás Nyílásos homlokzatok esetén a tűzterjedési gát kritériumait nem kielégítő homlokzati megoldásoknál továbbá nyílásos homlokzatokon
Accorde Alapkezelő Zrt. Accorde Prémium Alapok Alapja Befektetési Alap 2016. I. Féléves jelentés
 Accorde Alapkezelő Zrt. Accorde Prémium Alapok Alapja Befektetési Alap 2016. I. Féléves jelentés (Időszak: 2016.02.02-2016.06.30.) I. Vagyonkimutatás indulás: 02.02. Vége: 2016.06.30. Instrumentum Érték
Accorde Alapkezelő Zrt. Accorde Prémium Alapok Alapja Befektetési Alap 2016. I. Féléves jelentés (Időszak: 2016.02.02-2016.06.30.) I. Vagyonkimutatás indulás: 02.02. Vége: 2016.06.30. Instrumentum Érték
ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL. (2004. IV. negyedév) Budapest, 2005. április
 ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL (2004. IV. negyedév) Budapest, 2005. április Évközi minta az egészségügyi bér- és létszámstatisztikából Vezet i összefoglaló Módszertan Táblázatok:
ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL (2004. IV. negyedév) Budapest, 2005. április Évközi minta az egészségügyi bér- és létszámstatisztikából Vezet i összefoglaló Módszertan Táblázatok:
E4 A Gyermekkori szervezett lakossági emlőszűrések hatása az emlőműtétek
 08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
Az aktiválódásoknak azonban itt még nincs vége, ugyanis az aktiválódások 30 évenként ismétlődnek!
 1 Mindannyiunk életében előfordulnak jelentős évek, amikor is egy-egy esemény hatására a sorsunk új irányt vesz. Bár ezen események többségének ott és akkor kevésbé tulajdonítunk jelentőséget, csak idővel,
1 Mindannyiunk életében előfordulnak jelentős évek, amikor is egy-egy esemény hatására a sorsunk új irányt vesz. Bár ezen események többségének ott és akkor kevésbé tulajdonítunk jelentőséget, csak idővel,
irányítószám: Ország: Magyarország
 25/23-2/2015. A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI I.1.) AZ AJÁNLATKÉRŐKÉNT SZERZŐDŐ FÉL NEVE ÉS CÍME Hivatalos név: Országos Nyugdíjbiztosítási Főigazgatóság
25/23-2/2015. A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI I.1.) AZ AJÁNLATKÉRŐKÉNT SZERZŐDŐ FÉL NEVE ÉS CÍME Hivatalos név: Országos Nyugdíjbiztosítási Főigazgatóság
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Armisarte 25 mg/ml koncentrátum oldatos infúzióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A koncentrátum milliliterenként 25 mg pemetrexed tartalmaz
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Armisarte 25 mg/ml koncentrátum oldatos infúzióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A koncentrátum milliliterenként 25 mg pemetrexed tartalmaz
Művesekezelés anyagainak beszerzése a Semmelweis Egyetem Transzplantációs és Sebészeti Klinika részére
 Művesekezelés anyagainak beszerzése a Semmelweis Egyetem Transzplantációs és Sebészeti Klinika részére Közbeszerzési Értesítő száma: 2015/145 Művesekezelés anyagainak beszerzése 24 hónapra Beszerzés tárgya:
Művesekezelés anyagainak beszerzése a Semmelweis Egyetem Transzplantációs és Sebészeti Klinika részére Közbeszerzési Értesítő száma: 2015/145 Művesekezelés anyagainak beszerzése 24 hónapra Beszerzés tárgya:
EURÓPAI UNIÓ AZ EURÓPAI PARLAMENT 2006/0287 (COD) PE-CONS 3648/2/07 REV 2
 EURÓPAI UNIÓ AZ EURÓPAI PARLAMENT A TANÁCS Brüsszel, 2008. február 26. (OR. en) 2006/0287 (COD) PE-CONS 3648/2/07 REV 2 ENV 447 ENT 104 CODEC 899 JOGI AKTUSOK ÉS EGYÉB ESZKÖZÖK Tárgy: AZ EURÓPAI PARLAMENT
EURÓPAI UNIÓ AZ EURÓPAI PARLAMENT A TANÁCS Brüsszel, 2008. február 26. (OR. en) 2006/0287 (COD) PE-CONS 3648/2/07 REV 2 ENV 447 ENT 104 CODEC 899 JOGI AKTUSOK ÉS EGYÉB ESZKÖZÖK Tárgy: AZ EURÓPAI PARLAMENT
Belépési útmutató a MIAG weboldalra www.miag.com
 Belépési útmutató a MIAG weboldalra www.miag.com Classification level: Public MEMBER OF METRO GROUP 1 Tartalom 1. Fontos tudnivaló p. 3 2. Bejelentkezés a www.miag.com weboldalra p. 4-5 3. E-mail cím regisztrálása
Belépési útmutató a MIAG weboldalra www.miag.com Classification level: Public MEMBER OF METRO GROUP 1 Tartalom 1. Fontos tudnivaló p. 3 2. Bejelentkezés a www.miag.com weboldalra p. 4-5 3. E-mail cím regisztrálása
ÖSSZEFOGLALÁS BEVEZETÉS
 6. ÉVFOLYAM, 2. SZÁM 2010. április Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY Indukciós kemoterápia és cetuximab-kezelés a lokálisan elôrehaladott fej-nyaki laphámrák ellátásában: egy
6. ÉVFOLYAM, 2. SZÁM 2010. április Jou r n a l of Cl i n i c a l On c o l o g y EREDETI KÖZLEMÉNY Indukciós kemoterápia és cetuximab-kezelés a lokálisan elôrehaladott fej-nyaki laphámrák ellátásában: egy
A nyelôcsôrák szimultán radio-kemoterápiája (saját eredményeink alapján)
 A nyelôcsôrák szimultán radio-kemoterápiája (saját eredményeink alapján) Eredeti közlemény Patonay Péter, Naszály Attila, Mayer Árpád Fôvárosi Önkormányzat Uzsoki utcai Kórháza, Fôvárosi Onkoradiológiai
A nyelôcsôrák szimultán radio-kemoterápiája (saját eredményeink alapján) Eredeti közlemény Patonay Péter, Naszály Attila, Mayer Árpád Fôvárosi Önkormányzat Uzsoki utcai Kórháza, Fôvárosi Onkoradiológiai
III. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ
 III. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ 11 ALKALMAZÁSI ELŐÍRÁS 12 1. A GYÓGYSZER MEGNEVEZÉSE Dexrazoxán tartalmú gyógyszer (lásd I. Melléklet) 500 mg por oldatos infúzióhoz. [Lásd I. Melléklet
III. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ 11 ALKALMAZÁSI ELŐÍRÁS 12 1. A GYÓGYSZER MEGNEVEZÉSE Dexrazoxán tartalmú gyógyszer (lásd I. Melléklet) 500 mg por oldatos infúzióhoz. [Lásd I. Melléklet
ORSZÁGOS KÖRNYEZETEGÉSZSÉGÜGYI INTÉZET
 ORSZÁGOS KÖRNYEZETEGÉSZSÉGÜGYI INTÉZET 197 Budapest, Gyáli út 2-6. Levélcím: 1437 Budapest Pf.: 839 Telefon: (6-1) 476-11 Fax: (6-1) 21-148 http://efrirk.antsz.hu/oki/ A PARLAGFŰ POLLENSZÓRÁSÁNAK ALAKULÁSA
ORSZÁGOS KÖRNYEZETEGÉSZSÉGÜGYI INTÉZET 197 Budapest, Gyáli út 2-6. Levélcím: 1437 Budapest Pf.: 839 Telefon: (6-1) 476-11 Fax: (6-1) 21-148 http://efrirk.antsz.hu/oki/ A PARLAGFŰ POLLENSZÓRÁSÁNAK ALAKULÁSA
Beszerzések, közbeszerzési eljárások; Összeférhetetlenség, szabálytalanság. Előadó: dr. Keszler Gábor NFFKÜ Zrt.
 Beszerzések, közbeszerzési eljárások; Összeférhetetlenség, szabálytalanság Előadó: dr. Keszler Gábor NFFKÜ Zrt. Irányadó jogszabályok - az EGT Finanszírozási Mechanizmus és a Norvég Finanszírozási Mechanizmus
Beszerzések, közbeszerzési eljárások; Összeférhetetlenség, szabálytalanság Előadó: dr. Keszler Gábor NFFKÜ Zrt. Irányadó jogszabályok - az EGT Finanszírozási Mechanizmus és a Norvég Finanszírozási Mechanizmus
Szusza Ferenc labdarúgó sportlétesítmény fejlesztése
 Szusza Ferenc labdarúgó sportlétesítmény fejlesztése Közbeszerzési Értesítő száma: 2015/124 A Szusza Ferenc Stadion labdarúgó sportlétesítmény fejlesztése keretében a Beszerzés tárgya: létesítmény valamint
Szusza Ferenc labdarúgó sportlétesítmény fejlesztése Közbeszerzési Értesítő száma: 2015/124 A Szusza Ferenc Stadion labdarúgó sportlétesítmény fejlesztése keretében a Beszerzés tárgya: létesítmény valamint
PARADIGMA VÁLTÁS AZ ASZTMA BRONCHIALE MEGÍTÉLÉSÉBEN ÉS KEZELÉSÉBEN. Dr. Kovács Lajos SE. I. sz. Gyermekklinika Budapest
 PARADIGMA VÁLTÁS AZ ASZTMA BRONCHIALE MEGÍTÉLÉSÉBEN ÉS KEZELÉSÉBEN Dr. Kovács Lajos SE. I. sz. Gyermekklinika Budapest ASZTMA GONDOZÁS SZEMPONTJAI Triggerek Aktuális tünetek Légzésfunkció KONTROLLÁLTSÁG
PARADIGMA VÁLTÁS AZ ASZTMA BRONCHIALE MEGÍTÉLÉSÉBEN ÉS KEZELÉSÉBEN Dr. Kovács Lajos SE. I. sz. Gyermekklinika Budapest ASZTMA GONDOZÁS SZEMPONTJAI Triggerek Aktuális tünetek Légzésfunkció KONTROLLÁLTSÁG
Statisztika 2016. március 11. A csoport Neptun kód
 Statisztika 2016. március 11. A csoport Név Neptun kód 1. Egy közösségben az élelmiszerre fordított kiadások az alábbiak szerint alakultak: osszeg (ezer Ft) csalad(db) 20 7 20:1 30 12 30:1 40 20 40:1 50
Statisztika 2016. március 11. A csoport Név Neptun kód 1. Egy közösségben az élelmiszerre fordított kiadások az alábbiak szerint alakultak: osszeg (ezer Ft) csalad(db) 20 7 20:1 30 12 30:1 40 20 40:1 50
[GVMGS11MNC] Gazdaságstatisztika
![[GVMGS11MNC] Gazdaságstatisztika [GVMGS11MNC] Gazdaságstatisztika](/thumbs/40/21500887.jpg) [GVMGS11MNC] Gazdaságstatisztika 4 előadás Főátlagok összehasonlítása http://uni-obudahu/users/koczyl/gazdasagstatisztikahtm Kóczy Á László KGK-VMI Viszonyszámok (emlékeztető) Jelenség színvonalának vizsgálata
[GVMGS11MNC] Gazdaságstatisztika 4 előadás Főátlagok összehasonlítása http://uni-obudahu/users/koczyl/gazdasagstatisztikahtm Kóczy Á László KGK-VMI Viszonyszámok (emlékeztető) Jelenség színvonalának vizsgálata
HIRDETMÉNY AKCIÓK, KEDVEZMÉNYEK
 HIRDETMÉNY KONDÍCIÓS LISTÁK ÉS ÜGYFÉLTÁJÉKOZTATÓK MÓDOSÍTÁSÁRÓL ÉS VÁLTOZÁSÁRÓL I. A módosítással érintett kondíciós listák és ügyféltájékoztatók A CIB Bank Zrt. (1027 Budapest, Medve u. 4-14.; cégjegyzékszám.:
HIRDETMÉNY KONDÍCIÓS LISTÁK ÉS ÜGYFÉLTÁJÉKOZTATÓK MÓDOSÍTÁSÁRÓL ÉS VÁLTOZÁSÁRÓL I. A módosítással érintett kondíciós listák és ügyféltájékoztatók A CIB Bank Zrt. (1027 Budapest, Medve u. 4-14.; cégjegyzékszám.:
8. melléklet a 92/2011. (XII. 30.) NFM rendelethez A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI
 1 8. melléklet a 92/2011. (XII. 30.) NFM rendelethez A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI I.1) AZ AJÁNLATKÉRŐKÉNT SZERZŐDŐ FÉL NEVE ÉS CÍME Hivatalos név: Fővárosi
1 8. melléklet a 92/2011. (XII. 30.) NFM rendelethez A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI I.1) AZ AJÁNLATKÉRŐKÉNT SZERZŐDŐ FÉL NEVE ÉS CÍME Hivatalos név: Fővárosi
Munkaerő-piaci helyzetkép. Csongrád megye
 CSONGRÁD MEGYEI KORMÁNYHIVATAL MUNKAÜGYI KÖZPONTJA Munkaerő-piaci helyzetkép Csongrád megye 2013. június 6721 Szeged, Bocskai u. 10-12. +36 (62) 561-561 +36 (62) 561-551 www.csmkh.hu csongradkh-mk@lab.hu
CSONGRÁD MEGYEI KORMÁNYHIVATAL MUNKAÜGYI KÖZPONTJA Munkaerő-piaci helyzetkép Csongrád megye 2013. június 6721 Szeged, Bocskai u. 10-12. +36 (62) 561-561 +36 (62) 561-551 www.csmkh.hu csongradkh-mk@lab.hu
Nemzeti Edzés Központ válogatott tenisz edzéseken való részvétel és egyéb időpontok igénybevétele a téli időszakban
 Nemzeti Edzés Központ válogatott tenisz edzéseken való részvétel és egyéb időpontok igénybevétele a téli időszakban Általános tudnivalók (1) A válogatott edzések helyszíne: Nemzeti Edzés Központ, Mikoviny
Nemzeti Edzés Központ válogatott tenisz edzéseken való részvétel és egyéb időpontok igénybevétele a téli időszakban Általános tudnivalók (1) A válogatott edzések helyszíne: Nemzeti Edzés Központ, Mikoviny
Keretszerződés költöztetési, szállítási feladatok ellátására a Pécsi Tudományegyetemen-2- AF módosítás
 Keretszerződés költöztetési, szállítási feladatok ellátására a Pécsi Tudományegyetemen-2- AF módosítás Közbeszerzési Értesítő száma: 2015/44 Beszerzés tárgya: Keretszerződés költöztetési, szállítási feladatok
Keretszerződés költöztetési, szállítási feladatok ellátására a Pécsi Tudományegyetemen-2- AF módosítás Közbeszerzési Értesítő száma: 2015/44 Beszerzés tárgya: Keretszerződés költöztetési, szállítási feladatok
Címzett: Markus Goddemeier E-mail: markus.goddemeier@proteinsimple.com Fax: +49 (0)162 985 79 53
 8. melléklet a 92/2011. (XII.30.) NFM rendelethez A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI I.1) AZ AJÁNLATKÉRŐKÉNT SZERZŐDŐ FÉL NEVE ÉS CÍME Hivatalos név: MTA Kísérleti
8. melléklet a 92/2011. (XII.30.) NFM rendelethez A SZERZŐDÉS TELJESÍTÉSÉRE VONATKOZÓ INFORMÁCIÓK I. SZAKASZ: A SZERZŐDÉS ALANYAI I.1) AZ AJÁNLATKÉRŐKÉNT SZERZŐDŐ FÉL NEVE ÉS CÍME Hivatalos név: MTA Kísérleti
Útmutató a vízumkérő lap kitöltéséhez
 Útmutató a vízumkérő lap kitöltéséhez A vízumkérő lap ( Visa application form of the People s Republic of China, Form V. 2013 ) az egyik legfontosabb dokumentum, amit a kínai vízumra való jelentkezésnél
Útmutató a vízumkérő lap kitöltéséhez A vízumkérő lap ( Visa application form of the People s Republic of China, Form V. 2013 ) az egyik legfontosabb dokumentum, amit a kínai vízumra való jelentkezésnél
Beszámoló: a kompetenciamérés eredményének javítását célzó intézkedési tervben foglaltak megvalósításáról. Őcsény, 2015. november 20.
 Őcsényi Perczel Mór Általános Iskola székhelye: 7143 Őcsény, Perczel Mór utca 1. Tel: 74/496-782 e-mail: amk.ocseny@altisk-ocseny.sulinet.hu Ikt.sz.: /2015. OM: 036345 Ügyintéző: Ősze Józsefné Ügyintézés
Őcsényi Perczel Mór Általános Iskola székhelye: 7143 Őcsény, Perczel Mór utca 1. Tel: 74/496-782 e-mail: amk.ocseny@altisk-ocseny.sulinet.hu Ikt.sz.: /2015. OM: 036345 Ügyintéző: Ősze Józsefné Ügyintézés
Az új SM terápiák szemészeti vonatkozásai
 Az új SM terápiák szemészeti vonatkozásai Magyar Szemorvostársaság Neuroophthalmológiai Szekciójának Szimpóziuma 2011 Június 16. Terápia Gyulladáscsökkentés Neuroregeneráció Immunmoduláló kezelések Első
Az új SM terápiák szemészeti vonatkozásai Magyar Szemorvostársaság Neuroophthalmológiai Szekciójának Szimpóziuma 2011 Június 16. Terápia Gyulladáscsökkentés Neuroregeneráció Immunmoduláló kezelések Első
A GYOMOR DAGANATOS MEGBETEGEDÉSEI
 A GYOMOR DAGANATOS MEGBETEGEDÉSEI DR. LÉNÁRT ZSUZSANNA SZEGEDI TUDOMÁNYEGYETEM I.SZ. BELGYÓGYÁSZATI KLINIKA A GYOMOR JÓINDULATÚ DAGANATAI ("protrudáló gyomorlaesiók", " gyomorpolypusok") eredetük szerint
A GYOMOR DAGANATOS MEGBETEGEDÉSEI DR. LÉNÁRT ZSUZSANNA SZEGEDI TUDOMÁNYEGYETEM I.SZ. BELGYÓGYÁSZATI KLINIKA A GYOMOR JÓINDULATÚ DAGANATAI ("protrudáló gyomorlaesiók", " gyomorpolypusok") eredetük szerint
3. Az integrált KVTF-ÁNTSZ közös szállópor mérési rendszer működik. A RENDSZER ÁLTAL VÉGZETT MÉRÉSEK EREDMÉNYEI, ÉS AZOK ÉRTÉKELÉSE
 ÁNTSZ Országos Tisztifőorvosi Hivatal Országos Tiszti Főorvos 1097 Budapest, Gyáli út 2 6. 1437 Budapest, Pf. 839 Központ: (1) 476-1100 Telefon: (1) 476-1242 Telefax: (1) 215-4492 E-mail: tisztifoorvos@oth.antsz.hu
ÁNTSZ Országos Tisztifőorvosi Hivatal Országos Tiszti Főorvos 1097 Budapest, Gyáli út 2 6. 1437 Budapest, Pf. 839 Központ: (1) 476-1100 Telefon: (1) 476-1242 Telefax: (1) 215-4492 E-mail: tisztifoorvos@oth.antsz.hu
ÖSSZEFOGLALÁS BEVEZETÉS
 3. ÉVFOLYAM, 5. SZÁM 2007. OKTÓBER JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az adjuváns kezelésként háromhavonta alkalmazott depó leuprorelin-acetát és a cyclophosphamid + methotrexat + fluorouracil
3. ÉVFOLYAM, 5. SZÁM 2007. OKTÓBER JOURNAL OF CLINICAL ONCOLOGY EREDETI KÖZLEMÉNY Az adjuváns kezelésként háromhavonta alkalmazott depó leuprorelin-acetát és a cyclophosphamid + methotrexat + fluorouracil
Ramucirumab egy új gyógyszer az onkológiában
 Ramucirumab egy új gyógyszer az onkológiában Telekes András dr. 1, 2 Deme Dániel 2 1 Bajcsy-Zsilinszky Kórház, Onkológia, Budapest 2 Szent Lázár Megyei Kórház, Onkológia, Salgótarján A ramucirumab egy
Ramucirumab egy új gyógyszer az onkológiában Telekes András dr. 1, 2 Deme Dániel 2 1 Bajcsy-Zsilinszky Kórház, Onkológia, Budapest 2 Szent Lázár Megyei Kórház, Onkológia, Salgótarján A ramucirumab egy
Intézményi jelentés. Összefoglalás. Medgyessy Ferenc Gimnázium és Művészeti Szakközépiskola 4031 Debrecen, Holló László sétány 6 OM azonosító: 031202
 FIT-jelentés :: 2010 Medgyessy Ferenc Gimnázium és Művészeti Szakközépiskola 4031 Debrecen, Holló László sétány 6 Figyelem! A 2010. évi Országos kompetenciaméréstől kezdődően a szövegértés, illetve a matematika
FIT-jelentés :: 2010 Medgyessy Ferenc Gimnázium és Művészeti Szakközépiskola 4031 Debrecen, Holló László sétány 6 Figyelem! A 2010. évi Országos kompetenciaméréstől kezdődően a szövegértés, illetve a matematika
ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL. (2004. III. negyedév) Budapest, 2004. december
 ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL (2004. III. negyedév) Budapest, 2004. december Évközi minta az egészségügyi bér- és létszámstatisztikából Vezet i összefoglaló Módszertan Táblázatok:
ÉVKÖZI MINTA AZ EGÉSZSÉGÜGYI BÉR- ÉS LÉTSZÁMSTATISZTIKÁBÓL (2004. III. negyedév) Budapest, 2004. december Évközi minta az egészségügyi bér- és létszámstatisztikából Vezet i összefoglaló Módszertan Táblázatok:
Jelentéskészítő TEK-IK () Válaszadók száma = 610
 Jelentéskészítő TEK-IK () Válaszadók száma = 0 Általános mutatók Szak értékelése - + átl.=. Felmérés eredmények Jelmagyarázat Kérdésszöveg Válaszok relatív gyakorisága Bal pólus Skála Átl. elt. Átlag Medián
Jelentéskészítő TEK-IK () Válaszadók száma = 0 Általános mutatók Szak értékelése - + átl.=. Felmérés eredmények Jelmagyarázat Kérdésszöveg Válaszok relatív gyakorisága Bal pólus Skála Átl. elt. Átlag Medián
A tüdő adenocarcinomák szubklasszifikációja. Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5.
 A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
Boldva és Vidéke Taka r ékszövetkezet
 A Takarékszövetkezet jelen ben szereplő, változó kamatozású i termékei esetében i kamatváltozást tesz közzé, az állandó (fix) kamatozású i termékek esetében pedig a 2014.06.15-től lekötésre kerülő ekre
A Takarékszövetkezet jelen ben szereplő, változó kamatozású i termékei esetében i kamatváltozást tesz közzé, az állandó (fix) kamatozású i termékek esetében pedig a 2014.06.15-től lekötésre kerülő ekre
Jogszabályváltozások. Érettségi 2015/2016 tanév tavasz. Dr. Kun Ágnes osztályvezető
 Érettségi 2015/2016 tanév tavasz Jogszabályváltozások Dr. Kun Ágnes osztályvezető Jász-Nagykun-Szolnok Megyei Kormányhivatal Oktatási és Hatósági Osztály 2016. április 19. Az érettségi vizsga vizsgaszabályzatának
Érettségi 2015/2016 tanév tavasz Jogszabályváltozások Dr. Kun Ágnes osztályvezető Jász-Nagykun-Szolnok Megyei Kormányhivatal Oktatási és Hatósági Osztály 2016. április 19. Az érettségi vizsga vizsgaszabályzatának
III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó részeinek módosításai
 III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó részeinek módosításai Megjegyzés: Az alkalmazási előírást és a betegtájékoztatót ezt követően az illetékes nemzeti hatóságok a referencia
III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó részeinek módosításai Megjegyzés: Az alkalmazási előírást és a betegtájékoztatót ezt követően az illetékes nemzeti hatóságok a referencia
Boldva és Vidéke Taka r ékszövetkezet
 A Takarékszövetkezet jelen ben szereplő, változó kamatozású i termékei esetében i kamatváltozást tesz közzé, az állandó (fix) kamatozású i termékek esetében pedig a 2014.08.13-tól lekötésre kerülő ekre
A Takarékszövetkezet jelen ben szereplő, változó kamatozású i termékei esetében i kamatváltozást tesz közzé, az állandó (fix) kamatozású i termékek esetében pedig a 2014.08.13-tól lekötésre kerülő ekre
