Egyetemi doktori (PhD) értekezés tézisei PAMAM DENDRIMEREK VIZES OLDATBELI VISELKEDÉSE ÉS KÖLCSÖNHATÁSA KISMOLEKULÁKKAL.
|
|
|
- Dávid Németh
- 8 évvel ezelőtt
- Látták:
Átírás
1 Egyetemi doktori (PhD) értekezés tézisei PAMAM DENDRIMEREK VIZES OLDATBELI VISELKEDÉSE ÉS KÖLCSÖNHATÁSA KISMOLEKULÁKKAL Kéri Mónika Témavezető: Bányai István, egyetemi tanár DEBRECENI EGYETEM Kémiai Tudományok Doktori Iskola Debrecen, 2015
2
3 Kéri Mónika doktori (PhD) értekezés tézisei I. BEVEZETÉS ÉS CÉLKITŰZÉSEK A dendrimerek szabályosan elágazó szerkezetű, mesterséges makromolekulák. A poli(amido-amin) (PAMAM) dendrimerek etiléndiamin és akrilsav egységekből épülnek fel. A monomerek generációkat felépítve hoznak létre nanoméretű, közel gömb alakú makromolekulákat. Az elágazási pontokban tercier aminocsoportok, az ágakon peptidkötések és terminális (primer) aminocsoportok találhatók (1. ábra). A tercier és primer aminok protonálódása révén a molekula akár több mint száz pozitív töltésre is szert tehet. Hidrofil karakterűek, vízben nagyon jól oldódnak. Oldatbeli viselkedésük, kölcsönhatásaik kis molekulákkal, valamint a ph hatása a dendrimerek oldatbeli szerkezetére nagyon fontos az alkalmazhatóság szempontjából. 1. ábra: 2. generációs PAMAM dendrimer felépítése és funkciós csoportjai A PAMAM dendrimerek oldatbeli szerkezetének és a közeggel való kölcsönhatásának a megismerésére eddig neutronszórással nyertek kísérleti adatokat, molekuladinamikai számításokkal pedig modelleket alkottak. A molekulák méretének és belső struktúrájának ph-függő változásával, valamint a molekula belsejében kialakuló üregek méretével kapcsolatban azonban a megalkotott modellek és a kísérleti eredmények különböznek. 1
4 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal A dendrimerek szerepe a gyógyszerkutatásban igen jelentős, mert gyógyszermolekulákkal kölcsönhatásba lépve, mint gyógyszerszállító részecskék, szerepük lehet a rák kemoterápiás kezelésében. A hatóanyag molekulái kovalensen köthetők a végcsoportokra, vagy a feltételezett nanoméretű üregekbe (pl.: hidrofób kölcsönhatással) építhetők be. A dendrimerek polielektrolit jellege miatt fontos és érdekes kérdés a PAMAM dendrimerek ionokkal való kölcsönhatása. Molekuladinamikai szimulációk szerint az ellenionok a dendrimer töltését kompenzálva összehúzzák a struktúrát. A töltött makromolekula viselkedése ellenionok jelenlétében a számos belső töltés miatt nem írható le az ismert formulákkal. Az előállított PAMAM dendrimereket sok esetben foszfát pufferben vizsgálják, és az esetleges orvosi alkalmazás szempontjából is fontos a makromolekulák foszfátionokkal való kölcsönhatásának vizsgálata. A PAMAM dendrimereket gyakorlatilag felfedezésük óta alkalmazzák nanorészecskék templátjaként, hiszen a nanorészecskét kapszulázva vagy sztérikusan stabilizálva, vízoldhatóvá teszik azt. Az arany nanorészecskéket az utóbbi időben igen széles körben kutatják és alkalmazzák számos előnyös tulajdonságuk miatt. Katalizátorként való alkalmazásuk mellett a rákgyógyításban, valamint röntgen és CT (számítógépes tomográfia) képalkotó eljárásokban kontrasztanyagként való felhasználását is vizsgálják. Az arany nanorészecskék 5. generációs PAMAM dendrimerekkel való stabilizálásának módja az irodalom alapján nem egyértelmű. Az olyan polielektrolitok, mint a poli(amido-amin) (PAMAM) dendrimerek, oldatbeli szerkezetének, egyensúlyi folyamatainak, dinamikájának ismerete igen fontos, ezért munkánk során célul tűztük ki az 5. generációs PAMAM dendrimerek oldatbeli viselkedésének, oldószerrel (H 2 O), kisméretű ionokkal (H 3 O +, Au III, PO 4 3- ), molekulákkal (doxorubicin) és kolloidokkal (különböző méretű arany nanorészecskék) való kölcsönhatásának vizsgálatát. Az eredmények tekintetében következtetünk a lehetséges alkalmazásokra. 2
5 Kéri Mónika doktori (PhD) értekezés tézisei II. ALKALMAZOTT VIZSGÁLATI MÓDSZEREK Az 5. generációs (G5) NH 2 -végcsoportú poli(amido-amin) (PAMAM) dendrimer (G5.NH 2, Dendritech) molekula mágneses magrezonanciás (NMR) jellemzését, valamint a különböző kismolekulákkal, kolloidokkal való kölcsönhatásának vizsgálatát Bruker Avance DRX 400 típusú NMR készülékkel végeztük. A spektrumok kiértékelése Mestrec és MestreNova 8.1 szoftverekkel történt. A dendrimer 1 H jeleinek azonosítására és a térbeli szerkezet meghatározására 1 H, 13 C, COSY (Correlation Spectroscopy), NOESY (Nuclear Overhauser Effect Spectroscopy), 13 C és 15 N HMBC (Heteronuclear Multiple Bond Correlation) egy és kétdimenziós spektrumokat vettünk fel a D 2 O-ban feloldott makromolekuláról. A dendrimer molekulák protonálódását 1 H NMR titrálással követtük (ph 2-12,6), az oldat ph értékét DCl és NaOD oldatokkal állítottuk. A dendrimer belső szerkezetének és vízmolekulákkal való kölcsönhatásának vizsgálata során szilárd, szárított dendrimer kristályt vízzel titrálva ( vízmolekula/dendrimer) dendrimergélt hoztunk létre. A gél állagú anyag pórusainak méretét NMR krioporozimetriás módszerrel határoztuk meg, mely során a műanyag NMR csőbe helyezett gélt folyékony nitrogénnel illetve szárított levegővel hűtöttük (239 K legalacsonyabb hőmérséklet, Eurotherm hőmérsékletszabályozó egység, Bruker BSCU V. hűtőegység), és 0,5 K fokonként felvettük a mintában lévő folyadék fázis 1 H NMR spektrumát. Az olvadáspont-csökkenés értékéből a Gibbs-Thomson-egyenlet (1) alapján következtettünk a pórusok méretére. nk c Tm f Tm f T (1) / / r 0 ahol T m/f az olvadás- és fagyáspontcsökkenés, T 0 a tömbfázis és T m/f a pórusba zárt folyadék fázisátmeneti hőmérséklete, K c a közegre jellemző konstans, n geometriai tényező, r a pórus mérete. A PAMAM dendrimer foszfátionokkal való kölcsönhatásának jellemzésére 1 H és 31 P NMR spektrumokat vettünk fel különböző ph 3
6 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal értékeken és foszfát-koncentrációknál. A kívánt ph-értéknek megfelelően változtattuk a Na 2 HPO 4 és NaH 2 PO 4 2H 2 O arányát. T 1 relaxációs, NOESY és DOSY (Diffusion Ordered Spectroscopy) NMR méréseket végeztünk. A dendrimer protonálódását foszfátionok nélkül és jelenlétükben phpotenciometriával is vizsgáltuk (I = 0,2 M KCl, T = 298 K). A dendrimer protonálódási állandóit, a protonált csoportok számát és a foszfátionok jelenlétében kialakult új részecske összetételét a HYPERQUAD számítógépes programmal határoztuk meg. Gyógyszermolekulaként a doxorubicinnal (DOX) való kölcsönhatást vizsgálatuk 3 különböző végcsoporttal (ecetsavval, borostyánkősavval és glicidollal) funkcionalizált PAMAM dendrimer (G5.Ac, G5.SAH és G5.GlyOH) esetében. A DOX-szal való kölcsönhatás lehetőségének vizsgálatához vizes közegű DOX G5.Ac mintát készítettünk, melyet trietil-aminnal semlegesítettünk. A szilárdfázisú DOX dendrimer kompozitok előállítása a következő módon történt: a DOX HCl metanolos oldatát semlegesítés után adtuk a háromféle dendrimer vizes oldatához. Kevertetést és centrifugálást követően a dendrimer DOX komplexeket liofilizáltuk. Oldatbeli viselkedésüket D 2 O-ba visszaoldva, 1 H, DOSY és NOESY NMR kísérletekkel vizsgáltuk. A dendrimerrel stabilizált arany nanorészecske szintézise során elsőként a dendrimer oldatához HAuCl 4 -oldatot adtunk, az Au III -ionokkal töltött dendrimerről 1 H és DOSY NMR spektrumokat vettünk fel. Az Au III redukciója NaBH 4 -del történt. A dendrimer arany hibrid részecskéről 1 H és DOSY NMR spektrumokat készítettünk. Az átlagos diffúziós együtthatókból következtettünk a hibrid részecske hidrodinamikai méretére, melyet az Einstein-Stokes egyenlet (2) segítségével számoltunk: R H = k BT 6πηD (2) ahol R H a hidrodinamikai sugár, k B a Boltzmann-állandó, T a hőmérséklet, η a közeg viszkozitása és D a diffúziós együttható. 4
7 Kéri Mónika doktori (PhD) értekezés tézisei III. ÚJ TUDOMÁNYOS EREDMÉNYEK 1. A G5.NH 2 dendrimer jellemzése, kölcsönhatása az oldószerrel és annak ionjaival 1.1. A G5.NH 2 dendrimer 1 H NMR jeleinek azonosítása: Azonosítottuk a G5.NH 2 dendrimer különböző kémiai környezetben lévő protonjait a molekula 1 H NMR spektrumában, amely az irodalomban sok esetben tévesen szerepel, és átfogó NMR jellemzést készítettünk a makromolekuláról. A dendrimer egy dendronjának CH 2 -csoportjait, az elágazásokat figyelmen kívül hagyva, 1-24 számozással jelöltük (3. ábra). A kémiai környezetet tekintve 6 féle CH 2 -csoportot különítettünk el az ábrán különböző színnel jelölve. A továbbiakban a dendrimer protonjainak azonosítására a külső hat CH 2 -csoport számozását használtuk ppm (t1) ábra: G5.NH 2 dendrimer 1 H NMR spektruma és a jelek azonosítása (10 mg/g dendrimer D 2 O-ban, ph = 10,5, T = 298 K) G0 G1 G2 G3 G4 G5 3. ábra: G5.NH 2 dendrimer CH 2 -csoportjainak számozása. 5
8 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal Az 1 H NMR spektrum (2. ábra) azonosításához COSY, 13 C HMBC és HSQC spektrumokat vettünk fel. A NOESY spektrum alapján térbeli közelséget a skalárisan csatolt protonokon kívül a tercier nitrogének körüli protonok mutattak. 15 N HMBC spektrumon is azonosítottuk a dendrimer három féle típusú N-tartalmú csoportját A G5.NH 2 dendrimer kölcsönhatása vízmolekulákkal, a dendrimergél pórusainak jellemzése: Meghatároztuk a G5.NH 2 dendrimergélben található pórusok méreteloszlását NMR krioporozimetriás módszerrel. Megállapítottuk, hogy a 3,6 és 5,2 nm átlagos átmérőjű pórusokat a dendrimer molekulák közrefogják. Kimutattuk, hogy a dendrimer gélben a víz diffúziója gátolt, a pórusok összefüggőek, faluk átjárható a víz számára vízmolekula/dendrimer aránynál 1,8 és 2,6 nm sugarú pórusokat találtunk a pórusok alakját gömbnek feltételezve (4. ábra) és 3000 vízmolekula/dendrimer aránynál már csak a nagyobb pórusok vannak jelen vízmolekula/dendrimer arány esetén már jelentős részben a tömbfázisú víz detektálható. Ez az eredmény jó egyezést mutat az általunk korábban meghatározott, modelltől függően kb as hidratációs számmal. ΔI% / Δr p ,8 nm ~2,6 nm G5.NH 2 : Víz 1 : 1000 Gauss 1 : 2000 Gauss 1 : 3000 Gauss 1 : 4000 Gauss r p (nm) 4. ábra: Pórusméreteloszlás G5.NH 2 dendrimergélben. 6
9 Kéri Mónika doktori (PhD) értekezés tézisei A pórusméreteket és a dendrimer kb. 6 nm-es átmérőjét figyelembe véve, megállapítottuk, hogy a pórusokat legalább két dendrimer molekula fogja közre. A diffúziós együttható diffúziós idő függése lineáris. A víz diffúziója a víztartalom növekedésével gyorsul, megközelíti a tömbfázisú vízét A G5.NH 2 dendrimer kölcsönhatása oxóniumionokkal: Kétféle módszerrel meghatároztuk a G5 PAMAM dendrimer tercier, N (T) és primer, N (P) aminocsoportjainak csoportállandóit. NMR titrálással igazoltuk a ph-potenciometriával meghatározott csoportállandók hovatartozását, illetve elkülönítettük a különböző helyzetben lévő tercier aminocsoportokat. ph-potenciometriás titrálással a tercier nitrogén esetén pk N(T) = 5,7(2), a primer N-ek esetében pk N(P) = 8,9(2). A protonálódó csoportok száma: 119 db tercier illetve 123 db primer aminocsoport, így megállapítottuk, hogy a dendrimer gyakorlatilag megfelel a megadott szerkezetnek (teljesen szabályos szerkezet esetén: 126 db tercier és 128 db primer aminocsoport). NMR titrálást is végeztünk ph 2-12,6 között. Az NMR titrálással igazoltuk, hogy a G5.NH 2 dendrimer primer aminocsoportjainak protonálódása a ~7,5-10,5 ph-tartományban, míg a tercier aminocsoportok protonálódása ph ~4 és 8,5 között történik. A protonjelek kémiai eltolódásának ph-függő változásából is meghatároztuk a csoportállandókat. A primer aminocsoportok esetében a pk N(P) = 8,7. A tercier nitrogének esetében a jelek megkettőződése alapján megállapítottuk, hogy a tercier aminok egy része kevésbé (pk N(T) = 5,76), másik része erősebben köti a protonokat (pk N(T) = 5,96). Az NMR titrálás során kapott 1 H NMR spektrumsorozat fontos alapot képez a G5.NH 2 dendrimer ph-változással járó reakcióinak NMR vizsgálatához. A spektrum ilyen mértékű, ph-függő változását az irodalomban is sok esetben figyelmen kívül hagyják. 7
10 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal 2. A G5.NH 2 dendrimer kölcsönhatása ionokkal, kismolekulákkal 2.1. Foszfátionok beépülése a G5.NH 2 dendrimer molekulába: Többrétű NMR vizsgálatok alapján megállapítottuk, hogy az oldatbeli szerkezetvizsgálatokban és biológiai vizsgálatokban rendszeresen alkalmazott foszfát puffer (H 2 PO 4 - /HPO 4 2- ) specifikus kölcsönhatásba lép a G5.NH 2 dendrimerrel. A kölcsönhatás mértéke és természete függ a phtól és a koncentráció-viszonyoktól. ph<6 és ph>8 esetben a foszfátionok a dendrimer végcsoportjaival ionpárt képeznek, míg ph = 6-8 között valószínűleg a dendrimer belsejében, N (T) H 2 PO 4 formában kötődnek. a) G5.NH 2 foszfát ph = 6,2 b) G5.NH 2 foszfát ph = 5,8 c) G5.NH 2 ph = 6, HN 24 H 23 N 22 O N + HN O 19 N O NH NH ábra: A G5.NH 2 1 H NMR spektruma foszfátionok jelenlétében (a és b) és azok nélkül (c) (10 mg/g dendrimer D 2 O-ban). A tercier aminocsoportok körüli protonok (19-22) 1 H NMR jeleinek kémiai eltolódása megnő, a jelek kettőződése kifejezettebb foszfátionok hatására (5. ábra). A tercier aminocsoportok protonálódása során eltérő módon viselkednek a külső, 5. generáció protonjai (19-22-es protonok) és a belső tercier nitrogénekhez közeli protonok (1-18-as protonok). A dendrimer szerkezetét ez alapján 3 zónára osztottuk: a primer aminocsoportok és a hozzájuk közeli es CH 2 -csoportok egy külső 8
11 Kéri Mónika doktori (PhD) értekezés tézisei zónát alkotnak. Az átmeneti zónában lévő protonok (5. generáció es protonjai) a kisebb árnyékoltság miatt nagyobb kémiai eltolódásnál jelentkeznek az 1 H NMR spektrumon. A T 1 relaxációs idejük rövidebb (T 1 = 0,33-0,4 s), amit a feltehetően kisebb korrelációs idő, azaz gyorsabb mozgás magyaráz, így NMR jeleik felbontása jobb. A belső zóna protonjai (belső generációk 1-18-as protonjai) kisebb kémiai eltolódású jelet adnak, és T 1 relaxációjuk lassabb (T 1 = 0,39-0,43 s) a protonálódási ph-tartományban, mint az átmeneti zóna protonjaié. Mivel a molekula belsejében helyezkednek el, a csoportok mozgása korlátozott, a rotációskorrelációs idő nagyobb, a jelek felbontása rosszabb. Az aminocsoportok bázicitása megnő foszfátionok jelenlétében. NMR titrálással meghatároztuk a dendrimer tercier és primer aminocsoportjainak csoportállandóit foszfátionok jelenlétében: a kettévált csúcsoknak megfelelően pk N(T) 6,75 illetve 6,5 (az átmeneti és a belső zóna protonjainak kémiai eltolódásából), míg a pk N(P) = 9,7. A foszfát nélküli dendrimerre jellemző pk értékeknél nagyobb csoportállandók arra utalnak, hogy a foszfátionok jelenlétében a dendrimer aminocsoportjai erősebben kötik a protonokat. Megállapítottuk, hogy a foszfátionok egy dinamikai egységet képeznek a dendrimerrel a teljes ph-tartományban. A foszfátionok diffúziója a teljes ph tartományban lassabb a szabad ionokénál, tehát azok egy része együtt mozog a dendrimerrel. Kimutattuk, hogy ph 6-8 tartományban a dendrimer mérete csökken (gyorsabban diffundál). A dendrimer méretcsökkenését azzal magyaráztuk, hogy a belső tercier aminocsoportok 8-nál kisebb ph-n kezdenek protonálódni, pozitív töltésüket a H 2 PO - 4 /HPO 2-4 -ionok leárnyékolják, gátolva a protonált csoportok közötti taszítást (6. ábra). Ebben a ph-tartományban a foszfátionok relaxáció sebessége jelentősen megnő, ami 31 P spektrumokon jelszélesedést okoz. Ezt azzal magyarázzuk, hogy a foszfátionok a dendrimer belsejében is tartózkodnak, aminek következtében a rotációs-korrelációs idejük megnő. Növekvő foszfátion-koncentrációnál a dendrimer mérete tovább csökken. Számításaink szerint akár 145 H 2 PO - 4 /HPO 2-4 -ion is beépülhet a dendrimer molekulába. ph-potenciometriás méréseink azt mutatták, hogy 9
12 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal H-kötés is kialakul a deprotonált tercier aminocsoportok és a dihidrogénfoszfátionok között, N (T) H 2 PO 4 -összetétel szerint. ph ábra: A PAMAM dendrimer szerkezetének változása a hidrogén- és dihidrogén-foszfátionokkal való kölcsönhatás során. ph<6 és ph>8 esetben a foszfátionok relaxációja nem tér el a szabad foszfátionokétól, de a diffúzió sebességük kisebb. Ebből arra következtettünk, hogy a foszfátionok elsősorban a dendrimer végcsoportjainak töltését kompenzálják. Ezt alátámasztja az is, hogy a dendrimer diffúzió sebessége (mérete) közel azonos a szabad dendrimerével G5.NH 2 dendrimer ionpár képzése Au III -ionokkal: Megállapítottuk, hogy a G5.NH 2 PAMAM dendrimer protonált primer aminocsoportjai az Au III -ionokkal ionpárt képeznek, a dendrimerstabilizált aranykolloidok képződését tehát nem előzi meg komplexképződés. Az Au III -ionok ([AuCl x (OH) 4-x ] - ) koncentráció-növekedésével, az egyre savasabb közegben csak a dendrimer külső (23-as és 24-es) CH 2 - csoportjainak 1 H NMR csúcsai mutattak kisebb kémiai eltolódás értéket az adott ph-n az arany nélküli dendrimerhez képest. A nagyobb + árnyékoltság az NH 3 [AuCl x (OH) 4-x ] - ionpár kialakulására enged következtetni. 10
13 Kéri Mónika doktori (PhD) értekezés tézisei 2.3. Különböző módon funkcionalizált G5 PAMAM dendrimerek kölcsönhatása doxorubicinnal (DOX): A doxorubicin nem kovalens, kismértékű kölcsönhatásba lép a funkcionalizált dendrimerekkel. A szilárd preparátumokba viszonylag kevés DOX-ot tudtunk beépíteni. Kimutattuk, hogy az ecetsavval (G5.Ac) és borostyánkősavval (G5.SAH) funkcionalizált G5 PAMAM dendrimerek jelentős mértékben, míg a glicidollal funkcionalizált dendrimer (G5.GlyOH) kevésbé kötötte a DOX-ot. Igazoltuk, hogy a DOX molekulák egy része erősen kötődik a G5.Ac és G5.SAH dendrimer molekulához, együtt mozog azzal. Az erősen kötött és a gyengén kötött vagy szabad doxorubicin molekulák között lassú kémiai csere áll fent az 1 H NMR időskálán, így szeparált csúcsokat látunk a spektrumokon. Az erős kölcsönhatást a belső deprotonált tercier aminocsoportok és a doxorubicin molekulán található hidroxilcsoportok között kialakuló hidrogénkötések okozhatják. A G5.SAH esetében az enyhén lúgos közegben deprotonált karboxil csoportok miatt kialakulhat gyenge elektrosztatikus kölcsönhatás is a pozitívan töltött DOX molekulákkal. A gyengén kötött és szabad DOX molekulák közötti cserefolyamat gyors. Megállapítottuk, hogy a glicidollal (G5.GlyOH) funkcionált dendrimerrel a doxorubicin egy része együtt mozog, de a kölcsönhatást nem tudtuk jellemezni. 3. G5.NH 2 dendrimer kölcsönhatása kolloidokkal 3.1. Arany nanorészecskék stabilizálása G5.NH 2 dendrimer molekulákkal: Megállapítottuk, hogy 3 vagy 4 G5.NH 2 dendrimer fog közre egy arany nanorészecskét, így a kölcsönhatás természete átmenetet képez a sztérikus stabilizálás és a dendrimerbe kapszulázás között. 11
14 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal G5.NH 2 dendrimerrel stabilizált 1,9-2,6 nm-es arany nanorészecskéket vizsgáltunk különböző arany dendrimer arányoknál (25, 50, 75, 100 Au III /G5.NH 2 ). A minták 1 H NMR spektrumain az arany nanorészecskével való kölcsönhatás a makromolekula külső protonjainak kémiai eltolódását változtatja meg, amiből megállapítottuk, hogy az arany nanorészecskék a dendrimer külső rétegével vannak kölcsönhatásban. A transzmissziós elektronmikroszkópos és a diffúzió adatok összevetéséből arra következtettünk, hogy oldatfázisban arany-tartalmú (hibrid nanorészecskék) és szabad dendrimer molekulák vannak egyensúlyban. Közöttük az 1 H NMR kémiai eltolódás skáláján a cserefolyamat gyors. A hibrid részecskék diffúzió együtthatóinak részletes elemzésével arra jutottunk, hogy a hibrid részecskék mérete 8-10 nm. A legvalószínűbb magyarázat az, hogy 3 vagy 4 dendrimer fog közre egy arany nanorészecskét, amely a dendrimer molekulák periférikus részébe épül be (7. ábra). A stabilizálásnak ezt a módját alátámasztják a korábban részletezett NMR krioporozimetriás eredmények is. 7. ábra: 3 illetve 4 G5.NH 2 dendrimerrel stabilizált arany nanorészecske. 12
15 Kéri Mónika doktori (PhD) értekezés tézisei IV. AZ EREDMÉNYEK HASZNOSÍTÁSI LEHETŐSÉGEI A doktori disszertációmban leírt eredmények összességében hozzájárulnak a PAMAM dendrimerek különböző célú felhasználásainak hatékonyabbá tételéhez. A gyógyszermolekulák kapszulázása, kontrasztanyagok szállítása során ismerni kell a kölcsönhatás jellegét, és nem elhanyagolható a közeg, az ott előforduló ionok és a ph hatása sem. A dendrimer méretének jelentős a szerepe ezekben az alkalmazásokban, így minősítési eljárások, analitikai protokollok során is. Az ötödik generációs, leggyakrabban alkalmazott dendrimerek kolloidstabilizáló hatásának részletes ismerete elősegíti a nanorészecskék kapszulázásának tervezését, és annak természetének megértését. Az eredmények bemutatják a legkülönbözőbb NMR módszerek alkalmazhatóságát kolloid rendszerek, és nem dendrimer, polielektrolit jellegű makromolekulák vizsgálatára. A makromolekulákon túl az NMR használható diszperziós kolloidok tanulmányozására is, amelynek mindennapi gyakorlatába beépülhet az NMR diffúziometria. Igazoltuk, hogy az NMR krioporozimetria lágy anyagok pórusméretének meghatározására is felhasználható. 13
16 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal V. TUDOMÁNYOS KÖZLEMÉNYEK Az értekezés alapját képező közlemények: 1. Mónika Kéri, Chen Peng, Xiangyang Shi and István Bányai NMR characterization of G5_PAMAM.NH 2 entrapped atomic and molecular assemblies The Journal of Physical Chemistry B, 2015 Epub változat, nyomtatás előtt (IP:3,377) 2. Zhang M, Guo R, Kéri M, Bányai I, Zheng Y, Cao M, Cao X, Shi X Impact of dendrimer surface functional groups on the release of doxorubicin from dendrimer carriers. The Journal of Physical Chemistry B, 2014, 118 (6), (IP:3,377) független hivatkozások: 1 Egyéb közlemények: 1. Mónika Kéri, László Palcsu, Marianna Túri, Enikő Heim, Andrea Cébely, István Bányai 13 C-NMR Analysis of Cellulose Samples of Different Preparation Methods Cellulose, 2015 Revízió alatt (IP:3,476) 2. István Bányai, Mónika Kéri, Zoltán Nagy, Márta Berka and Lajos P. Balogh Self-diffusion of water and poly(amidoamine) dendrimers in dilute aqueous solutions Soft Matter, 2013, 9, (IP: 4,151) független hivatkozások: 4 3. Kéri Mónika: Milyen halból főzzünk halászlevet? (Hortobágyi halastavakból vett halminták ICP analízise) Természet világa (Természettudományi Közlöny) 131.évf.8.sz Kéri Mónika: A laboratórium régen és most Természet világa (Természettudományi Közlöny) 130.évf.6.sz
17 Kéri Mónika doktori (PhD) értekezés tézisei Poszterek: 1. Zoltán Nagy*, Mónika Kéri*, István Bányai and Lajos Balogh PAMAM dendrimers in solution: Interactions with small molecules and ions 10th International Symposium on Applied Bioinorganic Chemistry, ISABC, September, 2009, Debrecen, Hungary 2. István Bányai*, Mónika Kéri*, Zoltán Nagy, Márta Berka Dynamics and Hydration of PAMAM_G5 dendrimers as PGSE NMR sees EUROMAR 2011 Conference, August, 2011, Frankfurt am Main, Germany Előadások: 1. Kéri Mónika*, Nagy Zoltán, Bányai István, Balogh Lajos PAMAM dendrimerek kölcsönhatása foszfát- és vanadátionokkal vizes oldatban MTA Kolloidkémiai és Anyagtudományi Munkabizottsági Ülés, október , Mátrafüred 2. Bányai István*, Kéri Mónika, Nagy Zoltán, Balogh Lajos Where are the phosphates in PAMAM_NH2 dendrimers? Chemical Speciation in Solution and at Solid/Solution Interfaces, Symposium, September 2010, Umeå University, Umeå, Sweden 3. Kéri Mónika PAMAM dendrimerek kölcsönhatása foszfát- és vanadátionokkal vizes oldatban Doktoranduszok Fóruma, MTA Tudomány Napja konferencia sorozat, november 4., Debrecen 4. Rácz András, Takács Anett, Kócs Tamara, Serra Bendegúz, Kéri Mónika, Tóth Imre, Bányai István* Triklór-etilén oxidációja hidrogén-peroxiddal: katalízis vanádium komplexekkel MKE 1. Nemzeti Konferencia, május , Sopron 15
18 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal 5. Prof István Bányai*, Mónika Kéri, prof Lajos Peter Balogh Interaction of poly(amidoamine) dendrimers with small molecules in dilute aqueous solutions: Multinuclear NMR studies 85th Colloid and Surface Science Symposium June Montreal, Canada 6. Istvan Banyai*, Monika Keri and Lajos P. Balogh Unexpected Dynamic Behavior of Hydrated Poly(Amidoamine) Dendrimers in Dilute Aqueous Solutions:Interaction with Small Molecules. 7th International Dendrimer Symposium (IDS7), June 26 - July 1, 2011, Gaithersburg, Maryland, USA 7. Kéri Mónika*, Bányai István PAMAM dendrimerek kölcsönhatása foszfát- és vanadátionokkal vizes oldatban XXXIV. Kémiai Előadói Napok, november 2-4. Szeged 8. Bányai István*, Kéri Mónika, Nagy Zoltán Unusual NMR methods for colloids évi NMR Munkabizottsági Ülés, május 4-5. Balatonszemes 9. Mónika Kéri*, Zoltán Nagy, Márta Berka, Krisztina László, István Bányai Pore size distribution of RF polymer aerogels and gelated PAMAM dendrimer as seen by NMR cryoporosimetry 10th Conference on Colloid Chemistry, augusztus Budapest 10. Bányai István*, Nagy Zoltán, Kéri Mónika Kolloidok a mágnesben: a szilárd- és folyadékfázis határán évi NMR Munkabizottsági Ülés, május Pécs 11. István Bányai*, Mónika Kéri, Krisztina László and Zoltán Nagy Liquid NMR for solid state structures DCIRM (Debrecen Colloquium on Inorganic Reaction Mechanisms), Debrecen, M Kéri, C Peng, Z Nagy, X Shi, I Bányai* Cavities in G5_PAMAM.NH2 Dendrimer. How do they exist? 8th International Dendrimer Symposium (IDS), Madrid,
19 Kéri Mónika doktori (PhD) értekezés tézisei 13. Mónika Kéri, Zoltán Nagy, István Bányai* Cavities in macromolecules: NMR cryoporometry approach Mini - conference with Attila Szabo, 20 June 2014, Debrecen 14. Mónika Kéri*, István Bányai, Zoltán Nagy Dynamic interaction of phosphate ions with G5 PAMAM dendrimer ECIRM (European Colloquium on Inorganic Reaction Mechanisms), June 2014, Debrecen 15 Kéri Mónika*, Xiangyang Shi, Nagy Zoltán, Bányai István Arany kolloid kapszulázása dendrimerekben: nagy és kisfelbontású NMR vizsgálatok MTA Kolloidkémiai Munkabizottság szeptember , Eger 16. Kéri Mónika*, Bányai István Porózus anyagok jellemzése NMR krioporozimetria és diffúziometria alkalmazásával 3. Környezetkémiai Szimpózium, október 9-10., Lajosmizse * az előadást illetve posztert bemutató személy 17
20 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal Hitelesített publikációs lista: 18
21 19 Kéri Mónika doktori (PhD) értekezés tézisei
22 PAMAM dendrimerek vizes oldatbeli viselkedése és kölcsönhatása kismolekulákkal Köszönetnyilvánítás: A kutatás a TÁMOP A/2-11/ azonosító számú Nemzeti Kiválóság Program című kiemelt projekt által nyújtott személyi támogatással valósult meg. A projekt az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával valósult meg. A kutatás infrastruktúrája a TÁMOP A-11/1/KONV számú ENVIKUT projekt által biztosított forrásból valósult meg. A projekt az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával valósul meg. A kínai kutatócsoporttal való együttműködést a TÉT_12_CN számú kínai-magyar kétoldalú kutatói program támogatta. 20
PAMAM DENDRIMEREK VIZES OLDATBELI VISELKEDÉSE ÉS KÖLCSÖNHATÁSA KISMOLEKULÁKKAL
 DE TTK 1949 PAMAM DENDRIMEREK VIZES OLDATBELI VISELKEDÉSE ÉS KÖLCSÖNHATÁSA KISMOLEKULÁKKAL Egyetemi doktori (PhD) értekezés Kéri Mónika Témavezető: Bányai István, egyetemi tanár DEBRECENI EGYETEM Természettudományi
DE TTK 1949 PAMAM DENDRIMEREK VIZES OLDATBELI VISELKEDÉSE ÉS KÖLCSÖNHATÁSA KISMOLEKULÁKKAL Egyetemi doktori (PhD) értekezés Kéri Mónika Témavezető: Bányai István, egyetemi tanár DEBRECENI EGYETEM Természettudományi
HIDROFIL HÉJ KIALAKÍTÁSA
 HIDROFIL HÉJ KIALAKÍTÁSA POLI(N-IZOPROPIL-AKRILAMID) MIKROGÉL RÉSZECSKÉKEN Róth Csaba Témavezető: Dr. Varga Imre Eötvös Loránd Tudományegyetem, Budapest Természettudományi Kar Kémiai Intézet 2015. december
HIDROFIL HÉJ KIALAKÍTÁSA POLI(N-IZOPROPIL-AKRILAMID) MIKROGÉL RÉSZECSKÉKEN Róth Csaba Témavezető: Dr. Varga Imre Eötvös Loránd Tudományegyetem, Budapest Természettudományi Kar Kémiai Intézet 2015. december
Mikrohullámú abszorbensek vizsgálata
 Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Aerogél alapú gyógyszerszállító rendszerek. Tóth Tünde Anyagtudomány MSc
 Aerogél alapú gyógyszerszállító rendszerek Tóth Tünde Anyagtudomány MSc 2016. 04. 22. 1 A gyógyszerszállítás problémái A hatóanyag nem oldódik megfelelően Szelektivitás hiánya Nem megfelelő eloszlás A
Aerogél alapú gyógyszerszállító rendszerek Tóth Tünde Anyagtudomány MSc 2016. 04. 22. 1 A gyógyszerszállítás problémái A hatóanyag nem oldódik megfelelően Szelektivitás hiánya Nem megfelelő eloszlás A
Reakciókinetika és katalízis
 Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Kolloidstabilitás. Berka Márta 2010/2011/II
 Kolloidstabilitás Berka Márta 2010/2011/II Kolloid stabilitáshoz taszítás kell. Sztérikus stabilizálás V R V S sztérikus stabilizálás: liofil kolloidok alkalmazása védőhatás adszorpció révén (természetes
Kolloidstabilitás Berka Márta 2010/2011/II Kolloid stabilitáshoz taszítás kell. Sztérikus stabilizálás V R V S sztérikus stabilizálás: liofil kolloidok alkalmazása védőhatás adszorpció révén (természetes
XXXVII. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok gyesülete songrád Megyei soportja és a Magyar Kémikusok gyesülete rendezvénye XXXVII. KÉMII LŐÓI NPOK Program és előadás-összefoglalók Szegedi kadémiai izottság Székháza Szeged, 2014.
Magyar Kémikusok gyesülete songrád Megyei soportja és a Magyar Kémikusok gyesülete rendezvénye XXXVII. KÉMII LŐÓI NPOK Program és előadás-összefoglalók Szegedi kadémiai izottság Székháza Szeged, 2014.
4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel
 4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel A kisméretű peptidek közül az oldalláncban negatív töltésű karboxilcsoportokat tartalmazó AspAsp és AspAspAsp ligandumok komplexképződését
4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel A kisméretű peptidek közül az oldalláncban negatív töltésű karboxilcsoportokat tartalmazó AspAsp és AspAspAsp ligandumok komplexképződését
Pórusos polimer gélek szintézise és vizsgálata és mi a közük a sörgyártáshoz
 Pórusos polimer gélek szintézise és vizsgálata és mi a közük a sörgyártáshoz Póta Kristóf Eger, Dobó István Gimnázium Témavezető: Fodor Csaba és Szabó Sándor "AKI KÍVÁNCSI KÉMIKUS" NYÁRI KUTATÓTÁBOR MTA
Pórusos polimer gélek szintézise és vizsgálata és mi a közük a sörgyártáshoz Póta Kristóf Eger, Dobó István Gimnázium Témavezető: Fodor Csaba és Szabó Sándor "AKI KÍVÁNCSI KÉMIKUS" NYÁRI KUTATÓTÁBOR MTA
Általános Kémia. Sav-bázis egyensúlyok. Ecetsav és sósav elegye. Gyenge sav és erős sav keveréke. Példa8-1. Példa 8-1
 Sav-bázis egyensúlyok 8-1 A közös ion effektus 8-1 A közös ion effektus 8-2 ek 8-3 Indikátorok 8- Semlegesítési reakció, titrálási görbe 8-5 Poliprotikus savak oldatai 8-6 Sav-bázis egyensúlyi számítások,
Sav-bázis egyensúlyok 8-1 A közös ion effektus 8-1 A közös ion effektus 8-2 ek 8-3 Indikátorok 8- Semlegesítési reakció, titrálási görbe 8-5 Poliprotikus savak oldatai 8-6 Sav-bázis egyensúlyi számítások,
Mikrohullámú abszorbensek vizsgálata 4. félév
 Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata 4. félév Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata 4. félév Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Új típusú csillag kopolimerek előállítása és funkcionalizálása. Doktori értekezés tézisei. Szanka Amália
 Új típusú csillag kopolimerek előállítása és funkcionalizálása Doktori értekezés tézisei Szanka Amália Eötvös Loránd Tudományegyetem, Természettudományi Kar Kémia Doktori Iskola Szintetikus kémia, anyagtudomány,
Új típusú csillag kopolimerek előállítása és funkcionalizálása Doktori értekezés tézisei Szanka Amália Eötvös Loránd Tudományegyetem, Természettudományi Kar Kémia Doktori Iskola Szintetikus kémia, anyagtudomány,
VILÁGÍTÓ GYÓGYHATÁSÚ ALKALOIDOK
 VILÁGÍTÓ GYÓGYHATÁSÚ ALKALIDK Biczók László, Miskolczy Zsombor, Megyesi Mónika, Harangozó József Gábor MTA Természettudományi Kutatóközpont Anyag- és Környezetkémiai Intézet Hordozóanyaghoz kötődés fluoreszcenciás
VILÁGÍTÓ GYÓGYHATÁSÚ ALKALIDK Biczók László, Miskolczy Zsombor, Megyesi Mónika, Harangozó József Gábor MTA Természettudományi Kutatóközpont Anyag- és Környezetkémiai Intézet Hordozóanyaghoz kötődés fluoreszcenciás
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Kémiai reakciók. Közös elektronpár létrehozása. Általános és szervetlen kémia 10. hét. Elızı héten elsajátítottuk, hogy.
 Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Javítókulcs (Kémia emelt szintű feladatsor)
 Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. C 2. B. fenolos hidroxilcsoport, éter, tercier amin db. ; 2 db. 4. észter 5. E 6. A tercier amino-nitrogén. 7. Pl. a trimetil-amin reakciója HCl-dal.
Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. C 2. B. fenolos hidroxilcsoport, éter, tercier amin db. ; 2 db. 4. észter 5. E 6. A tercier amino-nitrogén. 7. Pl. a trimetil-amin reakciója HCl-dal.
XXXVI. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVI. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVI. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Ciklodextrinek alkalmazási lehetőségei kolloid diszperz rendszerekben
 Ciklodextrinek alkalmazási lehetőségei kolloid diszperz rendszerekben Vázlat I. Diszperziós kolloidok stabilitása általános ismérvek II. Ciklodextrinek és kolloidok kölcsönhatása - szorpció - zárványkomplex-képződés
Ciklodextrinek alkalmazási lehetőségei kolloid diszperz rendszerekben Vázlat I. Diszperziós kolloidok stabilitása általános ismérvek II. Ciklodextrinek és kolloidok kölcsönhatása - szorpció - zárványkomplex-képződés
Szerkesztették Laufer Noémi SZTE TTIK Alkalmazott és Környezeti Kémiai Tanszék Endrődi Balázs SZTE TTIK Fizikai Kémiai és Anyagtudományi Tanszék
 Szerkesztették Laufer Noémi SZTE TTIK Alkalmazott és Környezeti Kémiai Tanszék Endrődi Balázs SZTE TTIK Fizikai Kémiai és Anyagtudományi Tanszék ISBN 978 963 315 06 7 KALCIUM-HIDROXID OLDHATÓSÁGA LÚGOS
Szerkesztették Laufer Noémi SZTE TTIK Alkalmazott és Környezeti Kémiai Tanszék Endrődi Balázs SZTE TTIK Fizikai Kémiai és Anyagtudományi Tanszék ISBN 978 963 315 06 7 KALCIUM-HIDROXID OLDHATÓSÁGA LÚGOS
CO 2 aktiválás - a hidrogén tárolásban
 CO 2 aktiválás a hidrogén tárolásban PAPP Gábor 1, HORVÁTH Henrietta 1, PURGEL Mihály 1, BARANYI Attila 2, JOÓ Ferenc 1,2 1 MTADE Homogén Katalízis és Reakciómechanizmusok Kutatócsoport, 4032 Debrecen,
CO 2 aktiválás a hidrogén tárolásban PAPP Gábor 1, HORVÁTH Henrietta 1, PURGEL Mihály 1, BARANYI Attila 2, JOÓ Ferenc 1,2 1 MTADE Homogén Katalízis és Reakciómechanizmusok Kutatócsoport, 4032 Debrecen,
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 2. előadás: 1/18 Kinetika: Kísérletekkel megállapított sebességi egyenlet(ek). A kémiai reakció makroszkópikus, fenomenológikus jellemzése. 1 Mechanizmus: Az elemi lépések
Reakciókinetika és katalízis 2. előadás: 1/18 Kinetika: Kísérletekkel megállapított sebességi egyenlet(ek). A kémiai reakció makroszkópikus, fenomenológikus jellemzése. 1 Mechanizmus: Az elemi lépések
PhD DISSZERTÁCIÓ TÉZISEI
 Budapesti Muszaki és Gazdaságtudományi Egyetem Fizikai Kémia Tanszék MTA-BME Lágy Anyagok Laboratóriuma PhD DISSZERTÁCIÓ TÉZISEI Mágneses tér hatása kompozit gélek és elasztomerek rugalmasságára Készítette:
Budapesti Muszaki és Gazdaságtudományi Egyetem Fizikai Kémia Tanszék MTA-BME Lágy Anyagok Laboratóriuma PhD DISSZERTÁCIÓ TÉZISEI Mágneses tér hatása kompozit gélek és elasztomerek rugalmasságára Készítette:
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén
 ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Badari Andrea Cecília
 Nagy nitrogéntartalmú bio-olajokra jellemző modellvegyületek katalitikus hidrodenitrogénezése Badari Andrea Cecília MTA Természettudományi Kutatóközpont, Anyag- és Környezetkémiai Intézet, Környezetkémiai
Nagy nitrogéntartalmú bio-olajokra jellemző modellvegyületek katalitikus hidrodenitrogénezése Badari Andrea Cecília MTA Természettudományi Kutatóközpont, Anyag- és Környezetkémiai Intézet, Környezetkémiai
Sav bázis egyensúlyok vizes oldatban
 Sav bázis egyensúlyok vizes oldatban Disszociációs egyensúlyi állandó HAc H + + Ac - ecetsav disszociációja [H + ] [Ac - ] K sav = [HAc] NH 4 OH NH 4 + + OH - [NH + 4 ] [OH - ] K bázis = [ NH 4 OH] Ammóniumhidroxid
Sav bázis egyensúlyok vizes oldatban Disszociációs egyensúlyi állandó HAc H + + Ac - ecetsav disszociációja [H + ] [Ac - ] K sav = [HAc] NH 4 OH NH 4 + + OH - [NH + 4 ] [OH - ] K bázis = [ NH 4 OH] Ammóniumhidroxid
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Készítette: NÁDOR JUDIT. Témavezető: Dr. HOMONNAY ZOLTÁN. ELTE TTK, Analitikai Kémia Tanszék 2010
 Készítette: NÁDOR JUDIT Témavezető: Dr. HOMONNAY ZOLTÁN ELTE TTK, Analitikai Kémia Tanszék 2010 Bevezetés, célkitűzés Mössbauer-spektroszkópia Kísérleti előzmények Mérések és eredmények Összefoglalás EDTA
Készítette: NÁDOR JUDIT Témavezető: Dr. HOMONNAY ZOLTÁN ELTE TTK, Analitikai Kémia Tanszék 2010 Bevezetés, célkitűzés Mössbauer-spektroszkópia Kísérleti előzmények Mérések és eredmények Összefoglalás EDTA
AZ AEROSZOL RÉSZECSKÉK HIGROSZKÓPOS TULAJDONSÁGA. Imre Kornélia Kémiai és Környezettudományi Doktori Iskola
 AZ AEROSZOL RÉSZECSKÉK HIGROSZKÓPOS TULAJDONSÁGA Doktori (PhD) értekezés tézisei Imre Kornélia Kémiai és Környezettudományi Doktori Iskola Konzulens: Dr. Molnár Ágnes tudományos főmunkatárs Pannon Egyetem
AZ AEROSZOL RÉSZECSKÉK HIGROSZKÓPOS TULAJDONSÁGA Doktori (PhD) értekezés tézisei Imre Kornélia Kémiai és Környezettudományi Doktori Iskola Konzulens: Dr. Molnár Ágnes tudományos főmunkatárs Pannon Egyetem
Az élethez szükséges elemek
 Az élethez szükséges elemek 92 elemből kb. 25 szükséges az élethez Szén (C), hidrogén (H), oxigén (O) és nitrogén (N) alkotja az élő szervezetekben előforduló anyag 96%-t A fennmaradó 4% legnagyobb része
Az élethez szükséges elemek 92 elemből kb. 25 szükséges az élethez Szén (C), hidrogén (H), oxigén (O) és nitrogén (N) alkotja az élő szervezetekben előforduló anyag 96%-t A fennmaradó 4% legnagyobb része
Kolloidkémia 1. előadás Első- és másodrendű kémiai kötések és szerepük a kolloid rendszerek kialakulásában. Szőri Milán: Kolloidkémia
 Kolloidkémia 1. előadás Első- és másodrendű kémiai kötések és szerepük a kolloid rendszerek kialakulásában 1 Órarend 2 Kurzussal kapcsolatos emlékeztető Kurzus: Az előadás látogatása ajánlott Gyakorlat
Kolloidkémia 1. előadás Első- és másodrendű kémiai kötések és szerepük a kolloid rendszerek kialakulásában 1 Órarend 2 Kurzussal kapcsolatos emlékeztető Kurzus: Az előadás látogatása ajánlott Gyakorlat
4.3. Az AcLysSerProValValGluGly heptapeptid Al(III)-kötő sajátságának jellemzése
 4.3. Az AcLysProValValGly heptapeptid Al(III)-kötő sajátságának jellemzése Az Al(III)fehérje kölcsönhatás megismerése céljából olyan neurofilamentum peptidfragmenst vizsgáltunk, mely az oldalláncban oxigén
4.3. Az AcLysProValValGly heptapeptid Al(III)-kötő sajátságának jellemzése Az Al(III)fehérje kölcsönhatás megismerése céljából olyan neurofilamentum peptidfragmenst vizsgáltunk, mely az oldalláncban oxigén
DOKTORI ÉRTEKEZÉS TÉZISEI HÁROMFÁZISÚ MEGOSZLÁS ALKALMAZÁSA ÉLELMISZERFEHÉRJÉKVIZSGÁLATÁBAN
 DOKTORI ÉRTEKEZÉS TÉZISEI HÁROMFÁZISÚ MEGOSZLÁS ALKALMAZÁSA ÉLELMISZERFEHÉRJÉKVIZSGÁLATÁBAN Szamos Jenő KÖZPONTI ÉLELMISZER-TUDOMÁNYI KUTATÓINTÉZET Budapest 2004 A doktori iskola megnevezése: tudományága:
DOKTORI ÉRTEKEZÉS TÉZISEI HÁROMFÁZISÚ MEGOSZLÁS ALKALMAZÁSA ÉLELMISZERFEHÉRJÉKVIZSGÁLATÁBAN Szamos Jenő KÖZPONTI ÉLELMISZER-TUDOMÁNYI KUTATÓINTÉZET Budapest 2004 A doktori iskola megnevezése: tudományága:
KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont. HCl (1 pont) HCO 3 - (1 pont) Ca 2+ (1 pont) Al 3+ (1 pont) Fe 3+ (1 pont) H 2 O (1 pont)
 KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont 1. Adja meg a következő ionok nevét, illetve képletét! (12 pont) Az ion neve Kloridion Az ion képlete Cl - (1 pont) Hidroxidion (1 pont) OH - Nitrátion NO
KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont 1. Adja meg a következő ionok nevét, illetve képletét! (12 pont) Az ion neve Kloridion Az ion képlete Cl - (1 pont) Hidroxidion (1 pont) OH - Nitrátion NO
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz november 30. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr) Róka
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz november 30. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr) Róka
Oldódás, mint egyensúly
 Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott =
Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott =
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával. www.chem.elte.hu/pr
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1) Mikor kapott Paul Ehrlich orvosi Nobel-díjat? A) Idén. B) Pont 100 éve, 1908-ban. C) Nem
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1) Mikor kapott Paul Ehrlich orvosi Nobel-díjat? A) Idén. B) Pont 100 éve, 1908-ban. C) Nem
Speciális fluoreszcencia spektroszkópiai módszerek
 Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2000
 Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
. -. - Baris A. - Varga G. - Ratter K. - Radi Zs. K.
 2. TEREM KEDD Orbulov Imre 09:00 Bereczki P. -. - Varga R. - Veres A. 09:20 Mucsi A. 09:40 Karacs G. 10:00 Cseh D. Benke M. Mertinger V. 10:20 -. 10:40 14 1. TEREM KEDD Hargitai Hajnalka 11:00 I. 11:20
2. TEREM KEDD Orbulov Imre 09:00 Bereczki P. -. - Varga R. - Veres A. 09:20 Mucsi A. 09:40 Karacs G. 10:00 Cseh D. Benke M. Mertinger V. 10:20 -. 10:40 14 1. TEREM KEDD Hargitai Hajnalka 11:00 I. 11:20
KARBONSAV-SZÁRMAZÉKOK
 KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
A POLIELEKTROLIT/TENZID ASSZOCIÁCIÓ SZABÁLYOZÁSA NEMIONOS TENZIDEK ÉS POLIMEREK SEGÍTSÉGÉVEL
 Doktori értekezés tézisei A POLIELEKTROLIT/TENZID ASSZOCIÁCIÓ SZABÁLYOZÁSA NEMIONOS TENZIDEK ÉS POLIMEREK SEGÍTSÉGÉVEL FEGYVER EDIT Témavezető: Dr. Mészáros Róbert, egyetemi docens Kémia Doktori Iskola
Doktori értekezés tézisei A POLIELEKTROLIT/TENZID ASSZOCIÁCIÓ SZABÁLYOZÁSA NEMIONOS TENZIDEK ÉS POLIMEREK SEGÍTSÉGÉVEL FEGYVER EDIT Témavezető: Dr. Mészáros Róbert, egyetemi docens Kémia Doktori Iskola
AZ ANYAGI HALMAZOK ÉS A MÁSODLAGOS KÖTÉSEK. Rausch Péter kémia-környezettan
 AZ ANYAGI HALMAZOK ÉS A MÁSODLAGOS KÖTÉSEK Rausch Péter kémia-környezettan Hogy viselkedik az ember egyedül? A kémiában ritkán tudunk egyetlen részecskét vizsgálni! - az anyagi részecske tudja hogy kell
AZ ANYAGI HALMAZOK ÉS A MÁSODLAGOS KÖTÉSEK Rausch Péter kémia-környezettan Hogy viselkedik az ember egyedül? A kémiában ritkán tudunk egyetlen részecskét vizsgálni! - az anyagi részecske tudja hogy kell
a) H 3 PO 4 pk a értékeinek meghatározására, b) üdítőital foszfor tartalmának meghatározására, c) pirofoszfát bomlásának követésére Dr.
 31 P NMR spektroszkópia alkalmazása: a) H 3 PO 4 pk a értékeinek meghatározására, b) üdítőital foszfor tartalmának meghatározására, c) pirofoszfát bomlásának követésére Dr. Bodor Andrea Bevezetés: A 31
31 P NMR spektroszkópia alkalmazása: a) H 3 PO 4 pk a értékeinek meghatározására, b) üdítőital foszfor tartalmának meghatározására, c) pirofoszfát bomlásának követésére Dr. Bodor Andrea Bevezetés: A 31
Az elektromos kettősréteg. Az elektromos potenciálkülönbség eredete, értéke és az azt befolyásoló tényezők. Kolloidok stabilitása.
 Az elektromos kettősréteg. Az elektromos potenciálkülönbség eredete, értéke és az azt befolyásoló tényezők. Kolloidok stabilitása. Adszorpció oldatból szilárd felületre Adszorpció oldatból Nem-elektrolitok
Az elektromos kettősréteg. Az elektromos potenciálkülönbség eredete, értéke és az azt befolyásoló tényezők. Kolloidok stabilitása. Adszorpció oldatból szilárd felületre Adszorpció oldatból Nem-elektrolitok
23. Indikátorok disszociációs állandójának meghatározása spektrofotometriásan
 23. Indikátorok disszociációs állandójának meghatározása spektrofotometriásan 1. Bevezetés Sav-bázis titrálások végpontjelzésére (a mőszeres indikáció mellett) ma is gyakran alkalmazunk festék indikátorokat.
23. Indikátorok disszociációs állandójának meghatározása spektrofotometriásan 1. Bevezetés Sav-bázis titrálások végpontjelzésére (a mőszeres indikáció mellett) ma is gyakran alkalmazunk festék indikátorokat.
Oldódás, mint egyensúly
 Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott K
Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott K
Polimer nanokompozitok; előállítás, szerkezet és tulajdonságok
 Budapesti Műszaki és Gazdaságtudományi Egyetem Műanyag- és Gumiipari Tanszék Polimer nanokompozitok; előállítás, szerkezet és tulajdonságok PhD értekezés tézisei Készítette: Pozsgay András György Témavezető:
Budapesti Műszaki és Gazdaságtudományi Egyetem Műanyag- és Gumiipari Tanszék Polimer nanokompozitok; előállítás, szerkezet és tulajdonságok PhD értekezés tézisei Készítette: Pozsgay András György Témavezető:
ÖNSZERVEZŐDŐ AMFIFILIKUS OLIGOMEREK
 Természettudományi és Technológiai Kar ÖNSZERVEZŐDŐ AMFIFILIKUS OLIGOMEREK SELF-ASSEMBLY BEHAVIOR OF AMPHIPHILIC OLIGOMERS doktori (PhD) értekezés tézisei Szöllősi László Zsolt Témavezető: Dr. Zsuga Miklós
Természettudományi és Technológiai Kar ÖNSZERVEZŐDŐ AMFIFILIKUS OLIGOMEREK SELF-ASSEMBLY BEHAVIOR OF AMPHIPHILIC OLIGOMERS doktori (PhD) értekezés tézisei Szöllősi László Zsolt Témavezető: Dr. Zsuga Miklós
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
Spektroszkópiai módszerek 2.
 Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
LABORATÓRIUMI PIROLÍZIS ÉS A PIROLÍZIS-TERMÉKEK NÉHÁNY JELLEMZŐJÉNEK VIZSGÁLATA
 LABORATÓRIUMI PIROLÍZIS ÉS A PIROLÍZIS-TERMÉKEK NÉHÁNY JELLEMZŐJÉNEK VIZSGÁLATA TOLNERLászló -CZINKOTAImre -SIMÁNDIPéter RÁCZ Istvánné - SOMOGYI Ferenc Mit vizsgáltunk? TSZH - Települési szilárd hulladék,
LABORATÓRIUMI PIROLÍZIS ÉS A PIROLÍZIS-TERMÉKEK NÉHÁNY JELLEMZŐJÉNEK VIZSGÁLATA TOLNERLászló -CZINKOTAImre -SIMÁNDIPéter RÁCZ Istvánné - SOMOGYI Ferenc Mit vizsgáltunk? TSZH - Települési szilárd hulladék,
Többértékű savak és bázisok Többértékű savnak/lúgnak azokat az oldatokat nevezzük, amelyek több protont képesek leadni/felvenni.
 ELEKTROLIT EGYENSÚLYOK : ph SZÁMITÁS Általános ismeretek A savak vizes oldatban protont adnak át a vízmolekuláknak és így megnövelik az oldat H + (pontosabban oxónium - H 3 O + ) ion koncentrációját. Erős
ELEKTROLIT EGYENSÚLYOK : ph SZÁMITÁS Általános ismeretek A savak vizes oldatban protont adnak át a vízmolekuláknak és így megnövelik az oldat H + (pontosabban oxónium - H 3 O + ) ion koncentrációját. Erős
Szakértesítő 1 Interkerám szakmai füzetek A folyósító szerek viselkedése a kerámia anyagokban
 Szakértesítő 1 Interkerám szakmai füzetek A folyósító szerek viselkedése a kerámia anyagokban A folyósító szerek viselkedése a kerámia anyagokban Bevezetés A kerámia masszák folyósításkor fő cél az anyag
Szakértesítő 1 Interkerám szakmai füzetek A folyósító szerek viselkedése a kerámia anyagokban A folyósító szerek viselkedése a kerámia anyagokban Bevezetés A kerámia masszák folyósításkor fő cél az anyag
Diffúzió. Diffúzió. Diffúzió. Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
 Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Közös elektronpár létrehozása
 Kémiai reakciók 10. hét a reagáló részecskék között közös elektronpár létrehozása valósul meg sav-bázis reakciók komplexképződés elektronátadás és átvétel történik redoxi reakciók Közös elektronpár létrehozása
Kémiai reakciók 10. hét a reagáló részecskék között közös elektronpár létrehozása valósul meg sav-bázis reakciók komplexképződés elektronátadás és átvétel történik redoxi reakciók Közös elektronpár létrehozása
Doktori értekezés KATIONOS POLIELEKTROLITOK ÉS ANIONOS TENZIDEK KÖZÖTTI KÖLCSÖNHATÁS
 Doktori értekezés KATIONOS POLIELEKTROLITOK ÉS ANIONOS TENZIDEK KÖZÖTTI KÖLCSÖNHATÁS Készítette: MEZEI AMÁLIA Eötvös Loránd Tudományegyetem Kémiai Intézet, Fizikai Kémiai Tanszék Határfelületi- és Nanoszerkezetek
Doktori értekezés KATIONOS POLIELEKTROLITOK ÉS ANIONOS TENZIDEK KÖZÖTTI KÖLCSÖNHATÁS Készítette: MEZEI AMÁLIA Eötvös Loránd Tudományegyetem Kémiai Intézet, Fizikai Kémiai Tanszék Határfelületi- és Nanoszerkezetek
A diffúzió leírása az anyagmennyiség időbeli változásával A diffúzió leírása a koncentráció térbeli változásával
 Kapcsolódó irodalom: Kapcsolódó multimédiás anyag: Az előadás témakörei: 1.A diffúzió fogalma 2. A diffúzió biológiai jelentősége 3. A részecskék mozgása 3.1. A Brown mozgás 4. Mitől függ a diffúzió erőssége?
Kapcsolódó irodalom: Kapcsolódó multimédiás anyag: Az előadás témakörei: 1.A diffúzió fogalma 2. A diffúzió biológiai jelentősége 3. A részecskék mozgása 3.1. A Brown mozgás 4. Mitől függ a diffúzió erőssége?
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
ATOMEMISSZIÓS SPEKTROSZKÓPIA
 ATOMEMISSZIÓS SPEKTROSZKÓPIA Elvi jellemzők, amelyek meghatározzák a készülék felépítését magas hőmérsékletű fényforrás (elsősorban plazma, szikra, stb.) kis méretű sugárforrás (az önabszorpció csökkentése
ATOMEMISSZIÓS SPEKTROSZKÓPIA Elvi jellemzők, amelyek meghatározzák a készülék felépítését magas hőmérsékletű fényforrás (elsősorban plazma, szikra, stb.) kis méretű sugárforrás (az önabszorpció csökkentése
Molekulák alakja és polaritása, a molekulák között működő legerősebb kölcsönhatás
 Molekulák alakja és polaritása, a molekulák között működő legerősebb kölcsönhatás I. Egyatomos molekulák He, Ne, Ar, Kr, Xe, Rn - a molekula alakja: pontszerű - a kovalens kötés polaritása: NINCS kötés
Molekulák alakja és polaritása, a molekulák között működő legerősebb kölcsönhatás I. Egyatomos molekulák He, Ne, Ar, Kr, Xe, Rn - a molekula alakja: pontszerű - a kovalens kötés polaritása: NINCS kötés
Fluorozott ruténium tartalmú katalizátorok előállítása és alkalmazása transzfer-hidrogénezési reakciókban
 ELTE TTK, Környezettan BSc, Szakdolgozat védés Budapest, 2013. június 17. 1/11 luorozott ruténium tartalmú katalizátorok előállítása és alkalmazása transzfer-hidrogénezési reakciókban öldesi Marcella ELTE
ELTE TTK, Környezettan BSc, Szakdolgozat védés Budapest, 2013. június 17. 1/11 luorozott ruténium tartalmú katalizátorok előállítása és alkalmazása transzfer-hidrogénezési reakciókban öldesi Marcella ELTE
Modellvizsgálatok a természetes vizek arzénmentesítésére
 Modellvizsgálatok a természetes vizek arzénmentesítésére Készítette: Kauker Zsófia Témavezető: Oltiné dr. Varga Margit 2012. Tartalomjegyzék 1. Bevezetés 2. Irodalmi áttekintés 2.1 Az arzén 2.2 Az arzénmentesítés
Modellvizsgálatok a természetes vizek arzénmentesítésére Készítette: Kauker Zsófia Témavezető: Oltiné dr. Varga Margit 2012. Tartalomjegyzék 1. Bevezetés 2. Irodalmi áttekintés 2.1 Az arzén 2.2 Az arzénmentesítés
DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI MOLIBDÉN TARTALMÚ POLIIZOBUTILÉN-POLIBOROSTYÁNKŐSAV ALAPÚ MOTOROLAJ ADALÉKOK ELŐÁLLÍTÁSA ÉS VIZSGÁLATA
 DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI MOLIBDÉN TARTALMÚ POLIIZOBUTILÉN-POLIBOROSTYÁNKŐSAV ALAPÚ MOTOROLAJ ADALÉKOK ELŐÁLLÍTÁSA ÉS VIZSGÁLATA Készítette: Kis Gábor Témavezető: Dr. Bartha László Vegyészmérnöki
DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI MOLIBDÉN TARTALMÚ POLIIZOBUTILÉN-POLIBOROSTYÁNKŐSAV ALAPÚ MOTOROLAJ ADALÉKOK ELŐÁLLÍTÁSA ÉS VIZSGÁLATA Készítette: Kis Gábor Témavezető: Dr. Bartha László Vegyészmérnöki
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
XL. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XL. KÉMIAI ELŐADÓI NAPOK Szegedi Akadémiai Bizottság Székháza Szeged, 2017. október 16-18. Szerkesztették:
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XL. KÉMIAI ELŐADÓI NAPOK Szegedi Akadémiai Bizottság Székháza Szeged, 2017. október 16-18. Szerkesztették:
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
Válasz Tombácz Etelkának az MTA doktorának disszertációmról készített bírálatában feltett kérdéseire és megjegyzéseire
 Válasz Tombácz Etelkának az MTA doktorának disszertációmról készített bírálatában feltett kérdéseire és megjegyzéseire Tisztelt Professzor nő! Először bírálatában feltett kérdéseire válaszolok majd a bírálatban
Válasz Tombácz Etelkának az MTA doktorának disszertációmról készített bírálatában feltett kérdéseire és megjegyzéseire Tisztelt Professzor nő! Először bírálatában feltett kérdéseire válaszolok majd a bírálatban
Diffúzió. Diffúzió sebessége: gáz > folyadék > szilárd (kötőerő)
 Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Fogorvosi anyagtan fizikai alapjai 2.
 Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok Kiemelt témák: Viszkozitás Víz és nyál Kristályok - apatit Polimorfizmus Kristályhibák
Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok Kiemelt témák: Viszkozitás Víz és nyál Kristályok - apatit Polimorfizmus Kristályhibák
MTA DOKTORI ÉRTEKEZÉS
 MTA DOKTORI ÉRTEKEZÉS ELLENTÉTES TÖLTÉSŐ POLIELEKTROLITOK ÉS TENZIDEK ASSZOCIÁCIÓJA Mészáros Róbert Eötvös Loránd Tudományegyetem Kémiai Intézet Budapest, 2009. december Köszönetnyilvánítás Ezúton szeretném
MTA DOKTORI ÉRTEKEZÉS ELLENTÉTES TÖLTÉSŐ POLIELEKTROLITOK ÉS TENZIDEK ASSZOCIÁCIÓJA Mészáros Róbert Eötvös Loránd Tudományegyetem Kémiai Intézet Budapest, 2009. december Köszönetnyilvánítás Ezúton szeretném
Számítástudományi Tanszék Eszterházy Károly Főiskola.
 Networkshop 2005 k Geda,, GáborG Számítástudományi Tanszék Eszterházy Károly Főiskola gedag@aries.ektf.hu 1 k A mérés szempontjából a számítógép aktív: mintavételezés, kiértékelés passzív: szerepe megjelenítés
Networkshop 2005 k Geda,, GáborG Számítástudományi Tanszék Eszterházy Károly Főiskola gedag@aries.ektf.hu 1 k A mérés szempontjából a számítógép aktív: mintavételezés, kiértékelés passzív: szerepe megjelenítés
Membránszerkezet Nyugalmi membránpotenciál
 Membránszerkezet Nyugalmi membránpotenciál 2011.11.15. A biológiai membránok fő komponense. Foszfolipidek foszfolipid = diglicerid + foszfát csoport + szerves molekula (pl. kolin). Poláros fej (hidrofil)
Membránszerkezet Nyugalmi membránpotenciál 2011.11.15. A biológiai membránok fő komponense. Foszfolipidek foszfolipid = diglicerid + foszfát csoport + szerves molekula (pl. kolin). Poláros fej (hidrofil)
Anyagvizsgálati módszerek Elektroanalitika. Anyagvizsgálati módszerek
 Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
Az atom- olvasni. 1. ábra Az atom felépítése 1. Az atomot felépítő elemi részecskék. Proton, Jele: (p+) Neutron, Jele: (n o )
 Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
NMR a peptid- és fehérje-kutatásban
 NMR a peptid- és fehérje-kutatásban A PDB adatbázisban megtalálható NMR alapú fehérjeszerkezetek számának alakulása az elmúlt évek során 4000 3500 3000 2500 2000 1500 1000 500 0 1987 1988 1989 1990 1991
NMR a peptid- és fehérje-kutatásban A PDB adatbázisban megtalálható NMR alapú fehérjeszerkezetek számának alakulása az elmúlt évek során 4000 3500 3000 2500 2000 1500 1000 500 0 1987 1988 1989 1990 1991
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Szacharóz OH HO O O OH HO O OH HO OH HO 1
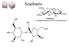 Szacharóz 1 A jelek átfedése miatt oldószer váltás DMS helyett D2 Measured by... Evaluated by... NMR-01 Bruker Avance-500 103.59 92.08 81.28 DEPTq 300K ns=1k D2 115 110 105 100 95 90 85 80 75 70 65 60
Szacharóz 1 A jelek átfedése miatt oldószer váltás DMS helyett D2 Measured by... Evaluated by... NMR-01 Bruker Avance-500 103.59 92.08 81.28 DEPTq 300K ns=1k D2 115 110 105 100 95 90 85 80 75 70 65 60
Válasz Prof. Dr. Tombácz Etelka Ellentétes töltésű polielektrolitok és tenzidek asszociációja című MTA doktori értekezésre adott bírálatára
 Válasz Prof. Dr. Tombácz Etelka Ellentétes töltésű polielektrolitok és tenzidek asszociációja című MTA doktori értekezésre adott bírálatára Mindenekelőtt szeretném megköszönni Prof. Dr. Tombácz Etelkának
Válasz Prof. Dr. Tombácz Etelka Ellentétes töltésű polielektrolitok és tenzidek asszociációja című MTA doktori értekezésre adott bírálatára Mindenekelőtt szeretném megköszönni Prof. Dr. Tombácz Etelkának
TDK Tájékoztató 2015 Területek, témák, lehetőségek
 TDK Tájékoztató 2015 Területek, témák, lehetőségek Menyhárd Alfréd Fizikai Kémia és Anyagtudományi Tanszék Tanszékvezető Pukánszky Béla Budapest 2015. március 18. 1 Fizikai-kémia A kémia azon ága, amely
TDK Tájékoztató 2015 Területek, témák, lehetőségek Menyhárd Alfréd Fizikai Kémia és Anyagtudományi Tanszék Tanszékvezető Pukánszky Béla Budapest 2015. március 18. 1 Fizikai-kémia A kémia azon ága, amely
Fényérzékeny amorf nanokompozitok: technológia és alkalmazásuk a fotonikában. Csarnovics István
 Új irányok és eredményak A mikro- és nanotechnológiák területén 2013.05.15. Budapest Fényérzékeny amorf nanokompozitok: technológia és alkalmazásuk a fotonikában Csarnovics István Debreceni Egyetem, Fizika
Új irányok és eredményak A mikro- és nanotechnológiák területén 2013.05.15. Budapest Fényérzékeny amorf nanokompozitok: technológia és alkalmazásuk a fotonikában Csarnovics István Debreceni Egyetem, Fizika
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
VÍZKÉMIA TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 KÖRNYEZETMÉRNÖKI MESTERKÉPZÉS TÖRZSANYAG TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014 1 Tartalomjegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
KÖRNYEZETMÉRNÖKI MESTERKÉPZÉS TÖRZSANYAG TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2014 1 Tartalomjegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
Kolloid állapotjelzők. Molekuláris kölcsönhatások. Határfelületi jelenségek: fluid határfelületek
 Kolloid állapotjelzők. Molekuláris kölcsönhatások. Határfelületi jelenségek: fluid határfelületek Dr. Berka Márta Debreceni Egyetem TEK Kolloid- és Környezetkémiai Tanszék http://dragon.unideb.hu/~kolloid/
Kolloid állapotjelzők. Molekuláris kölcsönhatások. Határfelületi jelenségek: fluid határfelületek Dr. Berka Márta Debreceni Egyetem TEK Kolloid- és Környezetkémiai Tanszék http://dragon.unideb.hu/~kolloid/
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
Reológia Mérési technikák
 Reológia Mérési technikák Reológia Testek (és folyadékok) külső erőhatásra bekövetkező deformációját, mozgását írja le. A deformációt irreverzibilisnek nevezzük, ha a az erőhatás megszűnése után a test
Reológia Mérési technikák Reológia Testek (és folyadékok) külső erőhatásra bekövetkező deformációját, mozgását írja le. A deformációt irreverzibilisnek nevezzük, ha a az erőhatás megszűnése után a test
TDK Tájékoztató 2017 Területek, témák, lehetőségek
 TDK Tájékoztató 2017 Területek, témák, lehetőségek Menyhárd Alfréd Fizikai Kémia és Anyagtudományi Tanszék Kállay Mihály Tanszékvezető Budapest 2017. február 16. 1 Egyensúly Szerkezet Változás Fizikai-kémia
TDK Tájékoztató 2017 Területek, témák, lehetőségek Menyhárd Alfréd Fizikai Kémia és Anyagtudományi Tanszék Kállay Mihály Tanszékvezető Budapest 2017. február 16. 1 Egyensúly Szerkezet Változás Fizikai-kémia
Biofizika szeminárium. Diffúzió, ozmózis
 Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
KONDUKTOMETRIÁS MÉRÉSEK
 A környezetvédelem analitikája KON KONDUKTOMETRIÁS MÉRÉSEK A GYAKORLAT CÉLJA: A konduktometria alapjainak megismerése. Elektrolitoldatok vezetőképességének vizsgálata. Oxálsav titrálása N-metil-glükamin
A környezetvédelem analitikája KON KONDUKTOMETRIÁS MÉRÉSEK A GYAKORLAT CÉLJA: A konduktometria alapjainak megismerése. Elektrolitoldatok vezetőképességének vizsgálata. Oxálsav titrálása N-metil-glükamin
Kémiai alapismeretek 6. hét
 Kémiai alapismeretek 6. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék biner 2013. október 7-11. 1/15 2013/2014 I. félév, Horváth Attila c Egyensúly:
Kémiai alapismeretek 6. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék biner 2013. október 7-11. 1/15 2013/2014 I. félév, Horváth Attila c Egyensúly:
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 7. előadás NMR spektroszkópia Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék NMR, Nuclear Magnetic
Műszeres analitika II. (TKBE0532) 7. előadás NMR spektroszkópia Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék NMR, Nuclear Magnetic
MEDINPROT Gépidő Pályázat támogatásával elért eredmények
 A kisszögű röntgenszórási módszer fejlesztése fehérjék oldatfázisú mérésére Bóta Attila, Wacha András, Varga Zoltán MTA TTK Biológiai Nanokémia Kutatócsoport 1117 Bp. Magyar Tudósok krt. 2. MEDINPROT Gépidő
A kisszögű röntgenszórási módszer fejlesztése fehérjék oldatfázisú mérésére Bóta Attila, Wacha András, Varga Zoltán MTA TTK Biológiai Nanokémia Kutatócsoport 1117 Bp. Magyar Tudósok krt. 2. MEDINPROT Gépidő
Modern Fizika Labor. 2. Az elemi töltés meghatározása. Fizika BSc. A mérés dátuma: nov. 29. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. nov. 29. A mérés száma és címe: 2. Az elemi töltés meghatározása Értékelés: A beadás dátuma: 2011. dec. 11. A mérést végezte: Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. nov. 29. A mérés száma és címe: 2. Az elemi töltés meghatározása Értékelés: A beadás dátuma: 2011. dec. 11. A mérést végezte: Szőke Kálmán Benjamin
XXXVIII. KÉMIAI ELŐADÓI NAPOK
 Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVIII. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Magyar Kémikusok Egyesülete Csongrád Megyei Csoportja és a Magyar Kémikusok Egyesülete rendezvénye XXXVIII. KÉMIAI ELŐADÓI NAPOK Program és előadás-összefoglalók Szegedi Akadémiai Bizottság Székháza Szeged,
Textíliák felületmódosítása és funkcionalizálása nem-egyensúlyi plazmákkal
 Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Textíliák felületmódosítása és funkcionalizálása nem-egyensúlyi plazmákkal Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán
Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Textíliák felületmódosítása és funkcionalizálása nem-egyensúlyi plazmákkal Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán
