kémia ember a természetben műveltségterület Tanulói Bmunkafüzet Készítette Péter Orsolya Albert Attila
|
|
|
- Csenge Faragóné
- 9 évvel ezelőtt
- Látták:
Átírás
1 Tanulói Bmunkafüzet S z ö v e g é r t é s s z ö v e g a l k o t á s Készítette Péter Orsolya Albert Attila kémia ember a természetben műveltségterület 3 A klór reakciói 8 A kén olvadása és forrása 10 A kénsav hígítása 12 A nátrium tulajdonságai 18 A zajtalan gyufa feltalálása 20 Hogyan kerül a mészkő a Bükk-hegységből a házunk falába? 25 A vaskohó felépítése és működése
2 A KIADVÁNY KHF/867-9/2009 ENGEDÉLYSZÁMON IDŐPONTTÓL TANKÖNYVI ENGEDÉLYT KAPOTT. EDUCATIO KHT. KOMPETENCIAFEJLESZTŐ OKTATÁSI PROGRAM KERETTANTERV A KIADVÁNY A NEMZETI FEJLESZTÉSI TERV HUMÁNERÕFORRÁS-FEJLESZTÉSI OPERATÍV PROGRAM KÖZPONTI PROGRAM (PEDAGÓGUSOK ÉS OKTATÁSI SZAKÉRTÕK FELKÉSZÍTÉSE A KOMPETENCIA ALAPÚ KÉPZÉS ÉS OKTATÁS FELADATAIRA) KERETÉBEN KÉSZÜLT, A SULINOVA OKTATÁSI PROGRAMCSOMAG RÉSZEKÉNT LÉTREJÖTT TANULÓI INFORMÁCIÓHORDOZÓ. A KIADVÁNY SIKERES HASZNÁLATÁHOZ SZÜKSÉGES A TELJES OKTATÁSI PROGRAMCSOMAG ISMERETE ÉS HASZNÁLATA. A TELJES PROGRAMCSOMAG ELÉRHETŐ: CÍMEN. fejlesztési programvezető Kerner anna Felelõs szerkesztõ nagy milán Szakmai lektor Dr. kalmár zoltán A TANKÖNYVVÉ NYILVÁNÍTÁSI ELJÁRÁSBAN KÖZREMŰKÖDŐ SZAKÉRTŐK Tantárgypedagógiai szakértő: Dr. Réz Ferenc Tudományos-szakmai szakértő: Dr. Tóth Zoltán Technológiai szakértő: Csonka Vilmosné albert attila, péter orsolya, 2008 EDUCATIO KHT., 2008 RAKTÁRI SZÁM: TÖMEG: TERJEDELEM: H-BSZE GR. 3,92 A/5 ÍV
3 Munkalap A klór reakciói A klór a periódusos rendszer VII. a főcsoportjának második eleme. Vegyértékhéján hét elektron helyezkedik el, így egy elektron felvételével éri el a számára stabilis állapotot jelentő nemesgázelektronszerkezetet. Ezt kétféleképpen érheti el: ionképzéssel vagy molekulaképzéssel. Ionképzés Az ionképzés lényege az, hogy a klóratom olyan atommal lép kémiai reakcióba, amelyik egy elektront képes neki átadni, így abból pozitív töltésű ion: kation, a klóratomból pedig negatív töltésű ion: anion képződik. Az így keletkező vegyületben az ellentétes töltésű ionokat elektrosztatikus vonzás, azaz ionkötés tartja össze. Jó példa erre a hétköznapi életünkből is jól ismert konyhasónak, a nátrium-kloridnak a képződése: 2 Na + Cl 2 = 2 NaCl A nátriumatom külső elektronhéján egy, a klóratom elektronhéján hét vegyértékelektron tartózkodik. Egy elektron átadásával mindkét atom stabilis, nemesgáz-elektronszerkezetű ionná alakul. Láthatjuk, hogy a nátriumatomból úgy képződött nátriumion, hogy elektront adott át a klóratomnak. A nátriumatom így oxidálódott, a klóratom pedig elektron felvételével redukálódott. Mivel a nátriumatom elektront adott át a klóratomnak, redukálta azt, a nátrium tehát ebben a reakcióban redukálószerként viselkedett. A klóratom elektron leadására késztette a nátriumatomot, így oxidálta azt. A reakcióban a klór oxidálószer volt. Molekulaképzés Ismerünk olyan eseteket is, amikor szintén redukció és oxidáció megy végbe, mégsem tökéletes az elektronátadás, mert az elektront leadó atom részben megtartja a kölcsönhatásba lépő elektront. Ezt akkor tapasztalhatjuk, amikor a klór nem fémekkel, hanem nemfémes elemekkel lép kölcsönhatásba. Ilyenkor ugyanis a klóratom nem veszi át a nemfémes elem atomjának elektronját, csak részben magához köti azt. Ilyen átalakulás jellemző a hidrogén és a klór reakciójakor. H 2 + Cl 2 = 2 HCl A hidrogénatom nem adja át úgy a vegyérték-elektronját, mint ahogyan azt a nátriumatom esetében láttuk, hanem részben megtartja. Ekkor a klóratom és a hidrogénatom egy-egy elektronját adja a kémiai kötésbe, kovalens kötés kialakulása közben. A közös két elektron többet tartózkodik a klóratom környezetében, így a klóratom negatív, a hidrogénatom pedig pozitív pólusként jelenik meg. Mindkét atom kialakította a számára kedvező nemesgázszerkezetet, de ezt molekulaképzéssel érték el. A klóratom átvette a hidrogénatom elektronját, azaz redukálódott, így oxidálószer volt. A hidrogénatom átadta a klóratomnak az elektronját, oxidálódott, így redukálószer volt.
4 4 szövegértés szövegalkotás kémia 8. Összefoglalás A redoxireakciók tehát kétféleképpen mehetnek végbe, teljes vagy részleges elektronátmenettel. Az első esetben ionkötés alakul ki, ezt láttuk a nátrium-klorid esetében, a második esetben kovalens kötés jött létre, ezt láttuk a hidrogén-klorid esetében. 1. Olvasd el figyelmesen a szöveg első bekezdését! 2. Keresd ki a szövegből! a) Mi a klór reakcióinak a hajtóereje? b) Hogyan érheti el a klór ezt a stabilis állapotot? c) Hány elektronos a nemesgázszerkezet? 3. Olvasd el figyelmesen az ionképzésről szóló bekezdéseket! 4. Keresd ki a szövegből, hogy mi a) a kation; b) az anion; c) az ionkötés! 5. Fogalmazd meg a 2. bekezdés alapján, hogy mi az ionképzés lényege! 6. Ehhez a feladathoz, ha szükségesnek tartod, használhatod a Természettudományi kislexikont! A 4. bekezdés szövege alapján párosítsd a kémiai fogalmakat a jelentésükkel! Kösd össze egy vonallal az összetartozó párokat! Az oxidáció A redukálószer A redukció Az oxidálószer olyan anyag, amely elektront ad le elektronleadás olyan anyag, amely elektront vesz föl elektronfelvétel
5 tanulói MUNKAFÜZET A klór reakciói 5 7. Az alábbi információk a nátriumatomra, illetve a klóratomra vonatkoznak. Helyezd el őket a táblázatban a szöveg 4. bekezdésének alapján! Elektront adott le. Oxidálódott. Oxidálószerként viselkedett. Redukálódott. Elektront vett fel. Redukálószerként viselkedett. Nátriumatom Klóratom 8. Írd be az alábbi ábra alá a következő kifejezéseket! nátriumatom nátriumion kloridion klóratom 1. ábra 9. Olvasd el figyelmesen a molekulaképzésről szóló bekezdéseket! 10. Az alábbi mondatokból kiderül, hogy miben különbözik a molekulaképzés az ionképzéstől! Egészítsd ki a mondatokat a szöveg alapján! Molekulaképzés során nem tökéletes az elektronátadás, mert az elektront leadó atom a kölcsönhatásba lépő elektront. Ezt akkor tapasztaljuk, amikor a klór nem fémekkel, hanem lép kölcsönhatásba.
6 6 szövegértés szövegalkotás kémia 8. Ilyenkor a klóratom nem veszi át a nemfémes elem atomjának elektronját, csak azt. A molekulaképzés során nem ionkötés, hanem jön létre. 11. Az alábbi információk a hidrogénatomra, illetve a klóratomra vonatkoznak. Helyezd el őket a táblázatban a szöveg alapján! Elektront adott le. Oxidálódott. Oxidálószerként viselkedett. Redukálódott. Elektront vett fel. Redukálószerként viselkedett. Hidrogénatom Klóratom 12. Olvasd el az utolsó bekezdést! 13. Hasonlítsd össze az ionképzést a molekulaképzéssel! Helyezd el az alábbi információkat a táblázatban! részleges teljes ion kovalens
7 tanulói MUNKAFÜZET A klór reakciói 7 Redoxireakciók Ionképzés Molekulaképzés elektronátmenettel megy végbe. elektronátmenettel megy végbe. alakul ki. kötés alakul ki.
8 MUNKALAP A kén olvadása és forrása 1. Olvassátok el figyelmesen az alábbi szöveget! A mellékletben található kártyák a kén olvadását és forrását mutatják be. Ha a ként kémcsőben melegítjük, halmazállapota megváltozik. Szilárd halmazállapotból hígan folyóvá, majd sűrűn folyóvá, ezután ismét hígan folyóvá, végül gáz-halmazállapotúvá válik. 2. Karikázzátok be a szöveges kártyákon a halmazállapotra utaló kifejezéseket! 3. A bekarikázott kifejezéseket írjátok be a fejlécre! (A kártyák tetejére.) 4. Az első feladatban található szöveg alapján tegyétek sorrendbe a kártyákat! 5. Húzzátok alá a szöveges kártyákon azokat a kifejezéseket, melyek a kénmolekulák formájára utalnak! 6. Párosítsátok a szöveges kártyákat a hozzájuk tartozó ábrákkal!
9 tanulói MUNKAFÜZET A kén olvadása és forrása 9 MELLÉKLET A kén olvadása és forrása Szilárd halmazállapotban a nyolc-atomos kénmolekulák egymás melletti gyűrűk formájában helyezkednek el. A molekulákon belül kovalens kötések, a molekulák között gyenge, másodrendű kötések hatnak. A kén olvadáspontján a kénmolekulák közötti másodrendű kötések felszakadnak, a molekulák egymáson könnyen elgördülnek. A kristályrács összeomlik, a szilárd kén megolvad, és hígan folyóvá válik. További hőmérséklet-emelés hatására a kéngyűrűk felszakadnak, és kígyózóan tekergő láncokká alakulnak. A láncok egymással összegubancolódnak, így sűrűn folyó kénolvadékhoz jutunk. További energiaközlés hatására a láncok egyre kisebb darabokra szakadnak fel. A kis kénmolekulákban a kénatomok száma változó, a kis molekulák könynyen elgördülnek egymáson, a kénolvadék ismét hígan folyóvá válik. A forráspontját elérve a kén gázhalmazállapotba kerül. Atomjai leginkább kétatomos molekulák formájában elhagyják a folyadékot, és a gáztérbe kerülnek.
10 Munkalap 1. Olvassátok el figyelmesen az alábbi szöveget, és tanulmányozzátok a hozzá tartozó ábrát! A kénsav hígítása A kénsav nagy sűrűségű, színtelen folyadék. Tömény vizes oldata 98%-os, így kémiai reakciókhoz gyakran hígítanunk kell. A tömény kénsav hígítása azonban nagy körültekintést igényel. A 98%-os kénsav üvegén a következő címkét találhatjuk: R: 35 S: KÉNSAV tömény H 2 SO 4 M = 98 g/mol A kénsav vízzel való érintkezése nagy hőfelszabadulással jár. Amennyiben a tömény kénsavhoz öntjük a vizet, a kénsavba kerülő víz olyan gyorsan felmelegszik, hogy gőzzé alakulhat, és kénsavcseppeket magával hozva szétfröccsenhet. Amennyiben a kénsavat óvatosan, vékony sugárban adjuk a vízhez, akkor a baleset elkerülhető. A vizet állandóan kevergessük, miközben óvatosan öntjük hozzá a kénsavat! 2. Keressétek ki a szövegből a kénsav tulajdonságait! a) Sűrűsége: b) Színe: 3. Egészítsétek ki az alábbi mondatot az első bekezdés alapján! A kénsavat kémiai reakciókhoz gyakran hígítanunk kell, mert oldata -os.
11 tanulói MUNKAFÜZET A kénsav hígítása Nézzétek meg figyelmesen a kénsav címkéjét! Másoljátok le azt a jelet, amelyik a kénsav moláris tömegét jelenti! 5. A második bekezdés alapján húzzátok alá a kénsav helyes hígításának módját! a) A tömény kénsavhoz kell a vizet önteni. b) A vízhez kell önteni a kénsavat vékony sugárban. 6. Mi történik, ha nem megfelelő módon hígítják a kénsavat? 7. Képzeld el, hogy a tömény kénsavat előállító gyár felkért arra, hogy készíts új címkét a termék számára! Írj egymondatos szöveget, melyből a vásárlók megismerik a kénsav helyes hígításának módját! Készíts rajzot is a szöveg mellé!
12 Munkalap A nátrium tulajdonságai Dolgozzatok párokban! Végezzétek el az alábbi kísérletet! A kísérlet elvégzéséhez használjatok gumikesztyűt és védőszemüveget! Vegyetek ki a petróleumból egy darab nátriumot, majd helyezzétek szűrőpapírra! Vágjatok le belőle egy kisebb darabot, és itassátok le felületéről a petróleumot! Figyeljétek meg felületének változását a szabad levegőn! Tegyétek vissza a fémet a petróleumba! 2. Tapasztalataitok alapján egészítsétek ki az alábbi mondatot! A nátrium külső felülete színű, de friss vágási felülete Csillogó felülete azonban hamarosan 3. Készítsetek a pároddal munkanaplót az elvégzett kísérletről! Soroljátok fel a munka egyes lépéseit! (Segítenek a megadott igék!) a) (kivettük) b) (leitattuk) c) (kettévágtuk) d) (visszatettük) 4. Olvassátok el figyelmesen az alábbi, nátriumról szóló szöveget! Vannak fémek, amelyek jelentős szerepet játszanak köznapi életünkben úgy, hogy elemi formában gyakorlatilag sohasem találkozunk velük. Ilyen fém a nátrium, amely elemi állapotban igen reakcióképes, így a természetben nem fordul elő, vegyületei formájában azonban igen fontos szerepet játszik. A konyhasó, az üveg, a mosószerek és számos más anyag tartalmazza a nátrium pozitív töltésű ionját különféle vegyületekbe kötve. Láthattuk, hogy a sárgás felületű fémdarabok folyadékban állnak. Ez a folyadék a petróleum, ami paraffin-szénhidrogének keveréke. Kis reakciókészsége miatt nem lép kémiai kölcsönhatásba a reakcióképes nátriummal. Ha a nátriumot kivesszük a petróleumból, jól látható a felületén a sárgás kéreg, amely lassú oxidációs folyamatok eredménye. Mivel puha fém, késsel vágható, vágási felülete csillogó, fémfényű. Ekkor tárul elénk a nátrium igazi arca. Csillogó felülete hamarosan eltompul, a fém gyorsan oxidálódik. Felületét nátrium-oxidból álló réteg vonja be, megszüntetve a csillogást.
13 tanulói MUNKAFÜZET A nátrium tulajdonságai Foglaljátok össze a pároddal, hogy mit tudtatok meg a nátriumról! Keressétek ki a fenti szövegből a nátrium tulajdonságait! a) A kémiai elemeknek melyik csoportjába tartozik? b) Felületének színe: c) Miért vágható késsel? d) Vágási felületének színe: e) Hogyan fordul elő a természetben? f) Milyen a reakcióképessége?
14 MUNKALAP (2) A nátrium tulajdonságai Dolgozzatok párokban! Végezzétek el az alábbi kísérletet! Vegyetek ki egy kis darab nátriumot a petróleumból, és tegyétek fenolftalein indikátort tartalmazó vízbe! A kísérlet elvégzéséhez használjatok gumikesztyűt és védőszemüveget! 2. Pakoljátok el az eszközöket és az edényeket! Most is használjatok gumikesztyűt! A szűrőpapíron esetlegesen ottmaradt nátriumdarabkákat gondosan gyűjtsétek össze és tegyétek vissza a petróleum alá! Szemetesbe dobva lángra lobbanhat, és tüzet okozhat. A nát riumhidroxid oldat maró hatású, így ügyeljetek arra, hogy szemetekbe, kezetekre ne fröccsenjen! 3. Tapasztalataitok alapján válaszoljatok az alábbi kérdésekre! a) Mi történt a nátriummal a vízben? b) Milyen színű csíkot húzott maga után a fenolftaleinnel megfestett nátrium-hidroxidoldat? 4. Készítsetek munkanaplót a kísérlet egyes lépéseiről! a) b) c) d) 5. Olvassátok el figyelmesen az alábbi szöveget, melyből megtudhatjátok, hogy milyen kémiai folyamat játszódott le a kísérlet során! A nátrium kis sűrűségénél fogva a víz tetején úszik. Úgy mondjuk, hogy rohangál a víz felszínén, ugyanis a vízzel kémiai kölcsönhatásba lépve hidrogéngázt fejleszt. 2 Na + 2 H 2 O = 2 NaOH + H 2 A fejlődő hidrogéngáz a nátriumdarabkát ide-oda mozgatja. Az alacsony olvadáspontú fém golyóvá olvad össze, így egy ezüstfehér fémgolyó futkározása figyelhető meg a víz felszínén. A látványt még fokozza, hogy a mozgó fémgolyó, a fenolftaleinnel megfestett nátrium-hidroxidoldat ciklámenszínű csíkot húz maga után a vízen. A reakció során keletkező nátrium-hidroxid lúgos kémhatását a fenolftalein ciklámenszínnel jelzi.
15 tanulói MUNKAFÜZET A nátrium tulajdonságai Keressétek ki a szövegből, hogy milyen gáz mozgatja a vízen a nátriumdarabkát! 7. Keressétek ki a szövegből, hogyan keletkezik ez a gáz! 8. Másoljátok ki azt a mondatot a szövegből, amelyikből kiderül, hogy miért húz maga után a nátrium ciklámenszínű csíkot! 9. A fenti kérdésekre adott válaszaitok alapján meséljétek el a párotoknak, hogy mit láttatok a kísérlet során, és magyarázzátok el neki, hogy mi okozta ezt a jelenséget! 10. A szövegek alapján válaszoljatok az alábbi kérdésekre! Írjátok le, hogy mit kell tenni a kísérletek során a balesetek elkerülésének érdekében! a) Mit kell használni a kísérlet közben és az elpakolásnál is? b) Mit kell tenni a nátriummal a kísérlet elvégzése után? c) Mire kell ügyelni, ha nátrium-hidroxid-oldattal végzünk kísérletet?
16 MUNKALAP (3) Csillagszóró készítése 1. Olvassátok el figyelmesen az alábbi szöveget! Törjünk porrá 10 gramm bárium-nitrátot, és keverjük össze 3 gramm keményítővel! Keverjünk hozzá 1 gramm alumíniumporból és 4-5 gramm durva vasporból álló fémkeveréket, és öntsünk hozzá annyi forró vizet, hogy a keverék masszaszerű, gyúrható legyen! A masszát vigyük fel cm-es drótdarabkákra, és az így kapott csillagszórókat alaposan szárítsuk ki! A szárítást szabad levegőn 2-3 napig vagy 110 fokos sütőben néhány percig végezzük! A kiszáradt csillagszórók meggyújtva szikrázva égnek el. Mi történik, amikor meggyújtunk egy csillagszórót? A bárium-nitrát hevítés hatására oxigén fejlődése közben bomlik. A felszabaduló oxigénben az alumíniumpor és a vaspor elég, az alumínium égése közben fehér fénnyel világít, az égő durva vasporszemcsék szikrázva vasoxiddá alakulnak. A keményítő a keverék összetartására, összeragasztására szolgál. 2. Dolgozzatok párokban! Keressétek ki a szövegből a csillagszóró hozzávalóit! Adjátok meg a szükséges mennyiséget is! Mennyiség Hozzávaló 3. Az alábbiakban a csillagszóró készítésének lépéseit olvashatjátok. Egészítsétek ki a mondatokat a szöveg alapján a hiányzó igékkel! a) porrá 10 gramm bárium-nitrátot! b) 3 gramm keményítővel!
17 tanulói MUNKAFÜZET Csillagszóró készítése 17 c) hozzá a fémkeveréket! d) hozzá forró vizet! e) a masszát drótdarabkákra! f) a csillagszórókat! 4. Készítsetek csillagszórókat a leírás alapján!4. Készítsetek csillagszórókat a leírás alapján! 5. Keressétek ki a szöveg második bekezdéséből, hogy a csillagszóró égésének csodálatos látványában milyen szerepet játszik a) az alumínium: b) a vaspor: 6. Fogalmazzátok meg egy mondatban, hogy mire való a csillagszóró! 7. Meséljétek el osztálytársaitoknak a csillagszórókhoz kötődő karácsonyi élményeiteket!
18 Munkalap 1. Az alábbi szöveg a Tudománytörténet című fejezetbe tartozik. Fogalmazzátok meg, milyen témájú olvasmányokat és feladatokat tartalmazhat ez az anyagrész! Segít az alábbi két definíció! Tudományág: a tudománynak meghatározott tárgykörrel foglalkozó ága. Történet: valaminek a múltja és fejlődése elmondva és leírva. 2. Olvassátok el figyelmesen az alábbi szöveget! A zajtalan gyufa feltalálása A zajtalan gyufát Irinyi János magyar tudós találta fel 1836-ban. Irinyi gyufái az előző gyufáktól eltérően zaj és kellemetlen szag nélkül gyulladtak meg. A tudós fehér foszfor és ólom-dioxid keverékét vitte fel egy fapálcika végére, s ez a keverék dörzsölés hatására lángra lobbant. A fehér foszfor érdekes tulajdonsága, hogy gyulladási hőmérséklete 60 o C, így a súrlódás során ke-letkezett hő hatására foszfor-oxiddá égett el. Az égéshez szükséges oxigént az ólomdioxid oxigéntartalma szolgáltatta. A fehér foszforral készült gyufának ugyanakkor hátrányos tulajdonságai is voltak. A fehér foszfor ugyanis erős méreg, ami a szervezetbe kerülve kis menynyiségben is halált okoz. A mai gyufák meggyulladásához fehér foszfor helyett nem mérgező vörös foszfort alkalmaznak. Ez a foszfor üvegporral és ragasztóval keverve található a gyufásdoboz oldalán. A gyufa feje foszfort nem, viszont kénport, keményítőt és oxidálószereket tartalmaz. Dörzsölés hatására a gyufásdoboz oldaláról levált kis mennyiségű vörös foszfor átalakul fehér foszforrá, az meggyullad, és meggyújtja a fapálcikát. Az így kapott gyufa ugyancsak zajtalanul gyullad, de azzal az előnyös tulajdonsággal is rendelkezik, hogy foszfortartalma nem mérgező. 3. A szöveg háromfajta gyufát említ: zajos gyufát, Irinyi zajtalan gyufáját és mai gyufát. Írjátok az alábbi tulajdonságok betűjelét a halmazokba! a) Meggyulladását zaj kíséri. b) Fehér foszfort tartalmaz. c) Zajtalanul gyullad. d) Meggyulladását kellemetlen szag kíséri. e) Alapja egy fapálcika. f) Feje keményítőt tartalmaz.
19 tanulói MUNKAFÜZET A zajtalan gyufa feltalálása 19 Zajos gyufa Irinyi zajtalan gyufája Mai gyufa 4. Soroljátok fel Irinyi János gyufájának előnyös és hátrányos tulajdonságait! Előnyös tulajdonságok: Hátrányos tulajdonságok: 5. Állapítsátok meg az alábbi állításokról, hogy igazak vagy hamisak! a) A fehér foszfor erős méreg. b) Magyar tudós találta fel a gyufát. c) A mai gyufák feje vörös foszfort tartalmaz. d) A fehér foszfor balesetet okozhat. e) A zajtalan gyufát a 19. században találták fel.
20 Munkalap Hogyan kerül a mészkő a Bükk-hegységből a házunk falába? Sok érdekességgel találkozhat az, aki elgondolkodik azon, hogy vajon hogyan kerül a mészkő a hegységekből a házaink falába. A mészkő évmilliókkal ezelőtt keletkezett a Földön a tenger mélyére leülepedett mészvázas állatkák maradványaiból. Évmilliók alatt a tengerek mélye a felszínre került, és mára számos mészkőhegység emelkedik ki magas hegységek formájában. Egyik ilyen hazai hegységünk a Bükk-hegység, amely az Északi-középhegység tagja. A Bükk anyaga mészkő, kémiailag kalcium-karbonát. A mészkő fehér színű, magas olvadáspontú vegyület. Vízben szinte egyáltalán nem oldódik, a szén-dioxidot magában oldó esővíz azonban kissé oldja. Így oldja fel a víz a mészkövet, a cseppkőbarlang belsejében pedig az oldott mészkő kiválása közben képződnek a cseppkövek. De ezek mellett az értékes kincsek mellett maga a kőzet is fontos építőanyag. A hegységből kibányászott mészkövet őrlés után mészégető kemencékben 900 o C hőmérsékletre hevítik. Ekkor a mészkő hő hatására bomlik, égetett mész és szén-dioxid képződik belőle. Mészégetés CaCO 3 = CaO + CO 2 A habarcs megkötése: Ca(OH) 2 + CO 2 = CaCO 3 Mészoltás: CaO + H 2 O = Ca(OH) 2 Ezt a folyamatot mészégetésnek nevezzük, a keletkező kalcium-oxidot pedig égetett mésznek hívjuk. Az égetett mész fehér por, amely víz hozzáadására hőfejlődés közben oltott mésszé, kalcium-hidroxiddá alakul. A kalcium-hidroxid vízben rosszul oldódik, így a vízzel való összekeverés után nem egy átlátszó oldatot, hanem fehér színű, oldhatatlan kristályokat tartalmazó
21 tanulói MUNKAFÜZET Hogyan kerül a mészkő anyagot kapunk. Ez a mésztej. A mésztej erősen lúgos kémhatású, maró anyag, bőrre kerülve és szembe fröccsenve sérülést okoz. Az így keletkezett mésztejet homokkal összekeverik, így készül a habarcs. Ez az anyag a téglák összeragasztására kiválóan alkalmas, hiszen kalcium-hidroxid-tartalma meg tudja kötni a levegőből a szén-dioxidot, így ismét visszaalakul mészkővé. A reakció gyors lejátszódásához szén-dioxidra van szükség. A szén-dioxid a levegő természetes alkotója, azonban olyan kis koncentrációban van jelen, hogy a reakció hosszú időt vesz igénybe. Az átalakulás meggyorsítása érdekében a ház fala mellett fát égetnek, mert a fa égése során keletkező szén-dioxid be tud épülni a ház falába. Az égés során keletkező hőnek is nagy szerepe van a keletkező víz elpárologtatásában. A homokot magába kötő mészkő jó ragasztóanyaga a tégláknak, több száz évig is szilárdan tarthatja a téglákat az épületek falában. 1. Először olvasd el a szöveg címét! Fogalmazd meg szóban a társaidnak, hogy szerinted miről fog szólni a szöveg! 2. Most olvasd el figyelmesen a szöveg első két bekezdését! 3. Keresd ki az első bekezdésből, hogy a) miből keletkezik a mészkő; b) hogyan keletkezik a mészkőhegység! 4. Keresd ki a második bekezdésből a mészkő tulajdonságait! a) Kémiai összetétele: b) Színe: c) Olvadáspontja: d) Oldódása: 5. Adjál címet az első két bekezdésnek! 6. Olvasd el figyelmesen a harmadik és a negyedik bekezdést!
22 22 szövegértés szövegalkotás kémia Nézd meg figyelmesen az első ábrát! Írd mellé a szöveg alapján, hol látod a) a Bükk hegységet; b) a kibányászott mészkövet; c) a mészégető kemencét! 8. Egy vállalat égetett meszet akar előállítani. Adj tanácsot a vezetőjének a harmadik bekezdés mondatai alapján, hogy milyen munkálatokat kell elvégezniük ahhoz, hogy a hegységben található mészkőből égetett meszet kapjanak! a) b) c) 9. Keresd ki a negyedik bekezdésből, hogy milyen kémiai összetételű a) az égetett mész; b) az oltott mész! 10. Másold ki a szövegből azt a mondatot, amelyik az alábbi kémiai folyamatot írja le szavakkal: CaCO 3 à CaO + CO Másold ki a szövegből azt az egyenletet, amely azt mutatja, hogy az égetett mész fehér por, amely víz hozzáadására hőfejlődés közben oltott mésszé, kalcium-hidroxiddá alakul! 12. Válaszolj az alábbi találós kérdésekre a negyedik bekezdés alapján! Melyik az a mészkőből származó anyag, amelynek az állaga a) fehér por; b) fehér színű oldat? 13. Egy építkezésen sok munkás dolgozik. Az egyik anyag, amire szükségük van, nagyon veszélyes. Keresd ki a szövegből, melyik ez az anyag!
23 tanulói MUNKAFÜZET Hogyan kerül a mészkő Készíts a kőművesek számára egy figyelmeztető plakátot, melyből megtudják, miért kell óvatosan bánniuk ezzel az anyaggal! 15. Másold ki a szövegből a mésztej előállításának egyenletét! 16. Adj címet a harmadik és negyedik bekezdésnek! 17. Olvasd el figyelmesen az utolsó két bekezdést! 18. Adj címet az utolsó két bekezdésnek! 19. Készíts egy listát is a kőművesek számára, melyben felsorolod, milyen anyagokat kell beszerezniük ahhoz, hogy habarcsot állítsanak elő! Keresd ki a szövegből ezeket az anyagokat! a) b) c) 20. Keresd ki a szövegből! a) Mire használják a habarcsot? b) Mivé alakul a habarcs szén-dioxid hatására? c) Hogyan segítik elő az építkezéseknél a reakció lejátszódását?
24 24 szövegértés szövegalkotás kémia Az alábbiakban annak a folyamatnak az összefoglalását látod, hogyan keletkezik a mészkőből habarcs. A szöveg alapján írd be a hiányzó helyekre az alábbi anyagok neveit! égetett mész, mészkő, habarcs, mésztej, szén-dioxid, oltott mész őrlés, égetés 23. Magyarázd el röviden a padtársadnak, hogy milyen jelentősége van a mészkőnek az építkezésekben!
25 Munkalap 1. Olvassátok el figyelmesen az alábbi szöveget! Nézzétek meg alaposan a vaskohó felépítését bemutató képet is! A vaskohó felépítése és működése vasérc koksz mészkő forró levegő A fenti ábrán a vasgyártásra alkalmas nagyolvasztó, más néven vaskohó felépítését láthatjátok. A kohó tetején töltik be a vasérc, a salakképző anyagok és a koksz keverékét. A vasérc különféle vas-oxidok keveréke, salakképző anyagnak mészkőport használnak. A koksz, ami a vas-oxidokat redukálja, fekete kőszén felhasználásával készült mesterséges szén. A keverék begyújtva meggyullad, a kohó alján befúvatott forró levegő oxigéntartalma segíti az égési folyamatot. A kohó közepe táján 1000 o C-nál magasabb hőmérséklet alakul ki. A mészkő elbomlik, szén-dioxid keletkezik, ami az izzó koksszal reakcióba lépve szén-monoxiddá redukálódik. A magas hőmérsékleten a szén és a szén-monoxid elvonja a vas-oxidokból az oxigént, ezáltal szén-monoxiddá, szén-dioxiddá oxidálódnak. A vas-oxidok redukálódnak, elemi vas keletkezik. Ezt a folyamatot mutatják be az alábbi egyenletek: Fe 2 O C = 2 Fe + 3 CO Fe 2 O CO = 2 Fe + 3 CO 2 Az olvadt vas a kohó alján helyezkedik el. A nála kisebb sűrűségű salak az olvadt vas tetején úszik, meggátolva azt, hogy a vas az oxigén hatására visszaalakuljon vas-oxiddá. Időről időre lecsapolják az olvadt vasat, amelyet öntésre vagy acélgyártásra használnak fel.
26 26 szövegértés szövegalkotás kémia Keressétek ki a szövegből azoknak az anyagoknak a nevét, amelyek szükségesek a vasgyártáshoz! 3. A szöveg alapján határozzátok meg, milyen anyag a) a vasérc: b) a koksz: 4. A vaskohóban olvadt vasat állítanak elő. Keressétek ki a szövegből, hogy mire használják az olvadt vasat! 5. Korábbi kémiai tanulmányaitok alapján adjátok meg a következő kémiai folyamatok jelentését! Segítséget nyújthat a Természettudományi kislexikon. a) Redukció: b) Oxidáció: 6. Keressétek ki a szövegből, hogy mi a szerepe a vasgyártásban az alábbi anyagoknak! a) Mészkőpor: b) Koksz: c) Oxigén: d) Szén: e) Salak: 7. A szöveg és a kép alapján mutassátok be a vasgyártás folyamatának lépéseit! Az egyes lépések megfogalmazásában segítenek a sorok elején lévő igék! a) (betöltik) b) (meggyullad) c) (elbomlik) d) (keletkezik) e) (redukálódik) f) (elvonja)
27 tanulói MUNKAFÜZET A vaskohó felépítése és működése 27 g) (oxidálódnak) h) (keletkezik) i) (lecsapolják) 8. A vaskohóról való ismereteitek alapján adjátok meg, mit jelenthet a következő kifejezés: népek kohója! 9. Nézzetek körül az osztályteremben és az iskolában! Gyűjtsétek össze minél több olyan tárgynak a nevét, melynek előállításához vasra van szükség!
28
Javítóvizsga. Kalász László ÁMK - Izsó Miklós Általános Iskola Elérhető pont: 235 p
 Név: Elérhető pont: 5 p Dátum: Elért pont: Javítóvizsga A teszthez tollat használj! Figyelmesen olvasd el a feladatokat! Jó munkát.. Mi a neve az anyag alkotórészeinek? A. részecskék B. összetevők C. picurkák
Név: Elérhető pont: 5 p Dátum: Elért pont: Javítóvizsga A teszthez tollat használj! Figyelmesen olvasd el a feladatokat! Jó munkát.. Mi a neve az anyag alkotórészeinek? A. részecskék B. összetevők C. picurkák
b./ Hány gramm szénatomban van ugyanannyi proton, mint 8g oxigénatomban? Hogyan jelöljük ezeket az anyagokat? Egyforma-e minden atom a 8g szénben?
 1. Az atommag. a./ Az atommag és az atom méretének, tömegének és töltésének összehasonlítása, a nukleonok jellemzése, rendszám, tömegszám, izotópok, nuklidok, jelölések. b./ Jelöld a Ca atom 20 neutront
1. Az atommag. a./ Az atommag és az atom méretének, tömegének és töltésének összehasonlítása, a nukleonok jellemzése, rendszám, tömegszám, izotópok, nuklidok, jelölések. b./ Jelöld a Ca atom 20 neutront
A kén tartalmú vegyületeket lúggal főzve szulfid ionok keletkeznek, amelyek az Pb(II) ionokkal a korábban tanultak szerint fekete csapadékot adnak.
 Egy homokot tartalmazó tál tetejére teszünk a pépből egy kanállal majd meggyújtjuk az alkoholt. Az alkohol égésekor keletkező hőtől mind a cukor, mind a szódabikarbóna bomlani kezd. Az előbbiből szén az
Egy homokot tartalmazó tál tetejére teszünk a pépből egy kanállal majd meggyújtjuk az alkoholt. Az alkohol égésekor keletkező hőtől mind a cukor, mind a szódabikarbóna bomlani kezd. Az előbbiből szén az
Elektrokémia. A nemesfém elemek és egymással képzett vegyületeik
 Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
RAJZ ÉS VIZUÁLIS KULTÚRA 5. évfolyam
 SZÖVEGÉRTÉS-SZÖVEGALKOTÁS RAJZ ÉS VIZUÁLIS KULTÚRA 5. évfolyam TANULÓI MUNKAFÜZET Készítette: Ternákné Gábori Gabriella Molnár Krisztina 3 Az ókori Egyiptom építészete 8 Az ókori görög szobrászatról A
SZÖVEGÉRTÉS-SZÖVEGALKOTÁS RAJZ ÉS VIZUÁLIS KULTÚRA 5. évfolyam TANULÓI MUNKAFÜZET Készítette: Ternákné Gábori Gabriella Molnár Krisztina 3 Az ókori Egyiptom építészete 8 Az ókori görög szobrászatról A
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 9. osztály A változat
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály A változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály A változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY
 MAGYAR TERMÉSZETTUDOMÁNYI TÁRSULAT HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY A megyei (fővárosi) forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:...
MAGYAR TERMÉSZETTUDOMÁNYI TÁRSULAT HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY A megyei (fővárosi) forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:...
Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek. fémek
 Kémiai kötések Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek fémek Fémek Szürke színűek, kivétel a színesfémek: arany,réz. Szilárd halmazállapotúak, kivétel a higany. Vezetik az
Kémiai kötések Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek fémek Fémek Szürke színűek, kivétel a színesfémek: arany,réz. Szilárd halmazállapotúak, kivétel a higany. Vezetik az
Speciálkollégium. Dr. Fintor Krisztián Magyary Zoltán Posztdoktori Ösztöndíj TÁMOP 4.2.4.A/2-11-1-2012-0001 Nemzeti Kiválóság Program Szeged 2014
 Speciálkollégium Dr. Fintor Krisztián Magyary Zoltán Posztdoktori Ösztöndíj TÁMOP 4.2.4.A/2-11-1-2012-0001 Nemzeti Kiválóság Program Szeged 2014 A beton kioldódási folyamata Kioldás, kilúgozás (Leaching):
Speciálkollégium Dr. Fintor Krisztián Magyary Zoltán Posztdoktori Ösztöndíj TÁMOP 4.2.4.A/2-11-1-2012-0001 Nemzeti Kiválóság Program Szeged 2014 A beton kioldódási folyamata Kioldás, kilúgozás (Leaching):
A víz fizikai, kémiai tulajdonságai, felhasználhatóságának korlátai
 Kuti Rajmund Szakál Tamás Szakál Pál A víz fizikai, kémiai tulajdonságai, felhasználhatóságának korlátai Bevezetés Az utóbbi tíz évben a klímaváltozás és a globális civilizációs hatások következtében Földünk
Kuti Rajmund Szakál Tamás Szakál Pál A víz fizikai, kémiai tulajdonságai, felhasználhatóságának korlátai Bevezetés Az utóbbi tíz évben a klímaváltozás és a globális civilizációs hatások következtében Földünk
3. változat. 2. Melyik megállapítás helyes: Az egyik gáz másikhoz viszonyított sűrűsége nem más,
 3. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg az egyszerű anyagok számát
3. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg az egyszerű anyagok számát
EÖTVÖS LABOR EÖTVÖS JÓZSEF GIMNÁZIUM TATA FELADATLAPOK KÉMIA. 8., 9., 10. évfolyam, tehetséggondozó szakkör Tanári segédanyag
 FELADATLAPOK KÉMIA 8., 9., 10. évfolyam, tehetséggondozó szakkör Tanári segédanyag Barsiné Pirityi Mária Petroviczné Gál Ibolya Pozsgayné Tóth Ildikó Rovácsné Simon Erika ajánlott korosztály: 8. évfolyam
FELADATLAPOK KÉMIA 8., 9., 10. évfolyam, tehetséggondozó szakkör Tanári segédanyag Barsiné Pirityi Mária Petroviczné Gál Ibolya Pozsgayné Tóth Ildikó Rovácsné Simon Erika ajánlott korosztály: 8. évfolyam
Kuti Rajmund. A víz tűzoltói felhasználhatóságának lehetőségei, korlátai
 Kuti Rajmund A víz tűzoltói felhasználhatóságának lehetőségei, korlátai A tűzoltóság a bevetések 90%-ban ivóvizet használ tűzoltásra, s a legtöbb esetben a kiépített vezetékes hálózatból kerül a tűzoltó
Kuti Rajmund A víz tűzoltói felhasználhatóságának lehetőségei, korlátai A tűzoltóság a bevetések 90%-ban ivóvizet használ tűzoltásra, s a legtöbb esetben a kiépített vezetékes hálózatból kerül a tűzoltó
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2016. május 13. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2016. május 13. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Kémia
ÉRETTSÉGI VIZSGA 2016. május 13. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2016. május 13. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Kémia
KÉMIA. Kiss Árpád Országos Közoktatási Szolgáltató Intézmény Vizsgafejlesztő Központ 2003
 KÉMIA Kiss Árpád Országos Közoktatási Szolgáltató Intézmény Vizsgafejlesztő Központ 2003 ű érettségire felkészítő tananyag tanterve /11-12. ill. 12-13. évfolyam/ Elérendő célok: a természettudományos gondolkodás
KÉMIA Kiss Árpád Országos Közoktatási Szolgáltató Intézmény Vizsgafejlesztő Központ 2003 ű érettségire felkészítő tananyag tanterve /11-12. ill. 12-13. évfolyam/ Elérendő célok: a természettudományos gondolkodás
A javításhoz kb. az érettségi feladatok javítása az útmutató irányelv. Részpontszámok adhatók. Más, de helyes gondolatmenetet is el kell fogadni!
 Megoldások A javításhoz kb. az érettségi feladatok javítása az útmutató irányelv. Részpontszámok adhatók. Más, de helyes gondolatmenetet is el kell fogadni! **********************************************
Megoldások A javításhoz kb. az érettségi feladatok javítása az útmutató irányelv. Részpontszámok adhatók. Más, de helyes gondolatmenetet is el kell fogadni! **********************************************
KÉMIA TANMENETEK 7-8-9-10 osztályoknak
 KÉMIA TANMENETEK 7-8-9-10 osztályoknak Néhány gondolat a mellékletekhez: A tanterv nem tankönyvhöz készült, hanem témakörökre bontva mutatja be a minimumot és az optimumot. A felsőbb osztályba lépés alapja
KÉMIA TANMENETEK 7-8-9-10 osztályoknak Néhány gondolat a mellékletekhez: A tanterv nem tankönyvhöz készült, hanem témakörökre bontva mutatja be a minimumot és az optimumot. A felsőbb osztályba lépés alapja
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 9. osztály C változat
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály C változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály C változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
A XVII. VegyÉSZtorna I. fordulójának feladatai és megoldásai
 Megoldások: 1. Mekkora a ph-ja annak a sósavoldatnak, amelyben a kloridion koncentrációja 0,01 mol/dm 3? (ph =?,??) A sósav a hidrogén-klorid (HCl) vizes oldata, amelyben a HCl teljesen disszociál, mivel
Megoldások: 1. Mekkora a ph-ja annak a sósavoldatnak, amelyben a kloridion koncentrációja 0,01 mol/dm 3? (ph =?,??) A sósav a hidrogén-klorid (HCl) vizes oldata, amelyben a HCl teljesen disszociál, mivel
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését!
 I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
Általános iskola (7-8. évfolyam)
 Általános iskola (7-8. évfolyam) TÉMAKÖR / Vizsgálat megnevezése Vizsgálat sorszáma Jelleg (T=tanulói; D=demonstrációs; Tg=Tehetséggondozó) ANYAG, KÖLCSÖNHATÁS, ENERGIA, INFORMÁCIÓ Ismerkedés a laboratóriumi
Általános iskola (7-8. évfolyam) TÉMAKÖR / Vizsgálat megnevezése Vizsgálat sorszáma Jelleg (T=tanulói; D=demonstrációs; Tg=Tehetséggondozó) ANYAG, KÖLCSÖNHATÁS, ENERGIA, INFORMÁCIÓ Ismerkedés a laboratóriumi
KÉMIA Kiss Árpád Országos Közoktatási Szolgáltató Intézmény Vizsgafejlesztő Központ 2003
 KÉMIA Kiss Árpád Országos Közoktatási Szolgáltató Intézmény Vizsgafejlesztő Központ 2003 I. RÉSZLETES ÉRETTSÉGI VIZSGAKÖVETELMÉNY A) KOMPETENCIÁK A vizsgázónak a követelményrendszerben és a vizsgaleírásban
KÉMIA Kiss Árpád Országos Közoktatási Szolgáltató Intézmény Vizsgafejlesztő Központ 2003 I. RÉSZLETES ÉRETTSÉGI VIZSGAKÖVETELMÉNY A) KOMPETENCIÁK A vizsgázónak a követelményrendszerben és a vizsgaleírásban
Eötvös József Általános Iskola és AMI Helyi tanterv 2013
 Kerettantervi megfelelés Eötvös József Általános Iskola és AMI KÉMIA 1.5 órára 7.osztály Jelen helyi tanterv-ajánlás az 51/2012. (XII.21.) EMMI rendelet: 2. melléklet 2.2.10.1 Kémia 7-8. alapján készült.
Kerettantervi megfelelés Eötvös József Általános Iskola és AMI KÉMIA 1.5 órára 7.osztály Jelen helyi tanterv-ajánlás az 51/2012. (XII.21.) EMMI rendelet: 2. melléklet 2.2.10.1 Kémia 7-8. alapján készült.
B. feladat elvégzendő és nem elvégzendő kísérletei, kísérletleírásai. 1. Cink reakciói
 B. feladat elvégzendő és nem elvégzendő kísérletei, kísérletleírásai 1. Cink reakciói Három kémcsőbe öntsön rendre 2cm 3-2cm 3 vizet, 2 mol/dm 3 koncentrációjú sósavat, rézszulfát-oldatot, és mindegyik
B. feladat elvégzendő és nem elvégzendő kísérletei, kísérletleírásai 1. Cink reakciói Három kémcsőbe öntsön rendre 2cm 3-2cm 3 vizet, 2 mol/dm 3 koncentrációjú sósavat, rézszulfát-oldatot, és mindegyik
MATEMATIKAI KOMPETENCIATERÜLET A
 MATEMATIKAI KOMPETENCIATERÜLET A Matematika 2. évfolyam eszközök diákok és csoportok részére 1. félév A kiadvány KHF/4001-18/2008. engedélyszámon 2008.08.18. időponttól tankönyvi engedélyt kapott Educatio
MATEMATIKAI KOMPETENCIATERÜLET A Matematika 2. évfolyam eszközök diákok és csoportok részére 1. félév A kiadvány KHF/4001-18/2008. engedélyszámon 2008.08.18. időponttól tankönyvi engedélyt kapott Educatio
Csermák Mihály: Kémia 8. Panoráma sorozat
 Csermák Mihály: Kémia 8. Panoráma sorozat Kedves Kollégák! A Panoráma sorozat kiadványainak megalkotása során két fő szempontot tartottunk szem előtt. Egyrészt olyan tankönyvet szerettünk volna létrehozni,
Csermák Mihály: Kémia 8. Panoráma sorozat Kedves Kollégák! A Panoráma sorozat kiadványainak megalkotása során két fő szempontot tartottunk szem előtt. Egyrészt olyan tankönyvet szerettünk volna létrehozni,
ÚTMUTATÓ ÉS TANMENETJAVASLAT Kecskésné-sorozat Kémia 8.
 ÚTMUTATÓ ÉS TANMENETJAVASLAT Kecskésné-sorozat Kémia 8. Oktatáskutató és Fejlesztő Intézet, Budapest 1 Az Útmutató és tanmenetjavaslat Kecskés Andrásné Kiss Zsuzsanna Rozgonyi Jánosné: Kémia 8. című, NT-00877-es
ÚTMUTATÓ ÉS TANMENETJAVASLAT Kecskésné-sorozat Kémia 8. Oktatáskutató és Fejlesztő Intézet, Budapest 1 Az Útmutató és tanmenetjavaslat Kecskés Andrásné Kiss Zsuzsanna Rozgonyi Jánosné: Kémia 8. című, NT-00877-es
KÉMIA I. RÉSZLETES ÉRETTSÉGIVIZSGA-KÖVETELMÉNY A) KOMPETENCIÁK
 KÉMIA I. RÉSZLETES ÉRETTSÉGIVIZSGA-KÖVETELMÉNY A) KOMPETENCIÁK A vizsgázónak a követelményrendszerben és a vizsgaleírásban meghatározott módon, az alábbi kompetenciák meglétét kell bizonyítania: - a természettudományos
KÉMIA I. RÉSZLETES ÉRETTSÉGIVIZSGA-KÖVETELMÉNY A) KOMPETENCIÁK A vizsgázónak a követelményrendszerben és a vizsgaleírásban meghatározott módon, az alábbi kompetenciák meglétét kell bizonyítania: - a természettudományos
A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja. KÉMIÁBÓL I. kategóriában ÚTMUTATÓ
 Oktatási ivatal A versenyző kódszáma: A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja Munkaidő: 300 perc Elérhető pontszám: 100 pont KÉMIÁBÓL I. kategóriában
Oktatási ivatal A versenyző kódszáma: A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja Munkaidő: 300 perc Elérhető pontszám: 100 pont KÉMIÁBÓL I. kategóriában
Elméleti alapok: Fe + 2HCl = FeCl 2 +H 2 Fe + S = FeS FeS + 2HCl = FeCl 2 + H 2 S
 6. gyakorlat. Keverék, vegyület,oldat, elegy, szuszpenzió, emulzió fogalma. A vegyületek termikus hatásra bekövetkezı változásai: olvadás, szublimáció, bomlás: kristályvíz vesztés, krakkolódás. Oldódás
6. gyakorlat. Keverék, vegyület,oldat, elegy, szuszpenzió, emulzió fogalma. A vegyületek termikus hatásra bekövetkezı változásai: olvadás, szublimáció, bomlás: kristályvíz vesztés, krakkolódás. Oldódás
KÉMIA I. RÉSZLETES ÉRETTSÉGI VIZSGAKÖVETELMÉNY A) KOMPETENCIÁK
 KÉMIA Elvárt kompetenciák: I. RÉSZLETES ÉRETTSÉGI VIZSGAKÖVETELMÉNY A) KOMPETENCIÁK induktív következtetés (egyedi tényekből az általános törvényszerűségekre) deduktív következtetés (az általános törvényszerűségekből
KÉMIA Elvárt kompetenciák: I. RÉSZLETES ÉRETTSÉGI VIZSGAKÖVETELMÉNY A) KOMPETENCIÁK induktív következtetés (egyedi tényekből az általános törvényszerűségekre) deduktív következtetés (az általános törvényszerűségekből
Szakmai ismeret A V Í Z
 A V Í Z A hidrogén oxidja (H 2 O). A Földön 1 az egyik legelterjedtebb vegyület, molekula (2H 2 O). Színtelen, szagtalan folyadék, légköri (1013 mbar ~ 1013 hpa) nyomáson 0 o C-on megfagy, 100 o C-on forr,
A V Í Z A hidrogén oxidja (H 2 O). A Földön 1 az egyik legelterjedtebb vegyület, molekula (2H 2 O). Színtelen, szagtalan folyadék, légköri (1013 mbar ~ 1013 hpa) nyomáson 0 o C-on megfagy, 100 o C-on forr,
KÉMIA OLIMPIÁSZ. 45. évfolyam, 2008/2009 tanév
 KÉMIA OLIMPIÁSZ 45. évfolyam, 2008/2009 tanév D kategória az ötéves gimnáziumok 1. évfolyama, a hatéves gimnáziumok 1. és 2. évfolyama, a nyolcéves gimnáziumok tercier és kvartér, valamint az alapiskolák
KÉMIA OLIMPIÁSZ 45. évfolyam, 2008/2009 tanév D kategória az ötéves gimnáziumok 1. évfolyama, a hatéves gimnáziumok 1. és 2. évfolyama, a nyolcéves gimnáziumok tercier és kvartér, valamint az alapiskolák
KÉMIA 10. Osztály I. FORDULÓ
 KÉMIA 10. Osztály I. FORDULÓ 1) A rejtvény egy híres ember nevét és halálának évszámát rejti. Nevét megtudod, ha a részmegoldások betűit a számozott négyzetekbe írod, halálának évszámát pedig pici számolással.
KÉMIA 10. Osztály I. FORDULÓ 1) A rejtvény egy híres ember nevét és halálának évszámát rejti. Nevét megtudod, ha a részmegoldások betűit a számozott négyzetekbe írod, halálának évszámát pedig pici számolással.
1. feladat Összesen: 10 pont. 2. feladat Összesen: 6 pont. 3. feladat Összesen: 18 pont
 1. feladat Összesen: 10 pont Etil-acetátot állítunk elő 1 mol ecetsav és 1 mol etil-alkohol felhasználásával. Az egyensúlyi helyzet beálltakor a reakciót leállítjuk, és az elegyet 1 dm 3 -re töltjük fel.
1. feladat Összesen: 10 pont Etil-acetátot állítunk elő 1 mol ecetsav és 1 mol etil-alkohol felhasználásával. Az egyensúlyi helyzet beálltakor a reakciót leállítjuk, és az elegyet 1 dm 3 -re töltjük fel.
O k t a t á si Hivatal
 O k t a t á si Hivatal Országos Középiskolai Tanulmányi Verseny Kémia I. kategória 3. forduló Budapest, 2015. március 21. A verseny döntője három mérési feladatból áll. Mindhárom feladat szövege, valamint
O k t a t á si Hivatal Országos Középiskolai Tanulmányi Verseny Kémia I. kategória 3. forduló Budapest, 2015. március 21. A verseny döntője három mérési feladatból áll. Mindhárom feladat szövege, valamint
Kémia emelt szintű érettségi írásbeli vizsga ELEMZÉS (BARANYA) ÉS AJÁNLÁS KÉSZÍTETTE: NAGY MÁRIA
 Kémia emelt szintű érettségi írásbeli vizsga ELEMZÉS (BARANYA) ÉS AJÁNLÁS KÉSZÍTETTE: NAGY MÁRIA Idei gyorsjelentés http://eduline.hu/erettsegi_felveteli/2 015/7/16/Az_elmult_7_ev_legrosszab b_eredmenye_szulet_azozlb
Kémia emelt szintű érettségi írásbeli vizsga ELEMZÉS (BARANYA) ÉS AJÁNLÁS KÉSZÍTETTE: NAGY MÁRIA Idei gyorsjelentés http://eduline.hu/erettsegi_felveteli/2 015/7/16/Az_elmult_7_ev_legrosszab b_eredmenye_szulet_azozlb
Azonosító jel: KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA. 2009. október 28. 14:00. Az írásbeli vizsga időtartama: 240 perc
 É RETTSÉGI VIZSGA 2009. október 28. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2009. október 28. 14:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati KTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
É RETTSÉGI VIZSGA 2009. október 28. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2009. október 28. 14:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati KTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
A szilárd állapot. A szilárd állapot. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 A szilárd állapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Szobahőmérsékleten és légköri nyomáson szilárd halmazállapot létrejöttének feltétele, hogy a szilárd részecskék
A szilárd állapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Szobahőmérsékleten és légköri nyomáson szilárd halmazállapot létrejöttének feltétele, hogy a szilárd részecskék
KÉMIA A kerettanterv B változata alapján készült A kémia tanításának célja és feladatai
 KÉMIA A kerettanterv B változata alapján készült A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan sajátítsák el azt a kémiai műveltségtartalmat és
KÉMIA A kerettanterv B változata alapján készült A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan sajátítsák el azt a kémiai műveltségtartalmat és
HELYI TANTERV KÉMIA A KOCH VALÉRIA ISKOLAKÖZPONT 7. 8. OSZTÁLYA SZÁMÁRA
 HELYI TANTERV KÉMIA A KOCH VALÉRIA ISKOLAKÖZPONT 7. 8. OSZTÁLYA SZÁMÁRA Az általános iskolai kémiatanítás célja, hogy a tanulók sajátítsanak el olyan műveltségtartalmat, amely megismerteti velük a természetben
HELYI TANTERV KÉMIA A KOCH VALÉRIA ISKOLAKÖZPONT 7. 8. OSZTÁLYA SZÁMÁRA Az általános iskolai kémiatanítás célja, hogy a tanulók sajátítsanak el olyan műveltségtartalmat, amely megismerteti velük a természetben
KÉMIA 7-8. évfolyam A helyi tanterv a kerettanterv B változata alapján készült A kémia tanításának célja és feladatai
 KÉMIA 7-8. évfolyam A helyi tanterv a kerettanterv B változata alapján készült A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan sajátítsák el azt
KÉMIA 7-8. évfolyam A helyi tanterv a kerettanterv B változata alapján készült A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan sajátítsák el azt
VÍZKEZELÉS Kazántápvíz előkészítés ioncserés sómentesítéssel
 A víz keménysége VÍZKEZELÉS Kazántápvíz előkészítés ioncserés sómentesítéssel A természetes vizek alkotóelemei között számos kation ( pl.: Na +, Ca ++, Mg ++, H +, K +, NH 4 +, Fe ++, stb) és anion (Cl
A víz keménysége VÍZKEZELÉS Kazántápvíz előkészítés ioncserés sómentesítéssel A természetes vizek alkotóelemei között számos kation ( pl.: Na +, Ca ++, Mg ++, H +, K +, NH 4 +, Fe ++, stb) és anion (Cl
RAJZ ÉS VIZUÁLIS KULTÚRA 6. évfolyam
 SZÖVEGÉRTÉS-SZÖVEGALKOTÁS RAJZ ÉS VIZUÁLIS KULTÚRA 6. évfolyam TANULÓI MUNKAFÜZET Készítette: Molnár Krisztina 3 Az angyali üdvözlet Három festmény A KIADVÁNY KHF/4531-13/2008 ENGEDÉLYSZÁMON 2008. 12.
SZÖVEGÉRTÉS-SZÖVEGALKOTÁS RAJZ ÉS VIZUÁLIS KULTÚRA 6. évfolyam TANULÓI MUNKAFÜZET Készítette: Molnár Krisztina 3 Az angyali üdvözlet Három festmény A KIADVÁNY KHF/4531-13/2008 ENGEDÉLYSZÁMON 2008. 12.
MATEMATIKAI KOMPETENCIATERÜLET A
 MATEMATIKAI KOMPETENCIATERÜLET A Matematika 6. évfolyam TANULÓI MUNKAFÜZET 2. FÉLÉV A kiadvány KHF/4356-14/2008. engedélyszámon 2008.11.25. időponttól tankönyvi engedélyt kapott Educatio Kht. Kompetenciafejlesztő
MATEMATIKAI KOMPETENCIATERÜLET A Matematika 6. évfolyam TANULÓI MUNKAFÜZET 2. FÉLÉV A kiadvány KHF/4356-14/2008. engedélyszámon 2008.11.25. időponttól tankönyvi engedélyt kapott Educatio Kht. Kompetenciafejlesztő
 TAKÁCS CSABA KÉMIA EMLÉKVERSENY, IX. osztály, III. forduló - megoldás 2010 / 2011 es tanév, XVI. évfolyam 1. a) 2008. dec. 30-án, az ENSZ Közgyűlés 63. ülésszakán Etiópia előterjesztésére határozták el.
TAKÁCS CSABA KÉMIA EMLÉKVERSENY, IX. osztály, III. forduló - megoldás 2010 / 2011 es tanév, XVI. évfolyam 1. a) 2008. dec. 30-án, az ENSZ Közgyűlés 63. ülésszakán Etiópia előterjesztésére határozták el.
Tanulói munkafüzet. Kémia. 7. évfolyam 2015.
 Tanulói munkafüzet Kémia 7. évfolyam 2015. Összeállította: Tóthné Tamás Ildikó Lektorálta: Dávid Ágnes Szakképző Iskola és ban 1 KÉMIA 7. OSZTÁLY Tanulói munkafüzet Szakképző Iskola és ban 2 Tartalom MUNKA-ÉS
Tanulói munkafüzet Kémia 7. évfolyam 2015. Összeállította: Tóthné Tamás Ildikó Lektorálta: Dávid Ágnes Szakképző Iskola és ban 1 KÉMIA 7. OSZTÁLY Tanulói munkafüzet Szakképző Iskola és ban 2 Tartalom MUNKA-ÉS
100% = 100 pont A VIZSGAFELADAT MEGOLDÁSÁRA JAVASOLT %-OS EREDMÉNY: EBBEN A VIZSGARÉSZBEN A VIZSGAFELADAT ARÁNYA 40%.
 Az Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről szóló 133/2010. (IV. 22.) Korm. rendelet alapján. Szakképesítés, szakképesítés-elágazás, rész-szakképesítés,
Az Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről szóló 133/2010. (IV. 22.) Korm. rendelet alapján. Szakképesítés, szakképesítés-elágazás, rész-szakképesítés,
(3) (3) (3) (3) (2) (2) (2) (2) (4) (2) (2) (3) (4) (3) (4) (2) (3) (2) (2) (2)
 TAKÁCS CSABA KÉMIA EMLÉKVERSENY, IX. osztály, II. forduló - megoldás 2009 / 2010 es tanév, XV. évfolyam 1. a) Albertus, Magnus; német polihisztor (1250-ben) (0,5 p) b) Brandt, Georg; svéd kémikus (1735-ben)
TAKÁCS CSABA KÉMIA EMLÉKVERSENY, IX. osztály, II. forduló - megoldás 2009 / 2010 es tanév, XV. évfolyam 1. a) Albertus, Magnus; német polihisztor (1250-ben) (0,5 p) b) Brandt, Georg; svéd kémikus (1735-ben)
1. Melyik az az elem, amelynek csak egy természetes izotópja van? 2. Melyik vegyület molekulájában van az összes atom egy síkban?
 A 2004/2005. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja KÉMIA (II. kategória) I. FELADATSOR 1. Melyik az az elem, amelynek csak egy természetes izotópja van? A) Na
A 2004/2005. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja KÉMIA (II. kategória) I. FELADATSOR 1. Melyik az az elem, amelynek csak egy természetes izotópja van? A) Na
MATEMATIKAI KOMPETENCIATERÜLET A
 MATEMATIKAI KOMPETENCIATERÜLET A Matematika 5. évfolyam eszközök diákok és csoportok részére 1. félév A kiadvány KHF/4633-13/2008. engedélyszámon 2008.12.16. időponttól tankönyvi engedélyt kapott Educatio
MATEMATIKAI KOMPETENCIATERÜLET A Matematika 5. évfolyam eszközök diákok és csoportok részére 1. félév A kiadvány KHF/4633-13/2008. engedélyszámon 2008.12.16. időponttól tankönyvi engedélyt kapott Educatio
Készült az 51/2012. (XII. 21.) EMMI rendelet 2. sz. melléklet 2.2.10.2 (B) változatához a Mozaik Kiadó ajánlása alapján
 KÉMIA 7-8. Készült az 51/2012. (XII. 21.) EMMI rendelet 2. sz. melléklet 2.2.10.2 (B) változatához a Mozaik Kiadó ajánlása alapján A kémia tanításának célja és feladatai A kémia tanításának célja és feladata,
KÉMIA 7-8. Készült az 51/2012. (XII. 21.) EMMI rendelet 2. sz. melléklet 2.2.10.2 (B) változatához a Mozaik Kiadó ajánlása alapján A kémia tanításának célja és feladatai A kémia tanításának célja és feladata,
EMELT SZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2016. május 13. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2016. május 13. 8:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Kémia
ÉRETTSÉGI VIZSGA 2016. május 13. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2016. május 13. 8:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Kémia
BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék. Hőkezelés 2. (PhD) féléves házi feladat. Acélok cementálása. Thiele Ádám WTOSJ2
 BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Hőkezelés. (PhD) féléves házi feladat Acélok cementálása Thiele Ádám WTOSJ Budaest, 11 Tartalomjegyzék 1. A termokémiai kezeléseknél lejátszódó
BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Hőkezelés. (PhD) féléves házi feladat Acélok cementálása Thiele Ádám WTOSJ Budaest, 11 Tartalomjegyzék 1. A termokémiai kezeléseknél lejátszódó
Oktatáskutató és Fejlesztő Intézet TÁMOP-3.1.1-11/1-2012-0001 XXI. századi közoktatás (fejlesztés, koordináció) II. szakasz KÉMIA 4.
 Oktatáskutató és Fejlesztő Intézet TÁMOP-3.1.1-11/1-2012-0001 XXI. századi közoktatás (fejlesztés, koordináció) II. szakasz KÉMIA 4. MINTAFELADATSOR KÖZÉPSZINT 2015 Az írásbeli vizsga időtartama: 120 perc
Oktatáskutató és Fejlesztő Intézet TÁMOP-3.1.1-11/1-2012-0001 XXI. századi közoktatás (fejlesztés, koordináció) II. szakasz KÉMIA 4. MINTAFELADATSOR KÖZÉPSZINT 2015 Az írásbeli vizsga időtartama: 120 perc
A vas-oxidok redukciós folyamatainak termodinamikája
 BUDAESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyag- és gyártástechnológia (hd) féléves házi feladat A vas-oxidok redukciós folyamatainak termodinamikája Thiele Ádám WTOSJ Budapest, 11
BUDAESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyag- és gyártástechnológia (hd) féléves házi feladat A vas-oxidok redukciós folyamatainak termodinamikája Thiele Ádám WTOSJ Budapest, 11
ELTE Kémiai Intézet (http://www.chem.elte.hu) kislexikonja a vörösiszap-katasztrófával kapcsolatos fogalmak magyarázatára 2010. október 18.
 ELTE Kémiai Intézet (http://www.chem.elte.hu) kislexikonja a vörösiszap-katasztrófával kapcsolatos fogalmak magyarázatára 2010. október 18. A vörösiszap-katasztrófáról tudósító hírekben sok olyan kifejezés
ELTE Kémiai Intézet (http://www.chem.elte.hu) kislexikonja a vörösiszap-katasztrófával kapcsolatos fogalmak magyarázatára 2010. október 18. A vörösiszap-katasztrófáról tudósító hírekben sok olyan kifejezés
Tartalmi követelmények kémia tantárgyból az érettségin
 Témakör 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
Témakör 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1996
 1996 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1996 I. Az alábbiakban megadott vázlatpontok alapján írjon 1-1,5 oldalas dolgozatot! Címe: ALKÉNEK Alkének fogalma. Elnevezésük elve példával.
1996 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1996 I. Az alábbiakban megadott vázlatpontok alapján írjon 1-1,5 oldalas dolgozatot! Címe: ALKÉNEK Alkének fogalma. Elnevezésük elve példával.
MATEMATIKAI KOMPETENCIATERÜLET B
 MATEMATIKAI KOMPETENCIATERÜLET B Földünk és környezetünk 10. évfolyam TANULÓI MUNKAFÜZET Készítette: Kiss Gábor A kiadvány KHF/4585-12/2008. engedélyszámon 2008.12.16. időponttól tankönyvi engedélyt kapott
MATEMATIKAI KOMPETENCIATERÜLET B Földünk és környezetünk 10. évfolyam TANULÓI MUNKAFÜZET Készítette: Kiss Gábor A kiadvány KHF/4585-12/2008. engedélyszámon 2008.12.16. időponttól tankönyvi engedélyt kapott
- 2 db Erlenmeyer-lombik - 2 db mérőhenger - 2 db tölcsér - labormérleg - szűrőpapír
 1. A talaj vízmegkötő képességének vizsgálata Kötelező védőeszközök Szükséges eszközök - 2 db Erlenmeyer-lombik - 2 db mérőhenger - 2 db tölcsér - labormérleg - szűrőpapír Szükséges anyagok - talajminták
1. A talaj vízmegkötő képességének vizsgálata Kötelező védőeszközök Szükséges eszközök - 2 db Erlenmeyer-lombik - 2 db mérőhenger - 2 db tölcsér - labormérleg - szűrőpapír Szükséges anyagok - talajminták
A kémia tanításának célja és feladatai
 7. évfolyam A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan sajátítsák el azt a kémiai műveltségtartalmat és szemléletet, amely a 21. század kulturált
7. évfolyam A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan sajátítsák el azt a kémiai műveltségtartalmat és szemléletet, amely a 21. század kulturált
A VÍZ OLDOTT SZENNYEZŐANYAG-TARTALMÁNAK ELTÁVOLÍTÁSA IONCSERÉVEL
 A VÍZ OLDOTT SZENNYEZŐANYAG-TARTALMÁNAK ELTÁVOLÍTÁSA IONCSERÉVEL ELTE Szerves Kémiai Tanszék A VÍZ OLDOTT SZENNYEZŐANYAG -TARTALMÁNAK ELTÁVOLÍTÁSA IONCSERÉVEL Bevezetés A természetes vizeket (felszíni
A VÍZ OLDOTT SZENNYEZŐANYAG-TARTALMÁNAK ELTÁVOLÍTÁSA IONCSERÉVEL ELTE Szerves Kémiai Tanszék A VÍZ OLDOTT SZENNYEZŐANYAG -TARTALMÁNAK ELTÁVOLÍTÁSA IONCSERÉVEL Bevezetés A természetes vizeket (felszíni
A vér vizsgálata. 12. B. biológia fakultációsainak projektje 2015.03.30-31.
 A vér vizsgálata 12. B. biológia fakultációsainak projektje 2015.03.30-31. Vérkenet készítése Menete: Alkoholos vattával letörölt ujjbegyünket szúrjuk meg steril tűvel.töröljük le az első vércseppet, majd
A vér vizsgálata 12. B. biológia fakultációsainak projektje 2015.03.30-31. Vérkenet készítése Menete: Alkoholos vattával letörölt ujjbegyünket szúrjuk meg steril tűvel.töröljük le az első vércseppet, majd
Klasszikus analitikai módszerek:
 Klasszikus analitikai módszerek: Azok a módszerek, melyek kémiai reakciókon alapszanak, de az elemzéshez csupán a tömeg és térfogat pontos mérésére van szükség. A legfontosabb klasszikus analitikai módszerek
Klasszikus analitikai módszerek: Azok a módszerek, melyek kémiai reakciókon alapszanak, de az elemzéshez csupán a tömeg és térfogat pontos mérésére van szükség. A legfontosabb klasszikus analitikai módszerek
52 522 06 0000 00 00 Erőművi kazángépész Erőművi kazángépész
 A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
Laboratóriumi technikus laboratóriumi technikus 54 524 01 0010 54 02 Drog és toxikológiai
 É 049-06/1/3 A 10/007 (II. 7.) SzMM rendelettel módosított 1/006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján.
É 049-06/1/3 A 10/007 (II. 7.) SzMM rendelettel módosított 1/006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján.
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
ÉLETPÁLYA- ÉPÍTÉS MATEMATIKA TANÁRI ÚTMUTATÓ KOMPETENCIATERÜLET B. 6. évfolyam
 ÉLETPÁLYA- ÉPÍTÉS KOMPETENCIATERÜLET B MATEMATIKA TANÁRI ÚTMUTATÓ 6. évfolyam A kiadvány az Educatio Kht. kompetenciafejlesztő oktatási program kerettanterve alapján készült. A kiadvány a Nemzeti Fejlesztési
ÉLETPÁLYA- ÉPÍTÉS KOMPETENCIATERÜLET B MATEMATIKA TANÁRI ÚTMUTATÓ 6. évfolyam A kiadvány az Educatio Kht. kompetenciafejlesztő oktatási program kerettanterve alapján készült. A kiadvány a Nemzeti Fejlesztési
KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2010. május 12. BIOLÓGIA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2010. május 12. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
ÉRETTSÉGI VIZSGA 2010. május 12. BIOLÓGIA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2010. május 12. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2014. május 19. FIZIKA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2014. május 19. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Fizika
ÉRETTSÉGI VIZSGA 2014. május 19. FIZIKA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2014. május 19. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Fizika
MATEMATIKAI KOMPETENCIATERÜLET A
 MATEMATIKAI KOMPETENCIATERÜLET A Matematika 3. évfolyam Diák mérőlapok A kiadvány KHF/3992-8/2008. engedélyszámon 2008.08.8. időponttól tankönyvi engedélyt kapott Educatio Kht. Kompetenciafejlesztő oktatási
MATEMATIKAI KOMPETENCIATERÜLET A Matematika 3. évfolyam Diák mérőlapok A kiadvány KHF/3992-8/2008. engedélyszámon 2008.08.8. időponttól tankönyvi engedélyt kapott Educatio Kht. Kompetenciafejlesztő oktatási
T I T - M T T. Hevesy György Kémiaverseny. országos döntő. Az írásbeli forduló feladatlapja. 8. osztály. 2. feladat:... pont. 3. feladat:...
 T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 8. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 8. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
munkafüzet MUNKAFÜZET Kémia Kísérleti tankönyv
 Kísérleti tankönyv FI-505050702 978-963-682-823-3 7 Kémia MUNKAFÜZET A teljes munkafüzet interneten keresztül is megtekinthetô az Oktatáskutató és Fejlesztô Intézet honlapján (ofi.hu). Kémia munkafüzet
Kísérleti tankönyv FI-505050702 978-963-682-823-3 7 Kémia MUNKAFÜZET A teljes munkafüzet interneten keresztül is megtekinthetô az Oktatáskutató és Fejlesztô Intézet honlapján (ofi.hu). Kémia munkafüzet
MUNKAANYAG. Dabi Ágnes. A villamos ívhegesztés fajtái, berendezései, anyagai, segédanyagai, berendezésének alkalmazása
 Dabi Ágnes A villamos ívhegesztés fajtái, berendezései, anyagai, segédanyagai, berendezésének alkalmazása A követelménymodul megnevezése: Gépészeti kötési feladatok A követelménymodul száma: 0220-06 A
Dabi Ágnes A villamos ívhegesztés fajtái, berendezései, anyagai, segédanyagai, berendezésének alkalmazása A követelménymodul megnevezése: Gépészeti kötési feladatok A követelménymodul száma: 0220-06 A
MIT TUDOK A TERMÉSZETRŐL? INTERNETES VETÉLKEDŐ KÉMIA FELADATMEGOLDÓ VERSENY
 JAVÍTÓKULCS Elérhető összes pontszám: 115 pont 1.) Nyelvészkedjünk! (10 pont) Az alábbiakban kémiai elemek magyar névváltozatai vannak felsorolva a nyelvújítás korából. Írd a megfelelő kifejezések mellé
JAVÍTÓKULCS Elérhető összes pontszám: 115 pont 1.) Nyelvészkedjünk! (10 pont) Az alábbiakban kémiai elemek magyar névváltozatai vannak felsorolva a nyelvújítás korából. Írd a megfelelő kifejezések mellé
Nátrium és Kalcium részösszefoglaló feladatlap
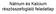 Nátrium és Kalcium részösszefoglaló feladatlap 1. Írd le a következő elemek és vegyületek kémiai nevét: 1.NaOH, 2.Ca, 3.Mg, 4.CaCO 3, 5.NaCl, 6.Na 2 CO 3 7.CaSO 4, 8.Ca(OH) 2, 9.CaO, 10CO 2, 11.HCl, 12.Na,
Nátrium és Kalcium részösszefoglaló feladatlap 1. Írd le a következő elemek és vegyületek kémiai nevét: 1.NaOH, 2.Ca, 3.Mg, 4.CaCO 3, 5.NaCl, 6.Na 2 CO 3 7.CaSO 4, 8.Ca(OH) 2, 9.CaO, 10CO 2, 11.HCl, 12.Na,
Kémia 9. osztály. 1. Lángfestés.. 2. 2. Gázok áramlási sebessége... 4. 3. Túltelített oldatok... 6
 Kémia 9. osztály 1 Kémia 9. osztály Tartalom 1. Lángfestés.. 2 2. Gázok áramlási sebessége..................................................... 4 3. Túltelített oldatok............................................................
Kémia 9. osztály 1 Kémia 9. osztály Tartalom 1. Lángfestés.. 2 2. Gázok áramlási sebessége..................................................... 4 3. Túltelített oldatok............................................................
Helyi tanterv KÉMIA I. TÍPUS. 7 10. évfolyam 2008.
 Éltes Mátyás Egységes Gyógypedagógiai Módszertani Intézmény, Általános Iskola, Speciális Szakiskola és Egységes Pedagógiai Szakszolgálat Helyi tanterv KÉMIA I. TÍPUS 7 10. évfolyam 2008. Officina Bona
Éltes Mátyás Egységes Gyógypedagógiai Módszertani Intézmény, Általános Iskola, Speciális Szakiskola és Egységes Pedagógiai Szakszolgálat Helyi tanterv KÉMIA I. TÍPUS 7 10. évfolyam 2008. Officina Bona
KÉMIA. 7 10. évfolyam. Célok és feladatok
 KÉMIA 7 10. évfolyam Célok és feladatok Az Ember a természetben műveltségi terület legfontosabb célja, hogy a tanulók a három természettudományos tantárgy (fizika, kémia, biológia) és a földrajz segítségével
KÉMIA 7 10. évfolyam Célok és feladatok Az Ember a természetben műveltségi terület legfontosabb célja, hogy a tanulók a három természettudományos tantárgy (fizika, kémia, biológia) és a földrajz segítségével
HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY
 MAGYAR TERMÉSZETTUDOMÁNYI TÁRSULAT HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY Országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont
MAGYAR TERMÉSZETTUDOMÁNYI TÁRSULAT HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY Országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont
v1.04 Analitika példatár
 Bevezető A példatár azért készült, hogy segítséget kapjon az a tanuló, aki eredményesen akarja elsajátítatni az analitikai számítások alapjait. Minden feladat végén dőlt karakterekkel megtalálható az eredmény.
Bevezető A példatár azért készült, hogy segítséget kapjon az a tanuló, aki eredményesen akarja elsajátítatni az analitikai számítások alapjait. Minden feladat végén dőlt karakterekkel megtalálható az eredmény.
A TERMÉSZETES VIZEK KEMÉNYSÉGE
 A TERMÉSZETES VIZEK KEMÉNYSÉGE Mi van a természetes vizekben? oldott anyagok és lebegő szennyezések is Az eső és a hó tartalmaz e szennyezést? nem, ezek a legtisztábbak A csapadékvíz csak a gázokat oldja
A TERMÉSZETES VIZEK KEMÉNYSÉGE Mi van a természetes vizekben? oldott anyagok és lebegő szennyezések is Az eső és a hó tartalmaz e szennyezést? nem, ezek a legtisztábbak A csapadékvíz csak a gázokat oldja
5.20 Kémia a 7 8. évfolyama számára
 5.20 az EMMI kerettanterv 51/2012. (XII. 21.) EMMI rendelet 2. melléklet 2.2.10.2 (B) változatához A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan
5.20 az EMMI kerettanterv 51/2012. (XII. 21.) EMMI rendelet 2. melléklet 2.2.10.2 (B) változatához A kémia tanításának célja és feladatai A kémia tanításának célja és feladata, hogy a tanulók fokozatosan
9. Osztály. Kód. Szent-Györgyi Albert kémiavetélkedő
 9. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
9. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
D1 A szólások jelentése
 Oldatok SZKA103_33 tanulói oldatok 3. évfolyam 143 Diákmelléklet D1 A szólások jelentése Beszéljétek meg, majd írjátok a következő szólások mellé, hogy szerintetek melyik, mit jelent! Lóg az eső lába.
Oldatok SZKA103_33 tanulói oldatok 3. évfolyam 143 Diákmelléklet D1 A szólások jelentése Beszéljétek meg, majd írjátok a következő szólások mellé, hogy szerintetek melyik, mit jelent! Lóg az eső lába.
Kémiai reakciók Műszaki kémia, Anyagtan I. 11. előadás
 Kémiai reakciók Műszaki kémia, Anyagtan I. 11. előadás Dolgosné dr. Kovács Anita egy.doc. PTE MIK Környezetmérnöki Tanszék Kémiai reakció Kémiai reakció: különböző anyagok kémiai összetételének, ill. szerkezetének
Kémiai reakciók Műszaki kémia, Anyagtan I. 11. előadás Dolgosné dr. Kovács Anita egy.doc. PTE MIK Környezetmérnöki Tanszék Kémiai reakció Kémiai reakció: különböző anyagok kémiai összetételének, ill. szerkezetének
KÉMIA KÖZÉPSZINTŰ SZÓBELI VIZSGA TÉMAKÖREI, KÍSÉRLETEI ÉS KÍSÉRLETLEÍRÁSAI. A feladat témakörei
 KÉMIA KÖZÉPSZINTŰ SZÓBELI VIZSGA TÉMAKÖREI, KÍSÉRLETEI ÉS KÍSÉRLETLEÍRÁSAI A feladat témakörei 1.Atomszerkezet 2.A periódusos rendszer 3.Kémiai kötések 4.Molekulák, összetett ionok 5.Anyagi halmazok 6.Egykomponensű
KÉMIA KÖZÉPSZINTŰ SZÓBELI VIZSGA TÉMAKÖREI, KÍSÉRLETEI ÉS KÍSÉRLETLEÍRÁSAI A feladat témakörei 1.Atomszerkezet 2.A periódusos rendszer 3.Kémiai kötések 4.Molekulák, összetett ionok 5.Anyagi halmazok 6.Egykomponensű
NE FELEJTSÉTEK EL BEÍRNI AZ EREDMÉNYEKET A KIJELÖLT HELYEKRE! A feladatok megoldásához szükséges kerekített értékek a következők:
 A Szerb Köztársaság Oktatási Minisztériuma Szerbiai Kémikusok Egyesülete Köztársasági verseny kémiából Kragujevac, 2008. 05. 24.. Teszt a középiskolák I. osztálya számára Név és utónév Helység és iskola
A Szerb Köztársaság Oktatási Minisztériuma Szerbiai Kémikusok Egyesülete Köztársasági verseny kémiából Kragujevac, 2008. 05. 24.. Teszt a középiskolák I. osztálya számára Név és utónév Helység és iskola
2 képzıdése. értelmezze Reakciók tanult nemfémekkel
 Emelt szint: Az s mezı fémei 1. Az alkálifémek és alkáliföldfémek összehasonlító jellemzése (anyagszerkezet, kémiaiés fizikai jellemzık, elıfordulás, elıállítás, élettani hatás). Használja a periódusos
Emelt szint: Az s mezı fémei 1. Az alkálifémek és alkáliföldfémek összehasonlító jellemzése (anyagszerkezet, kémiaiés fizikai jellemzık, elıfordulás, elıállítás, élettani hatás). Használja a periódusos
KÉMIA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Kémia középszint 1512 ÉRETTSÉGI VIZSGA 2015. október 20. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
Kémia középszint 1512 ÉRETTSÉGI VIZSGA 2015. október 20. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
természetismeret szövegértés szövegalkotás Tanulói Bmunkafüzet Készítette Boronkai Dóra
 Tanulói Bmunkafüzet S Z Ö V E G É R T É S S Z Ö V E G A L K O T Á S Készítette Boronkai Dóra természetismeret szövegértés szövegalkotás 3 Tájékozódás a földgömbön 14 Hazánk nagy dombvidéke, a Dunántúli-dombság
Tanulói Bmunkafüzet S Z Ö V E G É R T É S S Z Ö V E G A L K O T Á S Készítette Boronkai Dóra természetismeret szövegértés szövegalkotás 3 Tájékozódás a földgömbön 14 Hazánk nagy dombvidéke, a Dunántúli-dombság
Fejlesztendő területek, kompetenciák:
 KÉMIA A tanterv célja annak elérése, hogy középiskolai tanulmányainak befejezésekor minden tanuló birtokában legyen a kémiai alapműveltségnek, ami a természettudományos alapműveltség része. Ezért szükséges,
KÉMIA A tanterv célja annak elérése, hogy középiskolai tanulmányainak befejezésekor minden tanuló birtokában legyen a kémiai alapműveltségnek, ami a természettudományos alapműveltség része. Ezért szükséges,
Azonosító jel: KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA. 2006. október 31. 14:00. Az írásbeli vizsga időtartama: 240 perc
 É RETTSÉGI VIZSGA 2006. október 31. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2006. október 31. 14:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
É RETTSÉGI VIZSGA 2006. október 31. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2006. október 31. 14:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
FIGYELEM. Elkészítés időpontja: 2007. 01. 15. Felülvizsgálat időpontja: 2015. 06. 19. Verziószám: 4
 BIZTONSÁGI ADATLAP 1. SZAKASZ: A KEVERÉK ÉS A VÁLLALAT/VÁLLALKOZÁS AZONOSÍTÁSA 1.1. Termékazonosító: 1.2. A keverék megfelelő azonosított felhasználása, illetve ellenjavallt felhasználása: Szaniter tisztító,
BIZTONSÁGI ADATLAP 1. SZAKASZ: A KEVERÉK ÉS A VÁLLALAT/VÁLLALKOZÁS AZONOSÍTÁSA 1.1. Termékazonosító: 1.2. A keverék megfelelő azonosított felhasználása, illetve ellenjavallt felhasználása: Szaniter tisztító,
(11) Lajstromszám: E 006 537 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000637T2! (19) HU (11) Lajstromszám: E 006 37 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 708911 (22) A bejelentés napja:
!HU00000637T2! (19) HU (11) Lajstromszám: E 006 37 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 708911 (22) A bejelentés napja:
Csoportosítsa és jellemezze a veszélyes anyagokat!
 Csoportosítsa és jellemezze a veszélyes anyagokat! Ismertesse a tűzoltó anyagok veszélyes reakcióit veszélyes anyagokkal! A veszélyes anyagok csoportosítása: MIÉRT VAN SZÜKSÉG A VESZÉLYES ANYAGOK CSOPORTOSÍTÁSÁRA???
Csoportosítsa és jellemezze a veszélyes anyagokat! Ismertesse a tűzoltó anyagok veszélyes reakcióit veszélyes anyagokkal! A veszélyes anyagok csoportosítása: MIÉRT VAN SZÜKSÉG A VESZÉLYES ANYAGOK CSOPORTOSÍTÁSÁRA???
8. osztály megoldások
 8. osztály 8. osztály megoldások 1. Melyik kémiai változás az alábbiak közül? (A) a vasúti sín nyáron kiterjed (B) a fa elkorhad (C) az alumíniumlábas átforrósodik (D) a szénakazal kigyullad (E) a must
8. osztály 8. osztály megoldások 1. Melyik kémiai változás az alábbiak közül? (A) a vasúti sín nyáron kiterjed (B) a fa elkorhad (C) az alumíniumlábas átforrósodik (D) a szénakazal kigyullad (E) a must
