SiRNS-technológia, a jövô génterápiája?
|
|
|
- Viktor Juhász
- 8 évvel ezelőtt
- Látták:
Átírás
1 SiRNS-technológia, a jövô génterápiája? RÁCZ ZSUZSANNA és HAMAR PÉTER DR. Semmelweis Egyetem, Általános Orvostudományi Kar, Kórélettani Intézet, Budapest A genetikában új korszak kezdôdött 17 éve, amikor a petúniában felfedezték a koszuppressziót. Késôbb a koszuppressziót azonosították a növényekben és alacsonyabb rendû eukariótákban megfigyelt RNS-interferenciával (RNSi). Bár a növényekben ez ôsi vírusellenes gazdaszervezeti védekezômechanizmus, emlôsökben az RNSi élettani szerepe még nincs teljesen tisztázva. Az RNSi-t rövid kettôs szálú interferáló RNS-ek (short interfering RNA, sirns) irányítják. A jelen cikkben összefoglaljuk az RNSi történetét és mechanizmusát, az sirns-ek szerkezete és hatékonysága közötti összefüggéseket, a célsejtbe való bejuttatás virális és nem virális módjait. Az sirns-ek klinikai alkalmazásának legfontosabb akadálya az in vivo alkalmazás. Bár a hidrodinamikus kezelés állatokban hatékony, embereknél nem alkalmazható. Lehetôséget jelent viszont a szervspecifikus katéterezés. A szintetizált sirns-ek ismert mellékhatásait szintén tárgyaljuk. Bár a génterápia ezen új területén számos problémával kell szembenézni, a sikeres in vitro és in vivo kísérletek reményt jelentenek emberi betegségek sirns-sel történô kezelésére. Kulcsszavak: RNS-interferencia (RNSi), rövid interferáló RNS (sirns), bevitel, humán génterápia SiRNA technology, the gene therapy of the future? A new era in genetics started 17 years ago, when co-suppression in petunia was discovered. Later, co-suppression was identified as RNA interference (RNAi) in many plant and lower eukaryote animals. Although an ancient antiviral host defense mechanism in plants, the physiologic role of RNAi in mammals is still not completely understood. RNAi is directed by short interfering RNAs (sirnas), one subtype of short double stranded RNAs. In this review we summarize the history and mechanisms of RNAi. We also aim to highlight the correlation between structure and efficacy of sirnas. Delivery is the most important obstacle for sirna based gene therapy. Viral and nonviral deliveries are discussed. In vivo delivery is the next obstacle to clinical trials with sirnas. Although hydrodynamic treatment is effective in animals, it cannot be used in human therapy. One possibility is organ selective catheterization. The known side effects of synthesized sirnas are also discussed. Although there are many problems to face in this new field of gene therapy, successful in vitro and in vivo experiments raise hope for treating human disease with sirna. Keywords: RNA interference (RNAi), short interfering RNA (sirna), delivery, human gene therapy (Beérkezett: november 21.; elfogadva: november 26.) A génterápia lehetôsége a jelenlegi legérdekesebb témák egyike. A DNS kettôs spirálszerkezet felfedezésének ötvenedik évfordulóján Watson kijelentette a Time magazinnak, hogy ötven éve a legérdekfeszítôbb projekt a genetikai anyag szerkezetének a feltárása volt [1]. Ezzel kezdôdôen a génterápia a tudományos-fantasztikus irodalomból a klinikai kezelések realisztikusan választható lehetôségévé lépett elô. Bár az elsô klinikai kipróbálásokat súlyos, nem kívánt események miatt betiltották: tízbôl két páciensnél T-sejtes leukémia fejlôdött ki X-kapcsolt súlyos kombinált immunhiány (X-linked severe combined immune deficiency, X-SCID) kezelésére irányuló retrovírus alapú génterápiát követôen [1]. Ennek ellenére az amerikai Élelmiszer- és Gyógyszer-engedélyezési Hivatal (Food and Drug Administration) több mint 169, különbözô fázisokban lévô génterápiás klinikai kipróbálást tart nyilván [2]. Az RNS-interferencia (RNSi), amelyet rövid interferáló RNS-k (sirns-ek) segítségével végzünk, a génterápia legígéretesebb területeinek egyikévé vált. Az sirns-ek alkalmazásának lehetôségei a fertôzô és autoimmun betegségektôl a rosszindulatú daganatokig és genetikai rendellenességekig terjedhetnek [3]. DOI: /OH n 153 n 2008 n 149. évfolyam, 4. szám n
2 Az RNS-interferenciával elért géncsendesítés története és élettani szerepe Az RNS-interferencia (RNSi) a géncsendesítés egy típusa, amit elôször növényekben [4] és gerinctelenekben [5] figyeltek meg. Növényekben az RNSi megvédi a génállományt a vírusoktól és a transzpozonoktól, de az emlôssejtekben betöltött szerepét még nem ismerjük teljesen. Az RNS-interferenciát elôször a petúniában írták le [6]. Jorgensen és munkatársai kimutatták, hogy a kívülrôl bejuttatott molekulák képesek a gazdaszervezet génjeinek expresszióját módosítani. Ezt a folyamatot koszuppressziónak nevezték el. Késôbb Mello és munkatársai antiszensz RNS-eket (asrns-eket) alkalmaztak a Caenorhabditis elegans hengeresféregben. Ez volt a géncsendesítés elsô állatmodellje [7]. Megfigyelték, hogy ha a C. elegansba hosszú kettôs szálú RNS-eket (double stranded RNA, dsrns) juttattak be, az a homológ hírvivô (messenger) RNS (mrns) célzott degradációját okozta. Továbbá a dsrns szensz és antiszensz RNS-szálainak egyszerre történô beadása akár tízszer hatékonyabb csendesítést eredményezett, mint egy szál egyedüli használata. Ezt az eljárást poszttranszkripciós géncsendesítésnek (post-transcriptional gene silencing, PTGS) nevezték el. Feltételezték még, hogy a PTGS a növényekben, gombákban és Drosophilában megfigyelt koszuppresszió rokona [8]. Bár az RNSi alacsonyabb rendû eukariótákban történô felfedezése nem váltott ki számottevô érdeklôdést, az orvosbiológiai kutatás figyelme egy csapásra az RNSi-re irányult, amikor felfedezték emlôssejtekben való elôfordulását. Tuschl és munkatársai kimutatták, hogy az RNSi emlôseredetû tenyésztett sejtekben sirnsekkel kiváltható [9]. Mostanáig az sirns-eket már sikeresen alkalmazták géncsendesítésre számos állatmodellben, mint például nematoda- [10], Drosophila- [11], hidra- [12], zebradánió- [13], egér- [14, 15] és patkánymodellekben [16]. Az RNS-interferencia in vivo funkciója a gazdaszervezet védelme vírusoktól és idegen génektôl, mivel a vírusok életciklusa során gyakran keletkeznek dsrns-ek [17]. Az idegen RNS-szekvenciák felismerése és hasítása a vírusos fertôzés gátlását eredményezi. Bár az RNSi a növényekben ôsi vírusellenes védelem, még nem tisztázott, hogy az ilyen típusú PTGS-mechanizmusnak van-e szerepe az emlôssejtek természetes vírusellenes védelmében vagy a génszabályozás más folyamataiban. Az RNSi biokémiai mechanizmusa A hosszú dsrns-eket a ribonukleázok Rnáz-III családjába tartozó Dicer alakítja át sirns-é. Az sirns-eknek van egy szabad 5 -foszfát végük, amit 19 bázispár (bp) hosszú kettôs szálú RNS követ, a 3 végen két párosítatlan nukleotidból álló túlnyúló résszel [18]. A felismert sirns-ek beépülnek az RNS indukálta csendesítô (RNA induced silencing complex, RISC) több alegységbôl álló ribonukleoprotein-komplexbe. A RISC-ben az sirns-ek széttekerednek, szensz és antiszensz szálakra bomlanak. Az antiszensz szál irányítja a célmrns felismerését és hasítását. Az aktivált RISC tartalmazza az antiszensz RNS-szálat, továbbá egy fehérjét, amely homológ a növényi Argonaute géncsalád termékével (fehérjetermékek, amelyek az RNSi-ben részt vevô RNS-kötô fehérjék), továbbá más, nem jellemzett faktorokat is tartalmaz, amelyek közé tartozik egy, a cél-rns hasításáért felelôs endonukleáz. Az mrns elhasítása következtében a transzkripció és transzláció teljes folyamata megszakad. Más szóval, a fehérjeszintézis a genom intaktsága mellett gátlódik (1. ábra). Az RNSi élettartama Az RNSi-vel végzett csendesítés nem teljes, ami azt jelenti, hogy az eredmény a génexpresszió visszaszorítása (knockdown) és nem a kiiktatása (knockout). Gyorsan osztódó sejtekben az sirns transzfekciójának a transzfekció után 2 3 napig van maximális hatása, a csendesítô hatás maximum egy hétig tart. A hatékony csendesítés elvesztése feltételezhetôen a sejtosztódásokkal bekövetkezô sirns-hígulásnak tudható be. A végállapotú differenciált sejtekben, mint például a makrofágokban, az in vivo RNSi-hatások több napig tartanak egyetlen dózis beadása után [19]. ITR Csomagolási jel E1 régió* Vírusgének (kapszid fehérjék, replikáció enzimei) E3 régió* ITR = invertált terminális ismétlôdés, * = kivágható és/vagy beilleszthetô régió E4 régió* ITR 1. ábra Adenovírus-vektorok szerkezete 2008 n 149. évfolyam, 4. szám n 154 n O R V O S I H E T I L A P
3 Bejuttatási stratégiák Az RNSi-t alkalmazó terápia számára a bejuttatás még komoly akadályt jelent, mivel az emlôssejtek sejtmembránja az sirns-ek számára nem átjárható, és a legtöbb in vitro kísérletben alkalmazott transzfekciós módszer nem alkalmazható in vivo. Továbbá a gyors vesekiválasztás miatt az sirnsek in vivo felezési ideje nagyon rövid (a másodpercek/percek tartományba esik). A szintetikus sirns-ek bejuttatására megoldás lehet az sirns-prekurzorok expressziója vírusvektorokból, esetleg a komplexálás, vagy összekapcsolás hordozó lipidekkel vagy fehérjékkel (2. ábra). Az sirns-ek egyszerû peptidekhez kapcsolásáról kimutatták, hogy felerôsíti az sirns-ek sejtmembránon keresztüli transzportját [20]. A sejtspecifikus bejuttatás, amely során az sirns-eket sejtfelszíni receptorligandokhoz vagy antitestekhez kapcsoljuk, lecsökkenthetné a potenciális toxicitást mind a virális, mind a nem virális eredetû vektorrendszerekben. Számos vírusalapú és nem vírusalapú expressziós rendszer teszi lehetôvé az sirns-ek sejtekbe juttatását, mint például adenovírus, adenoasszociált vírus, onkoretrovírus, lentivírusvektorok, liposzómák, nanorészecskék vagy peptid-lipid transzfekciós eljárások. Vírusalapú bejuttatási stratégiák Az újabb vírusalapú RNSi-vel végzett génterápiás kísérletekben többfajta vírusvektort alkalmaztak, a leggyakoribbakat (adenovírus-, adenoasszociált vírus-, retrovírus- és lentivírusvektorokat) ebben a fejezetben tekintjük át. Az adenovírus-vektorokat (AdV-k) gyakran alkalmazzák génterápiás kísérletekben, sôt klinikai kísérletekben is. Az AdV-knek számos elônye van: egyszerû nagy titerben elôállítani, viszonylag nagy méretû transzgént képesek a célsejtbe juttatni (az AdV-k képesek több mint 30 kb méretû transzgénnel in vivo transzdukálni sejteket), széles a sejttropizmusuk, nem épülnek be a gazdasejt genomjába, a géntranszfer nagy hatásfokú, az AdV-knek emberekben alacsony a patogenitása [21]. Szisztémás beadást követôen az adenovírusok perceken belül felhalmozódnak a májban a szinuszoidális fenesztrációknak köszönhetôen. Az AdV-k alkalmazásának fô hátránya a transzgénexpresszió rövidsége (néhány naptól pár hétig tart) és a vektorok által expresszált vírusfehérjék okozta gyulladásos reakció. Ezek a vírusfehérjék röviddel a beadás után stimulálják a veleszületett immunrendszert. Továbbá a beadás után 2 7 nappal a vektor által kódolt MHC-prezentált fehérjék beindítják a szerzett immunválaszt, általában azt követôen, hogy a gazdasejtek antitesteket termeltek a vírus kapszid antigénjei ellen [22]. Elôállíthatók olyan rekombináns adenovírus-vektorok, amelyeknél a vírusgéneket az E1-, E2- és E3-régiókban vagy az E4-régió és a vírusgenom vége közötti részben terápiás célú szekvenciákkal helyettesítik. Sejtmag Transzkripció mrns DNS Fehérjeszintézis Aktív RISC Célszekvencia mrns-lebomlás Citoplazma 2. ábra A csendesítô mechanizmus: RNSi szintén inicializálható kémiailag szintetizált sirns-ek sejtekbe juttatásával. Ezek a molekulák bázispár méretû RNS-ek, amelyek a célszekvenciával homológok Az egyik leggyakrabban alkalmazott adenovírus-vektor az 5. típusú adenovírus (Ad5). Az Ad5-bôl származik az adenovírus-vektorok elsô és második generációja és az úgynevezett nagy kapacitású vagy kibelezett vektorok. Az elsô generációs vektorokból kivágták az E1-régiót, a második generációs vektorokból az E1- mellett az E2- és/vagy az E4-régiókat is. Az elsô generációs vektoroknak lehet további deletiója az E3-régióban, amely régió a vírusreplikációért felel. A nagy kapacitású (high capacity, HC) vagy kibelezett (gutted) Ad-vektorokból hiányzik az összes kódoló vírusgén, csak az invertált terminális ismétlôdéseket (inverted terminal repeats, ITR-ek) és a csomagolási jelet (packaging signal) tartalmazzák, amirôl kimutatták, hogy in vivo csökkenti a toxicitást és az immunogenitást [23]. A replikációkompetens (replication-competent, RC) Ad-vektorok az E1A- és E1Brégiókban tartalmaznak deletiókat is, amelyek fehérjetermékei (E1A, E1B) normális esetben megkötik és inaktiválják a Retinoblastoma-proteint (Rb) és a p53-at, így aktiválva a sejtciklust. Tehát az RC-Ad-vektorokat alkalmazhatjuk p53- vagy Rb-negatív tumorokban [24]. Adenoasszociált vírus vektorok. A Dependovirus nemzetség tagjai, az adenoasszociált vírusok (AAV) számára a replikációhoz szükséges egy ún. segítô vírus, mint például adenovírus. Miután a gazdasejt sejtmagjába bekerül, az AAV-nak kétfajta életciklusa lehet: a litikus és a lizogén útvonal. Az elsô a segítô vírussal fertôzött sejtekben fejlôdik ki, míg a lizogén útvonal esetében nincs szükség a segítô vírusra, és az AAV-genom beépül a 19. kromoszóma hosszú karjára és ott marad látens alakban [25]. A gazdaszervezet genomjába történô beépülése miatt az AAV-vektorokból származó transzgénexpresszió akár 18 hónap hosszan is tarthat (lásd késôbb). Az expresszió ezen hosszú élettartama kihasználható RNSi-ben, ha hosszú távú expresszió szükséges. O R V O S I H E T I L A P n 155 n 2008 n 149. évfolyam, 4. szám
4 AAV-vektorok birtokolják mind az adenovírus-, mind a retrovírusvektorok elônyeit, amelyek a következôk: gének átvitele különbözô sejttípusokba, még osztódó és nem osztódó sejtekbe is, széles gazdaválaszték, alacsony szintû immunválasz, génexpresszió megnyúlt élettartama (akár 18 hónappal az raav injektálása után). A retrovírusvektorral létrehozott géntranszfer vonzó az orvosbiológiai kutatás számára, mivel a retrovírusoknak számos elônyük van a többi vírussal szemben. A retrovírus virion körülbelül nm átmérôjû, a gazdasejt plazmamembránjából származó lipid-kettôsrétegbe burkolva. A retrovírusok egyik legfontosabb elônye az, hogy képesek a saját egyszálú RNS-genomjukat a gazdasejt genomjába transzformálni. Ez a stabil integráció a célsejt genomjába akár 8 9 kb idegen DNS tartós bevitelét teszi lehetôvé. A retrovírusvektorok használhatók még rövidhajtû-rns (short hairpin RNA, shrns) bejuttatására RNS-polimeráz- III- (Pol-III-) promóter, mint például U6 vagy H1 (lásd alább) szabályozása alatt. A replikációra képtelen retrovírusokból hiányzik az összes vírusgén, a vírus elôállításához szükségük van csomagoló sejtvonalra vagy segítô vírusra (helper virus). A hibás replikációjú retrovírusvektorok nagy elônye a transzgén nagyobb mérete és az enyhébb immunválasz. A retrovírust alkalmazó génterápiás kísérletek egyik fô hátránya a transzgén beillesztése során potenciálisan fellépô mutagenezis. Egy retrovírusgenom aktívan átíródó génekbe és/vagy protoonkogénekbe integrálása rosszindulatú daganatokhoz vezethet, mint például az X-kromoszómához kötött súlyos kombinált immunhiányosság kifejlôdése (X-linked severe combined immune deficiency, X-SCID) retrovírust alkalmazó génterápiás kezelés után tíz páciensbôl kettônél [26]. A retrovírusok azon képessége, hogy visszaalakulhatnak replikációra képes retrovírusokká (replication-competent retrovirus, RCR), azt jelenti, hogy a gazdasejt genomjába történô véletlenszerû retrovírus-integráció következtében lehetôvé válik a daganatok elôfordulása és az onkogénaktiválódás (insertiós mutagenezis). A hatékony fertôzéshez számos vírusfajtánál szükséges a sejtosztódás, így a nem osztódó sejteket általában nehéz transzdukálni. A retrovírusok egyik alosztálya, a Lentivírusok családja képes megfertôzni nem osztódó sejteket, és képes a transzgének hosszú távú expresszióját fenntartani. A tudomány jelenlegi állása szerint már sikeresen transzfektáltak lentivírusvektorokkal számos sejttípust. Népszerûvé teszi a lentivírusvektorokat a génterápiás kísérletekben az a képességük, hogy a gazda genomjába stabilan integrálódnak. Az adenovírus-transzgénexpresszió 6 hetével szemben a lentivírus-expresszió akár 6 hónap is lehet. A vírusvektorok segítségével végzett génterápiát összefoglalva, a fentebb említett összes vírusvektort már alkalmazták RNSi-re. Mindegyik kísérlet fô része a megfelelô vektorrendszer kiválasztása volt. A szövetspecifikus promóterek és a célsejtek felszínén található specifikus receptorok ellen irányított vírusantigének széles skálája következtében szinte minden sejttípust transzdukálhatunk vírusvektorokkal. Továbbá a vírusvektorokat egyszerû elôállítani és alkalmazni. Ha stabil transzgénexpresszióra van szükségünk, retrovírus- és AAV-vektor-rendszereket kell alkalmaznunk. Az összes többi vektorból származó expresszió csak átmeneti. A vírusvektorok egyik fô hátránya a gazdaszervezet immunválasza és a vírust semlegesítô antitestek termelôdése röviddel a vírusvektor elsô beadása után, ami megakadályozza a virális vektor azonos szerotípusának ismételt alkalmazását. Ennek a problémának a megoldásában segíthet a vírusantigének változtatása. A gazdatropizmus szélesítésére vagy szûkítésére alkalmazhatjuk a pszeudotipizálást és a vírus burkának módosítását. Nem vírusalapú bejuttatási stratégiák Amint az feljebb látható, a vírusvektorok számos esetben nem alkalmazhatók. Ilyenkor meg kell fontolni a nem vírusos bejuttatási módszereket. Számos stratégia létezik hatékony nem vírusos bejuttatás elérésére mind in vitro, mind in vivo. Az sirns-ek in vivo bejuttatásából származó gyógyászati elônyt egereken már igazolták. Szintetikus sirns-ek in vivo sejtbe juttathatók módosított hidrodinamikus transzfekciós eljárással, egy nagynyomású injektáló módszerrel, amelyet eredetileg antiszensz oligonukleotidok és plazmid- DNS bejuttatására dolgoztak ki. Rágcsálóknál a hidrodinamikus kezelésre a farok vagy a hímvesszô vénáit alkalmazhatjuk. Amikor az sirns-eket gyorsan (másodpercek alatt), nagy térfogatban (az állat keringô vértérfogatának %-át) intravénásan injektáljuk, a folyadék feltorlódik a vena cava vénás rendszerében, és olyan magas vénás és kapilláris nyomást hoz létre, amely átpréseli az sirns-eket a bô vérellátású parenchimás szervek (máj, vese, stb.) endothel rétegén [19]. Korábbi kísérletekben hidrodinamikus kezelést követôen egerek májában a hepatocyták körülbelül 90%- a felvette az sirns-t, ami a Fas-apoptózis-receptor expresszióját 80 90%-ban gátolta [15]. Bár egerekben hatékony, a hidrodinamikus kezelés nem alkalmazható humán klinikumban. Esetleg megfelelô alternatíva lehet az sirns helyi bejuttatása szövetekbe kisebb térfogatú injekcióval vagy helyi (szervspecifikus) vénák katéterezésével. Már számos kísérletben bizonyították, hogy az sirns-ek bejuttathatók a központi idegrendszerbe [27], a szubretinális térbe [28] és a peritonealis üregbe [29], ahol ki is fejtik hatásukat. Az sirns-ek sejtekbe történô bejuttatását megvalósíthatjuk rövidhajtû-rns-eket (short hairpin RNS, shrns) expresszáló plazmidokkal is. A sejtek sikeres transzfekció után elkezdik termelni a kódolt shrns-t. Az shrns-ek rövid, speciális szerkezetû RNS-ek: szensz szál hajtûkanyar (5 9 bp) komplementer antiszensz szál. Az shrns szintézisét követôen a hajtût a termelô sejtben található Dicer hasítja, az eredmény sirns (3. ábra). Mivel ez a folyamat a sejtek belsejében történik, és az shrns-rendszerek (shrnst kódoló plazmidok) jóval stabilabbak biológiai folyadékok n 149. évfolyam, 4. szám n 156 n O R V O S I H E T I L A P
5 Vírus Plazmid (shrns) Citoplazma Virális vektor ssrna Dicer RNS dependens RNS polimeráz ATP dsrna Liposzóma sirns 3. ábra Külsô és belsô útvonalak, amelyeken gátló sirns kerülhet a sejtbe [a jobb oldali nyilak: RNSi élettani szerepe, szaggatott nyilak (balra): az sirns közvetlen bejuttatása a sejtekbe gyógyászati céllal] ban, mint az sirns-ek [30], a csendesítési hatékonyság felerôsödik. Bizonyos szövetekben vagy sejttípusokban úgy érhetjük el az shrns-k expresszióját, hogy az shrns-eket szövetspecifikus vagy indukálható promóterrel rendelkezô plazmidokban expresszáljuk. Az sirns-sel végzett géncsendesítés lehetséges mellékhatásai Az sirns-ek nagy koncentrációban való alkalmazása az interferonrendszer aktiválásához vezethet, vagy elôfordulhat, hogy a célgénen kívül más géneket is elcsendesít (off-target hatás). Interferonválasz A duplex RNS-molekulák a sejtek citoplazmájában mélyreható élettani reakciót válthatnak ki. Egyetlen dsrns-molekula (amely a legtöbb vírusfertôzés esetén kialakul) elég ahhoz, hogy indukálja az interferonok (IFN) szintézisét. Az interferonok többfunkciós citokinek, amelyek a gazdaszervezet immunológiai funkcióit modulálják, és képesek gátolni a tumorsejt-növekedést és a vírusreplikációt. A legtöbb dsrns vagy vírusfertôzés az I. típusú IFN-okat indukálja, ezek az IFN-α és az IFN-β. A citoplazmában található dsrns aktiválja a dsrns aktiválta fehérje-kináz-r-t (protein kinase-r, PKR). A dsrns PKR-hez kötôdése a PKR autofoszforilációjához vezet. Az aktiválást követôen két reakcióút ismert a PKR-tôl kiindulva. Az elsô reakcióút során az aktivált PKR aktiválja a nukleáris (transzkripciós) faktor (NF)-κB-t az IκB-regulátor-fehérje foszforilálásával. Az aktivált NF-κB transzlokálódik a sejtmagba, és aktiválja a promóter régióikban NF-κB-kötôhellyel rendelkezô gének transzkripcióját [31], ezek közül is leggyakrabban az IFN-β génjét. Az aktivált PKR-tôl ismert másik reakcióút a transzlációs elongációt iniciáló faktor-α alegységének (EIFα) a foszforilációja. Az EIFα foszforilációjának hatására gátlódik a transzláció és ezzel a sejt teljes (nem specifikus) fehérjeszintézise. A vírusellenes válasz részeként a dsrns-ek aktiválják a 2,5 - oligoadenilát-szintetázt (2,5 -oligoadenylate synthetase, OAS), ami az ATP hosszú oligoadenilát-láncokká történô feldarabolása révén aktiválja a ribonukleáz-l-t (RNázL). Az aktív RNázL lebontja a nem specifikus celluláris RNS-eket, így felfüggeszti a vírusfertôzést. Az IFN-válasz kiváltásának PKR-független útján a dsrns közvetlenül is aktiválhatja az IFN-ek expresszióját. A szintézist követôen a sejt környezetébe bocsájtja az IFN-eket (parakrin hatás). A kiválasztott IFN-ek a környezô sejtekben indukálják az IFN-stimulált géneket (ISG-k) [32]. Az sirns-kísérletek elsô éveiben azt gondolták, hogy az sirns-ek túl kicsik ahhoz, hogy interferonválaszt indukáljanak. Sledz és munkatársai felfedezték, hogy a különbözô célgének ellen tervezett sirns-ek interferonválaszt aktiváltak in vitro [33]. Fish és munkatársai megfigyelték, hogy 21 nt hosszúságú shrns-szekvenciákat expresszáló lentivírusvektorokkal fertôzött sejtekben az OAS1-gén indukálódott [34]. Ugyanakkor, saját kísérleteinkben 2 különbözô sirnst alakalmazva nem találtunk emelkedést az OAS1 expressziójában in vivo. O R V O S I H E T I L A P n 157 n 2008 n 149. évfolyam, 4. szám
6 A célgéneken kívüli csendesítés (off-target silencing) Az sirns és a cél-mrns közötti tökéletes bázispárosítás következtében a csendesítés specifikus. Megfigyelték azonban [35], hogy az sirns-ek magas koncentrációja képes célgéneken kívüli más gének csendesítésére is (off-target silencing). A célponton kívüli csendesítés azt jelenti, hogy az sirns nemkívánatos módon, csak részlegesen komplementer szekvenciákat is gátol. A multiplex endokrin neoplázia 1- (MEN1-) gén ellen célzott tíz sirns-bôl a négy leghatékonyabb közül egy fokozta a p53- és a p21-expressziót, egy másik sirns csökkentette a p21 mennyiségét, míg további kettô nem okozott jelentôs változást a p53- és p21-szintekben az áltranszfektált sejtekhez képest. Az sirns-ek 10 nmre titrálása csökkentette a MEN1-gén csendesítését, de nem szüntette meg a p53-ra és a p21-re gyakorolt nem specifikus hatást [36]. Következésképpen, a célgénen kívüli csendesítés hatását már alacsony koncentrációjú sirns is kiválthatja. A probléma megoldható az sirns-ek gondos tervezésével és/vagy különbözô sirns-szekvenciák tesztelésével, hogy kiválasszuk a legjobb célspecifikus/célon kívüli profillal rendelkezô szekvenciát. Sledz és munkatársai megfigyelték, hogy hosszú, 500 bp méretû dsrns-ek (amelyek megtalálhatók Drosophilában és hengeresféregben) a PKR aktiválásával képesek nem specifikus szuppressziót létrehozni (a nem specifikus szuppresszió PKR-hiányos sejtekben 25%-os volt, a vad fenotípusú sejtek 75%-ával szemben) [33]. Jackson és munkatársai megfigyelték, hogy emlôssejttenyészetben az eredeti sirns-koncentráció ezredére csökkentése sem szüntette meg teljesen a célgénen kívüli csendesítést. Továbbá olyan nem célzott gének csendesítése, amelyek az sirns csak tizenegy folyamatosan illeszkedô nukleotidját tartalmazták, elég volt a célponton kívüli csendesítés kiváltásához [37]. A nem szekvenciaspecifikus (célon kívüli) csendesítés problémájának megoldása a különbözô szekvenciák in vivo (állatmodellekben végzett) tesztelése lehet. Az RNSi gyógyászati alkalmazása A genetikai anyagban elôforduló bármilyen elváltozás a géncsendesítés célpontja lehet. A genetikai elváltozások mellett RNSi-vel szintén kezelhetünk fertôzéseket (mind akut, mind krónikus), neurodegeneratív betegségeket és rosszindulatú daganatokat (lásd késôbb). A fulmináns hepatitis mérsékelése [15], ischaemiareperfusio utáni vesekárosodás [16], gyulladás [29] vagy bakteriális szeptikus sokk [38] szintén gátolható sirns-ekkel. Az RNSi-t alkalmazó terápia segítségével eddig kezelt vírusos fertôzések magukban foglalják a következôket: hepatitis-c vírus [39] indukálta májbetegség, súlyos akut légzési szindróma (severe acute respiratory syndrome, SARS) [40], humánpapillomavírus-fertôzésre (HPV) visszavezethetô tumorgenezis [45], vírusos influenza [41], HIV-1 [42] és számos további vírusfertôzés. Kimutatták, hogy az RNSi számos más intracelluláris patogén ellen is hatékony, például a Mycobacterium [43] és a Trypanosoma [44] ellen. Az RNSi helyi sirns-injektálással alkalmazható a tumornövekedés lassítására [45], az áttétképzôdés, illetve a rák vascularisatiójának gátlására is. Az RNSi-t mind in vitro, mind in vivo sikeresen alkalmazták rosszindulatú daganatok ellen. Az sirns-eket és shrns-eket alkalmazták az agy- [46], mell- [47] és petefészektumorok [48] állatmodelljeiben. Neurodegeneratív betegségek szintén lehetnek az RNSi gyógyászati célpontjai, mivel a mutáns gének csendesítése lassíthatja számos progresszív neurodegeneratív betegség kifejlôdését, mint például az Alzheimer-kórt [49] vagy a Huntington-kórt [50]. Az RNSi-t alkalmazó terápia szerepe óriási mértékben nôtt. Jelenleg a legfontosabb kérdés az sirns-eknek a terápiás hatás helyére való juttatása. Klinikai vizsgálatok várhatóak fertôzô, örökletes, neurodegeneratív és rákos betegségek sirns-ekkel történô kezelésére. Támogatás Kísérleteinket az NIH Research Grant #R03 TW07069 támogatásával végeztük, melyet a Fogarty International Center és a National Institute of Diabetes and Digestive and Kidney Diseases közösen szponzorál. További támogatást az OTKA T049022, NF69278 (HP) pályázatok nyújtottak. Irodalom [1] Milhavet, O., Gary, D. S., Mattson, M. P.: Pharmacol. Rev., RNA Interference in Biology and Medicine. 2003, 55, [2] www. clinicaltrials. gov. ghv. nlm. nih. gov [3] Devroe, E., Silver, P. A.: Therapeutic potential of retroviral RNAi vectors. Expert Opin. Biol. Ther., 2004, 4, [4] Vaucheret H., Beclin C., Fegard M. J.: Post-transcriptional gene silencing in plants. Cell Sci., 2001, 114, [5] Agrawal, N., Malhotra, P., Bhatnagar, R. K.: sirna-directed silencing of transgene expressed in cultured insect cells. Biochem. Biophys. Res. Commun., 2004, 320, [6] Napoli, C., Lemieux, C., Jorgensen, R.: Introduction of a chimeric chalcone synthase gene into petunia results in reversible co-suppression of homologous genes in trans. Plant Cell, 1990, 2, [7] Grishok, A., Mello, C. C.: RNAi (nematodes: Ceanorhabditis elegans). Adv. Genet., 2002, 46, [8] Hammond, S. M., Berstein, E., Beach, D. és mtsa: An RNA-directed nuclease mediates post-transcriptional gene silencing in Drosophila cells. Nature, 2000, 404, [9] Elbashir, S. M., Harboth, J.; Lendeckel, W. és mtsai: Duplexes of 21-nt RNAs mediate RNA interference in cultured mammalian cells. Nature, 2001, 411, [10] Fire, A., Xu, S., Montgomery, M. K. és mtsai: Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature, 1998, 391, [11] Kennerdell, J. R., Carthew, R. W: Use of ds-rna mediated genetic interference to demonstrate that frizzled and frizzled 2 act in the wingless pathway. Cell, 1998, 95, [12] Lohmann, J. U., Endl, I., Bosch, T. C.: Silencing of developmental genes in Hydra. Dev. Biol., 1999, 214, n 149. évfolyam, 4. szám n 158 n O R V O S I H E T I L A P
7 [13] Wargelius, A., Ellingsen, S., Fjose, A.: Double-stranded RNA induces specific developmental defects in zebrafish embryos. Biochem. Biophys. Res. Commun., 1999, 263, [14] Song, E., Lee, S. K., Wang, J. és mtsai: RNA interference targeting Fas protects mice from fulminant hepatitis. Nature Medicine, 2003, 9, [15] Hamar, P., Song, E., Kökény, G. és mtsai: Small interfering RNA targeting Fas protects mice from renal ischemia-reperfusion injury. PNAS, 2004, 101, [16] Gou, D., Narasaraju, T., Reddy, N. és mtsai: Gene silencing in alveolar type II cells using cell-specific promoter in vitro and in vivo. Nucleic Acids Res., 2004, 32, 134. [17] Kumar, M., Carmichael, G. G.: Antisense RNA: function and fate of duplex RNA in higher eukaryotes. MMBR, 1998, 62, [18] Zamore, P. D., Tuschl, T., Sharp, P. és mtsa: RNAi: Doublestranded RNA directs the ATP-dependent cleavage of mrna at 21 to 23 nucleotide intervals. Cell, 2000, 101, [19] McCaffrey, A. P., Meuse, L., Pham, T. T. és mtsai: RNA interference in adult mice. Nature, 2002, 418, [20] Simeoni, F., Morris, M. C., Heutz, F.: Insight into the mechanism of the peptide-based gene delivery system MPG: implications for delivery of sirnas into mammalian cells. Nucleic Acids Res., 2003, 31, [21] Vorburger, S. A., Hunt, K. K.: Adenoviral gene therapy. The Oncologist, 2002, 7, [22] Bessis, N., GarciaCozar, F. J. Boissier, M. C.: Immune responses to gene therapy vectors: influence on vector function and effector mechanisms. Gene Therapy, 2004, 11, [23] Gao, G. P., Yang, Y., Wilson, J. M.: Biology of adenovirus vectors with E1 and E4 deletions for liver-directed gene therapy. J. Virol., 1996, 70, [24] Benrt, K., Liang, M., Ye, X. és mtsai: A new type of adenovirus vector that utilizes homologous recombination to achieve tumor-specific replication. J. Virol., 2002, 76, [25] Samulski, R. J., Zhu, X., Xiao, X. és mtsai: Targeted integration of adeno-associated virus (AAV) into human chromosome 19. The EMBO Journal, 1991, 17, [26] Hacein-Bey-Abina, S., Von Kalle, C., Schmidt, M. és mtsai: LMO2-associated clonal Tcell proliferation in two patients after gene therapy for SCID-X1. Science, 2003, 302, [27] Davidson, B. L., Paulson, H. L.: Molecular medicine for the brain: silencing of deisease genes with RNA interference. Lancet Neurol., 2004, 3, [28] Reich, S. J., Fosnot, J., Kuroki, A. és mtsai: Small interfering RNA (sirna) targeting VEGF efficiently inhibits ocular neovascularization in a mouse model. J. Molecular Vision, 2003, 9, [29] Flynn, M. A., Casey, D. G., Todryk, S. M. és mtsa: Efficient delivery of small interfering RNA for inhibition of IL-12p40 expression in vivo. J. Inflamm. (Lond)., 2004, 1, [30] Paddison, P. J., Caudy, A. A., Bernstein, E. és mtsai: Short hairpin RNAs (shrnas) induce sequence-specific silencing in mammalian cells. Genes Dev., 2002, 16, [31] Bonnet, M. C., Weil, R., Dam, E. és mtsai: PKR stimulates NFκB irrespective of its kinase function by interacting with the IκB kinase complex. Mol. Cell. Biol., 2000, 20, [32] Kumar, M., Carmichael, G. G.: Antisense RNA: function and fate of duplex RNA in higher eukaryotes. Microbiol. Mol. Biol. Rev., 1998, 62, [33] Sledz, C. A., Holko, M., Veer, M. J. és mtsai: Activation of the interferon system by short-interfering RNAs. Nat. Cell. Biol., 2003, 5, [34] Fish, R. J., Kruithof, E. K. O.: Short-term cytotoxic effects and long-term instability of RNAi delivered using lentiviral vectors. BMC Mol. Biol., 2004, 5, [35] Scacheri, P. C., Rozenblatt-Rosen, O., Caplan, N. J. és mtsai: Short interfering RNAs can induce unexpected and divergent changes in the levels of untargeted proteins in mammalian cells. PNAS, 2004, 101, [36] Walters, D. K., Jelinek, D. F.: The Effectiveness of Double- Stranded Short Inhibitory RNAs (sirnas) May Depend on the Method of Transfection. Antisense Nucleic Acid Drug Dev., 2002, 12, [37] Jackson, A. L., Bartz, S. R., Schelter, J. és mtsai: Expression profiling reveals off-target gene regulation by RNAi. Nature Biotechnology, 2003, 21, [38] Reiley, W., Zhang, M., Wu, X. és mtsai: Regulation of the Deubiquitinating Enzyme CYLD by IκB Kinase Gamma- Dependent Phosphorylation. Mol. Cell. Biol., 2005, 25, [39] Kapaida, S. B., Brideau-Andersen, A., Chisari, F. V.: Interference of hepatitis C virus RNA replication by short interfering RNAs Proc. Natl. Acad. Sci. USA, 2003, 100, [40] Wang, Z., Ren, L., Zhao, X. és mtsai: Inhibition of Severe Acute Respiratory Syndrome Virus Replication by Small Interfering RNAs in Mammalian Cells. J. Virol., 2004, 78, [41] Ge, Q., Filip, L., Bai, A. és mtsai: Inhibition of influenza virus production in virus-infected mice by RNA interference. Proc. Natl. Acad. Sci. USA, 2004, 101, [42] Song, E., Lee, S. K., Dykxhoorn, D. M. és mtsai: Sustained Small Interfering RNA-Mediated Human Immunodeficiency Virus Type 1 Inhibition in Primary Macrophages. J. Virol., 2003, 77, [43] Vieira, O. V., Harrison, R. E., Scott, C. C. és mtsai: Acquisition of Hrs, an Essential Component of Phagosomal Maturation, Is Impaired by Mycobacteria. Mol. Cell. Biol., 2004, 24, [44] Liang, X. H., Liu, Q., Michaeli, S.: Small nucleolar RNA interference induced by antisense or double-stranded RNA in trypanosomatids. Proc. Natl. Acad. Sci. USA, 2003, 100, [45] Schiffelers, R. F., Ansari, A., Xu, J. és mtsai: Cancer sirna therapy by tumor selective delivery with ligand-targeted sterically stabilized nanoparticle. Nucleic Acids Res., 2004, 32, [46] Boado, R. J.: RNA Interference and Nonviral Targeted Gene Therapy of Experimental Brain Cancer. NeuroRX, 2005, 2, [47] Onodera, Y., Hashimoto, S., Hashimoto, A. és mtsai: Expression of AMAP1, an ArfGAP, provides novel targets to inhibit breast cancer invasive activities. The EMBO Journal, 2005, 24, [48] Menendez, J. A., Vellon, L., Mehmi, I. és mtsai: Inhibition of fatty acid synthase (FAS) suppresses HER2/neu (erbb-2) oncogene overexpression in cancer cells. PNAS USA, 2004, 101, [49] Miller, V. M., Gouvion, C. M., Davidson, B. L. és mtsa: Targeting Alzheimer s disease genes with RNA interference: an efficient strategy for silencing mutant alleles. Nucleic Acids Res., 2004, 32, [50] Dou, F., Netzer, W. J., Tanemura, K. és mtsai: Chaperones increase association of tau protein with microtubules. Proc. Natl. Acad. Sci. USA, 2003, 100, (Hamar Péter dr., Budapest, Nagyvárad tér 4., hampet@net.sote.hu) O R V O S I H E T I L A P n 159 n 2008 n 149. évfolyam, 4. szám
Hamar Péter. RNS világ. Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. www.meetthescientist.hu 1 26
 Hamar Péter RNS világ Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. 1 26 Főszereplők: DNS -> RNS -> fehérje A kód lefordítása Dezoxy-ribo-Nuklein-Sav: DNS az élet kódja megkettőződés (replikáció)
Hamar Péter RNS világ Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. 1 26 Főszereplők: DNS -> RNS -> fehérje A kód lefordítása Dezoxy-ribo-Nuklein-Sav: DNS az élet kódja megkettőződés (replikáció)
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei)
 Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Az RNS-interferencia és klinikai alkalmazásai
 Az RNS-interferencia és klinikai alkalmazásai MUNKÁCSY GYÖNGYI 1, TULASSAY ZSOLT DR. 2,3 és GYÔRFFY BALÁZS DR. 1 1 MTA-SE Gyermekgyógyászati és Nephrológiai Kutatócsoport, Budapest 2 Semmelweis Egyetem,
Az RNS-interferencia és klinikai alkalmazásai MUNKÁCSY GYÖNGYI 1, TULASSAY ZSOLT DR. 2,3 és GYÔRFFY BALÁZS DR. 1 1 MTA-SE Gyermekgyógyászati és Nephrológiai Kutatócsoport, Budapest 2 Semmelweis Egyetem,
TÉMAKÖRÖK. Ősi RNS világ BEVEZETÉS. RNS-ek tradicionális szerepben
 esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk.
 A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A preventív vakcináció lényege :
 Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Vese génterápia (RNSi) és lupus nephritis IVIG kezelésének mellékhatás-vizsgálata egérmodellen
 Vese génterápia (RNSi) és lupus nephritis IVIG kezelésének mellékhatás-vizsgálata egérmodellen Doktori értekezés Dr. Rácz Zsuzsanna Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Témavezető:
Vese génterápia (RNSi) és lupus nephritis IVIG kezelésének mellékhatás-vizsgálata egérmodellen Doktori értekezés Dr. Rácz Zsuzsanna Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Témavezető:
Elcsendesített RNS-ek vagy a genom immunrendszere
 BIOTECHNOLÓGIAI FEJLESZTÉSI OLITIKA, KUTATÁSI IRÁNYOK Elcsendesített RNS-ek vagy a genom immunrendszere Tárgyszavak: genom; védelem; immunrendszer; RNS-csendesítés. A génkészlet fokozatos változása vírusok
BIOTECHNOLÓGIAI FEJLESZTÉSI OLITIKA, KUTATÁSI IRÁNYOK Elcsendesített RNS-ek vagy a genom immunrendszere Tárgyszavak: genom; védelem; immunrendszer; RNS-csendesítés. A génkészlet fokozatos változása vírusok
RNS-ek. 1. Az ősi RNS Világ: - az élet hajnalán. 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek
 RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
A növényi génexpresszió RNS-szintű minőségbiztosítási rendszereinek molekuláris biológiája. Silhavy Dániel
 A növényi génexpresszió RNS-szintű minőségbiztosítási rendszereinek molekuláris biológiája Silhavy Dániel MTA Doktori Pályázat Doktori ÉrtekezésTézisei Mezőgazdasági Biotechnológiai Kutatóközpont Gödöllő,
A növényi génexpresszió RNS-szintű minőségbiztosítási rendszereinek molekuláris biológiája Silhavy Dániel MTA Doktori Pályázat Doktori ÉrtekezésTézisei Mezőgazdasági Biotechnológiai Kutatóközpont Gödöllő,
Molekuláris terápiák
 Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Fehérje expressziós rendszerek. Gyógyszerészi Biotechnológia
 Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
A vírus gazda kapcsolatban fontos szerepet játszó az RNS silencing generálta kis RNS-ek meghatározása, jellemzése
 A PÁLYÁZAT EREDMÉNYEINEK BEMUTATÁSA. A vírus gazda kapcsolatban fontos szerepet játszó az RNS silencing generálta kis RNS-ek meghatározása, jellemzése Az RNS silencing egy géninaktivációs mechanizmus,
A PÁLYÁZAT EREDMÉNYEINEK BEMUTATÁSA. A vírus gazda kapcsolatban fontos szerepet játszó az RNS silencing generálta kis RNS-ek meghatározása, jellemzése Az RNS silencing egy géninaktivációs mechanizmus,
Klónozás: tökéletesen egyforma szervezetek csoportjának előállítása, vagyis több genetikailag azonos egyed létrehozása.
 Növények klónozása Klónozás Klónozás: tökéletesen egyforma szervezetek csoportjának előállítása, vagyis több genetikailag azonos egyed létrehozása. Görög szó: klon, jelentése: gally, hajtás, vessző. Ami
Növények klónozása Klónozás Klónozás: tökéletesen egyforma szervezetek csoportjának előállítása, vagyis több genetikailag azonos egyed létrehozása. Görög szó: klon, jelentése: gally, hajtás, vessző. Ami
17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására
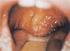 11. 2016. nov 30. 17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására 17.3. ábra A sejtközötti térben és a sejten belül élő és szaporodó kórokozók ellen kialakuló védekezési mechanizmusok
11. 2016. nov 30. 17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására 17.3. ábra A sejtközötti térben és a sejten belül élő és szaporodó kórokozók ellen kialakuló védekezési mechanizmusok
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése
 Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
eljárásokkal Doktori tézisek Szatmári Tünde Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Sugárterápia Program
 Agydaganatok sugárterápia iránti érzékenységének növelése génterápiás eljárásokkal Doktori tézisek Szatmári Tünde Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Sugárterápia Program Doktori
Agydaganatok sugárterápia iránti érzékenységének növelése génterápiás eljárásokkal Doktori tézisek Szatmári Tünde Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Sugárterápia Program Doktori
A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban
 BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
Vírusellenes szerek. Készítette hidasi Nóra: Gruiz Katalin Környezeti mikrobiológia és biotechnológia c. előadásához
 Vírusellenes szerek Készítette hidasi Nóra: Gruiz Katalin Környezeti mikrobiológia és biotechnológia c. előadásához Vírusok Sejtes szerveződés nélküli szubmikroszkópikus obligát sejtparaziták. Örökítő
Vírusellenes szerek Készítette hidasi Nóra: Gruiz Katalin Környezeti mikrobiológia és biotechnológia c. előadásához Vírusok Sejtes szerveződés nélküli szubmikroszkópikus obligát sejtparaziták. Örökítő
Immunológia alapjai előadás MHC. szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
A biológia szerepe az egészségvédelemben
 A biológia szerepe az egészségvédelemben Nagy Kinga nagy.kinga@mail.bme.hu 2017.10.24 Mikróbák az ember szolgálatában (Néhány példán keresztül bemutatva) Antibiotikumok (gombák, baktériumok) Restrikciós
A biológia szerepe az egészségvédelemben Nagy Kinga nagy.kinga@mail.bme.hu 2017.10.24 Mikróbák az ember szolgálatában (Néhány példán keresztül bemutatva) Antibiotikumok (gombák, baktériumok) Restrikciós
Rekombináns Géntechnológia
 Rekombináns Géntechnológia Tartalom: 1 1. Biotechnológia, géntechnológia, társadalom 2. Genetikai rekombináció 3. Génbevitel tenyésztett sejtekbe 4. Genetikailag módosított szervezetek (GMO-k) 4a. Transzgénikus
Rekombináns Géntechnológia Tartalom: 1 1. Biotechnológia, géntechnológia, társadalom 2. Genetikai rekombináció 3. Génbevitel tenyésztett sejtekbe 4. Genetikailag módosított szervezetek (GMO-k) 4a. Transzgénikus
Zárójelentés T ( )
 Zárójelentés T 48852 (2005-2008) Összefoglaló A Cymbidium ringspot vírussal fertőzött növényekből származó kis RNS-ek analízise során azt találtuk, hogy a virális kis RNS-ek a genom kitüntetett helyeiről
Zárójelentés T 48852 (2005-2008) Összefoglaló A Cymbidium ringspot vírussal fertőzött növényekből származó kis RNS-ek analízise során azt találtuk, hogy a virális kis RNS-ek a genom kitüntetett helyeiről
HUMAN IMMUNODEFICIENCY VIRUS (HIV) ÉS AIDS
 HUMAN IMMUNODEFICIENCY VIRUS (HIV) ÉS AIDS Dr. Mohamed Mahdi MD. MPH. Department of Infectology and Pediatric Immunology University of Debrecen 2010 Történelmi tények a HIV-ről 1981: Első megjelenés San
HUMAN IMMUNODEFICIENCY VIRUS (HIV) ÉS AIDS Dr. Mohamed Mahdi MD. MPH. Department of Infectology and Pediatric Immunology University of Debrecen 2010 Történelmi tények a HIV-ről 1981: Első megjelenés San
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
INTRACELLULÁRIS PATOGÉNEK
 INTRACELLULÁRIS PATOGÉNEK Bácsi Attila, PhD, DSc etele@med.unideb.hu Debreceni Egyetem, ÁOK Immunológiai Intézet INTRACELLULÁRIS BAKTÉRIUMOK ELLENI IMMUNVÁLASZ Példák intracelluláris baktériumokra Intracelluláris
INTRACELLULÁRIS PATOGÉNEK Bácsi Attila, PhD, DSc etele@med.unideb.hu Debreceni Egyetem, ÁOK Immunológiai Intézet INTRACELLULÁRIS BAKTÉRIUMOK ELLENI IMMUNVÁLASZ Példák intracelluláris baktériumokra Intracelluláris
Vírusok Szerk.: Vizkievicz András
 Vírusok Szerk.: Vizkievicz András A vírusok az élő- és az élettelen világ határán állnak. Önmagukban semmilyen életjelenséget nem mutatnak, nincs anyagcseréjük, önálló szaporodásra képtelenek. Paraziták.
Vírusok Szerk.: Vizkievicz András A vírusok az élő- és az élettelen világ határán állnak. Önmagukban semmilyen életjelenséget nem mutatnak, nincs anyagcseréjük, önálló szaporodásra képtelenek. Paraziták.
VIRÁLIS RNS SILENCING SZUPRESSZOROK MŰKÖDÉSI MECHHANIZMUSAI
 VIRÁLIS RNS SILENCING SZUPRESSZOROK MŰKÖDÉSI MECHHANIZMUSAI DR. LAKATOS LÓRÁNT SZTE ÁOK BŐRGYÓGYÁSZATI ÉS ALLERGOLÓGIAI KILNIKA 2017 Összefoglaló TARTALOMJEGYZÉK...2 BEVEZETÉS...3 CÉLKITŰZÉSEK...6 EREDMÉNYEK
VIRÁLIS RNS SILENCING SZUPRESSZOROK MŰKÖDÉSI MECHHANIZMUSAI DR. LAKATOS LÓRÁNT SZTE ÁOK BŐRGYÓGYÁSZATI ÉS ALLERGOLÓGIAI KILNIKA 2017 Összefoglaló TARTALOMJEGYZÉK...2 BEVEZETÉS...3 CÉLKITŰZÉSEK...6 EREDMÉNYEK
Biológus MSc. Molekuláris biológiai alapismeretek
 Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
13. RNS szintézis és splicing
 13. RNS szintézis és splicing 1 Visszatekintés: Az RNS típusai és szerkezete Hírvivő RNS = mrns (messenger RNA = mrna) : fehérjeszintézis pre-mrns érett mrns (intronok kivágódnak = splicing) Transzfer
13. RNS szintézis és splicing 1 Visszatekintés: Az RNS típusai és szerkezete Hírvivő RNS = mrns (messenger RNA = mrna) : fehérjeszintézis pre-mrns érett mrns (intronok kivágódnak = splicing) Transzfer
Doktori értekezés tézisei
 Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Nan Wang, Qingming Dong, Jingjing Li, Rohit K. Jangra, Meiyun Fan, Allan R. Brasier, Stanley M. Lemon, Lawrence M. Pfeffer, Kui Li
 Supplemental Material IRF3-dependent and NF- B-independent viral induction of the zinc-finger antiviral protein Nan Wang, Qingming Dong, Jingjing Li, Rohit K. Jangra, Meiyun Fan, Allan R. Brasier, Stanley
Supplemental Material IRF3-dependent and NF- B-independent viral induction of the zinc-finger antiviral protein Nan Wang, Qingming Dong, Jingjing Li, Rohit K. Jangra, Meiyun Fan, Allan R. Brasier, Stanley
Allergia immunológiája 2012.
 Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
OTKA ZÁRÓJELENTÉS
 NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
Lele Zsolt. MTA Kísérleti Orvostudományi Kutatóintézet
 A hal mint modellállat a kutatásban Lele Zsolt MTA Kísérleti Orvostudományi Kutatóintézet A hal mint modellállat a kutatásban Halfajták A hal mint modellállat a kutatásban Halfajták Gazdaságilag jelentıs
A hal mint modellállat a kutatásban Lele Zsolt MTA Kísérleti Orvostudományi Kutatóintézet A hal mint modellállat a kutatásban Halfajták A hal mint modellállat a kutatásban Halfajták Gazdaságilag jelentıs
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
RNS-ek. 1. Az ősi RNS Világ: - az élet hajnalán. 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek
 RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció 5.
RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció 5.
Az adenovírusok morfológiája I.
 Adenovírusok A vírusok Elnevezésük a latin virus szóból ered, amelynek jelentése méreg. A vírusok a legkisebb ismert entitások. Csak elektronmikroszkóppal tanulmányozhatóak, mert méretük 20-400 nanométerig
Adenovírusok A vírusok Elnevezésük a latin virus szóból ered, amelynek jelentése méreg. A vírusok a legkisebb ismert entitások. Csak elektronmikroszkóppal tanulmányozhatóak, mert méretük 20-400 nanométerig
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Immunológia I. 4. előadás. Kacskovics Imre
 Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
DOKTORI ÉRTEKEZÉS TÉZISEI AZ OPPORTUNISTA HUMÁNPATOGÉN CANDIDA PARAPSILOSIS ÉLESZTŐGOMBA ELLENI TERMÉSZETES ÉS ADAPTÍV IMMUNVÁLASZ VIZSGÁLATA
 DOKTORI ÉRTEKEZÉS TÉZISEI AZ OPPORTUNISTA HUMÁNPATOGÉN CANDIDA PARAPSILOSIS ÉLESZTŐGOMBA ELLENI TERMÉSZETES ÉS ADAPTÍV IMMUNVÁLASZ VIZSGÁLATA TÓTH ADÉL TÉMAVEZETŐ: DR. GÁCSER ATTILA TUDOMÁNYOS FŐMUNKATÁRS
DOKTORI ÉRTEKEZÉS TÉZISEI AZ OPPORTUNISTA HUMÁNPATOGÉN CANDIDA PARAPSILOSIS ÉLESZTŐGOMBA ELLENI TERMÉSZETES ÉS ADAPTÍV IMMUNVÁLASZ VIZSGÁLATA TÓTH ADÉL TÉMAVEZETŐ: DR. GÁCSER ATTILA TUDOMÁNYOS FŐMUNKATÁRS
Vírusok szerkezete, osztályozása, általános tulajdonságai és szaporodása
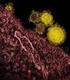 Vírusok szerkezete, osztályozása, általános tulajdonságai és szaporodása Történeti áttekintés Ramses kr.e. 1100 bőrlaesiok a múmián himlő Kanyaró és himlő pontos leírása: Rhazes kr.u. 900 Egyiptomi múmia
Vírusok szerkezete, osztályozása, általános tulajdonságai és szaporodása Történeti áttekintés Ramses kr.e. 1100 bőrlaesiok a múmián himlő Kanyaró és himlő pontos leírása: Rhazes kr.u. 900 Egyiptomi múmia
Orvosi Genomtudomány 2014 Medical Genomics 2014. Április 8 Május 22 8th April 22nd May
 Orvosi Genomtudomány 2014 Medical Genomics 2014 Április 8 Május 22 8th April 22nd May Hét / 1st week (9. kalendariumi het) Takács László / Fehér Zsigmond Magyar kurzus Datum/ido Ápr. 8 Apr. 9 10:00 10:45
Orvosi Genomtudomány 2014 Medical Genomics 2014 Április 8 Május 22 8th April 22nd May Hét / 1st week (9. kalendariumi het) Takács László / Fehér Zsigmond Magyar kurzus Datum/ido Ápr. 8 Apr. 9 10:00 10:45
Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter
 Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter Áttekintés Miért éppen a nyuszik? Védekezés módja Vakcina jellemzői Vakcina működése Ráfertőzési
Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter Áttekintés Miért éppen a nyuszik? Védekezés módja Vakcina jellemzői Vakcina működése Ráfertőzési
B-sejtek szerepe az RA patológiás folyamataiban
 B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
DNS replikáció. DNS RNS Polipeptid Amino terminus. Karboxi terminus. Templát szál
 DNS replikáció DNS RNS Polipeptid Amino terminus Templát szál Karboxi terminus Szuper-csavarodott prokarióta cirkuláris DNS Hisztonok komplexe DNS hisztonokra történő felcsvarodása Hiszton-kötött negatív
DNS replikáció DNS RNS Polipeptid Amino terminus Templát szál Karboxi terminus Szuper-csavarodott prokarióta cirkuláris DNS Hisztonok komplexe DNS hisztonokra történő felcsvarodása Hiszton-kötött negatív
Transzgénikus vírusrezisztencia II. Stratégiák, fajták, előnyök, kockázatok
 BIOTECHNOLÓGIA O I ROVATVEZETŐ: Dr. Heszky László akadémikus Az előző részben bemutattuk a vírusok molekuláris szerkezetét és szaporodásának folyamatait, melyek ismerete alapvetően szükséges volt a géntechnológiai
BIOTECHNOLÓGIA O I ROVATVEZETŐ: Dr. Heszky László akadémikus Az előző részben bemutattuk a vírusok molekuláris szerkezetét és szaporodásának folyamatait, melyek ismerete alapvetően szükséges volt a géntechnológiai
Immunológia alapjai. Az immunválasz szupressziója Előadás. A szupresszióban részt vevő sejtes és molekuláris elemek
 Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
A Telomerase-specific Doxorubicin-releasing Molecular Beacon for Cancer Theranostics
 A Telomerase-specific Doxorubicin-releasing Molecular Beacon for Cancer Theranostics Yi Ma, Zhaohui Wang, Min Zhang, Zhihao Han, Dan Chen, Qiuyun Zhu, Weidong Gao, Zhiyu Qian, and Yueqing Gu Angew. Chem.
A Telomerase-specific Doxorubicin-releasing Molecular Beacon for Cancer Theranostics Yi Ma, Zhaohui Wang, Min Zhang, Zhihao Han, Dan Chen, Qiuyun Zhu, Weidong Gao, Zhiyu Qian, and Yueqing Gu Angew. Chem.
A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata
 Ph.D. ÉRTEKEZÉS TÉZISEI A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata Buzás-Bereczki Orsolya Témavezetők: Dr. Bálint Éva Dr. Boros Imre Miklós Biológia
Ph.D. ÉRTEKEZÉS TÉZISEI A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata Buzás-Bereczki Orsolya Témavezetők: Dr. Bálint Éva Dr. Boros Imre Miklós Biológia
A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban
 A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban Doktori (PhD) értekezés Siklódi Erika Rozália Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna, tanszékvezető egyetemi
A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban Doktori (PhD) értekezés Siklódi Erika Rozália Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna, tanszékvezető egyetemi
Egy emlős mesterséges kromoszóma több génnel történő. feltöltésének új módszere
 Egy emlős mesterséges kromoszóma több génnel történő feltöltésének új módszere Ph. D. értekezés tézisei Tóth Anna Témavezető: Dr. Katona Róbert tudományos főmunkatárs MTA SZBK Genetikai Intézet Biológia
Egy emlős mesterséges kromoszóma több génnel történő feltöltésének új módszere Ph. D. értekezés tézisei Tóth Anna Témavezető: Dr. Katona Róbert tudományos főmunkatárs MTA SZBK Genetikai Intézet Biológia
Mire jó a modellalkotás? Jelenségek megmagyarázásának eszköze.
 Modellalkotás Mire jó a modellalkotás? Jelenségek megmagyarázásának eszköze. ok-okozati összefüggések feltárása összefüggések, mintázatok megmagyarázása "miért?" és "hogyan?" kérdések megválaszolása predikció
Modellalkotás Mire jó a modellalkotás? Jelenségek megmagyarázásának eszköze. ok-okozati összefüggések feltárása összefüggések, mintázatok megmagyarázása "miért?" és "hogyan?" kérdések megválaszolása predikció
3. Kombinált, amelynek van helikális és kubikális szakasza, pl. a bakteriofágok és egyes rákkeltő RNS vírusok.
 Vírusok Szerkesztette: Vizkievicz András A XIX. sz. végén Dmitrij Ivanovszkij orosz biológus a dohány mozaikosodásának kórokozóját próbálta kimutatni. A mozaikosodás a levél foltokban jelentkező sárgulása.
Vírusok Szerkesztette: Vizkievicz András A XIX. sz. végén Dmitrij Ivanovszkij orosz biológus a dohány mozaikosodásának kórokozóját próbálta kimutatni. A mozaikosodás a levél foltokban jelentkező sárgulása.
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
A PET szerepe a gyógyszerfejlesztésben. Berecz Roland DE KK Pszichiátriai Tanszék
 A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
AZ IMMUNRENDSZER VÁLASZAI A HPV FERTŐZÉSSEL KAPCSOLATOS KÉRDÉSEINKRE RAJNAVÖLGYI ÉVA DE OEC Immunológiai Intézet
 AZ IMMUNRENDSZER VÁLASZAI A HPV FERTŐZÉSSEL KAPCSOLATOS KÉRDÉSEINKRE RAJNAVÖLGYI ÉVA DE OEC Immunológiai Intézet A méhnyak rák előfordulása / év / 100 000 nő WHO 2005 A KÓROKOZÓK ÉS AZ IMMUNRENDSZER KÉTIRÁNYÚ
AZ IMMUNRENDSZER VÁLASZAI A HPV FERTŐZÉSSEL KAPCSOLATOS KÉRDÉSEINKRE RAJNAVÖLGYI ÉVA DE OEC Immunológiai Intézet A méhnyak rák előfordulása / év / 100 000 nő WHO 2005 A KÓROKOZÓK ÉS AZ IMMUNRENDSZER KÉTIRÁNYÚ
Az RNS-interferencia és távlatai
 Sipiczki Mátyás Az RNS-interferencia és távlatai Genetika és genom-projektek A modern biológia egyik leggyorsabban és leglátványosabban fejlődő területe a genetika, az a tudomány, amely az öröklődés mechanizmusát
Sipiczki Mátyás Az RNS-interferencia és távlatai Genetika és genom-projektek A modern biológia egyik leggyorsabban és leglátványosabban fejlődő területe a genetika, az a tudomány, amely az öröklődés mechanizmusát
A C1 orf 124/Spartan szerepe a DNS-hiba tolerancia útvonalban
 Ph.D. tézisek A C1 orf 124/Spartan szerepe a DNS-hiba tolerancia útvonalban Írta: Juhász Szilvia Témavezető: Dr. Haracska Lajos Magyar Tudományos Akadémia Szegedi Biológiai Kutatóközpont Genetikai Intézet
Ph.D. tézisek A C1 orf 124/Spartan szerepe a DNS-hiba tolerancia útvonalban Írta: Juhász Szilvia Témavezető: Dr. Haracska Lajos Magyar Tudományos Akadémia Szegedi Biológiai Kutatóközpont Genetikai Intézet
http://www.rimm.dote.hu Tumor immunológia
 http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE
 Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Összefoglalás első fejezete
 Összefoglalás Az utóbbi években a transzkriptómikai vizsgálatokban alkalmazott technológiák fejlődésének köszönhetően a genom kutatás területén jelentős előrehaladás figyelhető meg. A disszertáció első
Összefoglalás Az utóbbi években a transzkriptómikai vizsgálatokban alkalmazott technológiák fejlődésének köszönhetően a genom kutatás területén jelentős előrehaladás figyelhető meg. A disszertáció első
Génátvitel magasabb rendű állatokba elméleti megfontolások, gyakorlati eredmények és génterápiás lehetőségek
 MEZÕGAZDASÁGI BIOTECHNOLÓGIÁK Génátvitel magasabb rendű állatokba elméleti megfontolások, gyakorlati eredmények és génterápiás lehetőségek Tárgyszavak: génátvitel; transzfekció; transzgenézis; génterápia;
MEZÕGAZDASÁGI BIOTECHNOLÓGIÁK Génátvitel magasabb rendű állatokba elméleti megfontolások, gyakorlati eredmények és génterápiás lehetőségek Tárgyszavak: génátvitel; transzfekció; transzgenézis; génterápia;
A szervezet védekezése vírusfertőzésekkel szemben, antivirális kemoterápia, virális vakcinák
 A szervezet védekezése vírusfertőzésekkel szemben, antivirális kemoterápia, virális vakcinák Cytotoxicitás Antitest termelés B sejt Antigen presenting cell (APC) - MHCII B cell receptor Plazmasejt immunoglobulin
A szervezet védekezése vírusfertőzésekkel szemben, antivirális kemoterápia, virális vakcinák Cytotoxicitás Antitest termelés B sejt Antigen presenting cell (APC) - MHCII B cell receptor Plazmasejt immunoglobulin
2012/1 A FIZIKAI-KÉMIAI MÓDSZEREK SZEREPE A LIPOSZÓMA ALAPÚ KIS INTERFERÁLÓ RNS (SIRNS) SZÁLLÍTÓRENDSZEREK
 VIZSGÁLATI MÓDSZEREK TESTING METHODS A FIZIKAI-KÉMIAI MÓDSZEREK SZEREPE A LIPOSZÓMA ALAPÚ KIS INTERFERÁLÓ RNS (SIRNS) SZÁLLÍTÓRENDSZEREK JELLEMZÉSÉBEN ROLE OF PHYSICOCHEMICAL METHODS FOR CHARACTERIZATION
VIZSGÁLATI MÓDSZEREK TESTING METHODS A FIZIKAI-KÉMIAI MÓDSZEREK SZEREPE A LIPOSZÓMA ALAPÚ KIS INTERFERÁLÓ RNS (SIRNS) SZÁLLÍTÓRENDSZEREK JELLEMZÉSÉBEN ROLE OF PHYSICOCHEMICAL METHODS FOR CHARACTERIZATION
Ismeretlen eredetű tüdőgyulladás megjelenése a SARS kórokozó vírusának azonosítása nemzetközi összefogással
 BIOTECHNOLÓGIA AZ EGÉSZSÉGÜGYBEN Ismeretlen eredetű tüdőgyulladás megjelenése a SARS kórokozó vírusának azonosítása nemzetközi összefogással Tárgyszavak: SARS; vírus; koronavírus; vakcina; kutatás; vírusmutáció.
BIOTECHNOLÓGIA AZ EGÉSZSÉGÜGYBEN Ismeretlen eredetű tüdőgyulladás megjelenése a SARS kórokozó vírusának azonosítása nemzetközi összefogással Tárgyszavak: SARS; vírus; koronavírus; vakcina; kutatás; vírusmutáció.
Immunológia 4. A BCR diverzitás kialakulása
 Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
AZ IS30 BAKTERIÁLIS INSZERCIÓS ELEM CÉLSZEKVENCIA VÁLASZTÁSÁNAK MOLEKULÁRIS TÉNYEZŐI DOKTORI ÉRTEKEZÉS TÉZISEI SZABÓ MÓNIKA
 AZ IS30 BAKTERIÁLIS INSZERCIÓS ELEM CÉLSZEKVENCIA VÁLASZTÁSÁNAK MOLEKULÁRIS TÉNYEZŐI DOKTORI ÉRTEKEZÉS TÉZISEI SZABÓ MÓNIKA Gödöllő 2007. 1 A Doktori Iskola megnevezése: Szent István Egyetem Biológia Tudományi
AZ IS30 BAKTERIÁLIS INSZERCIÓS ELEM CÉLSZEKVENCIA VÁLASZTÁSÁNAK MOLEKULÁRIS TÉNYEZŐI DOKTORI ÉRTEKEZÉS TÉZISEI SZABÓ MÓNIKA Gödöllő 2007. 1 A Doktori Iskola megnevezése: Szent István Egyetem Biológia Tudományi
Vese génterápia (RNSi) és lupus nephritis IVIG kezelésének mellékhatás-vizsgálata egérmodellen. Doktori tézisek. Dr.
 Vese génterápia (RNSi) és lupus nephritis IVIG kezelésének mellékhatás-vizsgálata egérmodellen Doktori tézisek Dr. Rácz Zsuzsanna Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Témavezető:
Vese génterápia (RNSi) és lupus nephritis IVIG kezelésének mellékhatás-vizsgálata egérmodellen Doktori tézisek Dr. Rácz Zsuzsanna Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Témavezető:
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az adaptív immunválasz kialakulása. Erdei Anna Immunológiai Tanszék ELTE
 Az adaptív immunválasz kialakulása Erdei Anna Immunológiai Tanszék ELTE NK sejt T Bev. 1. ábra Immunhomeosztázis A veleszületett immunrendszer elemei nélkül nem alakulhat ki az adaptív immunválasz A veleszületett
Az adaptív immunválasz kialakulása Erdei Anna Immunológiai Tanszék ELTE NK sejt T Bev. 1. ábra Immunhomeosztázis A veleszületett immunrendszer elemei nélkül nem alakulhat ki az adaptív immunválasz A veleszületett
I. A sejttől a génekig
 Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
Epigenetikai Szabályozás
 Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Hua Wang, Marianne Gauthier, Jamie R. Kelly, Rita J. Miller, Ming Xu, William D. O Brien, Jr. and Jianjun Cheng
 Hua Wang, Marianne Gauthier, Jamie R. Kelly, Rita J. Miller, Ming Xu, William D. O Brien, Jr. and Jianjun Cheng Pünkösti Zoltán Csoportgyűlés, 2016. április 12. Nem természetes cukrok metabolikus címkézése:
Hua Wang, Marianne Gauthier, Jamie R. Kelly, Rita J. Miller, Ming Xu, William D. O Brien, Jr. and Jianjun Cheng Pünkösti Zoltán Csoportgyűlés, 2016. április 12. Nem természetes cukrok metabolikus címkézése:
A C. elegans TRA-1/GLI/Ci szex-determinációs faktor célgénjeinek meghatározása és analízise. Doktori értekezés tézisei.
 A C. elegans TRA-1/GLI/Ci szex-determinációs faktor célgénjeinek meghatározása és analízise Doktori értekezés tézisei Hargitai Balázs Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Doktori
A C. elegans TRA-1/GLI/Ci szex-determinációs faktor célgénjeinek meghatározása és analízise Doktori értekezés tézisei Hargitai Balázs Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Doktori
Új terápiás lehetőségek helyzete. Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály
 Új terápiás lehetőségek helyzete Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály Mucopolysaccharidosisok MPS I (Hurler-Scheie) Jelenleg elérhető oki terápiák Enzimpótló kezelés
Új terápiás lehetőségek helyzete Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály Mucopolysaccharidosisok MPS I (Hurler-Scheie) Jelenleg elérhető oki terápiák Enzimpótló kezelés
Génterápia Általános áttekintés
 Génterápia Általános áttekintés A molekuláris medicina rohamléptekkel történő fejlődése lehetővé tette a humán betegségek molekuláris diagnosztikáját; a sejtekben átmenetileg megjelenő idegen nukleinsavak
Génterápia Általános áttekintés A molekuláris medicina rohamléptekkel történő fejlődése lehetővé tette a humán betegségek molekuláris diagnosztikáját; a sejtekben átmenetileg megjelenő idegen nukleinsavak
 RÉSZLETES BESZÁMOLÓ Az OTKA által támogatott konzorcium működésében az Uzsoki utcai Kórház feladata a szövetminták gyűjtése, előzetes feldolgozása, ill. a betegek utánkövetése, valamint az utánkövétésre
RÉSZLETES BESZÁMOLÓ Az OTKA által támogatott konzorcium működésében az Uzsoki utcai Kórház feladata a szövetminták gyűjtése, előzetes feldolgozása, ill. a betegek utánkövetése, valamint az utánkövétésre
Fehérje O-Glikoziláció (O-GlcNAc) szerepe különböző betegségekben, detektálási lehetőségei
 Fehérje O-Glikoziláció (O-GlcNAc) szerepe különböző betegségekben, detektálási lehetőségei Nagy T., Frank D., Miseta A., Kovács GL. Laboratóriumi Medicina Intézet, ÁOK, Pécsi Tudományegyetem, Pécs 2010
Fehérje O-Glikoziláció (O-GlcNAc) szerepe különböző betegségekben, detektálási lehetőségei Nagy T., Frank D., Miseta A., Kovács GL. Laboratóriumi Medicina Intézet, ÁOK, Pécsi Tudományegyetem, Pécs 2010
A növény inváziójában szerepet játszó bakteriális gének
 A növény inváziójában szerepet játszó bakteriális gének merisztéma korai szimbiotikus zóna késői szimbiotikus zóna öregedési zóna gyökér keresztmetszet NODULÁCIÓ növényi jel Rhizobium meliloti rhizobium
A növény inváziójában szerepet játszó bakteriális gének merisztéma korai szimbiotikus zóna késői szimbiotikus zóna öregedési zóna gyökér keresztmetszet NODULÁCIÓ növényi jel Rhizobium meliloti rhizobium
Biomolekuláris nanotechnológia. Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium
 Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 6. előadás Humorális és celluláris immunválasz A humorális (B sejtes) immunválasz lépései Antigén felismerés B sejt aktiváció: proliferáció, differenciálódás
Immunológiai módszerek a klinikai kutatásban 6. előadás Humorális és celluláris immunválasz A humorális (B sejtes) immunválasz lépései Antigén felismerés B sejt aktiváció: proliferáció, differenciálódás
(11) Lajstromszám: E 007 949 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007949T2! (19) HU (11) Lajstromszám: E 007 949 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 835738 (22) A bejelentés napja:
!HU000007949T2! (19) HU (11) Lajstromszám: E 007 949 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 835738 (22) A bejelentés napja:
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Antiszenz oligodezoxinukleotidok A géncsendesítés új eszközei magasabbrendű növényekben
 DOKTORI ÉRTEKEZÉS TÉZISEI Antiszenz oligodezoxinukleotidok A géncsendesítés új eszközei magasabbrendű növényekben Emine Dinç Témavezető: Dr. Sándor Bottka tudományos főmunkatárs Magyar Tudományos Akadémia
DOKTORI ÉRTEKEZÉS TÉZISEI Antiszenz oligodezoxinukleotidok A géncsendesítés új eszközei magasabbrendű növényekben Emine Dinç Témavezető: Dr. Sándor Bottka tudományos főmunkatárs Magyar Tudományos Akadémia
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
