Génterápia Általános áttekintés
|
|
|
- Ágnes Tóth
- 7 évvel ezelőtt
- Látták:
Átírás
1 Génterápia Általános áttekintés A molekuláris medicina rohamléptekkel történő fejlődése lehetővé tette a humán betegségek molekuláris diagnosztikáját; a sejtekben átmenetileg megjelenő idegen nukleinsavak kimutatásától (fertőzések) a szomatikus sejtekben történt mutáción át (karcinogenezis) a csírasejteket ért mutációkig (öröklődő betegségek). Ismertté vált a betegségek egy részének genetikai háttere; a hatalmas léptekkel növekedő elméleti tudás (köztük a humán genom project befejezése) lehetőséget adott rá, hogy az ismereteket klinikai gyakorlatban alkalmazva a betegségek génszinten kezelhetőek legyenek. Ezek a terápiás megközelítések, amelyeket molekuláris terápiának vagy génterápiának nevezünk, az elmúlt évtizedekben hatalmas fejlődésen mentek keresztül, részletes tárgyalásuk messze túlmutat a konzultáció keretein. A génterápia megítélésénél figyelembe kell vennünk, hogy sok esetben kísérleti stádiumú kezelésekről van szó; az első értékelhető próbálkozások húsz éve kezdődtek (összehasonlításul, a csontvelő transzplantáció 1958-ban kezdődött és a hetvenes évek elejére a túlélés 1%-os volt). A jelenleg folyó klinikai próbákról a oldal ad felvilágosítást. A próbálkozások elsősorban olyan eseteken folynak, ahol a betegség súlyossága meghaladja a terápia kockázatát. Etikai okokból a betegektől nem vonják meg a génterápiától független kezelési formákat, ami a génterápia eredményességének megítélését tovább nehezíti. A génterápia célja, hogy sejtbe juttatott nukleinsavakkal a hibás, betegséget okozó gént pótoljuk, módosítsuk vagy kiüssük. A nukleinsavakat többnyire vektorokba építik be, amelyek segítik a molekula sejtbe való bejutását. A vektorok adása történhet in vivo vagy ex vivo. Utóbbi esetben a beavatkozást a betegtől nyert sejteken laboratóriumi körülmények között végzik, majd a sejteket a módosítás után visszajuttatják a betegbe (autológ transzplantáció). A vektorokat két nagy csoportba osztjuk, virális illetve nem-virális. Jelen pillanatban a klinikai próbák 90 százalékában virális vektorokat használnak. A vírusokkal történt génbevitelt transzdukciónak, míg általánosságban a DNS beépülését a genomba inzerciónak nevezzük. Attól függően, milyen vektort választunk, a terápiás hatású DNS molekula beépülhet a gazdasejt kromoszóma állományába (és továbbjut az utódsejtekbe) vagy extrakromoszómális DNS formájában marad. Létrehozható mesterséges emberi kromoszóma (human artificial chromosomes, HAC) mely a sejtbe juttatva mint új kromoszóma működik. Ezek a biztonságos és hosszú távú expressziót biztosító vektorok egyelőre kísérleti körülmények közt működnek, mivel a mesterséges mikro-kromoszómák konstrukciója és sejtbe történő bejuttatása technikailag nehézkes és rendkívül nagy kihívást jelent a kutatók számára. A génpótlás a leggyakrabban alkalmazott klinikai eljárás; a mutáns gén mellett megjelenő normál gén expressziója pótolni képes a hiányzó (mutáns) fehérjét. A kezdeti génterápia azokat a recesszív, monogénes, funkcióvesztő mutáció következtében kialakult betegségeket célozta meg, ahol ha nem történik meg a fehérje pótlása a betegség halálos kimenetelű. Technikailag jóval nehezebb a hibás gének módosítása és kiütése. Ezen a területen nagy előrelépést jelentett a cink-ujj nukleázok felfedezése. Ezekkel a módosított transzkripciós faktorokkal lehetővé válhat a DNS irányított, specifikus szekvenciákon történő vágása, amelyet rekombináció követ. Fejlesztésük folyamatos ( ). Kívülről bevitt nukleinsavakkal lehetőség van a génexpresszió és a fehérje funkció befolyásolására is, ilyenkor nem a genetikai állományba avatkoznak be, a 1
2 terápia nem a DNS, hanem az RNS szintjén történik ban Nobel díjjal jutalmazták az RNS interferencia (RNAi) felfedezését, ami mrns-ek irányított, szekvencia specifikus lebontását jelenti. A génexpresszió szabályozásának ezt a módját, amely a sejtekben fiziológiásan is jelen van, a mikro-rns (mirns) molekulák közvetítik. Ezek a rövid (19-23 nukleotid) genomban kódolt RNS molekulák számos élettani folyamatban (egyedfejlődés, proliferáció, apoptózis, differenciáció) szerepet játszanak, és expressziójuk megváltozását kimutatták számos betegségben, köztük daganatokban. Az RNS interferencia laboratóriumi kutatásokban bármely gén expressziójának gátlását (lecsendesítését) lehetővé teszi, és a humán diagnosztikus és terápiás alkalmazások köre is egyre szélesebb. A sejtbe juttatott vagy a sejten belül expresszált rövid kettősláncú RNS molekulák (small interfering RNS, sirns) komplementer módon kötődnek a cél-mrns molekulához, indukálják annak lebontását, így szekvencia specifikus gátlást eredményeznek. Az RNS aptamerek specifikus és stabil háromdimenziós szerkezettel rendelkeznek, ami specifikus és stabil kötődést eredményez a célmolekulához. A célmolekula lehet sejtfelszíni receptor, így az aptamerekhez kötött molekulák csatolt áruként irányítottan tudnak a sejtekbe jutni. Ilyen szállítmány lehet tumor-ellenes gyógyszer, enzim, vagy akár sirns. Az antisense (ellenirányú) oligonukleotidok komplementerek a mutáns sense mrns lánccal, kötődésük megakadályozza a mutáns mrns transzlációját. Számos antisense terápia áll klinikai próba alatt, egyes szerek (antivirális, koleszterin szint csökkentő) engedélyezésre kerültek. Az antisense-hez hasonlóan a ribozimek (enzimaktivitással bíró RNS molekulák) is specifikusan kötődnek a cél-mrns molekulához, és lebontják azt. Bizonyos esetekben nem elegendő a normál fehérje pótlása, mert a mutáns fehérje (domináns negatív mutáció) elnyomja a fiziológiás fehérje működését. A mutáns fehérjét kódoló RNS molekulák specifikusan bonthatóak a fent ismertetett módszerekkel. Technikai nehézségek Az elmúlt 10 év főbb feladatai közé tartozott a vektor rendszerek finomítása, biztonságosabbá tétele, és termelésük gazdaságosságának javítása. In vivo terápia esetén a lokálisan vagy szisztémásan adott vektor ideális esetben csak a célsejtekhez jut el, azaz sejtspecifikus, ami nem-virális vektor esetén specifikus ligandok, virális vektor esetén módosított vírus burok fehérjékkel érhető el. A vektornak át kell jutnia az esetleges endothelium barrieren, és be kell jutnia a sejtmagba. A bejuttatott DNS molekula elhelyezkedhet extrakromoszómálisan, vagy beépülhet a gazdasejt kromoszóma állományába. Az extrakromoszómális forma nem osztódó sejtekben sokáig fenn tud maradni, osztódó sejtekből viszont kihígul. A beépülésre képes vektorok előnye, hogy a beépült DNS molekulát a sejt osztódása során keletkezett utódsejtek is tartalmazni fogják, hátránya viszont, hogy (mivel a beépülés nem irányítottan történik) a beépülés gének aktivációját/inaktivációját eredményezheti (inzerciós mutagenezis). A terápiás gén expressziójának időtartama szerzett betegségek (fertőzés, tumor) esetén átmeneti időre kell hogy szorítkozzon, míg genetikai betegségek esetén többnyire egész életen át tartó. A hosszútávú sikeres génterápia egyik fő akadálya a vektor vagy a terápiás géntermék elleni immunválasz. A mesterséges vírusok vad típusú társaikhoz hasonlóan, kiváltják az immunrendszer reakcióját. Különösen igaz ez azokra a szerotípusokra, amelyekkel a legtöbb felnőtt már találkozott élete során. 2
3 A génterápiában használt különböző vektorok, és a hozzájuk kapcsolódó terápiás próbálkozások 1. Virális vektorok 1.1 retrovirális vektorok A retrovírusok manipulációjából nyert vektorok előnye, hogy a provírus kódoló része könnyen lecserélhető a terápiás génre, és a vírus életciklusa során a provírus integrálódik a genomba. A beépíthető inzert maximális mérete 8-10 kilobázis (kb). Hátrányuk, hogy a beépülés inszerciós mutagenezishez, a kezelt sejtek tumoros malformációjához vezethet. Döntően csak osztódó sejteket fertőznek meg. A retrovirális vektorok voltak az első humán génterápiás eljárás választott vektorai (adenozin-deamináz hiány (ADA)) és velük történt az első sikeres génterápiás eljárás is (severe combined immunodeficiency (SCID)). Mivel a sejt DNS állományába történő beavatkozás hatását nem lehet pontosan kiszámítani, mindkét terápia olyan immunhiányos betegségben történt, ahol a betegség kezelés néhány év alatt halálhoz vezet. Az immunrendszer részét képező leukociták differenciációja számos ponton zavart szenvedhet, amely súlyos kombinált immundeficienciát (severe combined immunodeficiency, SCID) eredményez. Ennek egyik formája egy nukleotid anyagcserében szerepet játszó enzim, az adenozin deamináz génjének mutációja miatt alakul ki ben egy 4 éves kislány megfelelő donor hiányában nem részesülhetett csontvelő transzplantációban, így a szülők tájékoztatása után ex vivo génterápiát végeztek, a gyermektől nyert csontvelősejteket a funkcionális ADA gént tartalmazó retrovírussal transzformálták, majd a sejteket visszajuttatták (autológ csontvelő transzplantáció). A beavatkozást követően a beteg felépült, normál életet élt és él a mai napig. A génterápia sikere mégsem volt egyértelműsíthető, mert a génterápia megkezdése előtt egy új enzimpótló terápiát dolgoztak ki (ADA-PEG) amelyet etikai okokból nem vontak meg a betegtől. A párhuzamos terápia egyrészt megnehezítette a génterápia megítélését, másrészt annak kivitelezését is, mivel a funkcióképes ADA gént hordozó sejteknek nem volt növekedési előnyük a mutáns gént hordozó sejtekkel szemben. A SCID egy másik formáját a citokinek differenciációs hatását közvetítő sejtfelszíni receptor génjének mutációja eredményezi. Egy 2000-ben megjelent közleményben a SCID sikeres ex-vivo génterápiájáról számoltak be, a betegek a génterápiás kezelésnek köszönhetően 4 évvel később funkcióképes immunrendszerrel bírtak és normál életvitelt folytattak. Ugyanakkor beigazolódott a retrovirális vektorok legsúlyosabb szövődményétől, az inzerciós mutagenezistől való félelem; a betegek ötödénél a kezeléssel egyértelműen kapcsolatba hozható leukémia fejlődött ki. Ez a génterápiás vektorok továbbfejlesztését, a kezelések biztonságának további újragondolását tette szükségessé. Az egygénes betegségek (SCID, cisztás fibrózis, Duchenne-féle muszkuláris disztrófia) mellett előtérbe került az összetettebb genetikai hátterű betegségek, mint a tumorok és a kardiovaszkuláris betegségek kezelése. Tumor terápia részeként klinikai próbákban retrovírusokkal transzdukáltak autológ T sejtes limfocitákat. Az ily módon tumor antigén ellenessé tett limfociták remissziót idéztek elő. 1.2 Lentivirális vektorok A retrovírusok egy alcsoportja, a lentivírusok nem osztódó sejteket is képesek transzdukálni. A terápiák biztonsága érdekében létrehoztak magukat inaktiváló 3
4 retrovírusokat, melyek lényege, hogy nem tartalmaznak olyan promoter elemeket, amelyek a beépülés helyétől távolabb levő géneket aktiválni képesek (hiányzó enhanszer hatás). -globin cdns-t expresszáló lentivírussal ex vivo transzdukálták egy thalassaemiában szenvedő beteg hematopoetikus sejtjeit, és ezzel sikerült a beteg transzfúzó függését megszüntetni. HIV-alapú lentivirális vektorokkal kísérletet tettek a HIV eliminálására is; nem kódoló RNS molekulák expresszálásával a HIV receptorának expresszióját és a HIV replikációját gátolták. 1.3 Adenovirális vektorok Az adenovirális vektorok előnye, hogy sokféle sejt transzdukálható, jó hatásfokkal, nagyméretű genomjuk lehetővé teszi nagyméretű inzertek (8 kb) sejtbe juttatását. A vektor episzómális (extrakromoszómális) marad, így hatása osztódó sejtekben többnyire átmeneti. Nyugvó sejtekben amennyiben nem lép fel immunválasz, hosszú távon stabil terápiás plazmaszint érhető el termeltetett fehérjékből (koagulációs faktorok, 1 antitripszin, erythropoietin). Történtek (egyelőre ellentmondásos) klinikai próbák onkolítikus tumorvírusokkal, amelyek csak tumorsejtekben replikálódnak. A cukorbetegség terápiájában kísérletek folynak sejt transzkripciós faktorokkal a sejtek újraprogramozására és ezzel a hyperglikémia rendezésére. Az adenovírus szisztémás adása kiválthatja az immunrendszer reakcióját, ami súlyos toxikus következményekkel járhat. Folynak próbálkozások az adenovírusok szerotípusának módosítására, ami az immunválasz mérséklését eredményezhetné, de adenovírusok esetében technikailag ez sokkal nehezebb, mint retrovírusok esetében. A génterápia első halálos szövődményét a terápiás céllal használt adenovírusra adott masszív immunválasz okozta 1999-ben. A beteg az urea ciklus egyik központi enzimének, az ornitin transzkarbamoiláznak defektusában szenvedett. 1.4 Adeno-asszociált vírusok Az adeno-asszociált vírusok előnye, hogy integrálódnak a genomba és integrációjuk helye, amely a 19-es kromoszóma egy specifikus részén történik, megjósolhatóbb, mint a retrovírusoké. További előnyük, hogy nem-osztódó sejteken is végezhető transzdukció, nem váltanak ki immunválaszt és könnyen előállíthatók nagy mennyiségben (magas titer) Hátrányuk, hogy a bevihető terápiás DNS szakaszok mérete korlátozott (5 kb). A vírust előnyös tulajdonságai miatt több génregulációt befolyásoló kísérletben használták, mivel itt a kisméretű inzert nem jelent hátrányt. Duchenne-féle disztrófiában, melyet a disztrofint kódoló, az eddig ismert legnagyobb emberi gén mutációja okoz, a vírussal bevitt RNS molekulákkal sikerült exon kihagyást (exon skipping) indukálni és ezzel működőképes fehérjét termeltetni. Tumor terápiákban onkogének mrns termékeit sikeresen lebontották AAV által expresszált sirns molekulákkal. Több öröklődő vakság esetében sikerrel alkalmaztak génterápiát. Leber-féle veleszületett vakságban a normál gént hordozó AAV subretinális infúziója ígéretes és biztonságos kezelésnek bizonyult. A próbában résztvevő betegek látása kivétel nélkül javult, minél fiatalabb életkorban kezdték a kezelést annál nagyobb mértékben. Jelenleg folyó kísérletekben az izmot mint fehérje gyárat próbálják használni, melyben lipoprotein lipázt (LPL), α1 antitripszint és véralvadási faktorokat termelnek ben a gyártó cég kérte egy LPL expresszáló vektor, a Glybera forgalomba hozatalát. A klinikai próbák már egyetlen dózis esetén is igazolták 4
5 lipoprotein lipáz deficienciában a Glybera pozitív hatásait, köztük az életet veszélyeztető szövődmény, a hasnyálmirigy gyulladásának megelőzését. A központi idegrendszer betegségeiben, elsősorban a Parkinson kór kezelésében AAV transzdukcióval sejtbe juttatott terápiás gének (neurotranszmitter termelés befolyásolása, a dopamin szintézis enzimei, növekedési faktorok) bevitele már irányítottan (valós idejű mágneses rezonanciás képalkotás (real-time MR imaging)) történhet, akár sejttípus függően. 2. Nem virális vektorok Miután a DNS bejut a citoplazmába (többnyire endocitózissal), fehérjékkel komplexet képez, amelyek a sejten belüli vándorlást befolyásolják, szabályozzák. A nem-virális terápia esetében a sejtmag membránja jelenti a döntő akadályt a bevitt DNS számára. A jelenleg folyó vizsgálatok a sejtmagba történő bejutás hatásfokának javítására irányulnak, peptidek, natív vagy mesterségesen előállított fehérjék, transzkripciós faktor kötőhelyek segítségével. Rendkívül nagy számban kerültek kifejlesztésre szintetikus biológiailag lebomló polimer, melyek a DNS molekulával összekeverve nanorészecskéket hoznak létre. A nem-virális vektoroknak az a hátránya, hogy hatásfokuk elmarad a virális vektorok hatásfokától, a fejlesztések eredményeként bizonyos esetekben eltűnt. Bár a vektorok az esetek döntő részében episzómálisan helyezkednek el, kísérletek folynak irányított inzerciójukra laboratóriumi körülmények között előállított transzpozonokkal (pl. Csipkerózsika (Sleeping Beauty) transzpozon). A génterápia jövője A személyre szabott medicina korában vagyunk, amikor a jóslatok szerint a teljes humán genom szekvenálása rövid időn belül 1000 dollár alá esik, és kiválthatja a születéskor végzett génteszteket. A génterápiával párhuzamosan egy új terület, az őssejt kutatás került az érdeklődés középpontjába; várhatóan a génterápiával kombinált őssejtterápia a jövő terápiái közt fog szerepelni. Erre példa a következő, vírusos májgyulladás kezelésére történt póbálkozás. Vírusos hepatitis krónikus formájában (HBV, HCV) a májtranszplantátum sejtjeit májban található őssejtekből, vagy májsejtté differenciált pluripotens őssejtekből hozzák létre. A transzplantátum újra fertőződését módosított sejtekkel próbálják megakadályozni oly módon, hogy vírus ellenes sirns molekulákat expresszálnak a transzplantátum sejtjeiben. 5
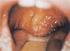
6 Melléklet, kiegészítő információ: Esettanulmány Leber Congenital Amaurosis, LCA ( ) génterápiája Háttér információ A látás kémiája és a Retinal Pigment Epithelium Specific Protein, 65 KD, RPE65 funkciója ( ) Az RPE65 egy izomerohidroláz aktivitással rendelkező enzim, amely transz-retinil észtereket alakít át 11-cisz-retinollá a retina pigment epitheliumában (RPE). Az RPE a retina fotoreceptor sejtjeivel szoros kapcsolatban álló hámréteg (Ld. alábbi ábrát), amely fontos szerepet játszik a retina metabolizmusában és a látás kémiai ciklusának fenntartásában. A retina sejtszintű morfológiája (K. Palczewski, J Biol Chem 2012; 287: 1616-) A látási ciklus során a 11-cisz-retinal opszinhoz kötődik és így képződik rodopszin, amelyben fény foton abszorpciója után 11-cisz transz-retinal fotoizomerizáció történik és ez eredményez olyan konformációváltozást a rodopszinban, amely után az kölcsönhatásba lép heterotrimer G fehérjével a szignál továbbításához. A transz-retinal leválik az opszin kromofor kötőhelyéről és egy NADPH-függő transzretinol dehidrogenáz transz- retinollá alakítja át. Ezt követően a transz-retinolnak át kell mennie a szomszédos RPE sejtekbe. Ezt a lépést a retinol zsírsavval történő észterifikációja teszi lehetővé, amelyet lecitin-retinol acil transzferáz katalizál. Az RPE sejtekben a retinil észterek raktár zárványokat képeznek, amelyek szubsztrátot biztosítanak az RPE65 számára. Az utóbbi enzim hidroláz és izomeráz aktivitása eredményeként a transz-retinol felszabadul és 11-ciszretinollá alakul, amelyet dehidrogenáz oxidál 11-cisz retinállá. A ciklus befejező lépése a 11-cisz retinál diffúziója a fotoreceptor sejtekbe, ahol opszinhoz kötődik. A látás kémiai ciklusát az alábbi ábra foglalja össze. 6
7 A látás kémiai ciklusa (K. Palczewski, J Biol Chem 2012; 287: 1616-) A Leber-féle kongenitális amaurosis (LCA) olyan autoszomális recesszív betegség, amely kisgyerekkorban a látás teljes elvesztésével jár. A betegség hátterében az RPE65 hiánya áll. Jellemző, hogy kezdetben a vakság ellenére a retinasejtek sejtek szerkezete hosszú éveken át relatíve megtartott, de az idő múltával progresszíve pusztulnak. Az LCA génterápiás kezelése e gyógyítási eljárás egyik sikertörténete, amely jelenleg egyedüliként III. fázisú klinikai kipróbálás stádiumában van ( kezdete augusztus, vége 2014 december, végleges lezárása 2028 december). A sikeres eljárást Katherine High és Jean Bennett munkacsoportjai dolgozták ki ( ). AAV vektorba építették be az RPE65 gént és 1 szubretinális injekcióval vitték be a beteg rosszabbik szemébe. Tizenkét betegen (8-tól 44 éves korig) 3 kísérletes dózist alkalmaztak (1,5x10 10 vektor genom, 4,8x10 10 vektor genom és 1,5x10 11 vektor genom) és eddig 2 éves megfigyelés eredményeiről tudtak beszámolni. Minden beteg fényérzékenysége javult, a pupilla reakció szerint legalább 2 nagyságrenddel. A kezelésre a gyerekek reagáltak a legjobban, egy 8 éves fiú teljesen visszanyerte látását ( ). Általános jelentőséggel bír az a tény, hogy egyelőre semmilyen mellékhatás nem jelentkezett. 7
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk.
 A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei)
 Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Molekuláris terápiák
 Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
TÉMAKÖRÖK. Ősi RNS világ BEVEZETÉS. RNS-ek tradicionális szerepben
 esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
A preventív vakcináció lényege :
 Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Az ellenanyagok szerkezete és funkciója. Erdei Anna Immunológiai Tanszék ELTE
 Az ellenanyagok szerkezete és funkciója Erdei Anna Immunológiai Tanszék ELTE Bev. 1. ábra Immunhomeosztázis A veleszületett és az adaptív immunrendszer szorosan együttműködik az immunhomeosztázis fenntartásáért
Az ellenanyagok szerkezete és funkciója Erdei Anna Immunológiai Tanszék ELTE Bev. 1. ábra Immunhomeosztázis A veleszületett és az adaptív immunrendszer szorosan együttműködik az immunhomeosztázis fenntartásáért
Hamar Péter. RNS világ. Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. www.meetthescientist.hu 1 26
 Hamar Péter RNS világ Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. 1 26 Főszereplők: DNS -> RNS -> fehérje A kód lefordítása Dezoxy-ribo-Nuklein-Sav: DNS az élet kódja megkettőződés (replikáció)
Hamar Péter RNS világ Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. 1 26 Főszereplők: DNS -> RNS -> fehérje A kód lefordítása Dezoxy-ribo-Nuklein-Sav: DNS az élet kódja megkettőződés (replikáció)
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE
 Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Immunológia I. 4. előadás. Kacskovics Imre
 Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia 4. A BCR diverzitás kialakulása
 Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Új terápiás lehetőségek helyzete. Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály
 Új terápiás lehetőségek helyzete Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály Mucopolysaccharidosisok MPS I (Hurler-Scheie) Jelenleg elérhető oki terápiák Enzimpótló kezelés
Új terápiás lehetőségek helyzete Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály Mucopolysaccharidosisok MPS I (Hurler-Scheie) Jelenleg elérhető oki terápiák Enzimpótló kezelés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
RNS-ek. 1. Az ősi RNS Világ: - az élet hajnalán. 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek
 RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
Immunológia alapjai előadás MHC. szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
HUMAN IMMUNDEFICIENCIA VÍRUS (HIV) ÉS AIDS
 HUMAN IMMUNDEFICIENCIA VÍRUS (HIV) ÉS AIDS Dr. Mohamed Mahdi MD. MPH. Department of Infectology and Pediatric Immunology University of Debrecen (MHSC) 2012 Diagnózis HIV antitest teszt: A HIV ellen termel
HUMAN IMMUNDEFICIENCIA VÍRUS (HIV) ÉS AIDS Dr. Mohamed Mahdi MD. MPH. Department of Infectology and Pediatric Immunology University of Debrecen (MHSC) 2012 Diagnózis HIV antitest teszt: A HIV ellen termel
Molekuláris genetikai vizsgáló. módszerek az immundefektusok. diagnosztikájában
 Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Rekombináns Géntechnológia
 Rekombináns Géntechnológia Tartalom: 1 1. Biotechnológia, géntechnológia, társadalom 2. Genetikai rekombináció 3. Génbevitel tenyésztett sejtekbe 4. Genetikailag módosított szervezetek (GMO-k) 4a. Transzgénikus
Rekombináns Géntechnológia Tartalom: 1 1. Biotechnológia, géntechnológia, társadalom 2. Genetikai rekombináció 3. Génbevitel tenyésztett sejtekbe 4. Genetikailag módosított szervezetek (GMO-k) 4a. Transzgénikus
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
I. A sejttől a génekig
 Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
A biológia szerepe az egészségvédelemben
 A biológia szerepe az egészségvédelemben Nagy Kinga nagy.kinga@mail.bme.hu 2017.10.24 Mikróbák az ember szolgálatában (Néhány példán keresztül bemutatva) Antibiotikumok (gombák, baktériumok) Restrikciós
A biológia szerepe az egészségvédelemben Nagy Kinga nagy.kinga@mail.bme.hu 2017.10.24 Mikróbák az ember szolgálatában (Néhány példán keresztül bemutatva) Antibiotikumok (gombák, baktériumok) Restrikciós
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Az adenovírusok morfológiája I.
 Adenovírusok A vírusok Elnevezésük a latin virus szóból ered, amelynek jelentése méreg. A vírusok a legkisebb ismert entitások. Csak elektronmikroszkóppal tanulmányozhatóak, mert méretük 20-400 nanométerig
Adenovírusok A vírusok Elnevezésük a latin virus szóból ered, amelynek jelentése méreg. A vírusok a legkisebb ismert entitások. Csak elektronmikroszkóppal tanulmányozhatóak, mert méretük 20-400 nanométerig
Sejtek - őssejtek dióhéjban. 2014. február. Sarkadi Balázs, MTA-TTK Molekuláris Farmakológiai Intézet - SE Kutatócsoport, Budapest
 Sejtek - őssejtek dióhéjban 2014. február Sarkadi Balázs, MTA-TTK Molekuláris Farmakológiai Intézet - SE Kutatócsoport, Budapest A legtöbb sejtünk osztódik, differenciálódik, elpusztul... vérsejtek Vannak
Sejtek - őssejtek dióhéjban 2014. február Sarkadi Balázs, MTA-TTK Molekuláris Farmakológiai Intézet - SE Kutatócsoport, Budapest A legtöbb sejtünk osztódik, differenciálódik, elpusztul... vérsejtek Vannak
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
4. A humorális immunválasz október 12.
 4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
Immunológia Alapjai. 13. előadás. Elsődleges T sejt érés és differenciálódás
 Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
In vivo szövetanalízis. Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra
 In vivo szövetanalízis Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra In vivo képalkotó rendszerek Célja Noninvazív módon Biológiai folyamatokat képes rögzíteni Élő egyedekben
In vivo szövetanalízis Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra In vivo képalkotó rendszerek Célja Noninvazív módon Biológiai folyamatokat képes rögzíteni Élő egyedekben
Epigenetikai Szabályozás
 Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Allergia immunológiája 2012.
 Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására
 11. 2016. nov 30. 17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására 17.3. ábra A sejtközötti térben és a sejten belül élő és szaporodó kórokozók ellen kialakuló védekezési mechanizmusok
11. 2016. nov 30. 17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására 17.3. ábra A sejtközötti térben és a sejten belül élő és szaporodó kórokozók ellen kialakuló védekezési mechanizmusok
Transzgénikus állatok előállítása
 Transzgénikus állatok előállítása A biotechnológia alapjai Pomázi Andrea Mezőgazdasági biotechnológia A gazdasági állatok és növények nemesítése új biotechnológiai eljárások felhasználásával. Cél: jobb
Transzgénikus állatok előállítása A biotechnológia alapjai Pomázi Andrea Mezőgazdasági biotechnológia A gazdasági állatok és növények nemesítése új biotechnológiai eljárások felhasználásával. Cél: jobb
Indukált pluripotens sejtek (IPs) 6 év alatt a Nobel-díjig...... és 8 év alatt az öngyilkosságig
 Indukált pluripotens sejtek (IPs) 6 év alatt a Nobel-díjig...... és 8 év alatt az öngyilkosságig induced Pluripotens Stem sejt (ipss) első közlemény 2006-ban egér / humán, embrionális / felnőtt fibroblasztok
Indukált pluripotens sejtek (IPs) 6 év alatt a Nobel-díjig...... és 8 év alatt az öngyilkosságig induced Pluripotens Stem sejt (ipss) első közlemény 2006-ban egér / humán, embrionális / felnőtt fibroblasztok
FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
Leukotriénekre ható molekulák. Eggenhofer Judit OGYÉI-OGYI
 Leukotriénekre ható molekulák Eggenhofer Judit OGYÉI-OGYI Mik is azok a leukotriének? Honnan ered az elnevezésük? - először a leukocitákban mutatták ki - kémiai szerkezetükből vezethető le - a konjugált
Leukotriénekre ható molekulák Eggenhofer Judit OGYÉI-OGYI Mik is azok a leukotriének? Honnan ered az elnevezésük? - először a leukocitákban mutatták ki - kémiai szerkezetükből vezethető le - a konjugált
Antigén, Antigén prezentáció
 Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A harkányi gyógyvízzel végzett vizsgálataink eredményei psoriasisban között. Dr. Hortobágyi Judit
 A harkányi gyógyvízzel végzett vizsgálataink eredményei psoriasisban 2007-2011 között Dr. Hortobágyi Judit Pikkelysömörre gyakorolt hatása 2007-től 2009-ig 1. Lokális hatása 2. Szisztémás hatása 3. Állatkísérlet
A harkányi gyógyvízzel végzett vizsgálataink eredményei psoriasisban 2007-2011 között Dr. Hortobágyi Judit Pikkelysömörre gyakorolt hatása 2007-től 2009-ig 1. Lokális hatása 2. Szisztémás hatása 3. Állatkísérlet
A BIOLÓGIAI GYÓGY- SZEREK FEJLESZTÉSÉNEK FINANSZÍROZÁSA ÉS TERÁPIÁS CÉLTERÜLETEI
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére A BIOLÓGIAI GYÓGY- SZEREK FEJLESZTÉSÉNEK FINANSZÍROZÁSA
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére A BIOLÓGIAI GYÓGY- SZEREK FEJLESZTÉSÉNEK FINANSZÍROZÁSA
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény
 A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
Az agy betegségeinek molekuláris biológiája. 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5.
 Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Az õssejtek, mint a génterápia fegyverhordozói
 Német Katalin Az õssejtek, mint a génterápia fegyverhordozói Az õssejtek, mint a génterápia fegyverhordozói Német Katalin PhD, Országos Gyógyintézeti Központ Haematológiai és Immunológiai Intézet nemet@biomembrane.hu
Német Katalin Az õssejtek, mint a génterápia fegyverhordozói Az õssejtek, mint a génterápia fegyverhordozói Német Katalin PhD, Országos Gyógyintézeti Központ Haematológiai és Immunológiai Intézet nemet@biomembrane.hu
avagy az ipari alkalmazhatóság kérdése biotechnológiai tárgyú szabadalmi bejelentéseknél Dr. Győrffy Béla, Egis Nyrt., Budapest
 Iparilag alkalmazható szekvenciák, avagy az ipari alkalmazhatóság kérdése biotechnológiai tárgyú szabadalmi bejelentéseknél Dr. Győrffy Béla, Egis Nyrt., Budapest Neutrokin α - jelentős kereskedelmi érdekek
Iparilag alkalmazható szekvenciák, avagy az ipari alkalmazhatóság kérdése biotechnológiai tárgyú szabadalmi bejelentéseknél Dr. Győrffy Béla, Egis Nyrt., Budapest Neutrokin α - jelentős kereskedelmi érdekek
A T sejtes immunválasz egy evolúciós szempontból váratlan helyzetben: Szervtranszplantáció
 A T sejtes immunválasz egy evolúciós szempontból váratlan helyzetben: Szervtranszplantáció Autotranszplantáció: saját szövet átültetése, pl. autológ bőrtranszplantáció, autológ őssejt-transzplantáció.
A T sejtes immunválasz egy evolúciós szempontból váratlan helyzetben: Szervtranszplantáció Autotranszplantáció: saját szövet átültetése, pl. autológ bőrtranszplantáció, autológ őssejt-transzplantáció.
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Studia Physiologica 20/2012. Sáfrány Géza. Agydaganatok kezelése génterápiával
 Studia Physiologica 20/2012 Sáfrány Géza Agydaganatok kezelése génterápiával Studia Physiologica Fasciculus 20 Agydaganatok kezelése génterápiával Sáfrány Géza A kötet megjelenését a Semmelweis Egyetem
Studia Physiologica 20/2012 Sáfrány Géza Agydaganatok kezelése génterápiával Studia Physiologica Fasciculus 20 Agydaganatok kezelése génterápiával Sáfrány Géza A kötet megjelenését a Semmelweis Egyetem
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői.
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Példák a független öröklődésre
 GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Immunológia alapjai előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B-sejt receptorok:
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B-sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B-sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje
 1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
12/4/2014. Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció. 1952 Hershey & Chase 1953!!!
 Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Molekuláris Medicina
 Molekuláris Medicina Molekuláris Medicina Őssejt terápia Génterápia Tumor terápia Immunterápia Egyéb terápiák Vakcinák Genetikai diagnosztika Orvosi genomika Terápiák Diagnosztikák Orvostudomány: régi
Molekuláris Medicina Molekuláris Medicina Őssejt terápia Génterápia Tumor terápia Immunterápia Egyéb terápiák Vakcinák Genetikai diagnosztika Orvosi genomika Terápiák Diagnosztikák Orvostudomány: régi
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
3. Általános egészségügyi ismeretek az egyes témákhoz kapcsolódóan
 11. évfolyam BIOLÓGIA 1. Az emberi test szabályozása Idegi szabályozás Hormonális szabályozás 2. Az érzékelés Szaglás, tapintás, látás, íz érzéklés, 3. Általános egészségügyi ismeretek az egyes témákhoz
11. évfolyam BIOLÓGIA 1. Az emberi test szabályozása Idegi szabályozás Hormonális szabályozás 2. Az érzékelés Szaglás, tapintás, látás, íz érzéklés, 3. Általános egészségügyi ismeretek az egyes témákhoz
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Klónozás: tökéletesen egyforma szervezetek csoportjának előállítása, vagyis több genetikailag azonos egyed létrehozása.
 Növények klónozása Klónozás Klónozás: tökéletesen egyforma szervezetek csoportjának előállítása, vagyis több genetikailag azonos egyed létrehozása. Görög szó: klon, jelentése: gally, hajtás, vessző. Ami
Növények klónozása Klónozás Klónozás: tökéletesen egyforma szervezetek csoportjának előállítása, vagyis több genetikailag azonos egyed létrehozása. Görög szó: klon, jelentése: gally, hajtás, vessző. Ami
Sejtfeldolgozás Felhasználás
 Sejtterápia Sejtfeldolgozás Felhasználás Fagyasztva tárolás Sejtmosás Alap sejtszelekció Komplex sejtszelekció Ex vivo sejtszaporítás Sejtaktiválás Immunizálás Génmodifikálás Köldökzsinórvér bank Limfocita
Sejtterápia Sejtfeldolgozás Felhasználás Fagyasztva tárolás Sejtmosás Alap sejtszelekció Komplex sejtszelekció Ex vivo sejtszaporítás Sejtaktiválás Immunizálás Génmodifikálás Köldökzsinórvér bank Limfocita
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Vírusellenes szerek. Készítette hidasi Nóra: Gruiz Katalin Környezeti mikrobiológia és biotechnológia c. előadásához
 Vírusellenes szerek Készítette hidasi Nóra: Gruiz Katalin Környezeti mikrobiológia és biotechnológia c. előadásához Vírusok Sejtes szerveződés nélküli szubmikroszkópikus obligát sejtparaziták. Örökítő
Vírusellenes szerek Készítette hidasi Nóra: Gruiz Katalin Környezeti mikrobiológia és biotechnológia c. előadásához Vírusok Sejtes szerveződés nélküli szubmikroszkópikus obligát sejtparaziták. Örökítő
Problémák és lehetőségek a helyreállító gyógyítás területén
 Problémák és lehetőségek a helyreállító gyógyítás területén Sarkadi Balázs MTA-TTK Enzimológiai Intézet, Semmelweis Egyetem 2017. december 13. Fejlett terápiás orvosi készítmények (ATMP): az EMA-CAT szerepe
Problémák és lehetőségek a helyreállító gyógyítás területén Sarkadi Balázs MTA-TTK Enzimológiai Intézet, Semmelweis Egyetem 2017. december 13. Fejlett terápiás orvosi készítmények (ATMP): az EMA-CAT szerepe
Fehérje expressziós rendszerek. Gyógyszerészi Biotechnológia
 Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban
 11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
TÁMOP-4.1.2-08/1/A-2009-0011 Tantárgy címe: Transzdifferenciáció és regeneratív medicina Dr. Balogh Péter és Dr. Engelmann Péter
 Előadás Előadás címe Dia Dia címe száma 1. Őssejtek és transzdifferenciáció: bevezetés, alapok 2. Őssejt-típusok, fenntartásuk és homeosztázisuk 3. Regeneráció állatmodellekben 2. Alapfogalmak 3. Őssejt-kutatás
Előadás Előadás címe Dia Dia címe száma 1. Őssejtek és transzdifferenciáció: bevezetés, alapok 2. Őssejt-típusok, fenntartásuk és homeosztázisuk 3. Regeneráció állatmodellekben 2. Alapfogalmak 3. Őssejt-kutatás
Új terápiás lehetőségek (receptorok) a kardiológiában
 Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Tudománytörténeti visszatekintés
 GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
GLIOMÁK KEZELÉSE CITOKINEKET TERMELŐ TUMORSEJT VAKCINÁCIÓVAL ÉS GYÓGYSZER- ÉRZÉKENYÍTŐ GÉNTERÁPIÁVAL EGÉR TUMOR MODELLEN
 GLIOMÁK KEZELÉSE CITOKINEKET TERMELŐ TUMORSEJT VAKCINÁCIÓVAL ÉS GYÓGYSZER- ÉRZÉKENYÍTŐ GÉNTERÁPIÁVAL EGÉR TUMOR MODELLEN DR. DÉSAKNAI SZILVIA SEMMELWEIS EGYETEM DOKTORI ISKOLA BUDAPEST, 2002 GLIOMÁK KEZELÉSE
GLIOMÁK KEZELÉSE CITOKINEKET TERMELŐ TUMORSEJT VAKCINÁCIÓVAL ÉS GYÓGYSZER- ÉRZÉKENYÍTŐ GÉNTERÁPIÁVAL EGÉR TUMOR MODELLEN DR. DÉSAKNAI SZILVIA SEMMELWEIS EGYETEM DOKTORI ISKOLA BUDAPEST, 2002 GLIOMÁK KEZELÉSE
Az adaptív immunválasz kialakulása. Erdei Anna Immunológiai Tanszék ELTE
 Az adaptív immunválasz kialakulása Erdei Anna Immunológiai Tanszék ELTE NK sejt T Bev. 1. ábra Immunhomeosztázis A veleszületett immunrendszer elemei nélkül nem alakulhat ki az adaptív immunválasz A veleszületett
Az adaptív immunválasz kialakulása Erdei Anna Immunológiai Tanszék ELTE NK sejt T Bev. 1. ábra Immunhomeosztázis A veleszületett immunrendszer elemei nélkül nem alakulhat ki az adaptív immunválasz A veleszületett
Biomolekuláris nanotechnológia. Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium
 Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A gyógyszer-metabolizáló enzimek fenokonverziója, avagy a személyre szabott terápia nehézségei
 A gyógyszer-metabolizáló enzimek fenokonverziója, avagy a személyre szabott terápia nehézségei Monostory Katalin MTA Természettudományi Kutatóközpont Személyre szabott gyógyítás one treatment, one size
A gyógyszer-metabolizáló enzimek fenokonverziója, avagy a személyre szabott terápia nehézségei Monostory Katalin MTA Természettudományi Kutatóközpont Személyre szabott gyógyítás one treatment, one size
Vásárhelyi Barna. Semmelweis Egyetem, Laboratóriumi Medicina Intézet. Az ösztrogénekimmunmoduláns hatásai
 Vásárhelyi Barna Semmelweis Egyetem, Laboratóriumi Medicina Intézet Az ösztrogénekimmunmoduláns hatásai Ösztrogénhatások Ösztrogénhatások Morbiditás és mortalitási profil eltérő nők és férfiak között Autoimmun
Vásárhelyi Barna Semmelweis Egyetem, Laboratóriumi Medicina Intézet Az ösztrogénekimmunmoduláns hatásai Ösztrogénhatások Ösztrogénhatások Morbiditás és mortalitási profil eltérő nők és férfiak között Autoimmun
13. RNS szintézis és splicing
 13. RNS szintézis és splicing 1 Visszatekintés: Az RNS típusai és szerkezete Hírvivő RNS = mrns (messenger RNA = mrna) : fehérjeszintézis pre-mrns érett mrns (intronok kivágódnak = splicing) Transzfer
13. RNS szintézis és splicing 1 Visszatekintés: Az RNS típusai és szerkezete Hírvivő RNS = mrns (messenger RNA = mrna) : fehérjeszintézis pre-mrns érett mrns (intronok kivágódnak = splicing) Transzfer
Dr. Fröhlich Georgina
 Sugárbiol rbiológia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Az ionizáló sugárzás biológiai hatásai - determinisztikus
Sugárbiol rbiológia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Az ionizáló sugárzás biológiai hatásai - determinisztikus
Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter
 Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter Áttekintés Miért éppen a nyuszik? Védekezés módja Vakcina jellemzői Vakcina működése Ráfertőzési
Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter Áttekintés Miért éppen a nyuszik? Védekezés módja Vakcina jellemzői Vakcina működése Ráfertőzési
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
A KOLESZTERIN SZERKEZETE. (koleszterin v. koleszterol)
 19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
