Az antimikrobiális szerek élelmiszertermelő állatokban való alkalmazására vonatkozó legjobb gyakorlat keretei az Európai Unióban
|
|
|
- Erzsébet Balog
- 9 évvel ezelőtt
- Látták:
Átírás
1 Európai Platform az Állatgyógyszerek Felelős Alkalmazásáért Az antimikrobiális szerek élelmiszertermelő állatokban való alkalmazására vonatkozó legjobb gyakorlat keretei az Európai Unióban
2 Tartalomjegyzék Háttér 3 1. Bevezetés 4 2. Mik az antimikrobiális hatóanyagok és milyen formában kerülnek felhasználásra? 5 3. Az állatok egészségének biztosítása 6 4. A betegség kórjelzése és kezelése 8 5. A gyógyszerek hatásos alkalmazása Nyilvántartások vezetése A gyógyszerek jövőbeli hatékonyságának védelme 11 Következtetések 13 2
3 Háttér Az Európai Platform az Állatgyógyszerek Felelős Alkalmazásáért elnevezésű szervezetet [EPRUMA] 2005-ben hozták létre. Küldetése, hogy elősegítse az állatgyógyszerek felelős alkalmazását az Európai Unióban (a 2004/28/EK irányelvvel módosított 2001/82/EK irányelvben meghatározott módon). Az EPRUMA a következő szervezetek érdekeit képviseli: COPA-COGECA (állattartó gazdák és szövetkezetek), EISA (Európai Kezdeményezés a Fenntartható Fejlődéséért a Mezőgazdaságban), FEFAC (takarmánygyártók), FESASS (állattartó gazdák állategészségügyi szervezetei), FVE (állatorvosok) és IFAH Európa (állat-egészségügyi ipar). A jelen dokumentum célja, hogy a legjobb gyakorlatot leíró keretprogram kidolgozásával hozzájáruljon az antimikrobiális szerek hatékonyságának megőrzéséhez. Míg e keretprogram alapelvei kötelező érvénnyel alkalmazandók, a dokumentum az egyes tagállamok konkrét igényeihez igazítható. Ennek eredménye egy, az egész Európai Unióban összehangolt és integrált megközelítés lesz, amely ugyanakkor figyelembe veszi az egyes tagállamok specifikus követelményeit is. Az EPRUMA kezdeményezés célja, hogy a mezőgazdaság területén alkalmazott erőforrások megfontolt alkalmazása tekintetében kiegészítse az EISA Európai IF keretprogramjában 1 leírt Integrált Gazdálkodást (IF) 2. 1 Az EISA egy európai IF keretprogramot dolgozott ki, amely a mezőgazdaság fenntartható fejlesztésére vonatkozó útmutató formájában határozza meg és jellemzi az Integrált Gazdálkodást. 2 Az Integrált Gazdálkodás (IF) egy olyan teljes körű farmirányítási rendszer, amely lefedi és meghaladja a helyes mezőgazdasági és környezeti feltételeknek való együttes megfelelés kereteit, és a gazdálkodás különböző szempontjait felölelve állat-egészségügyi, állatjólléti, élelmiszer-minőségi, élelmiszer-biztonsági és nyomonkövethetőségi, valamint környezetvédelmi biztosítékokat nyújt a gazdák és a fogyasztók számára. 3
4 1. Bevezetés A jó egészség nélkülözhetetlen az állatok jóllétéhez és optimális teljesítményéhez. A betegségek elleni védekezés ezért nélkülözhetetlen része minden sikeres állattartási programnak. Az egészséges állatok ugyanakkor biztonságos élelmiszereket termelnek. Ezért a betegségek elleni védekezés része a kitűnő minőségű élelmiszerek előállításának. Az antimikrobiális gyógyszerek értékes eszközök, melyek nélkülözhetetlenek az állatok egészségének és jóllétének folyamatos biztosításához. E gyógyszerek emellett jelentősen hozzájárulnak a haszonállattartó gazdálkodás termelékenységéhez és hatékonyságához. Az állat-egészségügyi ipar továbbra is a baktériumos eredetű fertőző betegségek kezelésére szolgáló antimikrobiális készítmények széles körével látja el az állatorvosi szakmát és az állattenyésztési ágazatot, és ezek a készítmények a fájdalom és a rossz közérzet megelőzése révén hozzájárulnak az állatok jóllétéhez. Az antimikrobiális gyógyszerek természetéből adódóan rezisztencia alakulhat ki velük szemben, ami csökkenti az adott készítmény hatékonyságát. Ez aláhúzza az antimikrobiális készítmények körültekintő használatának szükségességét. Az antibakteriális hatóanyagokat az EISA keretében leírt helyes telepvezetési gyakorlatot és integrált gazdálkodást (IF), valamint a megfelelően megtervezett vakcinázási programokat kiegészítő módon kell alkalmazni. Számos betegség elkerülhető vagy minimalizálható olyan tartástechnológiai eljárások alkalmazásával, amelyek jelentős mértékben csökkentik a betegségeket előidéző baktériumoknak való kitettséget, ezáltal optimalizálják az állatok tartási környezetét,többek között a jó higiéniai körülmények, a helyes takarmányozás és a megfelelő vakcinázási programok biztosítása révén. 2. Mik az antimikrobiális hatóanyagok és milyen formában kerülnek felhasználásra? Az antimikrobiális szó a legtöbb esetben az antibiotikus szóval azonos értelmű, és a baktériumokat elpusztító vagy azok szaporodását gátló anyagok megjelölésére használják. A legtöbb antimikrobiális anyagot baktériumok és gombák termelik természetes körülmények között, másokat az ember állít elő, de ez utóbbiak is az előbbiekével megegyező hatással rendelkeznek. Míg populárisan az antibiotikum szót használják, az antimikrobiális a helyes szó az ilyen anyagok teljes körének megjelölésére. A legtöbb használatban lévő antimikrobiális hatóanyag még ma is természetes eredetű, és fermentációs eljárásokkal állítják elő azokat. Az először használatra került antimikrobiális anyagok az 1930-as években felfedezett szulfonamidok és a penicillin voltak. Az 1940-es évek végére a gyógyszeripar számos olyan egyedi vegyületet fedezett fel és választott ki, melyek gátolták a baktériumok 4
5 szaporodását vagy elölték azokat így kibővült a rendelkezésre álló antimikrobiális osztályok köre. Jóllehet az azonos osztályba tartozó egyes vegyületek általában hasonló tulajdonságokkal rendelkeznek, a következők tekintetében különbözhetnek egymástól: Hatásspektrum: azok a baktériumfajok, melyekkel szemben az adott antimikrobiális anyag hatásos; Farmakokinetika: az antibiotikum felszívódása és eloszlása a kezelt állat szervezetében, majd az abból történő kiürülése; Toxicitás: egy gyógyszer potenciális ártalmas mellékhatásai. Ma már az antimikrobiális anyagok számos osztálya áll rendelkezésre állatokban való felhasználásra a legkülönbözőbb alkalmazási módokon, például bolusz formában, itatásos szuszpenzió (drench) formájában, a takarmányba keverve, injekcióban adva, tőgyinfúzió formájában, pesszáriumban, helyi kezelésre és az ivóvízben adva. A rendelkezésre álló osztályok az aminoglikozidok, a cephalosporinok, a (fluoro)kinolonok, a makrolidok, a penicillinek, a fenikolok, a pleuromutilinek, a polipeptidek, az ionofórok, a szulfonamidok és a tetraciklinek, hogy csak néhányat említsünk. E családok közül némelyeket kizárólag állat-egészségügyi alkalmazásra fejlesztettek ki. Azt megelőzően, hogy egy állatgyógyszer például egy antimikrobiális szer forgalomba kerülhetne, gyártójának bizonyítania kell a szabályozó hatóságok előtt, hogy az adott készítmény a javasolt felhasználási körülmények között megfelel a minőségi, ártalmatlansági és hatékonysági követelményeknek. Az engedélyezési eljárások szigorúak, és lehetővé teszik, hogy a felhasználó és a fogyasztó bízhasson az engedélyezett gyógyszerekben. A humán gyógyszerekhez hasonlóan az állatgyógyszerek ártalmatlanságát, minőségét és hatékonyságát is a független szabályozó hatóságokat kielégítő módon bizonyítani kell. Az antimikrobiális készítmények forgalomba hozatalának engedélyezése Az engedélyezési folyamat egy rendkívül részletes vizsgálat, amely kiterjed az új készítmény minden szempontjára. A kérelmező cég által a szakhatóságokhoz benyújtott vizsgálati eredményeken és adatokon alapszik. Az engedélyezési folyamat célja a következők biztosítása: Ártalmatlanság: a készítmény ártalmatlan mind a kezelt állatra, mind a kezelt állatoktól származó élelmiszerek fogyasztójára, továbbá a készítménnyel dolgozó személyekre és a környezetre nézve. Minőség: a készítmény egységesen magas minőségű, nem romlandó, és olyan stabilitással rendelkezik, amely biztosítja legalább a lejárati időig történő eltarthatóságát. Hatékonyság: a készítmény hatékonysága megfelel a használati utasításában és a címkeszövegében szereplő állításoknak. Az engedélyezési folyamat azonban nem ér véget ezen a ponton. A fentieken túlmenően a gyógyszerfelhasználóknak részt kell venniük a következő tevékenységben is: Farmakovigilancia (mellékhatás-figyelés): a készítmény mindennapi használata során esetlegesen megfigyelhető mellékhatásokra (nemkívánatos gyógyszerhatásokra) vonatkozó információk szisztematikus gyűjtése. 5
6 Az állatok, a fogyasztók, a felhasználók és a környezet biztonságának folyamatos biztosítása érdekében az egyes országok szakhatóságai folyamatosan ellenőrzik a nemkívánatos maradékanyagok jelenlétét is. Ezen túlmenően sok hatóság ellenőrzi az egyes készítményekből felhasznált mennyiségeket is, és folyamatosan figyeli az antimikrobiális hatóanyagokkal szembeni rezisztencia kialakulását a fontos baktériumok esetében. 3. Az állatok egészségének biztosítása Az állatok egészsége a helyes állattartási gyakorlattal kezdődik. Az állattartó gazdáknak rendszeresen ellenőrizniük kell állataik egész ségét és jóllétét. Szükség esetén megfelelő professzionális állatorvosi tanácsot kell kérniük a betegségek hatékony megelőzésével, kórjelzésével és kezelésével kapcsolatban. Az állatok egészségének e kulcsfontosságú elemei összhangban vannak az EISA integrált gazdálkodási (IF) keretprogramjával, különösen annak IX. fejezetével. Tartástechnológia Az állatok egészsége előfeltétele azok jóllétének. A megfelelő jólléti állapot segít az állatnak megőrizni a betegségekkel szembeni természetes ellenálló képességét, a jó egészség pedig az állat jó közérzetének előfeltétele. Mind az egészséget, mind a jóllétet nagymértékben befolyásolja az állatok tartásának módja, és azoknak összhangban kell lenniük az Európai Unió érvényes jogszabályaival. A környezeti feltételeket többek között a hőmérsékletet, a páratartalmat, a tiszta levegőt és almot, a megvilágítás mértékét stb. az állat igényeihez kell igazítani. Ugyanilyen fontos a tiszta ivóvíz, a megfelelő takarmány, a megfelelő mozgási lehetőség és az elegendő pihenőtér biztosítása. A stresszt el kell kerülni, mert az hátrányosan befolyásolja az állat fertőzésekkel szembeni ellenálló képességét. A fentieken túlmenően az állatok rendszeres ellenőrzése és a megfigyelések nyilvántartása is nélkülözhetetlen az állatok egészségét vagy jóllétét érintő betegségek korai diagnosztizálása érdekében. A jól megtervezett állat-egészségügyi terv minden gazdaság megfelelő működtetésének kulcsfontosságú eleme. Járványvédelem A járványvédelem különösen nagy figyelmet érdemel az állatok fertőző betegségekkel szembeni megvédése szempontjából. A járványvédelem célja, hogy minimálisra csökkentse a betegséget okozó mikroorganizmusok gazdaságba való behurcolásának lehetőségét például újonnan vásárolt állatokkal, a személy- és járműforgalom révén vagy kedvenc állatok közvetítésével, hogy csak néhány behurcolási módot említsünk. Túlzott pénzügyi befektetések nélkül is viszonylag egyszerű intézkedések foganatosíthatók, melyek nagyon hatásosan segíthetik az állatok egészségének biztosítását. Még ha egy intézkedés nem is tűnik teljesen hatásosnak, ez sem jelenti azt, hogy értéktelen lenne. A kórokozók 6
7 behurcolási kockázatának korlátozott mértékű csökkentése még mindig sokkal jobb, mint ha egyáltalán nem csökkentenénk e kockázatot. Vakcinák A vakcinák nagyon értékes eszközök számos fertőző betegség megelőzésében és az ellenük való védekezésben. Biztonságos és hatásos módon erősítik az állatok fertőzésekkel szembeni ellenálló képességét. Van azonban több olyan betegség, amelyek ellen (még) nem állnak rendelkezésre vakcinák. Ezekben az esetekben más megelőzési és védekezési eszközökre többek között állatgyógyszerek, például antibiotikumok alkalmazására lehet szükség. Ez vonatkozik például a következő szituációkra: azonnali kezelést igénylő heveny fertőzések; új betegségek. Mivel a vakcinák a természetes immunrendszeren keresztül fejtik ki hatásukat, használatukat mindig egy szélesebb stratégia összefüggéseiben kell fontolóra venni. A betegségmegelőzési programoknak ugyanolyan fontos részei az egyéb intézkedések például a jó higiénia, a jó tartástechnológia és a betegségfigyelés is. Az optimális stratégia az adott gazdaság helyi szituációjától és más tényezőktől, többek között az állatsűrűségtől, a kórokozók vadon élő állatokban való jelenlététől és a megbízható tesztek elérhetőségétől függ. A vakcinázott állatok megfelelő ellenőrzése a vakcinázási program alapvetően fontos része. Az állatorvos és az állattartó gazda együttműködése (állat-egészségügyi terv) A legkedvezőbb állat-egészségügyi státusz eléréséhez nélkülözhetetlen az állattartó gazda és az állatorvos közötti nyílt kommunikáció. Előnyös, ha erre az eszmecserére rendszeres időközönként, nem pedig csak problémák jelentkezésekor kerül sor. Szükség esetén ki kell kérni más szakértők, például állattartási, takarmányozási és higiéniai szakemberek tanácsát is. 7
8 Az állattartó gazdától kapott információk, valamint az állatok és a helyi körülmények vizsgálatával nyert adatok lehetővé teszik az állatorvos számára, hogy egy, az állatok egészségének és jóllétének fenntartható javítására alkalmas tökéletes megoldást javasoljon. A telepi nyilvántartások is segítenek abban, hogy az állattartó gazda bizonyítani tudja a helyes gazdálkodási gyakorlatnak való megfelelőséget. 4. A betegség kórjelzése és kezelése Ha betegség lép fel, az állatorvos megvizsgálja a beteg állatokat és tartási körülményeiket. A betegségek kórjelzése és kezelése szorosan összefügg egymással. Betegség fellépésekor az állatorvos megvizsgálja az állatot vagy állatokat és tartási körülményeiket. Az így szerzett információk alapján diagnosztizálja a betegséget, és eldönti, hogy milyen beavatkozásra van szükség. Ez a beavatkozás lehet az állatok tartásának módjával (takarmányozás/elhelyezés) kapcsolatos tanács vagy egy megfelelő (antimikrobiális) gyógyszer felírása. Ha szükséges, mintát lehet küldeni egy laboratóriumba a betegséget okozó baktérium pontos azonosítása és antibiotikumérzékenységének meghatározása, és ezek alapján a legmegfelelőbb terápia kiválasztása céljából. Ha azonban a laboratóriumi megerősítés nem lehetséges, az anti mik robiális szerek kiválasztása az állatorvos tapasztalata és klinikai megítélése alapján történik, a kérdéses gazdaságra jellemző korábbi antibiotikum-érzékenységi adatok alapján. Az állatorvos értékeli az általa kiválasztott kezelés eredményeit, és szükség esetén módosítja a kezelést. Az állatokat gyakran csoportosan tartják. Noha ez az állattartási gyakorlat és az állatjóllét szempontjából előnyös, azzal a kockázattal jár, hogy egy betegség fellépésekor az egész állatcsoport ki van téve a megbetegedés veszélyének. Emiatt néha az egész állatcsoportot kezelni kell. Ez például olyan esetekben szükséges, amikor ismert egy fertőző betegség jelenléte, és tapasztalatból tudjuk, hogy a kérdéses kórokozó meg fogja fertőzni a csoport legtöbb vagy akár összes állatát azt követően, hogy egy állatnál már jelentkeztek a fertőzés tünetei. Az ilyen gyógyszerhasználatot néha metafilaxisnak nevezik. A nagy állatállományokban kialakuló baktériumos fertőzések gyakran az állatok életének azonosítható és előre jelezhető szakaszaiban jelentkeznek, a légzőszervi problémák például az átcsoportosítás után, a colibacillosis a választás utáni időszakban, a szállítási betegség a szállítást követően, stb. Az ilyen szituációkban alkalmazott kezelést profilaktikus kezelésnek nevezzük. Az állattartó és az állatorvos tudják, hogy gazdaságukban a betegség kirobbanásának közvetlen veszélye áll fenn, és hogy körültekintő, szelektív és késedelem nélküli intézkedésekre van szükség a betegség megfelelő kezeléséhez. Amint az könnyen belátható, ezek a megelőző intézkedések hasonlóak a humán gyógyászat területén olyan esetekben tett lépésekhez, mint amilyenek például az iskolákban vagy kollégiumokban kialakuló bakteriális eredetű agyhártyagyulladás-járványok, amikor a fertőzésnek potenciálisan kitett diákcsoportot megelőző kezelésben részesítik. Azt követően, hogy az állatorvos eldöntötte, hogy az állatokat valamilyen antimikrobiális szerrel fogja kezelni, először is ki kell választania a legmegfelelőbb készítményt. A következő lépés az adott esetben diagnosztizált betegség kezelésére jóváhagyott 8
9 specifikus gyógyszerkészítmény alkalmazása az állatorvos szakértelme alapján. Egy sor antimikrobiális készítmény áll rendelkezésre, és az állatorvosnak szakmai ismeretei alapján azt a készítményt kell kiválasztania, amely az adott konkrét megbetegedés esetében a legmegfelelőbb hatásspektrummal rendelkezik. (Az idő előrehaladtával több különböző készítményt kell használni az antibiotikum-rezisztencia esetleges kialakulásának megakadályozása céljából.) Ugyanazon típusú javallatra (például légzőszervi betegségek, bélfertőzések vagy szisztémás betegségek ellen) folyamatosan ugyanazt a készítményt használni csak körültekintően szabad, hacsak az előzetesen elvégzett laboratóriumi vizsgálatok nem igazolták az adott betegségeket előidéző baktériumok kielégítő érzékenységét a készítmény iránt. Az állatorvos az idő előrehaladtával több különböző készítményt használhat a rezisztencia esetleges kialakulásának megakadályozására (ezt esetenként rotációs programnak nevezik), hogy biztosítsa a készítmények hosszú távú hatásosságát és minimálisra csökkentse a rezisztencia szelekciós nyomását. Az évek folyamán több új készítmény került forgalomba, és e készítmények tovább gazdagították az állatorvosok terápiás fegyvertárát. Az antimikrobiális szerek kulcsfontosságúak az állatbetegségek kezelése, megelőzése és az azokkal szembeni védekezés tekintetében. Az állatbetegségek kezelésekor az állatorvosok gyakran a betegségek elleni állományszintű védekezésre összpontosítanak. A humán gyógyászatban ugyanakkor az antimikrobiális szerekkel történő kezelés majdnem minden esetben egyedi, vagyis egy betegre irányul. Az antimikrobiális szerek profilaktikus vagy metafilaktikus alkalmazása olyan gyakorlat, amely előnyösnek bizonyult az állományok egészségének fenntartása szempontjából ennek egyik példája a tőgygyulladás kezelése. Az élelmiszertermelő állatok kezelésével foglalkozó állatorvosok számára kulcsfontosságú, hogy egyszerre több hatásos antimikrobiális szer álljon rendelkezésre. Szükséges, hogy az antimikrobiális szerek minden osztályából a biztonságos és hatásos készítmények széles köre álljon az állatorvos rendelkezésére, hogy megakadályozható legyen a rezisztens baktériumtörzsek potenciális kiszelektálódása annak következtében, hogy korlátozott számú készítményt túlzott mértékben használnak. Az állattartó gazdának, az állatorvosnak és más szakértőknek együtt kell dolgozniuk a kezelés megfelelő kimenetelének biztosítása érdekében. Előfordulhat, hogy a további kezeléseket a gazdának kell elvégeznie. Ebben az esetben nagyon fontos, hogy gondosan kövesse az állatorvos utasításait. Be kell számolnia az állatorvosnak minden olyan esetről, amikor váratlanul késik az állatok felgyógyulása. Ha az állat nem a várakozásoknak megfelelően reagál az alkalmazott kezelésre, szükség esetén valamilyen más formájú (alternatív) kezelést kell kezdeni. A végső választás az állatorvos feladata Ma az antimikrobiális szerek széles köre van forgalomban. Ezek számos tekintetben például az alkalmazási mód, az állat által való felvétel sebessége és mértéke, a hatásmechanizmus, a szövetekbe való behatolás sebessége és mértéke különböznek egymástól. Ugyanakkor a mikroorganizmusok között is eltérések vannak abban a tekintetben, hogy a különböző antimikrobiális szerek hogyan hatnak rájuk. Ezért az alkalmazandó antimikrobiális szer kiválasztásakor több kritériumot is figyelembe kell venni, például az állatot vagy állatokat megbetegítő mikroorganizmusok típusát, az antimikrobiális szerekkel szembeni rezisztencia előfordulását, az állatfajt, az antimikrobiális szer alkalmazásának módját stb. A megfelelő kezelést mindig az állatorvosnak kell kiválasztania az állatok és a helyi körülmények vizsgálatát és a diagnózis felállítását követően. 9
10 Kaszkád Kivételes esetekben, amikor egyetlen gyógyszer sincs engedélyezve, fennáll a lehetősége annak, hogy az állatorvos például az Európai Unió más országaiban vagy más állatfajok kezelésére engedélyezett készítményeket használjon. Ez a kivétel azért létezik, hogy az állatok elfogadhatatlan szenvedése megakadályozható legyen. Ezekben az esetekben az állatorvosnak konkrétan meghatározott lépéseket az úgynevezett kaszkádot kell követnie, és biztosítania kell, hogy az alkalmazott kezelés nem jár kockázattal az érintett állatokra és az állati eredetű élelmiszerek fogyasztóira nézve. 5. A gyógyszerek hatásos alkalmazása A kezelés sikerét az antimikrobiális szer megfelelő beadása és a helyes dózisnak a szükséges időn keresztül történő alkalmazása határozza meg. Az antimikrobiális gyógyszerek ajánlott adagolását a forgalomba hozatali engedélyért folyamodó cég részletesen vizsgálja a kérelem benyújtása előtt. A cél annak biztosítása, hogy az alkalmazott adag elég nagy legyen ahhoz, hogy az antimikrobiális szer megfelelő mennyiségben eljusson a fertőzés helyére és ott elég hosszú ideig megmaradjon, így biztosítva az állat felgyógyulását az adott betegségből. A klinikai siker eléréséhez a gyógyszer ismételt alkalmazására lehet szükség. Az emberorvoslás területén ez például úgy valósítható meg, hogy naponta háromszor egy tablettát veszünk be hét napon át. Ugyanez az elv vonatkozik az állatok kezelésére is. Akárcsak a humán gyógyszerek esetében, az állatgyógyszereknél is a címke tartalmazza a megfelelő és biztonságos alkalmazáshoz és tároláshoz szükséges információkat. Maximálisan megengedett maradékanyag-határérték (MRL) Élelmiszertermelő állatok esetében vizsgálatokra van szükség annak meghatározására, hogy a gyógyszer maradékanyagai milyen gyorsan ürülnek ki a kezelt állat szervezetéből. A maximálisan megengedett maradékanyag-határértékek (MRL) az antimikrobiális szer azon maximális szintjét fejezik ki, amely az állat szervezetében maradhat anélkül, hogy kockázatot jelentene az állatból előállított élelmiszerek fogyasztóira. Ezt követően meghatározzák az élelmezés-egészségügyi várakozási időt (a gyógyszer beadása és az állat levágása vagy az élelmiszer például a tej vagy a tojás nyerése között eltelt időt) annak biztosítása érdekében, hogy az esetlegesen az állat szervezetében viszszamaradó maradékanyagok mennyisége az MRL alatt van. A fogyasztók védelme érdekében nagyon széles biztonsági sávokat építenek be a rendszerbe. 10
11 6. Nyilvántartások vezetése A nyilvántartások vezetése tekintetében az Európai Unió minden tagállamában kötelező legalább öt évig megőrizni az élelmiszertermelő állatok kezelésére használt minden gyógyszerre többek között az antimikrobiális kezelésekre vonatkozó adatokat, függetlenül attól, hogy a kezelt állat még a gazdaságban van-e vagy sem. Ezen túlmenően az is ajánlott, hogy az állatorvos az állattartó gazdával együttműködve nyomon kövesse az adott gazdaságban jelentkezett fertőző betegségekkel kapcsolatos adatok összességét. A történeti adatok a laboratóriumi antibiotikum-érzékenységi vizsgálatok eredményeit is beleértve nagyon értékesek a jövőbeli kezelések megtervezésekor. A gyógyszerek biztonságos szállítása, tárolása és ártalmatlanná tétele tekintetében minden esetben be kell tartani a hatályos jogszabályi követelményeket. A nyilvántartásokból képet kaphatunk az antimikrobiális szereknek a gazdaságban történő folyamatos alkalmazásáról. A tendenciákat meg kell figyelni és a gyógyszerhasználatban bekövetkező változásokat meg kell vizsgálni. A gazdaság általános tartástechnológiai viszonyait folyamatos ellenőrzés alatt kell tartani. 7. A gyógyszerek jövőbeli hatékonyságának védelme A farmakovigilancia az a folyamat, melynek során a gyógyszerek ártalmatlanságával vagy hatékonyságával kapcsolatos aggályokat bejelentik az adott ország szakhatóságainak. Ha aggály merül fel, az állattartó gazdának ki kell kérnie az állatorvos tanácsát, és az esetről jelentést kell küldenie a hatóságoknak, ha az állatorvos azt gyanítja, hogy ártalmatlansági vagy hatékonysági probléma merült fel. E rendszer nagyon előnyös, mert lehetővé teszi a használatban lévő készítmények folyamatos ellenőrzését valós üzemi körülmények között. Az antibiotikum-érzékenység folyamatos ellenőrzése az állategészségügyi ipar által A rezisztencia az a jelenség, amikor egyes baktériumok többé már nem érzékenyek egy adott antibiotikummal való kezelés iránt. Ezért nagyon fontos a baktériumok antimikrobiális szerek iránti érzékenységének folyamatos nyomon követése. Az érzékenység folyamatos ellenőrzése egy összetett művelet, amely magában foglalja a reprezentatív minták gyűjtését és az eredmények egységes módszerekkel való értékelését. Ebben a tevékenységben a szabályozó hatóságokkal vagy a kormányzati hatóságokkal egyidejűleg részt vesz az állat-egészségügyi (állatgyógyszer-) ipar is. A rezisztenciaszintekre vonatkozó információk közlése lehetővé teszi az állatorvosok számára, hogy a szükséges információk birtokában hozzanak döntéseket azzal kapcsolatban, hogy mely antimikrobiális szereket lehet a siker legnagyobb esélyével használni. Az állati termelés területén kialakuló antibiotikumrezisztencia nyomon követésének emellett közegészségügyi jelentősége is van. 11
12 A rezisztencia kialakulása Az antimikrobiális szerek bizonyos baktériumfajok vagy fajcsoportok ellen fejtik ki hatásukat. Egy adott készítménynek egy adott baktériummal szembeni hatásosságát klinikai vizsgálatokkal bizonyítják. Kezdetben nagy hatékonyságot mutató eredményeket kell elérni. Minden baktériumpopuláció különböző baktériumegyedekből állhat azonban, melyek egymástól kissé eltérő genetikai tulajdonságokkal rendelkeznek. Néhány baktériumnak, amely a teljes baktériumpopuláció kis hányadát teszi ki, természetes képessége lehet arra, hogy túlélje az antimikrobiális szerrel végzett kezelést. Ennek eredményeképpen a rezisztens baktériumok életben maradnak, majd az idő előrehaladtával és az antimikrobiális szer használata miatt kialakuló szelekciós nyomás hatására a baktériumpopuláció egyre dominánsabb részévé válnak. Az idő előrehaladtával a kezelés hatásossága egyre csökkenhet, míg végül bekövetkezik az a helyzet, amikor a készítmény már nem képes hatékony védelmet nyújtani a betegség ellen. Ez az a pont, amikor kialakul a klinikai rezisztencia. Amint az könnyen belátható, a rezisztencia kialakulása rendszerint egy fokozatos folyamat, melynek során a minták idővel egyre nagyobb mértékű rezisztenciát mutatnak, noha egyes esetekben az antimikrobiális szerek több évtizeden át hatásosak maradhatnak. A fenti folyamat alternatívájaként a baktériumok mutálódhatnak vagy más baktériumok genetikai anyagát vehetik át, és így tesznek szert a kezelés túléléséhez szükséges képességre. Ebben az esetben az érzékenység és a rezisztencia közötti váltás viszonylag gyors Az idő előrehaladtával a kezelés hatásossága egyre csökkenhet, míg végül bekövetkezik az a helyzet, amikor a készítmény már nem képes hatékony védelmet nyújtani a betegség ellen. Ez az a pont, amikor kialakul a klinikai rezisztencia. Amint az könnyen belátható, a rezisztencia kialakulása rendszerint egy fokozatos folyamat, melynek során a minták idővel egyre nagyobb mértékű rezisztenciát mutatnak, noha egyes esetekben az antimikrobiális szerek több évtizeden át hatásosak maradhatnak. A fenti folyamat alternatívájaként a baktériumok mutálódhatnak vagy más baktériumok genetikai anyagát vehetik át, és így tesznek szert a kezelés túléléséhez szükséges képességre. Ebben az esetben az érzékenység és a rezisztencia közötti váltás viszonylag gyors lehet, ha a rezisztens baktériumok gyorsan szaporodnak és terjednek. A rezisztencia az esetek legnagyobb részében ez utóbbi folyamat révén alakul ki. Miután rezisztenssé váltak az antimikrobiális szerek egy adott típusával szemben, a baktériumok rezisztensek lehetnek az ugyanabba az osztályba tartozó rokon antimikrobiális szerekkel szemben is. Egyes esetekben a baktériumok az antimikrobiális szerek több különböző osztályával szemben is rezisztenssé válhatnak, vagyis multirezisztenciára tehetnek szert. 12
13 Következtetések Az antimikrobiális szerek kulcsfontosságú szerepet játszanak az állatok egészségének és jóllétének megvédésében. Az állatok betegségekkel szembeni megvédésével hozzájárulnak ahhoz, hogy az egészséges állatok kitűnő minőségű élelmiszereket termeljenek, ugyanakkor minimalizálják a környezet terhelését. E gyógyszerek forgalomba hozatalát egy átfogó engedélyezési folyamat előzi meg. Az állatorvosok rendelkeznek azokkal a szükséges részletes ismeretekkel, melyek birtokában ki tudják választani a legmegfelelőbb gyógyszereket és biztosítani tudják azok biztonságos használatát. Az állattartó gazdának kulcsszerepe van a betegségek megelőzésében és az antimikrobiális szerek helyes használatának biztosításában. Több mint 60 évvel ezelőtti bevezetésük óta az antimikrobiális szerek forradalmasították az állatorvosi gyakorlatot. E korai gyógyszerek közül sokat még ma is sikeresen használnak, jóllehet a rezisztencia kialakulása miatti hatékonyságcsökkenés kockázatával mindig számolni kell. Nélkülözhetetlen, hogy minden érintett fél együtt dolgozzon az antimikrobiális szerek biztonságos használatának biztosítása és a rezisztencia kialakulásának minimalizálása érdekében. Az antimikrobiális szerek használata tekintetében a vezérelv a lehető legkevesebbet, annyit, amennyi szükséges kell legyen, mivel mind a jelen, mind a jövő nemzedékeknek tartozunk azzal, hogy ezeket a szereket óvatosan és körültekintően használjuk. Ha így járunk el, ezek az értékes gyógyszerek a jövő generációknak is ugyanolyan előnyöket nyújtanak majd, mint amilyeneket nekünk nyújtanak. 13
14 Az EPRUMA tagszervezetei COPA-COGECA European Farmers and Agri-Cooperatives [Európai Gazdák és Mezőgazdasági Szövetkezetek] EISA European Initiative for Sustainable Development in Agriculture [Európai Kezdeményezés a Fenntartható Fejlődéséért a Mezőgazdaságban] FEFAC European Feed Manufacturers Federation [Európai Takarmánygyártók Szövetsége] FESASS European Federation for Animal Health and Sanitary Security [Európai Szövetség az Állategészségügyért és a Higiéniai Biztonságért] FVE Federation of Veterinarians of Europe [Európai Állatorvosok Szövetsége] IFAH EUROPE International Federation for Animal Health Europe [Nemzetközi Állat-egészségügyi Szövetség Európa] EPRUMA c/o IFAH-Europe AISBL Rue Defacqz, Brüsszel, Belgium Telefon: Fax: info@epruma.eu 14
I.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 I.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Aivlosin 42,5 mg/g gyógypremix sertések részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag: Tilvalozin
I.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Aivlosin 42,5 mg/g gyógypremix sertések részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag: Tilvalozin
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA. Coxevac d232 PI HU 2010-09-06 clean.doc
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE COXEVAC szuszpenziós injekció szarvasmarhának és kecskének 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml tartalmaz:
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE COXEVAC szuszpenziós injekció szarvasmarhának és kecskének 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml tartalmaz:
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Semicillin 250 mg kapszula BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Semicillin 250 mg kapszula BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
12/2001. (V. 4.) KöM EüM együttes rendelet. a vegyi anyagok kockázatának becsléséről és a kockázat csökkentéséről. A rendelet hatálya
 12/2001. (V. 4.) KöM EüM együttes rendelet a vegyi anyagok kockázatának becsléséről és a kockázat csökkentéséről A környezetvédelmi miniszter és az egészségügyi miniszter a kémiai biztonságról szóló 2000.
12/2001. (V. 4.) KöM EüM együttes rendelet a vegyi anyagok kockázatának becsléséről és a kockázat csökkentéséről A környezetvédelmi miniszter és az egészségügyi miniszter a kémiai biztonságról szóló 2000.
AZ ÁLLATGENETIKAI EROFORRÁSOKRA VONATKOZÓ GLOBÁLIS CSELEKVÉSI TERV és AZ INTERLAKENI NYILATKOZAT
 AZ ÁLLATGENETIKAI EROFORRÁSOKRA VONATKOZÓ GLOBÁLIS CSELEKVÉSI TERV és AZ INTERLAKENI NYILATKOZAT ÉLELMEZÉSI ÉS MEZOGAZDASÁGI CÉLÚ GENETIKAI EROFORRÁSOK BIZOTTSÁGA AZ ÁLLATGENETIKAI ERŐFORRÁSOKRA VONATKOZÓ
AZ ÁLLATGENETIKAI EROFORRÁSOKRA VONATKOZÓ GLOBÁLIS CSELEKVÉSI TERV és AZ INTERLAKENI NYILATKOZAT ÉLELMEZÉSI ÉS MEZOGAZDASÁGI CÉLÚ GENETIKAI EROFORRÁSOK BIZOTTSÁGA AZ ÁLLATGENETIKAI ERŐFORRÁSOKRA VONATKOZÓ
(Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ KÖZLEMÉNYEK BIZOTTSÁG
 2009.5.9. Az Európai Unió Hivatalos Lapja C 107/1 II (Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ KÖZLEMÉNYEK BIZOTTSÁG A Bizottság Közleménye Italok csomagolása, betétdíjas rendszerek
2009.5.9. Az Európai Unió Hivatalos Lapja C 107/1 II (Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ KÖZLEMÉNYEK BIZOTTSÁG A Bizottság Közleménye Italok csomagolása, betétdíjas rendszerek
ÚTMUTATÓ NYÍLT KÖZBESZERZÉSI ELJÁRÁSOK AJÁNLATI FELHÍVÁSÁHOZ
 ÚTMUTATÓ NYÍLT KÖZBESZERZÉSI ELJÁRÁSOK AJÁNLATI FELHÍVÁSÁHOZ 1 / 69 ÚTMUTATÓ NYÍLT KÖZBESZERZÉSI ELJÁRÁSOK AJÁNLATI FELHÍVÁSÁHOZ Az alábbi útmutató nyújt segítséget, iránymutatást és javaslatokat a Kbt.
ÚTMUTATÓ NYÍLT KÖZBESZERZÉSI ELJÁRÁSOK AJÁNLATI FELHÍVÁSÁHOZ 1 / 69 ÚTMUTATÓ NYÍLT KÖZBESZERZÉSI ELJÁRÁSOK AJÁNLATI FELHÍVÁSÁHOZ Az alábbi útmutató nyújt segítséget, iránymutatást és javaslatokat a Kbt.
Normaflore Max 6 milliárd
 Gyógyszerészeti és Egészségügyi Minőség- és Nyilvános Értékelő Jelentés Gyógyszernév: 6 milliárd por többszörösen antibiotikum-rezisztens Bacillus clausii spóra Nemzeti eljárás A forgalomba hozatali engedély
Gyógyszerészeti és Egészségügyi Minőség- és Nyilvános Értékelő Jelentés Gyógyszernév: 6 milliárd por többszörösen antibiotikum-rezisztens Bacillus clausii spóra Nemzeti eljárás A forgalomba hozatali engedély
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Meloxidyl 1,5 mg/ml belsőleges szuszpenzió kutyáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml tartalmaz
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Meloxidyl 1,5 mg/ml belsőleges szuszpenzió kutyáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml tartalmaz
TANÁCS. (Tájékoztatások)
 2006.11.14. C 276E/1 I (Tájékoztatások) TANÁCS 17/2006/EK KÖZÖS ÁLLÁSPONT (a Tanács által 2006. június 27-én elfogadva) a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról
2006.11.14. C 276E/1 I (Tájékoztatások) TANÁCS 17/2006/EK KÖZÖS ÁLLÁSPONT (a Tanács által 2006. június 27-én elfogadva) a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról
Mometazon furoát (monohidrát formájában)
 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Posatex szuszpenziós fülcsepp kutyák részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyagok: Orbifloxacin Mometazon furoát (monohidrát formájában) Posakonazol 8,5
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Posatex szuszpenziós fülcsepp kutyák részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyagok: Orbifloxacin Mometazon furoát (monohidrát formájában) Posakonazol 8,5
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA. Aktil Duo 400 mg/57mg/5 ml por belsoleges szuszpenzióhoz. amoxicillin/klavulánsav
 Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Aktil Duo 400 mg/57mg/5 ml por belsoleges szuszpenzióhoz amoxicillin/klavulánsav
Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Aktil Duo 400 mg/57mg/5 ml por belsoleges szuszpenzióhoz amoxicillin/klavulánsav
AZ EURÓPAI U IÓ TA ÁCSA. Brüsszel, 2008. augusztus 20. (OR. en) 11119/08 Intézményközi referenciaszám: 2006/0136 (COD) AGRILEG 116 E V 407 CODEC 867
 AZ EURÓPAI U IÓ TA ÁCSA Brüsszel, 2008. augusztus 20. (OR. en) 11119/08 Intézményközi referenciaszám: 2006/0136 (COD) AGRILEG 116 E V 407 CODEC 867 JOGI AKTUSOK ÉS EGYÉB ESZKÖZÖK Tárgy: A TANÁCS ÁLTAL
AZ EURÓPAI U IÓ TA ÁCSA Brüsszel, 2008. augusztus 20. (OR. en) 11119/08 Intézményközi referenciaszám: 2006/0136 (COD) AGRILEG 116 E V 407 CODEC 867 JOGI AKTUSOK ÉS EGYÉB ESZKÖZÖK Tárgy: A TANÁCS ÁLTAL
www.printo.it/pediatric-rheumatology/hu/intro
 www.printo.it/pediatric-rheumatology/hu/intro PAPA Szindróma Verzió 2016 1. MI A PAPA SZINDRÓMA 1.1 Mi ez? A PAPA a pyogen arthritis, pyoderma gangrenosum és acne" (gennykeltő ízületi gyulladás, üszkös
www.printo.it/pediatric-rheumatology/hu/intro PAPA Szindróma Verzió 2016 1. MI A PAPA SZINDRÓMA 1.1 Mi ez? A PAPA a pyogen arthritis, pyoderma gangrenosum és acne" (gennykeltő ízületi gyulladás, üszkös
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Tetran
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Tetran
Kemény kapszula Fehér, átlátszatlan kemény kapsula, a kapszula alsó részén CYSTAGON 150, felső részén MYLAN felirattal.
 1. A GYÓGYSZER MEGNEVEZÉSE CYSTAGON 150 mg kemény kapszula 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy kemény kapszula 150 mg ciszteamin-bitartarátot tartalmaz (merkaptamin-bitartarát formájában). A segédanyagok
1. A GYÓGYSZER MEGNEVEZÉSE CYSTAGON 150 mg kemény kapszula 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy kemény kapszula 150 mg ciszteamin-bitartarátot tartalmaz (merkaptamin-bitartarát formájában). A segédanyagok
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA. Javaslat: A TANÁCS IRÁNYELVE
 HU HU HU AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 28.4.2005 COM(2005) 171 végleges 2005/0062 (CNS) 2005/0063 (CNS) Javaslat: A TANÁCS IRÁNYELVE a madárinfluenza (klasszikus baromfipestis) elleni védekezésre
HU HU HU AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 28.4.2005 COM(2005) 171 végleges 2005/0062 (CNS) 2005/0063 (CNS) Javaslat: A TANÁCS IRÁNYELVE a madárinfluenza (klasszikus baromfipestis) elleni védekezésre
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA. Javaslat: AZ EURÓPAI PARLAMENT ÉS A TANÁCS / /EK RENDELETE. (ÉÉÉÉ. hónap NN.)
 AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 30.1.2009 COM(2009) 31 végleges 2009/0006 (COD) C6-0048/09 Javaslat: AZ EURÓPAI PARLAMENT ÉS A TANÁCS / /EK RENDELETE (ÉÉÉÉ. hónap NN.) a textiltermékek elnevezéséről
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 30.1.2009 COM(2009) 31 végleges 2009/0006 (COD) C6-0048/09 Javaslat: AZ EURÓPAI PARLAMENT ÉS A TANÁCS / /EK RENDELETE (ÉÉÉÉ. hónap NN.) a textiltermékek elnevezéséről
5.10. GYÓGYSZERANYAGOK SZENNYEZÉSVIZSGÁLATA
 5.10. Gyógyszeranyagok szennyezésvizsgálata Ph.Hg.VIII. Ph.Eur.6.5-1 Bevezetés 5.10. GYÓGYSZERANYAGOK SZENNYEZÉSVIZSGÁLATA 01/2008:51000 javított 6.5 Az Európai Gyógyszerkönyv gyógyszeranyag-cikkelyeit
5.10. Gyógyszeranyagok szennyezésvizsgálata Ph.Hg.VIII. Ph.Eur.6.5-1 Bevezetés 5.10. GYÓGYSZERANYAGOK SZENNYEZÉSVIZSGÁLATA 01/2008:51000 javított 6.5 Az Európai Gyógyszerkönyv gyógyszeranyag-cikkelyeit
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK AZ OLTANDÓK SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK AZ OLTANDÓK SZÁMÁRA Tetanol pur szuszpenziós injekció előretöltött fecskendőben adszorbeált tetanusz toxoid vakcina, tartósítószer nélkül Mielőtt beadnák Önnek ezt a vakcinát,
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK AZ OLTANDÓK SZÁMÁRA Tetanol pur szuszpenziós injekció előretöltött fecskendőben adszorbeált tetanusz toxoid vakcina, tartósítószer nélkül Mielőtt beadnák Önnek ezt a vakcinát,
Betegtájékoztató: Információk a felhasználó számára. Rabipur por és oldószer oldatos injekcióhoz Inaktivált veszettség elleni vakcina
 Betegtájékoztató: Információk a felhasználó számára Rabipur por és oldószer oldatos injekcióhoz Inaktivált veszettség elleni vakcina Mielőtt beadnák Önnek vagy gyermekének a Rabipur-t, olvassa el figyelmesen
Betegtájékoztató: Információk a felhasználó számára Rabipur por és oldószer oldatos injekcióhoz Inaktivált veszettség elleni vakcina Mielőtt beadnák Önnek vagy gyermekének a Rabipur-t, olvassa el figyelmesen
II. melléklet. Az EMA által beterjesztett tudományos következtetések, valamint a termékek forgalmazása és alkalmazása felfüggesztésének indokolása
 II. melléklet Az EMA által beterjesztett tudományos következtetések, valamint a termékek forgalmazása és alkalmazása felfüggesztésének indokolása 14 Tudományos következtetések A buflomedilt tartalmazó
II. melléklet Az EMA által beterjesztett tudományos következtetések, valamint a termékek forgalmazása és alkalmazása felfüggesztésének indokolása 14 Tudományos következtetések A buflomedilt tartalmazó
SEGÉDANYAG: Amagen 1 mg tabletta: vörös vas-oxid (E172), povidon, magnézium-sztearát, A típusú karboximetil-keményítõnátrium,
 AMAGEN 4 MG TABLETTA Amagen 1 mg tabletta Amagen 2 mg tabletta Amagen 3 mg tabletta Amagen 4 mg tabletta glimepiride HATÓANYAG: Amagen 1 mg tabletta: 1 mg glimepirid tablettánként. Amagen 2 mg tabletta:
AMAGEN 4 MG TABLETTA Amagen 1 mg tabletta Amagen 2 mg tabletta Amagen 3 mg tabletta Amagen 4 mg tabletta glimepiride HATÓANYAG: Amagen 1 mg tabletta: 1 mg glimepirid tablettánként. Amagen 2 mg tabletta:
(Nem jogalkotási aktusok) RENDELETEK
 2013.6.8. Az Európai Unió Hivatalos Lapja L 157/1 II (Nem jogalkotási aktusok) RENDELETEK A BIZOTTSÁG 503/2013/EU VÉGREHAJTÁSI RENDELETE (2013. április 3.) a géntechnológiával módosított élelmiszerek és
2013.6.8. Az Európai Unió Hivatalos Lapja L 157/1 II (Nem jogalkotási aktusok) RENDELETEK A BIZOTTSÁG 503/2013/EU VÉGREHAJTÁSI RENDELETE (2013. április 3.) a géntechnológiával módosított élelmiszerek és
A Pradaxa egy dabigatrán etexilát nevű hatóanyagot tartalmazó gyógyszer. Kapszula formájában kapható (75, 110 és 150 mg).
 EMEA/H/C/000829 EPAR-összefoglaló a nyilvánosság számára dabigatrán etexilát Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi felhasználásra
EMEA/H/C/000829 EPAR-összefoglaló a nyilvánosság számára dabigatrán etexilát Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi felhasználásra
50/2006. (VI. 28.) FVM rendelet. az állatgyógyászati készítményekről. Általános rendelkezések
 50/2006. (VI. 28.) FVM rendelet az állatgyógyászati készítményekről Az állategészségügyről szóló 2005. évi CLXXVI. törvény (a továbbiakban: Áeü.) 47. -a (2) bekezdésének 10. pontjában, a gyógyszertárak
50/2006. (VI. 28.) FVM rendelet az állatgyógyászati készítményekről Az állategészségügyről szóló 2005. évi CLXXVI. törvény (a továbbiakban: Áeü.) 47. -a (2) bekezdésének 10. pontjában, a gyógyszertárak
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA. Augmentin 500 mg/125 mg filmtabletta. amoxicillin/klavulánsav
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Augmentin 500 mg/125 mg filmtabletta amoxicillin/klavulánsav Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót.
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Augmentin 500 mg/125 mg filmtabletta amoxicillin/klavulánsav Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót.
5.2.6 ÁLLATGYÓGYÁSZATI VAKCINÁK ÉS IMMUNSZÉRUMOK ÁRTALMATLANSÁGÁNAK ÉRTÉKELÉSE
 5.2.6 ÁLLATGYÓGYÁSZATI VAKCINÁK ÉS IMMUNSZÉRUMOK ÁRTALMATLANSÁGÁNAK ÉRTÉKELÉSE A készítmény kifejezés alatt a teljes szövegben vakcina, illetve immunszérum értendő. 04/2013:50206 A készítményfejlesztés
5.2.6 ÁLLATGYÓGYÁSZATI VAKCINÁK ÉS IMMUNSZÉRUMOK ÁRTALMATLANSÁGÁNAK ÉRTÉKELÉSE A készítmény kifejezés alatt a teljes szövegben vakcina, illetve immunszérum értendő. 04/2013:50206 A készítményfejlesztés
ÖKOLÓGIAI NÖVÉNYTERMESZTÉS, VADON TERMŐ NÖVÉNYEK GYŰJTÉSE ÉS GOMBATERMESZTÉS
 ÖKOLÓGIAI NÖVÉNYTERMESZTÉS, VADON TERMŐ NÖVÉNYEK GYŰJTÉSE ÉS GOMBATERMESZTÉS A következőkben a biotermékek előállítását, jelölését és ellenőrzését szabályozó 834/2007/EK és 889/2008/EK rendeletek fontosabb
ÖKOLÓGIAI NÖVÉNYTERMESZTÉS, VADON TERMŐ NÖVÉNYEK GYŰJTÉSE ÉS GOMBATERMESZTÉS A következőkben a biotermékek előállítását, jelölését és ellenőrzését szabályozó 834/2007/EK és 889/2008/EK rendeletek fontosabb
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA. Sotalol AL 80 mg tabletta Sotalol AL 160 mg tabletta. szotalol hidroklorid
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Sotalol AL 80 mg tabletta Sotalol AL 160 mg tabletta szotalol hidroklorid Mielott elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Sotalol AL 80 mg tabletta Sotalol AL 160 mg tabletta szotalol hidroklorid Mielott elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi
Flexove 625 mg Tabletta Szájon át történő alkalmazás 1327 Lysaker, Norvégia Belgium - Navamedic ASA Vollsveien 13 C 1327 Lysaker, Norvégia
 I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN 1 Tagállam Forgalomba hozatali engedély
I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN 1 Tagállam Forgalomba hozatali engedély
A vemhes kancák és a csikók fontosabb féregélősködők okozta fertőzöttségei
 A vemhes kancák és a csikók fontosabb féregélősködők okozta fertőzöttségei Farkas Róbert SZIE ÁOTK Parazitológiai és Állattani Tanszék, 1078 Budapest, István u. 2. Farkas.Robert@aotk.szie.hu Az utóbbi
A vemhes kancák és a csikók fontosabb féregélősködők okozta fertőzöttségei Farkas Róbert SZIE ÁOTK Parazitológiai és Állattani Tanszék, 1078 Budapest, István u. 2. Farkas.Robert@aotk.szie.hu Az utóbbi
1. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/17
 1. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/17 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Meloxicam CEVA 1,5 mg/ml belsőleges szuszpenzió kutyáknak. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml
1. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/17 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Meloxicam CEVA 1,5 mg/ml belsőleges szuszpenzió kutyáknak. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml
Betegtájékoztató: Információk a felhasználó számára. Augmentin DUO 875 mg/125 mg filmtabletta. amoxicillin/klavulánsav
 Betegtájékoztató: Információk a felhasználó számára Augmentin DUO 875 mg/125 mg filmtabletta amoxicillin/klavulánsav Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
Betegtájékoztató: Információk a felhasználó számára Augmentin DUO 875 mg/125 mg filmtabletta amoxicillin/klavulánsav Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
MÓDOSÍTÁS: 1-239. HU Egyesülve a sokféleségben HU 2013/2022(INI) 18.7.2013. Jelentéstervezet Oreste Rossi (PE510.691v02-00)
 EURÓPAI PARLAMENT 2009-2014 Környezetvédelmi, Közegészségügyi és Élelmiszer-biztonsági Bizottság 18.7.2013 2013/2022(INI) MÓDOSÍTÁS: 1-239 Jelentéstervezet (PE510.691v02-00) az egészségügyi ellátással
EURÓPAI PARLAMENT 2009-2014 Környezetvédelmi, Közegészségügyi és Élelmiszer-biztonsági Bizottság 18.7.2013 2013/2022(INI) MÓDOSÍTÁS: 1-239 Jelentéstervezet (PE510.691v02-00) az egészségügyi ellátással
Humán inzulin, rdns (rekombináns DNS technológiával, Saccharomyces cerevisiae-ben előállított).
 1. A GYÓGYSZER MEGNEVEZÉSE Actraphane 30 InnoLet 100 NE/ml szuszpenziós injekció előretöltött injekciós tollban 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán inzulin, rdns (rekombináns DNS technológiával,
1. A GYÓGYSZER MEGNEVEZÉSE Actraphane 30 InnoLet 100 NE/ml szuszpenziós injekció előretöltött injekciós tollban 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán inzulin, rdns (rekombináns DNS technológiával,
Betegtájékoztató RYTMONORM 300 MG FILMTABLETTA. Rytmonorm 150 mg filmtabletta Rytmonorm 300 mg filmtabletta propafenon-hidroklorid
 RYTMONORM 300 MG FILMTABLETTA Rytmonorm 150 mg filmtabletta Rytmonorm 300 mg filmtabletta propafenon-hidroklorid HATÓANYAG: 150 mg propafenon-hidroklorid ill. 300 mg propafenon-hidroklorid filmtablettánként.
RYTMONORM 300 MG FILMTABLETTA Rytmonorm 150 mg filmtabletta Rytmonorm 300 mg filmtabletta propafenon-hidroklorid HATÓANYAG: 150 mg propafenon-hidroklorid ill. 300 mg propafenon-hidroklorid filmtablettánként.
AZ EURÓPAI PARLAMENT ÉS A TANÁCS IRÁNYELVE (2001. november 6.) az emberi felhasználásra szánt gyógyszerek közösségi kódexéről (2001/83/EK)
 2001L0083 HU 05.10.2009 008.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B AZ EURÓPAI PARLAMENT ÉS A TANÁCS IRÁNYELVE (2001. november
2001L0083 HU 05.10.2009 008.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B AZ EURÓPAI PARLAMENT ÉS A TANÁCS IRÁNYELVE (2001. november
Javaslat AZ EURÓPAI PARLAMENT ÉS A TANÁCS RENDELETE. az állategészségügyről. {SWD(2013) 160 final} {SWD(2013) 161 final}
 EURÓPAI BIZOTTSÁG Brüsszel, 2013.5.6. COM(2013) 260 final 2013/0136 (COD) Javaslat AZ EURÓPAI PARLAMENT ÉS A TANÁCS RENDELETE az állategészségügyről {SWD(2013) 160 final} {SWD(2013) 161 final} HU HU 1.
EURÓPAI BIZOTTSÁG Brüsszel, 2013.5.6. COM(2013) 260 final 2013/0136 (COD) Javaslat AZ EURÓPAI PARLAMENT ÉS A TANÁCS RENDELETE az állategészségügyről {SWD(2013) 160 final} {SWD(2013) 161 final} HU HU 1.
Leukémia (fehérvérûség)
 Leukémia (fehérvérûség) Leukémia - fehérvérûség A leukémia a rosszindulatú rákos megbetegedések azon formája, amely a vérképzõ sejtekbõl indul ki. A leukémia a csontvelõben lévõ éretlen és érettebb vérképzõ
Leukémia (fehérvérûség) Leukémia - fehérvérûség A leukémia a rosszindulatú rákos megbetegedések azon formája, amely a vérképzõ sejtekbõl indul ki. A leukémia a csontvelõben lévõ éretlen és érettebb vérképzõ
Az MNB szerepe a fizetési rendszerek fejlesztésében
 Az MNB szerepe a fizetési rendszerek fejlesztésében 2001/2 Készítette a Pénforgalmi önálló osztály Vezetõ: Prágay István fõosztályvezetõ Kiadja a Magyar Nemzeti Bank Titkárságának Tájékoztatási Osztálya
Az MNB szerepe a fizetési rendszerek fejlesztésében 2001/2 Készítette a Pénforgalmi önálló osztály Vezetõ: Prágay István fõosztályvezetõ Kiadja a Magyar Nemzeti Bank Titkárságának Tájékoztatási Osztálya
Kérdések és válaszok a gyógyászatisegédeszköz-támogatási rendszert érintő, 2009. augusztus 16-án hatályba lépő változásokkal kapcsolatban
 ORSZÁGOS EGÉSZSÉGBIZTOSÍTÁSI PÉNZTÁR Ártámogatási Főosztály 1139 Budapest, XIII. Váci út 73/A Telefon: 298-24-58, Telefax: 298-24-57, E-mail: atfo@oep.hu Kérdések és válaszok a gyógyászatisegédeszköz-támogatási
ORSZÁGOS EGÉSZSÉGBIZTOSÍTÁSI PÉNZTÁR Ártámogatási Főosztály 1139 Budapest, XIII. Váci út 73/A Telefon: 298-24-58, Telefax: 298-24-57, E-mail: atfo@oep.hu Kérdések és válaszok a gyógyászatisegédeszköz-támogatási
Az oldat tartalma milliliterenként: humán plazmaprotein... 200 mg (legalább 98%-os tisztaságú IgG)
 1. A GYÓGYSZER MEGNEVEZÉSE Hizentra 200 mg/ml oldatos injekció bőr alá történő beadásra 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán normál immunglobulin (SCIg). Az oldat tartalma milliliterenként: humán
1. A GYÓGYSZER MEGNEVEZÉSE Hizentra 200 mg/ml oldatos injekció bőr alá történő beadásra 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán normál immunglobulin (SCIg). Az oldat tartalma milliliterenként: humán
Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
 Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Cifloxin 250 mg filmtabletta Cifloxin 500 mg filmtabletta ciprofloxacin
Generated by Unregistered Batch DOC TO PDF Converter 2011.3.827.1514, please register! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Cifloxin 250 mg filmtabletta Cifloxin 500 mg filmtabletta ciprofloxacin
A pulzáló és folyamatos norfloxacin itatás összehasonlító vizsgálata csirkében és pulykában. Sárközy Géza
 A pulzáló és folyamatos norfloxacin itatás összehasonlító vizsgálata csirkében és pulykában Sárközy Géza Gyógyszertani és Méregtani tanszék Állatorvos-tudományi fakultás Szent István Egyetem Budapest 2002
A pulzáló és folyamatos norfloxacin itatás összehasonlító vizsgálata csirkében és pulykában Sárközy Géza Gyógyszertani és Méregtani tanszék Állatorvos-tudományi fakultás Szent István Egyetem Budapest 2002
Olvassa el figyelmesen az alábbi betegtájékoztatót, mely az Ön számára fontos információkat tartalmaz.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! -BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Ulcogant
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! -BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Ulcogant
Betegtájékoztató: Információk a felhasználó számára. Augmentin 250 mg/125 mg filmtabletta. amoxicillin/klavulánsav
 Betegtájékoztató: Információk a felhasználó számára Augmentin 250 mg/125 mg filmtabletta amoxicillin/klavulánsav Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
Betegtájékoztató: Információk a felhasználó számára Augmentin 250 mg/125 mg filmtabletta amoxicillin/klavulánsav Mielőtt elkezdi szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót,
VERSENYTANÁCS. 1054 Budapest, Alkotmány u. 5. 472-8864 Fax: 472-8860
 VERSENYTANÁCS 1054 Budapest, Alkotmány u. 5. 472-8864 Fax: 472-8860 Vj-105/2004/39. A Gazdasági Versenyhivatal versenytanácsa a Nestlé Hungária Kft. (Budapest) ellen fogyasztók megtévesztésének gyanúja
VERSENYTANÁCS 1054 Budapest, Alkotmány u. 5. 472-8864 Fax: 472-8860 Vj-105/2004/39. A Gazdasági Versenyhivatal versenytanácsa a Nestlé Hungária Kft. (Budapest) ellen fogyasztók megtévesztésének gyanúja
Betegtájékoztató: Információk a felhasználó számára. Bactroban 20 mg/g kenőcs mupirocin
 Betegtájékoztató: Információk a felhasználó számára Bactroban 20 mg/g kenőcs mupirocin Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára
Betegtájékoztató: Információk a felhasználó számára Bactroban 20 mg/g kenőcs mupirocin Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára
Familiáris mediterrán láz
 www.printo.it/pediatric-rheumatology/hu/intro Familiáris mediterrán láz Verzió 2016 1. MI AZ FMF 1.1 Mi ez? A familiáris mediterrán láz (Familial Mediterranean Fever, FMF) egy genetikailag öröklődő betegség.
www.printo.it/pediatric-rheumatology/hu/intro Familiáris mediterrán láz Verzió 2016 1. MI AZ FMF 1.1 Mi ez? A familiáris mediterrán láz (Familial Mediterranean Fever, FMF) egy genetikailag öröklődő betegség.
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Td-pur szuszpenziós injekció előretöltött fecskendőben tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 éven felüliek számára Mielőtt beadják
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Td-pur szuszpenziós injekció előretöltött fecskendőben tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 éven felüliek számára Mielőtt beadják
Antibiotikumok I. Selman Abraham Waksman 1888-1973
 Antibiotikumok I. Az antibiotikumok az élő szervezetek elsősorban mikroorganizmusok által termelt úgynevezett másodlagos anyagcseretermékek (szekunder metabolitok) legfontosabb csoportja. Ökológiai szerepük,
Antibiotikumok I. Az antibiotikumok az élő szervezetek elsősorban mikroorganizmusok által termelt úgynevezett másodlagos anyagcseretermékek (szekunder metabolitok) legfontosabb csoportja. Ökológiai szerepük,
A befogadó értékelés alkalmazása
 A befogadó értékelés alkalmazása Az Ügynökség Értékelési gyakorlat a befogadó intézményekben című projektje első fázisának végpontja a befogadó értékelés koncepciójának vitája, majd azt követően definciója
A befogadó értékelés alkalmazása Az Ügynökség Értékelési gyakorlat a befogadó intézményekben című projektje első fázisának végpontja a befogadó értékelés koncepciójának vitája, majd azt követően definciója
Fertőzésekkel szembeni immunitás, immunizálás
 Fertőzésekkel szembeni immunitás, immunizálás 1. Mit jelentenek az epitóp és a protektív antigén kifejezések? 2. Hasonlítsd össze a természetes és az adaptív immunválaszt! 3. Mi a vakcina? 4. Sorold fel
Fertőzésekkel szembeni immunitás, immunizálás 1. Mit jelentenek az epitóp és a protektív antigén kifejezések? 2. Hasonlítsd össze a természetes és az adaptív immunválaszt! 3. Mi a vakcina? 4. Sorold fel
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Tetanol pur betegtájékoztató - PIL alapján.doc BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Tetanol pur betegtájékoztató - PIL alapján.doc BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Loxicom 0,5 mg/ml belsőleges szuszpenzió kutyáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1,0 ml készítmény
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Loxicom 0,5 mg/ml belsőleges szuszpenzió kutyáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1,0 ml készítmény
BIZOTTSÁGI SZOLGÁLATI MUNKADOKUMENTUM A HATÁZSVIZSGÁLAT ÖSSZEFOGLALÁSA. amely a következő dokumentumot kíséri A TANÁCS IRÁNYELVE
 EURÓPAI BIZOTTSÁG Brüsszel, 2012.5.30. SWD(2012) 138 final BIZOTTSÁGI SZOLGÁLATI MUNKADOKUMENTUM A HATÁZSVIZSGÁLAT ÖSSZEFOGLALÁSA amely a következő dokumentumot kíséri A TANÁCS IRÁNYELVE az ionizáló sugárzás
EURÓPAI BIZOTTSÁG Brüsszel, 2012.5.30. SWD(2012) 138 final BIZOTTSÁGI SZOLGÁLATI MUNKADOKUMENTUM A HATÁZSVIZSGÁLAT ÖSSZEFOGLALÁSA amely a következő dokumentumot kíséri A TANÁCS IRÁNYELVE az ionizáló sugárzás
A BIZOTTSÁG 2006. december 8-i 1828/2006/EK RENDELETE
 A BIZOTTSÁG 2006. december 8-i 1828/2006/EK RENDELETE az Európai Regionális Fejlesztési Alapra, az Európai Szociális Alapra és a Kohéziós Alapra vonatkozó általános rendelkezések megállapításáról szóló
A BIZOTTSÁG 2006. december 8-i 1828/2006/EK RENDELETE az Európai Regionális Fejlesztési Alapra, az Európai Szociális Alapra és a Kohéziós Alapra vonatkozó általános rendelkezések megállapításáról szóló
SCORECARD ALAPÚ SZERVEZETIRÁNYÍTÁSI MÓDSZEREK BEMUTATÁSA
 Budapesti Gazdasági Főiskola KÜLKERESKEDELMI FŐISKOLAI KAR Nemzetközi marketing és teljes körű minőségirányítás szak Nappali tagozat Minőségirányítási menedzser szakirány SCORECARD ALAPÚ SZERVEZETIRÁNYÍTÁSI
Budapesti Gazdasági Főiskola KÜLKERESKEDELMI FŐISKOLAI KAR Nemzetközi marketing és teljes körű minőségirányítás szak Nappali tagozat Minőségirányítási menedzser szakirány SCORECARD ALAPÚ SZERVEZETIRÁNYÍTÁSI
II. melléklet. Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása
 II. melléklet Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása 10 Tudományos következtetések A Rocephin és kapcsolódó nevek (lásd I. melléklet) tudományos
II. melléklet Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása 10 Tudományos következtetések A Rocephin és kapcsolódó nevek (lásd I. melléklet) tudományos
Betegtájékoztató GLIMEPIRID-RATIOPHARM 4 MG TABLETTA. Glimepirid-ratiopharm 4 mg tabletta. HATÓANYAG: Glimepirid. 4 mg glimepirid tablettánként.
 GLIMEPIRID-RATIOPHARM 4 MG TABLETTA Glimepirid-ratiopharm 4 mg tabletta HATÓANYAG: Glimepirid. 4 mg glimepirid tablettánként. SEGÉDANYAG: Laktóz-monohidrát, A típusú karboximetil-keményítõ-nátrium, mikrokristályos
GLIMEPIRID-RATIOPHARM 4 MG TABLETTA Glimepirid-ratiopharm 4 mg tabletta HATÓANYAG: Glimepirid. 4 mg glimepirid tablettánként. SEGÉDANYAG: Laktóz-monohidrát, A típusú karboximetil-keményítõ-nátrium, mikrokristályos
Vállalkozás alapítás és vállalkozóvá válás kutatás zárójelentés
 TÁMOP-4.2.1-08/1-2008-0002 projekt Vállalkozás alapítás és vállalkozóvá válás kutatás zárójelentés Készítette: Dr. Imreh Szabolcs Dr. Lukovics Miklós A kutatásban részt vett: Dr. Kovács Péter, Prónay Szabolcs,
TÁMOP-4.2.1-08/1-2008-0002 projekt Vállalkozás alapítás és vállalkozóvá válás kutatás zárójelentés Készítette: Dr. Imreh Szabolcs Dr. Lukovics Miklós A kutatásban részt vett: Dr. Kovács Péter, Prónay Szabolcs,
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Mixtard 30 40 nemzetközi egység/ml szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 injekciós üveg 10 ml-t tartalmaz, ami 400 NE-gel egyenértékű.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Mixtard 30 40 nemzetközi egység/ml szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 injekciós üveg 10 ml-t tartalmaz, ami 400 NE-gel egyenértékű.
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA A BIZOTTSÁG KÖZLEMÉNYE A TANÁCSNAK ÉS AZ EURÓPAI PARLAMENTNEK
 HU HU HU AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 29.9.2008 COM(2008) 584 végleges A BIZOTTSÁG KÖZLEMÉNYE A TANÁCSNAK ÉS AZ EURÓPAI PARLAMENTNEK A 2004/24/EK irányelv által módosított 2001/83/EK irányelv
HU HU HU AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 29.9.2008 COM(2008) 584 végleges A BIZOTTSÁG KÖZLEMÉNYE A TANÁCSNAK ÉS AZ EURÓPAI PARLAMENTNEK A 2004/24/EK irányelv által módosított 2001/83/EK irányelv
VÁLLALATI INFORMÁCIÓS RENDSZEREK, INTERNETES TECHNIKÁK
 VÁLLALATI INFORMÁCIÓS RENDSZEREK, INTERNETES TECHNIKÁK A digitális gyár mint a termékéletciklusmenedzsment megvalósításának központi eleme A termékéletciklus-menedzsment lényege az üzleti folyamatok olyan
VÁLLALATI INFORMÁCIÓS RENDSZEREK, INTERNETES TECHNIKÁK A digitális gyár mint a termékéletciklusmenedzsment megvalósításának központi eleme A termékéletciklus-menedzsment lényege az üzleti folyamatok olyan
A BIZOTTSÁG KÖZLEMÉNYE AZ EURÓPAI PARLAMENTNEK
 HU HU HU EURÓPAI BIZOTTSÁG Brüsszel, 2011.2.22. COM(2011) 77 végleges 2008/0028 (COD) A BIZOTTSÁG KÖZLEMÉNYE AZ EURÓPAI PARLAMENTNEK az Európai Unió működéséről szóló szerződés 294. cikkének (6) bekezdése
HU HU HU EURÓPAI BIZOTTSÁG Brüsszel, 2011.2.22. COM(2011) 77 végleges 2008/0028 (COD) A BIZOTTSÁG KÖZLEMÉNYE AZ EURÓPAI PARLAMENTNEK az Európai Unió működéséről szóló szerződés 294. cikkének (6) bekezdése
Vélemény a BKV menetdíjainak 2008. évi tervezett emeléséről Bevezetés
 Vélemény a BKV menetdíjainak 2008. évi tervezett emeléséről Bevezetés A Fővárosi Önkormányzat ismét jelentősen, 13 százalékkal tervezi emelni a BKV menetdíjait. Amint az elmúlt évek tapasztalatai bebizonyították,
Vélemény a BKV menetdíjainak 2008. évi tervezett emeléséről Bevezetés A Fővárosi Önkormányzat ismét jelentősen, 13 százalékkal tervezi emelni a BKV menetdíjait. Amint az elmúlt évek tapasztalatai bebizonyították,
Javaslat A TANÁCS VÉGREHAJTÁSI RENDELETE
 EURÓPAI BIZOTTSÁG Brüsszel, 2013.10.30. COM(2013) 748 final 2013/0363 (NLE) Javaslat A TANÁCS VÉGREHAJTÁSI RENDELETE az Argentínából és Indonéziából származó biodízel behozatalára vonatkozó végleges dömpingellenes
EURÓPAI BIZOTTSÁG Brüsszel, 2013.10.30. COM(2013) 748 final 2013/0363 (NLE) Javaslat A TANÁCS VÉGREHAJTÁSI RENDELETE az Argentínából és Indonéziából származó biodízel behozatalára vonatkozó végleges dömpingellenes
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/18
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/18 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Oncept IL-2 liofilizátum és oldószer szuszpenziós injekcióhoz macska részére 2. MINŐSÉGI ÉS MENNYISÉGI
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/18 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Oncept IL-2 liofilizátum és oldószer szuszpenziós injekcióhoz macska részére 2. MINŐSÉGI ÉS MENNYISÉGI
MIKOR GONDOLJUNK ÉLELMISZER KÖZVETÍTETTE MEGBETEGEDÉSRE? (közismert néven ételmérgezésre, ételfertızésre)
 MIKOR GONDOLJUNK ÉLELMISZER KÖZVETÍTETTE MEGBETEGEDÉSRE? (közismert néven ételmérgezésre, ételfertızésre) Az élelmiszer fogyasztására visszavezethetı megbetegedések száma Magyarországon a becslések szerint
MIKOR GONDOLJUNK ÉLELMISZER KÖZVETÍTETTE MEGBETEGEDÉSRE? (közismert néven ételmérgezésre, ételfertızésre) Az élelmiszer fogyasztására visszavezethetı megbetegedések száma Magyarországon a becslések szerint
ATLASZ BAJNOK SPORT- ÉS RENDEZVÉNY (ESEMÉNY)- BALESETBIZTOSITÁS ÁLTALÁNOS FELTÉTELEI (MJK: ABSB 001-2009)
 QBE Insurance (Europe) Limited Magyarországi Fióktelepe Atlasz Bajnok ATLASZ BAJNOK SPORT- ÉS RENDEZVÉNY (ESEMÉNY)- BALESETBIZTOSITÁS ÁLTALÁNOS FELTÉTELEI (MJK: ABSB 001-2009) I. ÁLTALÁNOS RENDELKEZÉSEK
QBE Insurance (Europe) Limited Magyarországi Fióktelepe Atlasz Bajnok ATLASZ BAJNOK SPORT- ÉS RENDEZVÉNY (ESEMÉNY)- BALESETBIZTOSITÁS ÁLTALÁNOS FELTÉTELEI (MJK: ABSB 001-2009) I. ÁLTALÁNOS RENDELKEZÉSEK
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 100 mikrogramm flutikazon-propionát (mikronizált) adagonként.
 1. A GYÓGYSZER NEVE Flixotide Diskus 100 mikrogramm/adag adagolt inhalációs por Flixotide Diskus 250 mikrogramm/adag adagolt inhalációs por Flixotide Diskus 500 mikrogramm/adag adagolt inhalációs por 2.
1. A GYÓGYSZER NEVE Flixotide Diskus 100 mikrogramm/adag adagolt inhalációs por Flixotide Diskus 250 mikrogramm/adag adagolt inhalációs por Flixotide Diskus 500 mikrogramm/adag adagolt inhalációs por 2.
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Gynoflor hüvelytabletta BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Gynoflor hüvelytabletta BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE. Melosus 0,5 mg/ml belsőleges szuszpenzió macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL.
 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Melosus 0,5 mg/ml belsőleges szuszpenzió macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy ml tartalmaz: Hatóanyag: Meloxicam 0,5 mg Segédanyag: Nátrium-benzoát
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Melosus 0,5 mg/ml belsőleges szuszpenzió macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy ml tartalmaz: Hatóanyag: Meloxicam 0,5 mg Segédanyag: Nátrium-benzoát
TarTalomjegyzék a CIg Pannónia életbiztosító Nyrt. Általános életbiztosítási Feltételei
 Tartalomjegyzék Termékbemutató... 2 A CIG Pannónia Életbiztosító Nyrt. Általános Életbiztosítási Feltételei 1) Általános rendelkezések... 5 2) Biztosítási esemény... 5 3) Fogalmak... 5 4) A szerződés létrejötte...
Tartalomjegyzék Termékbemutató... 2 A CIG Pannónia Életbiztosító Nyrt. Általános Életbiztosítási Feltételei 1) Általános rendelkezések... 5 2) Biztosítási esemény... 5 3) Fogalmak... 5 4) A szerződés létrejötte...
Betegtájékoztató BCG-MEDAC POR ÉS OLDÓSZER INTRAVEZIKÁLIS SZUSZPENZIÓHOZ. BCG-medac por és oldószer intravezikális szuszpenzióhoz
 BCG-MEDAC POR ÉS OLDÓSZER INTRAVEZIKÁLIS SZUSZPENZIÓHOZ BCG-medac por és oldószer intravezikális szuszpenzióhoz HATÓANYAG: A készítmény hatóanyaga élõ BCG (Bacillus Calmette-Guérin) baktérium (a 1173-P2
BCG-MEDAC POR ÉS OLDÓSZER INTRAVEZIKÁLIS SZUSZPENZIÓHOZ BCG-medac por és oldószer intravezikális szuszpenzióhoz HATÓANYAG: A készítmény hatóanyaga élõ BCG (Bacillus Calmette-Guérin) baktérium (a 1173-P2
A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK
 EURÓPAI BIZOTTSÁG Brüsszel, 2016.1.29. COM(2016) 32 final A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK az élelmiszer-ellátási lánc vállalkozások közötti, tisztességtelen kereskedelmi gyakorlatairól
EURÓPAI BIZOTTSÁG Brüsszel, 2016.1.29. COM(2016) 32 final A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK az élelmiszer-ellátási lánc vállalkozások közötti, tisztességtelen kereskedelmi gyakorlatairól
Nyilvános Értékelő Jelentés. Alleopti Komfort. 20 mg/ml oldatos szemcsepp egyadagos tartályban. (nátrium-kromoglikát)
 Nyilvános Értékelő Jelentés Gyógyszernév: (nátrium-kromoglikát) Nemzeti eljárás A forgalomba hozatali engedély jogosultja: Sanofi-aventis Zrt. Kelt: 2014. november 11. TARTALOM NEM EGÉSZSÉGÜGYI SZAKEMBEREKNEK
Nyilvános Értékelő Jelentés Gyógyszernév: (nátrium-kromoglikát) Nemzeti eljárás A forgalomba hozatali engedély jogosultja: Sanofi-aventis Zrt. Kelt: 2014. november 11. TARTALOM NEM EGÉSZSÉGÜGYI SZAKEMBEREKNEK
A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK. a halászati és akvakultúra-termékek uniós ökocímkerendszerére vonatkozó lehetőségekről
 EURÓPAI BIZOTTSÁG Brüsszel, 2016.5.18. COM(2016) 263 final A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK a halászati és akvakultúra-termékek uniós ökocímkerendszerére vonatkozó lehetőségekről
EURÓPAI BIZOTTSÁG Brüsszel, 2016.5.18. COM(2016) 263 final A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK a halászati és akvakultúra-termékek uniós ökocímkerendszerére vonatkozó lehetőségekről
projekt címe: projektgazda: készítette: dátum:
 A vidékfejlesztési miniszter 45/2012. (V.8.) VM rendelete a nem emberi fogyasztásra szánt állati eredetű melléktermékekre vonatkozó állategészségügyi szabályok megállapításáról (Magyar Közlöny 2012/54.)
A vidékfejlesztési miniszter 45/2012. (V.8.) VM rendelete a nem emberi fogyasztásra szánt állati eredetű melléktermékekre vonatkozó állategészségügyi szabályok megállapításáról (Magyar Közlöny 2012/54.)
MINŐSÉGIRÁNYÍTÁSI KÉZIKÖNYV
 Nyilvántartásba vételi szám: Városi Művelődési Központ, Könyvtár és Alapfokú Művészeti Iskola 20-0071-06 Akkreditációs lajstromszám: MINŐSÉGIRÁNYÍTÁSI KÉZIKÖNYV Zalaszentgrót, Jóváhagyta: Varga István
Nyilvántartásba vételi szám: Városi Művelődési Központ, Könyvtár és Alapfokú Művészeti Iskola 20-0071-06 Akkreditációs lajstromszám: MINŐSÉGIRÁNYÍTÁSI KÉZIKÖNYV Zalaszentgrót, Jóváhagyta: Varga István
- Tartsa meg a betegtájékoztatót, mert a benne szereplő információkra a későbbiekben is szüksége lehet.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! ALKALMAZÁSI ELŐÍRÁS, BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! ALKALMAZÁSI ELŐÍRÁS, BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
HASZNÁLATI UTASÍTÁS Onsior 5 mg tabletta kutyáknak Onsior 10 mg tabletta kutyáknak Onsior 20 mg tabletta kutyáknak Onsior 40 mg tabletta kutyáknak
 HASZNÁLATI UTASÍTÁS Onsior 5 mg tabletta kutyáknak Onsior 10 mg tabletta kutyáknak Onsior 20 mg tabletta kutyáknak Onsior 40 mg tabletta kutyáknak 1. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK, TOVÁBBÁ
HASZNÁLATI UTASÍTÁS Onsior 5 mg tabletta kutyáknak Onsior 10 mg tabletta kutyáknak Onsior 20 mg tabletta kutyáknak Onsior 40 mg tabletta kutyáknak 1. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK, TOVÁBBÁ
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? A klinikai jelek és a vizsgálatok
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? A klinikai jelek és a vizsgálatok
genertel casco ÁLTALÁNOS VAGYONBIZTOSÍTÁSI FELTÉTELEK (ÁVF) GENERTEL CASCO BIZTOSÍTÁS KÜLÖNÖS FELTÉTELEI (GCKF)
 genertel casco ÁLTALÁNOS VAGYONBIZTOSÍTÁSI FELTÉTELEK (ÁVF) 2. oldal GENERTEL CASCO BIZTOSÍTÁS KÜLÖNÖS FELTÉTELEI (GCKF) 8. oldal GENERTEL CASCO ASSISTANCE SZOLGÁLTATÁS KÜLÖNÖS FELTÉTELEI (GCAKF) 21. oldal
genertel casco ÁLTALÁNOS VAGYONBIZTOSÍTÁSI FELTÉTELEK (ÁVF) 2. oldal GENERTEL CASCO BIZTOSÍTÁS KÜLÖNÖS FELTÉTELEI (GCKF) 8. oldal GENERTEL CASCO ASSISTANCE SZOLGÁLTATÁS KÜLÖNÖS FELTÉTELEI (GCAKF) 21. oldal
Lyme-kór (lyme-artritisz)
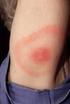 www.printo.it/pediatric-rheumatology/hu/intro Lyme-kór (lyme-artritisz) Verzió 2016 1. MI A LYME-KÓR 1.1 Mi ez? A Lyme-artritisz (Lyme-borreliózis) egyike a Borrelia burgdorferi baktérium által okozott
www.printo.it/pediatric-rheumatology/hu/intro Lyme-kór (lyme-artritisz) Verzió 2016 1. MI A LYME-KÓR 1.1 Mi ez? A Lyme-artritisz (Lyme-borreliózis) egyike a Borrelia burgdorferi baktérium által okozott
/2008. ( ) FVM rendelete
 1 A földművelésügyi és vidékfejlesztési miniszter /2008. ( ) FVM rendelete a növényvédő szerek forgalomba hozatalának és felhasználásának engedélyezéséről, valamint a növényvédő szerek csomagolásáról,
1 A földművelésügyi és vidékfejlesztési miniszter /2008. ( ) FVM rendelete a növényvédő szerek forgalomba hozatalának és felhasználásának engedélyezéséről, valamint a növényvédő szerek csomagolásáról,
www.printo.it/pediatric-rheumatology/hu/intro
 www.printo.it/pediatric-rheumatology/hu/intro Behcet-kór Verzió 2016 1. MI A BEHCET-KÓR 1.1 Mi ez? A Behçet-szindróma vagy Behçet-kór (BD) egy szisztémás vaszkulitisz (az egész testre kiterjedő érgyulladás),
www.printo.it/pediatric-rheumatology/hu/intro Behcet-kór Verzió 2016 1. MI A BEHCET-KÓR 1.1 Mi ez? A Behçet-szindróma vagy Behçet-kór (BD) egy szisztémás vaszkulitisz (az egész testre kiterjedő érgyulladás),
Az Advocate macskáknak 100 mg/ml imidaklopridot és 10 mg/ml moxidektint tartalmaz.
 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Advocate rácsepegtető oldat kistestű macskáknak és görényeknek Advocate rácsepegtető oldat nagytestű macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az Advocate macskáknak
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Advocate rácsepegtető oldat kistestű macskáknak és görényeknek Advocate rácsepegtető oldat nagytestű macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az Advocate macskáknak
Betegtájékoztató. Atópiás dermatitis. Összeállította dr. Molnár László
 Betegtájékoztató Atópiás dermatitis Összeállította dr. Molnár László Az atópiás dermatitis gyermekkorban az egyik leggyakrabban elôforduló bôrbetegség, a népesség 10-15%-ában fordul elô. Az utóbbi húsz
Betegtájékoztató Atópiás dermatitis Összeállította dr. Molnár László Az atópiás dermatitis gyermekkorban az egyik leggyakrabban elôforduló bôrbetegség, a népesség 10-15%-ában fordul elô. Az utóbbi húsz
DIÓSD VÁROS ÖNKORMÁNYZAT KÖZBESZERZÉSI SZABÁLYZATA. (Jóváhagyta Diósd Város Önkormányzat Képviselő-testületének... /2016. (II.25.) számú határozata)
 DIÓSD VÁROS ÖNKORMÁNYZAT KÖZBESZERZÉSI SZABÁLYZATA (Jóváhagyta Diósd Város Önkormányzat Képviselő-testületének... /2016. (II.25.) számú határozata) 2 Diósd Város Önkormányzat Képviselő-testülete (a továbbiakban:
DIÓSD VÁROS ÖNKORMÁNYZAT KÖZBESZERZÉSI SZABÁLYZATA (Jóváhagyta Diósd Város Önkormányzat Képviselő-testületének... /2016. (II.25.) számú határozata) 2 Diósd Város Önkormányzat Képviselő-testülete (a továbbiakban:
A mikroorganizmusok megkülönböztetése
 A mikroorganizmusok megkülönböztetése Robert Koch volt a következő jelentős kutató azok sorában, akik egyengették a penicillin felfedezéséhez vezető utat. Kifejlesztett egy táptalajt agaragarbói, amely
A mikroorganizmusok megkülönböztetése Robert Koch volt a következő jelentős kutató azok sorában, akik egyengették a penicillin felfedezéséhez vezető utat. Kifejlesztett egy táptalajt agaragarbói, amely
POLGÁRI TAKARÉKSZÖVETKEZET KOCKÁZATKEZELÉSSEL ÉS TŐKEMEGFELELÉSSEL KAPCSOLATOS INFORMÁCIÓK NYILVÁNOSSÁGRAHOZATALA. 2009. december 31.
 POLGÁRI TAKARÉKSZÖVETKEZET KOCKÁZATKEZELÉSSEL ÉS TŐKEMEGFELELÉSSEL KAPCSOLATOS INFORMÁCIÓK NYILVÁNOSSÁGRAHOZATALA 2009. december 31. 1 TARTALOMJEGYZÉK 1. BEVEZETÉS. 3 2. KOCKÁZATKEZELÉSI ELVEK, MÓDSZEREK.
POLGÁRI TAKARÉKSZÖVETKEZET KOCKÁZATKEZELÉSSEL ÉS TŐKEMEGFELELÉSSEL KAPCSOLATOS INFORMÁCIÓK NYILVÁNOSSÁGRAHOZATALA 2009. december 31. 1 TARTALOMJEGYZÉK 1. BEVEZETÉS. 3 2. KOCKÁZATKEZELÉSI ELVEK, MÓDSZEREK.
A Közép-dunántúli régió foglalkoztatási, munkaerő-piaci helyzetének alakulása
 Munkaerőpiaci információk a Közép-Dunántúlon A Közép-dunántúli régió foglalkoztatási, munkaerő-piaci helyzetének alakulása 2008. 1. A régió területi, földrajzi, népesség jellemzői A Közép-dunántúli régió
Munkaerőpiaci információk a Közép-Dunántúlon A Közép-dunántúli régió foglalkoztatási, munkaerő-piaci helyzetének alakulása 2008. 1. A régió területi, földrajzi, népesség jellemzői A Közép-dunántúli régió
ÁLTALÁNOS UTAZÁSI FELTÉTELEK. a TUI Austria Reiseveranstaltungs GmbH & Co KG által szervezett, német nyelven kiadott katalógusainak utazásaira
 ÁLTALÁNOS UTAZÁSI FELTÉTELEK a TUI Austria Reiseveranstaltungs GmbH & Co KG által szervezett, német nyelven kiadott katalógusainak utazásaira A fogyasztóvédelmi törvény értelmében Az utazási iroda felléphet
ÁLTALÁNOS UTAZÁSI FELTÉTELEK a TUI Austria Reiseveranstaltungs GmbH & Co KG által szervezett, német nyelven kiadott katalógusainak utazásaira A fogyasztóvédelmi törvény értelmében Az utazási iroda felléphet
Betegtájékoztató LAMICTAL 25 MG TABLETTA
 LAMICTAL 25 MG TABLETTA Lamictal 25 mg tabletta Lamictal 50 mg tabletta Lamictal 100 mg tabletta Lamictal 5 mg diszpergálódó/rágótabletta Lamictal 200 mg diszpergálódó/rágótabletta lamotrigin HATÓANYAG:
LAMICTAL 25 MG TABLETTA Lamictal 25 mg tabletta Lamictal 50 mg tabletta Lamictal 100 mg tabletta Lamictal 5 mg diszpergálódó/rágótabletta Lamictal 200 mg diszpergálódó/rágótabletta lamotrigin HATÓANYAG:
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE. Metacam 0,5 mg/ml belsőleges szuszpenzió macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL.
 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Metacam 0,5 mg/ml belsőleges szuszpenzió macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy ml tartalmaz: Hatóanyag: Meloxicam Segédanyag: Nátrium-benzoát 0,5 mg
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Metacam 0,5 mg/ml belsőleges szuszpenzió macskáknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy ml tartalmaz: Hatóanyag: Meloxicam Segédanyag: Nátrium-benzoát 0,5 mg
A Kormány 132/2004. (IV. 29.) Korm. rendelete
 6174 M A G Y A R K Ö Z L Ö N Y 2004/59. szám A Kormány 132/2004. (IV. 29.) Korm. rendelete a géntechnológiai tevékenység engedélyezési eljárási rendjérõl, valamint az eljárás során az Európai Bizottsággal
6174 M A G Y A R K Ö Z L Ö N Y 2004/59. szám A Kormány 132/2004. (IV. 29.) Korm. rendelete a géntechnológiai tevékenység engedélyezési eljárási rendjérõl, valamint az eljárás során az Európai Bizottsággal
II. A közbeszerzési érték és az értékhatárok meghatározására vonatkozó szabályok
 TAMÁSI VÁROS ÖNKORMÁNYZATÁNAK KÖZBESZERZÉSI SZABÁLYZAT A Tamási Város Önkormányzatai Képviselő-testülete a közbeszerzésekről szóló 2011. évi CVIII. törvény (továbbiakban Kbt.) 22. (1) bekezdésében meghatározott
TAMÁSI VÁROS ÖNKORMÁNYZATÁNAK KÖZBESZERZÉSI SZABÁLYZAT A Tamási Város Önkormányzatai Képviselő-testülete a közbeszerzésekről szóló 2011. évi CVIII. törvény (továbbiakban Kbt.) 22. (1) bekezdésében meghatározott
