KÍSÉRLETI MÉREGTAN. Növényvédelmi higiéniai és toxikológiai ismeretek modul
|
|
|
- Veronika Orosz
- 8 évvel ezelőtt
- Látták:
Átírás
1 KÍSÉRLETI MÉREGTAN Növényvédelmi higiéniai és toxikológiai ismeretek modul
2 Témakörök 1. Bevezetés a kísérleti toxikológiába 2. Egyszeri adagolású (akut) toxikológiai vizsgálatok 3. Ismételt adagolású toxikológiai vizsgálatok. Szubakut és szubkrónikus toxikológiai vizsgálatok 4. Ismételt adagolású toxikológiai vizsgálatok. Szaporodás biológiai toxicitási vizsgálatok 5. Ismételt adagolású toxikológiai vizsgálatok. Krónikus toxikológiai vizsgálatok 6. Mutagenetikai toxikológiai vizsgálatok 7. Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 8. Ökotoxikológiai vizsgálatok vízi élőszervezeteken 2
3 Bevezetés a kísérleti toxikológiába Állatkísérlet Állat kísérleti vagy egyéb tudományos célból való felhasználása, amely esetleg az állatnak fájdalmat, szenvedést, tartós nélkülözést vagy maradandó károsodást okozhat. 3
4 Bevezetés a kísérleti toxikológiába Állatkísérletek céljai vegyi anyagok (gyógyszerek, növényvédő szerek) kifejlesztéséhez, gyártásához; minőségi, hatékonysági és biztonsági tesztelése betegségek, fejlődési rendellenességek elkerülése, megelőzése, kezelése a természeti környezet védelme 4
5 Bevezetés a kísérleti toxikológiába Jogszabályok évi XXVIII. törvény az állatok védelméről és kíméletéről, módosítása: évi LXVIII. törvény 243/1998. (XII.31.) Korm. rendelet az állatkísérletek végzéséről 244/1998. (XII.31.) Korm. rendelet az állatvédelmi bírságról ETS 123. egyezmény 86/609/EEC direktíva 2010/63/EU irányelv (tudományos célokra felhasznált állatok védelméről) 5
6 Bevezetés a kísérleti toxikológiába Nem humán gerinces védelme (embrió, magzat nem!). Veszélyeztetett faj egyedét, háziasított faj kóbor egyedét, befogadott állatot nem szabad állatkísérletre használni. Főemlősök felhasználásának korlátozásai. 6
7 Bevezetés a kísérleti toxikológiába Állatkísérleteket csak felelős, kompetens ember végezhet. Az állatkísérletekre engedélyt kell kérni egyéni engedély max. 5 évig (MÁB, Kormányhivatal Élelmiszerlánc-biztonsági és Állategészségügyi Igazgatóság, Állatvédelmi Tanácsadó Testület Állatkísérleti Tudományos Etikai Tanácsa). Ellenőrzés állami feladat. 7
8 Bevezetés a kísérleti toxikológiába Nemzetközileg elfogadott kísérleti módszerek OECD ajánlások EPA ajánlások GLP követelményrendszer 8
9 Bevezetés a kísérleti toxikológiába Az állatkísérletek általános szabályai Kizárólag nyilvántartásba vett intézményben végezhető állatkísérlet. Nem végezhető állatkísérlet kozmetikai célra, illetve kozmetikumok tesztelésére. Nem végezhető állatkísérlet ha van elfogadott alternatív módszer. 9
10 Bevezetés a kísérleti toxikológiába Az állatkísérletek általános szabályai Nem végezhető állatkísérlet ha van olyan módszer, ami kevesebb állatot igényel vagy kevesebb fájdalmat. Részletes jegyzőkönyv-vezetés szükséges. Ha az állatkísérlet eredményét nem befolyásolja, akkor helyi vagy általános érzéstelenítés szükséges. 10
11 Bevezetés a kísérleti toxikológiába Kísérleti állat Bármely gerinces állatfaj egyede, amelyet állatkísérletre felhasználnak vagy felhasználni szándékoznak. Laboratóriumi állat (laborállat) Valamely állatfajnak az egyede, amelyet engedélyezett és nyilvántartott helyen, kísérlet céljára tenyésztenek. 11
12 Bevezetés a kísérleti toxikológiába Ideális állatmodell keringés, életfolyamatok láthatóak hasonlóság extrapolálhatóság ismételhetőség hozzáférhetőség kezelhetőség méret és szaporaság élettartam tartás olcsó 12
13 Bevezetés a kísérleti toxikológiába Ideális kísérleti állat (IEA) kb. 30 g szőrtelen átlátszó bőrű karma, foga csökevényes szelíd, barátságos füle nagy és könnyen véreztethető hőszabályozás honvágy 13
14 Bevezetés a kísérleti toxikológiába Kísérleti állat megválasztása Faj Rendszertani kategória, amelybe olyan egyedeket sorolunk, melyek hasonló felépítésűek és tulajdonságúak, melyek egymással géneket képesek kicserélni. Fajta Emberi tevékenység révén létrehozott olyan csoport, amelynek nincs saját elterjedési területe, de alaktani és élettani bélyegek alapján megkülönböztethető más fajtáktól. 14
15 Bevezetés a kísérleti toxikológiába Kísérleti állat megválasztása Alfaj Fajon belüli, a természetben létrejött rendszertani kategória földrajzi, környezeti okokból, vagy pedig időben szétvált evolúciós egység. 15
16 Bevezetés a kísérleti toxikológiába Kísérleti állat megválasztása Nem az ember modellezése a cél, illetve sosem az állat természetére vagyunk kíváncsiak. Ecetmuslica: genetika Törpesertés: gyomor-bélrendszer Kutya: inzulin Tengerimalac: C-vitamin 16
17 Bevezetés a kísérleti toxikológiába A leggyakoribb laborállatok házi-, illetve fehér egér (NUDE, SCID) vándor-, illetve fehérpatkány szíriai aranyhörcsög tengerimalac üregi-, illetve házinyúl 17
18 Bevezetés a kísérleti toxikológiába 18
19 Bevezetés a kísérleti toxikológiába 19
20 Bevezetés a kísérleti toxikológiába Ökotoxikológiai tesztszervezetek Szárazföldi környezet: madarak (tőkésréce, fürj ) hasznos ízeltlábúak (méh, fürkészdarázs, ragadozó atka ) talajlakók (giliszta, ugróvillás, baktérium ) Vízi környezet: halak (pisztráng, zebradánió ) gerinctelenek (Daphnia sp. ) algák vízi növények 20
21 Bevezetés a kísérleti toxikológiába 21
22 Bevezetés a kísérleti toxikológiába Alternatív módszerek in vitro technikák alacsonyabb rendű szervezetek használata immunológiai eljárások szerkezet-működés kapcsolat kvantitatív elemzése élettani folyamatok matematikai elemzése embereken való modellezés 22
23 Bevezetés a kísérleti toxikológiába 1. In vitro technikák organotipikus kultúrák sejtkultúrák Pl. HET-CAM teszt 2. Alacsonyabb rendű szervezetek használata Baktériumok, gombák, rovarok, puhatestűek Pl. AMES-teszt, LAL-teszt 23
24 Bevezetés a kísérleti toxikológiába 3. Immunológiai eljárások Pl. ELISA 4. Szerkezet-működés kapcsolat elemzése A molekulák szerkezete, fizikai-kémiai tulajdonságai és biológiai aktivitása közötti kapcsolatok alapján lehet jelezni valamely vegyület biológiai aktivitását, illetve toxicitását. 24
25 Bevezetés a kísérleti toxikológiába 5. Élettani folyamatok szimulálása Folyamatok leírása matematikai egyenlettel. 6. Emberi modell A klinikai fázisban, a biológiai vizsgálatok eredményeinek megerősítésére. 25
26 Bevezetés a kísérleti toxikológiába A kísérleti állatok elhelyezése Viszonylagos jólét teremtése (megfelelő levegő, azonos hőmérséklet, szabályozott fény, csíraszegény vagy legalábbis fertőzésmentes környezet) A kórokozók kizárása (vírusok, baktériumok, paraziták). 26
27 Bevezetés a kísérleti toxikológiába 27
28 Bevezetés a kísérleti toxikológiába 28
29 Bevezetés a kísérleti toxikológiába A higiéniai zsilip szerepe mikrobaszegény takarmány, ivóvíz és alomanyag sterilezett ketrecek és más berendezések csíramentessé szűrt levegő kórokozót nem hordozó ember 29
30 Bevezetés a kísérleti toxikológiába Állattartó rendszerek higiéniai fokozatai 1. Axénikus (csíramentes) (GF) Császármetszéssel (vagy embrió átültetéssel) nyert állatok, amelyeket izolátorban gnotobiotikus (csíramentes) technikákkal tartanak. Az állatok mikrobamentesek. 2. Meghatározott (specifikált) kórokozóktól mentes (SPF) Az állatok meghatározott kórokozóktól mentesek, amely kórokozók listáját és azok kimutatási módszereit meghatározzák. 30
31 Bevezetés a kísérleti toxikológiába Állattartó rendszerek higiéniai fokozatai 3. Császármetszéssel nyert zsilip mögött tartott (COBS) Az állatokat császármetszéssel nyerik és zsilip mögött tartják, amely zsilip távol tartja az állatokat a specifikus rágcsáló kórokozóktól. Az SPF kategória egy formája. 4. Vírus antitesttől mentes Az állatok vírus antitestektől, meghatározott rágcsáló vírus antitestektől mentesek. Az SPF kategória egy változata, meghatározott vírusoktól mentes állományt jelent. A meghatározott vírusok (antitesteinek) kimutatására szolgáló szerológiai módszerek megadásra kerülnek. 5. Hagyományos (konvencionális) (MD) 31
32 Bevezetés a kísérleti toxikológiába 32
33 Bevezetés a kísérleti toxikológiába 33
34 Bevezetés a kísérleti toxikológiába Az állatházi környezet tényezői 1. Abiotikus tényezők 1.1. Fizikai feltételek Környezeti körülmények fény: intenzitás, szín, periodicitás hőérzet: hőmérséklet, páratartalom, légáramlás illatok: állatok, vegyszerek Állatok férőhelye a ketrec vagy doboz anyaga és felépítése mozgás és játék alom 34
35 Bevezetés a kísérleti toxikológiába 1.2. Kémiai feltételek Takarmány 2. Biotikus tényezők 1.Fajon belüli sűrűség szocio-pszichológiai (Lee-Boot-, Whitten-, Bruce-hatás) 2.Fajok közötti állat-ember állat-mikroorganizmus állat-állat 35
36 Bevezetés a kísérleti toxikológiába 36
37 Bevezetés a kísérleti toxikológiába 37
38 Bevezetés a kísérleti toxikológiába Az állatház higiéniája Higiénia Az egészség megőrzéséhez szükséges tisztaság. Fertőtlenítés Olyan eljárás, amely a környezetbe került kórokozók elpusztítására, illetőleg fertőzőképességük megszüntetésére irányul. 38
39 Bevezetés a kísérleti toxikológiába A fertőtlenítés fokozatai Baktérium-szaporodást gátló (bakteriosztatikus) hatás A baktériumok nem pusztulnak el, csak fejlődésük, szaporodásuk gátolt. Csíraszámcsökkentő (szanációs) hatás A kórokozók mennyiségének olyan mértékű csökkentése, ami már nem vezet fertőzésre. Spóraölő (sporocid) hatás A spóraképző baktérium nemzetséghez tartozó baktériumok ellenálló spórái is elpusztulnak. 39
40 Bevezetés a kísérleti toxikológiába A fertőtlenítés fokozatai Baktériumölő (baktericid) hatás A baktériumok vegetatív formái elpusztulnak, a spórás alakok nem. Vírus-inaktiváló (virucid) hatás A vírusok elvesztik fertőző képességüket. Gombapusztító (fungicid) hatás A gombák és gombaelemek elpusztulnak. Parazitapusztító (paraziticid) hatás A kórokozó paraziták, és szaporító alakjaik pusztulnak el. 40
41 Bevezetés a kísérleti toxikológiába Fertőtlenítő eljárások fizikai kémiai kombinált 41
42 Bevezetés a kísérleti toxikológiába A fertőzés forrásai más laborállatok (állatbeszerzés) biológiai anyagok (termelés) kedvenc állatok személyzet (vektor) látogatók és időszakos személyzet (állatorvosok, felügyelők, állatszállítók) anyagok és berendezések (takarmány, alomanyag) 42
43 Bevezetés a kísérleti toxikológiába Kísérleti állatok takarmányozása Valamennyi állatnak, melyet kísérletben használnak vagy arra szánnak, gondoskodni kell a fajának, fajtájának megfelelő takarmányról, ivóvízről egészségéről és jólétéről. (Európa Tanács 123-as Konvenciója) 43
44 Bevezetés a kísérleti toxikológiába A takarmány felvétel hatása a kísérleti eredményekre 1.Közvetett eltérés a kísérleti anyag felvételében 2.Közvetlen a takarmányfelvétel önállóan hat a vizsgált tényezőkre (pl. daganatképződés, élettartam) 44
45 Bevezetés a kísérleti toxikológiába Az egységes takarmány előnyei minden táplálékigényt kielégít kedvező az állandósága kutatás számára gazdaságosabb Az állat nem válogathat! Mindig legyen táp és ivóvíz az állat előtt! 45
46 Bevezetés a kísérleti toxikológiába A kísérleti állatok táplálóanyag-igényét a következő tényezők határozzák meg alapvetően életkor élettani igénybevétel környezeti hőmérséklet mikrobiológiai környezet 46
47 Bevezetés a kísérleti toxikológiába Az állatházi munkák szervezésének fő szempontjai állat-szükséglet helyszükséglet (ketrec) takarmány-, ivóvíz- és alomanyag szükséglet nyilvántartás munkák sorrendezése munkaerő beosztás 47
48 Bevezetés a kísérleti toxikológiába Állatkísérletek tervezése állatok kiválasztása minőségi ellenőrzés, tartási feltételek, körülmények engedélyeztetés állatház: terv, felszerelés, személyzet képzettsége biztonság (biológiai veszélyek) nyilvántartás, jegyzőkönyv vezetés 48
49 Bevezetés a kísérleti toxikológiába 49
50 Bevezetés a kísérleti toxikológiába 50
51 Bevezetés a kísérleti toxikológiába 51
52 Bevezetés a kísérleti toxikológiába 52
53 Bevezetés a kísérleti toxikológiába 53
54 Bevezetés a kísérleti toxikológiába 54
55 Bevezetés a kísérleti toxikológiába 55
56 Bevezetés a kísérleti toxikológiába Kezelési módok 1. A gyomor-bélcsőbe történő adagolás (enterális kezelés) 2. Az emésztőkészülék megkerülésével történő adagolás (parenterális kezelés) 3. Helyi kezelés (szem, bőr) 4. A légutakon át történő adagolás (aerogén kezelés) 5. Különleges eljárások 56
57 Bevezetés a kísérleti toxikológiába Enterális kezelés perorálisan (p.o.) gyomorszonda rektálisan (p.r.) 57
58 Bevezetés a kísérleti toxikológiába Parenterális kezelés perkután (p.c.) intradermális (i.d.) szubkután (s.c.) intramuszkulárisan (i.m.) intravénásan (i.v.) intraperitoneálisan (i.p.) intracerebrálisan (i.c.) intraokulárisan (i.oc.) szub v. epidurálisan (e.du.) 58
59 Bevezetés a kísérleti toxikológiába Parenterális kezelés perkután (p.c.) intradermális (i.d.) szubkután (s.c.) intramuszkulárisan (i.m.) intravénásan (i.v.) intraperitoneálisan (i.p.) intracerebrálisan (i.c.) intraokulárisan (i.oc.) szub v. epidurálisan (e.du.) 59
60 Bevezetés a kísérleti toxikológiába Parenterális kezelés perkután (p.c.) intradermális (i.d.) szubkután (s.c.) intramuszkulárisan (i.m.) intravénásan (i.v.) intraperitoneálisan (i.p.) intracerebrálisan (i.c.) intraokulárisan (i.oc.) szub v. epidurálisan (e.du.) 60
61 Bevezetés a kísérleti toxikológiába Helyi kezelés 61
62 Bevezetés a kísérleti toxikológiába Aerogén kezelés és különleges eljárások intranazálisan (i. nas.) intratracheálisan (i. trach.) transzplantáció implantáció 62
63 Bevezetés a kísérleti toxikológiába Vérvétel leggyakrabban: torkolati vénából (v. jugularis) és combvénából (v. saphena) (v. femoralis) nyúl: fülvéna (v. auricularis marginalis) patkány, egér: farokvéna (v. coccigea lat.) (v. caudalis) 63
64 Bevezetés a kísérleti toxikológiába 64
65 Bevezetés a kísérleti toxikológiába A vizsgálatok időtartama Az állatkísérletek időtartama akut: max. 14 nap szubakut, szubkrónikus: max. 90 nap krónikus: 90 nap - 2 év 65
66 Bevezetés a kísérleti toxikológiába Eutanázia Az állatok leölésének humánus módja, mely minimális fájdalommal, félelemmel és kellemetlen érzettel jár. 66
67 Bevezetés a kísérleti toxikológiába Eutanázia kísérlet befejezésekor tudományos célból történő vér és egyéb szövet nyerése esetén fájdalom, kellemetlen érzet és szenvedés túllépi a megadott szintet az állatok egészsége és jóléte érdekében tenyésztésre alkalmatlanná váláskor 67
68 Bevezetés a kísérleti toxikológiába Az eutanázia módszerei 1. Fizikai módszerek Azonnali tudatvesztést kell okozniuk az agy fizikai sérülése következtében: lelövés (fej) rázkódás (ütés) elektromos kábítás nyaki diszlokáció lefejezés maceratio mikrohullámú besugárzás 68
69 Bevezetés a kísérleti toxikológiába Az eutanázia módszerei 2. Kémiai módszerek Megfelelő öntudatlanságot, fájdalomcsillapítást és izomrelaxációt biztosítanak: szén-dioxid, szén-monoxid kábító hatású illékony folyadékok (halotán, enfluron, isofluron) benzocainum trikain-metán-szulfonát etomidat és metomidat kvinaldin barbiturátok 69
70 Engedélyezési célú toxikológiai vizsgálatok 1. Engedélyezési célú toxikológiai vizsgálatok laborállatokon 2. Engedélyezési célú ökotoxikológiai vizsgálatok 70
71 Engedélyezési célú toxikológiai vizsgálatok Engedélyezési célú toxikológiai vizsgálatok laborállatokon 1. Egyszeri adagolású (akut) toxikológiai vizsgálatok 2. Ismételt adagolású toxikológiai vizsgálatok 2.1. Szubakut és szubkrónikus toxikológiai vizsgálatok 2.2. Szaporodás biológiai toxicitási vizsgálatok 2.3. Krónikus toxikológiai vizsgálatok 3. Mutagenetikai toxikológiai vizsgálatok 71
72 Egyszeri adagolású (akut) toxikológiai vizsgálatok A vizsgálatok célkitűzései: kideríteni a vizsgálati anyag toxicitásának jellegét, a különböző dózisok által kiváltott toxikus hatásokat, azok mértékét, összehasonlítani a vizsgálati anyag toxicitásának mértékét, már ismert toxicitású anyagokkal, megismerni a vizsgálati anyag által előidézett speciális toxikus hatásokat, azonosítani a célszervet, megbecsülni a legalacsonyabb letális vagy a legmagasabb, még nem letális dózis értékeket (toxicitási tartomány). 72
73 Egyszeri adagolású (akut) toxikológiai vizsgálatok A vizsgálatok célkitűzései: adatokat gyűjteni arról a kockázatról, melyet a vizsgálati anyag magas dózisban, akut hatás esetén (pl. baleset, mérgezés, környezeti katasztrófa, öngyilkosság, stb.) jelent, segítséget nyújtani a klinikusoknak az anyaggal történt mérgezés felismeréséhez és kezeléséhez, dóziskeresés a szubakut és krónikus (ismételt adagolású) állatkísérletekhez. 73
74 Egyszeri adagolású (akut) toxikológiai vizsgálatok LD 50 Az a méregadag mg/testtömeg kg-ban kifejezve, amely a kezelt állatok 50%-át elpusztítja a 14 napos megfigyelési időszak alatt LC 50 az a mg/m 3 -ben kifejezett méregkoncentráció a belélegzett levegőben, amely a kísérleti állatok 50%- át meghatározott idejű inhalációs kezelés során elpusztítja (mindkét nemre külön kell megadni!) 74
75 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut LD 50 meghatározása rágcsálókon Kísérleti állatfaj: labor patkány labor egér házinyúl Dózisok: min. 3 kontroll csoport (vivő szer) Állatszám: 5/ivar/csoport 75
76 Egyszeri adagolású (akut) toxikológiai vizsgálatok Kezelési módok: orális dermális inhalációs intraperitoneális A kezelések után 14 napos megfigyelési idő. 76
77 Egyszeri adagolású (akut) toxikológiai vizsgálatok Dózis-válasz összefüggés 77
78 Egyszeri adagolású (akut) toxikológiai vizsgálatok 78
79 Egyszeri adagolású (akut) toxikológiai vizsgálatok 79
80 Egyszeri adagolású (akut) toxikológiai vizsgálatok 80
81 Egyszeri adagolású (akut) toxikológiai vizsgálatok Dózistartomány keresés logaritmikus dózislépték szerint néhány állaton meghatározzák azt a tartományt, ahol várható lesz az ALD, illetve az LD 50 érték előfordulása. Limit teszt:5000 (2000) mg/ttkg (orális) 2000 mg/ttkg (dermális) 81
82 Egyszeri adagolású (akut) toxikológiai vizsgálatok Értékelendő paraméterek: testtömeg tápfogyasztás klinikai tünetek kórbonctan: elhullott állatok túlélő állatok 14 napos megfigyelés után szervtömeg mérés lehetséges kórszövettan lehetséges 82
83 Egyszeri adagolású (akut) toxikológiai vizsgálatok 83
84 Egyszeri adagolású (akut) toxikológiai vizsgálatok 84
85 Egyszeri adagolású (akut) toxikológiai vizsgálatok 85
86 Egyszeri adagolású (akut) toxikológiai vizsgálatok Ma már az LD 50 érték pontos, számszerű meghatározása nem hatósági követelmény. Helyette elfogadott a toxicitási kategóriába való besorolás, illetve a közelítő letális dózis megadása. A vizsgálatok elvégzésnél lényeges szempont: a lehető legtöbb információ a toxicitásról a lehető legkevesebb állat felhasználása 86
87 Egyszeri adagolású (akut) toxikológiai vizsgálatok Alternatív akut toxicitási vizsgálatok 1. Approximative Lethal Dose Method (ALD) dózisonként 1 állat tetszés szerinti dózisról indít dózislépték 1,5 szeres dózisemelés az első állat elhullásáig, a két utolsó dózis közötti tartomány ALD 87
88 Egyszeri adagolású (akut) toxikológiai vizsgálatok Alternatív akut toxicitási vizsgálatok 2. Up and Down Method becsült LD 50 értékről indul 1 állat dózisváltás faktora 1,3 ha életben marad dózisnövelés ha elhullik dóziscsökkentés 88
89 Egyszeri adagolású (akut) toxikológiai vizsgálatok Alternatív akut toxicitási vizsgálatok 3. The Fixed Dose Procedure elővizsgálatok több dózissal 1-1 állat/ivar/dózis javasolt dózisok: 5, 50, 300, 2000 mg/ttkg fővizsgálatban 5-5 állat/ivar a választott dózisban a fővizsgálatban a toxicitás nyilvánvaló jeleinek kell mutatkozniuk, de kerülni kell az állat elhullást a fővizsgálat menetét folyamatábra határozza meg az eredmény értékelésére, azaz a toxicitás osztályba sorolására külön táblázat alapján történik 89
90 Egyszeri adagolású (akut) toxikológiai vizsgálatok Alternatív akut toxicitási vizsgálatok 4. Acute Toxic Class Method induló dózisok: 5, 50, 300, 2000 mg/ttkg állatszám: 3/ivar a vizsgálat menetét az elhullások száma szabályozza a fővizsgálat menetét folyamatábra határozza meg az eredmény értékelésére, azaz a toxicitás osztályba sorolására külön táblázat alapján történik 90
91 Egyszeri adagolású (akut) toxikológiai vizsgálatok Alternatív akut toxicitási vizsgálatok 5. Quantitative Structure-Activity Relationship - QSAR nem szükséges hozzá élő állat a vizsgálati anyag kémiai szerkezetéből indulnak ki az eddig toxikológiai szempontból vizsgált vegyi anyagokat tartalmazó adatbázishoz történik a hasonlítás a számítógépes program becsült értéket tud adni a várható toxicitásra ill. letalitásra ma még csak szűrésre használják 91
92 Egyszeri adagolású (akut) toxikológiai vizsgálatok Szemirritáció vizsgálata házinyúlon A vizsgálati eredmények: adatot szolgáltatnak a szem felszínén - kötő-, szaru- és szivárványhártyán - azonnal, de legalább 24 órán belül jelentkező gyulladás jellegére, mértékére, lefolyására, kimenetelére és szükség szerint a kórbonctani és alapvető kórszövettani következményeire is 92
93 Egyszeri adagolású (akut) toxikológiai vizsgálatok A vizsgálati eredmények: felvilágosítást adnak a foglalkozási, valamint a véletlen - esetleg szándékos - emberi szemkárosodás lehetőségének és az ezzel kapcsolatos mérgezési veszélyességének a megítélésére támpontul szolgálnak a szemvédelmet biztosító egyéni védőeszköz fajták és azok használatának javaslatára 93
94 Egyszeri adagolású (akut) toxikológiai vizsgálatok A vizsgálati eredmények: vonatkozási adatot jelentenek a munkaegészségügyi várakozási idők meghatározására adatokat nyújtanak az emberi szem helyi - esetleg az ehhez csatlakozó általános - mérgezés tüneteinek, következményeinek valószínűsítésére, ezzel az elsősegélynyújtás és a gyógykezelés alapelveinek kidolgozására, illetve ezek javaslattételére 94
95 Egyszeri adagolású (akut) toxikológiai vizsgálatok Szemirritáció vizsgálata házinyúlon Kísérleti állatfaj: albínó házinyúl Dózis: 0,1 ml / g önkontrollos teszt Állatszám: 3 ph figyelembe vétele 2 11,5 95
96 Egyszeri adagolású (akut) toxikológiai vizsgálatok A kezelés előtt a szem állapotának ellenőrzése. Kezelés: kötőhártyazsákba. Kezelés utáni szemöblítés irritatív anyagok esetében. Testtömeg mérés. 96
97 Egyszeri adagolású (akut) toxikológiai vizsgálatok Megfigyelés: 1., 24., 48., 72. óra, 4. és 7. nap. Kórbonctan. Szövettani vizsgálat: igény szerint 3 szem/csoport. 97
98 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése I. Kötőhártya Pont A. Vérbőség Az erek a normálist meghaladóan, határozottabban láthatók 1 Kifejezettebb, sötétebb, karmazsinvörös szín 2 Diffúz, sötétvörös szín 3 98
99 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése Pont B. Duzzadás Enyhe duzzadás, beleértve a pislogó hártyát is 1 Szemhéjak részleges kifordulásával 2 Félig zárt, duzzadt szemhéjak 3 Teljesen zárt, duzzadt szemhéjak 4 99
100 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése Pont C. Váladékképződés Normálist meghaladó mennyiség 1 A szemhéjak széle nedves 2 A szemhéjak környéke is nedves 3 Értékelés: (A + B + C) x 2 Max.: 20 pont 10
101 Egyszeri adagolású (akut) toxikológiai vizsgálatok 10
102 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése Pont II. Szaruhártya A. Homály mértéke Elszórt, diffúz homály, a szivárványhártya világosan látható 1 A homályban átlátszó területek, a szivárványhártya részletei csak homályosan láthatók 2 Opálos homály, a szivárványhártya részletei nem láthatók 3 Intenzív opálos, a szivárványhártya láthatatlan 4 10
103 Egyszeri adagolású (akut) toxikológiai vizsgálatok 10
104 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése Pont B. A homály területe 1/4 rész vagy kisebb 1 1/2 résznél kisebb, de 1/4 résznél nagyobb 2 3/4 résznél kisebb, de 1/2 résznél nagyobb 3 Teljes felszín, 3/4 résznél nagyobb 4 Értékelés: A x B x 5 Max.: 80 pont 10
105 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése Pont III. Szivárványhártya A. Elváltozások Vérbő, redőzöttebb írisz, szaruhártya belövellt, az írisz fényre még enyhén reagál 1 Vérzéses, fényre nem reagál 2 Értékelés: A x 5 Max.: 10 pont 10
106 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut szemirritatív hatás értékelése Végső pontszám (irritációs index): I + II + III ( ) = 110 pont minden vizsgálati időponthoz tartozóan Megítélés: szuper irritatív erősen irritatív mérsékelten irritatív 0-19 nem vagy enyhén irritatív 10
107 Egyszeri adagolású (akut) toxikológiai vizsgálatok Bőrirritáció vizsgálata házinyúlon A vizsgálati eredmények: adatot szolgáltatnak a bőrön azonnal, de legalább 24 órán belül jelentkező gyulladás jellegére, mértékére, lefolyására, kimenetelére és szükség szerint a kórbonctani és alapvető kórszövettani következményeire is felvilágosítást adnak a foglalkozási, valamint a véletlen - esetleg szándékos - emberi bőrkárosodás lehetőségének és az ezzel kapcsolatos mérgezési veszélyességének a megítélésére 10
108 Egyszeri adagolású (akut) toxikológiai vizsgálatok A vizsgálati eredmények: támpontul szolgálnak a bőrvédelmet biztosító egyéni védőeszköz fajták és azok használatának javaslatára vonatkozási adatot jelentenek a munkaegészségügyi várakozási idők meghatározására adatokat nyújtanak az emberi bőr helyi mérgezés tüneteinek, következményeinek valószínűsítésére, ezzel az elsősegélynyújtás és a gyógykezelés alapelveinek kidolgozására, illetve ezek javaslattételére 10
109 Egyszeri adagolású (akut) toxikológiai vizsgálatok Bőrirritáció vizsgálata házinyúlon Kísérleti állatfaj: albínó házinyúl Dózis: 0,5 ml / g önkontrollos teszt Állatszám: 3 ph figyelembe vétele 2 11,5 10
110 Egyszeri adagolású (akut) toxikológiai vizsgálatok A kezelés előtt 24 órával szőrtelenítés 12 x 10 cm-es felületen. Kezelés: 4 órás expozíció. Abrázió: kettős kereszt karcolása a hátoldalon. Testtömeg mérése. 11
111 Egyszeri adagolású (akut) toxikológiai vizsgálatok Megfigyelés: 24., 48., 72., 96 óra. Kórbonctan. Szövettani vizsgálat: igény szerint (bőr). 11
112 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut bőrirritatív hatás értékelése A. Vérbőség pörkképződés Pont Nincs 0 Enyhe vérbőség (alig észlelhető) 1 Enyhe, de jól észlelhető vérbőség 2 Mérsékelt - súlyos vérbőség 3 Súlyos vérbőség (céklavörös, pörkösödés, mélybe terjedő elhalás) 4 11
113 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut bőrirritatív hatás értékelése B. Vizenyőképződés Pont Nincs 0 Enyhe ödéma (alig észrevehető) 1 Enyhe ödéma, a kezelt terület kifejezetten kiemelkedő 2 Mérsékelt - súlyos ödéma (a kezelt terület megközelítően 1 mm-re kiemelkedik) 3 Súlyos ödéma (a kezelt területen túlterjedő, 1 mm-t meghaladó kiemelkedés) 4 11
114 Egyszeri adagolású (akut) toxikológiai vizsgálatok Akut bőrirritatív hatás értékelése Végső pontszám (irritációs index): A kezelés után az ép és abráziós területek értékeinek átlaga. Megítélés: 0,0-0,5 nem irritatív 0,5-2,0 enyhén irritatív 2,0-5,0 mérsékelten irritatív 5,0-8,0 kifejezetten irritatív 11
115 Ismételt adagolású toxikológiai vizsgálatok Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok 2. Szaporodás biológiai toxicitási vizsgálatok 3. Krónikus toxikológiai vizsgálatok 11
116 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok A vizsgálatok célkitűzései: meghatározni a vizsgálati anyag toxikus hatásait olyan alacsony dózisokban, melyek még biztosítják a kísérleti állatok túlélését meghatározni a toxikus hatások dózisfüggését, beleértve a NOAEL értéket azonosítani a toxicitás célszervé(i)t 11
117 Ismételt adagolású toxikológiai vizsgálatok A vizsgálatok célkitűzései: információkat gyűjteni a lehetséges faji érzékenységbeli különbségekről információkat gyűjteni a humán kockázatbecsléshez információkat gyűjteni a krónikus toxicitási vizsgálatok tervezéséhez és a dózisválasztáshoz 11
118 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok Bőrszenzibilizáló hatás vizsgálata A vizsgálati anyagnak a tengerimalacok szőrtelenített bőrére történő ismételt bedörzsölésével (epikután) vagy bőrébe fecskendezésével (intrakután) végzett vizsgálat a túlérzékenység kifejlődésén (allergiás kontakt szenzibilizáció) alapuló bőr-, esetleg általános szenzibilizáció lehetőségének meghatározására irányul. 11
119 Ismételt adagolású toxikológiai vizsgálatok Bőrszenzibilizáló hatás vizsgálata Kísérleti állatfaj: albínó tengerimalac Dózis: elővizsgálattal határozzák meg Állatszám: 20 (10 kontroll ) Kezelés: epikután vagy intrakután Testtömeg mérése A kezelés előtt 24 órával szőrtelenítés (5x5cm) 11
120 Ismételt adagolású toxikológiai vizsgálatok Bőrszenzibilizáló hatás vizsgálata Kezelés menete: 7 naponta, összesen 3 alkalommal 6 órás expozíció (szenzibilizálás) Várakozás Kiváltás a 28. napon Értékelés 29., 30. napon a túlérzékenységi reakció foka és kiterjedése 12
121 Ismételt adagolású toxikológiai vizsgálatok Bőrszenzibilizáló hatás értékelése Pont Értékelés: nincs reakció 0 gyenge bőrpír 1 enyhe diffúz bőrpír 2 fokozott bőrpír (duzzanattal vagy Ø) 3 Kórbonctani vizsgálat 12
122 Ismételt adagolású toxikológiai vizsgálatok Bőrszenzibilizáló hatás értékelése Szenzibilizáló hatás: 0 nem szenzibilizáló 0,1-0,4 enyhén szenzibilizáló 0,5-1,9 gyengén szenzibilizáló 2,0-4,9 közepesen szenzibilizáló 5,0-8,0 erősen szenzibilizáló 12
123 Ismételt adagolású toxikológiai vizsgálatok Bőrszenzibilizáló hatás értékelése 12
124 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok Szubakut inhalációs vizsgálat Kísérleti állatfaj: labor patkány Dózisok: min. 3 kontroll csoport Állatszám: 5/ivar/csoport 12
125 Ismételt adagolású toxikológiai vizsgálatok Szubakut inhalációs vizsgálat Kezelés: inhalációs (4 óra) időtartam: 5 nap Kezelés után 14 napos megfigyelés. 12
126 Ismételt adagolású toxikológiai vizsgálatok Szubakut inhalációs vizsgálat Értékelendő paraméterek: testtömeg tápfogyasztás klinikai tünetek kórbonctan: elhullott állatok túlélő állatok 14 napos megfigyelés után szervtömeg mérés (abszolút, relatív) kórszövettan lehetséges 12
127 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata A vizsgálati eredmények: információt nyújtanak a toxikus hatások halmozódása (kumuláció), vagy az esetleges tűrőképesség növekedése (tolerancia) jellegének, mértékének megállapítására lehetővé teszik a szubakut és szubkrónikus etetési vizsgálatok megalapozottabb megtervezését 12
128 Ismételt adagolású toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata Kagan-féle módszer Kísérleti állatfaj: labor patkány Dózisok: min. 3 kontroll csoport Állatszám: 10/ivar/csoport 12
129 Ismételt adagolású toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata Kezelési időtartam: 4 hét (naponta 1x) Értékelendő paraméterek: klinikai tünetek testtömeg tápfogyasztás 12
130 Ismételt adagolású toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata Értékelendő paraméterek: kórbonctan: elhullott állatok túlélő állatok szervtömeg mérés kórszövettan 13
131 Ismételt adagolású toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata Lim-féle módszer Kísérleti állatfaj: labor patkány Dózisok: p. o. LD 50 9%-a ( 4 napig naponta 1x) dózis emelés 1,5x kontroll csoport Állatszám: 10/ivar/csoport 13
132 Ismételt adagolású toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata Kezelési időtartam: 4 hét (naponta 1x) Értékelendő paraméterek: klinikai tünetek testtömeg tápfogyasztás 13
133 Ismételt adagolású toxikológiai vizsgálatok Orális kumulatív toxicitás vizsgálata Értékelendő paraméterek: kórbonctan: elhullott állatok túlélő állatok szervtömeg mérés kórszövettan 13
134 Ismételt adagolású toxikológiai vizsgálatok Kumulatív hatás értékelése Kumulációs koefficiens = Értékelés: KI > 1 tolerancia KI < 1 kumulatív KI = 1 közömbös 13
135 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok 28 napos etetéses toxicitás vizsgálat rágcsálókon Kísérleti állatfaj: labor patkány labor egér Dózisok: min. 3 kontroll csoport Állatszám: 5/ivar/csoport 13
136 Ismételt adagolású toxikológiai vizsgálatok 28 napos etetéses toxicitás vizsgálat rágcsálókon Kezelés: orális (takarmány, ivóvíz, gyomorszonda) Takarmány hatóanyag tartalmának analitikai vizsgálata. Értékelendő paraméterek: klinikai tünetek testtömeg tápfogyasztás (vízfogyasztás) szemvizsgálat 13
137 Ismételt adagolású toxikológiai vizsgálatok Értékelendő paraméterek: hematológiai vizsgálat: mennyiségi és minőségi vérkép szérumvizsgálat: Na, K, enzimaktivitás (AST, ALT..), karbamid, fehérje, albumin, kreatinin, bilirubin, glükóz, epesavak vizeletvizsgálat (opcionális): mennyiség, átlátszóság, fehérje, glükóz, keton, vér, üledék, ph. 13
138 Ismételt adagolású toxikológiai vizsgálatok 28 napos etetéses toxicitás vizsgálat rágcsálókon Értékelendő paraméterek: kórbonctan: elhullott állatok túlélő állatok szervtömeg mérés kórszövettan tényleges hatóanyag felvétel 13
139 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok 90 napos etetéses toxicitás vizsgálat rágcsálókon Kísérleti állatfaj: labor patkány labor egér Dózisok: min. 3 kontroll csoport Állatszám: 10/feldolgozási időpont/ivar/csoport 13
140 Ismételt adagolású toxikológiai vizsgálatok 90 napos etetéses toxicitás vizsgálat rágcsálókon Kezelés: orális (takarmány, ivóvíz, gyomorszonda) Takarmány hatóanyag tartalmának analitikai vizsgálata. Értékelendő paraméterek: klinikai tünetek Testtömeg tápfogyasztás (vízfogyasztás) szemvizsgálat 14
141 Ismételt adagolású toxikológiai vizsgálatok Értékelendő paraméterek: hematológiai vizsgálat: mennyiségi és minőségi vérkép szérumvizsgálat: Na, K, enzimaktivitás (AST, ALT..), karbamid, fehérje, kreatinin, bilirubin, glükóz, epesavak Vizeletvizsgálat (opcionális): mennyiség, átlátszóság, fehérje, glükóz, keton, vér, üledék, ph. 14
142 Ismételt adagolású toxikológiai vizsgálatok 90 napos etetéses toxicitás vizsgálat rágcsálókon Értékelendő paraméterek: kórbonctan: elhullott állatok túlélő állatok szervtömeg mérés kórszövettan tényleges hatóanyag felvétel 14
143 Ismételt adagolású toxikológiai vizsgálatok 1. Szubakut és szubkrónikus toxikológiai vizsgálatok 90 napos etetéses toxicitási vizsgálat nem rágcsálókon Kísérleti állatfaj: beagle kutya mini sertés Dózisok: min. 3 kontroll csoport Állatszám: 4/ivar/csoport 14
144 Ismételt adagolású toxikológiai vizsgálatok 90 napos etetéses toxicitási vizsgálat nem rágcsálókon Kezelés: orális (takarmány, ivóvíz, gyomorszonda, kapszula) Takarmány hatóanyag tartalmának analitikai vizsgálata. Értékelendő paraméterek: klinikai tünetek testtömeg tápfogyasztás (vízfogyasztás) szemvizsgálat 14
145 Ismételt adagolású toxikológiai vizsgálatok 14
146 Ismételt adagolású toxikológiai vizsgálatok 14
147 Ismételt adagolású toxikológiai vizsgálatok Értékelendő paraméterek: hematológiai vizsgálat: mennyiségi és minőségi vérkép szérumvizsgálat: Ca, P, Cl, Na, K, koleszterin, enzimaktivitás (AST, ALT..), karbamid, fehérje, albumin, kreatinin, bilirubin, glükóz, epesavak vizeletvizsgálat: mennyiség, átlátszóság, fehérje, glükóz, keton, vér, ph. 14
148 Ismételt adagolású toxikológiai vizsgálatok 90 napos etetéses toxicitási vizsgálat nem rágcsálókon Értékelendő paraméterek: kórbonctan: elhullott állatok túlélő állatok szervtömeg mérés kórszövettan tényleges hatóanyag felvétel 14
149 Ismételt adagolású toxikológiai vizsgálatok 14
150 Ismételt adagolású toxikológiai vizsgálatok 15
151 Ismételt adagolású toxikológiai vizsgálatok 15
152 Ismételt adagolású toxikológiai vizsgálatok 2. Szaporodás biológiai toxicitási vizsgálatok A szaporodás-biológiai toxicitási vizsgálatok az utód nemzedék, vagy nemzedékek lehetséges károsodásait mutathatják ki, melyek esetleg anélkül következnek be, hogy a testidegen kémiai anyaggal érintkezőkön (expozíció) a károsodásnak a legkisebb jele is mutatkozna. 15
153 Ismételt adagolású toxikológiai vizsgálatok Szaporodás biológiai toxicitási vizsgálatok rendszere Reprodukciós toxicitási vizsgálat A kezelés kiterjed mindkét szülő ivarsejt képzésére, a preimplantációs fejlődésre, az implantációra, az organogenezisre, a fötogenezisre és a megszületett ivadékok fejlődésére. Teratológiai vizsgálat A vizsgálat célja, hogy minden organogenezis alatti károsodást feltárjon. Perinatalis és posztnatalis vizsgálat Célja, hogy a késői terhesség, a szülés és a szoptatás alatt bekövetkező károsodásokat felfedjen mind az anyákon, mind az ivadékokon. 15
154 Ismételt adagolású toxikológiai vizsgálatok 2. Szaporodás biológiai toxicitási vizsgálatok Teratológiai vizsgálat Kísérleti állatfaj (2 eltérő faj kötelező): labor patkány, labor egér új-zélandi fehér nyúl Dózisok: min. 3 kontroll csoport Állatszám: patkány: min. 20 vemhes nőstény/csoport nyúl: min. 16 vemhes nőstény/csoport 15
155 Ismételt adagolású toxikológiai vizsgálatok Teratológiai vizsgálat Kezelés módja: orális (gyomorszonda) Pároztatás: hüvelykenet vétele Kezelés ideje: naponta patkány: vemhesség napja között nyúl: a vemhesség nap között Megfigyelések az élő állat fázisban: klinikai tünetek (anyai halálozás) testtömeg, tápfogyasztás 15
156 Ismételt adagolású toxikológiai vizsgálatok Teratológiai vizsgálat Értékelendő paraméterek: Kórbonctan: patkány a vemhesség 20. napján nyúl a vemhesség 28. napján Boncoláskor az anyákon végzett megfigyelések: anyák makroszkópos vizsgálata petefészek vizsgálata sárgatest uterus vizsgálata - korai, késői elhalások ill. élő magzatok leszámolása 15
157 Ismételt adagolású toxikológiai vizsgálatok Teratológiai vizsgálat Magzatokon végzett vizsgálatok: élő magzatok neme, testsúlya, külső elváltozások placentasúly, elváltozások a placentán csontvázfestés (magzatok 50%) fixálás Bouin oldatban (magzatok 50%) zsigeri vizsgálat 15
158 Ismételt adagolású toxikológiai vizsgálatok 15
159 Ismételt adagolású toxikológiai vizsgálatok 2. Szaporodás biológiai toxicitási vizsgálatok 2-generációs reprodukciós toxicitási vizsgálat Kísérleti állatfaj: labor patkány labor egér Dózisok: minimálisan 3. kontroll Állatszám: min. 20 vemhes nőstény/csoport 15
160 Ismételt adagolású toxikológiai vizsgálatok 2-generációs reprodukciós toxicitási vizsgálat Kezelés módja: orális (takarmány, ivóvíz, gyomorszonda) Kezelés ideje: pároztatás előtt: hímek min. 60 nap nőstények - min. 14 nap pároztatás után: nőstények terhesség, szoptatás Megfigyelések az élő állat fázisban: klinikai tünetek testtömeg, tápfogyasztás (vízfogyasztás) 16
161 Ismételt adagolású toxikológiai vizsgálatok 2-generációs reprodukciós toxicitási vizsgálat Pároztatás: hüvelykenet vétele Hímek feldolgozása: kórbonctan kórszövettan Megfigyelések az élő állat fázisban: klinikai tünetek, toxicitás, moribund állapot, anyai elhullás testsúly, súlygyarapodás, tápfogyasztás (vízfogyasztás) 16
162 Ismételt adagolású toxikológiai vizsgálatok 2-generációs reprodukciós toxicitási vizsgálat Ellés: utódok száma, neme élve, halva születés makroszkópos elváltozások Megfigyelések az élő állat fázisban: klinikai tünetek (anyai elhullás) testtömeg, tápfogyasztás 16
163 Ismételt adagolású toxikológiai vizsgálatok 2-generációs reprodukciós toxicitási vizsgálat Utódokon végzett vizsgálatok: klinikai tünetek, toxicitás, elhullás testtömeg mérés: 1, 4, 7, 14, 21, 28. nap fejlődési próbák: fordulási reflex 1 napon fülkagyló felválása napon szemkinyílása napon 16
164 Ismételt adagolású toxikológiai vizsgálatok 2-generációs reprodukciós toxicitási vizsgálat Boncolás: az utódok leválasztásakor (28. nap) Nőstények feldolgozása: kórbonctan kórszövettan Utódok feldolgozása: Kórbonctan kórszövettan lehetséges 16
165 Ismételt adagolású toxikológiai vizsgálatok 2 vagy többgenerációs vizsgálat Az utód nemzedék (F 1 ) kezelése a leválasztás után (28. nap). F 0 F 1 Az utód nemzedékek (F x ) kezelése a leválasztás után (28. nap). F 0 F 1 F 2 16
166 Ismételt adagolású toxikológiai vizsgálatok 3. Krónikus toxikológiai vizsgálatok A vizsgálatok célkitűzései: meghatározni a vizsgálati anyag toxikus hatásait olyan alacsony dózisokban, melyek még biztosítják a kísérleti állatok túlélését meghatározni a toxikus hatások dózisfüggését, beleértve a NOAEL értéket azonosítani a toxicitás célszervé(i)t 16
167 Ismételt adagolású toxikológiai vizsgálatok A vizsgálatok célkitűzései: információkat gyűjteni a lehetséges faji érzékenységbeli különbségekről információkat gyűjteni a humán kockázatbecsléshez 16
168 Ismételt adagolású toxikológiai vizsgálatok 3. Krónikus toxikológiai vizsgálatok Krónikus etetése toxicitás vizsgálat Kísérleti állatfaj: labor patkány labor egér beagle kutya Dózisok: min. 3, kontroll csoport Állatszám: 20(10)/feldolgozási időpont/ivar/csoport 4/ivar/csoport 16
169 Ismételt adagolású toxikológiai vizsgálatok Krónikus etetése toxicitás vizsgálat Kezelés: orális (takarmány, ivóvíz) naponta 1 év (18-24 hónap) Takarmány hatóanyag tartalmának analitikai vizsgálata. Értékelendő paraméterek: klinikai tünetek testtömeg táp- és vízfogyasztás szemvizsgálat 16
170 Ismételt adagolású toxikológiai vizsgálatok Értékelendő paraméterek: hematológiai vizsgálat: mennyiségi és minőségi vérkép szérumvizsgálat: Ca, Na, K, koleszterin, glükóz, karbamid, kreatinin, fehérje, albumin, enzimaktivitás (AST, ALT ), bilirubin, epesavak. vizeletvizsgálat: mennyiség, átlátszóság, fehérje, glükóz, bilirubin, keton, vér, urobilinogén, ph. 17
171 Ismételt adagolású toxikológiai vizsgálatok Krónikus etetése toxicitás vizsgálat Értékelendő paraméterek: kórbonctan: elhullott állatok túlélő állatok szervtömeg mérés kórszövettan tényleges hatóanyag felvétel 17
172 Mutagenetikai toxikológiai vizsgálatok Mutagenetikai toxikológiai vizsgálatok 1. AMES teszt (Baktériumos lemez teszt) 2. Emlős csontvelői kromoszóma aberrációs teszt 3. Emlős eritrocita mikronukleusz teszt 4. Rágcsáló domináns letális teszt 17
173 Mutagenetikai toxikológiai vizsgálatok AMES teszt (Baktériumos lemez teszt) A teszt Salmonella typhimurium baktérium törzsekben méri a mutációs rátát. Salmonella typhimurium prototrof hisztidin szintézis. A tesztben a baktérium hisztidin auxotrof törzseit használják. Minél hatékonyabb mutagén a vizsgálati anyag, annál több baktérium revertál és egy adott tartományon belül dózisfüggő hatás mutatkozik. 17
174 Mutagenetikai toxikológiai vizsgálatok A tesztben használt baktériumtörzsek mindegyike hordoz a his- allélon kívül egy az excíziós javító rendszert inaktiváló és egy a baktérium tokjának képződését megakadályozó mutációt. Spontán reverziók száma csökken, a vizsgálati anyagok könnyebben jutnak be a sejtbe. érzékenyebb a teszt 17
175 Mutagenetikai toxikológiai vizsgálatok Az AMES tesztben használt törzsek his- alléljai is különbözőek. Báziscsere és frameshift mutációk találhatók a his allélokon. Így a vizsgálati anyag, különböző törzsekben mutatott reverziós hatékonyságából arra is következtethetünk, hogy milyen mechanizmuson keresztül érvényesül a mutagén hatás. 17
176 Mutagenetikai toxikológiai vizsgálatok Az ember és a Salmonella baktériumok között jelentős az evolúciós távolság, valamint a két élőlény típus között jelentős a fiziológiai különbség. A vizsgált vegyületet önmagában és patkány májából készült enzim kivonattal (S9) előkezelve is tesztelik. 17
177 Mutagenetikai toxikológiai vizsgálatok AMES teszt kivitelezése 1) Steril Petri-csészékbe minimál glukóz-agar (amely hisztidint csak nyomokban tartalmaz!) táptalajt öntenek. 2) Erre helyezik a vizsgálandó anyag oldatát (minimum 5 dózis, S9 mix) + pozitív és negatív kontroll. 3) Sterilizálják a Petri-csészéket. 4) A táptalaj felületére szélesztik az adott Salmonella typhimurium törzset (5 törzs). 5) 37 0 C-os termosztátba helyezik a csészéket óráig. 17
178 Mutagenetikai toxikológiai vizsgálatok 17
179 Mutagenetikai toxikológiai vizsgálatok Az inkubáció után megszámolják a képződött kolóniákat; ha a képződött telepek száma nagyobb, mint a kezeletlen (negatív) kontrollban akkor a vizsgálati anyag mutagén aktivitással bír. Mutagén (genotoxikus) hatásra dózisfüggő kolóniaszám emelkedés figyelhető meg, vagy reprodukálható emelkedés egy vagy több dózisban. 17
180 Mutagenetikai toxikológiai vizsgálatok 18
181 Mutagenetikai toxikológiai vizsgálatok Emlős csontvelői kromoszóma aberrációs teszt Az emlősök kromoszómáit 1952 óta tanulmányozzák. Két felfedezés segítette ezen kísérleti módszerek kifejlesztését: 1. Ha hipotóniás oldattal kezeljük, majd fixáljuk az osztódó sejteket, a kromoszómák kiterülnek, és egymástól eltávolodnak a kromoszómák könnyen vizsgálhatók. 18
182 Mutagenetikai toxikológiai vizsgálatok 2. Mitózis-gátlás kolhicinnel a kromoszómák a metafázisban látszanak a legjobban. 18
183 Mutagenetikai toxikológiai vizsgálatok A kísérleti módszer a vizsgálati anyagok által okozott szerkezeti (strukturális) kromoszóma aberrációk kimutatására alkalmas emlős sejtekben. A szerkezeti kromoszóma aberrációk kromatid és kromoszóma típusú aberrációk lehetnek. 18
184 Mutagenetikai toxikológiai vizsgálatok Kísérleti állatfaj: labor patkány labor egér kínai hörcsög Dózisok: legalább 3 (dóziskereső elővizsgálat) legmagasabb dózis (fővizsgálat) pozitív kontroll csoport kontroll csoport Állatszám: 5/nem/csoport 18
185 Mutagenetikai toxikológiai vizsgálatok Pozitív kontrollként használható vegyületek 18
186 Mutagenetikai toxikológiai vizsgálatok Kezelés: gyomorszonda intraperitoneális injekció A kísérleti állatok 50 %-ának feldolgozása a kezelés után 24 órával. A kísérleti állatok 50 %-ának feldolgozása a kezelés után 48 órával. A feldolgozás előtt intraperitoneális injekció mitózisgátlóval. A sejtek kinyerése a csontvelőből és a kromoszóma aberrációk analízise. 18
187 Mutagenetikai toxikológiai vizsgálatok Közvetlen a kísérleti állatok feldolgozása után a kinyert csontvelőt hipotóniás oldattal kezelik és fixálják. A sejteket tárgylemezre terítik és festik. Analízis: A mitotikus indexet a citotoxicitás mérésével kell meghatározni, amelyet minden kísérleti állat (kezelt, kontroll, pozitív kontroll) esetében legalább 1000 sejten végeznek. 18
188 Mutagenetikai toxikológiai vizsgálatok Mikroszkópos vizsgálat immerziós nagyítással. A kromoszómákat fényképezik és sorba rendezik; a statisztikai értékelést a kontroll adatokhoz viszonyítva végezik. A kísérlet alapegysége a sejt, ezért a kromoszóma aberrációkat tartalmazó sejtek százalékos gyakoriságát kell értékelni. A strukturális aberrációk számát és frekvenciáját kell megadni. 18
189 Mutagenetikai toxikológiai vizsgálatok Értékelés Mutagén (genotoxikus) hatásra dózisfüggő emelkedés figyelhető meg, vagy reprodukálható emelkedés egy vagy több dózisszinten, egy mintavételi időpontban a kromoszóma aberrációt hordozó sejtek számában. 18
190 Mutagenetikai toxikológiai vizsgálatok 19
191 Mutagenetikai toxikológiai vizsgálatok Kromoszóma aberrációk típusa emberi limfocitákban. (A) Chromosome-type aberrations. Tri, tricentrics; Dic, dicentrics; Tr, translocation; del, deletion. (B) Chromatid-type aberrations. (a) chromatid gaps; (b) chromosome gaps; (c) chromatid breaks; (d) chromosome breaks (NUpd: nonunion proximal and distal. NUp: non-union proximal. NUd: non-union distal. SU: sister union). (e-i), chromatid exchanges. C, complete exchange; I, incomplete exchange. 19
192 Mutagenetikai toxikológiai vizsgálatok Emlős eritrocita mikronukleusz teszt Ezen in vivo emlős gyors teszt a testidegen kémiai anyagok által okozott kromoszóma károsodások és/vagy a mitotikus apparátus károsodásának kimutatására alkalmas. A teszt alapja a kezelt állatok polikromáziás eritrocitáiban a mikronukleuszok megszaporodása. 19
193 Mutagenetikai toxikológiai vizsgálatok A mikronukleuszok kromoszóma fragmentumokból vagy teljes kromoszómákból képződnek, amelyek a mitozisban visszamaradnak. Amikor az eritroblaszt eritrocitává fejlődik a sejtmag kilökődik a sejtből, míg a mikronukleusz visszamarad a citoplazmában. 19
194 Mutagenetikai toxikológiai vizsgálatok 19
195 Mutagenetikai toxikológiai vizsgálatok Kísérleti állatfaj: - labor egér - labor patkány Állatszám: 5/nem/csoport (kontroll és pozitív kontroll) Elővizsgálat: a vizsgálati anyag toxicitásának meghatározására maximálisan tolerálható dózis (MTD) megállapítása (toxikus tünetek, esetleg elhullás) Kezelés: gyomorszonda, i.p. gyakoriság: egyszeri (esetenként 2x, 5x 24 órás időközzel) Dózisok: MTD, MTD 75%, MTD 50% 19
196 Mutagenetikai toxikológiai vizsgálatok Pozitív kontrollként használható vegyületek 19
197 Mutagenetikai toxikológiai vizsgálatok Feldolgozás: a kezelést követő 24. és 48. órában, csontvelői kenet készítése a femurból, a kenet festése May-Grünwald vagy Giemsa szerint. 19
198 Mutagenetikai toxikológiai vizsgálatok Mikroszkópos vizsgálat A mikronukleált polikromáziás eritrociták gyakoriságának megállapítása (MPCE) állatonként 2000 polikromáziás eritrocitát értékelnek a mikronukleusz incidenciára. A PCE/NC arány eritrociták arányát állatonként 1000 eritrocita leszámolása alapján határozzák meg. 19
199 Mutagenetikai toxikológiai vizsgálatok 19
200 Mutagenetikai toxikológiai vizsgálatok 20
201 Mutagenetikai toxikológiai vizsgálatok Értékelés Mutagén (genotoxikus) hatásra dózis és/vagy időfüggő emelkedés figyelhető meg a mikronukleált polikromáziás eritrociták előfordulásában, vagy egy ponton (idő, vagy dózis), két kísérletben előforduló mikronukleált polikromáziás eritrocita emelkedés. 20
202 Mutagenetikai toxikológiai vizsgálatok Értékelés A pozitív eredmény azt jelzi, hogy a vizsgálati anyag kromoszómatörést okoz, vagy megzavarja a húzórostok működését. Ebből arra következtethetünk, hogy ilyen károsodások előfordulhatnak más szövetben és más emlős fajokban, beleértve az embert is. Negatív eredmény esetén a vizsgálati anyag ilyen károsodást nem okoz, de nem zárható ki, hogy más szövetben vagy más fajon nem indukál-e ilyen károsodást. 20
203 Mutagenetikai toxikológiai vizsgálatok Rágcsáló domináns letális teszt Általánosan elfogadott tény, hogy a domináns letális mutációk kromoszóma károsodások (strukturális és numerikus aberrációk) következményei. A domináns letális mutáció az ivarsejtekben jelentkezik és nem eredményezi az ivarsejtek diszfunkcióját, viszont az embrió vagy a magzat halálát okozza. 20
204 Mutagenetikai toxikológiai vizsgálatok A hím állatokat kezelik a vizsgálati anyaggal, és kezeletlen szűz nőstényekkel pároztatják. A spermiogenezis egyes stádiumai külön-külön kerülnek vizsgálatra úgy, hogy megfelelő időközönként kezeletlen szűz nőstényekkel végzik el a pároztatást. A domináns letális mutáció értékelése a nőstény állatokon történik. 20
205 Mutagenetikai toxikológiai vizsgálatok 20
206 Mutagenetikai toxikológiai vizsgálatok Kísérleti állatfaj: - labor patkány - labor egér Állatszám: pároztatási intervallumonként vemhes nőstény/dózis (negatív és pozitív kontroll) (ivararány 1-1, 1-2) Kezelés: - gyomorszonda, i.p. Dózisok: 3 (legmagasabb toxikus) 20
207 Mutagenetikai toxikológiai vizsgálatok Pároztatás a spermiogenezis egyes stádiumai szerint kezeletlen szűz nőstényekkel: egér: 1-2, 3-4, 5-8 hét patkány: 1-4, 5-6, 7-10 hét Vemhesülés eredményének megállapítása hüvelykenettel. 20
208 Mutagenetikai toxikológiai vizsgálatok A vemhes nőstények exterminálása a vemhesség második felében (14. nap). Kórbonctani vizsgálat: méh tartalmának vizsgálata élő és elhalt implantátumok petefészek vizsgálata sárgatestek 20
209 Mutagenetikai toxikológiai vizsgálatok Posztimplantációs veszteség Az elhalt implantátumok nőstényenkénti számának növekedése a kontrollhoz képest (elhalt implantátum a teljes implantátumhoz viszonyítva). Preimplantációs veszteség Sárgatestek száma összevetve az összes implantátum nőstényenkénti számával. 20
210 Mutagenetikai toxikológiai vizsgálatok Értékelés Össz domináns letális hatás preimplantációs veszteség + posztimplantációs veszteség Az implantátumok számának egy adott intervallumban bekövetkező csökkenése sejtpusztulás (spermatociták és spermatogóniumok pusztulásának) következménye lehet (ivarsejtekben genotoxikus hatás). 21
211 Mutagenetikai toxikológiai vizsgálatok A) Kémiai szerkezet/fiz.kém. tulajdonságok B) IN VITRO GENOTOXIKOLÓGIAI TESZTEK génmutáció vizsgálata prokariótán AMES TESZT klasztogén (aneugén) hatás vizsgálata kínai hörcsög ovárium (CHO) sejten vagy humán perifériás lymphocytán KROMOSZÓMA ABERRÁCIÓS TESZT (-) (-) (+/±) nem genotoxikus nem genotoxikus genotoxikus minimális vagy masszív vagy szűk körű expozíció széles körű expozíció nincs további teendő 21
212 Mutagenetikai toxikológiai vizsgálatok C) IN VIVO TESZT SZOMATIKUS CÉLSEJTEN (rágcsáló csontvelői sejten) MIKRONUKLEUSZ TESZT vagy metafázis analízis (-) (-) (+) nem genotoxikus, nem genotoxikus, de in vivo genotoxikus de myelotoxikus nem is myelotoxikus szomatikus sejtben nincs további más célszerv nagy valószínűséggel genotoxikus teendő lehetséges humán karcinogén D) IN VIVO TESZT GERMINÁLIS CÉLSEJTEN (rágcsáló hím ivarsejten) DOMINÁNS LETÁLIS TESZT Célszerv és epigenetikus mechanizmus kutatás (-) (+) cytotoxikus in vivo nem in vivo germinális mutagén mitogén germinális peroxiszóma proliferátor mutagén nagy valószínűséggel humán hormonális hatású germinális mutagén tumor promoter DNS metiláció gátló CARCINOGENITÁSI VIZSGÁLAT (MTD két évig, két rágcsáló immunszuppresszor fajon) minden esetben elvégzendő masszív és/vagy széleskörű szilárd test expozíció esetén 21
213 Engedélyezési célú toxikológiai vizsgálatok 1. Engedélyezési célú toxikológiai vizsgálatok laborállatokon 2. Engedélyezési célú ökotoxikológiai vizsgálatok 21
214 Engedélyezési célú ökotoxikológiai vizsgálatok Az ökotoxikológiai vizsgálatok rendszere Szárazföldi környezet Madarak és emlősök Hasznos ízeltlábúak Makro és mikro talajlakó szervezetek Nem-cél növények Szennyvíz telepek Vízi környezet Halak Gerinctelenek Algák Vízi növények Üledéklakók 21
215 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Ökotoxikológiai vizsgálatok madarakon 1. Akut orális toxicitási vizsgálat madarakon 2. Etetéses toxicitási vizsgálat madarakon 3. Egy generációs reprodukciós toxicitási vizsgálat madarakon 4. Elfogadási/visszautasítási vizsgálat madarakon 5. Modell üzemi vizsgálat madarakon 6. Szabadföldi vadtoxikológiai vizsgálat 21
216 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Akut orális toxicitási vizsgálat madarakon A kísérlet elrendezése Legalább 5 dózis + 1 kontroll 10 madár/dózis A vizsgálat fázisai Akklimatizáció: 2 hét Kezelés: egyszer, orális Utómegfigyelés: 2 hét Értékelendő paraméterek Tünetek Takarmányfogyasztás Testtömeg Kórbonctani eredmények Eredmények LD 50, NOAEL értékek 21
217 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Etetéses toxicitási vizsgálat madarakon A kísérlet elrendezése Legalább 5 koncentráció + 1 kontroll 10 madár(fiatalok)/koncentráció A vizsgálat fázisai Akklimatizáció: 3 nap Expozíció: 5 nap (preparált takarmány) Utómegfigyelés: 2 hét Vizsgált paraméterek Tünetek Takarmányfogyasztás Testtömeg Kórbonctani eredmények Eredmények LC 50, NOAEC értékek 21
218 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Egy generációs reprodukciós toxicitási vizsgálat madarakon A kísérlet elrendezése Legalább 3 koncentráció+ 1 kontroll 36 madár/koncentráció A vizsgálat fázisai Akklimatizáció: 2 hét Expozíció: 6 (20) hét (preparált takarmány) Utómegfigyelés: 2 hét Utód megfigyelés: 2 hét 21
219 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Vizsgált paraméterek Tünetek Takarmányfogyasztás Testtömeg Kórbonctani eredmények Reprodukciós paraméterek (tojás paraméterek, utódok) Eredmény NOAEC érték 21
220 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Elfogadási/visszautasítási vizsgálat madarakon A kísérlet elrendezése madár/koncentráció A vizsgálat fázisai Akklimatizáció: 7 nap Expozíció: 1-5 nap (naponta max. 8 óra) (Expozíció előtt 16 órás éheztetés) Utómegfigyelés: 2 hét Vizsgált paraméterek Tünetek Takarmányfogyasztás Testtömeg Kórbonctani eredmények Eredmények A vizsgálati anyag elfogadás/visszautasítása 22
221 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 22
222 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 22
223 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Modell üzemi vizsgálat madarakon A kísérlet elrendezése 8 pár fürj, 3 hím 9 tojó tőkésréce A vizsgálat fázisai Akklimatizáció: 14 nap Expozíció: vizsgálati céltól függ Utómegfigyelés: 21 nap Vizsgált paraméterek Tünetek Takarmányfogyasztás, levélcsipkedés Testtömeg Kórbonctani eredmények (szövettani vizsgálat lehetséges) Eredmények Félszabadföldi körülmények között megfigyelhető letális és/vagy szubletális hatások, repellencia 22
224 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Szabadföldi vadtoxikológiai vizsgálat Kísérleti állatok A vizsgálati területen és annak közvetlen közelében élő, a területet rendszeresen, vagy alkalmilag látogató madarak és emlősök. 22
225 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken A vizsgálat fázisai Elő megfigyelés: legkevesebb 3 nap Kezelés: vizsgálati anyagtól függ Utómegfigyelés: az expozíciótól függ, de legalább l0 nap Vizsgált paraméterek A vadfajok egyedszáma, viselkedése, elhelyezkedése, mozgása Tünetek Kórbonctani eredmények A növényállomány fenológiája és a vadkár mértéke Speciális megfigyelések a vizsgálati céltól függően 22
226 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Eredmények Szabadföldi körülmények között, a valóságos expozíció mellett megfigyelhető esetleges káros hatások. 22
227 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Méheken végzett ökotoxikológiai vizsgálatok 1. Akut orális toxicitási teszt méheken 2. Akut kontakt toxicitási teszt méheken 3. Kontakt szermaradék toxicitási teszt méheken 4. Modell üzemi vizsgálat méheken 5. Szabadföldi vizsgálat méheken 22
228 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 22
229 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 22
230 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Akut orális és kontakt toxicitási teszt méheken Az állatok tartása: 4 cm magas, henger alakú izolátorokban Etetés: ad libitum 50 w/v %-os cukorszirup Az állatok előkészítése: CO 2 gázzal kábítás A kezelés előtti 2 órában éheztetés 23
231 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kezelés módja: Orális kezelés: a vizsgálati anyagot cukorszirupban 100 vagy 200 μl/méh mennyiségben Kontakt kezelés: az elkábított méhek torának dorzális részére mikro pipettával vagy mikro-applikátorral 1 μl/méh mennyiségben Környezeti feltételek: 25 ± 2 C, % páratartalom, sötétség 23
232 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 23
233 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Koncentrációk a fővizsgálatban: Legalább 5 Kontroll csoport: Tiszta cukor szirup az orális kezelésnél, illetve oldószer a kontakt kezelésnél Referencia anyag: Legalább 3 dózissal Az állatok száma: 30/dózis, izolátoronként 10/izolátor, vizsgálatban legalább kontroll limit tesztben legalább 30 kezelt + 30 kontroll Kezelés(expozíció): az oldatok elfogyasztásáig legfeljebb 6 óra (orális), illetve egyszeri (kontakt) 23
234 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Utómegfigyelés: 48 óra (legfeljebb 96 óra) Értékelés: mortalitás a és 48. órában, a megfigyelt tünetek leírása, a tesztoldat fogyasztásának mértéke Eredmény: LD 50, NOAEC, LOAEC A vizsgálat érvényessége: a mortalitás a kontroll csoportban legfeljebb 10 % 23
235 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kontakt szermaradék toxicitási teszt méheken Az állatok tartása és az expozíció módja: hasonló az akut vizsgálatokéhoz csak a ketrec nagyobb és a méheket a vizsgálati anyaggal permetezett növényzettel (kb. 15 g/izolátor) együtt tartják az izolátorokban Környezeti feltételek: C, % pára, sötétség Az állatok száma: legalább 6 ismétlés/dózis, izolátoronként 25 23
236 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Permetezés és növényzet: a permetezés kis méretű parcellákon, általában lucernán, mikroparcella permetezővel történik. Dózisok: ajánlott a legmagasabb gyakorlati dózis, de emellett lehet alacsonyabb vagy provokált (3x-os, 5x-ös) dózist is alkalmazni. Kontroll csoport: tiszta vízzel permetezett növényzet Referencia anyag: magas dózissal 23
237 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Növény mintavételek és expozíciók: permetezéstől számított és 24. órában (szükség esetén ) növény-mintavétel, majd a méhek exponálása 24 órán keresztül Értékelés: mortalitás és tünetek megfigyelése legalább egyszer az expozíciók első 4 órájában és a 24. órában Eredmény: az a legkorábbi növényminta-vételezési időpont amelyet követően a kezelt csoportokban a mortalitás 25 % alatti volt. Amennyiben ez az időpont 24 óránál több, az a legkorábbi növényminta-vételezési időpont, amelyet követően a kezelt csoportokban a mortalitás jelentősen nem tér el a kontrolltól 23
238 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Modell üzemi vizsgálat méheken Az állatok tartása: kis populáció méretű méhcsaládok kaptárakban, virágzó növényzetet tartalmazó izolátorokban. Az izolátorok 6 m szélesek, 9 m hosszúak és 2 m magasak, oldalainak belső szélén 0,5 m szélességben növényzettől mentes megfigyelő sávok kerülnek kialakításra. A növényzet 40 m 2 (2 x 8 m x 2,5 m). Etetés ad libitum 50 w/v %-os cukorszirup oldattal. A kaptárakra hullacsapda kerül. J e lm a g y a rá z a t: - k a p tá r - n ö v é n yz e t - m e g fig y e lő s á v - k ö z le k e d ő fo ly o s ó - ita tó /e te tő e d é n y 23
239 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken K o n to ll K1 K e z e lt T1 K o n to ll K2 ú R e fe re n c ia K e z e lt t R2 T2 bokr ok R e fe re n c ia R1 K o n to ll K3 R e fe re n c ia R3 K e z e lt T3 A méhcsaládok száma: dózisonként legalább 3, izolátoronként 1 (a kontroll csoport is) Dózisok: ajánlott a legmagasabb gyakorlati dózis, de emellett lehet alacsonyabb vagy provokált (3x-os, 5x-ös) dózist is alkalmazni. Kontroll csoport: tiszta vízzel permetezett növényzeten Referencia anyag: magas dózissal 23
240 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 24
241 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 24
242 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Permetezés: kis méretű parcellákon, mikroparcella permetezővel 24
243 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kísérleti periódusok: Elő megfigyelés: 2-3 nap, amíg a méhek megszokják az izolátort Permetezés: egyszeri vagy többszöri, a vizsgálati célnak megfelelően lehet este, hajnalban vagy a méhek intenzív gyűjtési időszakában Utómegfigyelés: legalább 7 nap Értékelés: Mortalitás: naponta a hullacsapdában és a megfigyelősávban Viráglátogatottság és a méhek viselkedése: 1 m 2 -es mérő parcellákon a kezelés előtt és a kezelés után több alkalommal A méhcsaládok erőnléte (népesség becslés): a kezelés előtt és a kísérlet végén A fiasítás állapota, nagysága és összetétele: a kezelés előtt és a kísérlet végén az összes lép megvizsgálásával Mindezt kiegészítheti analitikai vizsgálat is 24
244 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken t A vizsgálat érvényessége: Ne legyen jelentős mortalitás a kontroll csoportban, legyen jelentős mortalitás a referencia csoportban. 24
245 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Szabadföldi vizsgálat méheken Az állatok tartása: a kaptárak a vizsgálati területek közvetlen közelében, a kaptárakon hullacsapdák A méhcsaládok száma: területenként legalább 3 Vizsgálati területek: legalább két (kezelt és kontroll) hasonló ökológiai adottságú (talajtípus, fajta, agronómiai körülmények) jól izolált terület Dózis: a legmagasabb gyakorlati dózis Kontroll terület: kezeletlen vagy referencia anyaggal kezelt 24
246 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kísérleti periódusok: Elő megfigyelés: 2-5 nap, a méhcsaládok kitelepítése általában a virágzás kezdetén történik Permetezés: egyszeri vagy többszöri, a vizsgálati célnak megfelelően lehet este, hajnalban vagy a méhek intenzív gyűjtési időszakában Utómegfigyelés: általában a virágzás végéig 24
247 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Értékelés: Mortalitás: naponta hullacsapdában Viráglátogatottság és a méhek viselkedése: mérő sávokon a kezelés előtt és a kezelés után több alkalommal A méhcsaládok erőnléte (népesség becslés): a kezelés előtt és a kísérlet végén A fiasítás állapota, nagysága és összetétele: a kezelés előtt és a kísérlet végén az összes lép megvizsgálásával Mindezt kiegészítheti analitikai vizsgálat, kaptártömeg mérése 24
248 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Hasznos ízeltlábúakon végzett ökotoxikológiai vizsgálatok 1. Typlodromus pyri ízeltlábún végzett teszt 2. Aphidius rhopalosiphi ízeltlábún végzett teszt 3. Poecilus cupreus ízeltlábún végzett teszt 4. Chrysoperla carnea ízeltlábún végzett teszt 24
249 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 24
250 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 25
251 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken M ű a n y a g tá l T e s z t-a ré n a A Typlodromus pyri törzsfenntartása R o v a re n y v Ü v e g b o to c s k a Ü v e g la p V íz F e d ő le m e z S z iv a c s M ű a n y a g tá l T ö rlő k e n d ő 25
252 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 25
253 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Typlodromus pyri ízeltlábún végzett teszt Vizsgálati paraméterek: mortalitás szaporodás kikelési ráta A vizsgálat két szakasza: 1. Mortalitás 2. Szubletális hatások Referencia anyag: dimetoát hatóanyagú készítmény Környezeti paraméterek: 25 2 ºC % rel. páratartalom fényerősségmérés 16 óra világos/8 óra sötét 25
254 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 25
255 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 1. Szakasz Állatszám: 100 protonimfa/tesztcsoport Tesztcsoportok: 1 kontroll 5 kísérleti anyaggal kezelt 1 referencia anyaggal kezelt Párhuzamosok: 5 az összes tesztcsoportban A teszt időtartama: 7 nap 2. Szakasz Állatszám: életben maradtak (5 nőstény / 1 hím) Tesztcsoportok : 1 kontroll 3 kísérleti anyaggal kezelt (ahol a mortalitás < 50%) Párhuzamosok: 5 a kontrollban 3 a kezelt csoportban A teszt időtartama: 7 nap 25
256 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kezelés: 200 l/ha Etetés: Pinus sylvestris pollen Megfigyelések: - Mortalitás (1.szakasz) - A nőstények, hímek, peték és lárvák számának meghatározása (2. szakasz) - Kikelési ráta meghatározása Eredmények értékelése: - Mortalitás - Szaporodás - Összhatás - Statisztika 25
257 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 25
258 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 25
259 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 25
260 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Aphidius rhopalosiphi ízeltlábún végzett teszt A vizsgálat szakaszai: 1. Mortalitás 2. Szubletális hatások Referencia anyag: dimetoát hatóanyagú készítmény Környezeti paraméterek: 20 3 ºC % rel. páratartalom 1. sz.: lux, 2. sz.: lux 16 óra világos/8 óra sötét 26
261 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 26
262 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 1. Szakasz Állatszám: 5 hím és 5 őstény/párhuzamos Tesztcsoportok: 1 kontroll 1 kísérleti anyaggal kezelt 1 referencia anyaggal kezelt Párhuzamosok: 4 a kontrollban 4 a kezelt csoportban 1 a referencia anyaggal kezelt A teszt időtartama: 48 óra 2. Szakasz Állatszám: 1 nőstény darázs/párhuzamos Tesztcsoportok: 1 kontroll 1 kísérleti anyaggal kezelt Párhuzamosok: 14 a kontrollban 14 a kezelt csoportban A teszt időtartama: nap 26
263 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kezelés: 200 l/ha Etetés: 1:2 méz/víz arányú keverék a vattacsomóra Megfigyelések: - Mortalitás és tünetek(1. szakasz) - A szaporodás megfigyelése(2. szakasz) Eredmények értékelése: - Százalékos mortalitás - Korrigált mortalitás - Statisztika mortalitásra és szaporodásra 26
264 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 26
265 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 26
266 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Poecilus cupreus ízeltlábún végzett teszt Vizsgálati paraméterek: A vizsgálat időtartama: Állatszám: Tesztcsoportok : Párhuzamosok: Referencia anyag: mortalitás viselkedésben megnyilvánuló hatások legalább 14 nap 15 hím és 15 nőstény/koncentráció 1 kísérleti anyaggal kezelt 1 referencia anyaggal kezelt 5 az összes tesztcsoportban metil-paration hatóanyagú készítmény Környezeti paraméterek: 20 2 ºC % rel. páratartalom lux 16 óra világos/8 óra sötét 26
267 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 26
268 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 26
269 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Chrysoperla carnea ízeltlábún végzett teszt A vizsgálat szakaszai: Referencia anyag: 1. Lárvaállapot 2. Bebábozódás 3. Imágók 4. Peték dimetoát hatóanyagú készítmény Környezeti paraméterek: 24 2 ºC % rel. páratartalom ~ 1000 lux 16 óra világos/8 óra sötét 26
270 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Kezelés Etetés: lárvák lepkepete, imágók mesterséges táplálék Megfigyelések: - Lárvák mortalitása - Bebábozódás - Abnormális fejlődés - Peték száma és a lárvák kelési aránya a reprodukciós fázisban Eredmények értékelése - Lárvák, bábok és imágók mortalitása - Korrigált mortalitás - Statisztika mortalitásra és szaporodásra 27
271 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Makro és mikro talajlakó szervezeteken végzett ökotoxikológiai vizsgálatok 1. Giliszta toxikológiai vizsgálatok Szűrőpapír teszt földigilisztán Mesterséges talajteszt földigilisztán Reprodukciós teszt földigilisztán 27
272 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 2. Egyéb talajlakó organizmusok végzett ökotoxikológiai vizsgálatok Collembola teszt (talajlakó ugróvillás) Enchytraeus teszt (közönséges televényféreg) Csiga teszt Nitrogén és szén transzformációs teszt 27
273 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Szűrőpapír teszt földigilisztán A kísérlet elrendezése Legalább 5 koncentráció 10 giliszta/koncentráció A vizsgálat fázisai Expozíció: 48 óra (preparált szűrőpapír) Utómegfigyelés: 24 óra Vizsgált paraméterek Tünetek Eredmények LC 50, NOAEC értékek 27
274 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 27
275 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Mesterséges talajteszt földigilisztán A kísérlet elrendezése Legalább 5 koncentráció 4 ismétlés/koncentráció 10 giliszta/koncentráció A vizsgálat fázisai Akklimatizáció: 1 nap Expozíció: 14 nap (preparált talaj) Vizsgált paraméterek Tünetek Testtömeg Eredmények LC 50, NOAEC értékek 27
276 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Reprodukciós teszt földigilisztán A kísérlet elrendezése Legalább 2 koncentráció (4 ismétlés/konc.) 10 giliszta/koncentráció A vizsgálat fázisai Akklimatizáció: 1 nap Expozíció: 28 nap (preparált talaj) Inkubáció: 28 nap Vizsgált paraméterek Tünetek Takarmányfogyasztás Testtömeg Fiatal giliszták száma Eredmények NOAEC érték 27
277 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken Egyéb talajlakó organizmusok végzett ökotoxikológiai vizsgálatok Collembola teszt - talajlakó ugróvillás Enchytraeus teszt - közönséges televényféreg Csiga teszt Nitrogén és szén transzformációs teszt A N és C lebontásában, körforgásában résztvevő talaj mikroorganizmusok laboratóriumi tesztelését minden, a talajra jutó növényvédő szer esetén el kell végezni. 27
278 Ökotoxikológiai vizsgálatok szárazföldi élőszervezeteken 27
279 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Vízi élőszervezeteken végzett ökotoxikológiai vizsgálatok 1. Halakon végzett akut toxicitási vizsgálat 2. Halakon végzett krónikus toxicitási vizsgálat 3. Halivadékokon végzett krónikus toxicitási vizsgálat 4. A halak korai életszakaszára vonatkozó toxicitási vizsgálat 5. Reprodukciós toxicitási vizsgálat halakon 6. Akut immobilizációs vizsgálat Daphnia fajokon 7. Reprodukciós toxicitási vizsgálat Daphnia magnán 8. Édesvízi alga és cyanobaktérium növekedésére gyakorolt gátló hatás vizsgálata 9. Vízi növényre gyakorolt hatás 10. Üledéklakó árvaszúnyogokon végzett toxicitási vizsgálat 27
280 Ökotoxikológiai vizsgálatok vízi élőszervezeteken A vízi szervezetekre gyakorolt károsító hatást szükséges becsülni, ha a hatóanyag (készítmény) elérheti a felszíni vizet. Ha a hatóanyagot tartalmazó készítmény az előírt használat betartása mellett nem kerülhet érintkezésbe a felszíni vízzel, a toxikológiai osztályba sorolás céljából akkor is kell hal, Daphnia sp., alga akut toxicitás adat. 28
281 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Halakon végzett akut toxicitási vizsgálat Kísérleti állatok Szivárványos pisztráng, guppi, rizshal Zebradánió, ponty Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 7 hal/koncentráció Kísérleti fázisok Kezelés: 96 óra Megfigyelés: 96 óra Kísérleti paraméterek Klinikai tünetek (24, 48, 72, 96 órás mortalitás) ph mérése, oldott oxigén, hőmérséklet Eredmények LC 50 (96 órás), elhullást nem okozó max. cc., 100%-os elhullást okozó min. cc. 28
282 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Halakon végzett krónikus toxicitási vizsgálat Kísérleti állatok Szivárványos pisztráng, guppi, rizshal Zebradánió, ponty Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 7 hal/koncentráció Kísérleti fázisok Kezelés: 14 nap Megfigyelés: 14 nap Kísérleti paraméterek Klinikai tünetek ph mérése, oldott oxigén, hőmérséklet Eredmények elhullást nem okozó max. cc., 100%-os elhullást okozó min. cc., NOAEC (14 napos) 28
283 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Halivadékokon végzett krónikus toxicitási vizsgálat Kísérleti állatok Szivárványos pisztráng, rizshal, zebradánió Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 7 hal/koncentráció Kísérleti fázisok Kezelés: 28 nap Megfigyelés: 28 nap Kísérleti paraméterek Klinikai tünetek Testtömeg ph mérése, oldott oxigén, hőmérséklet Eredmények NOAEC (28 napos), LOAEC (28 napos) 28
284 Ökotoxikológiai vizsgálatok vízi élőszervezeteken A halak korai életszakaszára vonatkozó toxicitási vizsgálat Kísérleti állatok Szivárványos pisztráng, rizshal, zebradánió Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 30 ikra/koncentráció Kísérleti fázisok Kezelés: a kontroll állatok önálló táplálkozásáig (pisztráng 60 nap kelés után, zebradánió 30 nap kelés után ) Megfigyelés: a kontroll állatok önálló táplálkozásáig 28
285 Ökotoxikológiai vizsgálatok vízi élőszervezeteken A halak korai életszakaszára vonatkozó toxicitási vizsgálat Kísérleti paraméterek Klinikai tünetek (embriófejlődés állapotai, kelés és túlélés, makroszkópos elváltozások és rendellenes viselkedés) Testtömeg Testhossz ph mérése, oldott oxigén, hőmérséklet Eredmények NOAEC, LOAEC értékek 28
286 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Reprodukciós toxicitási vizsgálat halakon Kísérleti állatok Zebradánió, fathead minnow, medaka Kísérleti elrendezés Legalább 3 koncentráció + 1 kontroll 2 ismétlés/koncentráció 5 hím és nőstény hal/koncentráció Kísérleti fázisok Akklimatizáció: 1-2 hét Kezelés: 21 nap (nemi dimorfizmus, ívás) Megfigyelés: 21 nap 28
287 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Reprodukciós toxicitási vizsgálat halakon Kísérleti paraméterek Klinikai tünetek (túlélés, viselkedés és megjelenés, termékenység) ph mérése, oldott oxigén, hőmérséklet Kórbonctan Másodlagos ivari jelleg Vérvétel VTG analízis (zebradánió, fathead minnow) Fej/farok VTG analízis (zebradánió) VTG analízis májból (medaka) Kórszövettan Ivari mirigyek (here, petefészek) Eredmények Reprodukcióra gyakorolt káros hatás 28
288 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Akut immobilizációs vizsgálat Daphnia fajokon Kísérleti állatok Daphnia magna, Daphnia pulex Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 20 állat/koncentráció Kísérleti fázisok Kezelés: 48 óra Megfigyelés: 48 óra Kísérleti paraméterek Klinikai tünetek (immobilizáció; viselkedés és megjelenés) ph mérése, oldott oxigén, hőmérséklet Eredmények EC 50 (24 órás) és EC 50 (48 órás) 28
289 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Reprodukciós toxicitási vizsgálat Daphnia magnán Kísérleti állat Daphnia magna Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 40 állat/koncentráció Kísérleti fázisok Kezelés: 21 nap Megfigyelés: 21 nap Kísérleti paraméterek Klinikai tünetek (utódok, mortalitás, szülő állatok hossza) ph mérése, oldott oxigén, hőmérséklet Eredmények LOAEC és NOAEC értékek 28
290 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Édesvízi alga és cyanobaktérium növekedésére gyakorolt gátló hatás vizsgálata Kísérleti szervezetek Selenastrum capricornutum, Scenedesmus subspicatus Navicula pelliculosa, Anabaena flos-aquae Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 3 ismétlés/koncentráció Kísérleti fázisok Kezelés: 72 óra Kísérleti paraméterek Alga biomassza mérése (sejtszámlálás, sejttérfogat, optikai érzékenység, száraz tömeg) Eredmények EC 50 (72 órás),noaec (72 órás), LOAEC (72 órás) 29
291 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Vízi növényre gyakorolt hatás Kísérleti szervezetek Lemna gibba Lemna major Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 3 ismétlés/koncentráció Kísérleti fázisok Kezelés: 7 nap Kísérleti paraméterek Levélszám Változások a növény fejlődésében (levél méret, külső megjelenés, necrosis vagy chlorosis jelei, gyökér hossz ) Teljes levélterület, száraz tömeg és nedves tömeg Eredmények EC 50,NOAEC, LOAEC 29
292 Ökotoxikológiai vizsgálatok vízi élőszervezeteken Üledéklakó árvaszúnyogokon végzett toxicitási vizsgálat Kísérleti állatok Chironomus riparius, C. tentans, C. yohimatsui Kísérleti elrendezés Legalább 5 koncentráció + 1 kontroll 20 larva/koncentráció Kísérleti fázisok Kezelés: max. 28 nap C. riparius (65 nap C. tentans) Kísérleti paraméterek Előbukkanás (fejlődési idő, nőstény és hím szúnyogok száma, viselkedés) Növekedés és túlélés (immobilitás elhalás, száraz tömeg) ph mérése, oldott oxigén, hőmérséklet Eredmények EC 50, NOAEC, LOAEC értékek 29
293 Felhasznált források Kállai L. (2003): Laborállat könyv. Kallé-K Kft. kiadó, Budapest. OECD Guidelines for the Testing of Chemicals - Test 401 Acute oral toxicity - Test 402 Acute dermal toxicity - Test 403 Acute inhalation toxicity - Test 404 Acute Dermal Irritation/Corrosion - Test 405 Acute Eye Irritation/Corrosion - Test 420 Acute Oral Toxicity Fixed Dose Procedure - Test 423 Acute Oral Toxicity Acute Toxic Class Method - Test 425 Acute Oral Toxicity Up-and-Down-Procedure 29
294 Felhasznált források OECD Guidelines for the Testing of Chemicals - Test 406 Skin Sensitisation - Test 407 Repeated Dose 28-Day Oral Toxicity Study in Rodents - Test 408 Repeated Dose 90-day Oral Toxicity Study in Rodents - Test 409 Repeated Dose 90-day Oral Toxicity Study in Non-Rodents - Test 414 Prenatal Developmental Toxicity Study - Test 416 Two-Generation Reproduction Toxicity Study - Test 452 Chronic Toxicity Studies - Test 471 Bacterial Reverse Mutation Test 29
295 Felhasznált források OECD Guidelines for the Testing of Chemicals - Test 474 Mammalian Erythrocyte Micronucleus Test - Test 475 Mammalian Bone Marrow Chromosome Aberration Test - Test 478 Rodent Dominant Lethal Test - Test 223 Avian Acute Oral Toxicity Test - Test 205 Avian Dietary Toxicity Test - Test 206 Avian Reproduction Test - Test 213 Honeybees, Acute Oral Toxicity Test - Test 214 Honeybees, Acute Contact Toxicity Test - Test 207 Earthworm, Acute Toxicity Tests - Test 222 Earthworm Reproduction Test 29
296 Felhasznált források OECD Guidelines for the Testing of Chemicals - Test 203 Fish, Acute Toxicity Test - Test 215 Fish, Juvenile Growth Test - Test 229 Fish Short Term Reproduction Assay - Test 202 Daphnia sp., Acute Immobilisation Test - Test 211 Daphnia magna Reproduction Test - Test 201 Freshwater Alga and Cyanobacteria, Growth Inhibition Test - Test 221 Lemna sp. Growth Inhibition Test - Test 218 Sediment-water chironomid toxicity test using spiked water 29
297 Köszönöm a figyelmet! Készítette: Dr. Budai Péter Georgikon Kar Növényvédelmi Intézet AZ ELŐADÁS LETÖLTHETŐ: -
GYÓGYSZERÁRTALMAK GYÓGYSZERBIZTONSÁG GYÓGYSZERBIZTONSÁG GYÓGYSZERVIZSGÁLATOK GYÓGYSZERFEJLESZTÉS ELİADÓ DR. LEHEL JÓZSEF ÚJ ANYAG
 GYÓGYSZERÁRTALMAK GYÓGYSZERBIZTONSÁG ELİADÓ DR. LEHEL JÓZSEF GYÓGYSZERBIZTONSÁG GYÓGYSZERVIZSGÁLATOK GYÓGYSZERFEJLESZTÉS ÚJ ANYAG MINİSÉG HATÉKONYSÁG PREKLINIKAI ÁRTALMATLANSÁG KÖRNYEZETBIZTONSÁG KÉMIAI
GYÓGYSZERÁRTALMAK GYÓGYSZERBIZTONSÁG ELİADÓ DR. LEHEL JÓZSEF GYÓGYSZERBIZTONSÁG GYÓGYSZERVIZSGÁLATOK GYÓGYSZERFEJLESZTÉS ÚJ ANYAG MINİSÉG HATÉKONYSÁG PREKLINIKAI ÁRTALMATLANSÁG KÖRNYEZETBIZTONSÁG KÉMIAI
Toxicological Research Center
 IN VIVO ÉS IN VITRO GENOTOXIKOLÓGIAI VIZSGÁLATI MÓDSZEREK TAPASZTALATAI A VÁLTOZÓ MÓDSZERTANI KÖVETELMÉNYEK ÉS JOGSZABÁLYOK TÜKRÉBEN Vértesi Adél, Béres Erzsébet, Sebestyén István, Hirka Gábor, Toxi-Coop
IN VIVO ÉS IN VITRO GENOTOXIKOLÓGIAI VIZSGÁLATI MÓDSZEREK TAPASZTALATAI A VÁLTOZÓ MÓDSZERTANI KÖVETELMÉNYEK ÉS JOGSZABÁLYOK TÜKRÉBEN Vértesi Adél, Béres Erzsébet, Sebestyén István, Hirka Gábor, Toxi-Coop
Házi egér ,12% Vándorpatkány ,82% Tengerimalac ,66% Szíriai aranyhörcsög 16 0,01% Lófélék (lovak, szamarak és öszvérek)
 Uniós adatszolgáltatás Kínai törpehörcsög Kínai törpehörcsög Mongol futóegér 42 0,02% Mongol futóegér 0,04% Ismételt felhasználás Egyéb rágcsálók 86 0,04% Egyéb rágcsálók 0,08% Nem 194381 96,72% Házi nyúl
Uniós adatszolgáltatás Kínai törpehörcsög Kínai törpehörcsög Mongol futóegér 42 0,02% Mongol futóegér 0,04% Ismételt felhasználás Egyéb rágcsálók 86 0,04% Egyéb rágcsálók 0,08% Nem 194381 96,72% Házi nyúl
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
2.6.16. VIZSGÁLATOK IDEGEN KÓROKOZÓKRA HUMÁN ÉLŐVÍRUS-VAKCINÁKBAN
 2.6.16. Vizsgálatok idegen kórokozókra Ph.Hg.VIII. - Ph.Eur.7.0 1 2.6.16. VIZSGÁLATOK IDEGEN KÓROKOZÓKRA HUMÁN ÉLŐVÍRUS-VAKCINÁKBAN 01/2011:20616 Azokhoz a vizsgálatokhoz, amelyekhez a vírust előzőleg
2.6.16. Vizsgálatok idegen kórokozókra Ph.Hg.VIII. - Ph.Eur.7.0 1 2.6.16. VIZSGÁLATOK IDEGEN KÓROKOZÓKRA HUMÁN ÉLŐVÍRUS-VAKCINÁKBAN 01/2011:20616 Azokhoz a vizsgálatokhoz, amelyekhez a vírust előzőleg
2006R1907 HU 20.02.2009 004.001 147
 2006R1907 HU 20.02.2009 004.001 147 VIII. MELLÉKLET A LEGALÁBB 10 TONNA MENNYISÉGBEN GYÁRTOTT VAGY BEHOZOTT ANYAGOKRA VONATKOZÓ EGYSÉGESEN ELŐÍRT INFORMÁ ( 1 ) A 12. cikk (1) bekezdésének c) pontjával
2006R1907 HU 20.02.2009 004.001 147 VIII. MELLÉKLET A LEGALÁBB 10 TONNA MENNYISÉGBEN GYÁRTOTT VAGY BEHOZOTT ANYAGOKRA VONATKOZÓ EGYSÉGESEN ELŐÍRT INFORMÁ ( 1 ) A 12. cikk (1) bekezdésének c) pontjával
Post-experimental management: humane endpoints, euthanasia. Dániel Érces
 Reference number: 035/14 UNIVERSITY OF SZEGED, Institute of Surgical Research Animal experiments theory and practice C level SZEGEDI TUDOMÁNYEGYETEM, Sebészeti Műtéttani Intézet Az állatkísérletek elmélete
Reference number: 035/14 UNIVERSITY OF SZEGED, Institute of Surgical Research Animal experiments theory and practice C level SZEGEDI TUDOMÁNYEGYETEM, Sebészeti Műtéttani Intézet Az állatkísérletek elmélete
Genotoxikológia TOXIKOLÓGIA ÉS ÖKOTOXIKOLÓGIA IX. Genotoxikus anyagok. Kémiai mutagének 2012.11.23.
 TOXIKOLÓGIA ÉS ÖKOTOXIKOLÓGIA IX. Genotoxikológia és környezetvédelem. Karcinogén, mutagén és teratogén hatású kemikáliák. Genotoxikológiai tesztek, Aimes teszt, testvérkromatid eljárás Genotoxikológia
TOXIKOLÓGIA ÉS ÖKOTOXIKOLÓGIA IX. Genotoxikológia és környezetvédelem. Karcinogén, mutagén és teratogén hatású kemikáliák. Genotoxikológiai tesztek, Aimes teszt, testvérkromatid eljárás Genotoxikológia
2006R1907 HU
 2006R1907 HU 20.02.2009 004.001 152 IX. MELLÉKLET A LEGALÁBB 100 TONNA VAGY AZT MEGHALADÓ MENNYISÉGBEN ( 1 ) GYÁRTOTT VAGY BEHOZOTT ANYAGOKRA VONATKOZÓ EGYSÉGESEN ELŐÍRT INFORMÁ E melléklet szintjén a
2006R1907 HU 20.02.2009 004.001 152 IX. MELLÉKLET A LEGALÁBB 100 TONNA VAGY AZT MEGHALADÓ MENNYISÉGBEN ( 1 ) GYÁRTOTT VAGY BEHOZOTT ANYAGOKRA VONATKOZÓ EGYSÉGESEN ELŐÍRT INFORMÁ E melléklet szintjén a
EGY NÖVÉNYI EREDETŰ KIVONAT 14 NAPOS ISMÉTELT ADAGOLÁSÚ ORÁLIS TOXIKOLÓGIAI VIZSGÁLATA (PATOLÓGIAI MEGFIGYELÉSEK)
 EGY NÖVÉNYI EREDETŰ KIVONAT 14 NAPOS ISMÉTELT ADAGOLÁSÚ ORÁLIS TOXIKOLÓGIAI VIZSGÁLATA (PATOLÓGIAI MEGFIGYELÉSEK) Glávits Róbert, Szakonyiné Pasics Ilona, Hirka Gábor TOXI-COOP ZRT 2120 Dunakeszi, Pálya
EGY NÖVÉNYI EREDETŰ KIVONAT 14 NAPOS ISMÉTELT ADAGOLÁSÚ ORÁLIS TOXIKOLÓGIAI VIZSGÁLATA (PATOLÓGIAI MEGFIGYELÉSEK) Glávits Róbert, Szakonyiné Pasics Ilona, Hirka Gábor TOXI-COOP ZRT 2120 Dunakeszi, Pálya
1. 4. tételek. 1., A kórbonctan tárgya, feladata, vizsgáló módszerei
 1. 4. tételek 1., A kórbonctan tárgya, feladata, vizsgáló módszerei 1. A kórbonctan tárgya, feladata és vizsgáló módszerei 2. A kórbonctani és egyes kiegészítı diagnosztikai vizsgálatra szánt anyagok győjtésének
1. 4. tételek 1., A kórbonctan tárgya, feladata, vizsgáló módszerei 1. A kórbonctan tárgya, feladata és vizsgáló módszerei 2. A kórbonctani és egyes kiegészítı diagnosztikai vizsgálatra szánt anyagok győjtésének
Szeminárium vagy Gyakorlat Időpont: csütörtök Helyszín: Sebészeti. Műtéttani Intézet tanterem/hallgatói műtő
 AZ ÁLLATKÍSÉRLETEK ELMÉLETE ÉS GYAKORLATA B kurzus részletes tematikája Hét Dátum és időpont 1 Szeptember 16. 17.0-19.0 17. 8.00-11.00 18. 8.00-10.00 2 Szeptember 23. 17.0-19.0 24 8.00-11.00 25. 8.00-10.00
AZ ÁLLATKÍSÉRLETEK ELMÉLETE ÉS GYAKORLATA B kurzus részletes tematikája Hét Dátum és időpont 1 Szeptember 16. 17.0-19.0 17. 8.00-11.00 18. 8.00-10.00 2 Szeptember 23. 17.0-19.0 24 8.00-11.00 25. 8.00-10.00
VeyFo. VeyFo Jungtier - Oral Mulgat
 VeyFo VeyFo Jungtier - Oral Mulgat Különleges táplálási igényeket kielégítő/diétás/ kiegészítő takarmány borjak, malacok, bárányok, kecskegidák és kutyák részére Használati utasítás Trimetox 240 oldat
VeyFo VeyFo Jungtier - Oral Mulgat Különleges táplálási igényeket kielégítő/diétás/ kiegészítő takarmány borjak, malacok, bárányok, kecskegidák és kutyák részére Használati utasítás Trimetox 240 oldat
Érdemes vakcinázni a sertések 1-es típusú parvovírusa ellen
 1. oldal (összes: 6) 2. oldal (összes: 6) A PPV1 által okozott szaporodásbiológiai zavarok megelőzésére a tenyészkocák vakcinázását széles körben alkalmazzák. Fogékony sertésekben a PPV1 fertőződést követően
1. oldal (összes: 6) 2. oldal (összes: 6) A PPV1 által okozott szaporodásbiológiai zavarok megelőzésére a tenyészkocák vakcinázását széles körben alkalmazzák. Fogékony sertésekben a PPV1 fertőződést követően
Horgászati állatorvostan. Gödöllő, március 10.
 Horgászati állatorvostan Gödöllő, 2019. március 10. Dr. Baska Ferenc egyetemi docens Állatorvostudományi Egyetem Mobil: 06-20-5604183 (időegyeztetésre) E-mail: baska.ferenc@univet.hu honlap: http://www.baska.doctor.hu
Horgászati állatorvostan Gödöllő, 2019. március 10. Dr. Baska Ferenc egyetemi docens Állatorvostudományi Egyetem Mobil: 06-20-5604183 (időegyeztetésre) E-mail: baska.ferenc@univet.hu honlap: http://www.baska.doctor.hu
I. kategória II. kategória III. kategória 1. Jellemezd a sejtmag nélküli szervezeteket, a baktériumokat. Mutasd be az emberi betegségeket okozó
 Szóbeli tételek I. kategória II. kategória III. kategória 1. Jellemezd a sejtmag nélküli szervezeteket, a baktériumokat. Mutasd be az emberi betegségeket okozó baktériumokat és a védőoltásokat! 2. Jellemezd
Szóbeli tételek I. kategória II. kategória III. kategória 1. Jellemezd a sejtmag nélküli szervezeteket, a baktériumokat. Mutasd be az emberi betegségeket okozó baktériumokat és a védőoltásokat! 2. Jellemezd
A mangalica sertés takarmányozásának sajátosságai. Sárközi Tamás UBM Feed kft
 A mangalica sertés takarmányozásának sajátosságai Sárközi Tamás UBM Feed kft Az előadás tárgya 1, Malac takarmányozás 2, Koca takarmányozás 3, Hízó takarmányozás 4, Malacszám növelésének lehetősége A SERTÉSTAKARMÁNYOZÁSI
A mangalica sertés takarmányozásának sajátosságai Sárközi Tamás UBM Feed kft Az előadás tárgya 1, Malac takarmányozás 2, Koca takarmányozás 3, Hízó takarmányozás 4, Malacszám növelésének lehetősége A SERTÉSTAKARMÁNYOZÁSI
2. Biotranszformáció. 3. Kiválasztás A koncentráció csökkenése, az. A biotranszformáció fıbb mechanizmusai. anyagmennyiség kiválasztása nélkül
 2. Biotranszformáció 1. Kiválasztást fokozza 2. Az anyagot kevésbé toxikus formába alakítja (detoxifikáció ) 3. Az anyagot toxikusabb formába alakítja (aktiváció, parathion - paraoxon) Szerves anyagok
2. Biotranszformáció 1. Kiválasztást fokozza 2. Az anyagot kevésbé toxikus formába alakítja (detoxifikáció ) 3. Az anyagot toxikusabb formába alakítja (aktiváció, parathion - paraoxon) Szerves anyagok
(EGT-vonatkozású szöveg)
 2016.6.1. L 144/27 A BIZOTTSÁG (EU) 2016/863 RENDELETE (2016. május 31.) a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról (REACH) szóló 1907/2006/EK európai parlamenti
2016.6.1. L 144/27 A BIZOTTSÁG (EU) 2016/863 RENDELETE (2016. május 31.) a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról (REACH) szóló 1907/2006/EK európai parlamenti
TARTALOM. Előszó 9 BEVEZETÉS A BIOLÓGIÁBA
 Előszó 9 BEVEZETÉS A BIOLÓGIÁBA A biológia tudománya, az élőlények rendszerezése 11 Vizsgálati módszerek, vizsgálati eszközök 12 Az élet jellemzői, az élő rendszerek 13 Szerveződési szintek 14 EGYED ALATTI
Előszó 9 BEVEZETÉS A BIOLÓGIÁBA A biológia tudománya, az élőlények rendszerezése 11 Vizsgálati módszerek, vizsgálati eszközök 12 Az élet jellemzői, az élő rendszerek 13 Szerveződési szintek 14 EGYED ALATTI
KUTATÁSI JELENTÉS. DrJuice termékek Ezüstkolloid Hydrogél és Kolloid oldat hatásvizsgálata
 KUTATÁSI JELENTÉS A Bay Zoltán Alkalmazott Kutatási Közalapítvány Nanotechnológiai Kutatóintézet e részére DrJuice termékek Ezüstkolloid Hydrogél és Kolloid oldat hatásvizsgálata. E z ü s t k o l l o
KUTATÁSI JELENTÉS A Bay Zoltán Alkalmazott Kutatási Közalapítvány Nanotechnológiai Kutatóintézet e részére DrJuice termékek Ezüstkolloid Hydrogél és Kolloid oldat hatásvizsgálata. E z ü s t k o l l o
5.2.5. ÁLLATGYÓGYÁSZATI IMMUNOLÓGIAI GYÓGYSZEREK ELŐÁLLÍTÁSÁRA SZÁNT ÁLLATI EREDETŰ ANYAGOK
 1 5.2.5. ÁLLATGYÓGYÁSZATI IMMUNOLÓGIAI GYÓGYSZEREK ELŐÁLLÍTÁSÁRA SZÁNT ÁLLATI EREDETŰ ANYAGOK 07/2009:50205 javított 6.5 1. ALKALMAZÁSI TERÜLET Az állatgyógyászati célra szánt immunológiai gyógyszerek
1 5.2.5. ÁLLATGYÓGYÁSZATI IMMUNOLÓGIAI GYÓGYSZEREK ELŐÁLLÍTÁSÁRA SZÁNT ÁLLATI EREDETŰ ANYAGOK 07/2009:50205 javított 6.5 1. ALKALMAZÁSI TERÜLET Az állatgyógyászati célra szánt immunológiai gyógyszerek
A biológiai tényezők expozíciójával járótevékenységek munkahigiénés és foglalkozás-egészségügyi feltételei a munkavédelmi célvizsgálatok alapján
 A biológiai tényezők expozíciójával járótevékenységek munkahigiénés és foglalkozás-egészségügyi feltételei a munkavédelmi célvizsgálatok alapján Nédó Ferenc munkafelügyeleti referens NGM Munkavédelmi Főosztály
A biológiai tényezők expozíciójával járótevékenységek munkahigiénés és foglalkozás-egészségügyi feltételei a munkavédelmi célvizsgálatok alapján Nédó Ferenc munkafelügyeleti referens NGM Munkavédelmi Főosztály
Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter
 Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter Áttekintés Miért éppen a nyuszik? Védekezés módja Vakcina jellemzői Vakcina működése Ráfertőzési
Ha nem akarsz mellé-nyúl-ni, használj Nobivac Myxo-RHD-t! MSDay-MOM park, 2013.02.21. dr. Schweickhardt Eszter Áttekintés Miért éppen a nyuszik? Védekezés módja Vakcina jellemzői Vakcina működése Ráfertőzési
A klinikai vizsgálatokról. Dr Kriván Gergely
 A klinikai vizsgálatokról Dr Kriván Gergely Mi a klinikai vizsgálat? Olyan emberen végzett orvostudományi kutatás, amely egy vagy több vizsgálati készítmény klinikai, farmakológiai, illetőleg más farmakodinámiás
A klinikai vizsgálatokról Dr Kriván Gergely Mi a klinikai vizsgálat? Olyan emberen végzett orvostudományi kutatás, amely egy vagy több vizsgálati készítmény klinikai, farmakológiai, illetőleg más farmakodinámiás
Antibiotikumok a kutyapraxisban
 Antibiotikumok a kutyapraxisban Antibiotikum választás Bakteriális fertőzés Célzott Empirikus Megelőző Indokolt esetben Ismert betegség kiújulásának megelőzésére Rizikócsoportoknál Mikor ne adjunk? Nem
Antibiotikumok a kutyapraxisban Antibiotikum választás Bakteriális fertőzés Célzott Empirikus Megelőző Indokolt esetben Ismert betegség kiújulásának megelőzésére Rizikócsoportoknál Mikor ne adjunk? Nem
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST BIZTONSÁGI ADATLAP PROTECT B HANGYAIRTÓ POROZÓ 1. A KÉSZÍTMÉNY NEVE 2. ÖSSZETÉTEL
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT B HANGYAIRTÓ POROZÓ 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: A készítmény megnevezése:
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT B HANGYAIRTÓ POROZÓ 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: A készítmény megnevezése:
MÉREGHATÁST BEFOLYÁSOLÓ TÉNYEZŐK ELŐADÓ DR. LEHEL JÓZSEF
 MÉREGHATÁST BEFOLYÁSOLÓ TÉNYEZŐK ELŐADÓ DR. LEHEL JÓZSEF 2006.09.13. 1 BEFOLYÁSOLÓ TÉNYEZŐK XENOBIOTIKUM FIZIKAI-KÉMIAI KÉMIAI TULAJDONSÁGAI SZERVEZET BIOLÓGIAI SAJÁTOSSÁGAI KÖRNYEZET EGYÉB TULAJDONSÁGAI
MÉREGHATÁST BEFOLYÁSOLÓ TÉNYEZŐK ELŐADÓ DR. LEHEL JÓZSEF 2006.09.13. 1 BEFOLYÁSOLÓ TÉNYEZŐK XENOBIOTIKUM FIZIKAI-KÉMIAI KÉMIAI TULAJDONSÁGAI SZERVEZET BIOLÓGIAI SAJÁTOSSÁGAI KÖRNYEZET EGYÉB TULAJDONSÁGAI
Nano cink-oxid toxicitása stimulált UV sugárzás alatt és az N-acetilcisztein toxicitás csökkentő hatása a Panagrellus redivivus fonálféreg fajra
 Nano cink-oxid toxicitása stimulált UV sugárzás alatt és az N-acetilcisztein toxicitás csökkentő hatása a Panagrellus redivivus fonálféreg fajra KISS LOLA VIRÁG, SERES ANIKÓ ÉS NAGY PÉTER ISTVÁN Szent
Nano cink-oxid toxicitása stimulált UV sugárzás alatt és az N-acetilcisztein toxicitás csökkentő hatása a Panagrellus redivivus fonálféreg fajra KISS LOLA VIRÁG, SERES ANIKÓ ÉS NAGY PÉTER ISTVÁN Szent
Minőségbiztosítás gyógyszer és növényvédő szer vizsgáló laboratóriumokban
 GLP Minőségbiztosítás gyógyszer és növényvédő szer vizsgáló laboratóriumokban 31/1999. (VIII.6.) EÜM-FVM együttes rendelet az emberi felhasználásra kerülő gyógyszerekre és a növényvédő szerekre vonatkozó
GLP Minőségbiztosítás gyógyszer és növényvédő szer vizsgáló laboratóriumokban 31/1999. (VIII.6.) EÜM-FVM együttes rendelet az emberi felhasználásra kerülő gyógyszerekre és a növényvédő szerekre vonatkozó
Maprelin. Maprelin 75µg/ml oldat injekciós sertések számára A.U.V. Biotechnikai felhasználásra, csoportok vagy állományok kezelésére.
 Maprelin Maprelin 75µg/ml oldat injekciós sertések számára A.U.V Biotechnikai felhasználásra, csoportok vagy állományok kezelésére. Maprelin 75 μg/ml 1.A FORGALOMBA HOZATALI ENGEDÉLY JOOSULTJÁNAK, TOVÁBBÁ
Maprelin Maprelin 75µg/ml oldat injekciós sertések számára A.U.V Biotechnikai felhasználásra, csoportok vagy állományok kezelésére. Maprelin 75 μg/ml 1.A FORGALOMBA HOZATALI ENGEDÉLY JOOSULTJÁNAK, TOVÁBBÁ
1. TÁBLÁZAT: A FELHASZNÁLT ÁLLATOK SZÁMA SZÁRMAZÁSI HELYÜK SZERINT. Származás fajok szerint
 XI/810/95rev3 1.1. 1. TÁBLÁZAT: A FELHASZNÁLT ÁLLATOK SZÁMA SZÁRMAZÁSI HELYÜK SZERINT 1.2. 1.3. A jelentést tevő országon belül bejegyzett tenyésztő vagy beszállító létesítményből származó állatok Származás
XI/810/95rev3 1.1. 1. TÁBLÁZAT: A FELHASZNÁLT ÁLLATOK SZÁMA SZÁRMAZÁSI HELYÜK SZERINT 1.2. 1.3. A jelentést tevő országon belül bejegyzett tenyésztő vagy beszállító létesítményből származó állatok Származás
-pl. baktériumok és gombák toxinjai, mérgező növények, mérgező állati termékek, növényvédő szerek, különböző szennyező anyagok
 ÉLELEM ÚTJÁN TERJEDŐ MEGBETEGEDÉSEK = elfogyasztott ételben, italban levő mérgező hatású anyag (mikroorganizmus, mérgező növény, vegyi anyag) okoz Jellemzői: rövid lappangási idő heveny, robbanásszerű
ÉLELEM ÚTJÁN TERJEDŐ MEGBETEGEDÉSEK = elfogyasztott ételben, italban levő mérgező hatású anyag (mikroorganizmus, mérgező növény, vegyi anyag) okoz Jellemzői: rövid lappangási idő heveny, robbanásszerű
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése
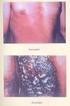 A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése Madas Balázs Gergely XXXIX. Sugárvédelmi Továbbképző Tanfolyam Hajdúszoboszló, Hunguest Hotel Béke 2014.
A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése Madas Balázs Gergely XXXIX. Sugárvédelmi Továbbképző Tanfolyam Hajdúszoboszló, Hunguest Hotel Béke 2014.
Az evolúció folyamatos változások olyan sorozata, melynek során bizonyos populációk öröklődő jellegei nemzedékről nemzedékre változnak.
 Evolúció Az evolúció folyamatos változások olyan sorozata, melynek során bizonyos populációk öröklődő jellegei nemzedékről nemzedékre változnak. Latin eredetű szó, jelentése: kibontakozás Időben egymást
Evolúció Az evolúció folyamatos változások olyan sorozata, melynek során bizonyos populációk öröklődő jellegei nemzedékről nemzedékre változnak. Latin eredetű szó, jelentése: kibontakozás Időben egymást
INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM
 INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM Szakközépiskola Tesztlapok Biológia - egészségtan tantárgy 12. évfolyam Készítette: Perinecz Anasztázia Név: Osztály: 1. témakör: Az élet kódja.
INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM Szakközépiskola Tesztlapok Biológia - egészségtan tantárgy 12. évfolyam Készítette: Perinecz Anasztázia Név: Osztály: 1. témakör: Az élet kódja.
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Magyarországi Evangélikus Egyház Sztehlo Gábor Evangélikus Óvoda, Általános Iskola és Gimnázium
 Témakörök Biológia Osztályozó vizsgákhoz 2012/2013 9. Természettudományos Osztálya-kémia tagozat A növények életműködései Légzés és kiválasztás Gázcserenylások működése Növényi párologtatás vizsgálata
Témakörök Biológia Osztályozó vizsgákhoz 2012/2013 9. Természettudományos Osztálya-kémia tagozat A növények életműködései Légzés és kiválasztás Gázcserenylások működése Növényi párologtatás vizsgálata
A SZARVASMARHA LÉGZŐSZERVI BETEGSÉG-KOMPLEXE
 VII. Praxismenedzsment Konferencia Budapest, 2013. november 23. A SZARVASMARHA LÉGZŐSZERVI BETEGSÉG-KOMPLEXE Fodor László Szent István Egyetem, Állatorvos-tudományi Kar, Járványtani és Mikrobiológiai Tanszék
VII. Praxismenedzsment Konferencia Budapest, 2013. november 23. A SZARVASMARHA LÉGZŐSZERVI BETEGSÉG-KOMPLEXE Fodor László Szent István Egyetem, Állatorvos-tudományi Kar, Járványtani és Mikrobiológiai Tanszék
Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje
 1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
ÁLLATKÍSÉRLETEK AZ ORVOSTUDOMÁNYBAN
 ÁLLATKÍSÉRLETEK AZ ORVOSTUDOMÁNYBAN Szabadon választott tantárgy az ÁOK, FOK, GYTK, TTIK, JGYPK II-V. éves hallgatói számára Kredit: 1. Tantárgyfelelős: Felvétel feltétele: A tantárgy oktatásának célja:
ÁLLATKÍSÉRLETEK AZ ORVOSTUDOMÁNYBAN Szabadon választott tantárgy az ÁOK, FOK, GYTK, TTIK, JGYPK II-V. éves hallgatói számára Kredit: 1. Tantárgyfelelős: Felvétel feltétele: A tantárgy oktatásának célja:
Kutatási terület: Haszonállatok egészségvédelme, állománydiagnosztika
 Dr. Abonyi Tamás Tanulmányok: Állatorvostudományi Egyetem, 1981. Kutatási terület: Haszonállatok egészségvédelme, állománydiagnosztika Korábbi munkahelyek: MTA Mezőgazdasági Kutató Intézet Kísérleti Gazdasága
Dr. Abonyi Tamás Tanulmányok: Állatorvostudományi Egyetem, 1981. Kutatási terület: Haszonállatok egészségvédelme, állománydiagnosztika Korábbi munkahelyek: MTA Mezőgazdasági Kutató Intézet Kísérleti Gazdasága
Az apróvadtenyésztés állategészségügyi gondjai
 Az apróvadtenyésztés állategészségügyi gondjai Dr. Beregi Attila Ph.D. Szent-István Egyetem Vadvilág Megőrzési Intézet Gödöllő 2011. Fogalom meghatározás Állathigiénia: integráló tudomány megelőzi a termelési
Az apróvadtenyésztés állategészségügyi gondjai Dr. Beregi Attila Ph.D. Szent-István Egyetem Vadvilág Megőrzési Intézet Gödöllő 2011. Fogalom meghatározás Állathigiénia: integráló tudomány megelőzi a termelési
Campylobacter a baromfi ólban, Campylobacter az asztalunkon. Dr. Molnár Andor Állatorvos, tudományos munkatárs Pannon Egyetem, Georgikon Kar
 Campylobacter a baromfi ólban, Campylobacter az asztalunkon Dr. Molnár Andor Állatorvos, tudományos munkatárs Pannon Egyetem, Georgikon Kar Bemutatkozás Ausztria-Magyarország határon átnyúló együttműködési
Campylobacter a baromfi ólban, Campylobacter az asztalunkon Dr. Molnár Andor Állatorvos, tudományos munkatárs Pannon Egyetem, Georgikon Kar Bemutatkozás Ausztria-Magyarország határon átnyúló együttműködési
Dr. Horváth Amanda emlékére
 Ez az előadás 1999. szeptemberében ugyanebben a formában hangzott el az OKI Pro Hygiene tudományos ülésén Hangozzék el most újra mentorom Dr. Horváth Amanda emlékére aki inspirálta és segítette azt a munkát,
Ez az előadás 1999. szeptemberében ugyanebben a formában hangzott el az OKI Pro Hygiene tudományos ülésén Hangozzék el most újra mentorom Dr. Horváth Amanda emlékére aki inspirálta és segítette azt a munkát,
Genetikai fejlesztések az állatjólét szolgálatában. Bikal november 22.
 Genetikai fejlesztések az állatjólét szolgálatában Bikal 2018. november 22. Alacsonyabb malac elhullás Alacsonyabb hizlaldai kiesés Javuló koca élettartam Magasabb hatékonyság Herélés elkerülése Állatjólét
Genetikai fejlesztések az állatjólét szolgálatában Bikal 2018. november 22. Alacsonyabb malac elhullás Alacsonyabb hizlaldai kiesés Javuló koca élettartam Magasabb hatékonyság Herélés elkerülése Állatjólét
VITAFORT ZRT Nemes Péter Vet- Produkt Kft.
 VITAFORT ZRT. 2016.06.02. Nemes Péter Vet- Produkt Kft. 1 Miért a Biosecurity Fotó: Dr. Horváth- Papp Imre 2 A biosecurity célja A kórokozók behurcolásának megakadályozása, hogy ne legyen: - szubklinikai
VITAFORT ZRT. 2016.06.02. Nemes Péter Vet- Produkt Kft. 1 Miért a Biosecurity Fotó: Dr. Horváth- Papp Imre 2 A biosecurity célja A kórokozók behurcolásának megakadályozása, hogy ne legyen: - szubklinikai
Fertőtlenítőszerek engedélyezése/engedély módosítása az átmeneti időszakban
 Fertőtlenítőszerek engedélyezése/engedély módosítása az átmeneti időszakban Cserháti Pálma MSc, biológus Országos Epidemiológiai Központ, Dezinfekciós osztály Biocidok és szabályozásuk Biocid termék: hatóanyag,
Fertőtlenítőszerek engedélyezése/engedély módosítása az átmeneti időszakban Cserháti Pálma MSc, biológus Országos Epidemiológiai Központ, Dezinfekciós osztály Biocidok és szabályozásuk Biocid termék: hatóanyag,
Megehetők-e az orvostechnikai eszközök?
 Megehetők-e az orvostechnikai eszközök? Az orvostechnikai eszközök fogalmi és besorolási szabályai 2014. március 28., Budapest Balázs György Ferenc, GYEMSZI- EMKI Főosztályvezető Az egészségügyről szóló
Megehetők-e az orvostechnikai eszközök? Az orvostechnikai eszközök fogalmi és besorolási szabályai 2014. március 28., Budapest Balázs György Ferenc, GYEMSZI- EMKI Főosztályvezető Az egészségügyről szóló
Az antibiotikum felhasználás csökkentésének lehetőségei a hazai gyakorlatban. Dr. Sándor Gergely Derzsy napok
 Az antibiotikum felhasználás csökkentésének lehetőségei a hazai gyakorlatban Dr. Sándor Gergely Derzsy napok 2019.06.06 Mikor használunk antibiotikumot a baromfiaknál? PROPHYLAXIS fogadjuk Enróra abból
Az antibiotikum felhasználás csökkentésének lehetőségei a hazai gyakorlatban Dr. Sándor Gergely Derzsy napok 2019.06.06 Mikor használunk antibiotikumot a baromfiaknál? PROPHYLAXIS fogadjuk Enróra abból
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
PULYKA NEVELÉSI, HÍZLALÁSI TECHNOLÓGIA
 PULYKA NEVELÉSI, HÍZLALÁSI TECHNOLÓGIA (TOJÁSTÓL VÁGÓHÍDIG) Törzsállomány Keltető Előnevelő Hízlaló 57 hét 1.,29-33 hét előnevelés, felkészítés a tojástermelésre 2.,24 hét tojástermelés 5 + 28 nap 1. Tojás
PULYKA NEVELÉSI, HÍZLALÁSI TECHNOLÓGIA (TOJÁSTÓL VÁGÓHÍDIG) Törzsállomány Keltető Előnevelő Hízlaló 57 hét 1.,29-33 hét előnevelés, felkészítés a tojástermelésre 2.,24 hét tojástermelés 5 + 28 nap 1. Tojás
Háhn Judit, Tóth G., Kriszt B., Risa A., Balázs A., Nyírő-Fekete B., Micsinai A., Szoboszlay S.
 Háhn Judit, Tóth G., Kriszt B., Risa A., Balázs A., Nyírő-Fekete B., Micsinai A., Szoboszlay S. Hungalimentaria 2019 Aquaworld Resort, Budapest 2019. április 24-25. Kik alkotják a konzorciumot? WESSLING
Háhn Judit, Tóth G., Kriszt B., Risa A., Balázs A., Nyírő-Fekete B., Micsinai A., Szoboszlay S. Hungalimentaria 2019 Aquaworld Resort, Budapest 2019. április 24-25. Kik alkotják a konzorciumot? WESSLING
Más gyógyszerekhez hasonlóan, a homeopátiás gyógyszerek sem szedhetők hosszabb ideig orvosi felügyelet nélkül (lásd 4.4 pont).
 1. A GYÓGYSZER NEVE Mastodynon belsőleges oldatos cseppek Homeopátiás gyógyszer 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 g oldat hatóanyag tartalma: Vitex agnus castus (Agnus castus) D1 20,0 g Iris versicolor
1. A GYÓGYSZER NEVE Mastodynon belsőleges oldatos cseppek Homeopátiás gyógyszer 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 g oldat hatóanyag tartalma: Vitex agnus castus (Agnus castus) D1 20,0 g Iris versicolor
Jar Professzionális Gépi Öblítőszer
 Készült: 2009/01/17. Biztonsági Adatlap 1. Készítmény azonosítása: Jar Professzionális Gépi Öblítőszer Gyártó Cég neve: Címe: Procter&Gamble MPD plus, s.r.o., Nábřeží Dr. Beneše 2307, 269 01, Rakovník,
Készült: 2009/01/17. Biztonsági Adatlap 1. Készítmény azonosítása: Jar Professzionális Gépi Öblítőszer Gyártó Cég neve: Címe: Procter&Gamble MPD plus, s.r.o., Nábřeží Dr. Beneše 2307, 269 01, Rakovník,
BIZTONSÁGI ADATLAP (a R.E.A.C.H. 1907/2006-os sorszámú Európai Szabályzat Annex II. sz. melléklete szerint) PYRUS 400 SC
 Referencia szám Frissítés sorszáma Frissítés dátuma 2009. április 15. BIZTONSÁGI ADATLAP (a R.E.A.C.H. 1907/2006-os sorszámú Európai Szabályzat Annex II. sz. melléklete szerint) PYRUS 400 SC 1. AZ ANYAG/KÉSZÍTMÉNY
Referencia szám Frissítés sorszáma Frissítés dátuma 2009. április 15. BIZTONSÁGI ADATLAP (a R.E.A.C.H. 1907/2006-os sorszámú Európai Szabályzat Annex II. sz. melléklete szerint) PYRUS 400 SC 1. AZ ANYAG/KÉSZÍTMÉNY
Partnereink termelési eredményei Vitafort takarmánnyal
 Partnereink termelési eredményei Vitafort takarmánnyal A takarmány önmagában nem elegendő a magas színvonalú termeléshez. Termelést befolyásoló tényezők Takarmány Genetika Egyéb tényezők (menedzsment,
Partnereink termelési eredményei Vitafort takarmánnyal A takarmány önmagában nem elegendő a magas színvonalú termeléshez. Termelést befolyásoló tényezők Takarmány Genetika Egyéb tényezők (menedzsment,
11. évfolyam esti, levelező
 11. évfolyam esti, levelező I. AZ EMBER ÉLETMŰKÖDÉSEI II. ÖNSZABÁLYOZÁS, ÖNREPRODUKCIÓ 1. A szabályozás információelméleti vonatkozásai és a sejtszintű folyamatok (szabályozás és vezérlés, az idegsejt
11. évfolyam esti, levelező I. AZ EMBER ÉLETMŰKÖDÉSEI II. ÖNSZABÁLYOZÁS, ÖNREPRODUKCIÓ 1. A szabályozás információelméleti vonatkozásai és a sejtszintű folyamatok (szabályozás és vezérlés, az idegsejt
I. MELLÉKLET GYÓGYSZERKÉSZÍTMÉNYEK NEVE, GYÓGYSZERFORMÁJA, HATÁSERŐSSÉGE, ÁLLATFAJOK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA
 I. MELLÉKLET GYÓGYSZERKÉSZÍTMÉNYEK NEVE, GYÓGYSZERFORMÁJA, HATÁSERŐSSÉGE, ÁLLATFAJOK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA EMEA/CVMP/166766/2006-HU 2006 májusban 1/7 Tagállam
I. MELLÉKLET GYÓGYSZERKÉSZÍTMÉNYEK NEVE, GYÓGYSZERFORMÁJA, HATÁSERŐSSÉGE, ÁLLATFAJOK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA EMEA/CVMP/166766/2006-HU 2006 májusban 1/7 Tagállam
Strobilurin és folpet típusú hatóanyagok kombinációja a biztosabb hatás érdekében.
 Magyarország Published on Syngenta (https://www.syngenta.hu) Fõoldal > Quadris Max Quadris Max Quadris Max módosítás: 2019.06.11. Gombaölő szer Növényvédő szer Munkaegészségügyi : 4 nap Kiszerelés: 1 l
Magyarország Published on Syngenta (https://www.syngenta.hu) Fõoldal > Quadris Max Quadris Max Quadris Max módosítás: 2019.06.11. Gombaölő szer Növényvédő szer Munkaegészségügyi : 4 nap Kiszerelés: 1 l
KARNYÚJTÁSNYIRA, MAGYARORSZÁGI
 KARNYÚJTÁSNYIRA, MAGYARORSZÁGI LABORATÓRIUMMAL KOCKÁZATMENTES GENETIKAI VIZSGÁLAT A MAGZATI KROMOSZÓMA-RENDELLENESSÉGEK KIMUTATÁSÁRA ÚJ KORSZAK A MAGZATI DIAGNOSZTIKÁBAN Ma már a várandós anya vérében
KARNYÚJTÁSNYIRA, MAGYARORSZÁGI LABORATÓRIUMMAL KOCKÁZATMENTES GENETIKAI VIZSGÁLAT A MAGZATI KROMOSZÓMA-RENDELLENESSÉGEK KIMUTATÁSÁRA ÚJ KORSZAK A MAGZATI DIAGNOSZTIKÁBAN Ma már a várandós anya vérében
Verzió 02.00 Felülvizsgálat dátuma 06.01.2015 Utolsó kiadás dátuma 11.02.2014 Első kiadás dátuma 21.09.2007
 1. SZAKASZ: Az anyag/keverék és a vállalat/vállalkozás azonosítása 1.1 azonosító Márkanév : 1.2 Az anyag vagy keverék megfelelő azonosított felhasználása, illetve ellenjavallt felhasználása Az anyag/keverék
1. SZAKASZ: Az anyag/keverék és a vállalat/vállalkozás azonosítása 1.1 azonosító Márkanév : 1.2 Az anyag vagy keverék megfelelő azonosított felhasználása, illetve ellenjavallt felhasználása Az anyag/keverék
Innovációs lehetőségek a LAB Research Kft-nél
 Innovációs lehetőségek a LAB Research Kft-nél 2011. április 06. Pannon Egyetem, Veszprém Gáty Szabolcs MBE vezető 1 LAB Research LAB Research, Kanada Alapítva:1998 Terjeszkedés: 2006, 2008 280 alkalmazott
Innovációs lehetőségek a LAB Research Kft-nél 2011. április 06. Pannon Egyetem, Veszprém Gáty Szabolcs MBE vezető 1 LAB Research LAB Research, Kanada Alapítva:1998 Terjeszkedés: 2006, 2008 280 alkalmazott
Állítsuk meg a bárányok kokcidiózist! Bogdán Éva haszonállat termékmenedzser Bayer Hungária Kft.
 Állítsuk meg a bárányok kokcidiózist! Bogdán Éva haszonállat termékmenedzser Bayer Hungária Kft. Mi a bárány-kokcidiózis? Kórokozó Eimeria spp. Kórokozóképes ség E. ovinoidalis +++ E. crandallis +/++ E.
Állítsuk meg a bárányok kokcidiózist! Bogdán Éva haszonállat termékmenedzser Bayer Hungária Kft. Mi a bárány-kokcidiózis? Kórokozó Eimeria spp. Kórokozóképes ség E. ovinoidalis +++ E. crandallis +/++ E.
Állatokon végzett vizsgálatok alternatíváinak használata a REACHrendelet
 Hiv.: ECHA-11-FS-06-HU ISBN-13: 978-92-9217-604-4 Állatokon végzett vizsgálatok alternatíváinak használata a REACHrendelet alapján A REACH-rendelet kidolgozásának és elfogadásának egyik legfontosabb oka
Hiv.: ECHA-11-FS-06-HU ISBN-13: 978-92-9217-604-4 Állatokon végzett vizsgálatok alternatíváinak használata a REACHrendelet alapján A REACH-rendelet kidolgozásának és elfogadásának egyik legfontosabb oka
DOWN-KÓR INTRAUTERIN SZŰRÉSI LEHETŐSÉGEI. 2013 szeptemberi MLDT-tagozati ülésen elhangzottak
 DOWN-KÓR INTRAUTERIN SZŰRÉSI LEHETŐSÉGEI 2013 szeptemberi MLDT-tagozati ülésen elhangzottak 21-es triszómia: Mi az a Down kór Down-kór gyakorisága: 0,13% Anya életkora (év) 20 25 30 35 40 45 49 Down-kór
DOWN-KÓR INTRAUTERIN SZŰRÉSI LEHETŐSÉGEI 2013 szeptemberi MLDT-tagozati ülésen elhangzottak 21-es triszómia: Mi az a Down kór Down-kór gyakorisága: 0,13% Anya életkora (év) 20 25 30 35 40 45 49 Down-kór
Nemzetközi kémiai biztonsági kártyák - R mondatok
 Nemzetközi kémiai biztonsági kártyák - R mondatok A veszélyes anyagok veszélyeire/kockázataira utaló R mondatok 1 Száraz állapotban robbanásveszélyes 10 Kismértékben tûzveszélyes. 11 Tûzveszélyes. 12 Fokozottan
Nemzetközi kémiai biztonsági kártyák - R mondatok A veszélyes anyagok veszélyeire/kockázataira utaló R mondatok 1 Száraz állapotban robbanásveszélyes 10 Kismértékben tûzveszélyes. 11 Tûzveszélyes. 12 Fokozottan
SZEGEDI TUDOMÁNYEGYETEM, ÁLTALÁNOS ORVOSTUDOMÁNYI KAR Az Állatkísérletek elmélete és gyakorlata B szint részletes programja
 Szegedi Tudományegyetem Általános Orvostudományi Kar Sebészeti 2017. december 06-december 15. Referencia szám: AA1.0/2015 / Referencia szám: AB1.0/2015 SZEGEDI TUDOMÁNYEGYETEM, ÁLTALÁNOS ORVOSTUDOMÁNYI
Szegedi Tudományegyetem Általános Orvostudományi Kar Sebészeti 2017. december 06-december 15. Referencia szám: AA1.0/2015 / Referencia szám: AB1.0/2015 SZEGEDI TUDOMÁNYEGYETEM, ÁLTALÁNOS ORVOSTUDOMÁNYI
BIZTONSÁGI ADATLAP. LANIRAT rágcsálóirtószer 1. A KÉSZÍTMÉNY NEVE:
 BIZTONSÁGI ADATLAP LANIRAT rágcsálóirtószer 1. A KÉSZÍTMÉNY NEVE: A készítmény típusa: rágcsálóirtó csalétek A készítmény megnevezése: LANIRAT rágcsálóirtószer Gyártó és forgalmazó: METATOX Peszticid Gyártó
BIZTONSÁGI ADATLAP LANIRAT rágcsálóirtószer 1. A KÉSZÍTMÉNY NEVE: A készítmény típusa: rágcsálóirtó csalétek A készítmény megnevezése: LANIRAT rágcsálóirtószer Gyártó és forgalmazó: METATOX Peszticid Gyártó
Minden leendő szülő számára a legfontosabb, hogy születendő gyermeke egészséges legyen. A súlyosan beteg gyermek komoly terheket ró a családra.
 Egészséges magzat, biztonságos jövő Minden leendő szülő számára a legfontosabb, hogy születendő gyermeke egészséges legyen. A súlyosan beteg gyermek komoly terheket ró a családra. A veleszületett fejlődési
Egészséges magzat, biztonságos jövő Minden leendő szülő számára a legfontosabb, hogy születendő gyermeke egészséges legyen. A súlyosan beteg gyermek komoly terheket ró a családra. A veleszületett fejlődési
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
PROCONT. kapszula. A lezárt preklinikai (állatkísérletes), nemzetközileg előírt vizsgálatok eredményei alapján kijelenthetjük, hogy a hatóanyag:
 PROCONT kapszula A Procont egy biológiai rendszerből származó, aktív daganatellenes hatóanyagot tartalmazó étrend-kiegészítő kapszula. Az izolált aktív anyag két, jól definiált csoport. Mindkét csoport
PROCONT kapszula A Procont egy biológiai rendszerből származó, aktív daganatellenes hatóanyagot tartalmazó étrend-kiegészítő kapszula. Az izolált aktív anyag két, jól definiált csoport. Mindkét csoport
Esemtan Invigorating Gel
 Verzió 01.06 Felülvizsgálat dátuma Nyomtatás Dátuma 1. AZ ANYAG/KÉSZÍTMÉNY ÉS A TÁRSASÁG/VÁLLALKOZÁS AZONOSÍTÁSA Termék tájékoztató Márkanév : Gyártó/Szállító : Schülke & Mayr GmbH Robert-Koch-Str. 2 22851
Verzió 01.06 Felülvizsgálat dátuma Nyomtatás Dátuma 1. AZ ANYAG/KÉSZÍTMÉNY ÉS A TÁRSASÁG/VÁLLALKOZÁS AZONOSÍTÁSA Termék tájékoztató Márkanév : Gyártó/Szállító : Schülke & Mayr GmbH Robert-Koch-Str. 2 22851
BIZTONSÁGI ADATLAP A 91/155 EECszabályozás szerint. Kiadás dátuma: 2007.06.07. Felülvizsgálva: 2010.12.15. Gardentop rágcsálóirtó blokk
 BIZTONSÁGI ADATLAP A 91/155 EECszabályozás szerint Kiadás dátuma: 2007.06.07. Felülvizsgálva: 2010.12.15. Gardentop rágcsálóirtó blokk Sds kód 0/06 1. Anyag/készítmény és vállalat azonosítása Termék azonosítása:
BIZTONSÁGI ADATLAP A 91/155 EECszabályozás szerint Kiadás dátuma: 2007.06.07. Felülvizsgálva: 2010.12.15. Gardentop rágcsálóirtó blokk Sds kód 0/06 1. Anyag/készítmény és vállalat azonosítása Termék azonosítása:
Szervetlen, fémorganikus és katalízis gyakorlatok. Függelék. ELTE Kémiai Intézet
 Szervetlen, fémorganikus és katalízis gyakorlatok Függelék ELTE Kémiai Intézet 1999-2009 107 Szervetlen, fémorganikus és katalízis gyakorlatok MÉREGKATEGÓRIÁK M-I Erős méreg M-II Méreg M-III Gyenge méreg
Szervetlen, fémorganikus és katalízis gyakorlatok Függelék ELTE Kémiai Intézet 1999-2009 107 Szervetlen, fémorganikus és katalízis gyakorlatok MÉREGKATEGÓRIÁK M-I Erős méreg M-II Méreg M-III Gyenge méreg
Tartalom. Javítóvizsga követelmények BIOLÓGIA...2 BIOLÓGIA FAKULTÁCIÓ...5 SPORTEGÉSZSÉGTAN évfolyam évfolyam évfolyam...
 Tartalom BIOLÓGIA...2 10. évfolyam...2 11. évfolyam...3 12. évfolyam...4 BIOLÓGIA FAKULTÁCIÓ...5 11. évfolyam...5 12. évfolyam...6 SPORTEGÉSZSÉGTAN...7 1 BIOLÓGIA 10. évfolyam Nappali tagozat Azírásbeli
Tartalom BIOLÓGIA...2 10. évfolyam...2 11. évfolyam...3 12. évfolyam...4 BIOLÓGIA FAKULTÁCIÓ...5 11. évfolyam...5 12. évfolyam...6 SPORTEGÉSZSÉGTAN...7 1 BIOLÓGIA 10. évfolyam Nappali tagozat Azírásbeli
Biobiztonság 5. Dr. Szatmári István
 Biobiztonság 5. Dr. Szatmári István A fertőzés lehetséges útjai A szem, orr és száj nyálkahártyája fröccsenés, spriccelés esetén Lenyelés pl. szájjal pipettázás, laborban történő evés, ivás esetén Belélegzés
Biobiztonság 5. Dr. Szatmári István A fertőzés lehetséges útjai A szem, orr és száj nyálkahártyája fröccsenés, spriccelés esetén Lenyelés pl. szájjal pipettázás, laborban történő evés, ivás esetén Belélegzés
Miért kell a nyuszimat vakcinázni?
 Miért kell a nyuszimat vakcinázni? A mixomatózis és a nyulak vérzéses betegsége (RHD- Rabbit Haemorrhagic Disease) két akár halálos kimenetelû (de megelôzhetô) fertôzô betegség, amely a nyulakat veszélyezteti.
Miért kell a nyuszimat vakcinázni? A mixomatózis és a nyulak vérzéses betegsége (RHD- Rabbit Haemorrhagic Disease) két akár halálos kimenetelû (de megelôzhetô) fertôzô betegség, amely a nyulakat veszélyezteti.
A perifériás neuropátia (PNP) morfológiai jellemzése
 Állategészségügyi Diagnosztikai Igazgatóság A perifériás neuropátia (PNP) morfológiai jellemzése Thuma Ákos 1, Szakáll Szabolcs 2, Glávits Róbert Derzsy napok Hajdúszoboszló, 2018.06.07. 1 NÉBIH-ÁDI 2
Állategészségügyi Diagnosztikai Igazgatóság A perifériás neuropátia (PNP) morfológiai jellemzése Thuma Ákos 1, Szakáll Szabolcs 2, Glávits Róbert Derzsy napok Hajdúszoboszló, 2018.06.07. 1 NÉBIH-ÁDI 2
 Oldalszám: 1/5 1 Anyag-/elkészítési- és cégmegjelölés A termékkel kapcsolatos anyagok Gyártó/forgalmazó: MC-BAUCHEMIE KFT. H-8246 Tótvázsony-Kövesgyűrpuszta Pf. 2. Tel./Fax.: +36/ 88 266 105 266 038 Információt
Oldalszám: 1/5 1 Anyag-/elkészítési- és cégmegjelölés A termékkel kapcsolatos anyagok Gyártó/forgalmazó: MC-BAUCHEMIE KFT. H-8246 Tótvázsony-Kövesgyűrpuszta Pf. 2. Tel./Fax.: +36/ 88 266 105 266 038 Információt
MELLÉKLET. a következőhöz: A BIZOTTSÁG (EU) /... FELHATALMAZÁSON ALAPULÓ RENDELETE
 EURÓPAI BIZOTTSÁG Brüsszel, 2018.4.30. C(2018) 2526 final ANNEX 1 MELLÉKLET a következőhöz: A BIZOTTSÁG (EU) /... FELHATALMAZÁSON ALAPULÓ RENDELETE az 1143/2014/EU európai parlamenti és tanácsi rendeletnek
EURÓPAI BIZOTTSÁG Brüsszel, 2018.4.30. C(2018) 2526 final ANNEX 1 MELLÉKLET a következőhöz: A BIZOTTSÁG (EU) /... FELHATALMAZÁSON ALAPULÓ RENDELETE az 1143/2014/EU európai parlamenti és tanácsi rendeletnek
No Change Service! Verzió 04.05 Felülvizsgálat dátuma 29.10.2012 Nyomtatás Dátuma 08.07.2014
 1. Az anyag/ keverék és a vállalat/ vállalkozás azonosítása 1.1 Termékazonosító Márkanév : 1.2 Az anyag vagy keverék megfelelő azonosított felhasználása, illetve ellenjavallt felhasználása Az anyag/keverék
1. Az anyag/ keverék és a vállalat/ vállalkozás azonosítása 1.1 Termékazonosító Márkanév : 1.2 Az anyag vagy keverék megfelelő azonosított felhasználása, illetve ellenjavallt felhasználása Az anyag/keverék
Dengue-láz. Dr. Szabó György Pócsmegyer
 Dengue-láz Dr. Szabó György Pócsmegyer Történelem Az ókori Kínában leírták. 1906-ban igazolták, hogy szúnyog terjeszti a betegséget. 1907-ben igazolták, hogy vírus. A II. világháború után kezdett megvadulni
Dengue-láz Dr. Szabó György Pócsmegyer Történelem Az ókori Kínában leírták. 1906-ban igazolták, hogy szúnyog terjeszti a betegséget. 1907-ben igazolták, hogy vírus. A II. világháború után kezdett megvadulni
Rovarméreg (méh, darázs) - allergia
 Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
A HÁZINYULAK NAGYÜZEMI TARTÁSÁNAK KÖVETELMÉNYEI
 TÁMOP-4.1.1.F-14/1/KONV-2015-0006 Egység, alprojekt/alprogram neve Rendezvény cím, dátum A HÁZINYULAK NAGYÜZEMI TARTÁSÁNAK KÖVETELMÉNYEI Előadó neve SZÁRMAZÁS, ELTERJEDÉS, DOMESZTIKÁCIÓ Nyúlszerű rágcsálók
TÁMOP-4.1.1.F-14/1/KONV-2015-0006 Egység, alprojekt/alprogram neve Rendezvény cím, dátum A HÁZINYULAK NAGYÜZEMI TARTÁSÁNAK KÖVETELMÉNYEI Előadó neve SZÁRMAZÁS, ELTERJEDÉS, DOMESZTIKÁCIÓ Nyúlszerű rágcsálók
Humán használatú vizek egészségkockázatának előrejelzése
 Humán használatú vizek egészségkockázatának előrejelzése Vargha Márta Országos Könyezetegészségügyi Intézet Vízhigiénés és Vízbiztonsági főosztály Vízzel kapcsolatos betegségek Vízben lévő mikroorganizmusok
Humán használatú vizek egészségkockázatának előrejelzése Vargha Márta Országos Könyezetegészségügyi Intézet Vízhigiénés és Vízbiztonsági főosztály Vízzel kapcsolatos betegségek Vízben lévő mikroorganizmusok
Élő metapneumovírus vakcina fejlesztése tojóállományok részére: ártalmatlansági és hatékonysági vizsgálatok. Hajdúszoboszló, június 2-3.
 Élő metapneumovírus vakcina fejlesztése tojóállományok részére: ártalmatlansági és hatékonysági vizsgálatok Dr. Kollár Anna, Dr. Soós Pál, Antalné Szalkai Teodóra, Dr. Tóth Ádám, Dr. Nagy Zoltán, Gubucz-Sombor
Élő metapneumovírus vakcina fejlesztése tojóállományok részére: ártalmatlansági és hatékonysági vizsgálatok Dr. Kollár Anna, Dr. Soós Pál, Antalné Szalkai Teodóra, Dr. Tóth Ádám, Dr. Nagy Zoltán, Gubucz-Sombor
Kémiai kóroki tényezők a növénytermesztés ágazatában. Készítette: Dr. Dóczi Ildikó Mende
 Kémiai kóroki tényezők a növénytermesztés ágazatában Készítette: Dr. Dóczi Ildikó Mende Bemutatkozás Pest megyében, Sülysáp és Úri község közötti területen található Sűrűpuszta, ahol két mezőgazdasági
Kémiai kóroki tényezők a növénytermesztés ágazatában Készítette: Dr. Dóczi Ildikó Mende Bemutatkozás Pest megyében, Sülysáp és Úri község közötti területen található Sűrűpuszta, ahol két mezőgazdasági
M. A. H. FOOD CONTROLL Kft. Mikrobiológiai vizsgáló Laboratóriuma Állategészségügyi Diagnosztikai Részleg BROILER PROGRAM
 BROILER PROGRAM Telepítés utáni mintavétel: élőállat-szállító autóról vett, lezárt csomagolású alompapír és 10 db útihulla (vagy 25 g meconium), mely a MSZ EN ISO 6579:2002/A1:2007 és a 180/2009 (XII:
BROILER PROGRAM Telepítés utáni mintavétel: élőállat-szállító autóról vett, lezárt csomagolású alompapír és 10 db útihulla (vagy 25 g meconium), mely a MSZ EN ISO 6579:2002/A1:2007 és a 180/2009 (XII:
PrenaTest Újgenerációs szekvenálást és z-score
 PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
Tájékoztató a Down szűrésről Első trimeszteri KOMBINÁLT TESZT
 Tájékoztató a Down szűrésről Első trimeszteri KOMBINÁLT TESZT A terhességek kb. 1%-ában az újszülött teljesen egészséges szülőktől súlyos szellemi vagy testi fogyatékkal születik. A veleszületett értelmi
Tájékoztató a Down szűrésről Első trimeszteri KOMBINÁLT TESZT A terhességek kb. 1%-ában az újszülött teljesen egészséges szülőktől súlyos szellemi vagy testi fogyatékkal születik. A veleszületett értelmi
A gyógyszerallergia és. Dr. Lukács Andrea
 A gyógyszerallergia és intolerancia a gyakorlatban Dr. Lukács Andrea AE (Adverseevent) Adverz esemény: adott gyógyszerkészítmény alkalmazása kapcsán jelentkező kellemetlen tünet, amely nem feltétlenül
A gyógyszerallergia és intolerancia a gyakorlatban Dr. Lukács Andrea AE (Adverseevent) Adverz esemény: adott gyógyszerkészítmény alkalmazása kapcsán jelentkező kellemetlen tünet, amely nem feltétlenül
dr. Kranjec Ferenc A modern holstein-fríz tehén reprodukciós jellegzetességei, annak javítására alkalmazható módszerek
 dr. Kranjec Ferenc A modern holstein-fríz tehén reprodukciós jellegzetességei, annak javítására alkalmazható módszerek Bodrog, Szerencsi MGZRT. A petefészek ellés utáni ciklusba lendülése Tejtermelés,
dr. Kranjec Ferenc A modern holstein-fríz tehén reprodukciós jellegzetességei, annak javítására alkalmazható módszerek Bodrog, Szerencsi MGZRT. A petefészek ellés utáni ciklusba lendülése Tejtermelés,
3/29/12. Biomatematika 2. előadás. Biostatisztika = Biometria = Orvosi statisztika. Néhány egyszerű definíció:
 Biostatisztika = Biometria = Orvosi statisztika Biomatematika 2. előadás Néhány egyszerű definíció: A statisztika olyan tudomány, amely a tömegjelenségekkel kapcsolatos tapasztalati törvényeket megfigyelések
Biostatisztika = Biometria = Orvosi statisztika Biomatematika 2. előadás Néhány egyszerű definíció: A statisztika olyan tudomány, amely a tömegjelenségekkel kapcsolatos tapasztalati törvényeket megfigyelések
Evolúció. Dr. Szemethy László egyetemi docens Szent István Egyetem VadVilág Megőrzési Intézet
 Evolúció Dr. Szemethy László egyetemi docens Szent István Egyetem VadVilág Megőrzési Intézet Mi az evolúció? Egy folyamat: az élőlények tulajdonságainak változása a környezethez való alkalmazkodásra Egy
Evolúció Dr. Szemethy László egyetemi docens Szent István Egyetem VadVilág Megőrzési Intézet Mi az evolúció? Egy folyamat: az élőlények tulajdonságainak változása a környezethez való alkalmazkodásra Egy
Az elhízás hatása az emberi szervezetre. Dr. Polyák József Pharmamedcor Kardiológiai Szakambulancia 1137. Budapest, Katona J. u. 27.
 Az elhízás hatása az emberi szervezetre Dr. Polyák József Pharmamedcor Kardiológiai Szakambulancia 1137. Budapest, Katona J. u. 27. Melyek az élő szervezet elemi életjelenségei közül minőségében testtömeg
Az elhízás hatása az emberi szervezetre Dr. Polyák József Pharmamedcor Kardiológiai Szakambulancia 1137. Budapest, Katona J. u. 27. Melyek az élő szervezet elemi életjelenségei közül minőségében testtömeg
A HACCP rendszer bevezetésének célja
 HACCP 4.tétel HACCP Lényege: - Nemzetközileg elfogadott módszer arra, hogy lehetséges veszélyeket azonosítsunk, értékeljünk, kezeljük a biztonságos élelmiszerek forgalmazása érdekében, - valamint rendszer
HACCP 4.tétel HACCP Lényege: - Nemzetközileg elfogadott módszer arra, hogy lehetséges veszélyeket azonosítsunk, értékeljünk, kezeljük a biztonságos élelmiszerek forgalmazása érdekében, - valamint rendszer
A Minőségbiztosítási egység (MBE) által végzett ellenőrzések GLP környezetben
 A Minőségbiztosítási egység (MBE) által végzett ellenőrzések GLP környezetben Bevezetés A GLP Minőségbiztosítási Program (Quality Assurance Program; QAP) keretén belül a Minőségbiztosítási egységnek (MBE)
A Minőségbiztosítási egység (MBE) által végzett ellenőrzések GLP környezetben Bevezetés A GLP Minőségbiztosítási Program (Quality Assurance Program; QAP) keretén belül a Minőségbiztosítási egységnek (MBE)
ÁGAZATI SZAKMAI ÉRETTSÉGI VIZSGA MEZŐGAZDASÁG ISMERETEK EMELT SZINTŰ SZÓBELI VIZSGA MINTAFELADATOK ÉS ÉRTÉKELÉSÜK
 MEZŐGAZDASÁG ISMERETEK EMELT SZINTŰ SZÓBELI VIZSGA MINTAFELADATOK ÉS ÉRTÉKELÉSÜK 1. tétel A feladat Ismertesse a gazdasági állataink tartásánál alkalmazott etetési módszereket és itatási módokat! Vázolja
MEZŐGAZDASÁG ISMERETEK EMELT SZINTŰ SZÓBELI VIZSGA MINTAFELADATOK ÉS ÉRTÉKELÉSÜK 1. tétel A feladat Ismertesse a gazdasági állataink tartásánál alkalmazott etetési módszereket és itatási módokat! Vázolja
