Acélgyártó eljárások
|
|
|
- Jakab Gulyás
- 8 évvel ezelőtt
- Látták:
Átírás
1 BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyagtudomány(szig1) féléves házi feladat Acélgyártó eljárások Thiele Ádám WTOSJ Budapest, 011
2 T A R T A L O M 1. Az acélgyártási folyamatok fizikai-kémiai alapjai Termodinamikai alapok A tömeghatás törvénye és a kémiai reakciók egyensúlyi állandója Aktivitás, koncentráció A kémiai reakciók termodinamikája Megoszlási törvény Az elemek acélfázisban történő oldódása Reakciókinetikai alapok Az acélgyártás legfőbb folyamatai Frissítés Dezoxidálás Kicsapásos dezoxidálás Diffúziós dezoxidálás Dezoxidálás vákuumban Történelmi acélgyártó eljárások Meteorvasak Bucavas előállítás Frisstűzi acélgyártás Kavaró eljárás Tégelyacélgyártás Szélfrissítéses konverteres acélgyártás Bessemer-eljárás Thomas-eljárás Modern acélgyártó eljárások Direkt módszerű acélgyártási eljárások Direkt redukciós eljárások Olvadék redukciós eljárások Nyersvas alapú acélgyártási eljárások Siemens-Martin eljárás Oxigén befúvásos konverteres acélgyártás (LD) Elektroacélgyártás Különleges acélgyártó eljárások és finomító eljárások Felhasznált irodalom... 14
3 1. Az acélgyártási folyamatok fizikai-kémiai alapjai 1.1. Termodinamikai alapok Az acélgyártás termodinamikai alapjainak tárgyalása során a lejátszódó folyamatok hőhatásával és sorrendiségével foglalkozunk A tömeghatás törvénye és a kémiai reakciók egyensúlyi állandója A tömeghatás törvénye szerint egy egyensúlyi kémiai reakcióban részvevő termékek egyensúlyi koncentrációjának megfelelő hatványon vett szorzatából és a kiindulási anyagok egyensúlyi koncentrációjának megfelelő hatványon vett szorzatából képzett tört értéke adott hőmérsékleten állandó. A hányadost a reakció egyensúlyi állandójának nevezzük. Egy általános kémiai reakcióra: ma nb A B (1) m n A (1) reakció sebessége a felső nyíl irányában: v k A m B A (1) reakció sebessége az alsó nyíl irányában: v k A B Ahol: k és k arányossági tényezők. Az egyensúlyi reakciók nem folynak le teljesen, hanem a kiindulási anyagok teljes elfogyása előtt megállnak, mert egyensúly jön létre a kiindulási anyagok és a reakció termékei között. Egyensúlyi állapotban a reakció az alsó és a felső nyíl irányában azonos sebességgel zajlik: v v Így a (), (3) és (4) egyenlet szerint: AB m n m n A B k m n n () (3) (4) k K (5) Ahol: K a reakció egyensúlyi állandója Aktivitás, koncentráció Az aktivitás a reális elegyek, olvadékok alkotóinak termodinamikai koncentrációja. Az aktivitás az adott körülmények között a vizsgált komponens tényleges, a folyamat során rendelkezésre álló szabad koncentrációját jelenti. Az aktivitással tehát figyelembe vesszük az adott rendszer komponenseinek kölcsönhatását. Így az ideális elegyekre, olvadékokra érvényes egyenletek (pl. a fentiek) érvényesek maradnak a reális termodinamikai viselkedésű olvadékokra és elegyekre is. A tiszta állapotú anyagok aktivitása egységnyi: a 1 (6) tiszta A gázelegyek aktivitása a parciális nyomással egyenlő: a gáz p (7) i Ideális elegyek és híg oldatok alkotóinak aktivitása a ténylegesen mérhető koncentrációval egyenlő: 3
4 a i x (8) ideális elegyre; i és a i c (9) híg oldatra. i A kémiai reakciók termodinamikája A kémiai folyamatok mindig együtt járnak a rendszer szabadentalpiájának megváltozásával, amely a következő képen fejezhető ki: G GRTln K H T S (10) Ahol: G - a rendszer szabadentalpia változása G - a standard szabadentalpia változás H - a reakció entalpia változása S - a reakció entrópia változása K - a reakció egyensúlyi állandója T - az abszolút hőmérséklet R - a gázállandó (8,314 J/Kmól) Egyensúlyba ért reakció esetén G 0. Ha G 0, akkor a reakció önként végbemegy a felső nyíl irányába. Ha G 0, akkor a reakció az alsó nyíl irányába folyik. Egyensúlyi állapotban ( G 0 ) a reakciók során keletkezett termékek képződésének standard szabadentalpia változásai a (10)-ből kifejezve: GRTln K H T S (11) Az acélgyártás során végbemenő reakciók szempontjából fontos fém-oxid képződés általános reakcióegyenlete: Me O MeO (1) A (1) reakció egyensúlyi állandója az (5) egyenlet szerint (az pontban leírtaknak megfelelően aktivitásokkal számolva): K a a a MeO Me O (13) Figyelembe véve a (6) egyenletet, mert a reakcióban tiszta anyagok vesznek részt, és a (7) egyenletet, a (13) egyenlet a következő képen egyszerűsödik: 1 (14) K PO Az acélgyártás során keletkező fém-oxidok képződésének standard szabadentalpiája a (11) és (14) egyenletek alapján: 4
5 1 GRTln RTln P O (15) P O Az összefüggés szerint a G függ a hőmérséklettől (és az oxigén parciális nyomásástól is). Az oxidok képződésének G f( T) függvényeit az 1. ábra mutatja. 1. ábra: Oxidok képződésének standard szabadentalpia-változása A diagramban alacsonyabb helyet elfoglaló oxidok kisebb oxigénnyomással és az oxigénhez való nagyobb affinitással rendelkeznek, vagyis stabilabbak. Így elméletileg minden olyan elem redukciót végezni, amelynek oxidképződését az adott hőmérsékleten negatívabb standard szabadentalpia-változás kíséri, mint a redukálandó oxid képződését, azaz grafikusan, a G f( T) egyenese alacsonyabban helyezkedik el a redukálandó oxid ugyanezen egyeneséhez képest az adott hőmérsékleten. Az egyensúlyi állandó hőmérséklettel történő változása, azaz az lg K f( T) függvény, a (11) lg K lg K egyenletből fejezhető ki R = 8,314 J/Kmól behelyettesítésével és ln K lg e 0, 4343 felhasználásával: H S GH TS RTln K 19,15lg K lg K (16) 19,15T 19,15 Az egyensúlyi állandó hőmérséklettel való változásának irányát a reakció exoterm vagy endoterm volta szabja meg. Exoterm folyamatoknál ( H 0 ) a hőmérséklet növekedésével 5
6 az egyensúlyi állandó értéke csökken, endoterm folyamatoknál ( H 0 ) a hőmérséklet növekedésével az egyensúlyi állandó értéke növekszik (állandó nyomás esetén). Egy egyensúlyi reakció során a kialakuló egyensúlyi összetétel nemcsak a hőmérsékletnek, hanem a nyomásnak is függvénye, ha a termékek összes moláris térfogata nem azonos a reagensek összes moláris térfogatával. A nyomás növekedése a térfogatcsökkenés irányába végbemenő reakciót segíti. (Pl. a Boudouard-reakciót, CO CO C a nyomás növekedése a térfogatcsökkenés irányába ható reakciót, azaz a CO elbomlását segíti.) Megoszlási törvény Az egymással nem elegyedő két folyékony fázisban (az acélgyártásban ez a fémfürdő és a salak), ha egy újabb, harmadik anyagot oldunk, akkor a két fázisban az oldott anyag koncentrációjának aránya adott hőmérsékleten állandó, ezt az állandót nevezzük megoszlási tényezőnek (L). A megoszlási törvényt pl. FeO-ra felírva: L FeO ( FeO) (17) FeO Ahol: L FeO - az FeO megoszlási tényezője ( FeO ) - az FeO wt%-os mennyisége a salakban FeO - az FeO wt%-os mennyisége a fémfürdőben A megoszlási egyensúly megváltoztatásával szabályozni lehet az oxigén áramlási irányát. A frissítés során pl. a salakból a fémfázisba történő oxigénáramlás szükséges, ezért ekkor a salak FeO tartalmát növelve, az L FeO állandósága miatt a ( FeO) FeO (18) reakció a felső nyíl irányába játszódik le (fémfürdőt oxidáló salak). Dezoxidáláskor a salak FeO tartalmának csökkenésével a (18) reakció az alsó nyíl irányába megy vége (fémfürdőt redukáló salak). A bázikus salak erősebben oxidáló salak, mint a savanyú salak. Pl C-on bázikus salakban (nagy CaO, MgO tartalom): L 1600bázikus FeO 50 (19) FeO 1 míg savanyú salakban (nagy SiO, FeO, MnO tartalom): L 1600savanyú FeO 100 (0) FeO Az elemek acélfázisban történő oldódása Az elemek acélfázisban történő oldódásának nagy szerepe van az acélgyártás reakcióinak termodinamikai elemzésekor, az acélok dezoxidálásakor, ötvözésekor. A folyékony vasban az acél ötvöző és szennyező elemeinek oldódása három csoportba osztható. 6
7 A vassal ideális oldatot alkotó ötvözőelemek a Cr, Co, Mn, Mo és a W. Ezek a vasban korlátlanul oldódnak (Mo-t és W-ot kivéve), a vassal nem képeznek vegyületet. A vassal nem ideális oldatot alkotó ötvözőelemek az Al, Cu, Ni, Si, V, Ti és a Zr. Ezek a vas olvadáspontján, a folyékony vasban tökéletesen oldódnak. Nemfémes elemek oldódása esetén az oldódás hőmérséklet és nyomásfüggő. Egyes kétatomos gázok nagy hőmérsékleten könnyen disszociálnak, majd atomos állapotban oldódnak a fémfürdőben (N, H, O ). A Sieverts-törvény megmutatja, hogy az acélgyártási folyamatokban fontos gázoknak oldódásának mennyisége arányos a fémfürdő feletti parciális nyomásuk négyzetgyökével. 1.. Reakciókinetikai alapok A termodinamikai vizsgálatok alapján csak a reakciók lejátszódásának lehetősége határozható meg, a reakciók mechanizmusának feltárásával, a reakciók sebességével a reakciókinetika foglalkozik. A termodinamikailag lehetséges reakciót a kinetikai feltételek hiánya akadályozhat meg a lejátszódásban. Az acélgyártási eljárások során a reakciókinetika négy fő folyamatot vizsgál: - Az anyagszállítás sebességének vizsgálata a valamely reakcióban részvevő anyag reakcióhelyre történő eljutására ad választ. - A kémiai reakciók sebességének vizsgálata. - A gázbuborék képződés feltételeinek vizsgálata. - Heterogén reakciók mechanizmusa, amelyek az acélgyártási folyamatok során a gáz-, salak- és a fémfázis között játszódnak le.. Az acélgyártás legfőbb folyamatai.1. Frissítés A frissítő periódus célja az acélfürdő C-, H - és P-tartalmának csökkentése és a hőmérséklet növelése. Az oxidáció több féle képen oldható meg: - levegő oxigénjével (Bessemer- és Thomas-eljárás) - oxidáló salakkal (Siemens-Martin eljárás) - tiszta oxigénnel (oxigén fúvatásos eljárások) - oxigén és argon együttes befúvásával (AOD) A kísérő elemek oxidációja oxigén vagy levegő befúvásos frissítés esetén közvetlenül az oxigén vagy a keletkező FeO hatására mehet végbe. Az oxidáló salakokkal történő frissítés esetén a nagy FeO tartalmú salak végzi a fém-salak fázishatáron a megoszlási törvénynek megfelelően (ld ). Az egyes elemek oxidációjakor jelentős hőmennyiség szabadul fel, ami emeli a fürdő hőmérsékletét. A karbon kiégésekor keletkező CO és CO élénk fővésbe hozza a fürdőt, ami ezáltal a fürdőt átkeveri, növeli az egyes fázisok közötti érintkezési felületet, növeli a reakciók sebességét, intenzívebbé teszi a hőátadást és elősegíti a gázok és a zárványok eltávozását. A karbonleégés sebessége a technológiai lépés fontos jellemzője, a szél és oxigénfrissítéses eljárások esetén kb. 0,3% C/min, az oxidáló salakos eljárásnál kb. 0,3% C/h. A foszfor eltávolítása bázikus, nagy CaO-tartalmú salakkal történik, a vasban oldott foszfor oxidációjával keletkező savanyú jellegű P O 5 -ot a kis bázicitású FeO-val szemben az erősen bázikus CaO stabilan megköti... Dezoxidálás Azért, hogy az acélfürdőben oldott kísérő elemek oxidációja kellő sebességgel menjen végbe, az oxidálószer feleslegben történő adagolása szükséges. Így a frissítés után az acél túlzottan nagy mennyiségű oxigént tartalmaz, többet mint amennyit szilárd állapotban oldani képes, ezért a kristályosodás során a kristályhatárokon FeO zárványok formájában kiválik és rontja a szilárdsági tulajdonságokat. A folyékony vasban az oldott oxigéntartalom már igen kis 7
8 mennyiségben is FeO-ként van jelen. A káros oxigénmennyiséget csökkenteni kell, vagy kevésbé káros oxidok formájában kell megkötni...1. Kicsapásos dezoxidálás A kicsapásos dezoxidálás lényege, hogy az acélfürdőben oldott oxigént (vagy FeO-t), olyan elemmel kötik meg, amelyiknek az oxigénhez való affinitása nagyobb, mint a vasé (vö. az oxidok képződésének szabadentalpia-változását mutató 1. ábra). A kicsapásos dezoxidálás általános reakcióegyenlete: FeO Me Fe MeO (1) Ahol Me a dezoxidáló elem, amely az oxigénhez való affinitás növekvő sorrendjében lehet: Mn, Si, Ti, Al, stb (az Al az acélban kettős szemcsenagyságot okozhat). A Mn-t és a Si-ot ferroötvözetek, az Al-ot legtöbb esetben tiszta fém formájában használják. A csak Mn-nal dezoxidált acélokban még marad oxigén, dermedéskor a karbontartalom hatására CO keletkezik. Az ilyen acélokat csillapítatlan acéloknak nevezik. A Mn-Si-mal és a Mn-Si-Almal dezoxidált acélok esetén dermedéskor nincs CO fejlődés. Ezeket csillapított acéloknak nevezzük. A képződött oxidnak kis olvadáspontúnak kell lennie, hogy ezáltal koagulálhasson, és így a dezoxidációs termékek növekedését elősegítse, valamint kis fajsúlyúnak kell lennie, hogy gyorsan a salakba emelkedhessen. A gömb alakúnak feltételezett dezoxidációs termék felemelkedését a Stokes-tétel írja le: g v fürdő zárvány r () 9 Ahol: v - a zárványok emelkedési sebessége g - a nehézségi gyorsulás - az acélfürdő viszkozitása fürdő - a fürdő sűrűsége zárvány - a dezoxidásiós termék sűrűsége... Diffúziós dezoxidálás Az acélfürdő oxigéntartalmát nemcsak az [FeO] redukciója útján, hanem az [FeO]-nak a salakba való eltávolításával is lehet csökkenteni. Ezt a módszert, amikor az FeO az acélfürdőből a redukáló salakba diffundál diffúziós dezoxidálásnak nevezzük. A megoszlási törvény értelmében (ld ) a salakban lévő szabad FeO-t csökkentve csökken az acél FeO tartalma is csökken anélkül, hogy dezoxidáló anyagot adnánk a fürdőbe. A vasnak a salakból a fémfürdőbe való visszaredukciójára speciális dezoxidáló keverékeket használnak, amelyek fő alkotója valamilyen karbonhordozó (koksz, faszén, grafit, kalciumkarbid, stb.) és legtöbbször emellett még ferrosziliciumot is hozagolnak. Ez két egyenlettel jellemezhető: ( FeO) ( Me) ( MeO) Fe (3) FeO ( FeO) (4) A vasnak a salakból való redukciója történhet szintetikus salakkal is, de ekkor a vas nem redukálódik vissza az acélfürdőbe, hanem a salak valamelyik fém oxidja köti meg a salakban. Ez egy egyenlettel fejezhető ki: 8
9 ( FeO) ( MeO) ( MeO FeO) (5) A diffúziós dezoxidáció esetén a karbonnal vagy karbiddal való dezoxidáció terméke gáznemű, így eltávozik az acélfürdőből, azonban a diffúziós dezoxidáció túl lassú, ezért általában összekapcsolják a kicsapásos dezoxidációval...3. Dezoxidálás vákuumban Vákuumban történő dezoxidáláskor olyan dezoxidálószerek kerülnek előtérbe, amelyek terméke elszívható gáz, így a reakció a termék keletkezésének irányába tolható el (vö ). Ez azonban csak akkor érvényes, ha reakció bal oldalán kevesebb mólnyi gáz van, mint a jobboldalon. A vákuum által a dezoxidáció hatékonyságára gyakorolt hatás kihasználására tökéletes lehetőséget csak a kondenzált állapotban lévő, illó oxidokat alkotó elemek alkalmazása nyújt. Ilyen elem a C. A karbonnal történő dezoxidálás reakcióegyenlete: {CO} y C Me O x Me y x y (6) A karbonnal, vákuumban végzett dezoxidáció előnye, hogy az egyensúlyi [C%][O%] szorzat értéke a CO parciális nyomás csökkenésével jelentősen csökken. Az elérhető legkisebb szorzatérték kb...1*10-1, amely torr p CO esetén érhető el. Ez azt jelenti, hogy O% = 0,001..0,00 és C% = 0,00..0,006. A p CO értéke argonbefúvással is csökkenthető (AOD acélgyártás) 3. Történelmi acélgyártó eljárások 3.1. Meteorvasak A legkorábbi (kb. hatezer éves) vastárgyak tulajdonképpen acélnak tekinthető vasmeteorokból készültek. A vasmeteorok vegyi összetételére jellemző, hogy nikkeltartalmuk akár 0% is lehet, egyéb ötvözőket viszont csak kis mennységben tartalmaznak. Ennek köszönhetően a vasmeteorok nagyon jól kovácsolhatóak, jól kovácstűzi-hegeszthetőek voltak, és a korróziónak is jobban ellenálltak, mint a későbbi korok kis karbontartalmú szénacélból készült vastárgyai. 3.. Bucavas előállítás A vas kb. i.e századi tűzi úton történő előállításának felfedezése feltételezhetően a rézkohászati technológiából eredeztethető. A vaselőállítás ősi módja szerint kis faszéntüzelésű kemencékben, közvetlenül a vasércből nyertek egy salakos vasszivacsot, ún. vasbucát. A vas az elérhető kis kohászati hőmérséklet mellett nem olvadt meg ezért csak csekély mértékben ötvöződött karbonnal. Az előállított néhány kilogramm tömegű vasbucát újrahevítették, tömörítették. Eközben a sok vasoxidot tartalmazó, ezáltal alacsony olvadáspontú salak jelentős része kifolyt, kipréselődött. A vas előállításának ezen ősi technológiáját mai szakkifejezéssel élve direkt módszerű vagy közvetlen acélgyártásnak nevezhetnénk. A technológia Magyarországon egészen az 1880-as évekig élt Frisstűzi acélgyártás A XVI. Században megjelent eljárás nyersvasból állított elő az ún. forrasztott acélt. Aknás kemencébe faszenet, nyersvasat és nagy FeO-tartalmú salakot adagoltak, majd az elegyet C körüli hőmérsékletre hevítették. A megolvadó nyersvas lecsepegett az akna aljára, az oxidáló kemenceatmoszféra és a nagy FeO-tartalmú salak hatására a kísérő elemei (C, Mn, Si és P) kioxidálódtak, bár a FeO-val történő foszfortalanítás tökéletlen volt. Az 9
10 eredetileg kb. C = 4,3% összetételű nyersvas karbontartalma fokozatosan csökkent. Elérve a likvidusz vonalat megkezdődött a szolidusz vonalig tartó kristályosodás. Mivel a nyersvas nagy karbontartalom mellett érte el a likvidusz hőmérsékletet, a benne oldott oxigén mennyisége még csekély volt. Az összeállt vasterméket kovácsolással salaktalanították és kovácshegesztették össze Kavaró eljárás Az 1784-ben bevezetett kavaró eljárás berendezése olyan rostélytüzelésű lángkemence volt, ahol az olvasztóteret tűzhíd választja el a rostélytól. Az olvasztótérbe nyersvasat és oxidáló anyagot (vasérc, reve, salak) adagoltak. Az olvadék kavarása eredményeként az olvadt nyersvas az olvadt oxidálóanyag vasoxid tartalmának hatására frissítődött. A vas kb C hőmérsékleten kristályosodott ki és állt össze gomolyává, amely salakszennyeződését kovácsolással távolították el Tégelyacélgyártás Az 1740-ben kialakult tégelyacélgyártás berendezése egy grafit és agyag keverékéből készült tégely volt. A betétanyag a kavart vagy frisstűzi acél, a salakképző kvarchomok vagy üvegcserép volt. A betét beadagolása után a tégelyt lezárták és kívülről hevítették. Az átolvasztási módszerrel homogénebb és tisztább terméket kaptak. A technológiát az elektroacélgyártás szorította ki a XX. században Szélfrissítéses konverteres acélgyártás Bessemer-eljárás Az 1855-ben szabadalmaztatott Bessemer-eljárás között adta a világ acéltermelésének túlnyomó részét. Ebben az időben jó minőségű, kis foszfortartalmú ércek és kis kéntartalmú szenek álltak rendelkezésre, így jó minőségű volt a nyersvasbetét. A jó minőségű alapanyagok kimerülésével párhuzamosan fejlődtek ki a bázikus bélést alkalmazó eljárások. Az eljárás berendezése a billenthető körte alakú konverter, amelybe a folyékony nyersvas beöntése után alulról fúvókákon keresztül levegőt fúvatnak be (.ábra).. ábra: A Bessemer-eljsárás berendezése A nyersvas fúvatásakor intenzív fürdőmozgás jön létre, amely gyorsan telíti a fürdőt oxigénnel: Fe O { } FeO (7) 10
11 A fürdőben oldódó [FeO] a kísérő elemeket oxidálja. Az oxidáció első periódusában a Si és a Mn, FeO Si ( SiO ) Fe FeO Mn ( MnO) Fe (8) (9) második periódusában a C oxidálódik: FeO C { CO} Fe {O }+C {CO} (indirekt) (30) (direkt) (31) A C oxidációja végén a vas oxidációja kezdődik meg, az acélfürdő [FeO]-tartalma fokozatosan növekszik, így a megoszlási törvény értelmében (17) a salak elkezd telítődni (FeO)-val. A Bessemer-eljárás savas bélésű, ezért kéntelenítést és foszfortalanítást nem lehet benne végezni. Az adag dezoxidálása FeMn, FeSi, Al, tükörvas felhasználásával történik Thomas-eljárás Az 1878-ben szabadalmaztatott Bessemer-eljárás között adta a világ acéltermelésének túlnyomó részét. Az eljárásnál a Bessemer-eljárás berendezését és elvét alkalmazzák, de a bázikus bélésű konverter és égetett mész adagolása teszi lehetővé a foszfor stabil megkötését kalciumfoszfát alakjában. A (7) reakció lejátszódása után: 4 P( FeO) ( PO 5) Fe 5 5 (3) ( PO 8 5) ( CaO) (4 CaOPO 5) (33) A frissítés első periódusában a Si, és a Mn oxidálódik a (8) és (9)-nek megfelelően, ezt követi a C (30) és (31), majd a P (3) és (3) szerinti oxidációja (ugyanis a hozagolt CaO kezdetben nem, csak az (FeO) megjelenésekor oldódik a salakban). 4. Modern acélgyártó eljárások Direkt és indirekt módszerű acélgyártást különböztetünk meg aszerint, hogy az acélgyártó eljárás közvetlenül az ércből, vagy a megelőző nyersvasgyártási lépés termékéből, a nyersvasból állítja elő az acélt. A legfontosabb mai acélgyártó eljárások csoportosítását a 3. ábra mutatja: Acélgyártó eljárások Direkt (közvetlenül az ércből) Indirekt (nyersvas alapú) Direkt redukciós - Gázredukciós - Szilárd karbon redukciós Olvadék redukciós - Egylépcsős - Kétlépcsős - Háromlépcsős Konverteres Siemens-Martin Eleketroacélgyártás - Oxigén befúvásos - (Szélfrissítéses) - Ívfényes kemecében - Indukciós kemencében 3. ábra: A fontosabb mai acélgyártó eljárások csoportosítása Különleges - Elektrosalakos - Vákuumos 11
12 4.1.Direkt módszerű acélgyártási eljárások A direkt módszerű acélgyártási technológiák a szilárd vasterméket, an ún. vasszivacsot előállító direkt redukciós eljárások és a folyékony (általában a nyersvashoz hasonló) vasterméket előállító olvadékredukciós eljárások csoportjára oszthatók. Ezek a technológiák még ma is lassan terjednek, jelenleg a teljes acéltermelésből kb. 5%-ban részesednek Direkt redukciós eljárások A direkt redukciós eljárások körébe tartozik minden olyan eljárás, amely dús (kis meddő tartalmú) vasércekből, szilárd állapotban, gáznemű (gázredukciós) vagy szilárd redukálószerek felhasználásával (szilárd karbon redukciós) kis C-tartalmú vasterméket állít elő. A nagy fémesítési fokkal (Fe fém /Fe össz >0,9) és minimális meddőtartalommal rendelkező vasszivacs elsődlegesen az elektroacélgyártás betétanyagaként használható fel. A kisebb fémesítési fokkal rendelkező vasszivacsok, mint előredukált betétanyagok a nagyolvasztóban kohósíthatók. A gázredukciós eljárás két fő egysége az aknás kemence típusú reaktor, amelyben a lefelé haladó érc vagy pellet színvassá történő redukcióját a CO és a H végzi. A másik fő egységben, a konvertálóberendezésben, a torokgázokat (CO, H O) többnyire földgázzal reagáltatva állítják elő a redukálógázt, amelynek összetétele általában CO=5-40%, H =35-55%, hőmérséklete C. A szilárd karbon redukciós eljárás során a finomszemcsés ércből, nagy reaktivitású kokszdarából és a salakképző anyagból álló betétanyag keverékét forgócsöves kemencében reagáltatják, így állítanak elő vasszivacsot. A redukciós hőmérséklet kb C. 008-ban a világ kb. 100Mt-ás acéltermeléséből a direkt redukciós technológiával előállított acél mennyisége 68,5Mt volt. A termelés 75%-a gázredukciós (Midrex 60% és HyL 15%), 5%-a szilárd karbon redukciós technológia alapú volt Olvadék redukciós eljárások Az olvadékredukciós eljárásokban ércporokat, előredukált vagy előredukálatlan érckoncentrátumokat állapotban többnyire gyenge minőségű szenek vagy szénporok felhasználásával, folyékony halmazállapotban, többnyire nyersvashoz hasonló összetételű folyékony vassá, illetve vasötvözetté redukálnak nagy hőmérsékleten ( C-on). Az olvadékredukciós eljárások három csoportba oszthatók. A ritkán alkalmazott egylépcsős eljárás során az olvadékredukcióban keletkező CO-ot oxigénnel elégetve közvetlenül fedezik a folyamat hőszükségletét. A kétlépcsős eljárás esetén az olvadékredukciós részben keletkezett CO-t visszavezetik az előredukciós térbe, ahol a CO elvégzi az érc előredukcióját. A hőt a távozó torokgázok elégetésével nyert villamos energiával biztosítják. Elterjedt kétlépcsős olvadékredukciós technológia az Inred- és az Elred-eljárás. A háromlépcsős technológiában az olvasztó és a redukciós tér között egy harmadik térben elhelyezett kokszágyon végzik az olvasztó térből érkező égéstermékek redukáló gázzá történő konverzióját. A redukáló gázt ezután a redukciós térben az érc előredukciójára hasznosítják. Elterjedt háromlépcsős olvadékredukciós technológia a Plasmamelt-, Kawasaki- és a Pirogaseljárás. 4.. Nyersvas alapú acélgyártási eljárások Siemens-Martin eljárás Az 1864-ben kialakult SM-eljárás berendezése a regeneratív tüzelésű lángkemence (4. ábra). Az SM-eljárás betétje lehet hulladék-nyersvas, nyersvas-érc és hulladék szén. A fissítést nemcsak a kemenceatmoszféra oxigéntartalma, hanem az oxidáló salak is végzi a fém-salak fázishatáron a megoszlási törvénynek (17) megfelelően. Az így a fémfázisban oldódó [FeO] a kísérőelemeket oxidálja. Az oxidáció sorrendje, Si, Mn majd P, a hőmérsékleten 1
13 növekedésével kerül egyre inkább előtérbe a C (30) egyenlet szerint oxidációja. Az oxidálódott foszfor bázikus salakban (nagy MgO és CaO tartalom) megköthető. Az SM eljárás dezoxidációs szakaszában FeMn, FeSi, Al, FeTi esetleg CaSi közvetlenül a csapolás előtt az üstbe vagy a folyadéksugárba történő adagolásával kicsapásos dezoxidálást, vagy redukáló salakkal diffúziós dezoxidálást is alkalmaznak (a..-ben leírtaknak megfelelően). 4. ábra: A SM- eljárás berendezése 4... Oxigén befúvásos konverteres acélgyártás (LD) Az oxigén befúvásos konverteres eljárásoknak három nagy csoportja létezik. A ráfúvásos oxigén konverteres eljárásnál az adag 75-90% folyékony nyersvas mellett acélhulladékból, vagy ércből áll. A tűzálló bélésű konverterbe az oxigént vízzel hűtött lándzsán keresztül 10-14bar nyomással juttatják be. A fenékfúvatásos oxigén konverteres eljárásnál az oxigén a konverter fenekén önmagát hűtő fúvókarendszeren jut a fémfürdőbe (hasonlóan a levegő frissítéses Bessemer és Thomas eljáráshoz, ld és 3.6..) Az argon-oxigén befúvásos konverteres eljárás (AOD) során oxigén és argon gáz keverékét fújják be a konverterbe, így csökkentve a keletkező CO parciális nyomásást, ezáltal javítva a dekarbonizálás hatásfokát (v.ö...3.). Ezzel az eljárással állítják elő a kis karbontartalmú, korrózió- és saválló acélokat. 5. ábra: Az LD-eljárás berendezése Elektroacélgyártás Az elektroacélgyártó eljárás kezdetei 1878-ra nyúlnak vissza. Az eljárás berendezése az ívfényes (6/a. ábra) vagy az indukciós kemence (6/b. ábra). Az elektrokemence fémbetétje szinte kizárólag acélhulladék, ritkán, akkor is csak kis mennyiségben használnak nyersvasat. Az elektrokemence atmoszférája ezért csak gyengén oxidáló, a kis mennyisében jelen lévő kísérőelemek oxidációját (különösen a foszforét) külön bevitt oxigénhordozóval (kis 13
14 mennyiségű érc, reve, ipari oxigén) kell biztosítani. Az elemek oxidációja [FeO] közvetítésével és az oxidációs termékek elsalakulása az SM-eljáráshoz hasonlóan történik. A jó minőségű acél gyártásának elengedhetetlen feltétele a fővés (v.ö..1.) Mivel a betét karbontartalma csekély, a CO keletkezéséhez valamilyen karbonhordozót (ált. kokszot) is be kell adni. Az elektroacélgyártás során a kemencében az oxidációs periódus alatt megtörténik az oxigénhez a vasnál kisebb affinitású fémek beötvözése is (Mo, Ni, Co, Cu). Az oxidációs periódus végén a keletkezett salakot lehúzzák. A salak eltávolítása után a dezoxidáló periódusban redukáló salakot képeznek, Mész, folypát és kokszpor keverékéből (diffúziós dezoxidálás). A további dezoxidálás Ferroötvözetekkel történik (kicsapásos dezoxidálás). Azokat az ötvözőfémeket, amelyek oxigénhez való affinitása a vasnál kisebb, a dezoxidáló periódus végén ötvözik be (Cr, V, Ti, Ce, Ta, B, Nb) azért, hogy kevés legyen az oxidos formában megkötődő veszteség. Az ívfényes kemencében a betét megolvasztásához és az acélfürdő felhevítéséhez szükséges hőt elektródák közötti villamos ív termeli. Az indukciós kemencében a betét a benne gerjesztett középfrekvenciás váltóáram Joule-hője hatására olvad meg. Az indukciós kemencében a fürdő álladó mozgásban van az indukált áram hatására, ez kedvez a gáztalanításnak. Az ívkemencében azonban a redukáló periódusban elmarad a fürdő fővése, így jelentős a fürdő gáztartalma. Ezt a káros gázok parciális nyomásának csökkentésével lehet elkerülni (ld. Sieverts-törvény, ). a b 6. ábra: Elektroacélgyártás a.) ívkemencében, b.) indukciós akemencében Különleges acélgyártó eljárások és finomító eljárások A nemfémes zárványok és gázok, valamint a dúsulások rontják az acél több fontos tulajdonságát, ezért ezek mennyisét csökkenteni kell a különleges igénybevételnek kitett acélok esetén. A metallurgiai folyamatok szerint három csoportba sorolhatók az acélfinomító eljárások. A salak-fém reakción alapuló eljárások során a salak legkedvezőbb összetételével állítják be a kívánt reakciók optimális egyensúlyi helyzetét a megoszlási törvény (17) alapján. Így dolgoznak az elektrosalakos olvasztókemencék és a szintetikus salakos eljárások. Az eljárások másik csoportjában elsősorban fizikai folyamatok érvényesülnek, amikor vákuumban vagy védőgázban olvasztják át az acélt, így csökkentve a gáz- és szennyezőtartalmát. Ide tartozik a vákuumos és a vákuumindukciós átolvasztás. Az előző két eljárás kombinációi az egyidejűleg salakkal és vákuummal, vagy védőgázzal dolgozó eljárások. Ilyenek a plazmasugaras, plazmaíves, vákuumindukciós, vákuumíves elektrosalakos leolvasztási eljárások. 5. Felhasznált irodalom Tylecote R.: The prehistory of metallurgy, London,
15 Remport G.: Magyarország vaskohászata az ipari forradalom előestéjén ( ), Budapest, 1995 Simon S., Sziklavári J., Szőke L.: Újabb technológiai megoldások az acélgyártásban, Budapest, 1978 Csabalik Gy., Szarka Gy.: Vaskohászattan 1, Budapest, 1985 Artinger I., Csikós G., Krállics Gy., Németh Á., Palotás B.: Fémek és kerámiák technológiája, Budapest, 000 Szegedi J.: Acélgyártás 1, Budapest, 1984 Szegedi J., Szabó Z.: Acélgyártás, Budapest, 1984 Csabalik Gy.: Acélgyártás 3, Budapest, 1984 Óvári A.: Vaskohászati kézikönyv, Budapest, 1985 Farkas O.: Nyersvasmetallurgia, Budapest, 1989 Pásztor G.: Kémiai metallurgia, Budapest, 1989 The Metals Society: Direct reduction of iron ore, London, 1979 Midrex: Word direct reduction statistics,
A vas-oxidok redukciós folyamatainak termodinamikája
 BUDAESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyag- és gyártástechnológia (hd) féléves házi feladat A vas-oxidok redukciós folyamatainak termodinamikája Thiele Ádám WTOSJ Budapest, 11
BUDAESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyag- és gyártástechnológia (hd) féléves házi feladat A vas-oxidok redukciós folyamatainak termodinamikája Thiele Ádám WTOSJ Budapest, 11
Mérnöki anyagismeret
 Mérnöki anyagismeret Termikus, villamos, mágneses tulajdonságok Alapanyagok gyártása Fémkohászat Vas- és acélgyártás Termikus tulajdonságok A szilárd anyagok az olvadás illetve amorf anyagok esetében a
Mérnöki anyagismeret Termikus, villamos, mágneses tulajdonságok Alapanyagok gyártása Fémkohászat Vas- és acélgyártás Termikus tulajdonságok A szilárd anyagok az olvadás illetve amorf anyagok esetében a
Nyersvas- és acélgyártás
 Nyersvas- és acélgyártás Anyagismeret Dr. Orbulov Imre Norbert Anyagtudomány és Technológia Tanszék KÖTELEZŐ SZAKIRODALOM Fémek és kerámiák technológiája Artinger Csikós Krállics Németh Palotás Könyvtár,
Nyersvas- és acélgyártás Anyagismeret Dr. Orbulov Imre Norbert Anyagtudomány és Technológia Tanszék KÖTELEZŐ SZAKIRODALOM Fémek és kerámiák technológiája Artinger Csikós Krállics Németh Palotás Könyvtár,
A foszfor archeometallurgiai szerepe a honfoglalás kori vasbucakohászat során
 A foszfor archeometallurgiai szerepe a honfoglalás kori vasbucakohászat során Alapvető kérdések: Hogyan kerül a foszfor a gyepvasércekbe és milyen ásványos formában van meg bennük? Hogyan redukálódik ki
A foszfor archeometallurgiai szerepe a honfoglalás kori vasbucakohászat során Alapvető kérdések: Hogyan kerül a foszfor a gyepvasércekbe és milyen ásványos formában van meg bennük? Hogyan redukálódik ki
Ajánlott a könyvespolcra Acélok, öntöttvasak Szabadíts Ödön FÉMEK TECHNOLÓGIÁJA FONTOS TUDNIVALÓK
 FÉMEK TECHNOLÓGIÁJA Orbulov Imre Norbert orbulov@eik.bme.hu FONTOS TUDNIVALÓK Az anyagszerkezettant tudni kell Cél: mérnöki anyagok, alakadási és kötési technológiák, anyagválasztás Laborok a G épületben,
FÉMEK TECHNOLÓGIÁJA Orbulov Imre Norbert orbulov@eik.bme.hu FONTOS TUDNIVALÓK Az anyagszerkezettant tudni kell Cél: mérnöki anyagok, alakadási és kötési technológiák, anyagválasztás Laborok a G épületben,
Fémkohászat. Vas- és acél gyártás Alumínium gyártás Réz- és szinesfém kohászat
 Fémkohászat Vas- és acél gyártás Alumínium gyártás Réz- és szinesfém kohászat A fémkohászat főbb folyamatai Érc előkészítés (törés, őrlés, szétválasztás) Nyers fém kinyerése A nyers fém finomítása Ötvözés
Fémkohászat Vas- és acél gyártás Alumínium gyártás Réz- és szinesfém kohászat A fémkohászat főbb folyamatai Érc előkészítés (törés, őrlés, szétválasztás) Nyers fém kinyerése A nyers fém finomítása Ötvözés
Olvasztár Olvasztár
 10/07 (II. 27.) SzMM rendelettel módosított 1/06 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről. Szakképesítés, szakképesítés-elágazás,
10/07 (II. 27.) SzMM rendelettel módosított 1/06 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről. Szakképesítés, szakképesítés-elágazás,
Az acélok szennyező anyagai
 BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyag- és gyártástechnológia (PhD) féléves házi feladat Az acélok szennyező anyagai Thiele Ádám WTOSJ2 Budapest, 2011 Tartalomjegyzék 1. Bevezetés...3
BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Anyag- és gyártástechnológia (PhD) féléves házi feladat Az acélok szennyező anyagai Thiele Ádám WTOSJ2 Budapest, 2011 Tartalomjegyzék 1. Bevezetés...3
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
ACÉLMETALLURGIA ALAPJAI. Anyagmérnök BSc-képzés. Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ. Miskolc, 2014.
 MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR METALLURGIAI ÉS ÖNTÉSZETI INTÉZET ACÉLMETALLURGIA ALAPJAI Anyagmérnök BSc-képzés Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS
MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR METALLURGIAI ÉS ÖNTÉSZETI INTÉZET ACÉLMETALLURGIA ALAPJAI Anyagmérnök BSc-képzés Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások.
 Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások. dr. Fábián Enikő Réka fabianr@eik.bme.hu BMEGEMTAGM3-HŐKEZELÉS 2016/2017 Kétalkotós ötvözetrendszerekkel kapcsolatos alapfogalmak Az alkotók
Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások. dr. Fábián Enikő Réka fabianr@eik.bme.hu BMEGEMTAGM3-HŐKEZELÉS 2016/2017 Kétalkotós ötvözetrendszerekkel kapcsolatos alapfogalmak Az alkotók
TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ
 TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ Vas-karbon diagram: A vas olvadáspontja: a) 1563 C. b) 1536 C. c) 1389 C. Mennyi a vas A1-el jelölt hőmérséklete? b) 1538 C. Mennyi a vas A2-el jelölt hőmérséklete?
TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ Vas-karbon diagram: A vas olvadáspontja: a) 1563 C. b) 1536 C. c) 1389 C. Mennyi a vas A1-el jelölt hőmérséklete? b) 1538 C. Mennyi a vas A2-el jelölt hőmérséklete?
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
ACÉLOK MÉRNÖKI ANYAGOK
 ACÉLOK MÉRNÖKI ANYAGOK 80%-a (5000 kg/fő/év) kerámia, kő, homok... Ebből csak kb. 7% a iparilag előállított cserép, cement, tégla, porcelán... 14%-a (870 kg/fő/év) a polimerek csoportja, melynek kb. 90%-a
ACÉLOK MÉRNÖKI ANYAGOK 80%-a (5000 kg/fő/év) kerámia, kő, homok... Ebből csak kb. 7% a iparilag előállított cserép, cement, tégla, porcelán... 14%-a (870 kg/fő/év) a polimerek csoportja, melynek kb. 90%-a
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Vas- karbon ötvözetrendszer
 Vas- karbon ötvözetrendszer Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos, és szaggatott vonallal is fel vannak
Vas- karbon ötvözetrendszer Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos, és szaggatott vonallal is fel vannak
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
ANYAGISMERET I. ACÉLOK
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK ANYAGISMERET I. ACÉLOK Dr. Palotás Béla Dr. Németh Árpád Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus Hipereutektikus
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK ANYAGISMERET I. ACÉLOK Dr. Palotás Béla Dr. Németh Árpád Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus Hipereutektikus
ACÉLOK HEGESZTHETŐSÉGE
 ACÉLOK HEGESZTHETŐSÉGE Budapesti Műszaki és Gazdaságtudományi Egyetem Mechanikai Technológia és Anyagszerkezettani Tanszék Dr. Palotás Béla Szerző: dr. Palotás Béla 1 A hegeszthetőség fogalma Az acél hegeszthetősége
ACÉLOK HEGESZTHETŐSÉGE Budapesti Műszaki és Gazdaságtudományi Egyetem Mechanikai Technológia és Anyagszerkezettani Tanszék Dr. Palotás Béla Szerző: dr. Palotás Béla 1 A hegeszthetőség fogalma Az acél hegeszthetősége
A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram)
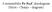 A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram) A vas-karbon egyensúlyi diagram alapvető fontosságú a vasötvözetek tárgyalásánál. Az Fe-C ötvözetekre vonatkozó ismereteket általában kettős
A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram) A vas-karbon egyensúlyi diagram alapvető fontosságú a vasötvözetek tárgyalásánál. Az Fe-C ötvözetekre vonatkozó ismereteket általában kettős
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Fémek és ötvözetek termikus viselkedése
 Anyagtudomány és Technológia Tanszék Fémek és ötvözetek termikus viselkedése Dr. Szabó Péter János szpj@eik.bme.hu Anyagszerkezettan és anyagvizsgálat BMEGEMTBGA1 2018/2019/2 Az előadás során megismerjük
Anyagtudomány és Technológia Tanszék Fémek és ötvözetek termikus viselkedése Dr. Szabó Péter János szpj@eik.bme.hu Anyagszerkezettan és anyagvizsgálat BMEGEMTBGA1 2018/2019/2 Az előadás során megismerjük
1. feladat Összesen 10 pont. 2. feladat Összesen 10 pont
 1. feladat Összesen 10 pont Töltse ki a táblázatot oxigéntartalmú szerves vegyületek jellemzőivel! Tulajdonság Egy hidroxil csoportot tartalmaz, moláris tömege 46 g/mol. Vizes oldatát ételek savanyítására
1. feladat Összesen 10 pont Töltse ki a táblázatot oxigéntartalmú szerves vegyületek jellemzőivel! Tulajdonság Egy hidroxil csoportot tartalmaz, moláris tömege 46 g/mol. Vizes oldatát ételek savanyítására
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján.
 A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Bevontelektródás ívhegesztés
 Budapesti Műszaki és Gazdaságtudományi Egyetem Bevontelektródás ívhegesztés Dr. Palotás Béla Mechanikai Technológia és Anyagszerkezettani Tanszék Bevontelektródás kézi ívhegesztés Consumable electrode:
Budapesti Műszaki és Gazdaságtudományi Egyetem Bevontelektródás ívhegesztés Dr. Palotás Béla Mechanikai Technológia és Anyagszerkezettani Tanszék Bevontelektródás kézi ívhegesztés Consumable electrode:
1. feladat Összesen: 8 pont. 2. feladat Összesen: 11 pont. 3. feladat Összesen: 7 pont. 4. feladat Összesen: 14 pont
 1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. Gázok oldhatósága vízben: 101 325 Pa nyomáson g/100 g vízben
 1. Gázok oldhatósága vízben: 101 325 Pa nyomáson g/100 g vízben t/ 0 C 0 20 30 60 O 2 0,006945 0,004339 0,003588 0,002274 H 2S 0,7066 0,3846 0,2983 0,148 HCl 82,3 72 67,3 56,1 CO 2 0,3346 0,1688 0,1257
1. Gázok oldhatósága vízben: 101 325 Pa nyomáson g/100 g vízben t/ 0 C 0 20 30 60 O 2 0,006945 0,004339 0,003588 0,002274 H 2S 0,7066 0,3846 0,2983 0,148 HCl 82,3 72 67,3 56,1 CO 2 0,3346 0,1688 0,1257
Szabadentalpia nyomásfüggése
 Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék. Hőkezelés 2. (PhD) féléves házi feladat. Acélok cementálása. Thiele Ádám WTOSJ2
 BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Hőkezelés. (PhD) féléves házi feladat Acélok cementálása Thiele Ádám WTOSJ Budaest, 11 Tartalomjegyzék 1. A termokémiai kezeléseknél lejátszódó
BUDAPESTI MŰSZAKI EGYETEM Anyagtudomány és Technológia Tanszék Hőkezelés. (PhD) féléves házi feladat Acélok cementálása Thiele Ádám WTOSJ Budaest, 11 Tartalomjegyzék 1. A termokémiai kezeléseknél lejátszódó
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Acélok nem egyensúlyi átalakulásai
 Acélok nem egyensúlyi átalakulásai Acélok egyensúlyitól eltérő átalakulásai Az ausztenit átalakulásai lassú hűtés Perlit diffúziós átalakulás α+fe 3 C rétegek szilárdság közepes martensit bainit finom
Acélok nem egyensúlyi átalakulásai Acélok egyensúlyitól eltérő átalakulásai Az ausztenit átalakulásai lassú hűtés Perlit diffúziós átalakulás α+fe 3 C rétegek szilárdság közepes martensit bainit finom
Károly Gyula Józsa Róbert KONVERTERES ACÉLGYÁRTÁS
 Károly Gyula Józsa Róbert KONVERTERES ACÉLGYÁRTÁS Miskolci Egyetem 2012/2013 Károly Gyula - Józsa Róbert műsz. tud. doktora Prof. emeritus okl. kohómérnök vezető mérnök KONVERTERES ACÉLGYÁRTÁS A digitális
Károly Gyula Józsa Róbert KONVERTERES ACÉLGYÁRTÁS Miskolci Egyetem 2012/2013 Károly Gyula - Józsa Róbert műsz. tud. doktora Prof. emeritus okl. kohómérnök vezető mérnök KONVERTERES ACÉLGYÁRTÁS A digitális
Acélok és öntöttvasak definíciója
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája ACÉLOK ÉS ALKALMAZÁSUK Dr. Palotás Béla palotasb@eik.bme.hu Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája ACÉLOK ÉS ALKALMAZÁSUK Dr. Palotás Béla palotasb@eik.bme.hu Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus
a réz(ii)-ion klorokomplexének előállítása...
 Általános és szervetlen kémia Laborelőkészítő előadás IX-X. (2008. október 18.) A réz(i)-oxid és a lecsapott kén előállítása Metallurgia, a fém mangán előállítása Megfordítható redoxreakciók Szervetlen
Általános és szervetlen kémia Laborelőkészítő előadás IX-X. (2008. október 18.) A réz(i)-oxid és a lecsapott kén előállítása Metallurgia, a fém mangán előállítása Megfordítható redoxreakciók Szervetlen
I. ANALITIKAI ADATOK MEGADÁSA, KONVERZIÓK
 I. ANALITIKAI ADATOK MEGADÁSA, KONVERZIÓK I.2. Konverziók Geokémiai vizsgálatok során gyakran kényszerülünk arra, hogy különböző kémiai koncentrációegységben megadott adatokat hasonlítsunk össze vagy alakítsuk
I. ANALITIKAI ADATOK MEGADÁSA, KONVERZIÓK I.2. Konverziók Geokémiai vizsgálatok során gyakran kényszerülünk arra, hogy különböző kémiai koncentrációegységben megadott adatokat hasonlítsunk össze vagy alakítsuk
13 Elektrokémia. Elektrokémia Dia 1 /52
 13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
1. A VÍZ SZÉNSAV-TARTALMA. A víz szénsav-tartalma és annak eltávolítása
 1. A VÍZ SZÉNSAV-TARTALMA A víz szénsav-tartalma és annak eltávolítása A természetes vizek mindig tartalmaznak oldott széndioxidot, CO 2 -t. A CO 2 a vizekbe elsősor-ban a levegő CO 2 -tartalmának beoldódásával
1. A VÍZ SZÉNSAV-TARTALMA A víz szénsav-tartalma és annak eltávolítása A természetes vizek mindig tartalmaznak oldott széndioxidot, CO 2 -t. A CO 2 a vizekbe elsősor-ban a levegő CO 2 -tartalmának beoldódásával
VÖRÖSISZAP HASZNOSÍTÁS ROMELT TECHNOLÓGIÁVAL PROJEKT ÖSSZEFOGLALÓ. Feladat. Termékek. Cél. Közreműködők BERUHÁZÁSI TERVEZET
 BERUHÁZÁSI TERVEZET VÖRÖSISZAP HASZNOSÍTÁS ROMELT TECHNOLÓGIÁVAL PROJEKT ÖSSZEFOGLALÓ Feladat Termékek Cél Vörösiszap és egyéb ipari hulladékok hasznosítására alkalmas létesítmény megvalósítása innovatív
BERUHÁZÁSI TERVEZET VÖRÖSISZAP HASZNOSÍTÁS ROMELT TECHNOLÓGIÁVAL PROJEKT ÖSSZEFOGLALÓ Feladat Termékek Cél Vörösiszap és egyéb ipari hulladékok hasznosítására alkalmas létesítmény megvalósítása innovatív
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Vas- karbon ötvözetrendszer. Összeállította: Csizmazia Ferencné dr.
 Vas- karbon ötvözetrendszer Összeállította: Csizmazia Ferencné dr. 1 Vas- Karbon diagram 2 Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Vas- karbon ötvözetrendszer Összeállította: Csizmazia Ferencné dr. 1 Vas- Karbon diagram 2 Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
5 előadás. Anyagismeret
 5 előadás Anyagismeret Ötvözet Legalább látszatra egynemű fémes anyag, amit két vagy több alkotó különböző módszerekkel való egyesítése után állítunk elő. Alapötvöző minden esetben fémes anyag. Ötvöző
5 előadás Anyagismeret Ötvözet Legalább látszatra egynemű fémes anyag, amit két vagy több alkotó különböző módszerekkel való egyesítése után állítunk elő. Alapötvöző minden esetben fémes anyag. Ötvöző
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2002
 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI FELVÉTELI FELADATOK 2002 JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden
1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI FELVÉTELI FELADATOK 2002 JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden
A gáz halmazállapot. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
Légköri termodinamika
 Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Energia. Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Lánghegesztés és lángvágás
 Dr. Németh György főiskolai docens Lánghegesztés és lángvágás 1 Lánghegesztés Acetilén (C 2 H 2 ) - oxigén 1:1 keveréke 3092 C 0 magas lánghőmérséklet nagy terjedési sebesség nagy hőtartalom jelentéktelen
Dr. Németh György főiskolai docens Lánghegesztés és lángvágás 1 Lánghegesztés Acetilén (C 2 H 2 ) - oxigén 1:1 keveréke 3092 C 0 magas lánghőmérséklet nagy terjedési sebesség nagy hőtartalom jelentéktelen
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Termokémia. Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Termokémia Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 A reakcióhő fogalma A reakcióhő tehát a kémiai változásokat kísérő energiaváltozást jelenti.
Termokémia Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 A reakcióhő fogalma A reakcióhő tehát a kémiai változásokat kísérő energiaváltozást jelenti.
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK
 ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
Fluidum-kőzet kölcsönhatás: megváltozik a kőzet és a fluidum összetétele és új egyensúlyi ásványparagenezis jön létre Székyné Fux V k álimetaszo
 Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Tüzeléstan előadás Dr. Palotás Árpád Bence
 Égéselméleti számítások Tüzeléstan előadás Dr. Palotás Árpád Bence Miskolci Egyetem - Tüzeléstani és Hőenergia Tanszék 2 Tüzelőanyagok Definíció Energiaforrás, melyből oxidálószer jelenlétében, exoterm
Égéselméleti számítások Tüzeléstan előadás Dr. Palotás Árpád Bence Miskolci Egyetem - Tüzeléstani és Hőenergia Tanszék 2 Tüzelőanyagok Definíció Energiaforrás, melyből oxidálószer jelenlétében, exoterm
Acélszerkezetek. 1. előadás 2012.02.10.
 Acélszerkezetek 1. előadás 2012.02.10. Az acél jellemzői Az acél a vas legfontosabb ötvözete, fő ötvözője a szén, mely 2,11 tömegszázalékot tartalmaz. Az acél olyan vasalapú ötvözet, melyet képlékeny átalakítással
Acélszerkezetek 1. előadás 2012.02.10. Az acél jellemzői Az acél a vas legfontosabb ötvözete, fő ötvözője a szén, mely 2,11 tömegszázalékot tartalmaz. Az acél olyan vasalapú ötvözet, melyet képlékeny átalakítással
Általános kémia képletgyűjtemény. Atomszerkezet Tömegszám (A) A = Z + N Rendszám (Z) Neutronok száma (N) Mólok száma (n)
 Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Összesen: 20 pont. 1,120 mol gázelegy anyagmennyisége: 0,560 mol H 2 és 0,560 mol Cl 2 tömege: 1,120 g 39,76 g (2)
 I. FELADATSOR (KÖZÖS) 1. B 6. C 11. D 16. A 2. B 7. E 12. C 17. E 3. A 8. A 13. D 18. C 4. E 9. A 14. B 19. B 5. B (E is) 10. C 15. C 20. D 20 pont II. FELADATSOR 1. feladat (közös) 1,120 mol gázelegy
I. FELADATSOR (KÖZÖS) 1. B 6. C 11. D 16. A 2. B 7. E 12. C 17. E 3. A 8. A 13. D 18. C 4. E 9. A 14. B 19. B 5. B (E is) 10. C 15. C 20. D 20 pont II. FELADATSOR 1. feladat (közös) 1,120 mol gázelegy
Általános Kémia, 2008 tavasz
 9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
Elektrokémia. A nemesfém elemek és egymással képzett vegyületeik
 Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV.
 TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
Diffúzió. Diffúzió. Diffúzió. Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
 Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Kémiai metallurgia-ii (Fémelőállítási folyamatok elméleti alapjai)
 MISKOLCI EGYETEM Műszaki Anyagtudományi Kar Kerpely Antal Anyagtudományok és Technológiák Doktori Iskola Kémiai metallurgia-ii (Fémelőállítási folyamatok elméleti alapjai) Dr. Kékesi Tamás TANTÁRGYLEÍRÁS
MISKOLCI EGYETEM Műszaki Anyagtudományi Kar Kerpely Antal Anyagtudományok és Technológiák Doktori Iskola Kémiai metallurgia-ii (Fémelőállítási folyamatok elméleti alapjai) Dr. Kékesi Tamás TANTÁRGYLEÍRÁS
REDOXI REAKCIÓK GYAKORLÁSA. Készítette: V.Baráth Csilla
 REDOXI REAKCIÓK GYAKORLÁSA Készítette: V.Baráth Csilla Milyen kapcsolat van köztük és a redoxi reakció között? 1.NEVEZD MEG A KÉPEN LÁTHATÓ RAJZFILM FIGURÁKAT! 1.NEVEZD MEG A KÉPEN LÁTHATÓ RAJZFILM FIGURÁKAT!
REDOXI REAKCIÓK GYAKORLÁSA Készítette: V.Baráth Csilla Milyen kapcsolat van köztük és a redoxi reakció között? 1.NEVEZD MEG A KÉPEN LÁTHATÓ RAJZFILM FIGURÁKAT! 1.NEVEZD MEG A KÉPEN LÁTHATÓ RAJZFILM FIGURÁKAT!
Anyagismeret. 3. A vas- karbon ötvözet
 Anyagismeret 3. A vas- karbon ötvözet A fémek és ötvözetek szerkezete Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Anyagismeret 3. A vas- karbon ötvözet A fémek és ötvözetek szerkezete Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Erre a célra vas(iii)-kloridot és a vas(iii)-szulfátot használnak a leggyakrabban
 A vasgálic 1 egy felhasználása Az Európai Unióhoz csatlakozva a korábbinál jóval szigorúbb előírásokat léptettek életbe a szennyvíztisztító telepek működését illetően. Az új szabályozás már jóval kevesebb
A vasgálic 1 egy felhasználása Az Európai Unióhoz csatlakozva a korábbinál jóval szigorúbb előírásokat léptettek életbe a szennyvíztisztító telepek működését illetően. Az új szabályozás már jóval kevesebb
SZERVETLEN KÉMIAI REAKCIÓEGYENLETEK
 SZERVETLEN KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Zárójel jelzi a reakciót, ami más témakörnél található meg. REAKCIÓK FÉMEKKEL fém
SZERVETLEN KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Zárójel jelzi a reakciót, ami más témakörnél található meg. REAKCIÓK FÉMEKKEL fém
ACÉLSZERKEZETEK I. - 1. Előadás
 ACÉLSZERKEZETEK I. - 1. Előadás Dr. RADNAY László PhD. Főiskolai Docens Debreceni Egyetem Műszaki Kar Építőmérnöki Tanszék E-mail: radnaylaszlo@gmail.com [1] In Memoriam Prof. Dr. Fernezelyi Sándor Prof.
ACÉLSZERKEZETEK I. - 1. Előadás Dr. RADNAY László PhD. Főiskolai Docens Debreceni Egyetem Műszaki Kar Építőmérnöki Tanszék E-mail: radnaylaszlo@gmail.com [1] In Memoriam Prof. Dr. Fernezelyi Sándor Prof.
ÜSTMETALLURGIA. Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR METALLURGIAI INTÉZET ÜSTMETALLURGIA Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ Miskolc, 2014 1. TANTÁRGYLEÍRÁS A tantárgy/kurzus
MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR METALLURGIAI INTÉZET ÜSTMETALLURGIA Nappali tagozat FÉMELŐÁLLÍTÁSI ÉS ÖNTÉSZETI SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ Miskolc, 2014 1. TANTÁRGYLEÍRÁS A tantárgy/kurzus
A Dunaferr acéllemez-gyártásának fenntartásához szükséges és mûködtethetô acélgyártási technológia
 Vaskohászat Rovatvezetôk: dr. Takács István dr. Verô Balázs SZÜCS LÁSZLÓ TAKÁCS ISTVÁN A Dunaferr acéllemez-gyártásának fenntartásához szükséges és mûködtethetô acélgyártási technológia A szerzôk áttekintik
Vaskohászat Rovatvezetôk: dr. Takács István dr. Verô Balázs SZÜCS LÁSZLÓ TAKÁCS ISTVÁN A Dunaferr acéllemez-gyártásának fenntartásához szükséges és mûködtethetô acélgyártási technológia A szerzôk áttekintik
Kémiai egyensúlyok [CH 3 COOC 2 H 5 ].[H 2 O] [CH3 COOH].[C 2 H 5 OH] K = k1/ k2 = K: egyensúlyi állandó. Tömeghatás törvénye
![Kémiai egyensúlyok [CH 3 COOC 2 H 5 ].[H 2 O] [CH3 COOH].[C 2 H 5 OH] K = k1/ k2 = K: egyensúlyi állandó. Tömeghatás törvénye Kémiai egyensúlyok [CH 3 COOC 2 H 5 ].[H 2 O] [CH3 COOH].[C 2 H 5 OH] K = k1/ k2 = K: egyensúlyi állandó. Tömeghatás törvénye](/thumbs/93/111111933.jpg) Kémiai egyensúlyok CH 3 COOH + C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O v 1 = k 1 [CH 3 COOH].[C 2 H 5 OH] v 2 = k 2 [CH 3 COOC 2 H 5 ]. [H 2 O] Egyensúlyban: v 1 = v 2 azaz k 1 [CH 3 COOH].[C 2 H 5 OH] = k
Kémiai egyensúlyok CH 3 COOH + C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O v 1 = k 1 [CH 3 COOH].[C 2 H 5 OH] v 2 = k 2 [CH 3 COOC 2 H 5 ]. [H 2 O] Egyensúlyban: v 1 = v 2 azaz k 1 [CH 3 COOH].[C 2 H 5 OH] = k
Mekkora az égés utáni elegy térfogatszázalékos összetétele
 1) PB-gázelegy levegőre 1 vonatkoztatott sűrűsége: 1,77. Hányszoros térfogatú levegőben égessük, ha 1.1. sztöchiometrikus mennyiségben adjuk a levegőt? 1.2. 100 % levegőfelesleget alkalmazunk? Mekkora
1) PB-gázelegy levegőre 1 vonatkoztatott sűrűsége: 1,77. Hányszoros térfogatú levegőben égessük, ha 1.1. sztöchiometrikus mennyiségben adjuk a levegőt? 1.2. 100 % levegőfelesleget alkalmazunk? Mekkora
Hegeszthetőség és hegesztett kötések vizsgálata
 Hegeszthetőség és hegesztett kötések vizsgálata A világhálón talált és onnan letöltött anyag alapján 1 Kötési módok áttekintése 2 Mi a hegesztés? Két fém között hő hatással vagy erőhatással vagy mindkettővel
Hegeszthetőség és hegesztett kötések vizsgálata A világhálón talált és onnan letöltött anyag alapján 1 Kötési módok áttekintése 2 Mi a hegesztés? Két fém között hő hatással vagy erőhatással vagy mindkettővel
Példatár Anyagtechnológia Elemi példa - 4.
 Budapesti Műszaki és Gazdaságtudományi Egyetem Szent István Egyetem Óbudai Egyetem Typotex Kiadó TÁMOP-4.1.2-08/A/KMR-0029 Példatár Anyagtechnológia Elemi példa - 4. Termikus nyomásszabályzó-ház gyártása
Budapesti Műszaki és Gazdaságtudományi Egyetem Szent István Egyetem Óbudai Egyetem Typotex Kiadó TÁMOP-4.1.2-08/A/KMR-0029 Példatár Anyagtechnológia Elemi példa - 4. Termikus nyomásszabályzó-ház gyártása
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
ÁGAZATI SZAKMAI ÉRETTSÉGI VIZSGA KOHÁSZATI ISMERETEK KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ A MINTAFELADATOKHOZ
 KOHÁSZATI ISMERETEK KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ A MINTAFELADATOKHOZ Teszt jellegű feladatok 1. Mit értünk aktív biztonság alatt? 2 pont a) A már bekövetkezett baleset súlyosságát
KOHÁSZATI ISMERETEK KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ A MINTAFELADATOKHOZ Teszt jellegű feladatok 1. Mit értünk aktív biztonság alatt? 2 pont a) A már bekövetkezett baleset súlyosságát
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Termodinamikai bevezető
 Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2016. május 13. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2016. május 13. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Kémia
ÉRETTSÉGI VIZSGA 2016. május 13. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI VIZSGA 2016. május 13. 8:00 Az írásbeli vizsga időtartama: 120 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Kémia
Általános és szervetlen kémia Laborelıkészítı elıadás IX-X.
 Általános és szervetlen kémia Laborelıkészítı elıadás IX-X. A réz(i)-oxid és a lecsapott kén előállítása Metallurgia, a fém mangán előállítása Megfordítható redoxreakciók Szervetlen vegyületek hőbomlása
Általános és szervetlen kémia Laborelıkészítı elıadás IX-X. A réz(i)-oxid és a lecsapott kén előállítása Metallurgia, a fém mangán előállítása Megfordítható redoxreakciók Szervetlen vegyületek hőbomlása
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
A kémiai és az elektrokémiai potenciál
 Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
A munkavégzés a rendszer és a környezete közötti energiacserének a D hőátadástól eltérő valamennyi más formája.
 11. Transzportfolyamatok termodinamikai vonatkozásai 1 Melyik állítás HMIS a felsoroltak közül? mechanikában minden súrlódásmentes folyamat irreverzibilis. disszipatív folyamatok irreverzibilisek. hőmennyiség
11. Transzportfolyamatok termodinamikai vonatkozásai 1 Melyik állítás HMIS a felsoroltak közül? mechanikában minden súrlódásmentes folyamat irreverzibilis. disszipatív folyamatok irreverzibilisek. hőmennyiség
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Atomok. szilárd. elsődleges kölcsönhatás. kovalens ionos fémes. gázok, folyadékok, szilárd anyagok. ionos fémek vegyületek ötvözetek
 Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás Hőáramlás (konvekció) olyan folyamat,
 2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás. 2.1. Hőáramlás (konvekció) olyan folyamat, amelynek során a hő a hordozóközeg áramlásával kerül
2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás. 2.1. Hőáramlás (konvekció) olyan folyamat, amelynek során a hő a hordozóközeg áramlásával kerül
A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja. KÉMIÁBÓL I. kategóriában ÚTMUTATÓ
 Oktatási ivatal A versenyző kódszáma: A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja Munkaidő: 300 perc Elérhető pontszám: 100 pont KÉMIÁBÓL I. kategóriában
Oktatási ivatal A versenyző kódszáma: A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny második fordulójának feladatlapja Munkaidő: 300 perc Elérhető pontszám: 100 pont KÉMIÁBÓL I. kategóriában
Hőtan I. főtétele tesztek
 Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Szóbeli vizsgatantárgyak. 1. Kohászati technológia 2. Kohászati géptan 3. Gazdasági, munkajogi, munka- és környezetvédelmi ismeretek 52 5432 06/V
 Szóbeli vizsgatantárgyak 1. Kohászati technológia 2. Kohászati géptan 3. Gazdasági, munkajogi, munka- és környezetvédelmi ismeretek 2 Kohászati technológia tantárgy szóbeli vizsgatételei 1. a. Ismertesse
Szóbeli vizsgatantárgyak 1. Kohászati technológia 2. Kohászati géptan 3. Gazdasági, munkajogi, munka- és környezetvédelmi ismeretek 2 Kohászati technológia tantárgy szóbeli vizsgatételei 1. a. Ismertesse
8. osztály 2 Hevesy verseny, megyei forduló, 2004.
 8. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
8. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
Anyagvizsgálati módszerek Elektroanalitika. Anyagvizsgálati módszerek
 Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
Mérnöki anyagok NGB_AJ001_1. 1. Ötvözők hatása 2. Szerkezeti acélok
 Mérnöki anyagok NGB_AJ001_1 1. Ötvözők hatása 2. Szerkezeti acélok Az ötvöző elemek kapcsolata az alapfémmel Szilárd oldatot képeznek szubsztitúciós szilárd oldatot alkotnak (Mn, Ni, Cr, Co, V) interstíciós
Mérnöki anyagok NGB_AJ001_1 1. Ötvözők hatása 2. Szerkezeti acélok Az ötvöző elemek kapcsolata az alapfémmel Szilárd oldatot képeznek szubsztitúciós szilárd oldatot alkotnak (Mn, Ni, Cr, Co, V) interstíciós
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam
 A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam A feladatok megoldásához csak
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam A feladatok megoldásához csak
PiAndTECH FluidKAT katalitikus izzóterek
 PiAndTECH FluidKAT katalitikus izzóterek Hő felszabadítás katalitikus izzótéren, (ULE) ultra alacsony káros anyag kibocsátáson és alacsony széndioxid kibocsátással. XIV. TÁVHŐSZOLGÁLTATÁSI KONFERENCIÁT
PiAndTECH FluidKAT katalitikus izzóterek Hő felszabadítás katalitikus izzótéren, (ULE) ultra alacsony káros anyag kibocsátáson és alacsony széndioxid kibocsátással. XIV. TÁVHŐSZOLGÁLTATÁSI KONFERENCIÁT
Minta feladatsor. Az ion képlete. Az ion neve O 4. Foszfátion. Szulfátion CO 3. Karbonátion. Hidrogénkarbonátion O 3. Alumíniumion. Al 3+ + Szulfidion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve Foszfátion Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve Foszfátion Szulfátion
