Az Aktin Filamentumok Hosszát Szabályozó Fehérjék Szerkezeti Dinamikája és Élettani Szerepük
|
|
|
- Laura Orbán
- 6 évvel ezelőtt
- Látták:
Átírás
1 Az Aktin Filamentumok Hosszát Szabályozó Fehérjék Szerkezeti Dinamikája és Élettani Szerepük Szatmári Dávid Zoltán Témavezetők: Prof. Dr. Nyitrai Miklós, Prof. Dr. Robert C. Robinson Interdiszciplináris Orvostudományok Doktori Iskola D93 Doktori Iskola vezetője: Prof. Dr. Sümegi Balázs Program (B-130): Funkcionális fehérjedinamika vizsgálata biofizikai módszerekkel Program vezetője: Prof. Dr. Nyitrai Miklós Pécsi Tudományegyetem, Általános Orvostudományi Kar Biofizikai Intézet Pécs, 2018
2 Irodalmi áttekintés Az aktin egy 42 kda-os globuláris fehérje. Az aktin az eukarióta sejtekben mikrofilamentumokat hoz létre, amik a citoszkeletális rendszer fő komponensét képezik. Izomsejtekben, a vékony filamentumok fő tömegét az aktin filamentumok adják és a szarkomer egyfajta vázrendszereként működnek. In vivo az aktin G-aktinként (globuláris) monomerként vagy polimer formában F-aktinként (filamentális) van jelen. Mindkettő elengedhetetlenűl fontos funkciót tölt be a sejt mobilitásában, összehúzódásában, osztódásában, intracelluláris transzport folyamatokban, jelátviteli folyamatokban és részt vesz a sejtek közötti kapcsolatok és a sejtalak fenntartásában. Egy lényeges szempont az aktin szerepében, hogy számos intracelluláris folyamatot az aktin és a sejtmembrán közötti kölcsönhatások szabályozzák. A gerincesekben három féle aktin izoforma fordul elő, az alfa, béta és gamma. Alfa aktint főként az izomszövetben találunk, ezek adják a kontraktilis egység fő tömegét. A béta és gamma aktin számos sejttípusban megtalálható mint a citoszkeletális rendszert alkotó elemek és a belső sejtmozgások szabályzói. A sejtek kontrolálják a mikrofilamentumaik mennyiségét, azok dinamikus hosszával lehetővé válik a citoszkeletális rendszer gyors átrendeződése, így tud a sejt gyorsan reagálni bármilyen külső vagy belső behatásra. Az aktin azon tulajdonsága, hogy hosszú filamentumokba polimerizálódik az alapja annak, hogy fontos szerepet tölt be több sejtfolyamatban, mint például a morfogenezis, membrán kicserélődés és sejtosztódás. Erős sejtadhéziók a szövetképződés során, vagy struktúrfehérjék a membránkitüremkedésekben is képesek ehhez a vázhoz kihorgonyozódni így segítve az endocitózis és a citokinézis folyamatát. Az aktin polimerizációja során vagy a motorfehérjékkel közreműködve képes erőt generálni, így játszik fontos szerepet a vezikulák és organellumok intracelluláris transzportjában, izomösszehúzódásban, sejtmozgásban, embriógenezisben és fokozza a daganatos sejtek inváziós képességét. Ahhoz, hogy ennyire sokoldalú legyen, az aktin hálózat térbeli és időbeli elrendeződését számos aktin kötő fehérje szabályozza. Ezek a szabályzó faktorok képesek szétszerelni az óriási aktin struktúrákat és új, egy adott sejtfolyamathoz szükséges szerkezetű aktin hálózat felépítését segítik. Ahhoz, hogy megértsük ezt az aktin alapú gépezetet, szükséges, hogy megvizsgáljuk a kötő fehérjék okozta aktin filamentumok konformációs és dinamikai változásait. Az aktin monomerek polimerizációja egy termikus diffúzió szabályozta folyamat. A monomerek spontán összekapcsolódását a magas magnézium és kálium koncentráció fokozza. A polimerizáció a nukleációval, néhány monomer összetapadásával kezdődik. A hajtó erő egy nem-egyensúlyi termodinamikai erő, a dimerek és trimerek entrópiája lecsökken a magas lokális monomer koncentráció miatt. Az aktin magok kialakulása után a filamentum növekedés (elongáció) 2
3 azonnal beindul, a filamentum két végén eltérő kinetikával. A gyorsan növekvő véget szakállas vagy plusz végnek, a lassan növekvőt pedig hegyes vagy negatív végnek nevezzük. A növekedés kinetikája függ a rendelkezésre álló szabad aktin monomerek koncentrációjától (C szabad ) és a monomer-filamentum kötési rátától (k a ). Végül, az elongáció egy reverzibilis dinamikus állapotot ér el, amiben a hossz növekedése nem számottevő. Ebben a szakaszban a polimerizáció egy steady-state egyensúlyba kerül, amit a monomer-polimer arány határoz meg és jellemzően, in vitro körülmények között, 0.1 μm monomer koncentrációt tart fenn. Azonban az átlagos filamentum hossz nem változik a folyamatos aktin asszociáció és disszociáció következtében, a negatív végen inkább a disszociáció, míg a pozitív végen inkább az asszociáció dominál. Az aktin kötő fehérjék (ABP) képesek aktin monomert vagy polimert illetve mindkettőt kötni. Azonban nem csak az ABP-k de más kis molekulák is képesek aktinhoz kötni, így befolyásolva az aktin citoszkeleton dinamikáját és katalizálva az aktin filamentumok polimerizációját vagy depolimerizációját. Ezek nem feltétlen vannak hatással a tágabb értelmeben vett sejtes folyamatokra, mint a sejt migráció vagy mechanoszenzoros érzékelés, de jól használhatók kísérleti célokra. Azon fehérjék, amik aktin filamentumot kötnek hatással lehetnek a filamentum össze- és szétszerelődésére, helyére és időbeli változására. Fiziológiás körülmények mellett az aktin monomerek filamentumokba polimerizálódnak, de a spontán depolimerizáció túl lassú folyamat ahhoz, hogy befolyásolja az in vivo megfigyelt aktin filamentumok gyors dinamikáját. Gelsolin, aktin depolimerizációs faktor ADF/cofilin, és számos más aktin szevering/depolimerizáló fehérje gyorsítani tudja a filamentumok szétszerelődését és elősegíti az aktin citoszkeleton újrarendeződését. Sok ABP, a G-aktin mennyiséget tudja szabályozni a monomerek szekvesztrálása vagy a nukleotid kicserélődésének gátlása/segítése révén. Az aktin kötő fehérjék szintén befolyásolják az aktin és más sejtkomponensek mint sejtmembrán, mikrotubulusok vagy más szabályzófehérjék kölcsönhatását. Miközben néhány aktin kötő fehérje szabályozza az aktin citoszkeletont, addig mások arra használják a kötött aktin monomereket vagy polimereket, hogy befolyásolják saját aktivitásukat vagy irányítsák saját lokalizációjukat. Struktúrális sokszínűség jellemzi az aktin kötő fehérjéket, azonban az aktin kötő konzervatív doméneket (ABD) szerkezetük alapján csoportosítjuk. A következő ABD csoportokat különítjük el: kalponin-homológia domén (CH), leucinban gazdag ismétlődés domén (LRR), forminhomológia2 domén (FH2), WASp-homológia2 domén (WH2), aktin-depolimerizációs faktor/cofilin domén (ADF/cofilin), gelsolin-homológia domén, miozin motor domén. Az F- aktin hosszt szabályozó fehérjék intracelluláris funkciója, azok szerkezeti dinamikájával és fiziológiásan releváns komplexeivel van kapcsolatban, így a teljes citoszkeleton 3
4 átrendeződése vagy a vékony filementumok hosszának optimalizálása a szükséges. A leiomodin izom specifikus, a gelsolin sokkal gyakoribb aktin kötő fehérje. Érdeklődésünk középpontjában ezen fehérjék szerkezeti változásai és az aktin kötésükhöz kapcsolható élettanilag fontos folyamatok állnak. Amíg a gelsolin egy szevering és sapkázó fehérje, addig a leiomodin nukleálja és elongálja az aktin polimerket. A gelsolin, főként a sejtmembrán PIP 2 - ben gazdag részei közelében tartózkodik és tudjuk, hogy a PIP 2 gátolja a gelsolin-aktin kölcsönhatást, eltávolítja a gelsolin sapkát a filamentum végéről. Így egyértelműnek tűnik a megállapítás, hogy a membrán PIP 2 szigetei segítik a filamentum végzáró sapkák eltávolítását, ami egy gyors és irányított filamentum növekedést eredményez, így nyomja el a sejtmembránt. A gelsolin ATP kötésének felfedezése óta gondoljuk azt, hogy a gelsolin számos funkciói közül néhányban fontos szerepet játszhat az ATP. Magas kálcium koncentráció mellett a gelsolin teljes aktivitást mutat, megváltozott szerkezetének hatására veszíti el ATP kötő képességét. Az ATP kötött gelsolin szerkezete nagyobb kálcium érzékenységet mutat. A tropomodulinok és leiomodinok homológ doménekből épülnek fel. Mindkettő tartalmaz tropomiozin-kötő domént (TMBS1 és/vagy 2), egy aktin-kötő domént (ABS1) és egy leucinban gazdag ismétlődés domént (ABS2/LRR) ami szintén aktin monomert köt. Ezen homlógiák mellett a leiomodin egy C-terminális nyúlvánnyal (C-term) hosszabb a tropomodulintól, ami tartalmaz egy prolinban gazdag régiót (PR, potenciálisan egy felismerési hely intracelluláris szignalizációs folyamatokban), egy helikális domént és egy Wiskott Aldrich szindróma fehérje (WASP) homológia2 (WH2) domént. Szívizom szarkomerekben a leiomodin2 és tropomodulin1 expressziója a miofibrillum érettségi szintjétől függ. Kálcium aktiválta gelsolin a pozitív véghez köt, míg a leiomodin a negatív véghez, de mindkettő képes a filamentum oldalához is kötni. Ez a két különböző F-aktin hossz szabályzó fehérje eltérő szerepet játszik abban, hogy hogyan változtatják meg az aktin filamentum polimerizációjának kinetikáját és dinamikáját. A gelsolin rövid sapkázott aktin polimereket mobilizál, míg a leiomodin az összehúzódáshoz szükséges aktomiozin komplexben stabilizálja a filamentumok optimális hosszát, de együttes szimultán funkciójuk eddig még nem vizsgált. Azonban több különböző adat együtteseként tudjuk jellemezni az izomsejtekben betöltött funkciójukat. Az aktivált gelsolin véletlenszerűen helyezkedik el a vékony filamentum mentén a szarkomerben és csökkenti azok hosszát, a tropomiozinnal versenyzik a kötőhelyekért a filamentumok mentén, így a gelsolin-tropomiozin komplex dinamikája befolyásolhatja a vékony filamentumok hosszát. A gelsolin fokozza az aktomiozin ATPáz aktivitását ami tropomiozin hatására növekszik, így egy kálciumtól független aktomiozin funkciót segítő fehérjekomplex jön létre. A leiomodin a szarkomer M-vonala 4
5 közelében illetve a vékony filamentum teljes hosszában megjelölőlhető. A leiomodin expressziója a miofibrillum érése során fokozódik majd a fehérje lokalizációjával egyre erősebben festődik. A leiomodinok többféle tropomiozin izoformához képesek kötni, így erősítik vagy gyengítik a leiomodin aktin polimerizációt fokozó hatását. Megállapították, hogy a tropomiozin befolyásolja a szívizom leiomodin2 hegyes vég kötő képességét, de nem befolyásolja a de novo nukleációs aktivitását, amit a leiomodin különböző állapotaihoz tartozó szerkezeti különbségei is magyaráznak. Egyelőre még nincs egyértelmű adat arra vonatkozóan, hogy a leiomodin miként kötődik a filamentum teljes hosszában és hatással vane a miozin ATPáz aktivitására. Célok A munkám célja volt, hogy több ismeretet gyűjtsünk az aktin filamentumok hosszát szabályozó fehérjék működéséről, elsősorban két különböző végkötő fehérjével foglalkoztam, a pozitív vég kötő citoplazmatikus gelsolinnal és a negatív véget kötő szívizom leiomodin2- vel. A hiányzó lépések tisztázásával, a gelsolin aktivációs ciklusa egyértelműen leírja a gelsolin szevering funkciójának szabályzását, így segítve a sejtmemebrán közeli citoszkeletális rendszer átrendeződésének megértését. A szívizom leiomodin2 aktin filamentum hossz növelő és aktin-tropomiozin-miozin komplex módosító funkciójának mélyebb megértése érdekében további vizsgálatok voltak szükségesek. A főbb célok a következők: ATP és kálcium együttes hatásának vizsgálata a gelsolin PIP 2 kötésére. Azonosítani a gelsolin sejtmembrán és citoplazma közti aktivációs ciklusának hiányzó lépéseit. Karakterizálni a szívizom leiomodin2 belső struktúrális tulajdonságait és a tropomodulin1-től különböző C-terminális régióját. Megismerni a leiomodin2 aktint kötegelő hatékonyságát. Feltérképezni a leiomodin2 vékonyfilamentum oldalkötő képességét és funkcionális jelentőségét. 5
6 Anyagok és Módszerek Fehérjék előkészítése és jelölése Kálcium kötött G-aktin, nyúl vázizom acetonforgácsból lett izolálva Spudich és Watt által kidolgozott módszer alapján, aminek Mossakowska és munkatársai által módosított protokolját használtam. Vázizom tropomiozint (Tpm1.1/2.2) egy korábbi protokol alapján preparáltam majd hidroxiapatit kromatográfiával tisztítottam. A humán citoplazma gelsolin és mutánsai különböző psy5 plazmid konstrukciók segítségével lettek expresszálva, mindegyik egy His-taget és az adott human gelsolin vagy mutánsai szekvenciáját tartalmazta, E. coli Rosetta2 (DE3) plys sejtekben. A Rattus norvegicus szívizom leiomodin2 és C-terminális fragmentuma ( as; Cterm) egy Twin-CN kitin-intein önhasító és tisztító rendszer segítségével lettek expresszálva és tisztítva. A ptyb1 plazmid DNS konstrukciókat Roberto Dominguez laborjából kaptuk. Az aktin Cys-374 aminósavját Alexa488-maleimiddel vagy Alexa532-maleimiddel a gyártó által meghatározott protokol alapján jelöltem meg, más mérésekhez IAEDANS-szel (5-((((2- iodoacetyl) amino) ethyl) amino) naphthalene-1-sulfonic acid) vagy IAF-fel (5- iodoacetoamidofluorescein) jelöltem, korábban ismertetett protokolok alapján. A pirén (N-1- pyrene-iodoacetamide) jelölés szintén egy korábban kidolgozott standard protokol alapján történt. Az aktin koncentrációját és a jelölés sikerességét abszorpciós fotometriával határoztam meg. Alexa488-maleimiddel és Alexa532-maleimiddel jelöltem a gelsolin mutánsok ciszteinjeit (Cys93, Cys188, Cys201, Cys304 és Cys645) a gyártó által meghatározott protokol alapján. Membrán vezikulák preparálása Foszfolipid vezikulákat James H. Morrissey módosított protokolja alapján készítettem (Protocol from James H. Morrissey, Dept. of Biochemistry, University of Illinois at Urbana- Champaign, Urbana, IL 61801, USA). Annyiban módosítottam, hogy 1%-os PIP 2 (PtdIns- (4,5)-P 2 (1,2-dipalmitoyl)) 79%-os PC (L-α-phosphatydilcholine) és 20%-os PS (3-snphosphatidyl-L-serine) lipid keveréket 20 µm rhodamin590 N-szukcinimidil észter tartalmú kloroform oldatban vettem fel. Fluoreszcencia spektroszkópiás módszerek A leiomodin2 intrinszik triptofánjait használva, fluoreszcencia emisszió kapcsolt szerkezeti dinamika méréseket végeztem. Steady-state fluoreszcencia kioltási kísérlettel, Alexa488 jelölt mutáns gelsolinok szerkezeti dinamikáját karakterizáltam. Az Alexa488 fluorofór emissziójának kiolthatósága a jelölt gelsolin fehérjelánc hozzáférhetőségét jellemzi, kálcium, ATP vagy PIP 2 vel alkotott komplexében. Steady-state anizotrópia mérésekkel jellemeztem 6
7 különböző, fluorofórral jelölt ATP és PIP 2 molekulák kötési dinamikáját. A leiomodin2 intrinszik triptofánjainak steady-state anizotrópia mérésével jellemeztem a leiomodin intradomén szerkezeti felxibilitását. A leiomodin intrinszik triptofánjain további fluoreszcencia élettartam és anizotrópia lecsengés méréseket végeztem kereszt-korrelációs fázis-modulációs módszerrel (ISS K2 multi-frekvenciás fázis fluoriméter). Tervezett gelsolin mutánsok interdomén FRET méréseivel további információt szereztem a gelsolin flexibiltásáról kálcium, ATP vagy PIP 2 kötés mellett. Inter-monomer FRET mérésekkel vizsgáltam az aktin filamentumok leiomodin2 oldalkötése által megváltozott flexibilitását. A leiomodin2 hatására megváltozó aktin polimerizációs tulajdonságainak vizsgálatára idő függő pirén-aktin emissziós méréseket végeztem. Az aktin polimerizációját jellemző kritikus koncentráció meghatározásához különböző koncentrációjú pirén-aktin oldatok emissziós vizsgálatát végeztem, leiomodin2 jelenlétében és hiányában. A leiomodin2 F-aktin kötődés kinetikáját leiomodin kötés hatására bekövetkező pirén jelölt F-aktin valós idejű emissziójának mérésével vizsgáltam, ún. stopped-flow gyorskinetikai módszerrel. Röntgen diffrakciós vizsgálatok, krisztallográfia Kálcium mentes gelsolin és Alexa488 jelölt mutáns gelsolin fehérjekristályokat hoztunk létre ún. sitting-drop vapor diffúziós módszerrel. Röntgen-diffrakciós mérésekkel meghatároztuk azok szerkezetét. PIP 2 kritikus micella képződési koncentrációjának meghatározása A PIP 2 1-(1-octadecanoyl-fluorescein-2R-octadecanoylphosphatidyl)inositol-4,5-bisphosphate kritikus koncentrációjának meghatározására fényszórás méréseket végeztünk. Mikroszkópos képalkotás Konfokális fluoreszcencia mikroszkópos képalkotással vizsgáltam, hogy ATP hatására hogyan változik meg a rhodamin590-nel töltött PIP 2 tartalmú membránvezikulák felszínén kötött Alexa488-gelsolin molekulák mennyisége. Koszedimentációs vizsgálatok Magas sebességű koszedimentációs vizsgálatokkal jellemeztem a leiomodin2 F-aktin komplexek só függő kötési tulajdonságait. Coupled assay Coupled assay vizsgálatokkal jellemeztem a leiomodin hatását a HMM Mg 2+ -ATPáz aktivitására. 7
8 Eredmények és megvitatásuk A gelsolin aktivációs ciklusa Korábban már bizonyították, hogy ATP és PIP 2 versenyeznek a K ATP csatornák kötőhelyéért. Itt sikerült bemutatni, hogy az ATP képes leszorítani a PIP 2 -t a gelsolin kötőhelyéről is fiziológiás puffer körülmények mellett in vitro. Mindemellett, foszfolipid vezikulák felszínén PIP 2 -kötött gelsolin fehérjét is képes az ATP leszorítani. Ebből következik, hogy a plazmamembrán felszínén kötött gelsolin fehérjék ATP hatására disszociálnak a PIP 2 molekulákról és ez az ATP indukálta disszociáció a hiányzó lépés a gelsolin aktivációs ciklusából, ami során átrendezi a membrán közeli aktin polimerket. Egyéb iránt az ATP vagy PIP 2 nem mindig kötődik gelsolinhoz. Azonban, ha a gelsolin sapkázott filamentumok a plazmamembrán felé mutatnak, akkor a filamentum pozitív végén kötött gelsolin mobilitása erősen korlátozott és a membrában lévő PIP 2 molekulák közelében a membrán átrendeződésével növeli a gelsolin lokális koncentrációját és klaszereket alakíthatnak ki. Ezen faktorok növelik a PIP 2 kötött gelsolin mennyiségét ezzel növelve a szabad végű filamentumok számát. Azt feltételezhetjük, hogy a szabad filamentumok közelében az ATP hatékonyan szorítja le a PIP 2 kötött gelsolint. Az aktivációs ciklus szakaszai, standard sejtes körülmények között: Aktiváció, a szabad kálcium mennyisége 10 nm fölé emelkedik, ami a gelsolin szerkezeti változását okozza, így a kötött ATP disszociál és lehetővé teszi a gelsolin aktin filamentumhoz kötését. Szevering, a gelsolin-aktin kötés legyengíti az aktin-aktin kölcsönhatás erősségét ez a filamentum szeveringjéhez vezet. Sapkázás, a gelsolin a filamentum pozitív végéhez köt és megakadályozza annak elongációját. Szabad vég létrejötte, amikor a gelsolin sapkázott filamentum a plazmamembrán PIP 2 molekuláival találkozik, akkor a sapkázó fehérje egy ismeretlen folyamat révén leválik a filamentum végéről. A szabad végű aktin polimer elongációja így folytatódhat és erőt gyakorol a sejtmembránra. Leválás, a gelsolin az ATP molekulák révén leválik a plazmamembrán PIP 2 molekuláiról, ami az ATP-gelsolin szabad diffúziójához vezet. A gelsolin visszatér inaktív állapotába ha a kálcium koncentrációja visszaesik. Ezen a módon a gelsolin ATP szint függő módon válik le a sejtmembrán PIP 2 molekuláiról, hogy teret engedjen más PIP 2 -érzékeny aktin szabályozó fehérjéknek, majd újra lehetővé válik a gelsolin aktivációs ciklusa ha a PIP 2 mennyisége újra megnő. 8
9 A szívizom leiomodin2 szerkezeti dinamikája és funkciója Vizsgálataink alapján a patkány szívizom leiomodin2 (Lmod2) hasonló szerkezeti és funkcionális tulajdonságokkal rendelkezik, mint a humán leiomodin2. A patkány szívizom Lmod2 több rendezetlen szerkezetű flexibilis régióval rendelkezik, a homológ tropomodulin és más leiomodin izoformákhoz hasonlóan. Sikerült bebizonyítani, hogy a Lmod2 hatással van az aktin dinamikájára és só függő módon növeli az aktin polimerizációját. Ebből arra következtethetünk, hogy a leiomodin2 fontos szerepet játszhat a vékony filamentumok összeszerelésében, ott ahol a tropomiozin és az érett aktin filamentumok már rendelkezésre állnak és nincs szükség újabb aktin polimerekre. Patkány szívizom sejtekben, a végkötéstől függetlenül, a Lmod2 az egész vékony filamentum mentén festődik de a szarkomer M-vonala közelében található a legnagyobb mennyiségben. Ezen megfigyelést alátámasztva sikerült megmutatni, hogy in vitro a Lmod2 a filamentumok oldalához is képes kötni. Illetve az oldalkötés hatására az aktin filamentum rugalmassága fokozódik. Mindamellett a gelsolin ilyen jellegű hatásától eltérően, az F-aktinhoz kötött Lmod2 lecsökkenti a miozin aktin által fokozott Mg 2+ -ATPáz aktivitását. Ezen, újonan leírt leiomodin kölcsönhatások bizonyára funkcionális jelentőséggel is bírnak. Az, hogy a Lmod2 nem csak a vékony filamentum végeihez lokalizált hanem a filamentum oldalához is köt, oda ahol a miozin II kötőhelyek vannak, valószínűsíti, hogy a leiomodin hatással lehet az akto-miozin komplex működésére. Nagy mennyiségű leiomodin2 kötődés hatására a vékony- és vastagfilamentum közötti kölcsönhatás gyengül és a komplex által generált erő lecsökken. A Lmod2 függő miozin II aktivitásával kapcsolatos eredményeink kiegészítik a nem olyan régen leközölt leiomodin2 aktivációs ciklus modelt, ami jól magyarázza az eredményeink in vivo jelentőségét. Korábbi adatok alapján a leiomodinnak nagy jelentősége lehet a szív fejlődése során, ugyanis a Lmod2 szabályozhatja az akto-miozin komplex kötési aktivitását, mivel az optimálisnál nagyobb erő generálás a még fejlődésben lévő gyenge struktúrák sérülését okozhatja, szóval a leiomodin2 egyfajta erő-puffer rendszerként működik. Az aktin filamentumok plasztikusságát a hossz szabályozó fehérjék szabják meg Az aktin filamentumok számos funkcióval rendelkeznek, aminek az alapját az ABP-k okozta filamentum hossz plasztikus dinamikája határozza meg. A negatív vagy pozitív vég sapkázása módosítja az aktin filamentum turnover kinetikáját és dinamikáját, lehetővé téve, hogy a citoplazmatikus gelsolin aktin oligomereket mobilizálva újrarendezze a citoszkeletális rendszert vagy, hogy a leiomodin2 hosszú erős aktin polimereket tartson fenn a szarkomerben. Gelsolin és leiomodin mindkettő rendelkezik egy aktivációs ciklussal és 9
10 mindkettő fontos szerepet játszik a sejtmozgásban és az embrionális izomsejtek fejlődésében. Az aktin filamentum ellentétes végeit sapkázzák, így eltérő módon befolyásolják a filamentumok hosszát, de mindkettő képes a filamenumok oldalához is kötni más-más hatást gyakorolva a miozin II aktivitására. Élettani funkciójuk bonyolult komplexeik összességével értelmezhető, aminek az eredménye az aktin filamentumok hosszának pontos, precíz hangolása. Publikációk Publikációk a tézishez kapcsolódóan Dávid Szatmári, Beáta Bugyi, Zoltán Ujfalusi, László Grama, Réka Dudás and Miklós Nyitrai Cardiac leiomodin2 binds to the sides of actin filaments and regulate the ATPase activity of myosin PLOS ONE 12:(10) Paper p. (2017) IF: David Szatmari, Bo Xue, Balakrishnan Kannan, Leslie D. Burtnick, Beáta Bugyi, Miklós Nyitrai, Robert C. Robinson ATP competes with PIP 2 for binding to gelsolin submitted (2017) Szilvia Barkó*, Dávid Szatmári*, Emőke Bódis, Katalin Türmer, Zoltán Ujfalusi, David Popp, Robert C Robinson, Miklós Nyitrai Large-scale purification and in vitro characterization of the assembly of MreB from Leptospira interrogans BIOCHIMICA ET BIOPHYSICA ACTA-GENERAL SUBJECTS 1860:(9) pp (2016) *equal contributors IF: Kollar V, Szatmari D, Grama L, Kellermayer MSZ Dynamic Strength of Titin's Z-Disk End JOURNAL OF BIOMEDICINE AND BIOTECHNOLOGY 2010: Paper p. (2010) IF: Kellermayer MSZ, Bianco P, Martonfalvi Z, Nagy A, Kengyel A, Szatmari D, Huber T, Linari M, Caremani M, Lombardi V Muscle thixotropy: More than just cross-bridges? Response to comment by Campbell and Lakie 10
11 BIOPHYSICAL JOURNAL 94:(1) pp (2008) IF: Bianco P, Nagy A, Kengyel A, Szatmari D, Martonfalvi Z, Huber T, Kellermayer MSZ Interaction forces between F-Actin and titin PEVK domain measured with optical tweezers BIOPHYSICAL JOURNAL 93:(6) pp (2007) IF: Összesített IF: Poszterek és konferencia előadások Szatmári Dávid, Bugyi Beáta, Ujfalusi Zoltán, Grama László, Dudás Réka és Nyitrai Miklós A szívizom leiomodin2 képes az aktin filamentumok oldalához kötni és szabályozza a miozin ATPáz aktivitását Sümeg, Hungary, May Membrán-Transzport Konferencia David Szatmari, Wei Lin Lee, Shi Min Jiang, Jonathan Hobley, Miklós Nyitrai, Robert C. Robinson STRUCTURAL DYNAMICS OF HUMAN GELSOLIN Melbourne, Australia, November The 37th Annual Conference of the Australian Society for Biophysics Szatmari D, Dudas R, Nyitrai M Expression and biophysical characterization of cardiac leiomodin 2 Budapest, Hungary, August th European Biophysics Congress Published abstract: EUROPEAN BIOPHYSICS JOURNAL 40:(Suppl 1) p. 61. (2011) Dávid Szatmári, Péter Sárkány, Béla Kocsis, Tamás Nagy, Attila Miseta, Robert C. Robinson and Miklós Nyitrai Intracellular ion concentration dependent remodelling of bacterial MreB assemblies Helsinki, Finnland, 4-8 June European Cytoskeletal Forum Meeting 2017 David Szatmari, Reka Dudas, Attila Nagy, Gabor Hild and Miklos Nyitrai Expression and biophysical characterization of exportin6 Palermo, Italy, 28 August 2 September th European Conference on the Spectroscopy of Biological Molecules 2009 Szatmári D, Huber T, Németh V, Kollár V, Grama L, Kellermayer MSZ A titin mechanoszenzor vizsgálata. Sümeg, Hungary, May
12 38. Membrán-Transzport Konferencia Huber T, Szatmári D, Mártonfalvi Zs, Kellermayer MSZ A titin PEVK domén szekvenciamotivumainak szerkezete és mechanikája 37. Membrán-transzport Konferencia Sümeg Hungary május (2007) Huber T, Szatmári D, Mártonfalvi Zs, Kellermayer MSZ The stucture and mechanics of the titin's PEVK domain sequence motifs IV. International Conference on Molecular Recognition Pécs Hungary 2007 August (2007) Huber T, Szatmári D, Mártonfalvi Zs, Murvai Ü, Kiss B, Karsai Á, Grama L, Kellermayer MSZ Imaging and manipulation of cells and molecules with atomic force microscopy and fluorescence- AFM combinations 25 th Congress for European Society for Microcirculation Budapest, August (2008) Kellermayer MSZ, Bianco P, Nagy A, Karsai Á, Kengyel A, Huber T, Kiss B, Mártonfalvi Zs, Szatmári D, Grama L Nanomechanhanics of of single biomolecules Joint meeting of Hungarian and German Biophysicists May Hünfeld Germany (2007) 12
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A citoszkeletális rendszer
 A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
Biofizika I 2013-2014 2014.12.02.
 ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Sejt. Aktin működés, dinamika plus / barbed end pozitív / szakállas vég 1. nukleáció 2. elongáció (hosszabbodás) 3. dinamikus egyensúly
 Biofizikai módszerek a citoszkeleton vizsgálatára I: Kinetikai és steady-state spektroszkópiai módszerek Sejt Citoszkeletális rendszerek Orbán József, 2014 április Institute of Biophysics Citoszkeleton:
Biofizikai módszerek a citoszkeleton vizsgálatára I: Kinetikai és steady-state spektroszkópiai módszerek Sejt Citoszkeletális rendszerek Orbán József, 2014 április Institute of Biophysics Citoszkeleton:
Komplex egyszerű Aktin alapú mikrofilamentum rsz. Hogyan vizsgálhatunk folyamatokat? Komplex egyszerű S E J T
 Biofizikai módszerek a citoszkeleton vizsgálatára I. Kinetikai, steady-state módszerek, spektroszkópiai vizsgálatok Komplex egyszerű S E J T A citoszkeletális rendszer Orbán József, 213 Április Aktin citoszkeleton
Biofizikai módszerek a citoszkeleton vizsgálatára I. Kinetikai, steady-state módszerek, spektroszkópiai vizsgálatok Komplex egyszerű S E J T A citoszkeletális rendszer Orbán József, 213 Április Aktin citoszkeleton
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
2. AKTIN-KÖTŐ FEHÉRJÉK
 A CITOSZKELETÁLIS RENDSZER 2011. 02. 15. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 2. AKTIN-KÖTŐ FEHÉRJÉK Citoszkeletális aktin HEp-2 sejtekben - rodamin-falloidin jelölés forrás: Nyitrai Miklós, Grama László,
A CITOSZKELETÁLIS RENDSZER 2011. 02. 15. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 2. AKTIN-KÖTŐ FEHÉRJÉK Citoszkeletális aktin HEp-2 sejtekben - rodamin-falloidin jelölés forrás: Nyitrai Miklós, Grama László,
Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására
 Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására Ujfalusi Zoltán Témavezető: PROF. DR. N YITRAI MIKLÓS Doktori iskola: I n t e r d i s z c i p l i n á r
Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására Ujfalusi Zoltán Témavezető: PROF. DR. N YITRAI MIKLÓS Doktori iskola: I n t e r d i s z c i p l i n á r
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
11/15/10! A CITOSZKELETÁLIS RENDSZER! Polimerizáció! Polimerizációs egyensúly! Erő iránya szerint:! 1. valódi egyensúly (aktin)" Polimer mechanika!
 11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI MOLEKULÁRIS MOZGÁS MOTORFEHÉRJÉK DR. BUGYI BEÁTA - BIOFIZIKA ELŐADÁS PÉCSI TUDOMÁNYEGYETEM
BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI MOLEKULÁRIS MOZGÁS MOTORFEHÉRJÉK DR. BUGYI BEÁTA - BIOFIZIKA ELŐADÁS PÉCSI TUDOMÁNYEGYETEM
A citoszkeleton Eukarióta sejtváz
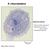 A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
A CITOSZKELETÁLIS RENDSZER Bugyi Beáta PTE ÁOK, Biofizikai Intézet. 9. A sejtmozgás mechanizmusai
 A CITOSZKELETÁLIS RENDSZER 2011. 05. 03. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 9. A sejtmozgás mechanizmusai Sejtmozgás, motilitás 1. Sejten belüli, intracelluláris mozgás izom összehúzódás organellumok
A CITOSZKELETÁLIS RENDSZER 2011. 05. 03. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 9. A sejtmozgás mechanizmusai Sejtmozgás, motilitás 1. Sejten belüli, intracelluláris mozgás izom összehúzódás organellumok
A citoszkeletális rendszer, motorfehérjék.
 A citoszkeletális rendszer, motorfehérjék. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus C. Mikrofilamentum SCIENCE PHOTO LIBRARY
A citoszkeletális rendszer, motorfehérjék. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus C. Mikrofilamentum SCIENCE PHOTO LIBRARY
A citoszkeletális rendszer, motorfehérjék.
 A citoszkeletális rendszer, motorfehérjék. SCIENCE PHOTO LIBRARY Huber Tamás 2012. 10. 15. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus
A citoszkeletális rendszer, motorfehérjék. SCIENCE PHOTO LIBRARY Huber Tamás 2012. 10. 15. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus
Kollár Veronika
 A harántcsíkolt izom szerkezete, az izommőködés és szabályozás molekuláris alapjai Kollár Veronika 2010. 11. 11. Az izom citoszkeletális filamentumok és motorfehérjék rendezett összeszervezıdésébıl álló
A harántcsíkolt izom szerkezete, az izommőködés és szabályozás molekuláris alapjai Kollár Veronika 2010. 11. 11. Az izom citoszkeletális filamentumok és motorfehérjék rendezett összeszervezıdésébıl álló
A citoszkeletális rendszer, a harántcsíkolt izom biofizikája.
 A citoszkeletális rendszer, a harántcsíkolt izom biofizikája. SCIENCE PHOTO LIBRARY Kupi Tünde 2010. 10. 19. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fı filamentum-osztály: A.
A citoszkeletális rendszer, a harántcsíkolt izom biofizikája. SCIENCE PHOTO LIBRARY Kupi Tünde 2010. 10. 19. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fı filamentum-osztály: A.
A citoszkeletális rendszer
 A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
Citoszkeleton. Sejtek rugalmassága. Polimer mechanika: Hooke-rugalmasság. A citoszkeleton filamentumai. Fogászati anyagtan fizikai alapjai 12.
 Fogászati anyagtan fizikai alapjai 12. Sejtek rugalmassága Citoszkeleton Eukariota sejtek dinamikus vázrendszere Három fő filamentum-osztály: A. Vékony (aktin) B. Intermedier C. Mikrotubulus Polimerizáció:
Fogászati anyagtan fizikai alapjai 12. Sejtek rugalmassága Citoszkeleton Eukariota sejtek dinamikus vázrendszere Három fő filamentum-osztály: A. Vékony (aktin) B. Intermedier C. Mikrotubulus Polimerizáció:
Tudjunk Egymásról Bugyi Beáta 22/11/2012
 Listeria monocytogenes Loisel, Boujemaa et al. Nature 1999 Összetett aktin hálózatok Spire/formin szinergia Reymann et al. Nature Materials 1 ADF/aktin Bosch, Bugyi B et al. Molecular Cell 7 Reymann et
Listeria monocytogenes Loisel, Boujemaa et al. Nature 1999 Összetett aktin hálózatok Spire/formin szinergia Reymann et al. Nature Materials 1 ADF/aktin Bosch, Bugyi B et al. Molecular Cell 7 Reymann et
A citoszkeleton. A citoszkeleton, a motorfehérjék, az izom és működésének szabályozása. A citoszkeleton. A citoszkeleton.
 , a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2012. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
, a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2012. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
Speciális fluoreszcencia spektroszkópiai módszerek
 Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét. Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet
 Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
A motorfehérjék definíciója. A biológiai motorok 12/9/2016. Motorfehérjék. Molekuláris gépek. A biológiai mozgás
 A motorfehérjék definíciója Motorfehérjék Nyitrai Miklós, 2016 november 30. Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése;
A motorfehérjék definíciója Motorfehérjék Nyitrai Miklós, 2016 november 30. Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése;
A biológiai mozgások. A biológiai mozgás molekuláris mechanizmusai. Motorfehérjék. Motorfehérjék közös tulajdonságai
 A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen 1 Motorfehérjék
A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen 1 Motorfehérjék
A citoszkeleton. A citoszkeleton, a motorfehérjék, az izom és működésének szabályozása. A citoszkeleton. A citoszkeleton. Az aktin.
 , a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2011. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
, a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2011. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
Sejtciklus. Sejtciklus. Centriólum ciklus (centroszóma ciklus) A sejtosztódás mechanizmusa. Mikrotubulusok és motor fehérjék szerepe a mitózisban
 A sejtosztódás mechanizmusa Mikrotubulusok és motor fehérjék szerepe a mitózisban 2010.03.23. Az M fázis alatti események: mag osztódása (mitózis) mitotikus orsó: MT + MAP (pl. motorfehérjék) citoplazma
A sejtosztódás mechanizmusa Mikrotubulusok és motor fehérjék szerepe a mitózisban 2010.03.23. Az M fázis alatti események: mag osztódása (mitózis) mitotikus orsó: MT + MAP (pl. motorfehérjék) citoplazma
Nanomedicina Szimpózium, 2008. Nanomechanika: Egyedi Biomolekulák Manipulálása. Kellermayer Miklós
 Nanomedicina Szimpózium, 28 Nanomechanika: Egyedi Biomolekulák Manipulálása Kellermayer Miklós Semmelweis Egyetem Általános Orvostudományi Kar Biofizikai és Sugárbiológiai Intézet ÉLŐ SEJTBEN: BONYOLULT
Nanomedicina Szimpózium, 28 Nanomechanika: Egyedi Biomolekulák Manipulálása Kellermayer Miklós Semmelweis Egyetem Általános Orvostudományi Kar Biofizikai és Sugárbiológiai Intézet ÉLŐ SEJTBEN: BONYOLULT
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
A harántcsíkolt izom struktúrája általános felépítés
 harántcsíkolt izom struktúrája általános felépítés LC-2 Izom LC1/3 Izom fasciculus LMM S-2 S-1 HMM rod Miozin molekula S-1 LMM HMM S-2 S-1 Izomrost H Band Z Disc csík I csík M Z-Szarkomér-Z Miofibrillum
harántcsíkolt izom struktúrája általános felépítés LC-2 Izom LC1/3 Izom fasciculus LMM S-2 S-1 HMM rod Miozin molekula S-1 LMM HMM S-2 S-1 Izomrost H Band Z Disc csík I csík M Z-Szarkomér-Z Miofibrillum
1. AKTIN CITOSZKELETON
 A CITOSZKELETÁLIS REDSZER 20. 02. 08.. AKTI CITOSZKELETO Citozeletáli atin HEp-2 ejteben - rodamin-falloidin jelölé forrá: yitrai Miló, Grama Lázló, PTE ÁOK, Biofiziai Intézet CITOSZKELETO CITO : ejt /
A CITOSZKELETÁLIS REDSZER 20. 02. 08.. AKTI CITOSZKELETO Citozeletáli atin HEp-2 ejteben - rodamin-falloidin jelölé forrá: yitrai Miló, Grama Lázló, PTE ÁOK, Biofiziai Intézet CITOSZKELETO CITO : ejt /
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET)
 Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET) Gerjesztés A gerjesztett állapotú elektron lecsengési lehetőségei Fluoreszcencia 10-9 s k f Foszforeszcencia 10-3 s k ph 10-15 s Fizika-Biofizika 2. Huber
Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET) Gerjesztés A gerjesztett állapotú elektron lecsengési lehetőségei Fluoreszcencia 10-9 s k f Foszforeszcencia 10-3 s k ph 10-15 s Fizika-Biofizika 2. Huber
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék
 Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2011. február 22. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2011. február 22. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
A biológiai mozgás molekuláris mechanizmusai
 BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
Biofizika I
 ÁTTEKINTÉS AZ IZOM 9. A HARÁNTCSÍKOLT IZOM SZERKEZETE ÉS MECHANIKÁJA 10. AZ IZOMMŰKÖDÉS ÉS SZABÁLYOZÁS MOLEKULÁRIS ALAPJAI TÍPUSAI: SZERKEZET és FUNKCIÓ MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSAI MECHANIKAI
ÁTTEKINTÉS AZ IZOM 9. A HARÁNTCSÍKOLT IZOM SZERKEZETE ÉS MECHANIKÁJA 10. AZ IZOMMŰKÖDÉS ÉS SZABÁLYOZÁS MOLEKULÁRIS ALAPJAI TÍPUSAI: SZERKEZET és FUNKCIÓ MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSAI MECHANIKAI
PÉCSI TUDOMÁNYEGYETEM. Biológia Doktori Iskola Mikroorganizmusok életfolyamatainak molekuláris analízise
 PÉCSI TUDOMÁNYEGYETEM Biológia Doktori Iskola Mikroorganizmusok életfolyamatainak molekuláris analízise Forminok hatása az aktin filamentum konformációs és dinamikai tulajdonságaira PhD értekezés tézisei
PÉCSI TUDOMÁNYEGYETEM Biológia Doktori Iskola Mikroorganizmusok életfolyamatainak molekuláris analízise Forminok hatása az aktin filamentum konformációs és dinamikai tulajdonságaira PhD értekezés tézisei
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék
 Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2012. február 21. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2012. február 21. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET)
 Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Biofizika szeminárium PTE ÁOK Biofizikai Intézet Huber Tamás 2014. 02. 11-13. A gerjesztett állapotú elektron lecsengési lehetőségei Gerjesztés Fluoreszcencia
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Biofizika szeminárium PTE ÁOK Biofizikai Intézet Huber Tamás 2014. 02. 11-13. A gerjesztett állapotú elektron lecsengési lehetőségei Gerjesztés Fluoreszcencia
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Biofizika I 2013-2014 2014.12.03.
 Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet A KERESZTHÍD CIKLUSHOZ KAPCSOLÓDÓ ERŐKIEJTÉS egy kereszthíd ciklus során a miozin II fej elmozdulása: í ~10 nm 10 10 egy kereszthíd
Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet A KERESZTHÍD CIKLUSHOZ KAPCSOLÓDÓ ERŐKIEJTÉS egy kereszthíd ciklus során a miozin II fej elmozdulása: í ~10 nm 10 10 egy kereszthíd
Motorfehérjék november 30.; Nyitrai
 Motorfehérjék 2011. november 30.; Nyitrai Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése; Gépek a mikro/nano-világban
Motorfehérjék 2011. november 30.; Nyitrai Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése; Gépek a mikro/nano-világban
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek
 Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek 2012. 11. 08. Fotonok és molekulák ütközése Fény (foton) ütközése a molekulákkal fényszóródás abszorpció E=hν
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek 2012. 11. 08. Fotonok és molekulák ütközése Fény (foton) ütközése a molekulákkal fényszóródás abszorpció E=hν
Membrántranszport. Gyógyszerész előadás Dr. Barkó Szilvia
 Membrántranszport Gyógyszerész előadás 2017.04.10 Dr. Barkó Szilvia Sejt membránok A sejtmembrán funkciói Védelem Kommunikáció Molekulák importja és exportja Sejtmozgás Általános szerkezet Lipid kettősréteg
Membrántranszport Gyógyszerész előadás 2017.04.10 Dr. Barkó Szilvia Sejt membránok A sejtmembrán funkciói Védelem Kommunikáció Molekulák importja és exportja Sejtmozgás Általános szerkezet Lipid kettősréteg
 2013. 09. 02. www.biofizika.aok.pte.hu Biofizika I. Kötelező tantárgy Tantárgyfelelős: Dr. Nyitrai Miklós Heti 2 óra előadás, 2 óra gyakorlat Félévközi számonkérés: Egy írásbeli dolgozat Félév végi vizsga:kollokvium
2013. 09. 02. www.biofizika.aok.pte.hu Biofizika I. Kötelező tantárgy Tantárgyfelelős: Dr. Nyitrai Miklós Heti 2 óra előadás, 2 óra gyakorlat Félévközi számonkérés: Egy írásbeli dolgozat Félév végi vizsga:kollokvium
a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál. Nyugalmi potenciál. 3 tényező határozza meg:
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
Citoszkeleton Sejtmozgás
 Citoszkeleton Sejtmozgás Citoszkeleton funkciói Sejtalak meghatározása Organellumok kihorgonyzása Organellumok mozgatása Húzószilárdság Kromoszóma mozgatás Sejtpolaritás Motilitás Citoszkeleton Mikrofilamentumok
Citoszkeleton Sejtmozgás Citoszkeleton funkciói Sejtalak meghatározása Organellumok kihorgonyzása Organellumok mozgatása Húzószilárdság Kromoszóma mozgatás Sejtpolaritás Motilitás Citoszkeleton Mikrofilamentumok
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Egy idegsejt működése. a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav,
 MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
A biológiai mozgások. Motorfehérjék. Motorfehérjék közös tulajdonságai 4/22/2015. A biológiai mozgás molekuláris mechanizmusai. Szerkezeti homológia
 A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai. Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen Motorfehérjék
A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai. Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen Motorfehérjék
Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai
 Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Jellemzői: általában akaratunktól függően működik, gyors, nagy erőkifejtésre képes, fáradékony.
 Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma összehúzódásáért
Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma összehúzódásáért
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Transzporterek vizsgálata lipidmembránokban Sarkadi Balázs MTA-SE Molekuláris Biofizikai Kutatócsoport, MTA-TTK Budapest
 Transzporterek vizsgálata lipidmembránokban 2016. Sarkadi Balázs MTA-SE Molekuláris Biofizikai Kutatócsoport, MTA-TTK Budapest Membrántranszport fehérjék típusok, lipid-kapcsolatok A membránok szerkezete
Transzporterek vizsgálata lipidmembránokban 2016. Sarkadi Balázs MTA-SE Molekuláris Biofizikai Kutatócsoport, MTA-TTK Budapest Membrántranszport fehérjék típusok, lipid-kapcsolatok A membránok szerkezete
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Izomműködés. Az izommozgás. az állati élet legszembetűnőbb külső jele a mozgás amőboid, ostoros ill. csillós és izomösszehúzódással
 Izomműködés Az izommozgás az állati élet legszembetűnőbb külső jele a mozgás amőboid, ostoros ill. csillós és izomösszehúzódással történő mozgás van Galenus id. II.szd. - az idegekből animal spirit folyik
Izomműködés Az izommozgás az állati élet legszembetűnőbb külső jele a mozgás amőboid, ostoros ill. csillós és izomösszehúzódással történő mozgás van Galenus id. II.szd. - az idegekből animal spirit folyik
2011. október 11. Szabad János
 2011. október 11 Szabad János szabad@mdbio.szote.u-szeged.hu Egy állatsejt szervez dése - Export a sejtmagból a citoplazmába - Import a citoplazmából a sejtmagba - Import a sejtszervecskékbe - A szekréciós
2011. október 11 Szabad János szabad@mdbio.szote.u-szeged.hu Egy állatsejt szervez dése - Export a sejtmagból a citoplazmába - Import a citoplazmából a sejtmagba - Import a sejtszervecskékbe - A szekréciós
Ph.D. értekezés. AZ IRSp53 FEHÉRJE SZEREPE A FILOPÓDIUM FORMÁLÁS FOLYAMATÁBAN
 Ph.D. értekezés AZ IRSp53 FEHÉRJE SZEREPE A FILOPÓDIUM FORMÁLÁS FOLYAMATÁBAN FUTÓ KINGA Pécsi Tudományegyetem, Általános Orvostudományi Kar, Biofizikai Intézet 2014 10 Program: Doktori Program vezetője:
Ph.D. értekezés AZ IRSp53 FEHÉRJE SZEREPE A FILOPÓDIUM FORMÁLÁS FOLYAMATÁBAN FUTÓ KINGA Pécsi Tudományegyetem, Általános Orvostudományi Kar, Biofizikai Intézet 2014 10 Program: Doktori Program vezetője:
K68464 OTKA pályázat szakmai zárójelentés
 K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM. Jelutak. 1. a sejtkommunikáció alapjai
 Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Történeti áttekintés. Eukarióta. Prokarióta. A citoszkeletális rendszer. Motorfehérjék. A biológiai mozgás molekuláris mechanizmusai.
 A citoszkeletális rendszer. Motorfehérjék. A biológiai mozgás molekuláris mechanizmusai. Előadásvázlat TK. 345-353. oldal citoszkeleton története polimer mechanika vizsgálómódszerek polimerizáció aktin
A citoszkeletális rendszer. Motorfehérjék. A biológiai mozgás molekuláris mechanizmusai. Előadásvázlat TK. 345-353. oldal citoszkeleton története polimer mechanika vizsgálómódszerek polimerizáció aktin
Biofizika I. DIFFÚZIÓ OZMÓZIS
 1. KÍSÉRLET 1. kísérlet: cseppentsünk tintát egy üveg vízbe Biofizika I. OZMÓZIS 2012. szeptember 5. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet 1. megfigyelés: a folt lassan szétterjed és megfesti az egész
1. KÍSÉRLET 1. kísérlet: cseppentsünk tintát egy üveg vízbe Biofizika I. OZMÓZIS 2012. szeptember 5. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet 1. megfigyelés: a folt lassan szétterjed és megfesti az egész
ÖSSZ-TARTALOM. 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3.
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
Izomszövet eredetű aktin izoformák termodinamikai és spektroszkópiai vizsgálata
 Izomszövet eredetű aktin izoformák termodinamikai és spektroszkópiai vizsgálata PhD értekezés Készítette: Orbán József Témavezetők: DR. LŐRINCZY DÉNES DR. HILD GÁBOR Doktori Iskola: Doktori Iskola vezető:
Izomszövet eredetű aktin izoformák termodinamikai és spektroszkópiai vizsgálata PhD értekezés Készítette: Orbán József Témavezetők: DR. LŐRINCZY DÉNES DR. HILD GÁBOR Doktori Iskola: Doktori Iskola vezető:
Lumineszcencia spektrometria összefoglaló
 Lumineszcencia spektrometria összefoglaló Ismétlés: fény (elektromágneses sugárzás) elnyelés: abszorpció elektron gerjesztés: excitáció alap és gerjesztett állapot atomi energiaszintek, energiaszintek
Lumineszcencia spektrometria összefoglaló Ismétlés: fény (elektromágneses sugárzás) elnyelés: abszorpció elektron gerjesztés: excitáció alap és gerjesztett állapot atomi energiaszintek, energiaszintek
A DAAM formin hatása az aktin dinamikájára
 PhD értekezés A DAAM formin hatása az aktin dinamikájára Barkó Szilvia Témavezető: Dr. Nyitrai Miklós Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet Pécs 2012 Interdiszciplináris
PhD értekezés A DAAM formin hatása az aktin dinamikájára Barkó Szilvia Témavezető: Dr. Nyitrai Miklós Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet Pécs 2012 Interdiszciplináris
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
A centriólum és a sejtek mozgási organellumai
 A centriólum A centriólum és a sejtek mozgási organellumai Egysejtű eukarióta sejtekben,soksejtű állatok sejtjeiben 9x3-triplet A,B és C tubulus alegységek hengerpalástszerű helyezkedéssel Hossza 0,3mm
A centriólum A centriólum és a sejtek mozgási organellumai Egysejtű eukarióta sejtekben,soksejtű állatok sejtjeiben 9x3-triplet A,B és C tubulus alegységek hengerpalástszerű helyezkedéssel Hossza 0,3mm
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
-Két fő korlát: - asztrogliák rendkívüli morfológiája -Ca szignálok értelmezési nehézségei
 Nature reviewes 2015 - ellentmondás: az asztrociták relatív lassú és térben elkent Ca 2+ hullámokkal kommunikálnak a gyors és pontos neuronális körökkel - minőségi ugrás kell a kísérleti és analitikai
Nature reviewes 2015 - ellentmondás: az asztrociták relatív lassú és térben elkent Ca 2+ hullámokkal kommunikálnak a gyors és pontos neuronális körökkel - minőségi ugrás kell a kísérleti és analitikai
Az izomszövet biokémiája. Izombetegségek. Szerkesztette: Fekete Veronika
 Az izomszövet biokémiája. Izombetegségek Szerkesztette: Fekete Veronika Az izomtípusok jellemzői Simaizom lassú nincs rajzolat Szívizom gyors harántcsíkolt Harántcsíkolt izom belső szervek akaratlan nem
Az izomszövet biokémiája. Izombetegségek Szerkesztette: Fekete Veronika Az izomtípusok jellemzői Simaizom lassú nincs rajzolat Szívizom gyors harántcsíkolt Harántcsíkolt izom belső szervek akaratlan nem
Biokatalitikus Baeyer-Villiger oxidációk Doktori (PhD) értekezés tézisei. Muskotál Adél. Dr. Vonderviszt Ferenc
 Biokatalitikus Baeyer-Villiger oxidációk Doktori (PhD) értekezés tézisei Készítette: Muskotál Adél Környezettudományok Doktori Iskola Témavezető: Dr. Vonderviszt Ferenc egyetemi tanár Pannon Egyetem Műszaki
Biokatalitikus Baeyer-Villiger oxidációk Doktori (PhD) értekezés tézisei Készítette: Muskotál Adél Környezettudományok Doktori Iskola Témavezető: Dr. Vonderviszt Ferenc egyetemi tanár Pannon Egyetem Műszaki
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015
 Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
A DAAM formin alcsalád szerepe az izomfejlődésben. A Ph.D. értekezés tézisei. Molnár Imre. Témavezető: Dr. Mihály József
 A DAAM formin alcsalád szerepe az izomfejlődésben A Ph.D. értekezés tézisei Molnár Imre Témavezető: Dr. Mihály József SZTE Biológia Doktori Iskola Magyar Tudományos Akadémia, Szegedi Biológiai Kutatóközpont,
A DAAM formin alcsalád szerepe az izomfejlődésben A Ph.D. értekezés tézisei Molnár Imre Témavezető: Dr. Mihály József SZTE Biológia Doktori Iskola Magyar Tudományos Akadémia, Szegedi Biológiai Kutatóközpont,
Speciális fluoreszcencia spektroszkópiai alkalmazások. Emlékeztető: az abszorpció definíciója. OD = A = - log (I / I 0 ) = ε (λ) c x
 Speciális fluoreszcencia spektroszkópiai alkalmazások Nyitrai Miklós; 2011 február 21. FRET Emlékeztető: az abszorpció definíciója I 0 I anyag OD = A = - log (I / I 0 ) = ε (λ) c x Röv: optical density
Speciális fluoreszcencia spektroszkópiai alkalmazások Nyitrai Miklós; 2011 február 21. FRET Emlékeztető: az abszorpció definíciója I 0 I anyag OD = A = - log (I / I 0 ) = ε (λ) c x Röv: optical density
Biológiai membránok és membrántranszport
 Biológiai membránok és membrántranszport Biológiai membránok A citoplazma membrán funkciói: térrészek elválasztása (egész sejt, organellumok) transzport jelátvitel Milyen a membrán szerkezete? lipidek
Biológiai membránok és membrántranszport Biológiai membránok A citoplazma membrán funkciói: térrészek elválasztása (egész sejt, organellumok) transzport jelátvitel Milyen a membrán szerkezete? lipidek
A Földön előforduló sejtek (pro- és eukarioták) közös és eltérő tulajdonságai. A sejtes szerveződés evolúciója.
 A tárgy neve: Sejtbiológia előadás 1. Jellege: Törzs Gazda tanszék: Állattani és Sejtbiológiai Tanszék Felelős oktató: Dr. Gulya Károly Kredit: 2 Heti óraszám: 2 Típus: előadás Számonkérés: K A Földön
A tárgy neve: Sejtbiológia előadás 1. Jellege: Törzs Gazda tanszék: Állattani és Sejtbiológiai Tanszék Felelős oktató: Dr. Gulya Károly Kredit: 2 Heti óraszám: 2 Típus: előadás Számonkérés: K A Földön
A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban
 BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
Sejtváz Sejtek mozgása
 Sejtváz Sejtek mozgása Sejtváz: Az eukarióta sejtekben vékony fonálszerű struktúra 3 fő alrendszer alkotja: Mikrofilamentumok: 7-9 nm átmérőjű aktinfonalakból áll; Intermedier filamentumok: 10 nm átmérőjűek;
Sejtváz Sejtek mozgása Sejtváz: Az eukarióta sejtekben vékony fonálszerű struktúra 3 fő alrendszer alkotja: Mikrofilamentumok: 7-9 nm átmérőjű aktinfonalakból áll; Intermedier filamentumok: 10 nm átmérőjűek;
A membránok és a citoszkeleton kapcsolata. A sejtosztódás és a sejtciklus. Előadó:Gönczi Mónika Debreceni Egyetem, ÁOK, Élettani Intézet
 2018 A membránok és a citoszkeleton kapcsolata. A sejtosztódás és a sejtciklus Előadó:Gönczi Mónika Debreceni Egyetem, ÁOK, Élettani Intézet A citoszkeleton alkotói Mikrofilamentumok Intermedier filamentumok
2018 A membránok és a citoszkeleton kapcsolata. A sejtosztódás és a sejtciklus Előadó:Gönczi Mónika Debreceni Egyetem, ÁOK, Élettani Intézet A citoszkeleton alkotói Mikrofilamentumok Intermedier filamentumok
tulajdonságaira és dinamikai jellemzőire
 PhD ÉRTEKEZÉS A for minok hatása az aktin filamentumok polimerizációs tulajdonságaira és dinamikai jellemzőire BUGYI BEÁTA Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet 2006. Program:
PhD ÉRTEKEZÉS A for minok hatása az aktin filamentumok polimerizációs tulajdonságaira és dinamikai jellemzőire BUGYI BEÁTA Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet 2006. Program:
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
A sejtváz. Mikrotubulusok (25 nm átmérő) Mikrofilamentumok (7 nm átmérő) Intermedier filamentumok (8-12 nm átmérő)
 A sejtváz A citoszkeleton, vagy sejtváz kötegek hálózatából felépülő struktúra, mely a sejt szilárdításán, alakjának biztosításán túl, a mozgásban, a szállításban is szerepet játszik. Három molekuláris
A sejtváz A citoszkeleton, vagy sejtváz kötegek hálózatából felépülő struktúra, mely a sejt szilárdításán, alakjának biztosításán túl, a mozgásban, a szállításban is szerepet játszik. Három molekuláris
A Caskin1 állványfehérje vizsgálata
 A Caskin1 állványfehérje vizsgálata Doktori tézisek Balázs Annamária Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezeto: Dr. Buday László egyetemi tanár, az orvostudományok doktora
A Caskin1 állványfehérje vizsgálata Doktori tézisek Balázs Annamária Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezeto: Dr. Buday László egyetemi tanár, az orvostudományok doktora
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól
 Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
AZ AKTIN AKTIVÁCIÓ ÚJ MECHANIZMUSA: Gyimesi Máté
 AZ AKTIN AKTIVÁCIÓ ÚJ MECHANIZMUSA: AZ AKTIN KÖZVETLENÜL AZ ERŐGENERÁLÓ LÉPÉST GYORSÍTJA MIOZIN II-BEN Gyimesi Máté Témavezető: Dr. Málnási-Csizmadia András Biológia Doktori Iskola, iskolavezető: Prof.
AZ AKTIN AKTIVÁCIÓ ÚJ MECHANIZMUSA: AZ AKTIN KÖZVETLENÜL AZ ERŐGENERÁLÓ LÉPÉST GYORSÍTJA MIOZIN II-BEN Gyimesi Máté Témavezető: Dr. Málnási-Csizmadia András Biológia Doktori Iskola, iskolavezető: Prof.
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Folyadékkristályok; biológiai és mesterséges membránok
 Folyadékkristályok; biológiai és mesterséges membránok Dr. Voszka István Folyadékkristályok: Átmenet a folyadékok és a kristályos szilárdtestek között (anizotróp folyadékok) Fonal, pálcika, korong alakú
Folyadékkristályok; biológiai és mesterséges membránok Dr. Voszka István Folyadékkristályok: Átmenet a folyadékok és a kristályos szilárdtestek között (anizotróp folyadékok) Fonal, pálcika, korong alakú
A plazma membrán mikrodomének szabályzó szerepe a sejtek növekedési és stressz érzékelési folyamataiban. Csoboz Bálint
 A PhD értekezés összefoglalása A plazma membrán mikrodomének szabályzó szerepe a sejtek növekedési és stressz érzékelési folyamataiban Csoboz Bálint Témavezető: Prof. László Vígh Biológia Doktori Iskola
A PhD értekezés összefoglalása A plazma membrán mikrodomének szabályzó szerepe a sejtek növekedési és stressz érzékelési folyamataiban Csoboz Bálint Témavezető: Prof. László Vígh Biológia Doktori Iskola
Foszforilációs és defoszforilációs szabályozási folyamatok vizsgálata konvencionális miozin II és nem-konvencionális miozin XVI motorfehérjék esetén
 PhD értekezés tézisei Foszforilációs és defoszforilációs szabályozási folyamatok vizsgálata konvencionális miozin II és nem-konvencionális miozin XVI motorfehérjék esetén Dr. Kengyel András Miklós Doktori
PhD értekezés tézisei Foszforilációs és defoszforilációs szabályozási folyamatok vizsgálata konvencionális miozin II és nem-konvencionális miozin XVI motorfehérjék esetén Dr. Kengyel András Miklós Doktori
KÉRDŐÍV PÁLYÁZATOK ELBÍRÁLÁSÁNAK SZEMPONTJAIHOZ
 KÉRDŐÍV PÁLYÁZATOK ELBÍRÁLÁSÁNAK SZEMPONTJAIHOZ A megpályázott munkakör: A megpályázott beosztás: EGYETEMI DOCENS IGAZGATÓ A PÁLYÁZÓ NEVE: Dr. Kellermayer Miklós Sándor Zoltán Születési éve: 1964 A megpályázott
KÉRDŐÍV PÁLYÁZATOK ELBÍRÁLÁSÁNAK SZEMPONTJAIHOZ A megpályázott munkakör: A megpályázott beosztás: EGYETEMI DOCENS IGAZGATÓ A PÁLYÁZÓ NEVE: Dr. Kellermayer Miklós Sándor Zoltán Születési éve: 1964 A megpályázott
Biofizika szeminárium. Diffúzió, ozmózis
 Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYEK KÁLIUM TÁPLÁLKOZÁSÁNAK GENETIKAI ALAPJAI előadás áttekintése A kálium szerepe a növényi szervek felépítésében
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYEK KÁLIUM TÁPLÁLKOZÁSÁNAK GENETIKAI ALAPJAI előadás áttekintése A kálium szerepe a növényi szervek felépítésében
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
