A négymilliárd éves nanotechnológia
|
|
|
- Lóránd Veres
- 6 évvel ezelőtt
- Látták:
Átírás
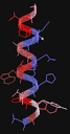
1 A négymilliárd éves nanotechnológia Tisztelt Hölgyeim és Uraim! Ha az önök kezében lenne egy öklömnyi szén, az enyémben pedig egy ugyanakkora gyémánt, cserélnének e velem? Kérdezhetném miért, hiszen mindkettő egyformán csupán szénatomokból áll. Csak annyi a különbség, hogy az egyikben egy kicsit másképpen vannak elrendezve az atomok, mint a másikban. Hasonlóképpen, egy kávéskanálnyi homok és a legmodernebb Pentium chip atomi összetételét tekintve is parányiak a különbségek. Vagy ha egy kevéske föld, víz és levegő atomjait kissé átcsoportosítjuk, akár egy fürt szőlőt is kaphatunk. Mindezek a példák nyilvánvalóan mutatják, hogy ugyanazokat az atomokat ügyesen elrendezve értékes és hasznos dolgokat állíthatunk elő, másféle elrendezésben pedig értéktelen és számunkra haszontalan dolgokhoz jutunk. Rendkívül fontos tehát, hogy képesek legyünk az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének befolyásolására. Ezt a képességet nevezzük technológiának. Általános értelemben a 100 nm alatti mérettartományban működő technológiákat hívjuk nanotechnológiának. A nanométeres mérettartomány a molekulák birodalma. A nanométeres méretskála megfelel a hajszál vastagsága százezred részének, de ezerszer kisebb még a baktériumok méreténél is. Nemcsak a parányi méretek jelentik az újdonságot a nanotechnológiában, hanem a gyökeresen új megközelítési mód is: a nanotechnológia egyik kiemelt célja, hogy kontrollált módon, atomokból építkezve hozzon létre molekuláris gépezeteket, amelyek rendelkeznek az önszerveződés képességével, azaz olyan gépezeteket, amelyek alkatrészeikből spontán módon, mindenféle külső beavatkozás nélkül összeállnak. Manapság gyakran halljuk, hogy a nanotechnológia a jövő ígérete, a XXI. század technológiája. Pedig a nanotechnológia nem új dolog, ősidők óta létezik, hiszen az élő szervezetek valójában nanotechnológiát alkalmaznak, bennük elsősorban fehérjékből felépülő, önszerveződésre képes molekuláris gépezetek működnek. Ebben az előadásban szeretném önöket egy kis kalandozásra hívni a fehérjék világába, bemutatva a biológiai rendszerekben található fehérje-alapú molekuláris gépezetek ámulatba ejtő tulajdonságait. Próbáljuk meg együtt megérteni, hogy mi teszi a fehérjéket különösen alkalmassá molekuláris gépezetek építésére, s hogyan alkalmazhatjuk a fehérjéket a mi saját nanotechnológiánk létrehozásában. 1
2 MIK AZOK A FEHÉRJÉK? A fehérjék az élet molekulái, az élő szervezetek legfontosabb anyagai. A nukleinsavak mellett talán a legbonyolultabb molekulák, amiket ismerünk. Első pillantásra egy fehérje több ezer, vagy akár több tízezer elsősorban C, H, O, N és S atom rendezett halmaza (ábra). A fehérjék valójában láncmolekulák (lineáris polimerek), amelyek 20-féle aminosav összekapcsolódásával jönnek létre. Minden aminosav azonos vázból és egy ahhoz csatlakozó egyedi oldalláncból épül fel (ábra). Az aminosavak azonos részeiken keresztül peptidkötéssel egymáshoz kapcsolódva alkotják a fehérjék polipeptidláncait, amelyek általában több száz aminosavból állnak. A polipeptidláncok váza periodikus szerkezet, amelyet a kapcsolódó oldalláncok tesznek változatossá. Mitől különlegesek a fehérjék? Noha az ember is képes lineáris polimereket szintetizálni, több lényegi különbség van a fehérjék és a mesterséges polimerek között: A mesterséges polimerláncok változó hosszával szemben az egyes fehérjék aminosavsorrendje, s ezáltal mérete és tömege szigorúan meghatározott. Míg a mesterséges polimereknek oldatban nem rendelkeznek határozott térszerkezettel, s nagyszámú konformáció között véletlenszerűen csaponganak, addig a fehérjék polipeptidlánca képes felvenni egy jól definiált kompakt térszerkezetet (ábra). (Ezen a dián láthatjuk, hogy miként tekeredik fel a hemoglobin fehérje polipetidlánca, s a hozzá kapcsolódó oldalláncokkal együtt miként eredményez egy tömör, kompakt térszerkezetet.) Valójában a térszerkezetre vonatkozó minden információ adott környezeti körülmények között az aminosavszekvenciában rejlik, azaz általában egy fehérje polipeptidlánca minden külső segítség nélkül képes kialakítani jól definiált térbeli szerkezetét. A fehérjék feltekeredettsége, kompakt térszerkezete teszi lehetővé, hogy változatos funkciókat lássanak el. FEHÉRJESZERKEZET MEGHATÁROZÁS Vajon hogyan határozható meg egy fehérjemolekula atomi precizitású szerkezete? A fehérjék bonyolult óriásmolekulák, ezért is csábító kihívás térszerkezetük meghatározása. Pontosabban ilyen volt egykoron, mára szinte rutinfeladattá vált. Manapság több mint húszezer fehérje szerkezetét ismerjük atomi precizitással, de ezek között sok rokon fehérje is található, amelyek különböző élőlényekben látnak el azonos funkciót. Összehasonlításképpen talán elég arra gondolnunk, hogy egy emberi sejtben kb. ötvenezer különféle fehérje működik. 2
3 Az összes felderített szerkezet a brookhaven-i fehérje adatbankban megtalálható. Az interneten keresztül ( bárki kedvére gyönyörködhet bennük. Az első fehérjék térszerkezetét az 1960-as években határozták meg. Kendrew és Perutz röntgendiffrakciós vizsgálatai 7 évnyi erőfeszítés eredményeként vezettek el a hemoglobin atomi szerkezetének leírásához. Egyetlen fehérjemolekula csak parányi mértékben téríti el a röntgensugarakat. Ahhoz, hogy mérhető röntgenszórást tapasztaljunk, sok ezer milliárdnyi fehérjemolekulából rendezett mintát kell előállítanunk. Általában ez azt jelenti, hogy a fehérjét kristályosítani kell. A fehérjék kristályosítása egyáltalán nem triviális feladat, hiszen miért is kellene a bonyolult alakú fehérjemolekuláknak képesnek lenniük a kristályképződésre. A tapasztalat mégis azt mutatja, hogy megfelelő körülmények között a legtöbb fehérje kristályosítható. A megfelelő körülmények megtalálása azonban esetenként akár több évnyi erőfeszítést is igényelhet. Sokan a fehérjekristályosítást egyfajta művészetnek tekintik, ami azért is találó megfogalmazás, mert az előállított kristályok szépsége olykor akár egy-egy műalkotáséval is vetekedhet (ábra). Korábban egy röntgendiffrakciós szerkezetanalízishez a milliméteres mérettartományt megközelítő kristályok előállítására volt szükség, amit aztán akár több hónapnyi adatgyűjtés majd szerkezetszámítás és finomítás követett. Ma már a sok nagyságrenddel intenzívebb szinkrotronos sugárforrásokat használva mikrométeres kristályok is vizsgálhatók, s kedvező esetben néhány nanoszekundumnyi idő alatt elegendő adat regisztrálható. Egy fehérjekristályról készült röntgenszórási kép valójában szabályosan elhelyezkedő sötétebb és világosabb foltok összessége (ábra), ahol a foltok intenzitása hordozza a fehérjeszerkezetre (pontosabban elektronsűrűségre) vonatkozó információt. Felmerülhet a kérdés, hogy egy kristályba rendeződött fehérjemolekula szerkezete vajon ugyanolyan-e, mint oldott állapotban. Számos megfigyelés utal arra, hogy igen. Egy tipikus fehérjekristály térfogatának ugyanis közel 70%-a víz. A fehérje molekulák között viszonylag kicsik a kontaktusok, az intermolekuláris térben tágas vízzel telt csatornák találhatók. A legtöbb enzimfehérje kristályos állapotban is működésre kész: a szubsztrát molekulák a vízzel telt csatornákon keresztül képesek a kristály belsejében lévő fehérjékhez diffundálni, majd azokhoz kötődve lejátszódik a fehérje által katalizált folyamat. A fehérjék térszerkezete nem csak röntgendiffrakciós kísérletek révén határozható meg, Az NMR spektroszkópiás szerkezetvizsgálat szerencsésen kiegészíti a röntgendiffrakciós analízist, mert nem igényel rendezett mintát, s természetes, vizes környezetükben képes tanulmányozni a fehérjéket. Hátránya viszont, hogy ezzel a módszerrel nagyobb méretű - jelenleg 300 aminosavnál hosszabb - fehérjék nem tanulmányozhatók. Az NMR spektroszkópiás módszerrel meghatározott szerkezetek gyakorlatilag megegyeznek a röntgendiffrakciós analízis eredményével, bizonyítva azt, hogy kristályos állapotban a fehérjék nem szenvednek el számottevő torzulást. A röntgendiffrakciós módszer alapvetően vizes közegben működőképes fehérjék szerkezetének meghatározására alkalmas. Ugyanakkor a membránfehérjék a sejtek életének számos létfontosságú folyamatában vesznek részt (pl. fotoszintézis, jelátvitel, 3
4 anyagtranszport). A membránfehérjéket természetes lipidkörnyezetükből kiszakítva elvesztik natív (feltekeredett, működőképes) térszerkezetüket, általában nem kristályosíthatók, vizes közegben nem tanulmányozhatók. Jelenleg az ismert fehérjeszerkezetek kevesebb, mint 1%-át teszik ki a membránfehérjék. Bár akadt már példa a lipidkörnyezetet szimuláló detergensek jelenlétében a membránfehérjék kristályosítására és röntgendiffrakciós szerkezetvizsgálatára, a membránfehérjéket egyszerűbbnek tűnik a membránon belül rendezni, ún. kétdimenziós kristályokat létrehozva belőlük. Az ilyen rendezett vékonyrétegek szerkezetvizsgálatára kínál megoldást az elektronmikroszkópia, amelynek segítségével szerencsés esetben ugyancsak atomi precizitású szerkezeti adatokat nyerhetünk. Az alacsonyhőmérsékletű EM segítségével a nem kristályosítható, nagy méretű szupramolekuláris komplexumok szerkezetének meghatározására is van esély. Ilyenkor az egyedi komplexumokról készített sokszor több ezernyi EM felvételt megfelelő orientációban számítógép segítségével egymásra helyezve (szuperponálva) a zajt kiátlagolhatjuk és eljuthatunk akár az atomi precizitású szerkezethez is. Ezzel az eljárással határoztuk meg nemrégiben a baktériumok flagelláris filamentumainak szerkezetét (ábra). A kiindulási EM felvételeken alig sejlik a filamentumok képe, de néhány száz felvétel kiátlagolása és analízise után megjelennek már az apró szerkezeti részletek is. A FEHÉRJÉK DINAMIKÁJA Az eddigiekben bemutatott fehérjeszerkezetek azt a képzetet kelthetik, mintha a fehérjék statikus objektumok lennének, az őket felépítő atomok szigorúan meghatározott pozíciókban helyezkednének el. Pedig ez egyáltalán nincsen így, a fehérjék örökös mozgásban, nyüzsgésben vannak, egyes részeik különböző időtartományokban lejátszódó mozgásokban vesznek részt (animáció). Ezek a mozgások rendkívül széles időskálát ölelnek fel, a pikoszekundumos (10-12 s) tartománytól akár az éves (10 6 s) időtartamokig, s az atomi rezgésektől és az oldalláncok gyors rotációs mozgásától, a működés során gyakran megfigyelhető relatív doménmozgásokon keresztül, a neurodegeneratív betegségek (prionbetegségek) hátterében álló lassú konformációs átrendeződésekig terjednek. A fizika törvényei szerint a molekuláris mozgások valójában elkerülhetetlenek. A fehérjékben egy hosszú evolúciós folyamat eredményeként ezek a konformációs fluktuációk irányítottan mennek végbe, s amint arra az előadás későbbi részében több példát is láthatunk majd, a fehérje egyes részeinek összehangolt, irányított mozgásai gyakran meghatározó szerepet játszanak a fehérjék működésében. A fehérjék szerkezetét fenntartó erők ismeretében a rendelkezésre álló atomi szerkezet alapján a molekuláris mozgások akár számítógéppel is szimulálhatók. Sajnos ezek a szimulációk az atomok (szabadsági fokok) rendkívül nagy száma miatt még a leggyorsabb 4
5 szuperszámítógépekkel is csak néhányszor 10 ns-os időtartamra végezhetők el. A kapott eredmények alapján sokszor lehetetlen következtetni pl. az enzimműködés szempontjából meghatározó milliszekundumos időskálán lejátszódó folyamatokra. Meglepő módon ezen dinamikus folyamatok tanulmányozásában éppen a röntgendiffrakciós szerkezetvizsgálat siet segítségünkre. Amint azt már említettük, a rendkívül intenzív szinkrotronos sugárforrásoknál az adatgyűjtés ma már akár néhány nanoszekundum alatt elvégezhető. Ahhoz, hogy egy kristályban lévő nagyszámú fehérjemolekula funkcionálisan releváns mozgásai ne átlagolják ki egymást, ezeket a mozgásokat valahogyan szinkronizálni kell. Egy kristályban elhelyezkedő enzim általában megőrzi katalitikus képességét, a kristályt átszövő vízzel telt csatornákon keresztül a bediffundáló szubsztrát molekulákat képes megkötni, majd átalakítani. Esetenként előállíthatók olyan un. fotoaktiválható szubsztrátanalógok, amelyek szerkezetükben hasonlítanak a természetes szubsztrátra, ezért az enzim képes megkötni őket, de a szerkezeti eltérések miatt mégsem játszódik le a katalitikus folyamat. A felesleges oldalcsoportot (vagy kémiai kötést) egy gyors és erős lézerimpulzussal lehasítva az összes enzimmolekula esetén egyszerre indíthatjuk el a katalitikus reakciót. A reakció elindítása után meghatározott időtartamonként (pl. milliszekundumonként) röntgen pillanatfelvételeket készítve jellemezhetjük a katalízis szempontjából meghatározó intramolekuláris mozgásokat. MIKÉNT TALÁLJA MEG EGY FEHÉRJE A NATÍV SZERKEZETÉT? A fehérjék egyik különleges sajátossága az, hogy jól definiált térszerkezetet (natív szerkezet) képesek felvenni. Az előzőekben áttekintettük, hogy miként vizsgálható és jellemezhető a fehérjék szerkezete. Próbáljuk most megérteni, hogyan jön létre ez a szerkezet, miként tekeredik fel egy fehérje polipeptidlánca. Egy egyszerű számítással beláthatjuk, hogy ez szinte lehetetlen feladat (Levinthal paradoxon). Tekintsünk egy átlagos méretű, 300 aminosavból álló fehérje polipeptidláncát. A polipeptidlánc periodikus szerkezet, amelyik aminosav egységenként két egyes kötést tartalmaz, amik körül a lánc szabadon elfordulhat (ábra). Valójában ez a forgás mégsem teljesen szabad, hiszen az aminosav oldalláncok nem ütközhetnek egymással ill. a főlánc atomjaival. Tételezzük fel, hogy a térbeli átfedések miatt ezek a változtatható kötésszögek átlagosan csak két értéket vehetnek fel (ezzel erősen alulbecsültük a lehetőségeket). Így minden egyes aminosav csupán a főlánc konformációkat tekintve 4-féle konformációt vehet fel, a teljes polipeptidlánc konformációinak száma pedig: N = = db Ha ehhez még hozzávesszük, hogy az aminosav oldalláncok is - sokszor több kötés körül is - szabad forgást végezhetnek, érzékelhetjük, hogy egy fehérje lehetséges konformációinak száma óriási. Számos kísérlet utal arra, hogy egy fehérje natív konformációja az energetikailag legkedvezőbb az abszolút szabadenergia minimumnak megfelelő - szerkezet. Elég talán arra utalnunk, hogy egy fehérje térszerkezetét sokféleképpen elronthatjuk (denaturálhatjuk), pl. 5
6 melegítéssel, a ph megváltoztatásával vagy akár a víz szerkezetét megváltoztató vegyszerekkel, mégis ha egy ilyen kitekeredett fehérjét ismét megfelelő környezeti körülmények közé helyezünk, az általában képes újra feltekeredni, s megtalálja működőképes (natív) szerkezetét. Egy átlagos méretű fehérje térszerkezetének kialakulása általában néhány másodpercet vesz igénybe. A legkedvezőbb kötési energiájú szerkezet megtalálására általános esetben nincsen más megbízható módszer, mint az összes lehetséges konformáció kipróbálása. Analógiaként gondoljunk csak arra, hogy ha a Földfelszín legmélyebb (= legalacsonyabb helyzeti energiájú) pontját kellene megkeresnünk, akkor ezt teljes biztonsággal csak úgy tehetjük meg, ha a Föld teljes felszínét bejárjuk, s mindenütt méréseket végzünk. A fehérjék esetében is egy sokdimenziós konformációs energiafelület legmélyebb pontját kell megtalálnunk. Minden lehetséges konformációhoz kiszámítható a neki megfelelő kötési energia, ezek közül kell egy feltekeredő fehérjének megtalálnia a legkedvezőbbet. Feltételezve, hogy egyetlen konformáció kipróbálása egy pikoszekundumot (10-12 s) vesz igénybe, lehetséges konformáció kipróbálásához másodpercre lenne szükség, ami messze meghaladja az Univerzum 15 milliárd éves életkorát. Minthogy a fehérjék mégiscsak feltekerednek, nem próbálhatják ki az összes lehetséges konformációt, valamilyen más mechanizmust kell követniük. Azt gondoljuk, hogy a fehérjék konformációs energiafelülete speciális alakú, amelyben a legmélyebb pont a teljes felület bejárása nélkül is könnyen megtalálható. (Pl. egy tölcsér alakú felületen bárhol is engedünk el egy golyót, az a teljes felület bejárása nélkül is mindig a legmélyebb pontba jut.) A vízoldékony fehérjék felületén túlnyomórészt vízkedvelő poláros, a belsejében víztaszító apoláros oldalláncokat találunk. A fehérjék feltekeredésük első néhány milliszekunduma alatt a víztaszító oldalláncok eltemetődése és egymással való kölcsönhatása révén egy apoláros maggal rendelkező kompakt szerkezetet vesznek fel. Ez az ún. hidrofób összeomlás a lehetséges konformációk számát drasztikusan csökkenti, amelyeket végigpróbálgatva van már esély a végső térszerkezet megtalálására. Bár a fehérjék szerkezetét kialakító és stabilizáló kölcsönhatásokat ismerjük, a lehetséges konformációk óriási száma miatt az abszolút energiaminimumnak megfelelő konformáció számítógépes megtalálása egyelőre reménytelen feladat. Éppen ezért távol állunk annak a problémának a megoldásától is, hogy egy adott aminosavszekvenciájú polipeptidlánc képes-e egyáltalán feltekeredni, létezik-e stabilis, jól meghatározott kompakt szerkezete. Pedig új fehérjék tervezéséhez, a fehérjékben rejlő lehetőségek kihasználásához ennek a problémának a megoldása elengedhetetlen. 6
7 MOLEKULÁRIS GÉPEZETEK AZ ÉLŐ SZERVEZETEKBEN Sokat tudunk már a fehérjékről, de egyáltalán érdemes-e ennyi energiát fordítani a fehérjék tanulmányozására? Miért érdekesek a fehérjék? Mert, amint azt az élő szervezetek esetében láthatjuk, önszerveződő molekuláris gépezetek építhetők belőlük. Az önszerveződés alatt azt értjük, hogy az egyes fehérje alegységek (alkatrészek) képesek felismerni egymást, meghatározott módon egymáshoz kapcsolódni, s minden külső beavatkozás nélkül létrehozni az adott szupramolekuláris struktúrát. Az élő szervezetekben található molekuláris gépezetek rendkívül változatos funkciók ellátására képesek. Találhatók közöttük: - molekuláris vegyiüzemek - energiaátalakítók - motorok - jelfelismerők és jelátalakítók - információ feldolgozó rendszerek - multifunkcionális gépezetek - programvezérelt összeszerelők Az enzimek olyan fehérjemolekulák, amelyek képesek egy-egy adott kémiai reakciót akár több milliárdszorosára felgyorsítani. Az enzimek sokszor egymáshoz kapcsolódva, egymással együttműködve összetett rendszereket alkotnak, amelyek végtermékeiket egymásnak átadva bonyolult reakciósorozatok véghezvitelére képesek. A fehérjék szerkezeti dinamikája döntően meghatározza az enzimatikus folyamat hatékonyságát. A fehérjék azért sokkal hatékonyabbak pl. a szervetlen katalizátoroknál, mert a működésük során dinamikus tulajdonságaik miatt szerkezetük folyamatosan idomulni képes a változó követelményekhez. Képesek felismerni és erősen megkötni az átalakítandó szubsztrátot. A szubsztrát bekötődése olyan konformációs átrendeződést idéz elő, amely lehetővé teszi az (az energiagátat lecsökkentve) az átmeneti termék erős kötését is, majd a kémiai reakció megtörténte után bekövetkező relaxációs folyamatok eredményeként képes könnyen elereszteni a végterméket, lehetővé téve az újabb katalitikus ciklus megkezdését. Az élő szervezetekben többféle energiaátalakító rendszerrel találkozhatunk, amelyek a fényenergia, kémiai és mechanikai energia egymásba alakítását végzik. A fotoszintetikus reakciócentrumok pl. nagy hatékonysággal alakítják át a fényenergiát kémiai energiává (ábra). Az így nyert energia végül energiadús vegyületek (ATP, NADH) formájában tárolódik. Az izmokban pedig kémiai energia felhasználásával történik mechanikai munkavégzés. 7
8 Valójában a sejtekben található energiaátalakítók közé tartoznak a molekuláris motorok is. Lineáris motorként működik pl. a kinezin fehérje, amely a sejtek vázát alkotó mikrotubulusok mentén haladva képes hasznos terhet szállítani (ábra). A molekula két lábdoménjével felváltva lépeget, minden egyes lépéshez egy-egy energiadús ATP molekula elbomlása biztosítja az energiát. Fejrészén keresztül képes specifikusan felismerni és megkötni a szállítandó célmolekulát. Ma már a kinezin mozgásának molekuláris részleteiről is sokat tudunk (animáció). A kinezin lépéseinek hossza 8 nm, átlagos mozgási sebessége 160 nm/s. A mai legmodernebb mérésétechnikákkal akár egyetlen pl. fluoreszcens festékkel megjelölt molekula mozgása is megbízhatóan nyomon követhető. Számos egyéb lineáris motorként működő fehérjét ismerünk, az izmok működése is azon alapul, hogy a miozin molekulák képesek mozogni az aktin szálak mentén. De fehérjékből nem csak lineáris, hanem rotációs (forgó mozgást végző) motorok is építhetők. Engedjék meg, hogy ennek kapcsán egy kicsit saját kutatásainkról is beszéljek önöknek. A baktériumok mozgásszervei a flagellumok, amelyek sejtmembránba ágyazott része magában foglal egy parányi, 50 nm átmérőjű molekuláris motort. Minden egyes motorhoz egy-egy 5-10 µm hosszúságú helikális filamentum csatlakozik, amely a flagellin fehérje több tízezer kópiájából épül fel (ábra). Ezek a helikális filamentumok a baktérium úszása során egyetlen nagy helikális köteggé állnak össze, amely tengelye körül forogva mintegy propellerként hajtja előre a baktériumot. A flagelláris motorok morfológiájukat tekintve nagyon hasonlítanak az ember által készített elektromotorokhoz, hengerszimmetrikus szerkezetűek, álló- és forgórészből állnak (animáció). Ezeket azonban nem elektronok, hanem protonok hajtják. Akár 100 ezres percenkénti fordulatszám elérésére is képesek, ami többszörösen meghaladja az F1-es versenyautók motorjainak fordulatszámát. Hatékonyságukat jellemzi, hogy egyetlen körülforduláshoz csupán protont használnak fel. A fehérjék rendkívül specifikus molekula felismerésre képesek, amelynek fontos szerepe van a környezettel való kommunikációban és az idegen anyagok elleni védekezésben is. Néha egyetlen kívülről érkező hormon molekula képes gyökeresen megváltoztatni egy sejt működését (ábra). A jelfelismerésben és jelfeldolgozásban a sejtmembránban elhelyezkedő és azon átnyúló ún. receptorfehérjék játszanak alapvető szerepet, amelyek külső részén a hírvivő molekula specifikus kötődése a fehérje egészére kiterjedő konformációváltozást indukál, beindítva a sejten belüli effektor funkciókat. A magasabbrendűek immunrendszerének működése azon alapul, hogy az immunglobulin molekulák akár több millió féle idegen molekulát képesek megbízhatóan felismerni. Valójában a természet nagyszámú 8
9 immunglobulin G variánst generál, amelyek abban különböznek egymástól, hogy az antigénkötésben szerepet játszó doménjeik 3 ill. 4 felületi hurokrégiójának aminosavszekvenciája eltér egymástól, ezáltal különféle kötőfelületek jönnek létre (ábra). Ezen véletlenszerűen generált kötőfelületek között a tapasztalat szerint mindig található olyan, amelyik képes az idegen makromolekula, vírus vagy sejt valamelyik felületi régiójához specifikusan és erősen kötődni. Multifunkcionális molekuláris gépezetek például a vírusok, amelyek képesek felismerni egy adott célsejtet, annak felületéhez erősen hozzákötődni, a sejtmembránt átlyukasztva saját DNS-üket a sejtbe juttatni, ami aztán a sejten belüli folyamatok irányítását átvéve nagy mennyiségben legyártatja a vírust alkotó fehérje és nukleinsav komponenseket. Ezek a komponensek önszerveződő képességüknél fogva működőképes vírusokká állnak össze, amelyek a sejtből sokszorozottan kiáramolva indulnak további támadásra. Talán hihetetlenül hangzik, de fehérjékből és nukleinsavakból programvezérelt összeszerelő rendszerek is építhetők. Ilyenek pl. a riboszómák, amelyek a fehérjék szintézisét végzik. (A nukleinsavak a DNS és RNS a fehérjékhez hasonlóan lineáris polimerek, amelyek azonban csupán négy féle építőelemből (nukleotidból) állnak. Az egyes fehérjék aminosavsorrendjét meghatározó információt a DNS molekula egy darabja tárolja, amelyet génnek nevezünk.) A DNS-ben tárolt információt hordozó hírvivő RNS molekulákat megkötve, az általuk hordozott lineáris információ alapján képesek legyártani a megfelelő fehérjét. Valójában az RNS molekula hordozza azt a digitális programot, ami vezérli a riboszóma működését. A riboszómák két alegysége három hatalmas RNS molekulából és több mint 50 fehérje komponensből épül fel. A riboszóma a legnagyobb molekuláris komplexum, amelynek szerkezetét atomi precizitással ismerjük (ábra). Ezek az óriási szupramolekuláris rendszerek is rendelkeznek az önszerveződés képességével, alkotóelemeikből, azokat megfelelő sorrendben és körülmények között összekeverve, kémcsőben is rekonstruálhatók. Valójában az RNS molekulák alkotják azt a vázat, amely térben rendezi a fehérje alegységeket, s a legfontosabb katalitikus lépéseket is az RNS molekulák végzik. A mai élőlények sejtjeinek működésében a riboszómák által szintetizált fehérjék játszanak meghatározó szerepet. A biológiai evolúció korai szakaszában valószínűleg az örökítő és katalitikus funkciók egyidejű ellátására is képes RNS molekulák irányították a primitív sejtek belső folyamatait (RNS világ). Az ősi RNS enzimek képességeik kiterjesztése érdekében fokozatosan kezdtek el fehérje természetű kiegészítőket - oligopeptideket és kisebb fehérjéket - használni, amelyek aztán a későbbiekben szinte teljesen kisajátították a sejtben zajló folyamatok irányítását. Az RNS-ek információtároló funkcióját pedig az erre a célra szerkezeti tulajdonságaik miatt alkalmasabb DNS molekulák vették át. Az RNS-ek és fehérjék ősi együttműködésének maradványai a riboszómák. 9
10 Vajon mi teszi alkalmassá a fehérjéket önszerveződő molekuláris gépezetek építésére? A válasz kissé paradox: mert a fehérjék megfelelően nagyok, s ugyanakkor elég kicsik is. A fehérjék kiterjedt felszínén több könnyen felismerhető régió található, amelyeken keresztül specifikusan képesek más fehérjékhez (molekulákhoz) való kapcsolódásra. A fehérje kölcsönhatásokban részt vevő kontaktfelszínek alakjukat és kölcsönhatási mintázatukat tekintve is komplementerek egymással. Ennek eredménye az, hogy csak a meghatározott partnerrel, szigorún meghatározott szerkezetű komplexumot alkotva jön létre a kölcsönhatás. Ugyanakkor a fehérjék kis mérete miatt a véletlenszerű hőmozgások (Brown mozgás) nagyon intenzívek, másodpercenként több tízmilliárdnyi relatív konformáció kipróbálására nyújtva lehetőséget. Ez magyarázza, hogy a fehérjealapú molekuláris gépezetek alegységei miként képesek a megfelelő módon, minden külső beavatkozás nélkül gyorsan összekapcsolódni. LEHET-E MÉG JOBB FEHÉRJÉKET CSINÁLNI? A bemutatott példák alapján láthatjuk, hogy a 4,5 milliárd éves földi evolúció eredményeként az élő rendszerekben található fehérjék fantasztikus dolgokra, rendkívül szerteágazó feladatok ellátására képesek. Kézenfekvő a kérdés, hogy miként használhatnánk fel őket a saját céljainkra. De előtte érdemes végiggondolnunk, hogy van-e esély esetleg még a létezőknél is jobb fehérjéket előállítani. Végezzünk ismét egy rövid számolást, becsüljük meg, hogy egy átlagos méretű, 300 aminosavból álló fehérjéből hány különbözőt (eltérő aminosavszekvenciájút) lehetne előállítani. Minthogy a szekvencia minden egyes pozíciójában 20-féle aminosav közül szabadon választhatunk, a lehetséges szekvenciák száma: N = = 20 Gigantikus számot kaptunk. Összehasonlításként számítsuk ki az Univerzum köbnanométerben mért térfogatát: az Univerzum mérete 15 milliárd fényév 3*10 35 nm az Univerzum térfogata nm 3 Egy fehérje átlagos térfogata néhány köbnanométer. Az ismert Univerzum köbnanométerben mért térfogata eltörpül a lehetséges fehérjeszekvenciák száma mellett. Másképpen megfogalmazva, ha képesek lennénk megszintetizálni a lehetséges fehérjeszekvenciákat, akkor azok egy parányi töredékével zsúfolásig teletömhetnénk az Univerzumot. Figyelembe db 10
11 véve, hogy Világegyetemünket meglehetősen ritkán tölti ki az anyag, azt kell mondanunk, hogy ha az összes létező anyagot fehérjék szintézisére használnánk, akkor is csak egy elenyésző töredékét gyárthatnánk le a lehetséges szekvenciáknak. A földi evolúció számára még sokkal korlátozottabb anyagmennyiség állt rendelkezésre. Az eltelt 4,5 milliárd év során a Földön a lehetséges fehérjeszekvenciák csak egy hihetetlenül parányi töredékének kipróbálására nyílt lehetőség. És ebből a parányi töredékből ámulatba ejtő tulajdonságú molekuláris gépezeteket lehetett konstruálni, olyan komplex rendszereket lehetett építeni, mint amilyenek pl. a baktériumok, halak, kutyák vagy emberek. Ha képesek lennénk tudatos fehérjetervezésre, ha meg tudnánk mondani, hogy egy adott aminosavszekvencia milyen térszerkezetet képes felvenni, s az milyen funkciót láthat el, akkor minden bizonnyal a természetben létező fehérjéknél jóval változatosabb előnyösebb tulajdonságokkal rendelkező fehérjéket állíthatnánk elő. FEHÉRJEALAPÚ NANOTECHNOLÓGIA A nanotechnológia alapvető célkitűzése, hogy alulról, atomokból ill. molekulákból építkezve hozzon létre működőképes rendszereket. Szerencsére a nanotechnológia kifejlesztésénél nem kell mindent magunknak kitalálnunk. Hiszen az orrunk előtt működik egy a négy milliárd éves földi evolúció eredményeként létrejött, bámulatos dolgokra képes fehérje alapú nanotechnológia. Az élő szervezetek példája azt mutatja, hogy a fehérjék kiválóan alkalmasak önszerveződő molekuláris gépezetek építésére. Miként használhatnánk fel őket a saját céljainkra? Az élő szervezetekben található molekuláris gépezetek szerkezetének, működési elveinek megértése jelenti az alapját a fehérjék nanotechnológiai alkalmazásának. A fehérjealapú nanotechnológia fejlődésének lehetséges forgatókönyve az alábbi lépéseken keresztül képzelhető el: - az élő rendszerekben található molekuláris gépezetek szerkezetének, működési mechanizmusának felderítése - a meglévő fehérjék tulajdonságainak célzott módosítása - fehérjetervezés - fehérjékből álló komplex rendszerek tervezése - másodgenerációs eszközök kifejlesztése - programvezérelt összeszerelő rendszerek létrehozása 11
12 Az elmúlt három évtized intenzív kutatásainak eredményeként az élő szervezetekben található molekuláris gépezetek szerkezetéről és működéséről már meglehetősen sok ismerettel rendelkezünk. Röviden tekintsük át, hogy a további lépéseket illetően hol tartunk ma. Fehérjék átformálása A fehérjék nanotechnológiai alkalmazásának kézenfekvő módja a természetes fehérjék célzott módosítása. Ilyenkor megpróbáljuk úgy megváltoztatni természetes fehérjék tulajdonságait, hogy általunk kívánt funkciók ellátására legyenek képesek. Az egyes fehérjék aminosavsorrendjét meghatározó információt a DNS molekula egy darabja tárolja, amelyet génnek nevezünk. Az élő szervezetekben található fehérjéket, pontosabban azok aminosavszekvenciáit, ma már képesek vagyunk a génsebészet módszereivel szinte tetszés szerint átalakítani. A problémát inkább az jelenti, hogy minél több aminosavat cserélünk ki, annál kevésbé tudjuk megjósolni a módosítások térszerkezeti következményeit. A génsebészet nem más, mint a nanotechnológia egy már jól működő formája. Segítségével képesek vagyunk tetszés szerint megváltoztatni és átalakítani egy DNS molekula nukleotidsorrendjét. Persze ebben nem csak a mi ügyességünk rejlik: valójában a baktériumoktól kölcsönözzük azokat a molekuláris eszközöket (fehérjéket), amelyek segítségével egy kiszemelt DNS darab elvágható, vagy éppen összeforrasztható, lemásolható és sokszorozható. Egy kiszemelt gén nukleotidsorrendjét átalakítva tetszés szerint megváltoztathatjuk az általa kódolt fehérje aminosavsorrendjét is, vagy akár gyökeresen új fehérjéket állíthatunk elő. A természetes fehérjék szerkezetének vizsgálata során felismert összefüggések, törvényszerűségek, szerveződési elvek sokat segítenek abban, hogy egy fehérje szerkezetében vagy tulajdonságaiban célzott módosításokat idézhessünk elő. Ma már viszonylag egyszerű feladatnak számít megnövelni egy fehérje hőstabilitását, megváltoztatni ph-toleranciáját, kötődési jellemzőit, az optimális működés feltételeit, módosítani katalitikus tulajdonságait. Módosított fehérjékkel hétköznapjainkban is gyakran találkozhatunk, mosóporaink pl. olyan enzimeket tartalmaznak, amelyek 90ºC-on, erősen lúgos körülmények között is kiválóan működnek. A módosított fehérjék jelenlegi nanotechnológiai alkalmazásai alapvetően két csoportba sorolhatók: egyrészt specifikus molekulafelismerő képességüket kihasználva bioszenzorok alapelemeiként érzékelési feladatokra használhatjuk őket, másrészt önszerveződő képességüket kiaknázva kiválóan alkalmazhatóak molekuláris objektumok építésére. Konkrét nanotechnológiai alkalmazásként hadd mutassam be, hogy miként hozhatunk létre rendezett kvantumpötty mintázatokat módosított fehérjék segítségével. A kvantumpötty néhány nanométeres átmérőjű parányi fémsziget. A kvantummechanika szerint egy parányi 12
13 fémpötty elektromos és optikai tulajdonságait (pl. színét, gerjeszthetőségét) elsősorban annak mérete, s nem pedig annak anyagi minősége határozza meg. A méret precíz kontrollja révén tehát az elektromos és optikai tulajdonságok is precízen szabályozhatók. Egy-egy ilyen fémszigetecske memóriaelemként funkcionálhat, amely akár egyetlen elektronnal vezérelhető. Kémiai úton rendkívül nehéz pontosan azonos méretű kvantumpöttyöket előállítani, fehérjék segítségével azonban egészen egyszerűen megvalósítható (animáció). A vérben található ferritin fehérje a vasatomok megkötését és tárolását végzi. 24 azonos alegységből áll, amelyek rendelkeznek az önszerveződés képességével, s spontán módon egy üreges, labdaszerű képződményt formálnak. A ferritin fémkötési tulajdonságainak génsebészeti módosításával különféle fémek specifikus felismerésére és megkötésére képes ferritin variánsokat állíthatunk elő, pl. olyanokat amelyek arany vagy éppen nikkel megkötésére képesek. A ferritin gömböcskék az alegységek közötti pórusokon keresztül oldatban begyűjtik a megfelelő fémionokat, s a belsejükben egy szigorúan meghatározott méretű fémgömb alakul ki. A fehérjék kristályosíthatóságát kihasználva a fémmagot tartalmazó ferritin molekulákból alkalmas felületen rendezett mintázatokat, ún. kétdimenziós kristályokat hozhatunk létre. Végeztül a fehérjeburkot eltávolítva (pl. UV vagy hőkezeléssel) rendezett kvantumpötty mintázathoz jutunk. Hogyan csinálhatunk átformált fehérjéken alapuló bioszenzorokat? A korábbiakban láttuk már, hogy a magasabbrendűek immunrendszerében meghatározó szerepet játszó IgG molekulák akár több millió féle idegen molekulát képesek megbízhatóan felismerni. Valójában a természet nagyszámú IgG variánst generál, amelyek abban különböznek egymástól, hogy az antigénkötésben szerepet játszó felületi hurokrégiók aminosavszekvenciája eltér egymástól, ezáltal különféle kötőfelületek jönnek létre. Az IgG doméneknél megfigyelt alapelveket alkalmazva más, eredetileg receptor tulajdonságokkal nem rendelkező fehérjék felületén is kialakíthatunk adott célmolekulára specifikus kötőhelyeket. Pl. Skerra és munkatársai a lipocalin fehérje felületi hurokrégióinak aminosavszekvenciáit variálása révén nagyszámú mutánst hoztak létre (ábra), majd ezek közül megfelelő szelekciós eljárások alkalmazásával kiválasztották egy adott célmolekula erős és specifikus megkötésére képes módosulatokat. Az így előállított mesterséges receptorok bioszenzorok alapeleméül szolgálhatnak. Pl. az ún. rezgőnyelves bioszenzorokban receptorainkat egy nagyfrekvenciával rezgetett parányi sziliciumlapkára rögzítjük (ábra). Ha a lapka felett átáramoltatott mintában jelen van a keresett komponens, akkor azt a lapka felületén lévő receptorok megkötik, ami tömegnövekedéssel és a rezgési frekvencia megváltozásával jár. Mindezt a lapkára bocsátott lézerfény eltérülésének megváltozása révén könnyen detektálhatjuk. Fehérjetervezés Természetesen a meglévő fehérjék tulajdonságainak módosításán túlmenősen az igazi kihívást a mesterséges fehérjék tervezése és létrehozása jelenti. A fehérjék tervezése még gyerekcipőben jár. Attól nagyon távol állunk, hogy egy adott aminosavszekvenciáról meg tudnánk mondani, hogy egyáltalán képes-e ill. milyen szerkezetté képes feltekeredni, s a feltekeredett szerkezet rendelkezik-e bármiféle hasznos funkcióval. Meglévő tapasztalataink 13
14 alapján azonban a siker reményében vállalkozhatunk arra, hogy egy kívánt szerkezettel (feltekeredési mintázattal) kompatibilis aminosavszekvenciá(ka)t keressünk. Így például DeGrado és munkatársai olyan aminosavszekvenciákat terveztek, amelyek képesek voltak kívánt α-helikális szerkezetű globuláris fehérjét formálni (ábra). Ezen mesterséges fehérjék felszínén sikerrel hoztak létre különféle ligandumok specifikus felismerésére képes kötőhelyeket. Bár egyszerűbb feltekeredési mintázatokat létre tudunk hozni, ezeket primitív funkciókkal fel tudjuk ruházni, mesterséges fehérjéink tulajdonságai messze elmaradnak természetes társaikétól. Ennek legfőbb oka az, hogy a fehérjék működésében meghatározó szereppel bíró dinamikai tulajdonságok tervszerű kialakítására egyelőre esély sincsen. Noha a tudatos fehérjetervezés még gyerekcipőben jár, léteznek olyan tudattalan módszerek, amelyek segítségével gyökeresen új fehérjék létrehozására is nyílik esély. Ezeket mesterséges vagy irányított evolúciós eljárásoknak hívjuk. Amint az a nevükből is kiderül, valójában a természetes evolúciós folyamat utánzásáról és felgyorsításáról van szó. Ilyenkor véletlenszerűen indukálunk változásokat egy fehérjét kódoló gén nukleotid szekvenciájában, vagy akár teljesen új géneket hozunk létre. A lényeg az, hogy nagyon nagyszámú variánst generálunk, baktériumok segítségével megszintetizáltatjuk a nekik megfelelő polipeptidláncokat, majd ezek közül megfelelő szelekciós módszerek alkalmazásával kihalásszuk a kívánt tulajdonságúakat. A fehérje-alapú nanotechnológia megvalósításának következő lépcsőfokát jelentené a mesterséges fehérjékből álló önszerveződő komplex rendszerek, molekuláris gépezetek létrehozása. Ilyen jellegű próbálkozások ezidáig még nem történtek. Persze a fehérjék technológiai alkalmazása során nyilvánvaló korlátokkal is szembe kell néznünk. Hiszen a fehérjék általában vizes közegben funkcionálnak, csak meglehetősen korlátozott környezeti körülmények között működőképesek. De hát mi magunk is fehérjealapú rendszerek vagyunk, s mégis tudunk pl. vasat olvasztani vagy éppen agyagot égetni. Természetesen nem a kezünket dugjuk bele a kemencébe, hanem eszközöket, szerszámokat használunk. A természetes fehérjék is hasonlóképpen használnak eszközöket, nem fehérje természetű kiegészítő csoportokat bizonyos feladatok megvalósítására. A fehérjék aminosav oldalláncai pl. nem nyelik el a látható fényt. A fotoszintetikus reakciócentrumok fénybegyűjtő komplexeiben a fehérjékhez kapcsolódva olyan hatalmas, kiterjedt delokalizált elektronrendszerrel rendelkező klorofillmolekulákat találunk amelyek kiváló hatásfokkal nyelik el a látható fényt, s továbbítják a fényelnyelés következtében szeparálódó töltéseket az őket alkalmazó fehérjéknek. Az ilyen fehérjék által organizált (irányított) kiegészítő csoportokat alkalmazó rendszereket nevezzük másodgenerációs fehérjealapú eszközöknek. S végezetül a fehérjealapú nanotechnológia igazán csábító kihívása a riboszómákhoz hasonlóan működő programvezérelt molekuláris összeszerelő rendszerek létrehozása lehet. 14
15 Az élő szervezetekben található molekuláris gépezetek ámulatba ejtő tulajdonságai sejtetik a fehérjealapú nanotechnológia távlatait. A gyökeresen új megközelítési módból adódóan minden korábbit felülmúló technológiai áttörés várható. Különösen nyilvánvaló ez a gyógyászat területén, ahol a ma alkalmazott módszerek alkalmatlansága, a molekuláris megközelítés fontossága magától értetődő. Milyen más lesz majd, ha a rákos daganatok kivagdosása helyett képesek leszünk a DNS szinten való beavatkozásra. Ha tudunk majd fehérjékből olyan parányi molekuláris gépezeteket konstruálni, amelyeket a vérbe juttatva azok megtalálják a beteg sejteket, s bennük kijavítják a DNS hibákat, amik a problémát okozzák. ÖSSZEFOGLALÁS A várakozások szerint a XXI. század a molekuláris biológia és a nanotechnológia évszázada lesz. Egyre nyilvánvalóbb, hogy a fehérjék mindkét területen meghatározó szerepet játszanak majd. A fehérjék olyan kivételes tulajdonságokkal rendelkező anyagok, amelyek kiválóan alkalmasak önszerveződő molekuláris rendszerek építésére. Érdemes ellesnünk az élő szervezetektől a fehérjealapú molekuláris gépezetek szerveződési elveit, megfejteni működésük mechanizmusát, hogy a magunk kedve szerint építhessünk talán még a természetben megfigyelhetőknél is lenyűgözőbb képességű nanoméretű eszközöket. 15
Bio-nanorendszerek. Vonderviszt Ferenc. Pannon Egyetem Nanotechnológia Tanszék
 Bio-nanorendszerek Vonderviszt Ferenc Pannon Egyetem Nanotechnológia Tanszék Technológia: képesség az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének befolyásolására. A technológiai
Bio-nanorendszerek Vonderviszt Ferenc Pannon Egyetem Nanotechnológia Tanszék Technológia: képesség az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének befolyásolására. A technológiai
Nano-biotechnológia: érzékelés és építkezés biológiai makromolekulák segítségével
 Nano-biotechnológia: érzékelés és építkezés biológiai makromolekulák segítségével Bionanotechnológia: hogyan lehet érzékelésre, építkezésre és egyéb dolgokra használni a biológiai makromolekulákat. Ismétlés:
Nano-biotechnológia: érzékelés és építkezés biológiai makromolekulák segítségével Bionanotechnológia: hogyan lehet érzékelésre, építkezésre és egyéb dolgokra használni a biológiai makromolekulákat. Ismétlés:
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Flagellin alapú filamentáris nanoszerkezetek létrehozása
 Flagellin alapú filamentáris nanoszerkezetek létrehozása Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium MTA Enzimológiai Intézete MTA MFA Bakteriális flagellumok Flagelláris filamentum: ~10
Flagellin alapú filamentáris nanoszerkezetek létrehozása Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium MTA Enzimológiai Intézete MTA MFA Bakteriális flagellumok Flagelláris filamentum: ~10
Biomolekuláris nanotechnológia. Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium
 Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Fehérjék. A fehérjék szerkezeti szintjei. Elsődleges szerkezet
 Fehérjék A fehérjék az élő szervezet számára nélkülözhetetlen molekulák, melyeket változatos térszerkezet és funkcionalitás jellemez. De úgy is fogalmazhatnánk, hogy a fehérjék olyan kivételes tulajdonságokkal
Fehérjék A fehérjék az élő szervezet számára nélkülözhetetlen molekulák, melyeket változatos térszerkezet és funkcionalitás jellemez. De úgy is fogalmazhatnánk, hogy a fehérjék olyan kivételes tulajdonságokkal
Nanotechnológia. Vonderviszt Ferenc. Veszprémi Egyetem Nanotechnológia Tanszék
 Nanotechnológia Vonderviszt Ferenc Veszprémi Egyetem Nanotechnológia Tanszék Ősi technológiák Mikroelektronika Technológia: képesség az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének
Nanotechnológia Vonderviszt Ferenc Veszprémi Egyetem Nanotechnológia Tanszék Ősi technológiák Mikroelektronika Technológia: képesség az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Az élő sejt fizikai Biológiája:
 Az élő sejt fizikai Biológiája: Modellépítés, biológiai rendszerek skálázódása Kellermayer Miklós Fizikai biológia Ma már nem csak kvalitatív megfigyeléseket, hanem kvantitatív méréseket végzünk (biológiai
Az élő sejt fizikai Biológiája: Modellépítés, biológiai rendszerek skálázódása Kellermayer Miklós Fizikai biológia Ma már nem csak kvalitatív megfigyeléseket, hanem kvantitatív méréseket végzünk (biológiai
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Kémiai reakciók mechanizmusa számítógépes szimulációval
 Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
sejt működés jovo.notebook March 13, 2018
 1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét. Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet
 Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői.
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1. Mely mennyiségek között teremt kapcsolatot a bizonytalansági reláció? A) a koordináta értéke
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1. Mely mennyiségek között teremt kapcsolatot a bizonytalansági reláció? A) a koordináta értéke
TRANSZPORTFOLYAMATOK A SEJTEKBEN
 16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
Építkezés biológiai makromolekulák segítségével
 A nanotechnológia két dologban különbözik az eddig ismert technológiáktól: Az egyik, hogy a nanométeres mérettartományban mozgunk, építkezünk. Nagyon fontos, hogy ez az építkezés alulról-felfelé építkezés,
A nanotechnológia két dologban különbözik az eddig ismert technológiáktól: Az egyik, hogy a nanométeres mérettartományban mozgunk, építkezünk. Nagyon fontos, hogy ez az építkezés alulról-felfelé építkezés,
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE
 AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
Immunológia alapjai előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B-sejt receptorok:
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B-sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B-sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Speciális fluoreszcencia spektroszkópiai módszerek
 Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Peptidek és fehérjék 1. Fehérjék Fehérjetekeredés. Fehérje (protein) Fehérje (protein) Aminosavak. Aminosavak
 Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
A kémiai energia átalakítása a sejtekben
 A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
12/4/2014. Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció. 1952 Hershey & Chase 1953!!!
 Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis
 Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
SCHRÖDINGER mi is az élet? Rausch Péter ELTE TTK kémia-környezettan
 Rausch Péter ELTE TTK kémia-környezettan A természettudományok nem véletlenül képeznek szerves egységet, hiszen a körülöttünk lévő világ a természet működését igyekeznek tudományos igényességgel leírni.
Rausch Péter ELTE TTK kémia-környezettan A természettudományok nem véletlenül képeznek szerves egységet, hiszen a körülöttünk lévő világ a természet működését igyekeznek tudományos igényességgel leírni.
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
A BIOLÓGIAI JELENSÉGEK FIZIKAI HÁTTERE Zimányi László
 A BIOLÓGIAI JELENSÉGEK FIZIKAI HÁTTERE Zimányi László Összefoglalás A négy alapvető fizikai kölcsönhatás közül az elektromágneses kölcsönhatásnak van fontos szerepe a biológiában. Atomi és molekuláris
A BIOLÓGIAI JELENSÉGEK FIZIKAI HÁTTERE Zimányi László Összefoglalás A négy alapvető fizikai kölcsönhatás közül az elektromágneses kölcsönhatásnak van fontos szerepe a biológiában. Atomi és molekuláris
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 30 Műszeres ÁSVÁNYHATÁROZÁS XXX. Műszeres ÁsVÁNYHATÁROZÁs 1. BEVEZETÉs Az ásványok természetes úton, a kémiai elemek kombinálódásával keletkezett (és ma is keletkező),
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 30 Műszeres ÁSVÁNYHATÁROZÁS XXX. Műszeres ÁsVÁNYHATÁROZÁs 1. BEVEZETÉs Az ásványok természetes úton, a kémiai elemek kombinálódásával keletkezett (és ma is keletkező),
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A lézer alapjairól (az iskolában)
 A lézer alapjairól (az iskolában) Dr. Sükösd Csaba c. egyetemi tanár Budapesti Műszaki és Gazdaságtudományi Egyetem Tartalom Elektromágneses hullám (fény) kibocsátása Hogyan bocsát ki fényt egy atom? o
A lézer alapjairól (az iskolában) Dr. Sükösd Csaba c. egyetemi tanár Budapesti Műszaki és Gazdaságtudományi Egyetem Tartalom Elektromágneses hullám (fény) kibocsátása Hogyan bocsát ki fényt egy atom? o
NANOTECHNOLOGIA 6. előadás
 NANOTECHNOLOGIA 6. előadás A plazmid: Ha meg akarjuk ismerni egy fehérje működését, akkor sokat kell belőle előállítanunk. Ezt akár úgy is megtehetjük, hogy a kívánt géndarabot egy baktérumba ültetjük
NANOTECHNOLOGIA 6. előadás A plazmid: Ha meg akarjuk ismerni egy fehérje működését, akkor sokat kell belőle előállítanunk. Ezt akár úgy is megtehetjük, hogy a kívánt géndarabot egy baktérumba ültetjük
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biofizika szeminárium. Diffúzió, ozmózis
 Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
A citoszolikus NADH mitokondriumba jutása
 A citoszolikus NADH mitokondriumba jutása Energiaforrásaink Fototróf: fotoszintetizáló élőlények, szerves vegyületeket állítanak elő napenergia segítségével (a fényenergiát kémiai energiává alakítják át)
A citoszolikus NADH mitokondriumba jutása Energiaforrásaink Fototróf: fotoszintetizáló élőlények, szerves vegyületeket állítanak elő napenergia segítségével (a fényenergiát kémiai energiává alakítják át)
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Az atommag összetétele, radioaktivitás
 Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Titokzatos gyümölcskocsonya
 Titokzatos gyümölcskocsonya A gyümölcstorta igazán csábító édesség és elkészíteni sem olyan nagy ördöngösség. Kivéve, ha valami mégsem sikerül. Például nem dermed meg a tetején a zselé De hát miért?! Hiszen
Titokzatos gyümölcskocsonya A gyümölcstorta igazán csábító édesség és elkészíteni sem olyan nagy ördöngösség. Kivéve, ha valami mégsem sikerül. Például nem dermed meg a tetején a zselé De hát miért?! Hiszen
A nanotechnológia lehetôsége az egészségügyben
 A nanotechnológia lehetôsége az egészségügyben Vonderviszt Ferenc, Veszprémi Egyetem, Mûszaki Informatikai Kar, Nanotechnológia Tanszék, Veszprém, MTA Mûszaki Fizikai és Anyagtudományi Kutatóintézet, Budapest
A nanotechnológia lehetôsége az egészségügyben Vonderviszt Ferenc, Veszprémi Egyetem, Mûszaki Informatikai Kar, Nanotechnológia Tanszék, Veszprém, MTA Mûszaki Fizikai és Anyagtudományi Kutatóintézet, Budapest
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
In vivo szövetanalízis. Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra
 In vivo szövetanalízis Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra In vivo képalkotó rendszerek Célja Noninvazív módon Biológiai folyamatokat képes rögzíteni Élő egyedekben
In vivo szövetanalízis Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra In vivo képalkotó rendszerek Célja Noninvazív módon Biológiai folyamatokat képes rögzíteni Élő egyedekben
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén
 Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Biológia egészségtan Általános iskola 7. osztály
 Általános iskola 7. osztály A tanuló értse az éghajlati övezetek kialakulásának okait és a biomok összetételének összefüggéseit az adott térségre jellemző környezeti tényezőkkel. Ismerje a globális környezetkárosítás
Általános iskola 7. osztály A tanuló értse az éghajlati övezetek kialakulásának okait és a biomok összetételének összefüggéseit az adott térségre jellemző környezeti tényezőkkel. Ismerje a globális környezetkárosítás
ELEMI RÉSZECSKÉK ATOMMODELLEK
 ELEMI RÉSZECSKÉK ATOMMODELLEK Az atomok felépítése Készítette: Horváthné Vlasics Zsuzsanna Mi van az atomok belsejében? DÉMOKRITOSZ (Kr.e. 460-370) az anyag nem folytonos parányi, tovább nem bontható,
ELEMI RÉSZECSKÉK ATOMMODELLEK Az atomok felépítése Készítette: Horváthné Vlasics Zsuzsanna Mi van az atomok belsejében? DÉMOKRITOSZ (Kr.e. 460-370) az anyag nem folytonos parányi, tovább nem bontható,
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
FELADATLISTA TÉMAKÖRÖK, ILLETVE KÉPESSÉGEK SZERINT
 FELADATLISTA TÉMAKÖRÖK, ILLETVE KÉPESSÉGEK SZERINT A feladatok kódját a Bevezetésben bemutatott tananyagtartalom- és képességmátrix alapján határoztuk meg. A feladat kódja a következőképpen épül fel: évfolyam/témakör1-témakör2/képesség1-képesség2/sorszám
FELADATLISTA TÉMAKÖRÖK, ILLETVE KÉPESSÉGEK SZERINT A feladatok kódját a Bevezetésben bemutatott tananyagtartalom- és képességmátrix alapján határoztuk meg. A feladat kódja a következőképpen épül fel: évfolyam/témakör1-témakör2/képesség1-képesség2/sorszám
A II. kategória Fizika OKTV mérési feladatainak megoldása
 Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
Mikrohullámú abszorbensek vizsgálata
 Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Evolúcióelmélet és az evolúció mechanizmusai
 Evolúcióelmélet és az evolúció mechanizmusai Az élet Darwini szemlélete Melyek az evolúció bizonyítékai a világban? EVOLÚCIÓ: VÁLTOZATOSSÁG Mutáció Horizontális géntranszfer Genetikai rekombináció Rekombináció
Evolúcióelmélet és az evolúció mechanizmusai Az élet Darwini szemlélete Melyek az evolúció bizonyítékai a világban? EVOLÚCIÓ: VÁLTOZATOSSÁG Mutáció Horizontális géntranszfer Genetikai rekombináció Rekombináció
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Makromolekulák. I. A -vázas polimerek szerkezete és fizikai tulajdonságai. Pekker Sándor
 Makromolekulák I. A -vázas polimerek szerkezete és fizikai tulajdonságai Pekker Sándor MTA SZFKI Telefon:392-2222/845, Fax:392-229, Email: pekker@szfki.hu SZFKI tanfolyam: www.szfki.hu/moodle/course/ a
Makromolekulák I. A -vázas polimerek szerkezete és fizikai tulajdonságai Pekker Sándor MTA SZFKI Telefon:392-2222/845, Fax:392-229, Email: pekker@szfki.hu SZFKI tanfolyam: www.szfki.hu/moodle/course/ a
FLAGELLINALAPÚ MOLEKULÁRIS OBJEKTUMOK LÉTREHOZÁSA. Sebestyén Anett
 Pannon Egyetem Műszaki Informatikai Kar Nanotechnológia Tanszék FLAGELLINALAPÚ MOLEKULÁRIS OBJEKTUMOK LÉTREHOZÁSA Doktori (PhD) értekezés tézisei Sebestyén Anett Környezettudományok Doktori Iskola Témavezető:
Pannon Egyetem Műszaki Informatikai Kar Nanotechnológia Tanszék FLAGELLINALAPÚ MOLEKULÁRIS OBJEKTUMOK LÉTREHOZÁSA Doktori (PhD) értekezés tézisei Sebestyén Anett Környezettudományok Doktori Iskola Témavezető:
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Farmakológus szakasszisztens Farmakológus szakasszisztens 2/34
 -06 Farmakológus szakasszisztens feladatok A 0/007 (II. 7.) SzMM rendelettel módosított /006 (II. 7.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés
-06 Farmakológus szakasszisztens feladatok A 0/007 (II. 7.) SzMM rendelettel módosított /006 (II. 7.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés
2. Ismert térszerkezetű transzmembrán fehérjék adatbázisa: a PDBTM adatbázis. 3. A transzmembrán fehérje topológiai adatbázis, a TOPDB szerver
 A 2005 és 2007 között megvalósított project célja transzmembrán fehérjék vizsgálata és az ehhez szükséges eljárások kifejlesztése volt. Ez utóbbi magába foglalta új adatbázisok és szerkezet becslő módszerek
A 2005 és 2007 között megvalósított project célja transzmembrán fehérjék vizsgálata és az ehhez szükséges eljárások kifejlesztése volt. Ez utóbbi magába foglalta új adatbázisok és szerkezet becslő módszerek
A felvétel és a leadás közötti átalakító folyamatok összességét intermedier - köztes anyagcserének nevezzük.
 1 Az anyagcsere Szerk.: Vizkievicz András Általános bevezető Az élő sejtekben zajló biokémiai folyamatok összességét anyagcserének nevezzük. Az élő sejtek nyílt anyagi rendszerek, azaz környezetükkel állandó
1 Az anyagcsere Szerk.: Vizkievicz András Általános bevezető Az élő sejtekben zajló biokémiai folyamatok összességét anyagcserének nevezzük. Az élő sejtek nyílt anyagi rendszerek, azaz környezetükkel állandó
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai
 Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai Az áramlási citométer és sejtszorter felépítése és működése Kereskedelmi forgalomban kapható készülékek 1 Fogalmak
Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai Az áramlási citométer és sejtszorter felépítése és működése Kereskedelmi forgalomban kapható készülékek 1 Fogalmak
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
BIOKÉMIA. Simonné Prof. Dr. Sarkadi Livia egyetemi tanár.
 BIOKÉMIA Simonné Prof. Dr. Sarkadi Livia egyetemi tanár e-mail: sarkadi@mail.bme.hu Tudományterületi elhelyezés Alaptudományok (pl.: matematika, fizika, kémia, biológia) Alkalmazott tudományok Interdiszciplináris
BIOKÉMIA Simonné Prof. Dr. Sarkadi Livia egyetemi tanár e-mail: sarkadi@mail.bme.hu Tudományterületi elhelyezés Alaptudományok (pl.: matematika, fizika, kémia, biológia) Alkalmazott tudományok Interdiszciplináris
Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben?
 Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben? Szalay Péter egyetemi tanár ELTE, Kémiai Intézet Elméleti Kémiai Laboratórium Van közös bennük? Egy kis történelem
Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben? Szalay Péter egyetemi tanár ELTE, Kémiai Intézet Elméleti Kémiai Laboratórium Van közös bennük? Egy kis történelem
DNS-számítógép. Balló Gábor
 DNS-számítógép Balló Gábor Bevezetés A nukleinsavak az élő szervezetek egyik legfontosabb alkotórészei. Ezekben tárolódnak ugyanis az öröklődéshez, és a fehérjeszintézishez szükséges információk. Bár a
DNS-számítógép Balló Gábor Bevezetés A nukleinsavak az élő szervezetek egyik legfontosabb alkotórészei. Ezekben tárolódnak ugyanis az öröklődéshez, és a fehérjeszintézishez szükséges információk. Bár a
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások
 Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Röntgen-gamma spektrometria
 Röntgen-gamma spektrométer fejlesztése radioaktív anyagok elemi összetétele és izotópszelektív radioaktivitása egyidejű meghatározására Szalóki Imre, Gerényi Anita, Radócz Gábor Nukleáris Technikai Intézet
Röntgen-gamma spektrométer fejlesztése radioaktív anyagok elemi összetétele és izotópszelektív radioaktivitása egyidejű meghatározására Szalóki Imre, Gerényi Anita, Radócz Gábor Nukleáris Technikai Intézet
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Informatikai eszközök fizikai alapjai Lovász Béla
 Informatikai eszközök fizikai alapjai Lovász Béla Kódolás Moduláció Morzekód Mágneses tárolás merevlemezeken Modulációs eljárások típusai Kódolás A kód megállapodás szerinti jelek vagy szimbólumok rendszere,
Informatikai eszközök fizikai alapjai Lovász Béla Kódolás Moduláció Morzekód Mágneses tárolás merevlemezeken Modulációs eljárások típusai Kódolás A kód megállapodás szerinti jelek vagy szimbólumok rendszere,
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Bioinformatika 2 6. előadás
 6. előadás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2018.10.08. PDBj: http://www.pdbj.org/ Fehérjék 3D szerkezeti adatbázisai - PDBj 2 2018.10.08.
6. előadás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2018.10.08. PDBj: http://www.pdbj.org/ Fehérjék 3D szerkezeti adatbázisai - PDBj 2 2018.10.08.
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
