A malignus melanóma molekuláris klasszifikációja és markerei
|
|
|
- Antal Faragó
- 9 évvel ezelőtt
- Látták:
Átírás
1 Összefoglaló közlemény 73 A malignus melanóma molekuláris klasszifikációja és markerei Tímár József 1, Hársing Judit 2, Somlai Beáta 2 Semmelweis Egyetem, Klinikai Központ, 1 2. Sz. Patológiai Intézet és 2 Bőr-, Nemikórtani és Bőronkológiai Klinika, Budapest A malignus melanóma patológiai klasszifikációja az utóbbi években csak az UV-besugárzással kapcsolatos jelenségek tekintetében változott. Ugyanakkor megszületett a melanóma molekuláris klasszifikációja, amely a három leggyakoribb génhiba mellett (BRAF, NRAS, CKIT) számos ritkább altípust azonosított. Ezek a markerek azonban nem alkalmasak a jó- és rosszindulatú melanocitás léziók elkülönítésére. Erre a célra az ún. melanómamarkerek sem alkalmasak, mivel ezek döntően a melanoszómákat alkotó fehérjék, amelyek elsősorban a differenciáldiagnosztikában nyújtanak segítséget. Újabban in situ hibridizációs eljárásokat alakítottak ki, melyek elég specifikusak a malignus pigmentsejtes léziókra. Újabb gondot okozhatnak az áttéti szövetekben (nyirokcsomó, bél, agy) normálisan is jelen lévő melanociták, mert ilyenkor csak molekuláris eszközökkel lehet a melanómasejteket azonosítani. Magyar Onkológia 57:73 78, 2013 Kulcsszavak: melanóma, molekuláris klasszifikáció, markerek Pathological classification of malignant melanoma did not change in the past decade, it was just completed with UVinduced skin alterations. A new feature, however, is the establishment of molecular classification of melanoma indicating that beside the most frequent genetic alterations (BRAF, NRAS, CKIT mutations) there is a wide variety of rare molecular subclasses. Unfortunately, none of these genetic alterations can be used to discriminate benign lesions from malignant ones. The frequently used melanoma markers are mostly melanosomal markers, therefore they are not helpful for this diagnostic purpose either. More recently, novel FISH kits have been developed analyzing characteristic copy number alterations specific for malignant melanoma. Though melanosomal markers are helpful in differencial diagnostics, the presence of normal melanocytes in various tissues (lymph nodes, intestine or brain) requires application of molecular techniques when melanoma metastasis is in question. Tímár J, Hársing J, Somlai B. Molecular classification and markers of malignant melanoma. Hungarian Oncology 57:73 78, 2013 Keywords: melanoma, molecular classification, markers Levelezési cím: Dr. Tímár József, Semmelweis Egyetem, 2. Sz. Patológiai Intézet, 1091 Budapest, Üllői út 93. Tel.: , jtimar@gmail.com Közlésre érkezett: április 1. Elfogadva: május 20. Magyar Onkológia 57:73 78, 2013
2 74 Tímár és mtsai A MALIGNUS MelanóMA MOLEKULÁRIS KLASSZIFIKÁCIÓJA A malignus melanóma morfológiai klasszifikációja kialakult és gyakorlatilag változatlan az elmúlt évtizedekben (1, 2). Etiológiáját tekintve a malignus melanómának familiáris, UV-indukált és nem UV-indukált formáit ismerjük, ez utóbbiak az akrolentiginózus, a mukozális és az uveális formák. Az elmúlt évek újdonsága az, hogy az UV-indukált melanómákat két nagy csoportra lehet osztani az UV-expozíció tartama szerint: a krónikus napfénykárosodás jegyeit mutató bőrben keletkező formára (chronic sun-induced damage, CSD) és az intermittáló nagy UV-expozíció talaján keletkező formára (intermittent UV exposure vagy non-csd) (3). Az elmúlt évtized megteremtette a malignus melanóma molekuláris (re)klasszifikációját az ún. vezető genetikai hibák felismerése alapján. A nem UV-indukált uveális melanómák esetében a melanokortin receptor (MC1R) jelpálya kis G fehérje génjeinek a mutációja jellemző (GNAQ és GNA11). A nem UV-indukált felszíni hámmelanómák esetében (mukozális melanóma és akrolentiginózus melanóma) gyakori (20-30%) a melanocitafunkciót szabályozó stem cell factor receptor KIT gén aktiváló mutációja a GIST tumorokhoz hasonló exonokban, azonban ez együtt jár génamplifikációval is. Érdekes, hogy egy neuronmarker, az NMDA-receptor GRIN2A az UV-indukált dezmoplasztikus és noduláris melanómák egy kisebb százalékában mutációt szenvedhet (3). Az UV-indukált melanómák domináló génhibái a növekedési faktor receptor jelpályák RAS-RAF útvonalának hibái: BRAF-mutáció (50%) vagy NRAS-mutáció (20%). Szemben a tüdő vagy a vastagbél adenokarcinómáival, ahol a növekedési faktor receptor maga is genetikailag károsodott lehet (EGFR-mutáció vagy génamplifikáció), UVindukált melanómák esetében a BRAF/NRAS kettős-vad 1. ábra. A malignus melanóma jelentősebb genetikai eltérései. Mutáns gén: kövérrel szedve sejtfelszín MC1R sejtmag GRIN2A KIT (EGFR) GNAQ,GNA11 CDK CDKN2A MITF NRAS BRAF MAPK p53 (MET) PI3K AKT mtor PTEN esetekben viszonylag ritka a KIT receptor mutációja, de 7,4%-ban EGFR-amplifikáció található (4). A melanómák fenotípusának szabályozója az MITF transzkripciós faktor, genetikai hibája (génamplifikáció) azonban ritka (<10%). Bár a sejtciklus-szabályozás zavarai igen gyakoriak melanómában, az ezt szabályozó kulcskomponensek genetikai hibái viszonylag ritkák (ciklin D %, CDKN2A <10%, p53 <10%). Más daganatokban gyakran aktivált az ún. lipidkináz-jelpálya (AKT-mTOR), és ez áll a melanómára is, melynek hátterében elsősorban a PTEN gátló elem hibája áll (<30%) (3, 5) (1. ábra). MelanóMAMARKEREK Melanómaspecifikus markert nem ismerünk, azok a markerek, amelyeket akár a patológiában, akár labora tóriumi diagnosztikában használnak, valamennyien mela no citaspeci fikus markerek, és ezek döntő többsége a melanociták sajátságos funkciójával, melanintermelésével összefüggő marker. A melanoszóma olyan sejtorganellum, amely a mela nin termelést végzi, mely az endoplazmás reti ku lumból, a Golgi-membránból, a lizoszomális, illetve endo szomá lis rendszer membránjaiból keletkezik. Négy fejlettségi formája ismert. A korábban pre-melanoszómának nevezett membránvezikulák nem tartalmaznak tirozinázt, viszont DOPA-pozitívak. Az I-es stádiumú melanoszómák így tirozináznegatívak, míg a II-es stádiumú melanoszómák, amelyek fibrillális elongált struktúrákat is tartalmaznak, már tirozinázpozitívak. A III-as stádiumú melanoszómákban jelenik meg a melanin pigment, és a IV-es stádiumban az alapstruktúra már alig kivehető (2. ábra) (6). A melanoszómákban három jellegzetes enzimet lehet kimutatni, a tirozinázt, a TRP-1-et és a dopakróm-tautomerázt (DCT). A tirozináz a tirozinból DOPA-kinont hoz létre. A DOPA-kinonból keletkezik két metabolit, az 5-SC-DOPA, illetve a DOPA-króm. A DOPA-krómot a DCT alakítja tovább indolszármazékokká. Ez utóbbi metabolitokból keletkezik az eumelanin (DHI-melanin). A DOPA-kinonból ciszteinútvonalon feomelanin keletkezik. A TRP-1 elsősorban nem mint pigmentmetabolizáló, hanem chaperonszerű fehérje, amely a tirozináz enzim funkcióját befolyásolja. A melanoszómák strukturális komponensei közül a legismertebb a gp100 vagy Pmel17, amely a melanoszómák fibrilláris komponensét alkotja, és az I. és II. stádiumú melanoszómákban már kimutatható (2. ábra). A melanoszómákban egy másik strukturális fehérjét is találhatunk, ez pedig a MART-1 vagy Melan-A, amelyet korábban melanómaspecifikus antigénnek ismertek, melyet a T-sejtek ismernek fel, de ez is gyakorlatilag melanoszomális fehérje. A melanocitáknak vannak sajátos receptorai, amelyek erre a sejttípusra jellemzőek, ezek Professional Publishing Hungary
3 A melanóma molekuláris klasszifikációja és markerei 75 közül a legfontosabb a melanokortin-1-receptor (MC1R), amely G-protein kapcsolt receptor, és a PKA jelátviteli úton aktiválódik (6). A melanociták és a melanómák is expresszálnak egy jellegzetes kalciumkötő fehérjét, az S100-at, amelynek két formája (α és a β) ismeretes, melyek homodimereket képeznek: melanómákban a β-izoforma expresszálódik (7). Ez nem melanó maspecifikus, mert a legtöbb endokrin sejttípus is exp resszálja, közöttük a gliómák, Schwannomák, neuro blasz tó mák, de a Langerhans-sejtek is. A melanociták neuro ekto der mális eredetűek, és e sejttípusok fejlődése során a neuron spe cifikus enoláz (NSE) a fejlődés korai stádiumában jelen van. Az NSE a glikolitikus útvonalban elhelyezkedő enzim, számos, nem csak neuroektodermális eredetű daganatban emelkedett szintet mutat, köztük a melanómákban is. A melanocitákban és melanómasejtekben számos glikopro tein expresszálódik, melyek egy része tumormarkerként vagy tumor antigénként szerepelhet. Ezek között az egyik legismertebb a TA90 tumorasszociált glikoprotein, amely immu no genitása miatt a melanómaellenes immunválaszban is szerepet játszik, és újabban azért merült fel jelentősége a melanóma kimutatásában, mert érzékeny PET-eljárásokat lehetett kidolgozni, amelyek a TA90 expressziója alapján azonosítják a metasztatikus daganatszövetet. A melanómák expresszálják az NG2 kondroitinszulfát típusú proteo glikánt, mely egy kd-os transzmembrán fehérje. Felhasználását a diagnosztikában az limitálja, hogy nagyon nehéz az immu no lógiai kimutatása a paraffinba ágyazott szövetekből. A melanómák számos daganatantigént expresszálnak, ezek között a diagnosztikában jelentősége van a MAGE3 csoportnak. A melanociták és melanómák egyik legfontosabb transzkripciós faktora az MITF, mely a melanociták differenciálódásáért felelős transzkripciós faktor, amely a melanómákban is megőrzi a funkcióját. A fentiekben említett valamennyi melanómamarker gyakorlatilag melanocitamarker, és ezért felhasználása a melanó ma differenciáldiagnosztikájában limitált (6, 7). Éppen ezért intenzíven folyik olyan markerek kutatása, amelyek a mela nocita-melanóma differenciáldiagnosztikában is segítséget tudnának nyújtani. A DNS-csip módszerek elterjedésével számos vizsgálatban tanulmányozták a melanómák expressziós mintázatát, hogy olyan géneket azonosítsanak, amelyek pre fe renciálisan a melanómákban expresszálódnak, de az eddigi vizsgálatok csak melanocitagéneket tártak fel. Az általunk folytatott ez irányú vizsgálatok több olyan gént azonosítottak, amelyek melanómaspecifikus expressziót mutatnak, és amelyek a naevusokban nem expresszálódnak. Ezek között a retinoblasztómaszerű p107-es fehérje, a rianodin receptor-2 kalciumcsatorna és a ciklin E fehérje érdemel említést (8). A melanómák genetikai vizsgálatai számos eltérést azonosítottak, azonban ezek döntő többsége nae vusok ban, illetve diszplasztikus naevusokban is kimutatható. Ilyen genetikai eltérés a mikroszatellita-instabilitás, amely a melanómák 10%-ában, de már a naevusok 10%-ában is kimutatható. Gyakori genetikai hiba a heterozigótaság elvesztése (LOH) számos gén esetében, azonban ezek jelentős része szintén már kimutatható a naevusokban is. Ebből a szempontból érdekes lehet a továbbiakban az apoptotikus proteázaktiváló faktor-1 génre vonatkozó hete ro zigó ta ság elvesztése, mert úgy tűnik, hogy érzékeny melanó mamarker lehet (9). A melanómák leggyakoribb genetikai eltérései a BRAF, illetve az NRAS gén mutációja, azonban mindkettő nagy gyakorisággal fordul elő már a naevusokban és diszplasztikus naevusokban. A p53 vagy p16 inaktiváló mutációja kisebb gyakorisággal előfordulhat, 2. ábra. Melanoszóma- és melanómamarkerek kapcsolata. a) Különböző érettségű melanoszómák elektronmikroszkópos képe. b) A melanoszómák érése és használható markereinek sémája. Tir=tirozináz, TRP1=tirozináz-csatolt fehérje-1, DCT= dopakróm-tautomeráz, ER=endoplazmás retikulum a b Pmel-17 DOPA I. II. III. IV. DOPA Pmel-17 Golgi ER Sejtmag Pmel-17 Magyar Onkológia 57:73 78, 2013
4 76 Tímár és mtsai azonban egyik mutáció sem tekinthető melanómaspecifikus genetikai eltérésnek, mivel prekurzor léziókban is jelen lehet. Fentiek alapján melanómaspecifikus génről vagy antigén ről nem tudunk, az eddig használt markerek valamennyien az egész melanocitavonalra jellemzőek, és a jóindulatú vagy diszplasztikus melanocitaléziókban is kimutathatóak. A kromoszomális instabilitás (CI) a malignus genotípus jellemzője, aminek eredménye a genom egyes területeinek vesztése, illetve fokális amplifikációja. Korai komparatív genomiális hibridizációs vizsgálatok, majd a korszerű teljesgenom-szekvenálási eredmények kimutatták, hogy a melanómákat e kromoszomális jellemzők alapján el lehet különíteni a naevusoktól és diszplasztikus naevusoktól. Ugyanakkor ezeknek az eljárásoknak a mindennapi rutinban történő használata nem lehetséges és túl költséges. Az elmúlt évtizedben ezért a gyakori és melanómára jellemző genomikai eltérésekre alapozva a mindennapi rutinban használható in situ hibridizációs módszereket fejlesztettek ki, és ezek közül egy bevezetésre került a rutindiagnosztikába is (10). A kit 4 színű fluoreszcens detekciós teszt, amely a 6. kromoszóma centromer próbáját (cep6), az ezen lévő RREB gén 6p25 és MYB gén 6q23 próbáit, valamint a ciklin D1 gén 11. kromoszóma q13 próbáját tartalmazza (11). Kiértékeléskor 4 feltétel legalább egyikének teljesülése szükséges a melanóma valószínűsítéséhez: a sejtek több mint 38%-a >2 jelet tartalmaz a CCND1-re vagy a sejtek több mint 55%-a több jelet tartalmaz a 6p25-re, mint a cep6-ra, a sejtek több mint 40%-a kevesebb MYB jelet tartalmaz, mint a cep6, illetve ha a sejteknek több mint 29%-a kettőnél több RREB1 jelet tartalmaz. E kritériumok használatával 95,4%- os specificitás és 86,7%-os szenzitivitás volt elérhető. Egy későbbi kiterjesztett validációs elemzésben a határértékeket a CCND1 esetében 19%-ra, míg az RREB1 esetében 16%-ra csökkentették, de a szenzitivitás és specificitás nem változott (10). MelanóMAMETASZTÁZIS AZONOSÍTÁSA Bőrléziók In transit vagy szatellitatumorok azonosítása során a dediffe ren ciált vagy amelanotikus melanómák esetében immunhisz to kémiai vizsgálathoz elsősorban az S-100β fehérje elleni antitesteket kell használni, de célszerű több markert is vizsgálni, miután a melanóma különböző antigénjeinek expressziója igen heterogén, egy-egy tumor esetében igen alacsony szinten lehet. Célszerű egy melanoszomális és egy nem melanoszomális markert kombinálni, éppen a pigmentáció eltérő szintje miatt. A melanoszomális markerek közül a patológiai vizsgálatok során a Melan-A vagy MART-1 jól használható, de miután ez késői melanoszómamarker, ennél érzékenyebbnek tűnik a tirozináz használata, amely korai melanoszomális marker, hasonlóan a HMB45 antitesttel kimutatható pmel17/gp100 antigénhez. Nem melanoszomális markerként az S100β használható. E markerek kombinálásával a melanómák azonosítása gyakorlatilag 100%-os lehet, azonban ha csak egy markert használunk, igen nagy eltérések lehetnek a detektálás sikerében. Nyirokcsomóáttétek A nyirokcsomók esetében a melanómasejtek kimutatásának problémája az, hogy fals pozitív és negatív eredményeket is adhat. A pigmentált sejtek kimutatása a nyirokcsomókban nem feltétlenül jelenti a melanómasejtek azonosítását, hiszen melanociták előfordulhatnak a nyirokcsomókban is. Ahogy korábban jeleztük, a melanómamarkerek egyben melanocitamarkerek is, tehát az erre alapozott vizsgálat félrevezető lehet, ezért a morfológiai paraméterekkel való összevetést is meg kell tenni. Kisebb sejtcsoportok esetében a citológiai abnormalitások jelenléte segíthet e sejteknek a normális melanocitáktól való elkülönítésében. A metasztatikus melanóma immunhisztokémiai detektálásának problémája az, hogy a kisebb sejtcsoportok, illetve az egyedi sejtek megtalálása attól (is) függ, hogy sorozatmetszetekből mennyit készítünk egy adott nyirokcsomóból. Alternatív módszerként kidolgozták a molekuláris biológiai diagnosztikát, amely ugyanazon melanoszomális géneket használja. A probléma itt is ugyanaz, mint amit a melanómaantigének azonosításánál már említettünk, hogy az egy markerre alapozott detektálás nem elég érzékeny, ezért egyre inkább terjed a többmarkeres detektálás. Különböző vizsgálatok szerint az immunhisztokémiailag, illetve HE-metszetek alapján negatív nyirokcsomók esetében a molekuláris biológiai vizsgálat az őrszemnyirokcsomók felében képes legalább egy melanómamarkert, és egy másik negyedében több mint egy melanómamarkert azonosítani. Hogy ennek a molekuláris detektálásnak mekkora a klinikopatológiai jelentősége, azt az mutatja, hogy önmagában egy pozitív marker kimutatása az őrszemnyirokcsomókban nem változtatja meg a beteg progresszióig eltelt túlélését. Ugyanakkor a kettő, illetve több molekuláris markerre alapozott kimutatás rövidebb betegségmentes, illetve teljes túléléssel társul (12 14). A probléma az, hogy ezek a gének nagyon alacsony szinten expresszálódnak a vizsgált metasztatikus szövetben. A nyirokcsomók esetében a legérzékenyebb molekuláris eljárás a valós idejű polimeráz-láncreakcióval végrehajtott vizsgálat, és ezek esetében a MART-1 melanómaantigént vagy a PAX-3 transzkripciós faktor expresszióját használták, így egy marker alkalmazásával is megfelelő érzékenységet lehetett elérni (15). Természetesen ugyanazon problémával szembesülünk itt is, mint más őrszemnyirokcsomó-vizsgálat esetében, hogy a markervizsgálatra felhasznált nyirokcsomórész- Professional Publishing Hungary
5 A melanóma molekuláris klasszifikációja és markerei 77 let nem vizsgálható patológiailag, illetve a nyirokcsomónak csak egy részét vizsgálva esély van arra, hogy fals negativitást kapunk, hiszen a nyirokcsomó másik patológiailag feldolgozott részében is előfordulhatnak áttéti daganatsejtek. A fentiek alapján el kell dönteni, hogy molekuláris vizsgálatra használjuk az őrszemnyirokcsomót vagy patológiai feldolgozásra. Ez utóbbi esetben azt sorozatmetszetekben kell vizsgálni. Miután a melanóma prognózisát nemcsak az érintett nyirokcsomók száma, hanem az adott nyirokcsomóban lévő daganatszövet mennyisége is befolyásolja, a stádiummeghatározáshoz a makroszkópos, illetve mikroszkópos áttét pontos méretének meghatározását kell elvégezni. A molekuláris eljárás egyrészt túl érzékeny, másrészt fontos morfológiai adatokról nem ad felvilágosítást, így a mai klinikai igényeknek nem igazán megfelelő. Zsigeri áttét Az alkalmazott módszer attól függ, hogy milyen módon nyerünk mintát az adott szövetből. A citológiai minták esetében a morfológia mellett célszerű immunhisztokémiát, illetve molekuláris eljárásokat alkalmazni. Tisztában kell azonban lennünk azzal, hogy melanociták a bőrön kívül más szervben is jelen lehetnek, így a gasztrointesztinális traktus nyálkahártyájában, illetve a központi idegrendszer lágyagyburkában is. Ennek megfelelően melanocita-antigének kimutatása e területeken önmagában nem feltétlenül jelenti melanómasejtek jelenlétét. Más szövetekben azonban és itt a máj és a tüdő lehet két olyan terület, ahol ennek jelentősége van a melanómaantigének, illetve melanociter gének és antigének kimutatása gyakorlatilag melanómaspecifikusnak tekinthető. Immunhisztokémiailag az S100β használata veszélyes, mert a Langerhans-sejtek, illetve idegi sejtek jelenléte zavarhatja a kimutatást, ezért célszerű a melanoszomális antigének használata, így a tirozináz, TRP1, DCT, illetve a MART-1 antigéné. Csontvelő, perifériás vér A keringő egyedi melanómasejtek kimutatásának kétféle módszere van, a melanómasejtek által szekretált proteinek detektálása, illetve a tumorsejtek direkt kimutatása. Ugyanazon molekuláris vagy immunhisztokémiai markereket célszerű használni, mint amit a szöveti kimutatás során használunk. A vérben sajnálatos módon ritkán használják a MART-1 és a tirozináz kimutatását, pedig ezek immunhisztokémai vagy molekuláris detektálása specifikus és érzékeny módszer. Jóval szélesebb körben használják az S100β szérumszintjének a kimutatását, amivel az a probléma, hogy ennek szenzitivitása I. és II. stádiumban gyakorlatilag minimális, és csak a III. és IV. stádiumban lehet megbízhatóan alkalmazni (16). Tudni kell azonban, hogy az S100β nem melanómaspecifikus, és számos nem daganatos betegségben is megemelkedhet a szérumszintje. A neuronspecifikus enoláz (NSE) gyakorlatilag kiesik a progrediáló melanóma diagnosztikájából és a terápia moni torizálására szolgáló vizsgáló eljárások közül. Egyes szer zők a melanómainhibitoros aktivitás (MIA) kimutatását használják, melynek azonban a szenzitivitása alacsony, az összehasonlító vizsgálatok szerint nem tudja felülmúlni az S100β diagnosztikus képességét. A csontvelőben, illetve a perifériás vérben a tirozináz en zim kimutatását elsősorban molekuláris módszerrel cél sze rű végezni. A melaninprekurzorok kémiai, illetve HPLC-s kimutatásai közül a 5-S-ciszteinil-DOPA (5-SCD) szé rum szint jének a vizsgálata igen széles körben tesztelt eljárás, melyről kiderült, hogy kevésbé érzékeny, mint az S100β (17). Valószínűleg itt a probléma az, hogy a melanómák melanint termelő képessége eltérő, mely heteroge nitás a melanoszomális pigmentek kimutatásában is megnyilvánul. Ezért célszerű egy korábbi melanoszomális differenciációs gén vagy fehérje kimutatására alapozni az ilyen markervizsgálatokat, mint amilyen a tirozináz vagy a gp100/pmel17, melyek a korai melanoszomális stádiumokban már jelen vannak, tehát így szérumszintjük vagy génexpressziójuk kimutatása kevésbé függ a melanoszomális rendszer daganatokban történő károsodásától. A szérum-ldh-aktivitás az utóbbi időben fontos progressziós mar kerré lépett elő, amely az előrehaladott, IV. stá diumú melanómák esetében egyértelmű negatív prognosztikus mar kerként szerepel. Az LDH-szint még az S100β szérumszintjénél is érzékenyebb progressziós marker, amely egyértelműen összefügg a betegek túlélésével (17). Az egyetlen probléma az, hogy minden szövetszéteséssel járó folyamatban is megemelkedik az LDH-szint, tehát egyszeri elvégzése nem elegendő, ezt néhány hónapon belül ismételni kell, és az ismételt emelkedésnek van prognosztikus jelentősége. Az LDH ugyanakkor nem melanómaspecifikus marker. Vajon akkor miért függ össze az LDH-szint a daganat progressziójával az előrehaladott melanómák esetében? Nagyon fontos tudni azt, hogy az LDH enzim expressziója a szöveti hipoxiával függ össze. Normális szövetekben hipoxia esetén a hipoxia transzkripciós faktor (HIF) aktivitásának megindulásával számos olyan gén kapcsolódik be, amelyek a hipoxia leküzdésében játszanak szerepet, melyek egyike az LDH. Melanómák esetében (is) az LDH-expresszió fokozódása a tumorszöveti hipoxiával áll kapcsolatban. Korai stádiumban a hipoxiás/ nekrotikus területek ritkák, így az LDH-szint nem emelkedett. Ezzel szemben a III. stádiumban már makroszkopikus nyirokcsomóáttétek is kialakulhatnak, és megemelkedhet az LDH-szint. Mindaddig, amíg ennél érzékenyebb indikátort nem találunk, nyilvánvalóan ez a marker fogja dominálni a IV. stádiumú betegek progressziójának monitorozását is. Magyar Onkológia 57:73 78, 2013
6 78 Tímár és mtsai IRODALOM 1. Orosz Zs. A melanoma malignum patológiai diagnosztikájának buktatói. Magyar Onkológia 47:27 41, Plótár V, Orosz Zs, Tóth E, Szentirmay Z. A melanoma malignum hisztopatológiai prognosztikus faktorai. Magyar Onkológia 51:39 46, Tímár J, Barbai T, Győrffy B, Rásó E. Understanding melanoma progression by gene expression signatures. Chapter 2. Cancer Genomics. Ed. Pfeffer U, Springer, Dordrecht 2013, pp Rákosy Z, Vizkeleti L, Ecsedi S, et al. EGFR gene copy number alterations in primary cutaneous malignant melanomas are associated with poor prognosis. Int J Cancer 121: , Vidwans SJ, Flaherty KT, Fisher DE, et al. A melanoma molecular disease model. PLoS One 6:e18257, Hearing VJ. Biogenesis of pigment granules: a sensitive way to regulate melanocyte function. J Dermatol Sci 37:3 14, Torabian S, Kashani-Sabet M. Biomarkers for melanoma. Curr Opin Oncol 17: , Deli T, Varga N, Ádám A, et al. Functional genomics of calcium channels in human melanoma cells. Int J Cancer 121:55 65, Mustika R, Budiyanto A, Nishigori C, et al. Decreased expression of Apaf-1 with progression of melanoma. Pigment Cell Res 18:59 62, Gerami P, Zembowicz A. Update of fluorescence in situ hybridization in melanoma. Arch Pathol Lab Med 135: , Takeuchi H, Morton DL, Kuo C, et al. Prognostic significance of molecular upstaging of paraffin-embedded sentinel lymph nodes in melanoma patients. J Clin Oncol 22: , Thomas JM. Time to re-evaluate sentinel node biopsy in melanoma post-multicenter selective lymphadenectomy trial. J Clin Oncol 23: , Voit C, Kron M, Rademaker J, et al. Molecular staging in stage II and III melanoma patients and its effect on long-term survival. J Clin Oncol 23: , Abrahamsen HN, Sorensen BS, Nexo E, et al. Pathologic assessment of melanoma sentinel nodes: a role for molecular analysis using quantitative real-time reverse transcription-pcr for MART-1 and tyrosinase messenger RNA. Clin Cancer Res 11: , Bánfalvi T, Udvarhelyi N, Orosz Z, et al. Heterogenous S-100B protein expression patterns in malignant melanoma and association with serum protein levels. Oncology 64: , Bánfalvi T, Boldizsár M, Gergye M, et al. Comparison of prognostic significance of serum 5-S-cysteinyldopa, LDH and S-100B protein in stage III IV malignant melanoma. Pathol Oncol Res 8: , 2002 H I R D E T M É N Y A MAGYAR PATHOLOGUSOK TÁRSASÁGA ÉS A MAGYAR ONKOLÓGUSOK TÁRSASÁGA által évre meghirdetett A digitális patológia alkalmazásának lehetôségei a XXI. századi betegellátásban címû KROMPECHER ÖDÖN pályázat nyertese: I. helyezést ért el: Gleason jeligével Székely Nóra Anna SE ÁOK V. évf. hallgató II. helyezett: Foxtrot jeligével Varga Anna Veronika SE ÁOK V. évf. hallgató III. helyezett: Tejeskávé jeligével Jakab Zsófia Lilla SE ÁOK IV. évf. hallgató Budapest, március MAGYAR PATHOLOGUSOK TÁRSASÁGA és MAGYAR ONKOLÓGUSOK TÁRSASÁGA VEZETÔSÉGE Professional Publishing Hungary
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
A malignus melanóma új TNM-klasszifikációja (AJCC, 2009) és az őrszemnyirokcsomó-biopszia patológiai jelentősége
 68 Összefoglaló közlemény A malignus melanóma új TNM-klasszifikációja (AJCC, 2009) és az őrszemnyirokcsomó-biopszia patológiai jelentősége Plótár Vanda 1, Liszkay Gabriella 2, Ladányi Andrea 1, Tóth Erika
68 Összefoglaló közlemény A malignus melanóma új TNM-klasszifikációja (AJCC, 2009) és az őrszemnyirokcsomó-biopszia patológiai jelentősége Plótár Vanda 1, Liszkay Gabriella 2, Ladányi Andrea 1, Tóth Erika
Géneltérések biológiai szerepe és prognosztikai jelentősége humán malignus melanomákban
 268 Doktori tézisek Géneltérések biológiai szerepe és prognosztikai jelentősége humán malignus melanomákban Vízkeleti Laura Debreceni Egyetem, Egészségtudományok Doktori Iskola, Debrecen Témavezető: Prof.
268 Doktori tézisek Géneltérések biológiai szerepe és prognosztikai jelentősége humán malignus melanomákban Vízkeleti Laura Debreceni Egyetem, Egészségtudományok Doktori Iskola, Debrecen Témavezető: Prof.
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény
 A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A hólyagrák aktuális kérdései a pathologus szemszögéből. Iványi Béla SZTE Pathologia
 A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
A melanoma progressziójának laboratóriumi markerei
 A melanoma progressziójának laboratóriumi markerei Eredeti közlemény Bánfalvi Teodóra, Édesné B. Mariann 1, Gergye Mária 2, Udvarhelyi Nóra 3, OroszZsolt 3, Gilde Katalin, Kremmer Tibor 1, Ottó Szabolcs
A melanoma progressziójának laboratóriumi markerei Eredeti közlemény Bánfalvi Teodóra, Édesné B. Mariann 1, Gergye Mária 2, Udvarhelyi Nóra 3, OroszZsolt 3, Gilde Katalin, Kremmer Tibor 1, Ottó Szabolcs
Genomiális eltérések és génexpressszió közötti kapcsolat vizsgálata, melanomák metasztázisképzésére jellemző genetikai markerek kutatása
 A 48750 OTKA pályázat eredményeit összefoglaló szakmai záróbeszámoló A pályázat címe Genomiális eltérések és génexpressszió közötti kapcsolat vizsgálata, melanomák metasztázisképzésére jellemző genetikai
A 48750 OTKA pályázat eredményeit összefoglaló szakmai záróbeszámoló A pályázat címe Genomiális eltérések és génexpressszió közötti kapcsolat vizsgálata, melanomák metasztázisképzésére jellemző genetikai
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében
 A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet. Frank Diagnosztika Szimpózium, DAKO workshop 2012.
 Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
20 éves a Mamma Klinika
 20 éves a Mamma Klinika A sejtdiagnosztika modern eszközei a diagnosztikában és terápiában dr Járay Balázs, dr Székely Eszter Medserv Kft, Semmelweis Egyetem II. Patológiai Intézet Budapest 1 22196 betegből
20 éves a Mamma Klinika A sejtdiagnosztika modern eszközei a diagnosztikában és terápiában dr Járay Balázs, dr Székely Eszter Medserv Kft, Semmelweis Egyetem II. Patológiai Intézet Budapest 1 22196 betegből
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Kappelmayer János. Malignus hematológiai megbetegedések molekuláris háttere. MOLSZE IX. Nagygyűlése. Bük, 2005 szeptember
 Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata
 Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
Emlődaganatok gyógyszeres kezelés. Dr.Tóth Judit DE OEC Onkológiai Tanszék
 Emlődaganatok gyógyszeres kezelés Dr.Tóth Judit DE OEC Onkológiai Tanszék Epidemiológia Kb.7000-8000 új eset évente Mo-on Idősebbek betegsége: -25 éves korban: 5/100 000-50 éves korban: 150/100 000-75
Emlődaganatok gyógyszeres kezelés Dr.Tóth Judit DE OEC Onkológiai Tanszék Epidemiológia Kb.7000-8000 új eset évente Mo-on Idősebbek betegsége: -25 éves korban: 5/100 000-50 éves korban: 150/100 000-75
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek?
 Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Jelátviteli uatk és daganatképződés
 Jelátviteli uatk és daganatképződés Tímár József Semmelweis Egyetem, Klinikai Központ 2.sz. Patológiai Intézet MTA-SE Molekuláris Onkológia Kutatócsoport, Budapest A HER-2 genetikája emberi daganatokban
Jelátviteli uatk és daganatképződés Tímár József Semmelweis Egyetem, Klinikai Központ 2.sz. Patológiai Intézet MTA-SE Molekuláris Onkológia Kutatócsoport, Budapest A HER-2 genetikája emberi daganatokban
EGYETEMI DOKTORI (Ph.D) TÉZISEK
 EGYETEMI DOKTORI (Ph.D) TÉZISEK 1 EGYETEMI DOKTORI (Ph.D) TÉZISEK Melanoma progresszióval összefüggı genetikai és génexpressziós változások Rákosy Zsuzsa Témavezetı: Dr. Balázs Margit tanszékvezetı egyetemi
EGYETEMI DOKTORI (Ph.D) TÉZISEK 1 EGYETEMI DOKTORI (Ph.D) TÉZISEK Melanoma progresszióval összefüggı genetikai és génexpressziós változások Rákosy Zsuzsa Témavezetı: Dr. Balázs Margit tanszékvezetı egyetemi
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere
 I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
Fejezetek a klinikai onkológiából
 Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. A patológiai, képalkotó és laboratóriumi diagnosztika jelentősége az onkológiában.
Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. A patológiai, képalkotó és laboratóriumi diagnosztika jelentősége az onkológiában.
A 22C3 PD-L1 tesztek értékelése intézetünkben. Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs
 A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A.) Biopsziás mintavétel lehetőségei és a biopsziás anyagok kezelésével kapcsolatos tudnivalók.
 II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
A KÜLÖNBÖZŐ ANTITESTEK REAKTIVITÁSA BENIGNUS ÉS MALIGNUS MELANOCITÁS DAGANATOKBAN
 A KÜLÖNBÖZŐ ANTITESTEK REAKTIVITÁSA BENIGNUS ÉS MALIGNUS MELANOCITÁS DAGANATOKBAN Plótár Vanda 1, Szentirmay Zoltán 2, Orosz Zsolt 1 Országos Onkológiai Intézet, 1 Daganatpatológiai, 2 Molekuláris Patológiai
A KÜLÖNBÖZŐ ANTITESTEK REAKTIVITÁSA BENIGNUS ÉS MALIGNUS MELANOCITÁS DAGANATOKBAN Plótár Vanda 1, Szentirmay Zoltán 2, Orosz Zsolt 1 Országos Onkológiai Intézet, 1 Daganatpatológiai, 2 Molekuláris Patológiai
A patológiai vizsgálatok szerepe a célzott terápia kialakításában, hatásának monitorozásában
 Magyar Tudomány 2007/8 A patológiai vizsgálatok szerepe a célzott terápia kialakításában, hatásának monitorozásában és a betegségek kimenetelének előrejelzésében Kopper László az orvostudomány doktora
Magyar Tudomány 2007/8 A patológiai vizsgálatok szerepe a célzott terápia kialakításában, hatásának monitorozásában és a betegségek kimenetelének előrejelzésében Kopper László az orvostudomány doktora
67. Pathologus Kongresszus
 A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján)
 pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
Daganatok kialakulásában szerepet játszó molekuláris folyamatok
 Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
 Sebész szerepe az axilla ellátásában Mersich Tamás Uzsoki utcai Kórház Sebészeti-onkosebészeti Osztály 2014. május 24. Kecskemét Bevezetés A nyirokcsomók sebészi eltávolítása felel a legtöbb szövődményért
Sebész szerepe az axilla ellátásában Mersich Tamás Uzsoki utcai Kórház Sebészeti-onkosebészeti Osztály 2014. május 24. Kecskemét Bevezetés A nyirokcsomók sebészi eltávolítása felel a legtöbb szövődményért
A rosszindulatú daganatos halálozás változása 1975 és 2001 között Magyarországon
 A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
III./5. GIST. Bevezetés. A fejezet felépítése. A.) Panaszok. B.) Anamnézis. Pápai Zsuzsanna
 III./5. GIST Pápai Zsuzsanna A fejezet célja: a GIST daganatok epidemiológiájának, tüneteinek, diagnosztikájának valamint, kezelési lehetőségeinek áttekintése egy beteg esetének bemutatásán keresztül.
III./5. GIST Pápai Zsuzsanna A fejezet célja: a GIST daganatok epidemiológiájának, tüneteinek, diagnosztikájának valamint, kezelési lehetőségeinek áttekintése egy beteg esetének bemutatásán keresztül.
E4 A Gyermekkori szervezett lakossági emlőszűrések hatása az emlőműtétek
 08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
meghatározásának jelentősége
 A HerHer-2 státusz meghatározásának jelentősége gyomorkarcinomában Tímár József, Szirtes Ildikó, Lotz Gábor, Kulka Janina SE 2.sz. Pathologiai Intézet 140 HER-2 fokozott expressziót mutató Emlőrák 20%
A HerHer-2 státusz meghatározásának jelentősége gyomorkarcinomában Tímár József, Szirtes Ildikó, Lotz Gábor, Kulka Janina SE 2.sz. Pathologiai Intézet 140 HER-2 fokozott expressziót mutató Emlőrák 20%
Kiemelt Kutatócsoportok Fóruma Melanoma primer tumor és metasztázis kialakulás kutatása Bőrgyógyászati nem-melanoma tumorok
 Kiemelt Kutatócsoportok Fóruma Melanoma primer tumor és metasztázis kialakulás kutatása Bőrgyógyászati nem-melanoma tumorok Kárpáti Sarolta, Sárdy Miklós a Semmelweis Egyetemen több intézetében zajló melanoma
Kiemelt Kutatócsoportok Fóruma Melanoma primer tumor és metasztázis kialakulás kutatása Bőrgyógyászati nem-melanoma tumorok Kárpáti Sarolta, Sárdy Miklós a Semmelweis Egyetemen több intézetében zajló melanoma
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
A bőrmelanoma kezelésének módjai. Dr. Forgács Balázs Bőrgyógyászati Osztály
 A bőrmelanoma kezelésének módjai Dr. Forgács Balázs Bőrgyógyászati Osztály Melanoma TNM (AJCC VIII.) A melanoma kezelés alapja (T:tumor, N:nyirokcsomó, M:metasztázis) T: Breslow érték a legközelebbi 0,1
A bőrmelanoma kezelésének módjai Dr. Forgács Balázs Bőrgyógyászati Osztály Melanoma TNM (AJCC VIII.) A melanoma kezelés alapja (T:tumor, N:nyirokcsomó, M:metasztázis) T: Breslow érték a legközelebbi 0,1
TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA. Dr. Kurgyis Zsuzsanna
 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA PhD tézis Dr. Kurgyis Zsuzsanna Bőrgyógyászati és Allergológiai Klinika Szegedi Tudományegyetem Szeged 2017 2 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA
TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA PhD tézis Dr. Kurgyis Zsuzsanna Bőrgyógyászati és Allergológiai Klinika Szegedi Tudományegyetem Szeged 2017 2 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA
A preventív vakcináció lényege :
 Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Dr. Erőss Loránd, Dr. Entz László Országos Idegtudományi Intézet
 Molekuláris Medicina Mindenkinek Semmelweis Egyetem, Neurológiai Klinika 2012. December 4. Dr. Erőss Loránd, Dr. Entz László Országos Idegtudományi Intézet Felosztás Neurofibromatózis I. (Recklinghausen
Molekuláris Medicina Mindenkinek Semmelweis Egyetem, Neurológiai Klinika 2012. December 4. Dr. Erőss Loránd, Dr. Entz László Országos Idegtudományi Intézet Felosztás Neurofibromatózis I. (Recklinghausen
Grádus rendszerek vizsgálata IAés IB stádiumú adenocarcinomákban
 Grádus rendszerek vizsgálata IAés IB stádiumú adenocarcinomákban Zombori Tamás, Furák József, Urbán Dániel, Némedi Réka, Nyári Tibor, Cserni Gábor, TiszlaviczLászló Pathologiai Intézet, ÁOK Szegedi Tudományegyetem
Grádus rendszerek vizsgálata IAés IB stádiumú adenocarcinomákban Zombori Tamás, Furák József, Urbán Dániel, Némedi Réka, Nyári Tibor, Cserni Gábor, TiszlaviczLászló Pathologiai Intézet, ÁOK Szegedi Tudományegyetem
SENTINEL NYIROKCSOMÓ SZCINTIGRÁFIA EMLŐRÁKBAN- MÓDSZERTANI ÚTMUTATÓ
 SENTINEL NYIROKCSOMÓ SZCINTIGRÁFIA EMLŐRÁKBAN- MÓDSZERTANI ÚTMUTATÓ Írta: Rajtár Mária 1. Háttér információk és definíciók Az emlőrák sebészi kezelése során az axillaris blockdissectióval eltávolított
SENTINEL NYIROKCSOMÓ SZCINTIGRÁFIA EMLŐRÁKBAN- MÓDSZERTANI ÚTMUTATÓ Írta: Rajtár Mária 1. Háttér információk és definíciók Az emlőrák sebészi kezelése során az axillaris blockdissectióval eltávolított
A malignus melanóma prognosztikus és prediktív markerei
 Összefoglaló közlemény 79 A malignus melanóma prognosztikus és prediktív markerei Rásó Erzsébet, Barbai Tamás, Győrffy Balázs, Tímár József Semmelweis Egyetem, 2. Sz. Patológiai Intézet, MTA-SE Molekuláris
Összefoglaló közlemény 79 A malignus melanóma prognosztikus és prediktív markerei Rásó Erzsébet, Barbai Tamás, Győrffy Balázs, Tímár József Semmelweis Egyetem, 2. Sz. Patológiai Intézet, MTA-SE Molekuláris
Dr. Nemes Nagy Zsuzsa Szakképzés Karl Landsteiner Karl Landsteiner:
 Az AB0 vércsoport rendszer Dr. Nemes Nagy Zsuzsa Szakképzés 2011 Az AB0 rendszer felfedezése 1901. Karl Landsteiner Landsteiner szabály 1901 Karl Landsteiner: Munkatársai vérmintáit vizsgálva fedezte fel
Az AB0 vércsoport rendszer Dr. Nemes Nagy Zsuzsa Szakképzés 2011 Az AB0 rendszer felfedezése 1901. Karl Landsteiner Landsteiner szabály 1901 Karl Landsteiner: Munkatársai vérmintáit vizsgálva fedezte fel
ALK+ tüdőrák a klinikai gyakorlatban. Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest
 ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában
 Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése
 Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése Kegyes Lászlóné 1, Némethné Lesó Zita 1, Varga Sándor Attiláné 1, Barna T. Katalin 1, Rombauer Edit 2 Dunaújvárosi Prodia Központi
Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése Kegyes Lászlóné 1, Némethné Lesó Zita 1, Varga Sándor Attiláné 1, Barna T. Katalin 1, Rombauer Edit 2 Dunaújvárosi Prodia Központi
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
I./5. fejezet: Daganatok növekedése és terjedése
 I./5. fejezet: Daganatok növekedése és terjedése Tímár József A fejezet célja, hogy a hallgató megismerje a daganatok növekedésének és biológiai viselkedésének alapjait. A fejezet teljesítését követően
I./5. fejezet: Daganatok növekedése és terjedése Tímár József A fejezet célja, hogy a hallgató megismerje a daganatok növekedésének és biológiai viselkedésének alapjait. A fejezet teljesítését követően
Epithelioid lágyrészdaganatok differenciáldiagnosztikája
 DAKOCytomation Workshop Budapest Epithelioid lágyrészdaganatok differenciáldiagnosztikája dr. Orosz Zsolt 2008. december 05. Epithelioid sejttípus Resembling epithelium In a general sense, a cell that
DAKOCytomation Workshop Budapest Epithelioid lágyrészdaganatok differenciáldiagnosztikája dr. Orosz Zsolt 2008. december 05. Epithelioid sejttípus Resembling epithelium In a general sense, a cell that
A neurofibromatózis idegrendszeri megnyilvánulása
 A neurofibromatózis idegrendszeri megnyilvánulása Molekuláris Medicina Mindenkinek Fókuszban a Neurofibromatózis Varga Edina Tímea SE Genomikai Medicina és Ritka Betegségek Intézete Neurofibromatózis I.
A neurofibromatózis idegrendszeri megnyilvánulása Molekuláris Medicina Mindenkinek Fókuszban a Neurofibromatózis Varga Edina Tímea SE Genomikai Medicina és Ritka Betegségek Intézete Neurofibromatózis I.
A GI daganatok onkológiai kezelésének alapelvei. dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika
 A GI daganatok onkológiai kezelésének alapelvei dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika Onkológiai ellátás Jelentősége Elvei Szemléletváltás szükségessége Klinikai onkológia Kemoterápia kit,
A GI daganatok onkológiai kezelésének alapelvei dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika Onkológiai ellátás Jelentősége Elvei Szemléletváltás szükségessége Klinikai onkológia Kemoterápia kit,
Semmelweis Egyetem Doktori Iskola Onkológia program. Melanoma malignum progressziójának követése tumormarkerekkel
 Semmelweis Egyetem Doktori Iskola Onkológia program Melanoma malignum progressziójának követése tumormarkerekkel Doktori (Ph.D.) értekezés tézisei dr. Bánfalvi Teodóra Témavezető: Prof. Dr. Tímár József
Semmelweis Egyetem Doktori Iskola Onkológia program Melanoma malignum progressziójának követése tumormarkerekkel Doktori (Ph.D.) értekezés tézisei dr. Bánfalvi Teodóra Témavezető: Prof. Dr. Tímár József
Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása.
 Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása. Kerekasztal moderátor Péter Ilona Dako Workshop A Frank Diagnosztika Kft. és az Országos Onkológiai Intézet szervezésében
Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása. Kerekasztal moderátor Péter Ilona Dako Workshop A Frank Diagnosztika Kft. és az Országos Onkológiai Intézet szervezésében
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
a legérzékenyebb markerkombináció emlôdaganatoknál
 TPA és CA 15-3 a legérzékenyebb markerkombináció emlôdaganatoknál Bevezetés Az emlôrák a leggyakoribb rosszindulatú betegség nôknél. Elôfordulásának gyakorisága 100.000 személybôl átlagosan 60 eset (1)
TPA és CA 15-3 a legérzékenyebb markerkombináció emlôdaganatoknál Bevezetés Az emlôrák a leggyakoribb rosszindulatú betegség nôknél. Elôfordulásának gyakorisága 100.000 személybôl átlagosan 60 eset (1)
mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban
 mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban Sebestyén A, Márk Á, Nagy N, Hajdu M, Csóka M*, SticzT, Barna G, Nemes K*, Váradi Zs*, KopperL
mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban Sebestyén A, Márk Á, Nagy N, Hajdu M, Csóka M*, SticzT, Barna G, Nemes K*, Váradi Zs*, KopperL
Chapter 10 Hungarian Summary. Az onkológiai gyógyszerfejlesztés eredetileg DNS-károsodást indukáló vegyületekre
 10 Összefoglaló Összefoglaló Az onkológiai gyógyszerfejlesztés eredetileg DNS-károsodást indukáló vegyületekre összpontosított, melyek az osztódó rákos sejteket célozzák meg. Jelenleg, nagy hangsúly fektetődik
10 Összefoglaló Összefoglaló Az onkológiai gyógyszerfejlesztés eredetileg DNS-károsodást indukáló vegyületekre összpontosított, melyek az osztódó rákos sejteket célozzák meg. Jelenleg, nagy hangsúly fektetődik
CD8 pozitív primér bőr T-sejtes limfómák 14 eset kapcsán
 CD8 pozitív primér bőr T-sejtes limfómák 14 eset kapcsán Szepesi Ágota 1, Csomor Judit 1, Marschalkó Márta 2 Erős Nóra 2, Kárpáti Sarolta 2, Matolcsy András 1 Semmelweis Egyetem I. Patológiai és Kísérlet
CD8 pozitív primér bőr T-sejtes limfómák 14 eset kapcsán Szepesi Ágota 1, Csomor Judit 1, Marschalkó Márta 2 Erős Nóra 2, Kárpáti Sarolta 2, Matolcsy András 1 Semmelweis Egyetem I. Patológiai és Kísérlet
73. Patológus Kongresszus Siófok, szeptember Előzetes program
 2017. szeptember 28. csütörtök 09:00 10:30 Rezidens metszetszeminárium 73. Patológus Kongresszus 09:00 09:40 Prof.Dr. Kemény Éva: SZTE SZAKK Pathologiai Intézet, Szeged Glomerulonephritisek 09:40 10:20
2017. szeptember 28. csütörtök 09:00 10:30 Rezidens metszetszeminárium 73. Patológus Kongresszus 09:00 09:40 Prof.Dr. Kemény Éva: SZTE SZAKK Pathologiai Intézet, Szeged Glomerulonephritisek 09:40 10:20
OPPONENSI VÉLEMÉNY. Dr. Kulka Janina MTA doktori értekezéséről
 1 OPPONENSI VÉLEMÉNY Dr. Kulka Janina MTA doktori értekezéséről Az értekezés témaválasztása korszerű és megfelel a XXI. századi emlő onkológia elvárásainak. A patológusok szerepe az emlőrák kórismézésében
1 OPPONENSI VÉLEMÉNY Dr. Kulka Janina MTA doktori értekezéséről Az értekezés témaválasztása korszerű és megfelel a XXI. századi emlő onkológia elvárásainak. A patológusok szerepe az emlőrák kórismézésében
Válasz Dr. Balázs Margit, az MTA doktora bírálatára
 Válasz Dr. Balázs Margit, az MTA doktora bírálatára Mindenek előtt tisztelettel köszönöm Balázs Margit Professzor Asszonynak, hogy elvállalta doktori munkám opponensi feladatát, valamint az elért eredményeinkre
Válasz Dr. Balázs Margit, az MTA doktora bírálatára Mindenek előtt tisztelettel köszönöm Balázs Margit Professzor Asszonynak, hogy elvállalta doktori munkám opponensi feladatát, valamint az elért eredményeinkre
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
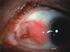
Intraocularis tumorok
 Intraocularis tumorok 25 évvel ezelőtt, ha egy szemben chorioidea melanomát találtunk, akkor a szemet enucleáltuk. Szemben lévő festékes daganat (melanoma chorioideae) Chorioidea melanoma miatt eltávolított,
Intraocularis tumorok 25 évvel ezelőtt, ha egy szemben chorioidea melanomát találtunk, akkor a szemet enucleáltuk. Szemben lévő festékes daganat (melanoma chorioideae) Chorioidea melanoma miatt eltávolított,
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
A fejezet felépítése. A.) Általános nevezéktan
 II./1.4. fejezet: Nevezéktan, stádiumbeosztás Torgyík László, Dank Magdolna A fejezet áttekintése során a hallgató megismerkedik az onkológiai kezelések során használatos kifejezések értemével és a TNM-osztályozás
II./1.4. fejezet: Nevezéktan, stádiumbeosztás Torgyík László, Dank Magdolna A fejezet áttekintése során a hallgató megismerkedik az onkológiai kezelések során használatos kifejezések értemével és a TNM-osztályozás
Melanomás betegek stádium szerinti megoszlása egy hazai centrumban
 EREDETI KÖZLEMÉNY Melanomás betegek stádium szerinti megoszlása egy hazai centrumban Tóth Veronika dr. Somlai Beáta dr. Hársing Judit dr. Hatvani Zsófia dr. Kárpáti Sarolta dr. Semmelweis Egyetem, Általános
EREDETI KÖZLEMÉNY Melanomás betegek stádium szerinti megoszlása egy hazai centrumban Tóth Veronika dr. Somlai Beáta dr. Hársing Judit dr. Hatvani Zsófia dr. Kárpáti Sarolta dr. Semmelweis Egyetem, Általános
DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI
 DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI MINTÁK DIAGNOSZTIKÁJÁBAN Doktori tézisek Ficsór Levente Semmelweis Egyetem, 2. sz. Belgyógyászati Klinika Klinikai Orvostudományok Doktori Iskola Programvezető:
DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI MINTÁK DIAGNOSZTIKÁJÁBAN Doktori tézisek Ficsór Levente Semmelweis Egyetem, 2. sz. Belgyógyászati Klinika Klinikai Orvostudományok Doktori Iskola Programvezető:
A patológiai vizsgálatok metodikája. 1. Biopsziástechnikák 2. Speciális vizsgálatok
 A patológiai vizsgálatok metodikája 1. Biopsziástechnikák 2. Speciális vizsgálatok Biopsziaindikációk Diffus/multifocalis eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges paraméterek
A patológiai vizsgálatok metodikája 1. Biopsziástechnikák 2. Speciális vizsgálatok Biopsziaindikációk Diffus/multifocalis eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges paraméterek
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK
 SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban. Doktori tézisek. Dr. Bogos Krisztina
 A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban Doktori tézisek Dr. Bogos Krisztina Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Pulmonológia program
A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban Doktori tézisek Dr. Bogos Krisztina Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Pulmonológia program
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
AZ ONKOLÓGIA HATÁRAI Válogatott fejezetek a klinikai onkológia és határterületei legaktuálisabb kérdéseiből TUDOMÁNYOS PROGRAM
 2015. október 15. (csütörtök) TUDOMÁNYOS PROGRAM 08.30 08.40 Köszöntő Prof. Dr. Mátyus László dékán DE Általános Orvostudományi Kar, Debrecen 08.40 08.45 Megnyitó, Bevezető Dr. Horváth Zsolt 08.45 11.00
2015. október 15. (csütörtök) TUDOMÁNYOS PROGRAM 08.30 08.40 Köszöntő Prof. Dr. Mátyus László dékán DE Általános Orvostudományi Kar, Debrecen 08.40 08.45 Megnyitó, Bevezető Dr. Horváth Zsolt 08.45 11.00
Túlélés elemzés október 27.
 Túlélés elemzés 2017. október 27. Néhány példa Egy adott betegség diagnózisától kezdve mennyi ideje van hátra a páciensnek? Tipikusan mennyi ideig élhet túl? Bizonyos ráktípus esetén mennyi idő telik el
Túlélés elemzés 2017. október 27. Néhány példa Egy adott betegség diagnózisától kezdve mennyi ideje van hátra a páciensnek? Tipikusan mennyi ideig élhet túl? Bizonyos ráktípus esetén mennyi idő telik el
"A genius is one per cent inspiration and ninety nine per cent perspiration." Thomas A. Edison
 "A genius is one per cent inspiration and ninety nine per cent perspiration." Thomas A. Edison Zorn-Keszthelyi Rita laborvezető Hisztopatológia Kft, Pécs www.histopat.hu Pécs, 2013. június 7. Alapítás
"A genius is one per cent inspiration and ninety nine per cent perspiration." Thomas A. Edison Zorn-Keszthelyi Rita laborvezető Hisztopatológia Kft, Pécs www.histopat.hu Pécs, 2013. június 7. Alapítás
NEM-VILÁGOSSEJTES VESERÁKOK
 NEM-VILÁGOSSEJTES VESERÁKOK SomoráczÁron SEMMELWEIS EGYETEM Általános Orvostudományi Kar 2. sz. Patológiai Intézet http://semmelweis.hu/patologia2 A vesesejtes daganatok osztályozása - WHO 2016 I. Új entitások
NEM-VILÁGOSSEJTES VESERÁKOK SomoráczÁron SEMMELWEIS EGYETEM Általános Orvostudományi Kar 2. sz. Patológiai Intézet http://semmelweis.hu/patologia2 A vesesejtes daganatok osztályozása - WHO 2016 I. Új entitások
Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Szövettan kérdései Ami a terápiát meghatározza és ami segíti Dr. Sápi Zoltán
 Szövettan kérdései Ami a terápiát meghatározza és ami segíti Dr. Sápi Zoltán 1.Számú Patológiai és Kísérleti Rákkutató Intézet Diagnózis (definitív): benignus, malignus, intermedier malignitás, borderline
Szövettan kérdései Ami a terápiát meghatározza és ami segíti Dr. Sápi Zoltán 1.Számú Patológiai és Kísérleti Rákkutató Intézet Diagnózis (definitív): benignus, malignus, intermedier malignitás, borderline
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén
 Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Sutton naevust utánzó melanoma. Sutton naevus like melanoma
 BÔRGYÓGYÁSZATI ÉS VENEROLÓGIAI SZEMLE 2016 92. ÉVF. 2. 76 80. DOI 10.7188/bvsz.2016.92.2.6 Sutton naevust utánzó melanoma Sutton naevus like melanoma DÓZSA ANIKÓ DR. 1, KÁROLYI ZSUZSÁNNA DR. 1, MÓROCZ
BÔRGYÓGYÁSZATI ÉS VENEROLÓGIAI SZEMLE 2016 92. ÉVF. 2. 76 80. DOI 10.7188/bvsz.2016.92.2.6 Sutton naevust utánzó melanoma Sutton naevus like melanoma DÓZSA ANIKÓ DR. 1, KÁROLYI ZSUZSÁNNA DR. 1, MÓROCZ
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet november 19., ÁOK, III.
 ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
A tüdő adenocarcinomák szubklasszifikációja. Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5.
 A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
A KRAS MUTÁCIÓJÁNAK HAZAI KÖRVIZSGÁLATA ( VALIDÁLÁSI VIZSGÁLAT) VASTAGBÉLRÁKBAN
 A KRAS MUTÁCIÓJÁNAK HAZAI KÖRVIZSGÁLATA ( VALIDÁLÁSI VIZSGÁLAT) VASTAGBÉLRÁKBAN Kopper László 1, Tímár József 2 1 Patológiai Szakmai Kollégium elnöke, Semmelweis Egyetem, I. sz. Patológiai és Kísérleti
A KRAS MUTÁCIÓJÁNAK HAZAI KÖRVIZSGÁLATA ( VALIDÁLÁSI VIZSGÁLAT) VASTAGBÉLRÁKBAN Kopper László 1, Tímár József 2 1 Patológiai Szakmai Kollégium elnöke, Semmelweis Egyetem, I. sz. Patológiai és Kísérleti
Immunológia alapjai előadás MHC. szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
Bevezetés. A fejezet felépítése
 II./3.8. fejezet: Szervátültetés kérdése daganatos betegségek esetén Langer Róbert, Végső Gyula, Horkay Ferenc, Fehérvári Imre A fejezet célja, hogy a hallgatók megismerkedjenek a szervátültetés és a daganatos
II./3.8. fejezet: Szervátültetés kérdése daganatos betegségek esetén Langer Róbert, Végső Gyula, Horkay Ferenc, Fehérvári Imre A fejezet célja, hogy a hallgatók megismerkedjenek a szervátültetés és a daganatos
Áramlási citometria 2011. / 4. Immunológiai és Biotechnológiai Intézet PTE KK
 Áramlási citometria 2011. / 4 Immunológiai és Biotechnológiai Intézet PTE KK Az áramlási citometria elve Az áramlási citometria ( Flow cytometria ) sejtek gyors, multiparaméteres vizsgálatára alkalmas
Áramlási citometria 2011. / 4 Immunológiai és Biotechnológiai Intézet PTE KK Az áramlási citometria elve Az áramlási citometria ( Flow cytometria ) sejtek gyors, multiparaméteres vizsgálatára alkalmas
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén
 Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Mit is csinál pontosan a patológus?
 Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
A pajzsmirigy benignus és malignus daganatai
 A pajzsmirigy benignus és malignus daganatai Dr. Boér András Országos Onkológiai Intézet 25 évesen az átlag népesség 10%-nak 70 évesen 55%-nak UH-gal van pajzsmirigy göbe, szoliter pajzsmirigygöb vagy
A pajzsmirigy benignus és malignus daganatai Dr. Boér András Országos Onkológiai Intézet 25 évesen az átlag népesség 10%-nak 70 évesen 55%-nak UH-gal van pajzsmirigy göbe, szoliter pajzsmirigygöb vagy
Vérszérum anyagcseretermékek jellemzése kezelés alatt lévő tüdőrákos betegekben
 http://link.springer.com/article/10.1007/s11306-016-0961-5 - Nyitott - Ingyenes Vérszérum anyagcseretermékek jellemzése kezelés alatt lévő tüdőrákos betegekben http://link.springer.com/article/10.1007/s11306-016-0961-5
http://link.springer.com/article/10.1007/s11306-016-0961-5 - Nyitott - Ingyenes Vérszérum anyagcseretermékek jellemzése kezelés alatt lévő tüdőrákos betegekben http://link.springer.com/article/10.1007/s11306-016-0961-5
Súlyos infekciók differenciálása a rendelőben. Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza
 Súlyos infekciók differenciálása a rendelőben Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza Miért probléma a lázas gyermek a rendelőben? nem beteg - súlyos beteg otthon ellátható
Súlyos infekciók differenciálása a rendelőben Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza Miért probléma a lázas gyermek a rendelőben? nem beteg - súlyos beteg otthon ellátható
KOPONYA-, ILLETVE SÚLYOS SÉRÜLTEK TRAUMÁHOZ KAPCSOLT KOAGULÓPÁTHIÁJÁNAK ÉS NEUROBIOMARKEREINEK VIZSGÁLATA. Vámos Zoltán, Ph.D.
 KOPONYA-, ILLETVE SÚLYOS SÉRÜLTEK TRAUMÁHOZ KAPCSOLT KOAGULÓPÁTHIÁJÁNAK ÉS NEUROBIOMARKEREINEK VIZSGÁLATA - Experimentális OxyológiaMunkacsoport kutatási együttműködésre történő felhívása - Vámos Zoltán,
KOPONYA-, ILLETVE SÚLYOS SÉRÜLTEK TRAUMÁHOZ KAPCSOLT KOAGULÓPÁTHIÁJÁNAK ÉS NEUROBIOMARKEREINEK VIZSGÁLATA - Experimentális OxyológiaMunkacsoport kutatási együttműködésre történő felhívása - Vámos Zoltán,
A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2.
 A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2. Vírusok szerepe a daganatok kialakulásában I/3. A környezet hatása a daganatok
A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2. Vírusok szerepe a daganatok kialakulásában I/3. A környezet hatása a daganatok
a hepatitis vírusok, elsősorban a hepatitis C vírus (HCV) okozta krónikus májbetegség egyes formái
 1. A kutatás célja a hepatitis vírusok, elsősorban a hepatitis C vírus (HCV) okozta krónikus májbetegség egyes formái kialakulásának és progressziójának a vizsgálata volt. A folyamatot a vírus sajátságainak,
1. A kutatás célja a hepatitis vírusok, elsősorban a hepatitis C vírus (HCV) okozta krónikus májbetegség egyes formái kialakulásának és progressziójának a vizsgálata volt. A folyamatot a vírus sajátságainak,
A melanoma malignum hisztopatológiai prognosztikus faktorai
 A melanoma malignum hisztopatológiai prognosztikus faktorai Összefoglaló Plótár Vanda 1, Orosz Zsolt 1, Tóth Erika 2, Szentirmay Zoltán 2 Országos Onkológiai Intézet, 1 Daganatpathologiai Osztály, 2 Molekuláris
A melanoma malignum hisztopatológiai prognosztikus faktorai Összefoglaló Plótár Vanda 1, Orosz Zsolt 1, Tóth Erika 2, Szentirmay Zoltán 2 Országos Onkológiai Intézet, 1 Daganatpathologiai Osztály, 2 Molekuláris
A malignus melanoma immundiagnosztikája
 malignus melanoma immundiagnosztikája Eredeti közlemény Szekeres György 1,3, attyáni Zita 1,2 1 Hisztopatológia KFT, Hisztopatológiai Laboratórium, Pécs, 2 Pécsi Tudományegyetem, Orvostudományi Centrum,
malignus melanoma immundiagnosztikája Eredeti közlemény Szekeres György 1,3, attyáni Zita 1,2 1 Hisztopatológia KFT, Hisztopatológiai Laboratórium, Pécs, 2 Pécsi Tudományegyetem, Orvostudományi Centrum,
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával
 Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
