KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 9. osztály B változat
|
|
|
- Márta Soósné
- 9 évvel ezelőtt
- Látták:
Átírás
1 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály B változat Beregszász 2005
2 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta : A kiadásért felel: Orosz Ildikó Felelıs szerkesztı: Gönczy Sándor A borítólapot tervezte: Gönczy Sándor Kiadja a Kárpátaljai Magyar Pedagógusszövetség Tankönyv- és Taneszköztanácsa Kárpátaljai Magyar Pedagógusszövetség Tankönyv- és Taneszköztanácsa Készült a Tankönyv- és Taneszköztanács sokszorosító mőhelyében A sokszorosítás Fábián Zoltán munkája 2
3 1. TEMATIKUS ÉRTÉKELÉS A periódusos törvény Jelöld a helyes válasz betőjelét! 1. Melyik betővel jelölt sorban vannak csak alkálifémek? A) Be, Mg, Ca, Ba; B) O, S, Se Te; C) C, Si, Ge, Sn; D) Li, Na, K, Rb; E) N, P, As, Sb. 2. Ki fogalmazta meg a periódusos törvényt? A) Demokritosz; B) Rutherford; C) Mengyelejev; D) Lomonoszov; E) Robert Boyle. 3. A kémiai elem rendszáma: A) az elektronok száma; B) a neutronok száma az atommagban; C) a protonok száma az atomm agban; D) a protonok és neutronok számának összege; E) a protonok, neutronok, elektronok számának összege. 4. Mely elemek tartoznak a III. csoport fıcsoportjába? A) Li, Na, K; B) Fe, Ru, Os; C) Cr, Mo, W; D) B, Al, Ga; E) C, Si, Ge. 5. Az atommagot alkotó részecskék: A) elektronok; B) neutronok; C) protonok és elektronok; D) protonok és neutronok; E) neutronok és elektronok. 6. A 8 rendszámú és 18 tömegszámú atom összetétele: A) 8 proton, 10 neutron, 10 elektron; B) 10 proton, 8 neutron, 18 elektron; C) 10 proton, 8 neutron, 10 elektron; D) 8 proton, 10 neutron, 8 elektron; E) 8 proton, 10 neutron, 18 elektron; 7. Rendszámuk alapján állapítsd meg az azonos csoportba tartozó elemeket: A) 8 és 25; B) 14 és 18; C) 20 és 23; D) 12 és 16; E) 4 és 48. 3
4 8. A 17 rendszámú elem legmagasabb oxidjának általános képlete: A) R 2 O 7 ; B) RO 3 ; C) R 2 O 5 ; D) RO 2 ; E) R 2 O Mely elemek kémiai tulajdonságai leginkább hasonlóak? A) B és Al; B) V és As; C) Na és K; D) C és N; E) Mg és Zn. 10. Melyik elem atommagja tartalmazhat 8 protont és 10 neutront? A) O; B) Ca; C) Cl; D) Mg; E) S. 11. Melyik elem illanó hidrogénvegyületének általános képlete RH 4? A) Br; B) Si; C) N; D) P; E) S. 12. Melyik kémiai elem amfoter jellegő? A) Na; B) Cl; C) Zn; D) C; E) N g tömegő két vegyértékő fém fölös mennyiségő vízzel vegyülve 5,6 l hidrogént fejleszt (n.k.k.). Melyik ez a fém? 14. Rendszámuk alapján állapítsd meg, melyik két elem legmagasabb oxidjának általános képlete RO Írd fel az oxidok képletét és nevét! A) 3 és 5; B) 7 és 15; C) 4 és 9; D) 6 és 14; E) 12 és Fejezd be a magreakció egyenletét! B+ n He+?
5 16. Írd fel az alábbi rendszámú kémiai elemek által alkotott egyszerő anyagok közötti kémiai reakció egyenletét, jelöld a reakció típusát és a keletkezett anyag nevét! A) 14 és 8; B) 1 és 9; C) 15 és Hány mol só keletkezik 10 g magnézium-oxid fölös mennyiségő salétromsavval való kölcsönhatásakor? 18. A kémiai elem a periódusos rendszer II csoportjának fıcsoportjában van, hidroxidjának relatív molekulatömege 74. Melyik ez az elem? 5
6 2. TEMATIKUS ÉRTÉKELÉS Kémiai kötés. Az anyag szerkezete Jelöld a helyes válasz betőjelét! 1. Ionos kötés jön létre: A) molekulák között; B) ionok között; C) különbözı atomok között; D) azonos atomok között; E) az atommag és az elektronburok között. 2. A gyémánt kristályrácsa: A) molekularács; B) ionrács; C) atomrács ; D) fémrács. 3. Az alkálifémek oxidációs száma vegyületeikben mindig: A) -2; B) -1; C) 0; D) +1; E) A nitrogén oxidációs száma melyik vegyületben +4? A) NH 3 ; B) NaNO 3 ; C) NO 2 ; D) Ca 3 N 2 ; E) N 2 O A redukció: A) elektronfelvétellel járó kémiai folyamat; B) elektronleadással járó kémiai folyamat; C) sem elektronleadással, sem elektronfelvétellel nem járó kémiai folyamat. 6. Milyen a kötéstípus a MgCl 2 képlető vegyületben? A) apoláris kovalens; B) poláris kovalens; C) ionos. 7. A nitrogén oxidációs száma melyik vegyületben a legalacsonyabb? A) N 2 O 3 ; B) NaNO 3 ; C) NH 3 ; D) NO 2 ; E) NO. 8. Melyik elektronhéj elektronjai alkotják a kémiai kötést a bróm molekulájában? A) 1; B) 2; C) 3; D) 4; E) 5. 6
7 9. Melyik anyag apoláris kovalens kötéső? A) NaCl; B) HBr; C) O 2 ; D) K 2 S; E) NH Melyik oxidáló-redukáló reakció egyenlete? A) LiOH+HCl=LiCl+H 2 O; B) BaCl 2 +Na 2 SO 4 =BaSO 4 +2NaCl; C) 3H 2 O+P 2 O 5 =2H 3 PO 4 ; D) Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ; E) Mg+2HCl=MgCl 2 +H Az elektronképletek közül melyik a Cl ion elektronképlete? A) 1s 2 2s 2 2p 6 3s 2 3p 6 ; B) 1s 2 2s 2 2p 6 3s 2 3p Az elem atomjának kettıvel több elektronja van, mint a kálium ionjának. Melyik az elem elektronképlete? A) 1s 2 2s 2 2p 6 3s 2 3p 6 ; B) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 ; C) 1s 2 2s 2 2p 6 3s 2 ; D) 1s 2 2s 2 2p 6 3s 2 3p 4 ; E) A) 1s 2 2s 2 2p Írd fel a 12 és 8 rendszámú elemek által alkotott egyszerő anyagok közötti kémiai reakció egyenletét! Milyen a keletkezett vegyület kötéstípusa? 14. Jelöld az elemek oxidációs számát a vegyületekben! ZnI 2, CrO 3, Cr 2 O 3, OsO 4, K 2 S, HPO 3, PbO, H 2, CCl 4, Na 2 CO Írd le egy-egy olyan vegyület képletét, amelyekben a nitrogénatom oxidációs száma rendre -3, +2, +5! 16. Fejezd be a reakcióegyenletet! Mi a redukálószer a reakció során? K+S 3 ponr 17. Hasonlítsd össze a Zn 2+ ion ës a Zn atom szerkezetét! 18. Az oxidáló-redukáló reakció során hány gramm vas-szulfid keletkezik 5,6 g tömegő vas fölös mennyiségő kénnel való kölcsönhatásakor? 7
8 3. TEMATIKUS ÉRTÉKELÉS Oldatok Jelöld a helyes válasz betőjelét! 1. Az oldatokra vonatkozóan melyik állítás nem igaz A) egynemő (homogén) rendszerek B) az oldószer általában folyadék C) az oldott anyag lehet gáz is D) az oldott anyagok mindig ionokra bomlanak E) lehetnek telítettek vagy telítetlenek 2. A gázok oldhatósága a hımérséklet csökkenésével: A növekszik; B) csökken; C) nem változik. 3. A vízben gyakorlatilag oldhatatlan: A) a mészkı; B) a cukor; C) a kénsav; D) az alkohol; E) a marónátron. 4. Az oldószer megtisztítható az oldott anyagoktól: A) ülepítéssel; B) szőréssel; C) lepárlással; D) bepárlással; E) a felsoroltak mindegyikével. 5. Melyik képlet kristályhidrát képlete? A) 5H 2 O; B) CO 2 ; C) BaO; D) HCl; E) Na 2 CO 3 10H 2 O. 6. Azok az anyagok, melyek vizes oldata vagy olvadéka nem vezeti az elektromos áramot: A) elektrolitok; B) anelektrolitok; C) kationok; D) anionok; E) a felsoroltak közül egyik sem g vízben feloldottak 15 g sót. Az oldott anyag tömegrésze az oldatban: A) 12%; B) 15%; C) 80%; D) 12,5%; E) 18,75%. 8
9 8. Mennyi a vízmentes só tömegrésze a rézgálicban, CuSO 4 5H 2 O: A) 50%; B) 54%; C) 60%; D) 64%; E)70%. 9. A kristályvíz tömege 15 g vasgálicban, FeSO 4 7H 2 O: A) 3,8 g; B) 5, 9 g; C) 6,8 g; D) 7,5 g; E) 8,3 g. 10. Melyik anyag oldhatósága növekszik a nyomás növelésével? A) a konyhasóé; B) a cukoré; C) a kálium-nitráté; D) az oxigéné; E) az alkoholé g oldatban, melyben a kénsav tömegrésze 60% az oldott anyag tömege: A) 150 g; B) 165 g; C) 180 g; D) 175 g; E) 190 g. 12. A legtöbb ion keletkezik az alábbi anyag disszociációjakor: A) CaCl 2 ; B) KNO 3 ; C) K 3 PO 4 ; D) BaCl 2 ; E) Na 2 SO Milyen anyagmennyiségő kálium-hidroxid és milyen térfogatú víz szükséges 500 g olyan oldat elkészítéséhez, melyben a KOH tömegrésze 2,8%? mol kálium-hidroxidot feloldottak 276 g vízben. Számítsd ki a KOH tömegrészét az oldatban mol anyagmennyiségő nátrium-hidroxidot feloldottak 480 g vízben. Számítsd ki a NaOH tömegrészét a keletkezett oldatban. 16. Számítsd ki a nátrium-szulfát tömegrészét a 32,2 g glaubersó, Na 2 SO 4 10H 2 O, 367,8 g vízben való oldásakor keletkezett oldatban. 17. Mekkora tömegő víz válik ki 34,4 g gipsz, CaSO 4 2H 2 O hevítésekor? 18. Fejezd be a reakcióegyenleteket, írd fel molekuláris és ionos formában! Jelöld melyik esetben megy végbe reakció. A) CaCl 2 +Na 2 CO 3 ; B) KCl+HNO 3. 9
10 4. TEMATIKUS ÉRTÉKELÉS Fémek (I) Jelöld a helyes válasz betőjelét! 1. A felsorolt kémiai elemek közül a fémekhez tartozik: A) bárium; B) kén; C) szén; D) nitrogén; E) bróm. 2. A természetben szabad állapotban elıforduló fém: A) Li; B) Cr; C) Pt; D)Al; E) Mn. 3. A felsorolt fémek közül a legalacsonyabb olvadáspontú: A) a kálium; B) a higany; C) a vas; D) a réz; E) a cink. 4. Az oxidtartalmú ércekhez tarozik: A) Fe 3 O 4 ; B) MgCl 2 ; C) MoS 2 ; D) FeCO 3 ; E) FeS Az elektrolízis folyamán a katód felé mozdulnak el: A) a kationok; B) az anionok; C) mindegyik ion; D) az elektronok; E) a felsoroltak egyike sem. 6. Melyik fém a legjobb elektromos vezetı: A) a réz; B) az alumínium; C) az ezüst; D) az ón; E) a vas. 7. Milyen anyag válik ki az anódon a NaCl olvadékának elektrolízisekor? A) nátrium; B) klór; C) víz; D) hidrogén; E) oxigén. 8. Melyik fém nem szorítja ki a hidrogént a savakból? A) cink; B) vas; C) magnézium; D) réz; E) alumínium. 9. Melyik esetben megy végbe kémiai reakció? A) Fe+ AlCl 3 ; B) Cu+FeSO 4 ; C) Zn+MgCl 2 ; D) Cu+AgNO 3 ; E) Hg+ CaCl 2 10
11 10. Szobahımérsékleten kiszorítja a hidrogént a vízbıl: A) az alumínium; B) a magnézium; C) a vas; D) a cink; E) a nátrium. 11. Melyik fém atomjának külsı elektronhéja 2s 1 elektronképlető? A) kálium; B) lítium; C) mangán; D) ezüst; E) bárium. 12. Nedvesség hatására a fémek korróziója: A) lelassul; B) fokozódik; C) nem változik. 13. Számítsd ki a 26 g cink kénsavval való kölcsönhatásakor keletkezı só tömegét! 14. Írd fel a réz szénnel való redukciójának egyenletét réz(ii)-oxidból! 15. Ahol lehet, fejezd be a reakcióegyenletet! A) Fe+MgSO 4 ; B) Mg+FeSO 4 ; C) Zn+HCl ; D) Zn+H 2 O ; E) Fe+H 2 SO 4. higított 16. Írd fel a réz(ii)-bromid vizes oldata elektrolízisének reakcióegyenletét és az elektródfolyamatok vázlatát! g alumínium-réz keverékre sósavval hatva 2,24 dm 3 normálállapotú hidrogént kaptak. Határozd meg a fémek tömegrészét a keverékben! 18. Határozd meg a 72 kg rézércbıl nyerhetı tiszta réz tömegét, melyben a réztartalmú ásvány, a kalkozin (Cu 2 S) tömegrésze 15%! 11
12 5. TEMATIKUS ÉRTÉKELÉS Fémek (II) Jelöld a helyes válasz betőjelét! 1. Melyik az alumínium elektronképlete? A) 1s 2 2s 2 2p 6 3s 2 3p 5 ; B) 1s 2 2s 2 2p 4 ; C) 1s 2 2s 2 2p 5 ; D) 1s 2 2s 2 2p 6 3s 2 3p 1 ; E) 1s 2 2s 2 2p 6 3s 2 3p 6 ; 2. A kalciumot elıállítják: A) a CaCl 2 hıbontásával; B) a mészkı hıbontásával; C) a CaCl 2 olvadékának elektrolízisével; D) a mész hıbontásával; E) a felsoroltaktól eltérı módon. 3. A gipsz képlete: A) CaSO 4 2H 2 O; B) CaSO 4 ; C) CaO; D) Ca(OH) 2 ; E) CaCO Az alumínium-hidroxid: A) bázisos tulajdonságú; B) savas tulajdonságú; C) amfoter tulajdonságú; 5. A fémoxidok alumíniummal való redukálásának módszere: A) eloxálás; B) pelletezés; C) fotolízis; D) aluminotermia; E) szilikotermia. 6. Melyik só vizes oldata lép reakcióba a vassal? A) BaCl 2 ; B) Ca(NO 3 ) 2 ; C) CuSO 4 ; D) NaCl; E) MgSO Melyik betővel jelzett sorban vannak csak a II. csoport fıcsoportjának elemei? A) Be, Na, Mg; B) Li, Na, K; C) Mg, Ca, Sr; D) B, Al, Ga; E) Na, K, Rb 8. A lítium-oxid és a kálium-hidroxid általános képlete: A) R 2 O és ROH; B) RO és R(OH) 2 ; C). R 2 O 3 és R(OH) 3. 12
13 9. Mennyi a rendszáma annak a kémiai elemnek, melynek atomjában a külsı héjon 1 elektron van? A) 12; B) 16; C) 20; D) 37; E) Melyik betővel jelzett sorban vannak csak bázisos oxidok? A) CaO, Li 2 O, CuO, FeO; B) Na 2 O, BaO, CO 2, Fe 2 O 3 ; C) Al 2 O 3, SO 2, SiO 2, MgO; D) Rb 2 O, FeO, SO 3, CuO; E) MgO, NO 2, Cl 2 O 7, P 2 O Vizes oldatban melyik só disszociál Ba 2+ ion keletkezésével? A) BaSO 4 ; B) BaCO 3 ; C) Ba 3 (PO 4 ) 2 ; D) BaCl 2 ; E) BaSiO Reakcióba lép a vassal az alábbi só vizes oldata: A) NaCl; B) AgNO 3 ; C) AlCl 3 ; D) Na 2 SO 4 ; E) BaCl Fejezzétek be a reakcióegyenleteket! A) Al+Fe 3 O 4 ; B) CaCO 3 ; C) NaOH+FeCl Mekkora térfogatú hidrogén válik ki (n.k.k.) 5 g kalcium fölös mennyiségő vízzel való kölcsönhatásakor? 15. A felsoroltak közül mely anyagok lépnek reakcióban a nátriumoxiddal? Írd fel a reakciók egyenletét! A) vas; B) víz; C) alumínium; D) kénsav; E) szén(ii)-oxid.. 13
14 16. Határozd meg 22,4 g vas anyagmennyiségét! 17. Mekkora tömegő oltott mész nyerhetı 140 g oltatlan mészbıl? 18. Számítsd ki a vas tömegrészarányát a piritben, FeS 2! 14
15 Tisztelt Kollégák! A feladatlapok az érvényben levı tanterv és N. M. Burinszka Kémia 9 tankönyvének magyar fordítása alapján lettek összeállítva a tanulók ismeteteinek értékelése céljából. Sajnos egyelıre nincs módunkban olyan feladatlapokat kiadni, amelyekbe a tanulók minden esetben beírhatják a válaszokat, mivel ezeket évenként újra kellene nyomtatni. Ez bizonyos mértékő kötöttséget jelentett a feladatlapok összeállításánál, azonban remélhetıleg így is segítséget jelent kiadványunk. Az 1 és ot érı feladatok teszt jellegőek, ezek megoldásánál használható a hátsó borítón bemutatott Válaszlap. A 3 pontot érı feladatokat írásban kell megoldani, a lehetıségek mértékében a megoldások számára megfelelı helyet biztosítottunk, tehát amennyiben megoldható a feladatlapok megfelelı számú sokszorosítása, akkor a tanulók beírhatják, jelölhetik a megoldásokat. Sokszorosítási lehetıség hiányában használható tetszıleges papírlap, a Válaszlapot is könnyen elkészíthetik a tanulók, vagy más módon jelölhetik a jó megoldásokat. Az elérhetı maximális pontszám mindig 36, ez a pontszám felel meg a 12-es osztályzatnak. Sikeres, eredményes munkát kívánva tisztelettel A szerkesztı 15
16 VÁLASZLAP Feladatlap száma: Változat: A tanuló neve Osztály A B C D E 16
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 9. osztály C változat
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály C változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály C változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 9. osztály A változat
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály A változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály A változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 9. osztály D változat
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály D változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 9. osztály D változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta A kiadásért felel: Orosz Ildikó Felelıs szerkesztı:
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS
 Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
KÉMIA. D változat TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 8. osztály
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály D változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály D változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor. Az ion képlete. Az ion neve O 4. Foszfátion. Szulfátion CO 3. Karbonátion. Hidrogénkarbonátion O 3. Alumíniumion. Al 3+ + Szulfidion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve Foszfátion Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve Foszfátion Szulfátion
KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont. HCl (1 pont) HCO 3 - (1 pont) Ca 2+ (1 pont) Al 3+ (1 pont) Fe 3+ (1 pont) H 2 O (1 pont)
 KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont 1. Adja meg a következő ionok nevét, illetve képletét! (12 pont) Az ion neve Kloridion Az ion képlete Cl - (1 pont) Hidroxidion (1 pont) OH - Nitrátion NO
KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont 1. Adja meg a következő ionok nevét, illetve képletét! (12 pont) Az ion neve Kloridion Az ion képlete Cl - (1 pont) Hidroxidion (1 pont) OH - Nitrátion NO
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
KÉMIA. C változat TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 8. osztály
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály C változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály C változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
1. feladat Összesen: 8 pont. 2. feladat Összesen: 11 pont. 3. feladat Összesen: 7 pont. 4. feladat Összesen: 14 pont
 1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
SZERVETLEN KÉMIAI REAKCIÓEGYENLETEK
 SZERVETLEN KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Zárójel jelzi a reakciót, ami más témakörnél található meg. REAKCIÓK FÉMEKKEL fém
SZERVETLEN KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Zárójel jelzi a reakciót, ami más témakörnél található meg. REAKCIÓK FÉMEKKEL fém
8. Osztály. Kód. Szent-Györgyi Albert kémiavetélkedő
 8. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
8. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
... Dátum:... (olvasható név)
 ... Dátum:... (olvasható név) (szak) Szervetlen kémia írásbeli vizsga A hallgató aláírása:. Pontok összesítése: I.. (10 pont) II/A. (10 pont) II/B. (5 pont) III.. (20 pont) IV.. (20 pont) V.. (5 pont)
... Dátum:... (olvasható név) (szak) Szervetlen kémia írásbeli vizsga A hallgató aláírása:. Pontok összesítése: I.. (10 pont) II/A. (10 pont) II/B. (5 pont) III.. (20 pont) IV.. (20 pont) V.. (5 pont)
29. Sztöchiometriai feladatok
 29. Sztöchiometriai feladatok 1 mól gáz térfogata normál állapotban (0 0 C, légköri nyomáson) 22,41 dm 3 1 mól gáz térfogata szobahőmérsékleten (20 0 C, légköri nyomáson) 24,0 dm 3 1 mól gáz térfogata
29. Sztöchiometriai feladatok 1 mól gáz térfogata normál állapotban (0 0 C, légköri nyomáson) 22,41 dm 3 1 mól gáz térfogata szobahőmérsékleten (20 0 C, légköri nyomáson) 24,0 dm 3 1 mól gáz térfogata
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Szent-Györgyi Albert kémiavetélkedő
 9. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
9. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján.
 A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
KÉMIA ÍRÁSBELI ÉRETTSÉGI FELVÉTELI FELADATOK 2004.
 KÉMIA ÍRÁSBELI ÉRETTSÉGI FELVÉTELI FELADATOK 2004. JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden megítélt
KÉMIA ÍRÁSBELI ÉRETTSÉGI FELVÉTELI FELADATOK 2004. JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden megítélt
Az anyagi rendszerek csoportosítása
 Kémia 1 A kémiai ismeretekről A modern technológiai folyamatok és a környezet védelmére tett intézkedések alig érthetőek kémiai tájékozottság nélkül. Ma már minden mérnök számára alapvető fontosságú a
Kémia 1 A kémiai ismeretekről A modern technológiai folyamatok és a környezet védelmére tett intézkedések alig érthetőek kémiai tájékozottság nélkül. Ma már minden mérnök számára alapvető fontosságú a
6. Melyik az az erős oxidáló- és vízelvonó szer, amely a szerves vegyületeket is roncsolja?
 10. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
10. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
Szent-Györgyi Albert kémiavetélkedő Kód
 Szent-Györgyi Albert kémiavetélkedő 11. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny
Szent-Györgyi Albert kémiavetélkedő 11. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny
2011/2012 tavaszi félév 3. óra
 2011/2012 tavaszi félév 3. óra Redoxegyenletek rendezése (diszproporció, szinproporció, stb.); Sztöchiometria Vegyületek sztöchiometriai együtthatóinak meghatározása elemösszetétel alapján Adott rendezendő
2011/2012 tavaszi félév 3. óra Redoxegyenletek rendezése (diszproporció, szinproporció, stb.); Sztöchiometria Vegyületek sztöchiometriai együtthatóinak meghatározása elemösszetétel alapján Adott rendezendő
Hevesy György Országos Kémiaverseny Kerületi forduló február évfolyam
 Hevesy György Országos Kémiaverseny Kerületi forduló 2013. február 20. 8. évfolyam A feladatlap megoldásához kizárólag periódusos rendszert és elektronikus adatok tárolására nem alkalmas zsebszámológép
Hevesy György Országos Kémiaverseny Kerületi forduló 2013. február 20. 8. évfolyam A feladatlap megoldásához kizárólag periódusos rendszert és elektronikus adatok tárolására nem alkalmas zsebszámológép
7. osztály Hevesy verseny, megyei forduló, 2003.
 Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
T I T M T T. Hevesy György Kémiaverseny. országos döntő. Az írásbeli forduló feladatlapja. 8. osztály
 T I T M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 8. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 8. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
3. feladat. Állapítsd meg az alábbi kénvegyületekben a kén oxidációs számát! Összesen 6 pont érhető el. Li2SO3 H2S SO3 S CaSO4 Na2S2O3
 10. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
10. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapa judeţeană 5 mai 2018 Ediţia a XIV-a. I Tétel pont
 CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapa judeţeană 5 mai 2018 Ediţia a XIV-a Munkaidő: 3 óra. A feladatok megoldásához használjátok az atomtömegek kerekített értékét a csatolmányban
CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapa judeţeană 5 mai 2018 Ediţia a XIV-a Munkaidő: 3 óra. A feladatok megoldásához használjátok az atomtömegek kerekített értékét a csatolmányban
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyz jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
1. feladat Összesen: 18 pont. 2. feladat Összesen: 9 pont
 1. feladat Összesen: 18 pont Különböző anyagok vízzel való kölcsönhatását vizsgáljuk. Töltse ki a táblázatot! második oszlopba írja, hogy oldódik-e vagy nem oldódik vízben az anyag, illetve ha reagál,
1. feladat Összesen: 18 pont Különböző anyagok vízzel való kölcsönhatását vizsgáljuk. Töltse ki a táblázatot! második oszlopba írja, hogy oldódik-e vagy nem oldódik vízben az anyag, illetve ha reagál,
T I T - M T T. Hevesy György Kémiaverseny. országos dönt. Az írásbeli forduló feladatlapja. 8. osztály. 2. feladat:... pont. 3. feladat:...
 T I T - M T T Hevesy György Kémiaverseny országos dönt Az írásbeli forduló feladatlapja 8. osztály A versenyz azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos dönt Az írásbeli forduló feladatlapja 8. osztály A versenyz azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
10. Osztály. Kód. Szent-Györgyi Albert kémiavetélkedő
 10. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
10. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
KÉMIA FELVÉTELI KÖVETELMÉNYEK
 KÉMIA FELVÉTELI KÖVETELMÉNYEK Atomszerkezettel kapcsolatos feladatok megoldása a periódusos rendszer segítségével, illetve megadott elemi részecskék alapján. Az atomszerkezet és a periódusos rendszer kapcsolata.
KÉMIA FELVÉTELI KÖVETELMÉNYEK Atomszerkezettel kapcsolatos feladatok megoldása a periódusos rendszer segítségével, illetve megadott elemi részecskék alapján. Az atomszerkezet és a periódusos rendszer kapcsolata.
1./ Jellemezd az anyagokat! Írd az A oszlop kipontozott helyére a B oszlopból arra az anyagra jellemző tulajdonságok számát! /10
 Név:.. Osztály.. 1./ Jellemezd az anyagokat! Írd az A oszlop kipontozott helyére a B oszlopból arra az anyagra jellemző tulajdonságok számát! /10 A B a) hidrogén... 1. sárga, szilárd anyag b) oxigén...
Név:.. Osztály.. 1./ Jellemezd az anyagokat! Írd az A oszlop kipontozott helyére a B oszlopból arra az anyagra jellemző tulajdonságok számát! /10 A B a) hidrogén... 1. sárga, szilárd anyag b) oxigén...
KÉMIA. B változat TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 8. osztály
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály B változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály B változat Beregszász 2005 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
a. 35-ös tömegszámú izotópjában 18 neutron található. b. A 3. elektronhéján két vegyértékelektront tartalmaz. c. 2 mól atomjának tömege 32 g.
 MAGYAR TANNYELVŰ KÖZÉPISKOLÁK IX. ORSZÁGOS VETÉLKEDŐJE AL IX.-LEA CONCURS PE ŢARĂ AL LICEELOR CU LIMBĂ DE PREDARE MAGHIARĂ FABINYI RUDOLF KÉMIA VERSENY - SZERVETLEN KÉMIA Marosvásárhely, Bolyai Farkas
MAGYAR TANNYELVŰ KÖZÉPISKOLÁK IX. ORSZÁGOS VETÉLKEDŐJE AL IX.-LEA CONCURS PE ŢARĂ AL LICEELOR CU LIMBĂ DE PREDARE MAGHIARĂ FABINYI RUDOLF KÉMIA VERSENY - SZERVETLEN KÉMIA Marosvásárhely, Bolyai Farkas
Az anyagi rendszerek csoportosítása
 Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
KÉMIA ÍRÁSBELI ÉRETTSÉGI-FELVÉTELI FELADATOK 2003.
 KÉMIA ÍRÁSBELI ÉRETTSÉGI-FELVÉTELI FELADATK 2003. JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden megítélt
KÉMIA ÍRÁSBELI ÉRETTSÉGI-FELVÉTELI FELADATK 2003. JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden megítélt
Javítóvizsga. Kalász László ÁMK - Izsó Miklós Általános Iskola Elérhető pont: 235 p
 Név: Elérhető pont: 5 p Dátum: Elért pont: Javítóvizsga A teszthez tollat használj! Figyelmesen olvasd el a feladatokat! Jó munkát.. Mi a neve az anyag alkotórészeinek? A. részecskék B. összetevők C. picurkák
Név: Elérhető pont: 5 p Dátum: Elért pont: Javítóvizsga A teszthez tollat használj! Figyelmesen olvasd el a feladatokat! Jó munkát.. Mi a neve az anyag alkotórészeinek? A. részecskék B. összetevők C. picurkák
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
A tudós neve: Mit tudsz róla:
 8. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
8. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
Minta vizsgalap I. Karikázza be az egyetlen megfelelő válasz betűjelét! (10x1 pont) 1. Melyik sorban szerepel csak só?
 Minta vizsgalap I. Karikázza be az egyetlen megfelelő válasz betűjelét! (10x) 1. Melyik sorban szerepel csak só? A) CH 3 COONa, K 2 SO 4, Na 3 PO 4, NH 4 Cl B) H 2 SO 4, Na 3 PO 4, NH 4 Cl, NaCl C) Fe(NO
Minta vizsgalap I. Karikázza be az egyetlen megfelelő válasz betűjelét! (10x) 1. Melyik sorban szerepel csak só? A) CH 3 COONa, K 2 SO 4, Na 3 PO 4, NH 4 Cl B) H 2 SO 4, Na 3 PO 4, NH 4 Cl, NaCl C) Fe(NO
KÖZSÉGI VERSENY KÉMIÁBÓL március 3.
 OKTATÁSI, TUDOMÁNYOS ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM, SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL 2018. március 3. TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA A tanuló jeligéje (három
OKTATÁSI, TUDOMÁNYOS ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM, SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL 2018. március 3. TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA A tanuló jeligéje (három
8. osztály 2 Hevesy verseny, megyei forduló, 2004.
 8. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
8. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek. fémek
 Kémiai kötések Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek fémek Fémek Szürke színűek, kivétel a színesfémek: arany,réz. Szilárd halmazállapotúak, kivétel a higany. Vezetik az
Kémiai kötések Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek fémek Fémek Szürke színűek, kivétel a színesfémek: arany,réz. Szilárd halmazállapotúak, kivétel a higany. Vezetik az
8. osztály 2 Hevesy verseny, megyei forduló, 2008.
 8. osztály 2 Hevesy verseny, megyei forduló, 2008. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
8. osztály 2 Hevesy verseny, megyei forduló, 2008. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
A SZERB KÖZTÁRSASÁG OKTATÁSI ÉS TUDOMÁNYÜGYI MINISZTÉRIUMA SZERB KÉMIKUSOK EGYESÜLETE. KÖZTÁRSASÁGI KÉMIAVERSENY (Varvarin, május 12.
 A SZERB KÖZTÁRSASÁG OKTATÁSI ÉS TUDOMÁNYÜGYI MINISZTÉRIUMA SZERB KÉMIKUSOK EGYESÜLETE KÖZTÁRSASÁGI KÉMIAVERSENY (Varvarin, 2012. május 12.) TUDÁSFELMÉRŐ FELADATLAP A VII. OSZTÁLY SZÁMÁRA A tanuló jeligéje:
A SZERB KÖZTÁRSASÁG OKTATÁSI ÉS TUDOMÁNYÜGYI MINISZTÉRIUMA SZERB KÉMIKUSOK EGYESÜLETE KÖZTÁRSASÁGI KÉMIAVERSENY (Varvarin, 2012. május 12.) TUDÁSFELMÉRŐ FELADATLAP A VII. OSZTÁLY SZÁMÁRA A tanuló jeligéje:
T I T - M T T. Hevesy György Kémiaverseny. országos döntő. Az írásbeli forduló feladatlapja. 7. osztály
 T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
ISMÉTLÉS, RENDSZEREZÉS
 ISMÉTLÉS, RENDSZEREZÉS A) változat 1. Egészítsd ki az ábrát a hiányzó anyagcsoportokkal és példákkal! ANYAGOK (összetétel szerint) egyszerű anyagok összetett anyagok......... oldat pl.... pl.... pl. levegő
ISMÉTLÉS, RENDSZEREZÉS A) változat 1. Egészítsd ki az ábrát a hiányzó anyagcsoportokkal és példákkal! ANYAGOK (összetétel szerint) egyszerű anyagok összetett anyagok......... oldat pl.... pl.... pl. levegő
Szent-Györgyi Albert kémiavetélkedő Kód
 9. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
9. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
KÉMIA. A változat TEMATIKUS ÉRTÉKELİ FELADATLAPOK. 8. osztály
 KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály A változat Beregszász 2005 1 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
KÉMIA TEMATIKUS ÉRTÉKELİ FELADATLAPOK 8. osztály A változat Beregszász 2005 1 A munkafüzet megjelenését a Magyar Köztársaság Oktatási Minisztériuma támogatta Véleményezte: Bak Éva A kiadásért felel: Orosz
Minta vizsgalap (2007/08. I. félév)
 Minta vizsgalap (2007/08. I. félév) I. Karikázza be az egyetlen megfelelő válasz betűjelét! (10x) 1. Melyik sorban szerepel csak só? A) CH 3 COONa, K 2 SO 4, Na 3 PO 4, NH 4 Cl B) H 2 SO 4, Na 3 PO 4,
Minta vizsgalap (2007/08. I. félév) I. Karikázza be az egyetlen megfelelő válasz betűjelét! (10x) 1. Melyik sorban szerepel csak só? A) CH 3 COONa, K 2 SO 4, Na 3 PO 4, NH 4 Cl B) H 2 SO 4, Na 3 PO 4,
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2000
 Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
1. feladat Összesen: 10 pont. 2. feladat Összesen: 14 pont
 1. feladat Összesen: 10 pont Az AsH 3 hevítés hatására arzénre és hidrogénre bomlik. Hány dm 3 18 ºC hőmérsékletű és 1,01 10 5 Pa nyomású AsH 3 -ből nyerhetünk 10 dm 3 40 ºC hőmérsékletű és 2,02 10 5 Pa
1. feladat Összesen: 10 pont Az AsH 3 hevítés hatására arzénre és hidrogénre bomlik. Hány dm 3 18 ºC hőmérsékletű és 1,01 10 5 Pa nyomású AsH 3 -ből nyerhetünk 10 dm 3 40 ºC hőmérsékletű és 2,02 10 5 Pa
Kémiai reakciók Műszaki kémia, Anyagtan I. 11. előadás
 Kémiai reakciók Műszaki kémia, Anyagtan I. 11. előadás Dolgosné dr. Kovács Anita egy.doc. PTE MIK Környezetmérnöki Tanszék Kémiai reakció Kémiai reakció: különböző anyagok kémiai összetételének, ill. szerkezetének
Kémiai reakciók Műszaki kémia, Anyagtan I. 11. előadás Dolgosné dr. Kovács Anita egy.doc. PTE MIK Környezetmérnöki Tanszék Kémiai reakció Kémiai reakció: különböző anyagok kémiai összetételének, ill. szerkezetének
Az 2008/2009. tanévi ORSZÁGOS KÖZÉPISKOLAI TANULMÁNYI VERSENY első (iskolai) fordulójának. feladatmegoldásai K É M I Á B Ó L
 ktatási Hivatal Az 2008/2009. tanévi RSZÁGS KÖZÉPISKLAI TANULMÁNYI VERSENY első (iskolai) fordulójának feladatmegoldásai K É M I Á B Ó L Az értékelés szempontjai Egy-egy feladat összes pontszáma a részpontokból
ktatási Hivatal Az 2008/2009. tanévi RSZÁGS KÖZÉPISKLAI TANULMÁNYI VERSENY első (iskolai) fordulójának feladatmegoldásai K É M I Á B Ó L Az értékelés szempontjai Egy-egy feladat összes pontszáma a részpontokból
Facultatea de Chimie și Inginerie Chimică, Universitatea Babeș-Bolyai Admitere 2015
 1. Az energiaszintek elektronokkal való feltöltésére vonatkozó kijelentések közül melyik igaz? A. A 3. héj maximum 8 elektront tartalmazhat. B. A 3d alhéj elektronokkal való feltöltése a 4s alhéj előtt
1. Az energiaszintek elektronokkal való feltöltésére vonatkozó kijelentések közül melyik igaz? A. A 3. héj maximum 8 elektront tartalmazhat. B. A 3d alhéj elektronokkal való feltöltése a 4s alhéj előtt
Általános és szervetlen kémia 1. hét
 Általános és szervetlen kémia 1. hét A tantárgy elméleti és gyakorlati anyaga http://cheminst.emk.nyme.hu A CAPA teszt-gyakorló program használata Kliens programot letölteni a weboldalról Bejelentkezés
Általános és szervetlen kémia 1. hét A tantárgy elméleti és gyakorlati anyaga http://cheminst.emk.nyme.hu A CAPA teszt-gyakorló program használata Kliens programot letölteni a weboldalról Bejelentkezés
ALPHA spektroszkópiai (ICP és AA) standard oldatok
 Jelen kiadvány megjelenése után történõ termékváltozásokról, új standardokról a katalógus internetes oldalán, a www.laboreszközkatalogus.hu-n tájékozódhat. ALPHA Az alábbi standard oldatok fémek, fém-sók
Jelen kiadvány megjelenése után történõ termékváltozásokról, új standardokról a katalógus internetes oldalán, a www.laboreszközkatalogus.hu-n tájékozódhat. ALPHA Az alábbi standard oldatok fémek, fém-sók
Általános és szervetlen kémia Laborelıkészítı elıadás VI
 Általános és szervetlen kémia Laborelıkészítı elıadás VI Redoxiegyenletek rendezésének általános lépései Példák fémoldódási egyenletek rendezésére Halogénvegyületek reakciói A gyakorlaton vizsgált redoxireakciók
Általános és szervetlen kémia Laborelıkészítı elıadás VI Redoxiegyenletek rendezésének általános lépései Példák fémoldódási egyenletek rendezésére Halogénvegyületek reakciói A gyakorlaton vizsgált redoxireakciók
7. osztály 2 Hevesy verseny, országos döntő, 2004.
 7. osztály 2 Hevesy verseny, országos döntő, 2004. Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő tíz feladat megoldására 90 perc áll rendelkezésedre.
7. osztály 2 Hevesy verseny, országos döntő, 2004. Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő tíz feladat megoldására 90 perc áll rendelkezésedre.
Hevesy verseny döntő, 2001.
 7. osztály 2 Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő kilenc feladat megoldására 90 perc áll rendelkezésedre. A feladatokat a számítási
7. osztály 2 Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő kilenc feladat megoldására 90 perc áll rendelkezésedre. A feladatokat a számítási
T I T - M T T. Hevesy György Kémiaverseny. országos döntő. Az írásbeli forduló feladatlapja. 7. osztály. 2. feladat:... pont. 3. feladat:...
 T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
Gyakorló feladatok. Egyenletrendezés az oxidációs számok segítségével
 Gyakorló feladatok Egyenletrendezés az oxidációs számok segítségével 1. Határozzuk meg az alábbi anyagokban a nitrogén oxidációs számát! a/ NH 3 b/ NO c/ N 2 d/ NO 2 e/ NH 4 f/ N 2O 3 g/ N 2O 4 h/ HNO
Gyakorló feladatok Egyenletrendezés az oxidációs számok segítségével 1. Határozzuk meg az alábbi anyagokban a nitrogén oxidációs számát! a/ NH 3 b/ NO c/ N 2 d/ NO 2 e/ NH 4 f/ N 2O 3 g/ N 2O 4 h/ HNO
NE FELEJTSÉTEK EL BEÍRNI AZ EREDMÉNYEKET A KIJELÖLT HELYEKRE! A feladatok megoldásához szükséges kerekített értékek a következők:
 A Szerb Köztársaság Oktatási Minisztériuma Szerbiai Kémikusok Egyesülete Köztársasági verseny kémiából Kragujevac, 2008. 05. 24.. Teszt a középiskolák I. osztálya számára Név és utónév Helység és iskola
A Szerb Köztársaság Oktatási Minisztériuma Szerbiai Kémikusok Egyesülete Köztársasági verseny kémiából Kragujevac, 2008. 05. 24.. Teszt a középiskolák I. osztálya számára Név és utónév Helység és iskola
Csermák Mihály: Kémia 8. Panoráma sorozat
 Csermák Mihály: Kémia 8. Panoráma sorozat Kedves Kollégák! A Panoráma sorozat kiadványainak megalkotása során két fő szempontot tartottunk szem előtt. Egyrészt olyan tankönyvet szerettünk volna létrehozni,
Csermák Mihály: Kémia 8. Panoráma sorozat Kedves Kollégák! A Panoráma sorozat kiadványainak megalkotása során két fő szempontot tartottunk szem előtt. Egyrészt olyan tankönyvet szerettünk volna létrehozni,
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam
 A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam A feladatok megoldásához csak
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam A feladatok megoldásához csak
Első alkalomra ajánlott gyakorlópéldák. Második alkalomra ajánlott gyakorlópéldák. Harmadik alkalomra ajánlott gyakorlópéldák
 Első alkalomra ajánlott gyakorlópéldák 1. Rajzolja fel az alábbi elemek alapállapotú atomjainak elektronkonfigurációját, és szaggatott vonallal jelölje az atomtörzs és a vegyértékhéj határát! Készítsen
Első alkalomra ajánlott gyakorlópéldák 1. Rajzolja fel az alábbi elemek alapállapotú atomjainak elektronkonfigurációját, és szaggatott vonallal jelölje az atomtörzs és a vegyértékhéj határát! Készítsen
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1999
 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1999 JAVÍTÁSI ÚTMUTATÓ I. HALOGÉNTARTALMÚ SZÉNVEGYÜLETEK A szénhidrogén és a halogén nevének összekapcsolásával Pl. CH 3 Cl metil-klorid, klór-metán
1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1999 JAVÍTÁSI ÚTMUTATÓ I. HALOGÉNTARTALMÚ SZÉNVEGYÜLETEK A szénhidrogén és a halogén nevének összekapcsolásával Pl. CH 3 Cl metil-klorid, klór-metán
Az elemek periódusos rendszere (kerekített relatív atomtömegekkel)
 Kedves versenyző! A kémia feladatsor megoldására 60 perc áll rendelkezésedre. Nem kell arra törekedned, hogy ennyi idő alatt minden feladatot megoldj, az a fontos, hogy minél több pontot szerezz! A feladatok
Kedves versenyző! A kémia feladatsor megoldására 60 perc áll rendelkezésedre. Nem kell arra törekedned, hogy ennyi idő alatt minden feladatot megoldj, az a fontos, hogy minél több pontot szerezz! A feladatok
T I T M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Sav bázis egyensúlyok vizes oldatban
 Sav bázis egyensúlyok vizes oldatban Disszociációs egyensúlyi állandó HAc H + + Ac - ecetsav disszociációja [H + ] [Ac - ] K sav = [HAc] NH 4 OH NH 4 + + OH - [NH + 4 ] [OH - ] K bázis = [ NH 4 OH] Ammóniumhidroxid
Sav bázis egyensúlyok vizes oldatban Disszociációs egyensúlyi állandó HAc H + + Ac - ecetsav disszociációja [H + ] [Ac - ] K sav = [HAc] NH 4 OH NH 4 + + OH - [NH + 4 ] [OH - ] K bázis = [ NH 4 OH] Ammóniumhidroxid
A 2007/2008. tanévi. Országos Középiskolai Tanulmányi Verseny. első (iskolai) fordulójának. javítási-értékelési útmutatója
 Oktatási Hivatal A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) fordulójának javítási-értékelési útmutatója KÉMIÁBÓL I-II. kategóriában Az 2007/2008. tanévi ORSZÁGOS KÖZÉPISKOLAI
Oktatási Hivatal A 2007/2008. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) fordulójának javítási-értékelési útmutatója KÉMIÁBÓL I-II. kategóriában Az 2007/2008. tanévi ORSZÁGOS KÖZÉPISKOLAI
Összesen: 20 pont. 1,120 mol gázelegy anyagmennyisége: 0,560 mol H 2 és 0,560 mol Cl 2 tömege: 1,120 g 39,76 g (2)
 I. FELADATSOR (KÖZÖS) 1. B 6. C 11. D 16. A 2. B 7. E 12. C 17. E 3. A 8. A 13. D 18. C 4. E 9. A 14. B 19. B 5. B (E is) 10. C 15. C 20. D 20 pont II. FELADATSOR 1. feladat (közös) 1,120 mol gázelegy
I. FELADATSOR (KÖZÖS) 1. B 6. C 11. D 16. A 2. B 7. E 12. C 17. E 3. A 8. A 13. D 18. C 4. E 9. A 14. B 19. B 5. B (E is) 10. C 15. C 20. D 20 pont II. FELADATSOR 1. feladat (közös) 1,120 mol gázelegy
Jegyzet. Kémia, BMEVEAAAMM1 Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens.
 Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
O k t a t á si Hivatal
 O k t a t á si Hivatal I. FELADATSOR 2013/2014. tanévi Országos Középiskolai Tanulmányi Verseny második forduló KÉMIA II. KATEGÓRIA Javítási-értékelési útmutató A következő kérdésekre az egyetlen helyes
O k t a t á si Hivatal I. FELADATSOR 2013/2014. tanévi Országos Középiskolai Tanulmányi Verseny második forduló KÉMIA II. KATEGÓRIA Javítási-értékelési útmutató A következő kérdésekre az egyetlen helyes
Kémia OKTV 2006/2007. II. forduló. A feladatok megoldása
 Kémia OKTV 2006/2007. II. forduló A feladatok megoldása Az értékelés szempontjai Csak a hibátlan megoldásokért adható a teljes pontszám. Részlegesen jó megoldásokat a részpontok alapján kell pontozni.
Kémia OKTV 2006/2007. II. forduló A feladatok megoldása Az értékelés szempontjai Csak a hibátlan megoldásokért adható a teljes pontszám. Részlegesen jó megoldásokat a részpontok alapján kell pontozni.
RIEŠENIE A HODNOTENIE TEORETICKÝCH ÚLOH Chemická olympiáda kategória Dz 49. ročník šk. rok 2012/13 Obvodné kolo
 RIEŠENIE A HODNOTENIE TEORETICKÝCH ÚLOH Chemická olympiáda kategória Dz 49. ročník šk. rok 2012/13 Obvodné kolo Helena Vicenová Maximális pontszám 60 pont A megoldás ideje: 60 perc 1. feladat megoldása
RIEŠENIE A HODNOTENIE TEORETICKÝCH ÚLOH Chemická olympiáda kategória Dz 49. ročník šk. rok 2012/13 Obvodné kolo Helena Vicenová Maximális pontszám 60 pont A megoldás ideje: 60 perc 1. feladat megoldása
T I T - M T T. Hevesy György Kémiaverseny. országos döntı. Az írásbeli forduló feladatlapja. 7. osztály
 T I T - M T T Hevesy György Kémiaverseny országos döntı Az írásbeli forduló feladatlapja 7. osztály A versenyzı azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos döntı Az írásbeli forduló feladatlapja 7. osztály A versenyzı azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Kémia középszint 0513 ÉRETTSÉGI VIZSGA 2005. május 18. KÉMIA KÖZÉPSZINTŰ ÉRETTSÉGI VIZSGA Az írásbeli vizsga időtartama: 120 perc JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ OKTATÁSI MINISZTÉRIUM Az írásbeli feladatok
Kémia középszint 0513 ÉRETTSÉGI VIZSGA 2005. május 18. KÉMIA KÖZÉPSZINTŰ ÉRETTSÉGI VIZSGA Az írásbeli vizsga időtartama: 120 perc JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ OKTATÁSI MINISZTÉRIUM Az írásbeli feladatok
KÖZSÉGI VERSENY KÉMIÁBÓL (2016. március 5.)
 SZERB KÖZTÁRSASÁG OKTATÁSI, TUDOMÁNYÜGYI ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL (2016. március 5.) TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA
SZERB KÖZTÁRSASÁG OKTATÁSI, TUDOMÁNYÜGYI ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL (2016. március 5.) TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA
Elektrokémia. A nemesfém elemek és egymással képzett vegyületeik
 Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY
 MAGYAR TERMÉSZETTUDOMÁNYI TÁRSULAT HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY A megyei (fővárosi) forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:...
MAGYAR TERMÉSZETTUDOMÁNYI TÁRSULAT HEVESY GYÖRGY ORSZÁGOS KÉMIAVERSENY A megyei (fővárosi) forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:...
Nátrium és Kalcium részösszefoglaló feladatlap
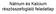 Nátrium és Kalcium részösszefoglaló feladatlap 1. Írd le a következő elemek és vegyületek kémiai nevét: 1.NaOH, 2.Ca, 3.Mg, 4.CaCO 3, 5.NaCl, 6.Na 2 CO 3 7.CaSO 4, 8.Ca(OH) 2, 9.CaO, 10CO 2, 11.HCl, 12.Na,
Nátrium és Kalcium részösszefoglaló feladatlap 1. Írd le a következő elemek és vegyületek kémiai nevét: 1.NaOH, 2.Ca, 3.Mg, 4.CaCO 3, 5.NaCl, 6.Na 2 CO 3 7.CaSO 4, 8.Ca(OH) 2, 9.CaO, 10CO 2, 11.HCl, 12.Na,
7. Kémia egyenletek rendezése, sztöchiometria
 7. Kémia egyenletek rendezése, sztöchiometria A kémiai egyenletírás szabályai (ajánlott irodalom: Villányi Attila: Ötösöm lesz kémiából, Példatár) 1.tömegmegmaradás, elemek átalakíthatatlansága az egyenlet
7. Kémia egyenletek rendezése, sztöchiometria A kémiai egyenletírás szabályai (ajánlott irodalom: Villányi Attila: Ötösöm lesz kémiából, Példatár) 1.tömegmegmaradás, elemek átalakíthatatlansága az egyenlet
Javítókulcs (Kémia emelt szintű feladatsor)
 Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. C 2. B. fenolos hidroxilcsoport, éter, tercier amin db. ; 2 db. 4. észter 5. E 6. A tercier amino-nitrogén. 7. Pl. a trimetil-amin reakciója HCl-dal.
Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. C 2. B. fenolos hidroxilcsoport, éter, tercier amin db. ; 2 db. 4. észter 5. E 6. A tercier amino-nitrogén. 7. Pl. a trimetil-amin reakciója HCl-dal.
2. csoport: Alkáliföldfémek
 2. csoport: Alkáliföldfémek Be: első előállítás F. Wöhler és A. B. Bussynak 1828, (előtte berill ásvány ism.) Mg, Ca, Sr, Ba első előállítása: Davy 1808 Ra felfedezése: Pierre és Marie Curie 1911 Az alkáliföldfémek
2. csoport: Alkáliföldfémek Be: első előállítás F. Wöhler és A. B. Bussynak 1828, (előtte berill ásvány ism.) Mg, Ca, Sr, Ba első előállítása: Davy 1808 Ra felfedezése: Pierre és Marie Curie 1911 Az alkáliföldfémek
Kémiai reakciók. Közös elektronpár létrehozása. Általános és szervetlen kémia 10. hét. Elızı héten elsajátítottuk, hogy.
 Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
1. feladat Összesen: 10 pont. 2. feladat Összesen: 11 pont
 1. feladat Összesen: 10 pont Egészítse ki a két elemre vonatkozó táblázatot! A elem B elem Alapállapotú atomjának vegyértékelektron-szerkezete: 5s 2 5p 5 5s 2 4d 5 Párosítatlan elektronjainak száma: Lezárt
1. feladat Összesen: 10 pont Egészítse ki a két elemre vonatkozó táblázatot! A elem B elem Alapállapotú atomjának vegyértékelektron-szerkezete: 5s 2 5p 5 5s 2 4d 5 Párosítatlan elektronjainak száma: Lezárt
0 1 2 3 4 5 6 7 8 9 0 E C D C E B B A E 1 A C D B B D D A A D 2 C E D A B C B C C E 3 C C B B E
 XII. FÉMEK XII. 1. FELELETVÁLASZTÁSOS TESZTEK 0 1 2 4 5 6 7 8 9 0 E C D C E B B A E 1 A C D B B D D A A D 2 C E D A B C B C C E C C B B E XII. 2. TÁBLÁZATKIEGÉSZÍTÉS Fémek összehasonlítása Kalcium Vas
XII. FÉMEK XII. 1. FELELETVÁLASZTÁSOS TESZTEK 0 1 2 4 5 6 7 8 9 0 E C D C E B B A E 1 A C D B B D D A A D 2 C E D A B C B C C E C C B B E XII. 2. TÁBLÁZATKIEGÉSZÍTÉS Fémek összehasonlítása Kalcium Vas
MINŐSÉGI KÉMIAI ANALÍZIS
 MINŐSÉGI KÉMIAI ANALÍZIS A minőségi analízis célja és feladata ismeretlen anyagok vegyületek, keverékek, ötvözetek, stb. összetételének meghatározása, annak megállapítása, hogy a különféle anyagok milyen
MINŐSÉGI KÉMIAI ANALÍZIS A minőségi analízis célja és feladata ismeretlen anyagok vegyületek, keverékek, ötvözetek, stb. összetételének meghatározása, annak megállapítása, hogy a különféle anyagok milyen
A tételek: Elméleti témakörök. Általános kémia
 A tételek: Elméleti témakörök Általános kémia 1. Az atomok szerkezete az atom alkotórészei, az elemi részecskék és jellemzésük a rendszám és a tömegszám, az izotópok, példával az elektronszerkezet kiépülésének
A tételek: Elméleti témakörök Általános kémia 1. Az atomok szerkezete az atom alkotórészei, az elemi részecskék és jellemzésük a rendszám és a tömegszám, az izotópok, példával az elektronszerkezet kiépülésének
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 9. évfolyam
 A feladatokat írta: Kódszám: Pócsiné Erdei Irén, Debrecen... Lektorálta: Kálnay Istvánné, Nyíregyháza 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 9. évfolyam A feladatok megoldásához
A feladatokat írta: Kódszám: Pócsiné Erdei Irén, Debrecen... Lektorálta: Kálnay Istvánné, Nyíregyháza 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 9. évfolyam A feladatok megoldásához
