2. Az atomelmélet alapjai, a periódusos rendszer
|
|
|
- Géza Fazekas
- 7 évvel ezelőtt
- Látták:
Átírás
1 . Az atomelmélet alapjai, a periódusos rendszer A világ nagyon összetett, sok szinten lehet tanulmányozni (az emberi méretektıl elindulva, kisebb részek felé haladva), rengeteg anyag van! Az anyagot felépítı elemi részecskék száma csak 3! Hogyan lesz ilyen változatos az anyag? Az anyagok rendkívüli változatossága mindössze mintegy 100 különbözı atomra vezethetı vissza, azok néhány elemi részecskére... Ennek megismerése igen hosszú folyamat volt. RÉGEN nem tudtak ennyit az anyagról. Hogyan alakult ki a modern kémia? Lavoisier ( ): tömegmegmaradás törvénye égéseket vizsgált, az égés után megmaradt anyag tömege megegyezett az azt megelızıvel Proust ( ): állandó súlyviszonyok törvénye (1799) a réz-karbonát ugyanakkora tömegszázalék rezet tartalmazott függetlenül attól, hogy milyen természetes forrásból származott vagy állította elı Adott vegyületben, az bárhonnan származik is, bármilyen módon állították elı, az alkotóelemek súlyaránya szigorúan állandó, és jellemzı az adott vegyületre. Dalton atomelmélete ( ) 1. Minden kémiai elem kis, oszthatatlan részekbıl, ún. atomokból áll. Kémiai változások során atomok nem hozhatók létre és nem pusztíthatók el.. Egy elem atomjainak tömege (súlya) és más tulajdonságai megegyeznek, de a különbözı elemek atomjainak tulajdonságai eltérnek. 3. A vegyületeket különbözı elemek atomjai kis egész számok arányában alkotják. 1.-> tömegmegmaradás., 3. -> állandó súlyviszonyok törvénye Dalton: többszörös súlyviszonyok törvénye (1805)., 3. -> ha két elem egynél több vegyületet képes, akkor vegyülı elemek tömegének arány kis egész szám (fólia) Gay-Lussac: vegyülı gázok térfogati törvényei (1808) gázreakciókban az egymással vegyülı és keletkezı gázok térfogatai azonos nyomáson és hımérsékleten úgy aránylanak egymáshoz, mint kis egész számok az Avogadro-tétel azonos hımérséklető és nyomású gázok egyenlı térfogataiban azonos a molekulák száma következmények: - molekulák egymáshoz viszonyított tömegei (mai szóval a relatív molekulatömegek) meghatározhatók. Oxigén legyen 3,00 egység, a többi ebbıl származik. - gázok moláris térfogata azonos hımérsékleten és nyomáson egyenlı - relatív atomtömegek meghatározása (fólia) A periódusos rendszer létrejötte, Mengyelejev jelentısége A XIX. század elején még nem ismerték az elemi részecskéket, de az egyes elemek hasonlóságát már látták: Johann Wolfgang Döbereiner (188) triádok: hasonló elemekbıl álló hármasok, amelyben az egyik elem atomtömege a másik kettıének kb. a számtani közepe elem atomtömeg / (g/mol) elem atomtömeg / (g/mol) klór 35,45 kalcium 40,08 bróm 79,90 stroncium 87,6 jód 16,90 bárium 137, számos tudós dolgozott a területen (Jean Baptiste Dumas, Leopold Gmelin, Ernst Lenssen, Max von Pettenkofer, J.P. Cooke) és azt találták, hogy a fentieken túlmutató összefüggések vannak az egyese elemek tulajdonságai között. A fluort hozzátették a halogének csoportjához, az oxigént, ként, szelént és tellúrt, illetve a nitrogént, foszfort, arzént, antimont és bizmutot egy-egy csoportba sorolták.
2 John Newlands angol kémikus 1865-ben észrevette, hogy ha az elemeket növekvı atomtömeg szerint sorrendbe állítja, minden nyolcadik hasonló fizikai és kémiai sajátosságokat mutat, amit a zenei oktávokhoz hasonlított. Bár sok elem esetén jól mőködött, több probléma is volt vele: -A kalciumnál nagyobb atomtömegő elemekre nem volt igaz - Miután több elemet (például a héliumot, neont, argont) felfedeztek, az új elemek nem fértek bele a táblázatba Lothar Meyer (német), Dmitrij Mengyelejev (orosz) kémikusok kb. ugyanabban az idıben ( körül) egymástól függetlenül hasonló eredményre jutottak. Az elemeket táblázatba helyezték növekvı atomtömegük szerint. Mengyelejev néhány elemet (17-et az akkor ismert 63-ból!) a sorrendtıl eltérıen helyezett el, hogy a tulajdonságaik jobban igazodjanak a szomszédjaikéhoz (az atomtömegek pontossága még nem érte el a mai szintet, ezért ezek egy részét mérési hibának gondolta, s ezzel párhuzamosan kijavította néhány elem atomtömegét), de ezek után sem volt a tulajdonságok szerint tökéletes a táblázat. Ekkor üres helyeket hagyott benne és megjósolta az ezekre a helyekre kerülı elemek tulajdonságait, atomtömegét. (fólia M. eredeti közleményében szereplı táblázatról) Cu Zn eka-al eka-si As Se Br M (g/mol) Mengyelejev eka-al elemét 1875-ben felfedezték és a gallium nevet kapta. A Ga a Mengyelejev által megjósolt tulajdonságokat mutatta, ami a rendszer helyességét megerısítette: eka-al Ga relatív atomtömeg 68 69,9 oxid összetétele Ea O 3 Ga O 3 olvadáspont alacsony 30,1 C forráspont magas 1983 C sőrőség 5,9 g/cm 3 5,91 g/cm 3 Végül Henry G. Moseley rendezte az elemeket rendszám szerint sorba 1914-ben. A periódusos rendszer ismertetése A mai legelterjedtebb periódusos rendszer az ún. hosszú periódusos rendszer (fóliák) sok változata van, különbözı dolgokat tőntetnek fel bennük mindig tartalmaz: sorszámokat (a rendszám) és vegyjel a sorok: periódusok 7 van belılük az oszlopok 18 van belılük nem minden oszlopban van elem az elsı 3 periódusban hasonló tulajdonságú elemek egy oszlopban hagyományos számozás: római számokkal I, II, III, illetve A és B jelöléssel modern számozás: arab számokkal 1-18 lantanoidák, aktinoidák külön, nagyon hasonló kémiai és fizikai tulajdonságok Miért ilyen a periódusos rendszer? válasz: a többelektronos atomok elektronszerkezete, lást késıbb. Az elektron Joseph J. Thompson (fizikai Nobel díj.) Az üveggel érintkezı katódsugár zöldes luminesszenciát eredményez Az útvonal elektród anyagtól és töltı gáztól független, me/e = 5,686 * 10-1 kg/c Millikan: e=1,60*10-19c me = 9,109*10-31 kg
3 Az atommag Ernst Rutherford 1µm vastagságú aranyfólia elızetes elképzelés: a pudding-modell a legtöbb részecske akadálytalanul áthaladt, de néhány visszapattant! (~1/8000 visszaverıdik, szóródik). A számítások szerint az atom belsejében, egy m sugarú gömbben van az atom tömegének jelentıs része, ezt atommagnak nevezte el. Így született meg a Rutherford-féle atommodell: atommag, körülötte az elektronok tetszıleges pályán keringenek, Coulomb-kh. ( bolygómodell ) Ha az atommag 1cm, akkor az atom 100m! Rutherford megállapította, hogy az atommagnak annyiszor 1,6*10-19 C töltése van, amennyi az atom sorszámának (Z) a periódusos rendszerben! Az elektroneutralitás miatt ennyi elektron is van az atomban. Problémák a Rutherford modellel: a mag körül keringı elektronok folyamatosan gyorsulnak, így energiát kellene sugározniuk, így az atom nem létezne tartósan. Az atomok színképei nem magyarázhatók vele meg Rutherford igazolta, hogy a hidrogén atommagja megtalálható más elemek magjában, univerzális építıelem. Ezt nevezhetjük a proton (p + ) születésnapjának. N + α H ben Walther Bothe és Herbert Becker Németországban azt találta, hogy ha nagyenergiájú polóniumból kisugárzott alfarészecskéket könnyő elemere (beríliumra, bórra, lítiumra) vezetnek, akkor szokatlanul nagy áthatolóképességő sugárzás keletkezik. Eleinte gamma sugárzásnak vélték, de a további kísérletek ezt nem támasztották alá. Végül 193-ben James Chadwick bizonyította be, hogy ez egy semleges részecskékbıl álló sugár, amelyet neutronnak neveztek el. Az atomokat felépítı elemi részecskék Az atomokat protonok, neutronok és elektronok építik fel, ezeket nevezzük elemi részecskéknek. Elemi részecskék tömeg relatív tömeg töltés relatív töltés e 9,10953*10-31 kg 1/1836 1,6019*10 19 C 1 p + 1,6765*10-7 kg 1,000 +1,6019*10 19 C +1 n 1,67495*10-7 kg 1, Összefoglalva: az atomok proton(ok)ból, elektron(ok)ból és általában neutronokból felépülı semleges részecskék, amelyek kémiai úton tovább nem bonthatók.
4 rendszám: az atommagban lévı protonok száma (jele Z) tömegszám: az atommagban lévı protonok és neutronok számának összege (jele A) (az elektronok tömege elhanyagolhatóan kicsi) a rendszámon múlik, hogy melyik elemrıl van szó elem: azonos rendszámú atomokból épül fel jelölése vegyjel: olyan egy vagy kétbetős jel, amely egy adott atomot illetve az elemet jelöli (latin nevek kezdbetői, Jöns Jakob Berzelius) pl: O, C, Ca nem mindegy a neutronok száma, ezek stabilizálják az atommagot ugyanahhoz a rendszámhoz (protonszámhoz) különbözı neutronszám tartozhat, ezek az izotópok (Z azonos, A különbözı) nuklid: egy elem adott neutronszámú atomja nuklid jelölése: Z A vegyjel vagy A vegyjel (a Z-t gyakran elhagyják, mert a vegyjel a nélkül is egyértelmő) vagy név-a pl. 6 1 C, 1 C, szén-1 egyetlen atom tömege igen kicsi (pl. egy szénatom 1,99*10 3 g), ezért inkább a relatív atomtömeget érdemes használni mi legyen az egység? legyen a hidrogén atom! Nem rossz, de rájöttek, hogy más atomokban a magot összetartó erık olyan nagyok, hogy jelentıs tömegcsökkenést okoznak, ezért érdemes inkább olyan atomot választani, amiben már hatnak magerık: Relatív atomtömeg: Külön megjelölés nélkül, a természetes izotóp-összetételő elem egy atomja átlagos tömegének viszonya a 1 C-nuklid tömegének 1/1 részéhez. Jól használható, mert az izotópok elıfordulási aránya általában csak kicsit változik. példa: a klór 35 Cl 75,77% 37 Cl 4,3% * 35 amu * 37 amu = amu A természetes elıfordulási arány miatt nem pontosan 1 a szén relatív atomtömege Szén-1: % gyakoriság, 1 amu Szén-13: 1.11 % gyakoriság, amu tömeg = (1 amu)(0.9889) + ( amu)(0.0111) = amu amu = 1.01 amu vannak olyan elemek, amelyeknek csak egy stabil izotópja van (pl. fluór), de pl. az ónnak 10! az izotópok kémiailag hasonlóan viselkednek, de bizonyos tulajdonságaik eltérnek (például az 35 U és 38 U) Az urán természetes izotópjai: 38 U (99.8%), 35 U (0.71%), 34 U (0.0054%). Az uránizotópok ipari mérető elválasztása gázcentrifugával történik. Urán-hexafluoridot (UF 6 ) választanak szét centrifugálással a moláris tömeg különbséget (mindössze 0,9%-os különbség!) felhasználva (a nehezebb 38 U izotópot tartalmazó molekulák kicsit lassabbak, mint a könnyebb izotópot tartalmazók). A hatékony elválasztáshoz nagysebességő centrifugákból álló centrifugasorozatot alkalmaznak.
5 Gázcentrifuga-sorozat urán dúsításhoz a radioaktivitás Becquerel fedezte fel (1896): az uránszurokérc nevő ásvány közelébe helyezett, de fényvédı papírba csomagolt fotolemezek megfeketedtek, mintha fény érte volna ıket az uránszurokérc magától röntgensugárzó! Marie Sklodovska, Pierre Curie különbözı uránásványokat vizsgáltak, és némelyik urántartalmánál sokkal jobban sugárzott. 10 tonna uránszurokérc feldolgozása után néhány mg olyan anyagot állítottak elı, ami az uránnál egymilliószor erısebben sugároz. Ez lett a rádium. Késıbb még erısebben sugárzó anyagot állítottak elı, ez lett a polónium. Késıbb korábban ismert elemekrıl is kiderült, hogy radioaktívak (pl. tórium, aktínium) az egyes izotópok nem egyforma stabilak, idıvel elbomlanak a bomlás sebességének jellemzése: a felezési idı: az az idı ami alatt az atomok fele elbomlik statisztikus folyamat, valószínőségek, nem tudjuk egy adott atomról elıre megmondani, hogy mikor bomlik el stabil izotópok: a föld korával összemérhetı felezési idı természetben nagyobb mennyiségben megtalálható radioaktív izotópok: nagyon hosszú felezési idık a sugárzást vizsgálva nem tudták annak intenzitását befolyásolni (hımérséklet emelése, kémiai reakciók) elektromágneses térben három részre bomlott (TK ábra) a negatív lemez felé eltérülı részt α, pozitív lemez felé eltérülıt β, az el nem térülıt γ sugárzásnak nevezték A radioaktív bomlás eredményeképpen keletkezı izotópok általában nem stabilak, tovább bomlanak. Így jönnek létre a bomlási sorok (TK ábra). az izotópok felhasználása maghasadás: atomreaktor, atombomba (kitérı a magot alkotó nukleonok közötti kötés erısségére, fúzió-hasadás, valamint Csernobil) radioaktív nyomjelzés: tápanyag útja a szervezetben anyagcsere-folyamatok gyógyszerek hatása mőtrágyák felhasználása kémiai reakciók mechanizmusa egyensúlyi folyamatok felszín alatti vizek követése sugárforrás: kóros sejtek elpusztítása fertıtlentés anyagszerkezeti, rejtett hibák felderítése
6 Térjünk vissza egy kicsit és nézzük meg micsodák az atomi színképek! Ehhez át kell ismételni néhány fogalmat: a fény tulajdonságai kettıs természete: részecske hullám nem ez vagy az, mindkettı, csak a vizsgálattól függıen másként mutatkozik a fény, mint hullám: elhajlás, polarizáció, interferencia a fény, mint részecske: fotoelektromos effektus, fotonok szóródása a fény, mint elektromágneses hullám c = λ * ν sebesség, frekvencia, hullámhossz, hullámszám c a fény sebessége, vákuumban, c 0 =, *10 8 m/s λ a fény hullámhossza ν a fény frekvenciája az anyagok színe különbözı hullámhosszúságú fényt különbözı mértékben nyelnek el az anyagok. egyszerő színek összetett színek anyagszerkezeti okok a fény kölcsönhatása az anyaggal abszorbció: az a folyamat, amely során a fény elnyelıdik az anyagban emisszió: az a folyamat, amely során az anyag fényt sugároz ki a fény energiája és a lehetséges kölcsönhatás helye/típusa (táblázat) a látható spektrum nap fényének bontása prizmával: színkép mint a szivárvány, minden szín meg van benne kísérlet: fénybontás cd-vel mesterségesen elıállított fény bontása: nincs meg minden szín, vonalak jelennek meg! (fóliák) a legegyszerőbb: a hidrogénatom színképe (fólia) A hidrogén gázt melegítve vonalas spektrumot kapunk. A látható tartományban a Balmer-féle sorozat esik.
7 empírikus összefüggés a színképvonalak hullámhosszára: Balmer (1885): képlet Általános, minden ismert sorozatra érvényes összefüggés: Rydberg: 1/λ = R* (1/k 1/n ) Bohr tudta elméletileg megmagyarázni ezt: A Bohr-féle atommodell a Rutherfond-féle atommodellbıl indul ki, posztulátumok: 1. Az elektronok az atomban nem keringhetnek tetszıleges sugarú pályákon, csak adott sugarú, adott energiájúakon (E = R h /n ). Ezeken a pályákon viszont energiaveszteség nélkül keringenek.. Az egyik kötött pályáról egy másik pályára történı átmenetnél az elektron által felvett, vagy kisugárzott energia megegyezik a két különbözı pályán lévı elektron energiájának különbségével. E i E j E = +R h /n j R h /n i = R h (1/n j 1/n i ) = hν az elektron keringési pályái n kis egész számokkal jellemezhetık, a pályák sugara n -tel arányosak néhány fogalom: - alapállapot: az elektron a legkisebb energiájú pályán van - gerjesztett állapot: az elektron nem a legkisebb energiájú pályán van - ionizáció: az elektront kiszakítjuk az atomból a hidrogénatom színképét jól lehetett értelmezni ez alapján: az alapállapotú atom gerjesztésekor az elektron nagyobb energiájú pályára kerül, majd egy vagy több lépésben vissza alapállapotba, miközben fotont/fotonokat bocsát ki. Így jönnek létre a spektrális sorozatok. fólia A hidrogén-atomra remekül mőködött a Bohr-féle atommodell, de a több elektront tartalmazó atomoknál csak pontatlanul tudja a színképeket magyarázni és a színképvonalak egyéb tulajdonságairól sem tud számot adni (felhasadás elektromos és mágneses térben). a kvantummechanikai atommodell Ami pontos az nem szemléletes, ami szemléletes az nem pontos. az anyagi részecskék állapota kapcsolatba hozható egy ún. hullámfüggvénnyel. A hullámfüggvények a kvantummechanikai állapotegyenlet megoldásai, kémiai szempontból az ún. Schrödinger-egyenletet kell tekinteni. Az egyenletben szerepelnek energiaértékek. Megoldást csak bizonyos energiaértékeknél lehet kapni. A megoldás során olyan paramétereket használnak, amelyek csak kis általában egész értékeket vehetnek fel, ezek a kvantumszámok. Az atomban lévı elektronok energiáját ezek a kvantumszámok határozzák meg. kvantumszám neve jele lehetséges értékei fıkvantumszám n 1,, 3,... mellékkvantumszám l 0, 1,..., (n-1) mágneses kvantumszám m l,..., 0,..., +l spinkvantumszám s ½, +½ hidrogén esetén a fı (többelektronos atomok esetén a fı és mellékkvantumszám együtt) határozza meg az elektron energiáját fıkvantumszám: távolság az atommagtól elektronhéjak betőjelek: n=1: K, n=: L, n=3: M, n=4: N mellékkvantumszám: az atompálya alakjával kapcsolatos alhéj l lehetséges értékei: 0 (n-1) betőjelek: l=0: s, l=1: p, l=: d, l=3: f a héj elnevezés félrevezetı! az elektron nem úgy viselkedik, mint várnánk (részecske / hullám)
8 Heisenberg-féle határozatlansági reláció: helyet és impulzust (p=m*v) nem lehet egyszerre tetszıleges pontossággal meghatározni. következmény: az atomon belül nem lehet pontosan megmondani, hogy hol van az elektron és hogyan mozog, csak az adható meg, hogy az adott térrészben mekkora valószínőséggel tartózkodik atompálya: az atommag körüli térnek az a része, ahol az elektron tartózkodási valószínősége 90%-nál nagyobb s- és p-pályák alakja atompályák fólia interaktív periódosos rendszer A hidrogén esetén csak egy elektron van az atomban. A többelektronos atomok esetén a fı és mellékkvantumszám együtt határozza meg az elektron energiáját. A periódusos rendszer és a többelektronos atomok elektronszerkezete közötti kapcsolat Ha egy atomba több elektron kerül mekkora energiája lesz? Ezt a kvantumelmélet alapján tudjuk megmondani: többelektronos atomok esetén a fı és mellékkvantumszám együtt határozza meg az elektron energiáját: Az atom úgy épül fel, hogy az összenergiája minimális legyen! naív gondolat: akkor az összes elektron menjen az n=1, l=0 pályára! Ez nem így történik! Pauli felismerte, hogy egy elektronnak nem lehet mind a négy kvantumszáma azonos (ez a Pauli-féle tilalmi elv) Induljunk ki ebbıl és számláljuk meg, hogy az egyes alhéjakon, héjakon mennyi elektron lehet! l=0 (azaz s alhéj): m=0, s= 1/, +1/, tehát 1*=db l=1 (azaz p alhéj): m= 1,0,+1, s= 1/, +1/, tehát 3*=6db l= (azaz d alhéj): m=, 1,0,+1,+, s= 1/, +1/, tehát 5*=10db l=3 (azaz f alhéj): m= 3,, 1,0,+1,+,+3, s= 1/, +1/, tehát 7*=14db azaz n=1 (K héj)> l=0> db n= (L héj)> l=0,1> 8db n=3 (M héj)> l=0,1,> 18db n=4 (N héj)> l=0,1,,3> 3db elektron lehet egy héjon Az elektronok száma az atomban (semleges!) egyenlı a protonok számával (Z, rendszám). A periódusos rendszerben rendszám szerint vannak sorban az elemek. Az elektronkonfiguráció leírja, hogy az elektronok miképpen oszlanak el a héjakon, alhéjakon, pályákon és mekkora a spinkvantumszámuk. Az elektronkonfiguráció jelölése: spdf-jelöléssel, azaz a fıkvantumszám számmal, mellékkvantumszám betővel, betöltöttség felsı indexben számmal pl. H: 1s 1 N: 1s s p 3 O: 1s s p 4 Ne: 1s s p 6 Na: 1s s p 6 3s 1 Felépülési elv: az energiaminimumra törekvés elve ÁTLÓS ÁBRA Na: 1s s p 6 3s 1 1s s p 6 3p 1 alapállapot 1. gerjesztett állapot ez a nátrium D vonala
9 Minden egyes rendszámnál van egy olyan elektronkonfiguráció, amelynek az energiája minimális. Ez az alapállapot. Ezt fel lehet tőntetni a periódusos rendszerben: periódusos rendszer elektronszerkezettel Az alapján, hogy éppen melyik héj töltıdik fel elektronokkal, beszélünk s-, p-, d- és f- mezıkrıl. A félig vagy teljesen betöltött alhéj különösen stabil, ami eltérésekhez vezet az elvárásainktól! Cr: 3d 5 4s 1 Pd: 4d 10 (de Ni: 3d 8 4s ) (Pt: 5d 9 6s 1 ) Mo: 4d 5 5s 1 Cu: 3d 10 5s 1 Gd: f 7 d 1 s Au: 5d 10 6s 1 Atomok, ionok elektronszerkezetének cellás ábrázolása: H, N, O elektronkonfigurációja cellás ábrázolással Miért így töltıdnek fel az azonos energiájú (degenerált) pályák? (Azaz miért lesznek az elektronok párosítatlanok a p pályán?) Az atom úgy épül fel, hogy az összenergiája minimális legyen! Ez akkor teljesül, ha az azonos energiájú pályákon az elektronok párosítatlan spinnel vannak jelen. Ezt mondja ki a Hund-szabály. A kémiai reakciókban leginkább az atomok legkülsı elektronhéján lévı elektronok vesznek részt. Ezért szokták a legkülsı elektronhéjat vegyértékhéjnak is nevezni. Nagyobb rendszámú elemek elektronkonfigurációjának feltőntetésénél nagyon sokat kellene írni, ezért gyakran csak a vegyértékhéj elektronkonfigurációját tőntetik fel részletesen: - az elızı nemesgáz vegyjelét írjuk bele: Na: Ne 3s 1 - a lezárt héjakat betőkkel jelöljük: Na: KL 3s 1 Adja meg spdf és cellás ábrázolással az alábbi részecskék elektronszerkezetét! Mire kell figyelni? - tudni kell, hogy melyik szám mit jelent a vegyjelben (melyik az elektronok, a protonok száma illetve az ion töltése) - ionok esetében az elektronok száma módosul a protonszámhoz képest 13 7 N : 18 8 O - : 19 9 F : 1 D : 4 He N : 1s s p 3 : : 1s s p 6 : : 1s s p 6 : (azonos az elızıvel, ez a két részecske izoelektronos) 1 D : 1s : 4 He + :, (nincs elektronja)
2. Az atomelmélet alapjai, a periódusos rendszer
 2. Az atomelmélet alapjai, a periódusos rendszer A világ nagyon összetett, sok szinten lehet tanulmányozni (az emberi méretektől elindulva, kisebb részek felé haladva), rengeteg anyag van! Az anyagot felépítő
2. Az atomelmélet alapjai, a periódusos rendszer A világ nagyon összetett, sok szinten lehet tanulmányozni (az emberi méretektől elindulva, kisebb részek felé haladva), rengeteg anyag van! Az anyagot felépítő
Boyle kísérlete. Boyle 1781-ben ónt hevített és azt tapasztalta, hogy annak tömege. Robert Boyle angol fizikus, kémikus
 Boyle kísérlete Boyle 1781-ben ónt hevített és azt tapasztalta, hogy annak tömege Robert Boyle 1627-1691 angol fizikus, kémikus A tömegmegmaradás törvénye Lavoisier kísérlete 1. Boyle tapasztalata: ónt
Boyle kísérlete Boyle 1781-ben ónt hevített és azt tapasztalta, hogy annak tömege Robert Boyle 1627-1691 angol fizikus, kémikus A tömegmegmaradás törvénye Lavoisier kísérlete 1. Boyle tapasztalata: ónt
2. Az atomelmélet alapjai, a periódusos rendszer
 2. Az atomelmélet alapjai, a periódusos rendszer A világ nagyon összetett, sok szinten lehet tanulmányozni (az emberi méretektől elindulva, kisebb részek felé haladva), rengeteg anyag van! Az anyagot felépítő
2. Az atomelmélet alapjai, a periódusos rendszer A világ nagyon összetett, sok szinten lehet tanulmányozni (az emberi méretektől elindulva, kisebb részek felé haladva), rengeteg anyag van! Az anyagot felépítő
Atommodellek. Az atom szerkezete. Atommodellek. Atommodellek. Atommodellek, A Rutherford-kísérlet. Atommodellek
 Démokritosz: a világot homogén szubsztanciájú oszthatatlan részecskék, atomok és a közöttük lévı őr alkotja. Az atom szerkezete Egy atommodellt akkor fogadunk el érvényesnek, ha megmagyarázza a tapasztalati
Démokritosz: a világot homogén szubsztanciájú oszthatatlan részecskék, atomok és a közöttük lévı őr alkotja. Az atom szerkezete Egy atommodellt akkor fogadunk el érvényesnek, ha megmagyarázza a tapasztalati
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Kémiai alapismeretek 2. hét
 Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2012. február 14. 1/15 2011/2012 II. félév, Horváth Attila c XIX sz. vége,
Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2012. február 14. 1/15 2011/2012 II. félév, Horváth Attila c XIX sz. vége,
ELEMI RÉSZECSKÉK ATOMMODELLEK
 ELEMI RÉSZECSKÉK ATOMMODELLEK Az atomok felépítése Készítette: Horváthné Vlasics Zsuzsanna Mi van az atomok belsejében? DÉMOKRITOSZ (Kr.e. 460-370) az anyag nem folytonos parányi, tovább nem bontható,
ELEMI RÉSZECSKÉK ATOMMODELLEK Az atomok felépítése Készítette: Horváthné Vlasics Zsuzsanna Mi van az atomok belsejében? DÉMOKRITOSZ (Kr.e. 460-370) az anyag nem folytonos parányi, tovább nem bontható,
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Az atommag összetétele, radioaktivitás
 Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
AZ ATOM. Atom: atommag + elektronfelhő = proton, neutron, elektron. Elemi részecskék
 AZ ATOM Atom: atommag + elektronfelhő = proton, neutron, elektron Elemi részecskék Atomok Dalton elmélete (1805): John DALTON 1766-1844 1. Az elemek apró részecskékből, atomokból állnak. Atom: görög szó
AZ ATOM Atom: atommag + elektronfelhő = proton, neutron, elektron Elemi részecskék Atomok Dalton elmélete (1805): John DALTON 1766-1844 1. Az elemek apró részecskékből, atomokból állnak. Atom: görög szó
Az ionizáló sugárzások fajtái, forrásai
 Az ionizáló sugárzások fajtái, forrásai magsugárzás Magsugárzások Röntgensugárzás Függelék. Intenzitás 2. Spektrum 3. Atom Repetitio est mater studiorum. Röntgen Ionizációnak nevezzük azt a folyamatot,
Az ionizáló sugárzások fajtái, forrásai magsugárzás Magsugárzások Röntgensugárzás Függelék. Intenzitás 2. Spektrum 3. Atom Repetitio est mater studiorum. Röntgen Ionizációnak nevezzük azt a folyamatot,
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK. Kalocsai Angéla, Kozma Enikő
 ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
FELADATMEGOLDÁS. Tesztfeladat: Válaszd ki a helyes megoldást!
 FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
Az atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen.
 MGFIZIK z atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen. Z TOMMG SZERKEZETE, RDIOKTIVITÁS PTE ÁOK Biofizikai Intézet Futó Kinga magfizika azonban még nem lezárt tudomány,
MGFIZIK z atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen. Z TOMMG SZERKEZETE, RDIOKTIVITÁS PTE ÁOK Biofizikai Intézet Futó Kinga magfizika azonban még nem lezárt tudomány,
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Mit tanultunk kémiából?2.
 Mit tanultunk kémiából?2. Az anyagok rendkívül kicsi kémiai részecskékből épülnek fel. Több milliárd részecske Mól az anyagmennyiség mértékegysége. 1 mol atom= 6. 10 23 db atom 600.000.000.000.000.000.000.000
Mit tanultunk kémiából?2. Az anyagok rendkívül kicsi kémiai részecskékből épülnek fel. Több milliárd részecske Mól az anyagmennyiség mértékegysége. 1 mol atom= 6. 10 23 db atom 600.000.000.000.000.000.000.000
8. AZ ATOMMAG FIZIKÁJA
 8. AZ ATOMMAG FIZIKÁJA Az atommag szerkezete (40-44 oldal) A tömegspektrométer elve Az atommag komponensei Izotópok Tömeghiány, kötési energia, stabilitás Magerők Magmodellek Az atommag stabilitásának
8. AZ ATOMMAG FIZIKÁJA Az atommag szerkezete (40-44 oldal) A tömegspektrométer elve Az atommag komponensei Izotópok Tömeghiány, kötési energia, stabilitás Magerők Magmodellek Az atommag stabilitásának
Modern fizika vegyes tesztek
 Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008.
 Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Kémiai alapismeretek 2. hét
 Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2014. szeptember 9.-12. 1/13 2014/2015 I. félév, Horváth Attila c Hullámtermészet:
Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2014. szeptember 9.-12. 1/13 2014/2015 I. félév, Horváth Attila c Hullámtermészet:
Thomson-modell (puding-modell)
 Atommodellek Thomson-modell (puding-modell) A XX. század elejére világossá vált, hogy az atomban található elektronok ugyanazok, mint a katódsugárzás részecskéi. Magyarázatra várt azonban, hogy mi tartja
Atommodellek Thomson-modell (puding-modell) A XX. század elejére világossá vált, hogy az atomban található elektronok ugyanazok, mint a katódsugárzás részecskéi. Magyarázatra várt azonban, hogy mi tartja
Az elektromágneses hullámok
 203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
OPTIKA. Fénykibocsátás mechanizmusa fényforrás típusok. Dr. Seres István
 OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
FIZIKA. Sugárzunk az elégedettségtől! (Atomfizika) Dr. Seres István
 Sugárzunk az elégedettségtől! () Dr. Seres István atommagfizika Atommodellek 440 IE Democritus, Leucippus, Epicurus 1803 1897 John Dalton J.J. Thomson 1911 Ernest Rutherford 19 Niels Bohr 3 Atommodellek
Sugárzunk az elégedettségtől! () Dr. Seres István atommagfizika Atommodellek 440 IE Democritus, Leucippus, Epicurus 1803 1897 John Dalton J.J. Thomson 1911 Ernest Rutherford 19 Niels Bohr 3 Atommodellek
A tudós neve: Mit tudsz róla:
 8. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
8. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
Atomfizika. A hidrogén lámpa színképei. Elektronok H atom. Fényképlemez. emisszió H 2. gáz
 Atomfizika A hidrogén lámpa színképei - Elektronok H atom emisszió Fényképlemez V + H 2 gáz Az atom és kvantumfizika fejlődésének fontos szakasza volt a hidrogén lámpa színképeinek leírása, és a vonalas
Atomfizika A hidrogén lámpa színképei - Elektronok H atom emisszió Fényképlemez V + H 2 gáz Az atom és kvantumfizika fejlődésének fontos szakasza volt a hidrogén lámpa színképeinek leírása, és a vonalas
Jegyzet. Kémia, BMEVEAAAMM1 Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens.
 Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Periódusosság. Általános Kémia, Periódikus tulajdonságok. Slide 1 of 35
 Periódusosság 3-1 Az elemek csoportosítása: a periódusos táblázat 3-2 Fémek, nemfémek és ionjaik 3-3 Az atomok és ionok mérete 3-4 Ionizációs energia 3-5 Elektron affinitás 3-6 Mágneses 3-7 Az elemek periodikus
Periódusosság 3-1 Az elemek csoportosítása: a periódusos táblázat 3-2 Fémek, nemfémek és ionjaik 3-3 Az atomok és ionok mérete 3-4 Ionizációs energia 3-5 Elektron affinitás 3-6 Mágneses 3-7 Az elemek periodikus
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár. Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár,
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Az atommag összetétele, radioaktivitás
 Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Az atom felépítése Alapfogalmak
 Anyagszerkezeti vizsgálatok 2017/2018. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Anyagszerkezeti vizsgálatok 2017/2018. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Magfizika tesztek. 1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem
 1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem 2. Mit nevezünk az atom tömegszámának? a) a protonok számát b) a neutronok számát c) a protonok és neutronok
1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem 2. Mit nevezünk az atom tömegszámának? a) a protonok számát b) a neutronok számát c) a protonok és neutronok
Atomfizika. Az atommag szerkezete. Radioaktivitás Biofizika, Nyitrai Miklós
 Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 13. Biofizika, Nyitrai Miklós Összefoglalás Atommag alkotói, szerkezete; Erős vagy magkölcsönhatás; Tömegdefektus. A kölcsönhatások világképe
Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 13. Biofizika, Nyitrai Miklós Összefoglalás Atommag alkotói, szerkezete; Erős vagy magkölcsönhatás; Tömegdefektus. A kölcsönhatások világképe
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Általános Kémia, BMEVESAA101
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Periódusosság. Általános Kémia, Periódikus tulajdonságok. Slide 1 of 35
 Periódusosság 11-1 Az elemek csoportosítása: a periódusos táblázat 11-2 Fémek, nemfémek és ionjaik 11-3 Az atomok és ionok mérete 11-4 Ionizációs energia 11-5 Elektron affinitás 11-6 Mágneses 11-7 Az elemek
Periódusosság 11-1 Az elemek csoportosítása: a periódusos táblázat 11-2 Fémek, nemfémek és ionjaik 11-3 Az atomok és ionok mérete 11-4 Ionizációs energia 11-5 Elektron affinitás 11-6 Mágneses 11-7 Az elemek
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
ATOMFIZIKA, RADIOAKTIVITÁS
 ATOMFIZIKA, RADIOAKTIVITÁS 2013. 11. 08. A biofizika fizikai alapjai Magfizika Az atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen. A magfizika azonban még nem lezárt
ATOMFIZIKA, RADIOAKTIVITÁS 2013. 11. 08. A biofizika fizikai alapjai Magfizika Az atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen. A magfizika azonban még nem lezárt
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet
 Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
61. Lecke Az anyagszerkezet alapjai
 61. Lecke Az anyagszerkezet alapjai GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési
61. Lecke Az anyagszerkezet alapjai GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési
Atomfizika. Az atommag szerkezete. Radioaktivitás Biofizika, Nyitrai Miklós
 Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 12. Biofizika, Nyitrai Miklós Miért hiszi mindenki azt, hogy az atomfizika egyszerű, szép és szerethető? A korábbiakban tárgyaltuk Az atom szerkezete
Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 12. Biofizika, Nyitrai Miklós Miért hiszi mindenki azt, hogy az atomfizika egyszerű, szép és szerethető? A korábbiakban tárgyaltuk Az atom szerkezete
Sugárzások kölcsönhatása az anyaggal
 Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Az atomok szerkezete. Az atomok szerkezete. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Az atomok szerkezete A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Atommodellek A kémiai szempontból legkisebb önálló részecskéket atomoknak nevezzük. Az atomok felépítésével kapcsolatos
Az atomok szerkezete A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Atommodellek A kémiai szempontból legkisebb önálló részecskéket atomoknak nevezzük. Az atomok felépítésével kapcsolatos
 http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
Az anyagi rendszerek csoportosítása
 Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Atommodellek. Ha nem tudod egy pincérnőnek elmagyarázni a fizikádat, az valószínűleg nem nagyon jó fizika. Rausch Péter kémia-környezettan tanár
 Atommodellek Ha nem tudod egy pincérnőnek elmagyarázni a fizikádat, az valószínűleg nem nagyon jó fizika. Ernest Rutherford Rausch Péter kémia-környezettan tanár Modellalkotás A modell a valóság nagyított
Atommodellek Ha nem tudod egy pincérnőnek elmagyarázni a fizikádat, az valószínűleg nem nagyon jó fizika. Ernest Rutherford Rausch Péter kémia-környezettan tanár Modellalkotás A modell a valóság nagyított
A SZERB KÖZTÁRSASÁG OKTATÁSI ÉS TUDOMÁNYÜGYI MINISZTÉRIUMA SZERB KÉMIKUSOK EGYESÜLETE. KÖZTÁRSASÁGI KÉMIAVERSENY (Varvarin, május 12.
 A SZERB KÖZTÁRSASÁG OKTATÁSI ÉS TUDOMÁNYÜGYI MINISZTÉRIUMA SZERB KÉMIKUSOK EGYESÜLETE KÖZTÁRSASÁGI KÉMIAVERSENY (Varvarin, 2012. május 12.) TUDÁSFELMÉRŐ FELADATLAP A VII. OSZTÁLY SZÁMÁRA A tanuló jeligéje:
A SZERB KÖZTÁRSASÁG OKTATÁSI ÉS TUDOMÁNYÜGYI MINISZTÉRIUMA SZERB KÉMIKUSOK EGYESÜLETE KÖZTÁRSASÁGI KÉMIAVERSENY (Varvarin, 2012. május 12.) TUDÁSFELMÉRŐ FELADATLAP A VII. OSZTÁLY SZÁMÁRA A tanuló jeligéje:
Az anyagi rendszerek csoportosítása
 Kémia 1 A kémiai ismeretekről A modern technológiai folyamatok és a környezet védelmére tett intézkedések alig érthetőek kémiai tájékozottság nélkül. Ma már minden mérnök számára alapvető fontosságú a
Kémia 1 A kémiai ismeretekről A modern technológiai folyamatok és a környezet védelmére tett intézkedések alig érthetőek kémiai tájékozottság nélkül. Ma már minden mérnök számára alapvető fontosságú a
Kormeghatározás gyorsítóval
 Beadás határideje 2012. január 31. A megoldásokat a kémia tanárodnak add oda! 1. ESETTANULMÁNY 9. évfolyam Olvassa el figyelmesen az alábbi szöveget és válaszoljon a kérdésekre! Kormeghatározás gyorsítóval
Beadás határideje 2012. január 31. A megoldásokat a kémia tanárodnak add oda! 1. ESETTANULMÁNY 9. évfolyam Olvassa el figyelmesen az alábbi szöveget és válaszoljon a kérdésekre! Kormeghatározás gyorsítóval
Az atom felépítése Alapfogalmak
 Anyagszerkezeti vizsgálatok 2018/2019. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Anyagszerkezeti vizsgálatok 2018/2019. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Mag- és neutronfizika
 Mag- és neutronfizika z elıadás célja: : megalapozni az atomenergetikai ismereteket félév során a következı témaköröket ismertetjük: Magfizikai alapfogalmak (atommagok, radioaktivitás) Sugárzás és anyag
Mag- és neutronfizika z elıadás célja: : megalapozni az atomenergetikai ismereteket félév során a következı témaköröket ismertetjük: Magfizikai alapfogalmak (atommagok, radioaktivitás) Sugárzás és anyag
Elektronok, atomok. Általános Kémia - Elektronok, Atomok. Dia 1/61
 Elektronok, atomok 2-1 Elektromágneses sugárzás 2-2 Atomi Spektrum 2-3 Kvantumelmélet 2-4 A Bohr Atom 2-5 Az új Kvantummechanika 2-6 Hullámmechanika 2-7 Kvantumszámok Dia 1/61 Tartalom 2-8 Elektronsűrűség
Elektronok, atomok 2-1 Elektromágneses sugárzás 2-2 Atomi Spektrum 2-3 Kvantumelmélet 2-4 A Bohr Atom 2-5 Az új Kvantummechanika 2-6 Hullámmechanika 2-7 Kvantumszámok Dia 1/61 Tartalom 2-8 Elektronsűrűség
Bevezetés a modern fizika fejezeteibe. 4. (a) Kvantummechanika. Utolsó módosítás: november 15. Dr. Márkus Ferenc BME Fizika Tanszék
 Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Színképelemzés. Romsics Imre 2014. április 11.
 Színképelemzés Romsics Imre 2014. április 11. 1 Más néven: Spektrofotometria A színképből kinyert információkból megállapítható: az atomok elektronszerkezete az elektronállapotokat jellemző kvantumszámok
Színképelemzés Romsics Imre 2014. április 11. 1 Más néven: Spektrofotometria A színképből kinyert információkból megállapítható: az atomok elektronszerkezete az elektronállapotokat jellemző kvantumszámok
Kémia ktervezıknekknek
 Környezetmérn Kémia rnököknek knek és s terméktervez ktervezıknekknek Wagner Ödön BME Szervetlen és s Analitikai Kémia K Tanszék wagner@mail.bme.hu Tel.: 463-31-06 Kurzussal kapcsolatos tudnivalók Vizsgaidıszakban
Környezetmérn Kémia rnököknek knek és s terméktervez ktervezıknekknek Wagner Ödön BME Szervetlen és s Analitikai Kémia K Tanszék wagner@mail.bme.hu Tel.: 463-31-06 Kurzussal kapcsolatos tudnivalók Vizsgaidıszakban
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
-A radioaktivitás a nem stabil (úgynevezett radioaktív) atommagok bomlásának folyamata. -Nagyenergiájú ionizáló sugárzást kelt Az elnevezés: - radio
 -A radioaktivitás a nem stabil (úgynevezett radioaktív) atommagok bomlásának folyamata. -Nagyenergiájú ionizáló sugárzást kelt Az elnevezés: - radio (sugároz) - activus (cselekvő) Különféle foszforeszkáló
-A radioaktivitás a nem stabil (úgynevezett radioaktív) atommagok bomlásának folyamata. -Nagyenergiájú ionizáló sugárzást kelt Az elnevezés: - radio (sugároz) - activus (cselekvő) Különféle foszforeszkáló
Izotóp geológia: Elemek izotópjainak használata geológiai folyamatok értelmezéséhez.
 Radioaktív izotópok Izotópok Egy elem különböző tömegű (tömegszámú - A) formái; Egy elem izotópjainak a magjai azonos számú protont (rendszám - Z) és különböző számú neutront (N) tartalmaznak; Egy elem
Radioaktív izotópok Izotópok Egy elem különböző tömegű (tömegszámú - A) formái; Egy elem izotópjainak a magjai azonos számú protont (rendszám - Z) és különböző számú neutront (N) tartalmaznak; Egy elem
Általános és szervetlen kémia 1. hét
 Általános és szervetlen kémia 1. hét A tantárgy elméleti és gyakorlati anyaga http://cheminst.emk.nyme.hu A CAPA teszt-gyakorló program használata Kliens programot letölteni a weboldalról Bejelentkezés
Általános és szervetlen kémia 1. hét A tantárgy elméleti és gyakorlati anyaga http://cheminst.emk.nyme.hu A CAPA teszt-gyakorló program használata Kliens programot letölteni a weboldalról Bejelentkezés
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Az atom szerkezete. Az eltérülés ritka de nagymértékű. Thomson puding atom-modellje nem lehet helyes.
 Az atom szerkezete Rutherford kísérlet (1911): Az atom pozitív töltése és a tömeg nagy része egy nagyon kis helyre összpontosul. Ezt nevezte el atommagnak. Az eltérülés ritka de nagymértékű. Thomson puding
Az atom szerkezete Rutherford kísérlet (1911): Az atom pozitív töltése és a tömeg nagy része egy nagyon kis helyre összpontosul. Ezt nevezte el atommagnak. Az eltérülés ritka de nagymértékű. Thomson puding
A periódusos rendszer, periodikus tulajdonságok
 A periódusos rendszer, periodikus tulajdonságok Szalai István ELTE Kémiai Intézet 1/45 Az előadás vázlata ˆ Ismétlés ˆ Történeti áttekintés ˆ Mengyelejev periódusos rendszere ˆ Atomsugár, ionsugár ˆ Ionizációs
A periódusos rendszer, periodikus tulajdonságok Szalai István ELTE Kémiai Intézet 1/45 Az előadás vázlata ˆ Ismétlés ˆ Történeti áttekintés ˆ Mengyelejev periódusos rendszere ˆ Atomsugár, ionsugár ˆ Ionizációs
Jelöljük meg a kérdésnek megfelelő válaszokat! 1, Hullámokról általában: alapösszefüggések a harmonikus hullámra. A Doppler-effektus
 Jelöljük meg a kérdésnek megfelelő válaszokat! 1, Hullámokról általában: alapösszefüggések a harmonikus hullámra. A Doppler-effektus Melyik egyenlet nem hullámot ír le? a) y = A sin 2π(ft x/λ) b) y = A
Jelöljük meg a kérdésnek megfelelő válaszokat! 1, Hullámokról általában: alapösszefüggések a harmonikus hullámra. A Doppler-effektus Melyik egyenlet nem hullámot ír le? a) y = A sin 2π(ft x/λ) b) y = A
Az atommag szerkezete
 Az atommag szerkezete Biofizika előadások 2013 november Orbán József PTE ÁOK Biofzikai Intézet Filozófusok / tudósok Történelem Aristoteles Dalton J.J.Thomson Bohr Schrödinger Pauli Curie házaspár Teller
Az atommag szerkezete Biofizika előadások 2013 november Orbán József PTE ÁOK Biofzikai Intézet Filozófusok / tudósok Történelem Aristoteles Dalton J.J.Thomson Bohr Schrödinger Pauli Curie házaspár Teller
I. ATOMOK, IONOK I. 1 3. FELELETVÁLASZTÁSOS TESZTEK
 I. ATMK, INK I. 1 3. FELELETVÁLASZTÁSS TESZTEK 0 1 2 3 4 5 6 7 8 9 0 A C C D C D A D C 1 C B C E* B E C C ** E 2 D C E D C B D A E C 3 A B D B B B D C D C 4 B B D B B D D C C D 5 D B * a negyedik, vagyis
I. ATMK, INK I. 1 3. FELELETVÁLASZTÁSS TESZTEK 0 1 2 3 4 5 6 7 8 9 0 A C C D C D A D C 1 C B C E* B E C C ** E 2 D C E D C B D A E C 3 A B D B B B D C D C 4 B B D B B D D C C D 5 D B * a negyedik, vagyis
KÉMIA FELVÉTELI KÖVETELMÉNYEK
 KÉMIA FELVÉTELI KÖVETELMÉNYEK Atomszerkezettel kapcsolatos feladatok megoldása a periódusos rendszer segítségével, illetve megadott elemi részecskék alapján. Az atomszerkezet és a periódusos rendszer kapcsolata.
KÉMIA FELVÉTELI KÖVETELMÉNYEK Atomszerkezettel kapcsolatos feladatok megoldása a periódusos rendszer segítségével, illetve megadott elemi részecskék alapján. Az atomszerkezet és a periódusos rendszer kapcsolata.
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
8. Osztály. Kód. Szent-Györgyi Albert kémiavetélkedő
 8. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
8. Osztály Kedves Versenyző! A jobb felső sarokban található mezőbe írd fel a verseny lebonyolításáért felelős személytől kapott kódot a feladatlap minden oldalára. A feladatokat lehetőleg a feladatlapon
Tartalom Az atom szerkezete... 1 9 Atom. Részecske. Molekula... 1 4 Atommodellek... 4 6 A.) J. Thomson féle atommodell...4 B.) A Rutherford-féle vagy
 Tartalom Az atom szerkezete... 1 9 Atom. Részecske. Molekula... 1 4 Atommodellek... 4 6 A.) J. Thomson féle atommodell...4 B.) A Rutherford-féle vagy bolygó atommodell... 4 5 C.) A Bohr-féle atommodell...
Tartalom Az atom szerkezete... 1 9 Atom. Részecske. Molekula... 1 4 Atommodellek... 4 6 A.) J. Thomson féle atommodell...4 B.) A Rutherford-féle vagy bolygó atommodell... 4 5 C.) A Bohr-féle atommodell...
Atommag, atommag átalakulások, radioaktivitás
 Atommag, atommag átalakulások, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Atommag, atommag átalakulások, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Magsugárzások, Radioaktív izotópok. Az atom alkotórészei. Az atom felépítése. A radioaktivitás : energia kibocsátása
 Magsugárzások, Radioaktív izotópok radioaktivitás : energia kibocsátása az atommagból részecskék vagy elektromágneses sugárzás formájában z atom felépítése z atom alkotórészei protonok neutronok nukleonok
Magsugárzások, Radioaktív izotópok radioaktivitás : energia kibocsátása az atommagból részecskék vagy elektromágneses sugárzás formájában z atom felépítése z atom alkotórészei protonok neutronok nukleonok
Atommodellek. Készítette: Sellei László
 Atommodellek Készítette: Sellei László Démokritosz Kr. e. V. sz. Az egyik legnehezebb kérdés, amire már az ókori görög tudomány is megpróbált választ adni: miből áll a világ? A világot homogén szubsztanciájú
Atommodellek Készítette: Sellei László Démokritosz Kr. e. V. sz. Az egyik legnehezebb kérdés, amire már az ókori görög tudomány is megpróbált választ adni: miből áll a világ? A világot homogén szubsztanciájú
Ónt hevítünk. Tömege: Kahootit!
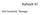 Ónt hevítünk. Tömege: Kahootit! A tömegmegmaradás törvénye Lavoisier kísérlete 1. Boyle tapasztalata: ónt hevítve annak tömege növekszik. 2. Lavoisier kísérlete: az ónt ZÁRT EDÉNYBEN hevítette. Megmérte
Ónt hevítünk. Tömege: Kahootit! A tömegmegmaradás törvénye Lavoisier kísérlete 1. Boyle tapasztalata: ónt hevítve annak tömege növekszik. 2. Lavoisier kísérlete: az ónt ZÁRT EDÉNYBEN hevítette. Megmérte
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Sugárzások kölcsönhatása az anyaggal
 Sugárzások kölcsönhatása az anyaggal Dr. Vincze Árpád vincze@oah.hu Mitől függ a kölcsönhatás? VÁLASZ: Az anyag felépítése A sugárzások típusai, forrásai és főbb tulajdonságai A sugárzások és az anyag
Sugárzások kölcsönhatása az anyaggal Dr. Vincze Árpád vincze@oah.hu Mitől függ a kölcsönhatás? VÁLASZ: Az anyag felépítése A sugárzások típusai, forrásai és főbb tulajdonságai A sugárzások és az anyag
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Bővített fokozatú SUGÁRVÉDELMI TANFOLYAM
 Bővített fokozatú SUGÁRVÉDELMI TANFOLYAM Sugárfizikai alapismeretek. A röntgen sugárzás keletkezése és tulajdonságai. Salik Ádám, sugárvédelmi szakértő salik.adam@osski.hu, 30-349-9300 ORSZÁGOS SUGÁRBIOLÓGIAI
Bővített fokozatú SUGÁRVÉDELMI TANFOLYAM Sugárfizikai alapismeretek. A röntgen sugárzás keletkezése és tulajdonságai. Salik Ádám, sugárvédelmi szakértő salik.adam@osski.hu, 30-349-9300 ORSZÁGOS SUGÁRBIOLÓGIAI
AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE
 AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE A Planck-féle sugárzási törvény Hipotézis 1.: A hősugárzást (elektromágneses hullámokat) kis, apró rezgő oszcillátorok hozzák létre. Egy ilyen oszcillátor
AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE A Planck-féle sugárzási törvény Hipotézis 1.: A hősugárzást (elektromágneses hullámokat) kis, apró rezgő oszcillátorok hozzák létre. Egy ilyen oszcillátor
Kémia I. Műszaki menedzser hallgatók számára
 Kémia I, Műszaki menedzser hallgatók számára Novák Csaba BME, Általános és Analitikai Kémia Tanszék, 2005. Kémia I. Műszaki menedzser hallgatók számára Kémia I. Műszaki menedzser hallgatók számára Novák
Kémia I, Műszaki menedzser hallgatók számára Novák Csaba BME, Általános és Analitikai Kémia Tanszék, 2005. Kémia I. Műszaki menedzser hallgatók számára Kémia I. Műszaki menedzser hallgatók számára Novák
A testek részecskéinek szerkezete
 A testek részecskéinek szerkezete Minden test részecskékből, atomokból vagy több atomból álló molekulákból épül fel. Az atomok is összetettek: elektronok, protonok és neutronok találhatók bennük. Az elektronok
A testek részecskéinek szerkezete Minden test részecskékből, atomokból vagy több atomból álló molekulákból épül fel. Az atomok is összetettek: elektronok, protonok és neutronok találhatók bennük. Az elektronok
I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag?
 I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag? Platón (i.e. 427-347), Arisztotelész (=i.e. 387-322): Végtelenségig
I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag? Platón (i.e. 427-347), Arisztotelész (=i.e. 387-322): Végtelenségig
Szilárdtestek sávelmélete. Sávelmélet a szabadelektron-modell alapján
 Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
Mit értünk a termikus neutronok fogalma alatt? Becsüljük meg a sebességüket 27 o C hőmérsékleten!
 Országos Szilárd Leó fizikaverseny Elődöntő 04. Minden feladat helyes megoldása 5 pontot ér. A feladatokat tetszőleges sorrenen lehet megoldani. A megoldáshoz bármilyen segédeszköz használható. Rendelkezésre
Országos Szilárd Leó fizikaverseny Elődöntő 04. Minden feladat helyes megoldása 5 pontot ér. A feladatokat tetszőleges sorrenen lehet megoldani. A megoldáshoz bármilyen segédeszköz használható. Rendelkezésre
MIKROFIZIKA. Atomok és molekulák. Avogadro törvénye. www.baranyi.hu 2010. szeptember 19. FIZIKA TÁVOKTATÁS
 MIKROFIZIKA Atomok és molekulák Avogadro törvénye A hidrogén a kémiai elemek között a legkönnyebb, részecskéi (atomjai) a legkissebbek. (A hidrogén kétatomos gáz, egyatomos állapotban nem fordul elő. Molekulája
MIKROFIZIKA Atomok és molekulák Avogadro törvénye A hidrogén a kémiai elemek között a legkönnyebb, részecskéi (atomjai) a legkissebbek. (A hidrogén kétatomos gáz, egyatomos állapotban nem fordul elő. Molekulája
Atomok, elektronok. Általános Kémia - Elektronok, Atomok. Dia 1/61
 , elektronok 2-1 Elektromágneses sugárzás 2-2 Atomi spektrum 2-3 Kvantumelmélet 2-4 Bohr-atom 2-5 Az új kvantummechanika 2-6 Hullámmechanika 2-7 A hidrogénatom hullámfüggvényei Dia 1/61 , elektronok 2-8
, elektronok 2-1 Elektromágneses sugárzás 2-2 Atomi spektrum 2-3 Kvantumelmélet 2-4 Bohr-atom 2-5 Az új kvantummechanika 2-6 Hullámmechanika 2-7 A hidrogénatom hullámfüggvényei Dia 1/61 , elektronok 2-8
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyz jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Az anyagok kettős (részecske és hullám) természete
 Az anyagok kettős (részecske és hullám) természete de Broglie hipotézise (1924-25): Bármilyen fénysebességgel mozgó részecskére: mc = p E = mc 2 = hn p = hn/c = h/ = h/p - de Broglie-féle hullámhossz Nem
Az anyagok kettős (részecske és hullám) természete de Broglie hipotézise (1924-25): Bármilyen fénysebességgel mozgó részecskére: mc = p E = mc 2 = hn p = hn/c = h/ = h/p - de Broglie-féle hullámhossz Nem
Átmenetifém-komplexek ESR-spektrumának jellemzıi
 Átmenetifém-komplexek ESR-spektrumának jellemzıi A párosítatlan elektron d-pályán van. Kevéssé delokalizálódik a fémionról, a fém-donoratom kötések meglehetısen ionos jellegőek. A spin-pálya csatolás viszonylag
Átmenetifém-komplexek ESR-spektrumának jellemzıi A párosítatlan elektron d-pályán van. Kevéssé delokalizálódik a fémionról, a fém-donoratom kötések meglehetısen ionos jellegőek. A spin-pálya csatolás viszonylag
Atomfizika I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag?
 Atomfizika I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag? Platón (i.e. 427-347), Arisztotelész (=i.e. 387-322): Végtelenségig
Atomfizika I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag? Platón (i.e. 427-347), Arisztotelész (=i.e. 387-322): Végtelenségig
Sugárzások kölcsönhatása az anyaggal. Dr. Vincze Árpád vincze@oah.hu
 Sugárzások kölcsönhatása az anyaggal Dr. Vincze Árpád vincze@oah.hu Mitől függ a kölcsönhatás? VÁLASZ: Az anyag felépítése A sugárzások típusai, forrásai és főbb tulajdonságai A sugárzások és az anyag
Sugárzások kölcsönhatása az anyaggal Dr. Vincze Árpád vincze@oah.hu Mitől függ a kölcsönhatás? VÁLASZ: Az anyag felépítése A sugárzások típusai, forrásai és főbb tulajdonságai A sugárzások és az anyag
Periódusosság. 9-1 Az elemek csoportosítása: a periódusostáblázat
 Periódusosság 9-1 Az elemek csoportosítása: aperiódusos táblázat 9-2 Fémek, nemfémek és ionjaik 9-3 Az atomok és ionok mérete 9-4 Ionizációs energia 9-5 Elektron affinitás 9-6 Mágneses 9-7 Az elemek periódikus
Periódusosság 9-1 Az elemek csoportosítása: aperiódusos táblázat 9-2 Fémek, nemfémek és ionjaik 9-3 Az atomok és ionok mérete 9-4 Ionizációs energia 9-5 Elektron affinitás 9-6 Mágneses 9-7 Az elemek periódikus
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését!
 I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
A sugárzások a rajz síkjára merőleges mágneses téren haladnak át γ α
 Radioaktivitás, α-, β- és γ-bomlás, radioaktív bomlástörvény, bomlási sorok. röntgen sugárzás (fékezési és karakterisztikus), a Moseley-törvény, az uger folyamat Radioaktivitás: 1896 Becquerel uránérc
Radioaktivitás, α-, β- és γ-bomlás, radioaktív bomlástörvény, bomlási sorok. röntgen sugárzás (fékezési és karakterisztikus), a Moseley-törvény, az uger folyamat Radioaktivitás: 1896 Becquerel uránérc
7. osztály 2 Hevesy verseny, megyei forduló, 2004.
 7. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
7. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
Az atomok szerkezete II.; A kémiai jelrendszer; A periódusos rendszer
 Az atomok szerkezete II.; A kémiai jelrendszer; A periódusos rendszer Műszaki kémia, Anyagtan I. 3-4. előadás Dolgosné dr. Kovács Anita egy. doc. PTE MIK Környezetmérnöki Tanszék Elektronszerkezet Az elektron
Az atomok szerkezete II.; A kémiai jelrendszer; A periódusos rendszer Műszaki kémia, Anyagtan I. 3-4. előadás Dolgosné dr. Kovács Anita egy. doc. PTE MIK Környezetmérnöki Tanszék Elektronszerkezet Az elektron
Stern Gerlach kísérlet. Készítette: Kiss Éva
 Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
