I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
|
|
|
- Renáta Fodorné
- 9 évvel ezelőtt
- Látták:
Átírás
1 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1
2 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (1 ml) vakcina Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú alumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al 3+ A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Szuszpenziós injekció. Zavaros fehér szuszpenzió. 4. KLINIKAI JELLEMZŐK 4.1 Terápiás javallatok A Twinrix Felnőtt alkalmazása hepatitis A és hepatitis B vírusfertőzés kockázatának kitett és erre fogékony felnőttek és 16 éves kor feletti serdülők számára javallott. 4.2 Adagolás és alkalmazás Adagolás - Adagolás Egy 1 ml-es adag ajánlott felnőtteknek és 16 éves vagy idősebb serdülőknek. - Alapimmunizálás Az alapimmunizálás általánosan ajánlott sémája szerinti adagolás 3 adag Twinrix Felnőtt beadásából áll, az első adagot egy választott napon, a második adagot 1 hónap múlva, a harmadik adagot az első adag beadása után 6 hónappal kell beadni. Különleges esetekben felnőtteknél, ha valaki elutazik 1 vagy több hónapon belül az első oltást követően, és nincs elegendő idő a 0, 1, 6 hónapos oltási séma szerinti oltáshoz, 3 intramuscularis injekciót kell beadni a 0., 7. és a 21. napon. Ebben az esetben 4. oltás beadása javasolt, az első oltás beadását követően 12 hónappal. Az ajánlott sémát be kell tartani. Az első adag beadása után az alapimmunizálás további adagjainak beadásakor ugyanazt a vakcinát kell használni. 2
3 - Emlékeztető oltások Az ellenanyagok hosszútávú perzisztálását igazoló adatok a Twinrix Felnőtt vakcina beadása után legfeljebb 15 évre vonatkoznak. Az alapimmunizálást követően az anti-hbs és anti-hav ellenanyagok mért értékei a kombinált vakcinák alkalmazása során abban az értéktartományban vannak, amelyet a monovalens vakcinákkal történő oltás után lehet elérni. Az ellenanyag csökkenés kinetikája is hasonló. Az emlékeztető oltásokra vonatkozó általános ajánlásokat így a monovalens vakcinákkal kapott tapasztalatok alapján lehet megadni. Hepatitis B Azon egészséges egyének részére, akik teljes alapimmunizálásban részesültek, emlékeztető oltások nem szükségesek. Azonban néhány kötelező védőoltási program magában foglalja az emlékeztető oltást, amit figyelembe kell venni. HBV fertőzésnek kitett egyének vagy betegek néhány csoportjában (pl. hemodializált vagy károsodott immunrendszerű betegek), megfontolandó a védelmet biztosító 10 NE/l antitestszint biztosítása. Hepatitis A Nem alakult ki egységes állásfoglalás arról, hogy egészséges immunitású egyéneknél, akik a hepatitis A oltásra reagáltak, szükséges-e emlékeztető oltások adása, amikor ellenanyag ugyan nem mutatható ki, de az immunmemória védettséget biztosíthat. Az emlékeztető oltást szorgalmazó ajánlás azon a feltevésen alapul, hogy az ellenanyagok szükségesek a védelemhez; a hepatitis A ellenes ellenanyagok számítások alapján legalább 10 éven át kimutathatók a szervezetben. Azon esetekben, amikor mind hepatitis A, mind hepatitis B emlékeztető oltásra szükség van, Twinrix Felnőtt adható. Másik lehetőség, hogy Twinrix Felnőtt vakcinával alapimmunizált egyének emlékeztető oltására a két monovalens vakcinát alkalmazzuk. Az alkalmazás módja A Twinrix Felnőtt intramuscularis injekció, célszerű a deltoid régióba beadni. Kivételes esetekben azon oltandóknál, akik thrombocytopeniások vagy vérzési rendellenességük van, az oltás subcutan beadható. Mindamellett ez a beadási mód az optimálisnál kisebb immunválaszt eredményezhet (lásd 4.4 pont). 4.3 Ellenjavallatok A hatóanyaggal vagy bármely segédanyaggal vagy neomicinnel szembeni túlérzékenység. Hepatitis A vagy hepatitis B vakcina korábbi beadása után észlelt túlérzékenység. A Twinrix Felnőtt készítmény beadását el kell halasztani akut, súlyos, lázas betegségben. 4.4 Különleges figyelmeztetések és az alkalmazással kapcsolatos óvintézkedések A tűszúrásra adott pszichés válaszként bármilyen oltás után vagy akár az oltás előtt is ájulás fordulhat elő, különösen serdülőknél. Az eszmélet visszanyerése alatt ezt több neurológiai tünet is kísérheti, mint például átmeneti látászavar, paraesthesia és tonusos-clonusos végtagmozgások. Fontos, hogy az ájulásból eredő sérülés elkerülése érdekében a beavatkozások megfelelő helyen történjenek. Lehetséges, hogy egyes egyének a hepatitis A vagy hepatitis B fertőzés inkubációs periódusában vannak a vakcina beadásakor. Nem ismert, hogy ilyen esetekben a Twinrix Adult kivédi-e a hepatitis A és hepatitis B megbetegedést. 3
4 A vakcina nem védi ki az egyéb ágensek, mint pl. hepatitis C, hepatitis E és más, ismerten a máj fertőzését eredményező - kórokozók által előidézett fertőzéseket. A Twinrix Felnőtt nem ajánlott posztexpozíciós prophylaxis (pl. injekciós tű okozta sérülés) céljára. A vakcinát nem vizsgálták immunkárosodott betegek esetén. Hemodializált betegekben és immunkárosodott egyéneknél nem alakul ki a védettséget biztosító anti-hav és anti-hbs ellenanyagmennyiség az alapimmunizálás során, ezért ezeknek a betegeknek további oltóanyag-adagokra lehet szükségük. Megfigyelték, hogy az obesitás (meghatározása szerint a BMI 30 kg/m 2 ) csökkenti a hepatitis A vakcinákra adott immunválaszt. Több tényezőnél megfigyelték, hogy csökkenti a hepatitis B vakcinára adott immunválaszt. Ezek a tényezők az idősebb életkor, hímnem, elhízottság, dohányzás, beadás módja, valamint néhány krónikus fekvőbetegség. Meg kell fontolni szerológiai vizsgálat elvégzését azoknál az oltandóknál, akiknél felmerül annak rizikója, hogy a teljes sorozat Twinrix Felnőtt vakcinával történt oltás után nem alakul ki megfelelő szeroprotekció. További dózisok adása megfontolandó azoknál az oltottaknál, akiknél nem alakult ki vagy nem optimális az immunválasz az oltás beadását követően. Mint minden injekciós vakcina esetén, megfelelően fel kell készülni a vakcina beadását követő ritkán fellépő anaphylaxiás események kivédésére. Minthogy az intradermálisan vagy a glutealis régióba intramusculárisan adott injekció esetleg nem eredményezi az optimális immunválasz kialakulását, ezen beadási módoktól tartózkodni kell. Mindazonáltal, kivételes esetekben, a Twinrix Felnőtt beadható subcutan is thrombocytopeniában vagy vérzési rendellenességekben szenvedőknek, minthogy ezen felnőttek intramuscularis oltása vérzést eredményezhet. (lásd: 4.2 pont) A TWINRIX FELNŐTT SEMMILYEN ESETBEN SEM ADHATÓ INTRAVASCULARISAN! Mint minden oltásnál, az oltottaknál a kellő immunválasz nem minden esetben alakul ki. 4.5 Gyógyszerkölcsönhatások és egyéb interakciók Nincsenek adatok a Twinrix Felnőtt valamint hepatitis A vagy hepatitis B specifikus immunglobulin együttes alkalmazásáról. Ugyanakkor, ha a monovalens hepatitis A és hepatitis B vakcina beadásával egyidejűleg specifikus immunglobulinokat is adtak, nem észleltek hatást a szerokonverzióra, bár ez az alkalmazási mód alacsonyabb ellenanyagtitereket eredményezhet. Mivel a Twinrix Felnőtt és más vakcinák együttes beadásával kapcsolatos vizsgálatokat nem végeztek, várható, hogy a különböző injekciós helyekre, különböző fecskendőkkel beadott készítmények egymással kölcsönhatásba nem lépnek. Immunszupresszív terápiában részesülő vagy immunhiányos betegeknél előfordul, hogy megfelelő immunválasz nem alakul ki. 4.6 Termékenység, terhesség és szoptatás Terhesség A Twinrix Felnőtt embrionális/magzati, perinatális és posztnatális túlélésre és fejlődésre gyakorolt hatását patkányokon tanulmányozták. Ez a vizsgálat nem utal a fertilitást, a terhességet, az embrionális/magzati fejlődést, szülést vagy a szülés utáni fejlődést közvetlenül vagy közvetett módon károsan befolyásoló hatásra. 4
5 Nem végeztek prospektív klinikai vizsgálatokat a Twinrix Felnőtt embrionális/magzati, perinatális és posztnatális túlélésre és fejlődésre gyakorolt hatásának értékelése céljából. A vakcinált nők körében limitált számban előforduló terhesség kimenetelére vonatkozó adatok alapján a Twinrix Felnőtt nem gyakorol nemkívánatos hatást sem a terhességre, sem a magzat/újszülött egészségi állapotára. Bár nem várható, hogy a rekombináns hepatitis B vírus felületi antigén nemkívánatos hatást fejtene ki a terhességre vagy a magzatra, ajánlatos a vakcinációt a szülés utánra halasztani, kivéve, ha az anyát sürgősen hepatitis B fertőzés elleni védelemben kell részesíteni. Szoptatás Nem ismert, hogy a Twinrix Felnőtt kiválasztódik-e az anyatejbe. Állatokon nem vizsgálták a Twinrix Felnőtt tejbe történő kiválasztódását. Annak eldöntésénél, hogy a Twinrix Felnőtt alkalmazása alatt folytassák vagy felfüggesszék a szoptatást, mérlegelni kell a szopás előnyét a csecsemő, valamint a Twinrix Felnőtt kezelés előnyét az anya számára. 4.7 A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre A Twinrix Felnőtt vakcia nem vagy csak elhanyagolható mértékben befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességet. 4.8 Nemkívánatos hatások, mellékhatások Klinikai vizsgálatok Az alábbiakban bemutatott biztonságossági profil egy, több mint 6000 oltotton, az adagonkénti események összevont elemzésén alapul, akiket a 0, 1, 6 hónapos standard séma (n = 5683) vagy a gyorsított, 0, 7, 21 napos séma szerint (n = 320) oltottak. Abban a két klinikai vizsgálatban, amelyekben a 0, 7, 21 napos séma szerint oltottak, az oltással összefüggésbe hozható összes általános és helyi reakciót az alábbiakban meghatározott gyakorisági kategóriák szerint jelentették. A negyedik adagnak a 12. hónapban történt beadása után a szisztémás és helyi mellékhatások incidenciája hasonló volt a 0., 7., 21. napon történt beadáskor tapasztaltakéval. Összehasonlító vizsgálatokban megállapították, hogy a Twinrix Felnőtt vakcina beadását követő jelentett, nem kívánt mellékhatások gyakorisága nem különbözött a monovalens vakcina beadását követő jelentett nem kívánt mellékhatások gyakoriságától. Az előfordulási gyakoriságok: Nagyon gyakori: 1/10 Gyakori: 1/100 és 1/10 Nem gyakori: 1/1000 és 1/100 Ritka: 1/ és 1/1000 Nagyon ritka: 1/ * a gyermekeknek szánt készítménnyel végzett klinikai vizsgálatokban észlelt mellékhatásokra vonatkozik Vérképzőszervi és nyirokrendszeri betegségek és tünetek ritka: lymphadenopathia Idegrendszeri betegségek és tünetek nagyon gyakori: fejfájás nem gyakori: szédülés ritka: hypaesthesia, paraesthesia Emésztőrendszeri betegségek és tünetek 5
6 gyakori: emésztőrendszeri tünetek, hasmenés, hányinger nem gyakori: hányás, hasi fájdalom* A bőr és a bőralatti szövet betegségei és tünetei ritka: kiütés,viszketés nagyon ritka: csalánkiütés A csont- ésizomrendszer, valamint a kötőszövet betegségei és tünetei nem gyakori: myalgia ritka: arthralgia Anyagcsere- és táplálkozási betegségek és tünetek ritka: étvágy csökkenés Fertőző betegségek és parazitafertőzések nem gyakori: felsőlégúti fertőzés Érbetegségek és tünetek ritka: hypotensio Általános tünetek, az alkalmazás helyén fellépő reakciók nagyon gyakori: fájdalom és bőrpír a beadás helyén, fáradtság gyakori: duzzanat a beadás helyén, helyi reakciók a beadás helyén (hematóma, viszketés és bőrbevérzés), rossz közérzet nem gyakori: láz ( 37,5 C) ritka: influenzaszerű megbetegedés, hidegrázás Posztmarketing surveillance A Twinrix vagy a GlaxoSmithKline monovalens hepatitis A vagy hepatitis B vakcinák alkalmazását követően az alábbi mellékhatásokat jelentették Vérképzőszervi és nyirokrendszeri betegségek és tünetek thrombocytopenia, thrombocytopeniás purpura Idegrendszeri betegségek és tünetek encephalitis, encephalopathia, neuritis, neuropathia, paralysis, convulsiók A bőr és a bőr alatti szövet betegségei és tünetei angioneurotikus oedema, övsömör, erythema multiforme A csont-izomrendszer és a kötőszövet betegségei és tünetei arthritis, izomgyengeség Fertőző betegségek és parazitafertőzések meningitis Érbetegségek és tünetek vasculitis Immunrendszeri betegségek és tünetek anafilaxia, allergiás reakciók, beleértve az anafilaxiás és anafilaktoid reakciókat és a szérumbetegség jellegű megbetegedéseket A monovalens hepatitis A és/vagy hepatitis B vakcinák széleskörű alkalmazását követően a következő nem kívánt eseményekről számoltak be napokkal vagy hetekkel a vakcináció után, azzal összefüggésben. 6
7 Laboratóriumi vizsgálatok eredményei kóros majfunkciós vizsgálati eredmények Idegrendszeri betegségek és tünetek sclerosis multiplex, myelitis, facialis paresis, polyneuritis mint Guillain-Barré-szindróma (felszálló paralysissel), látóideg-gyulladás Általános tünetek, az alkalmazás helyén fellépő reakciók Az injekció beadási helyén azonnal jelentkező fájdalom,szúró és égető érzés 4.9 Túladagolás Túladagolásról a posztmarketing surveillance során beszámoltak. A túladagolás után jelentett mellékhatások azonosak voltak az oltóanyag szokásos adagoláskor észlelt mellékhatásokkal. 5. FARMAKOLÓGIAI TULAJDONSÁGOK 5.1 Farmakodinámiás tulajdonságok Farmakoterápiás csoport: hepatitis vakcinák, ATC kód: J07BC20 A Twinrix Felnőtt kombinált vakcina, amelyet a tisztított, inaktivált hepatitis A (HA) vírus és a tisztított hepatitis B felületi antigén (HBsAg) külön-külön előállított és a HA esetében alumíniumhidroxidra, míg a HBsAg esetében alumínium-foszfátra adszorbeált termelési egységeinek elegyítésével állítanak elő. A HA vírust MRC 5 jelű humán diploid sejteken, a HBsAg-t genetikailag módosított élesztősejteken speciális közegben szaporított kultúrában állítják elő. A Twinrix Felnőtt HAV és HBV fertőzések elleni védettséget vált ki specifikus anti-hav és anti-hbs ellenanyagok képződésének indukálása révén. A hepatitis A és hepatitis B fertőzések elleni védettség 2-4 héten belül alakul ki. A klinikai vizsgálatokban hepatitis A elleni specifikus keringő ellenanyagok a felnőttek megközelítőleg 94 %- ában kialakultak 1 hónappal az első adag beadása után, míg 1 hónappal a harmadik adag beadása után (kb. A 7. hónapban) az oltottak 100 %-ában volt kimutatható ellenanyag. A hepatitis B elleni specifikus keringő ellenanyagot 1 hónappal az első adag beadása után a felnőttek 70 %-ában, míg a harmadik adag beadása után kb 99%-ában lehet kimutatni. A 0, 7 és 21 napos séma szerinti alapimmunizálásra és a negyedik adagnak a12 hónapban történő beadadására csak különleges körülmények között került sor felnőtteknél. Klinikai vizsgálatokban, amikor a Twinrix Felnőtt vakcinát ezen alapimmunizálási séma szerint alkalmazták, az oltottak 82%- ánál és 85%-ánál alakult ki anti-hbv antitest szeroprotektív szintje az első és az 5. héten a harmadik adag beadását követően (vagyis 1. ill. 2. hónappal a kezdő adag beadását követően). A hepatitis B elleni szeroprotekció 95,1%-ra emelkedett az első adag beadását követően három hónap elteltével. Az anti-hav antitest szeropozitivitás 100%, 99,5% és 100% volt a kezdeti adagot követő első, második és harmadik hónapban. A negyedik adag beadása után egy hónappal az összes oltottnál kialakult az anti-hbs antitest szeroprotekció és az anti-hav szeropozitívitás. Egy klinikai vizsgálatban, melyet 40 évesnél idősebb oltottakon végeztek, az anti-hav antitestek szeropozitivitási arányát és a hepatitis B elleni szeroprotekciót vizsgálták Twinrix Felnőtt vakcina 0, 1, 6 hónapos oltási sémának megfelelő adagolását követően, és a szeropozitivitási és szeroprotekciós arányokkal hasonlították össze, amiket monovalens hepatitis A és B vakcinák egyidejű, ellentétes karba történő adása után nyertek. 7
8 A hepatitis B-vel szembeni szeroprotekciós arány a Twinrix Felnőtt adását követően 92% volt a 7. hónapban, illetve 56% volt a 48. hónapban, szemben a GlaxoSmithKline Biologicals 20 µg-os, monovalens hepatitis B elleni vakcinájának adása után észlelt 80%-kal, illetve 43%-kal, valamint egy másik 10 µg-os, engedélyezett, hepatitis B elleni monovalens vakcina adása után észlelt 71%-os illetve 31%-os értékekkel. Az anti-hbs antitest koncentráció az életkor és a testtömeg-index növekedésével csökkent, és alacsonyabb volt férfiaknál, mint nőknél. Az anti-hav ellenanyagok szeropozitivitási aránya Twinrix Felnőtt adása után 97% volt mind a 7., mind a 48. hónapban, szemben a GlaxoSmithKline Biologicals monovalens hepatitis A vakcinájának adása után észlelt, sorrendben 99%-os, illetve 93%-os értékekkel (azonos időpontokban meghatározva), valamint egy másik, engedélyezett monovalens hepatitis A vakcina adása után észlelt 99%-os, illetve 97%-os értékkel. Az alanyok ugyanabból az oltás(ok)ból 48 hónappal az alapimmunizálás első adagja után egy emlékeztető adagot kaptak. Egy hónappal ezután az adag után a Twinrix Felnőtt-tel oltottak 95%-ánál az anti-hbv antitest szeroprotektív szintet ( 10 mne/ml) ért el, és a geometriai átlagkoncentráció (Geometric Mean Concentrations [GMC]) a 179-szeresére (a GMC 7234 mne/ml-re) nőtt, amely az immun memória kialakulását bizonyítja. Két hosszútávú, 17 és 43 év közötti felnőtteken végzett klinikai vizsgálatban a Twinrix Felnőtt vakcinával történő alapimmunizálást követően 15 év múlva 56 betegnek volt értékelhető vizsgálati eredménye. Az anti-hav szeropozitivitás aránya mindkét vizsgálatban100% volt, míg az anti-hbs szeroprotekciós arány sorrendben 89,3%, illetve 92,9% volt. A HAV és antihbs ellenanyag csökkenés kinetikája azonos volt a monovalens vakcinákéval. 5.2 Farmakokinetikai tulajdonságok Farmakokinetikai sajátosságok értékelése vakcinák esetében nem előírt. 5.3 A preklinikai biztonságossági vizsgálatok eredményei Az általános biztonságossági vizsgálatokból származó nem klinikai jellegű adatok azt igazolták, hogy a készítmény nem jelent különleges veszélyt az emberre (lásd 4.6 pont). 6. GYÓGYSZERÉSZETI JELLEMZŐK 6.1 Segédanyagok felsorolása Nátrium-klorid, Injekcióhoz való víz. Adjuvánsokat lásd 2. pontban 6.2 Inkompatibilitások Kompatibilitási vizsgálatok hiányában ez a gyógyszer nem keverhető más gyógyszerekkel. 6.3 Felhasználhatósági időtartam 3 év 6.4 Különleges tárolási előírások Hűtőszekrényben (2 C 8 C) tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 8
9 6.5 Csomagolás típusa és kiszerelése 1 ml szuszpenzió butil-gumidugóval lezárt (I típusú üveg) injekciós üvegben. 1x, 10x és 25x csomagolások. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba. 6.6 A megsemmisítésre vonatkozó különleges óvintézkedések és egyéb, a készítmény kezelésével kapcsolatos információk A tárolás során finom fehér üledék és tiszta, színtelen felülúszó megfigyelhető. Beadás előtt a vakcinát alaposan fel kell rázni amíg enyhén opálos, fehér szuszpenzió nem keletkezik, illetve ellenőrizni kell, hogy nem látható-e a készítményben idegen részecske és/vagy a fizikai megjelenése nem szokatlan-e. Ha bármelyik előfordulna, a vakcina nem használható fel. Bármilyen fel nem használt készítmény, illetve hulladékanyag megsemmisítését a helyi előírások szerint kell végrehajtani. 7. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgium 8. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/004 EU/1/96/020/005 EU/1/96/020/ A FORGALOMBA HOZATALI ENGEDÉLY ELSŐ KIADÁSÁNAK/ MEGÚJÍTÁSÁNAK DÁTUMA A forgalomba hozatali engedély első kiadásának dátuma: szeptember 20. A forgalomba hozatali engedély megújításának dátuma: szeptember A SZÖVEG ELLENŐRZÉSÉNEK DÁTUMA 9
10 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (1 ml) vakcina Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú lumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al 3+ A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Szuszpenziós injekció. Zavaros fehér szuszpenzió. 4. KLINIKAI JELLEMZŐK 4.1 Terápiás javallatok A Twinrix Felnőtt alkalmazása hepatitis A és hepatitis B vírusfertőzés kockázatának kitett és erre fogékony felnőttek és 16 éves kor feletti serdülők számára javallott. 4.2 Adagolás és alkalmazás Alkalmazás - Adagolás Egy 1 ml-es adag ajánlott felnőtteknek és 16 éves vagy idősebb serdülőknek. - Alapimmunizálás Az alapimmunizálás általánosan ajánlott sémája szerinti adagolás 3 adag Twinrix Felnőtt beadásából áll, az első adagot egy választott napon, a második adagot 1 hónap múlva, a harmadik adagot az első adag beadása után 6 hónappal kell beadni. Különleges esetekben felnőtteknél, ha valaki elutazik 1 vagy több hónapon belül az első oltást követően, és nincs elegendő idő a 0, 1, 6 hónapos oltási séma szerinti oltáshoz, 3 intramuscularis injekciót kell beadni a 0., 7. és a 21. napon. Ebben az esetben 4. oltás beadása javasolt, az első oltás beadását követően 12 hónappal. Az ajánlott sémát be kell tartani. Az első adag beadása után az alapimmunizálás további adagjainak beadásakor ugyanazt a vakcinát kell használni. 10
11 - Emlékeztető oltások Az ellenanyagok hosszútávú, perzisztálását igazoló adatok a Twinrix Felnőtt vakcina beadása után legfeljebb 15 évre vonatkoznak. Az alapimmunizálást követően az anti-hbs és anti-hav ellenanyagok mért értékei a kombinált vakcinák alkalmazása során abban az értéktartományban vannak, amelyet a monovalens vakcinákkal történő oltás után lehet elérni. Az ellenanyag csökkenés kinetikája is hasonló. Az emlékeztető oltásokra vonatkozó általános ajánlásokat így a monovalens vakcinákkal kapott tapasztalatok alapján lehet megadni. Hepatitis B Azon egészséges egyének részére, akik teljes alapimmunizálásban részesültek, emlékeztető oltások nem szükségesek. Azonban néhány kötelező védőoltási program magában foglalja az emlékeztető oltást, amit figyelembe kell venni. HBV fertőzésnek kitett egyének vagy betegek néhány csoportjában (pl. hemodializált vagy károsodott immunrendszerű betegek), megfontolandó a védelmet biztosító 10 NE/l antitestszint biztosítása. Hepatitis A Nem alakult ki egységes állásfoglalás arról, hogy egészséges immunitású egyéneknél, akik a hepatitis A oltásra reagálnak, szükséges-e emlékeztető oltások adása, amikor ellenanyag ugyan nem mutatható ki de az immunmemória védettséget biztosíthat. Az emlékeztető oltást szorgalmazó ajánlás azon a feltevésen alapul, hogy az ellenanyagok szükséges a védelemhez; a hepatitis A ellenes ellenanyagok számítások alapján legalább 10 éven át kimutathatók a szervezetben. Azon esetekben, amikor mind hepatitis A, mind hepatitis B emlékeztető oltásra szükség van, Twinrix Felnőtt adható. Másik lehetőség, hogy Twinrix Felnőtt vakcinával alapimmunizált egyének emlékeztető oltására a két monovalens vakcinát alkalmazzuk. Az alkalmazás módja A Twinrix Felnőtt intarmuscularis injekció, célszerű deltoid régióba beadni. Kivételes esetekben azon oltandóknál, akik thrombocytopeniások vagy vérzési rendellenességük van, az oltás subcutan beadható. Mindamellett ez a beadási mód az optimálisnál kisebb immunválaszt eredményezhet (lásd 4.4.pont). 4.3 Ellenjavallatok A hatóanyaggal vagy bármely segédanyaggal vagy neomicinnel szembeni túlérzékenység. Hepatitis A vagy hepatitis B vakcina korábbi beadása után észlelt túlérzékenység. A Twinrix Felnőtt készítmény beadását el kell halasztani akut, súlyos, lázas betegségben. 4.4 Különleges figyelmeztetések és az alkalmazással kapcsolatos óvintézkedések A tűszúrásra adott pszichés válaszként bármilyen oltás után vagy akár az oltás előtt is ájulás fordulhat elő, különösen serdülőknél. Az eszmélet visszanyerése alatt ezt több neurológiai tünet is kísérheti, mint például átmeneti látászavar, paraesthesia és tonusos-clonusos végtagmozgások. Fontos, hogy az ájulásból eredő sérülés elkerülése érdekében a beavatkozások megfelelő helyen történjenek. Lehetséges, hogy egyes egyének a hepatitis A vagy hepatitis B fertőzés inkubációs periódusában vannak a vakcina beadásakor. Nem ismert, hogy ilyen esetekben a Twinrix Felnőtt kivédi-e a hepatitis A és hepatitis B megbetegedést. 11
12 A vakcina nem védi ki az egyéb ágensek, mint pl. hepatitis C, hepatitis E és más, ismerten a máj fertőzését eredményező - kórokozók által előidézett fertőzéseket. A Twinrix Felnőtt nem ajánlott posztexpozíciós prophylaxis (pl. injekciós tű okozta sérülés) céljára. A vakcinát nem vizsgálták immunkárosodott betegek esetén. Hemodializált betegekben és immunkárosodott egyéneknél nem alakul ki a védettséget biztosító anti-hav és anti-hbs ellenanyagmennyiség az alapimmunizálás során, ezért ezeknek a betegeknek további oltóanyag-adagokra lehet szükségük. Megfigyelték, hogy az obesitás (meghatározása szerint a BMI 30 kg/m 2 ) csökkenti a hepatitis A vakcinákra adott immunválaszt Több tényezőnél megfigyelték, hogy csökkenti a hepatitis B vakcinára adott immunválaszt. Ezek a tényezők az idősebb életkor, hímnem, elhízottság, dohányzás, beadás módja, valamint néhány krónikus fekvőbetegség. Meg kell fontolni szerológiai vizsgálat elvégzését azoknál az oltandóknál, akiknél felmerül annak rizikója, hogy a teljes sorozat Twinrix Felnőtt vakcinával történt oltás után nem alakul ki megfelelő szeroprotekció. További dózisok adása megfontolandó azoknál az oltottaknál, akiknél nem alakult ki vagy nem optimális az immunválasz az oltás beadását követően. Mint minden injekciós vakcina esetén, megfelelően fel kell készülni a vakcina beadását követő ritkán fellépő anaphylaxiás események kivédésére. Minthogy az intradermálisan vagy a glutealis régióba intramusculárisan adott injekció esetleg nem eredményezi az optimális immunválasz kialakulását, ezen beadási módoktól tartózkodni kell. Mindazonáltal, kivételes esetekben, a Twinrix Felnőtt beadható subcutan thrombocytopeniában vagy vérzési rendellenességekben szenvedőknek, minthogy ezen felnőttek intramuscularis oltása vérzést eredményezhet. (lásd: 4.2 pont) A TWINRIX FELNŐTT SEMMILYEN ESETBEN SEM ADHATÓ INTRAVASCULARISAN! Mint minden oltásnál az oltottaknál a kellő immunválasz nem minden esetben alakul ki. 4.5 Gyógyszerkölcsönhatások és egyéb interakciók Nincsenek adatok a Twinrix Felnőtt valamint hepatitis A vagy hepatitis B specifikus immunglobulin együttes alkalmazásáról. Ugyanakkor, ha a monovalens hepatitis A és hepatitis B vakcina beadásával egyidejűleg specifikus immunglobulinokat is adtak, nem észleltek hatást a szerokonverzióra, bár ez az alkalmazási mód alacsonyabb ellenanyagtitereket eredményezhet. Mivel a Twinrix Felnőtt és más vakcinák együttes beadásával kapcsolatos vizsgálatokat nem végeztek, várható, hogy a különböző injekciós helyekre, különböző fecskendőkkel beadott készítmények egymással kölcsönhatásba nem lépnek. Immunszupresszív terápiában részesülő vagy immunhiányos betegeknél előfordul, hogy megfelelő immunválasz nem alakul ki Termékenység, terhesség és szoptatás Terhesség A Twinrix Felnőtt embrionális/magzati, perinatális és posztnatális túlélésre és fejlődésre gyakorolt hatását patkányokon tanulmányozták. Ez a vizsgálat nem utal a fertilitást, a terhességet, az embrionális/magzati fejlődést, szülést vagy a szülés utáni fejlődést közvetlenül vagy közvetett módon károsan befolyásoló hatásra. 12
13 Nem végeztek prospektív klinikai vizsgálatokat a Twinrix Felnőtt embrionális/magzati, perinatális és posztnatális túlélésre és fejlődésre gyakorolt hatásának értékelése céljából. A vakcinált nők körében limitált számban előforduló terhesség kimenetelére vonatkozó adatok alapján a Twinrix Felnőtt nem gyakorol nemkívánatos hatást sem a terhességre, sem a magzat/újszülött egészségi állapotára. Bár nem várható, hogy a rekombináns hepatitis B vírus felületi antigén nemkívánatos hatást fejtene ki a terhességre vagy a magzatra, ajánlatos a vakcinációt a szülés utánra halasztani, kivéve, ha az anyát sürgősen hepatitis B fertőzés elleni védelemben kell részesíteni. Szoptatás Nem ismert, hogy a Twinrix Felnőtt kiválasztódik-e az anyatejbe. Állatokon nem vizsgálták a Twinrix Felnőtt tejbe történő kiválasztódását. Annak eldöntésénél, hogy a Twinrix Felnőtt alkalmazása alatt folytassák vagy felfüggesszék a szoptatást, mérlegelni kell a szopás előnyét a csecsemő, valamint a Twinrix Felnőtt kezelés előnyét az anya számára. 4.7 A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre A Twinrix Felnőtt vakcia nem vagy csak elhanyagolható mértékben befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességet. 4.8 Nemkívánatos hatások, mellékhatások Klinikai vizsgálatok Az alábbiakban bemutatott biztonságossági profil egy, több mint 6000 oltotton, az adagonkénti események összevont elemzésén alapul, akiket a 0, 1, 6 hónapos standard séma (n = 5683) vagy a gyorsított, 0, 7, 21 napos séma szerint (n = 320) oltottak. Abban a két klinikai vizsgálatban, amelyekben a 0, 7, 21 napos séma szerint oltottak, az oltással összefüggésbe hozható összes általános és helyi reakciót az alábbiakban meghatározott gyakorisági kategóriák szerint jelentették. A negyedik adagnak a 12. hónapban történt beadása után a szisztémás és helyi mellékhatások incidenciája hasonló volt a 0., 7., 21. napon történt beadáskor tapasztaltakéval. Összehasonlító vizsgálatokban megállapították, hogy a Twinrix Felnőtt vakcina beadását követő jelentett, nem kívánt mellékhatások gyakorisága nem különbözött a monovalens vakcina beadását követő jelentett nem kívánt mellékhatások gyakoriságától. Az előfordulási gyakoriságok: Nagyon gyakori: 1/10 Gyakori: 1/100 és 1/10 Nem gyakori: 1/1000 és 1/100 Ritka: 1/ és 1/1000 Nagyon ritka: 1/ * a gyermekeknek szánt készítménnyel végzett klinikai vizsgálatokban észlelt mellékhatásokra vonatkozik Vérképzőszervi és nyirokrendszeri betegségek és tünetek ritka: lymphadenopathia Idegrendszeri betegségek és tünetek nagyon gyakori: fejfájás nem gyakori: szédülés ritka: hypaesthesia, paraesthesia Emésztőrendszeri betegségek és tünetek 13
14 gyakori: emésztőrendszeri tünetek, hasmenés, hányinger nem gyakori: hányás, hasi fájdalom* A bőr és a bőralatti szövet betegségei és tünetei ritka: kiütés,viszketés nagyon ritka: csalánkiütés A csont-izomrendszer és a kötőszövet betegségei és tünetei nem gyakori: myalgia ritka: arthralgia Anyagcsere- és táplálkozási betegségek és tünetek ritka: étvágy csökkenés Fertőző betegségek és parazitafertőzések nem gyakori: felsőlégúti fertőzés Érbetegségek és tünetek ritka: hypotensio Általános tünetek, az alkalmazás helyén fellépő reakció nagyon gyakori: fájdalom és bőrpír a beadás helyén, fáradtság gyakori: duzzanat a beadás helyén, helyi reakciók a beadás helyén (hematóma, viszketés és bőrbevérzés), rossz közérzet nem gyakori: láz ( 37,5 C) ritka: influenza-szerű megbetegedés, hidegrázás Posztmarketing surveillance A Twinrix vagy egyéb GlaxoSmithKline monovalens hepatitis A vagy hepatitis B vakcinák alkalmazását követően az alábbi mellékhatásokat jelentették Vérképzőszervi és nyirokrendszeri betegségek és tünetek thrombocytopenia, thrombocytopeniás purpura Idegrendszeri betegségek és tünetek encephalitis, encephalopathia, neuritis, neuropathia, paralysis, convulsiók A bőr és a bőr alatti szövetk betegségei és tünetei angioneurotikus oedema, övsömör, erythema multiforme A csont- és izomrendszer, valamint a kötőszövet betegségei és tünetei arthritis, izomgyengeség Fertőző betegségek és parazitafertőzések meningitis Érbetegségek és tünetek vasculitis Immunrendszeri betegségek és tünetek anafilaxia, allergiás reakciók, beleértve az anafilaxiás és anafilaktoid reakciókat és a szérumbetegség jellegű megbetegedéseket A monovalens hepatitis A és/vagy hepatitis B vakcinák széleskörű alkalmazását követően a következő nem kívánt eseményekről számoltak be napokkal vagy hetekkel a vakcináció után, azzal összefüggésben. 14
15 Laboratóriumi vizsgálatok eredményei kóros majfunkciós vizsgálati eredmények Idegrendszeri betegségek és tünetek sclerosis multiplex, myelitis, facialis paresis, polyneuritis mint Guillain-Barré-szindróma (felszálló paralysissel), látóideg-gyulladás Általános tünetek, az alkalmazás helyén fellépő reakciók Az injekció beadási helyén azonnal jelentkező fájdalom,szúró és égető érzés 4.9 Túladagolás Túladagolásról a posztmarketing surveillance során beszámoltak. A túladagolás után jelentett mellékhatások azonosak voltak az oltóanyag szokásos adagoláskor észlelt mellékhatásokkal. 5. FARMAKOLÓGIAI TULAJDONSÁGOK 5.1 Farmakodinámiás tulajdonságok Farmakoterápiás csoport: hepatitis vakcinák, ATC kód: J07BC20 A Twinrix Felnőtt kombinált vakcina, amelyet a tisztított, inaktivált hepatitis A (HA) vírus és a tisztított hepatitis B felületi antigén (HBsAg) külön-külön előállított és a HA esetében alumíniumhidroxidra, míg a HBsAg esetében alumínium-foszfátra adszorbeált termelési egységeinek elegyítésével állítanak elő. A HA vírust MRC 5 jelű humán diploid sejteken, a HBsAg-t genetikailag módosított élesztősejteken speciális közegben szaporított kultúrában állítják elő. A Twinrix Felnőtt HAV és HBV fertőzések elleni védettséget vált ki specifikus anti-hav és anti-hbs ellenanyagok képződésének indukálása révén. A hepatitis A és hepatitis B fertőzések elleni védettség 2-4 héten belül alakul ki. A klinikai vizsgálatokban hepatitis A elleni specifikus keringő ellenanyagok a felnőttek megközelítőleg 94 %- ában kialakultak 1 hónappal az első adag beadása után, míg 1 hónappal a harmadik adag beadása után (kb. A 7. hónapban) az oltottak 100 %-ában volt kimutatható ellenanyag. A hepatitis B elleni specifikus keringő ellenanyagot 1 hónappal az első adag beadása után a felnőttek 70 %-ában, míg a harmadik adag beadása után kb 99%-ában lehet kimutatni. A 0, 7 és 21 napos séma szerinti alapimmunizálásra és a negyedik adagnak a12 hónapban történő beadadására csak különleges körülmények között került sor felnőtteknél. Klinikai vizsgálatokban, amikor a Twinrix Felnőtt vakcinát ezen alapimmunizálási séma szerint alkalmazták, az oltottak 82%- ánál és 85%-ánál alakult ki anti-hbv antitest szeroprotektív szintje az első és az 5. héten a harmadik adag beadását követően (vagyis 1. ill. 2. hónappal a kezdő adag beadását követően). A hepatitis B elleni szeroprotekció 95,1%-ra emelkedett az első adag beadását követően három hónap elteltével. Az anti-hav antitest szeropozitivitás 100%, 99,5% és 100% volt a kezdeti adagot követő első, második és harmadik hónapban. A negyedik adag beadása után egy hónappal az összes oltottnál kialakult az anti-hbs antitest szeroprotekció és az anti-hav szeropozitívitás. Egy klinikai vizsgálatban, melyet 40 évesnél idősebb oltottakon végeztek, az anti-hav szeropozitivitási arányt és a hepatitis B elleni szeroprotekciót vizsgálták Twinrix Felnőtt vakcina 0,1,6 hónapos oltási sémának megfelelő adagolását követően, és ezen adatokat azokkal hasonlították össze, amiket monovalens hepatitis A és B vakcinák egyidejű, ellentétes karba történő adása után nyertek. A hepatitis B-vel szembeni szeroprotekciós arány Twinrix adását követően 92 % illetve 56 % volt a 7. hónapban, illetve 56% volt a 48. hónapban, szemben a GlaxoSmithKline Biologicals 20µg-os, 15
16 monovalens hepatitis B elleni vakcinájának adása után észlelt 80% illetve 43 %-kal, valamint egy másik 10µg-os, monovalens vakcina adása után észlelt 71% illetve 31%-os értékekkel. Az anti-hbs antitest koncentráció alacsonyabb volt, ha az életkor és a testtömeg index növekedett, és alacsonyabb volt férfiaknál, mint nőknél. Az anti-hav ellenanyagok szeropozitivitási aránya Twinrix Felnőtt adása után 97% volt mind a 7., mind a 48. hónapban, szemben a GlaxoSmithKline Biologicals monovalens hepatitis A vakcina adása után észlelt 99% illetve 93%-os értékekkel (azonos időpontokban meghatározva), valamint egy másik gyártó monovalens hepatitis A vakcinájának adása után 99%-os, illetve 97%-os értékkel. Az alanyok ugyanabból az oltás(ok)ból 48 hónappal az alapimmunizálás első adagja után egy emlékeztető adagot kaptak. Egy hónappal ezután az adag után a Twinrix Felnőtt-tel oltottak 95%-ánál az anti-hbv antitest szeroprotektív szintet ( 10 mne/ml) ért el, és a geometriai átlagkoncentráció (Geometric Mean Concentrations [GMC]) a 179-szeresére (a GMC 7234 mne/ml-re) nőtt, amely az immun memória kialakulását bizonyítja. Két hosszútávú, 17 és 43 év közötti felnőtteken végzett klinikai vizsgálatban a Twinrix Felnőtt vakcinával történő alapimmunizálást követően 15 év múlva 56 betegnek volt értékelhető vizsgálati eredménye. Az anti-hav szeropozitivitás aránya mindkét vizsgálatban100% volt, míg az anti-hbs szeroprotekciós arány sorrendben 89,3%, illetve 92,9% volt.. A HAV és anti-hbs ellenanyag csökkenés kinetikája azonos a monovalens vakcinákéval. 5.2 Farmakokinetikai tulajdonságok Farmakokinetikai sajátosságok értékelése vakcinák esetében nem előírt. 5.3 A preklinikai biztonságossági vizsgálatok eredményei Az általános biztonságossági vizsgálatokból származó nem klinikai jellegű adatok azt igazolták, hogy a készítmény nem jelent különleges veszélyt az emberre (lásd 4.6 pont). 6. GYÓGYSZERÉSZETI JELLEMZŐK 6.1 Segédanyagok felsorolása Nátrium-klorid, Injekcióhoz való víz. Adjuvánsokat lásd 2. pontban 6.2 Inkompatibilitások Kompatibilitási vizsgálatok hiányában ez a gyógyszer nem keverhető más gyógyszerekkel. 6.3 Felhasználhatósági időtartam 3 év 6.4 Különleges tárolási előírások Hűtőszekrényben (2 C 8 C) tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 6.5 Csomagolás típusa és kiszerelése 16
17 1 ml szuszpenzió előretöltött fecskendőben (I típusú üveg) butil gumidugattyúval lezárva., 1x, 10x és 25x csomagolás injekciós tűvel vagy injekciós tű nélkül. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba. 6.6 A megsemmisítésre vonatkozó különleges óvintézkedések és egyéb, a készítmény kezelésével kapcsolatos információk A tárolás során finom fehér üledék és tiszta, színtelen felülúszó megfigyelhető. Beadás előtt a vakcinát alaposan fel kell rázni amíg enyhén opálos, fehér szuszpenzió nem keletkezik, illetve ellenőrizni kell, hogy nem látható-e a készítményben idegen részecske és/vagy a fizikai megjelenése nem szokatlan-e. Ha bármelyik előfordulna, a vakcina nem használható fel. Bármilyen fel nem használt készítmény, illetve hulladékanyag megsemmisítését a helyi előírások szerint kell végrehajtani. 7. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA GlaxoSmithKline Biologicals s.a. Rue de l Institut Rixensart, Belgium 8. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/001 EU/1/96/020/002 EU/1/96/020/003 EU/1/96/020/007 EU/1/96/020/008 EU/1/96/020/ A FORGALOMBA HOZATALI ENGEDÉLY ELSŐ KIADÁSÁNAK/ MEGÚJÍTÁSÁNAK DÁTUMA A forgalomba hozatali engedély első kiadásának dátuma: szeptember 20. A forgalomba hozatali engedély megújításának dátuma: szeptember A SZÖVEG ELLENŐRZÉSÉNEK DÁTUMA 17
18 II. MELLÉKLET A. A BIOLÓGIAI EREDETŰ HATÓANYAG(OK) GYÁRTÓJA/GYÁRTÓI ÉS A GYÁRTÁSI TÉTELEK VÉGFELSZABADÍTÁSÁÉRT FELELŐS GYÁRTÁSI ENGEDÉLY JOGOSULTJA(I) B. A FORGALOMBA HOZATALI ENGEDÉLYBEN FOGLALT FELTÉTELEK 18
19 A. A BIOLÓGIAI EREDETŰ HATÓANYAG(OK) GYÁRTÓJA/GYÁRTÓI ÉS A GYÁRTÁSI TÉTELEK VÉGFELSZABADÍTÁSÁÉRT FELELŐS GYÁRTÁSI ENGEDÉLY JOGOSULTJA(I) A biológiai eredetű hatóanyag(ok) gyártójának/gyártóinak neve és címe GlaxoSmithKline Biologicals s.a., Rue de l Institut 89, 1330 Rixensart, Belgium A gyártási tételek végfelszabadításáért felelős gyártó(k) neve és címe GlaxoSmithKline Biologicals s.a., Rue de l Institut 89, 1330 Rixensart, Belgium B. A FORGALOMBA HOZATALI ENGEDÉLYBEN FOGLALT FELTÉTELEK A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁRA NÉZVE KÖTELEZŐ FORGALMAZÁSI ÉS RENDELHETŐSÉGI FELTÉTELEK ILLETVE KORLÁTOZÁSOK Orvosi rendelvényhez kötött gyógyszer. FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA Nem értelmezhető. EGYÉB FELTÉTELEK A gyártási tétel hivatalos végfelszabadítása: az Európai Parlament és Tanács módosított 2001/83/EK irányelvének 114. cikkelyének értelmében, a gyártási tétel hivatalos végfelszabadítását egy állami laboratórium vagy egy erre a célra kijelölt laboratórium végezheti. Időszakos Biztonsági Jelentés: A nevezett forgalomba hozatali engedély jogosultjának továbbra is évenként kell benyújtania az Időszakos Biztonsági Jelentést. 19
20 III. MELLÉKLET CÍMKESZÖVEG ÉS BETEGTÁJÉKOZTATÓ 20
21 A. CÍMKESZÖVEG 21
22 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt - szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált) 2. HATÓANYAG(OK) MEGNEVEZÉSE 1 adag (1 ml): Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú alumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al SEGÉDANYAGOK FELSOROLÁSA Nátrium-klorid Injekcióhoz való víz 4. GYÓGYSZERFORMA ÉS TARTALOM Szuszpenziós injekció 1 injekciós üveg 1 adag (1 ml) 5. AZ ALKALMAZÁSSAL KAPCSOLATOS TUDNIVALÓK ÉS AZ ALKALMAZÁS MÓDJA(I) Használat előtt olvassa el a mellékelt tájékoztatót! Intramuscularis alkalmazásra. Használat előtt felrázandó. 6. KÜLÖN FIGYELMEZTETÉS, MELY SZERINT A GYÓGYSZERT GYERMEKEKTŐL ELZÁRVA KELL TARTANI A gyógyszer gyermekektől elzárva tartandó! 7. TOVÁBBI FIGYELMEZTETÉS(EK), AMENNYIBEN SZÜKSÉGES 8. LEJÁRATI IDŐ 22
23 Felhasználható: 9. KÜLÖNLEGES TÁROLÁSI ELŐÍRÁSOK Hűtőszekrényben tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 10. KÜLÖNLEGES ÓVINTÉZKEDÉSEK A FEL NEM HASZNÁLT GYÓGYSZEREK VAGY AZ ILYEN TERMÉKEKBŐL KELETKEZETT HULLADÉKANYAGOK ÁRTALMATLANNÁ TÉTELÉRE, HA ILYENEKRE SZÜKSÉG VAN A megsemmisítés a helyi előírásoknak megfelelően történik. 11. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgium 12. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/ A GYÁRTÁSI TÉTEL SZÁMA Gy.sz.: 14. A GYÓGYSZER ÁLTALÁNOS BESOROLÁSA RENDELHETŐSÉG SZEMPONTJÁBÓL Orvosi rendelvényhez kötött gyógyszer. 15. AZ ALKALMAZÁSRA VONATKOZÓ UTASÍTÁSOK 16. BRAILLE ÍRÁSSAL FELTÜNTETETT INFORMÁCIÓK Braille írás alól felmentve 23
24 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált) 2. HATÓANYAG(OK) MEGNEVEZÉSE 1 adag (1 ml): Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú alumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al SEGÉDANYAGOK FELSOROLÁSA Nátrium-klorid Injekcióhoz való víz. 4. GYÓGYSZERFORMA ÉS TARTALOM Szuszpenziós injekció 10 injekciós üveg 10 x 1 adag 1 adag (1ml) 5. AZ ALKALMAZÁSSAL KAPCSOLATOS TUDNIVALÓK ÉS AZ ALKALMAZÁS MÓDJA(I) Használat előtt olvassa el a mellékelt tájékoztatót! Intramuscularis alkalmazásra. Használat előtt felrázandó. 6. KÜLÖN FIGYELMEZTETÉS, MELY SZERINT A GYÓGYSZERT GYERMEKEKTŐL ELZÁRVA KELL TARTANI A gyógyszer gyermekektől elzárva tartandó! 7. TOVÁBBI FIGYELMEZTETÉS(EK), AMENNYIBEN SZÜKSÉGES 8. LEJÁRATI IDŐ 24
25 Felhasználható: 9. KÜLÖNLEGES TÁROLÁSI ELŐÍRÁSOK Hűtőszekrényben tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 10. KÜLÖNLEGES ÓVINTÉZKEDÉSEK A FEL NEM HASZNÁLT GYÓGYSZEREK VAGY AZ ILYEN TERMÉKEKBŐL KELETKEZETT HULLADÉKANYAGOK ÁRTALMATLANNÁ TÉTELÉRE, HA ILYENEKRE SZÜKSÉG VAN A megsemmisítés a helyi előírásoknak megfelelően történik. 11. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgium 12. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/ A GYÁRTÁSI TÉTEL SZÁMA Gy.sz.: 14. A GYÓGYSZER ÁLTALÁNOS BESOROLÁSA RENDELHETŐSÉG SZEMPONTJÁBÓL Orvosi rendelvényhez kötött gyógyszer. 15. AZ ALKALMAZÁSRA VONATKOZÓ UTASÍTÁSOK 16. BRAILLE ÍRÁSSAL FELTÜNTETETT INFORMÁCIÓK Braille írás alól felmentve 25
26 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B(rDNS) (HAB) vakcina (adszorbeált) 2. HATÓANYAG(OK) MEGNEVEZÉSE 1 adag (1 ml): Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú alumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al SEGÉDANYAGOK FELSOROLÁSA Nátrium-klorid Injekcióhoz való víz 4. GYÓGYSZERFORMA ÉS TARTALOM Szuszpenziós injekció 25 injekciós üveg 25 x 1 adag 1 adag (1ml) 5. AZ ALKALMAZÁSSAL KAPCSOLATOS TUDNIVALÓK ÉS AZ ALKALMAZÁS MÓDJA(I) Használat előtt olvassa el a mellékelt tájékoztatót! Intramuscularis alkalmazásra. Használat előtt felrázandó. 6. KÜLÖN FIGYELMEZTETÉS, MELY SZERINT A GYÓGYSZERT GYERMEKEKTŐL ELZÁRVA KELL TARTANI A gyógyszer gyermekektől elzárva tartandó! 7. TOVÁBBI FIGYELMEZTETÉS(EK), AMENNYIBEN SZÜKSÉGES 8. LEJÁRATI IDŐ 26
27 Felhasználható: 9. KÜLÖNLEGES TÁROLÁSI ELŐÍRÁSOK Hűtőszekrényben tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 10. KÜLÖNLEGES ÓVINTÉZKEDÉSEK A FEL NEM HASZNÁLT GYÓGYSZEREK VAGY AZ ILYEN TERMÉKEKBŐL KELETKEZETT HULLADÉKANYAGOK ÁRTALMATLANNÁ TÉTELÉRE, HA ILYENEKRE SZÜKSÉG VAN A megsemmisítés a helyi előírásoknak megfelelően történik. 11. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgium 12. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/ A GYÁRTÁSI TÉTEL SZÁMA Gy.sz.: 14. A GYÓGYSZER ÁLTALÁNOS BESOROLÁSA RENDELHETŐSÉG SZEMPONTJÁBÓL Orvosi rendelvényhez kötött gyógyszer. 15. AZ ALKALMAZÁSRA VONATKOZÓ UTASÍTÁSOK 16. BRAILLE ÍRÁSSAL FELTÜNTETETT INFORMÁCIÓK Braille írás alól felmentve 27
28 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt - szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált) 2. HATÓANYAG(OK) MEGNEVEZÉSE 1 adag (1 ml): Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú alumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al SEGÉDANYAGOK FELSOROLÁSA Nátrium-klorid Injekcióhoz való víz 4. GYÓGYSZERFORMA ÉS TARTALOM Szuszpenziós injekció előretöltött fecskendőben 1 fecskendő 1 adag (1ml) 5. AZ ALKALMAZÁSSAL KAPCSOLATOS TUDNIVALÓK ÉS AZ ALKALMAZÁS MÓDJA(I) Használat előtt olvassa el a mellékelt tájékoztatót! Intramuscularis alkalmazásra. Használat előtt felrázandó. 6. KÜLÖN FIGYELMEZTETÉS, MELY SZERINT A GYÓGYSZERT GYERMEKEKTŐL ELZÁRVA KELL TARTANI A gyógyszer gyermekektől elzárva tartandó! 7. TOVÁBBI FIGYELMEZTETÉS(EK), AMENNYIBEN SZÜKSÉGES 8. LEJÁRATI IDŐ 28
29 Felhasználható: 9. KÜLÖNLEGES TÁROLÁSI ELŐÍRÁSOK Hűtőszekrényben tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 10. KÜLÖNLEGES ÓVINTÉZKEDÉSEK A FEL NEM HASZNÁLT GYÓGYSZEREK VAGY AZ ILYEN TERMÉKEKBŐL KELETKEZETT HULLADÉKANYAGOK ÁRTALMATLANNÁ TÉTELÉRE, HA ILYENEKRE SZÜKSÉG VAN A megsemmisítés a helyi előírásoknak megfelelően történik. 11. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgium 12. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/ A GYÁRTÁSI TÉTEL SZÁMA Gy.sz.: 14. A GYÓGYSZER ÁLTALÁNOS BESOROLÁSA RENDELHETŐSÉG SZEMPONTJÁBÓL Orvosi rendelvényhez kötött gyógyszer. 15. AZ ALKALMAZÁSRA VONATKOZÓ UTASÍTÁSOK 16. BRAILLE ÍRÁSSAL FELTÜNTETETT INFORMÁCIÓK Braille írás alól felmentve 29
30 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK 1. A GYÓGYSZER MEGNEVEZÉSE Twinrix Felnőtt - szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált) 2. HATÓANYAG(OK) MEGNEVEZÉSE 1 adag (1 ml): Hepatitis A vírus (inaktivált) 1,2 Hepatitis B felületi antigén 3,4 720 ELISA egység 20 mikrogramm 1 Humán diploid (MRC-5) sejtkúltúrán előállított 2 Víztartalmú alumínium-hidroxidhoz kötött 0,05 milligramm Al 3+ 3 Élesztősejteken (Saccharomyces cerevisiae) rekombináns DNS technológiával előállított 4 Alumínium-foszfáthoz kötött 0,4 milligramm Al SEGÉDANYAGOK FELSOROLÁSA Nátrium-klorid Injekcióhoz való víz 4. GYÓGYSZERFORMA ÉS TARTALOM Szuszpenziós injekció előretöltött fecskendőben 10 fecskendő 10 x 1 adag 1 adag (1ml) 5. AZ ALKALMAZÁSSAL KAPCSOLATOS TUDNIVALÓK ÉS AZ ALKALMAZÁS MÓDJA(I) Használat előtt olvassa el a mellékelt tájékoztatót! Intramuscularis alkalmazásra. Használat előtt felrázandó. 6. KÜLÖN FIGYELMEZTETÉS, MELY SZERINT A GYÓGYSZERT GYERMEKEKTŐL ELZÁRVA KELL TARTANI A gyógyszer gyermekektől elzárva tartandó! 7. TOVÁBBI FIGYELMEZTETÉS(EK), AMENNYIBEN SZÜKSÉGES 8. LEJÁRATI IDŐ 30
31 Felhasználható: 9. KÜLÖNLEGES TÁROLÁSI ELŐÍRÁSOK Hűtőszekrényben tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó. 10. KÜLÖNLEGES ÓVINTÉZKEDÉSEK A FEL NEM HASZNÁLT GYÓGYSZEREK VAGY AZ ILYEN TERMÉKEKBŐL KELETKEZETT HULLADÉKANYAGOK ÁRTALMATLANNÁ TÉTELÉRE, HA ILYENEKRE SZÜKSÉG VAN A megsemmisítés a helyi előírásoknak megfelelően történik. 11. A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgium 12. A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA(I) EU/1/96/020/ A GYÁRTÁSI TÉTEL SZÁMA Gy.sz.: 14. A GYÓGYSZER ÁLTALÁNOS BESOROLÁSA RENDELHETŐSÉG SZEMPONTJÁBÓL Orvosi rendelvényhez kötött gyógyszer. 15. AZ ALKALMAZÁSRA VONATKOZÓ UTASÍTÁSOK 16. BRAILLE ÍRÁSSAL FELTÜNTETETT INFORMÁCIÓK Braille írás alól felmentve 31
A vakcina nyomokban a gyártási folyamat során használt neomicint tartalmazhat (lásd 4.3 pont).
 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag
1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag
A vakcina nyomokban a gyártási folyamat során használt neomicint tartalmazhat (lásd 4.3 pont).
 1. A GYÓGYSZER NEVE Twinrix Gyermek szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag
1. A GYÓGYSZER NEVE Twinrix Gyermek szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 1 adag (1 ml) tartalma: Hepatitisz B felszíni antigén 1,2. 20 mikrogramm
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
Salmonella typhi (Ty2 törzs) Vi poliszacharidja
 1. A GYÓGYSZER NEVE Typherix oldat injekcióhoz előretöltött fecskendőben Hastífusz elleni poliszacharid vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A vakcina egy adagjának (0,5 ml) tartalma: Salmonella
1. A GYÓGYSZER NEVE Typherix oldat injekcióhoz előretöltött fecskendőben Hastífusz elleni poliszacharid vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A vakcina egy adagjának (0,5 ml) tartalma: Salmonella
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Gyermek szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Gyermek szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
A Havrix megfelel az Egészségügyi Világszervezet (WHO) biológiai anyagokra előírt követelményeinek.
 1. A GYÓGYSZER MEGNEVEZÉSE Havrix 1440 Elisa Egység szuszpenziós injekció előretöltött fecskendőben Havrix 720 Elisa Egység Junior szuszpenziós injekció előretöltött fecskendőben Hepatitis A vakcina antigén
1. A GYÓGYSZER MEGNEVEZÉSE Havrix 1440 Elisa Egység szuszpenziós injekció előretöltött fecskendőben Havrix 720 Elisa Egység Junior szuszpenziós injekció előretöltött fecskendőben Hepatitis A vakcina antigén
GYŰJTŐDOBOZ, AMELY 1 DOBOZBAN 50 DB SZUSZPENZIÓT TARTALMAZÓ INJEKCIÓS ÜVEGET ÉS 2 1 DOBOZBAN 25 DB EMULZIÓT TARTALMAZÓ INJEKCIÓS ÜVEGET TARTALMAZ
 A. CÍMKESZÖVEG 1 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK GYŰJTŐDOBOZ, AMELY 1 DOBOZBAN 50 DB SZUSZPENZIÓT TARTALMAZÓ INJEKCIÓS ÜVEGET ÉS 2 1 DOBOZBAN 25 DB EMULZIÓT TARTALMAZÓ INJEKCIÓS ÜVEGET TARTALMAZ
A. CÍMKESZÖVEG 1 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK GYŰJTŐDOBOZ, AMELY 1 DOBOZBAN 50 DB SZUSZPENZIÓT TARTALMAZÓ INJEKCIÓS ÜVEGET ÉS 2 1 DOBOZBAN 25 DB EMULZIÓT TARTALMAZÓ INJEKCIÓS ÜVEGET TARTALMAZ
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 1 adag (0,5 ml) tartalma: Hepatitisz B felszíni antigén 1,2.
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
B/Brisbane/60/2008 15,0 mikrogramm HA**
 1. A GYÓGYSZER MEGNEVEZÉSE Influvac szuszpenziós injekció előretöltött fecskendőben (2010/2011) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy 0,5 ml-es adag vakcina az alábbi törzsekhez tartozó influenzavírusok
1. A GYÓGYSZER MEGNEVEZÉSE Influvac szuszpenziós injekció előretöltött fecskendőben (2010/2011) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy 0,5 ml-es adag vakcina az alábbi törzsekhez tartozó influenzavírusok
Hidratált alumínium-hidroxidhoz adszorbeálva összesen: 0,50 milligramm Al 3+ 2
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
A Havrix hepatitis A vírus (HAV) fertőzés elleni aktív immunizálásra alkalmas HAV fertőzés veszélyének kitett személyek számára.
 1. A GYÓGYSZER NEVE Havrix 1440 szuszpenziós injekció előretöltött fecskendőben Havrix 720 Junior szuszpenziós injekció előretöltött fecskendőben Hepatitis A vakcina (inaktivált, adszorbeált) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Havrix 1440 szuszpenziós injekció előretöltött fecskendőben Havrix 720 Junior szuszpenziós injekció előretöltött fecskendőben Hepatitis A vakcina (inaktivált, adszorbeált) 2. MINŐSÉGI
ENGERIX-B szuszpenziós injekció gyermekeknek előretöltött fecskendőben
 ENGERIX-B szuszpenziós injekció gyermekeknek előretöltött fecskendőben hepatitis b antigen ATC-kód: J07BC01 GlaxoSmithKline 1x0,5 ml V 3703 Ft2777 Ft OGYI-T-8260 / 01 TTT-kód: 220149787 JÁRMŰ 2. Minőségi
ENGERIX-B szuszpenziós injekció gyermekeknek előretöltött fecskendőben hepatitis b antigen ATC-kód: J07BC01 GlaxoSmithKline 1x0,5 ml V 3703 Ft2777 Ft OGYI-T-8260 / 01 TTT-kód: 220149787 JÁRMŰ 2. Minőségi
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 1 adag (0,5 ml) tartalma: Hepatitisz B felszíni antigén 1,2.
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
Tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 évesnél idősebbek számára
 1. A GYÓGYSZER MEGNEVEZÉSE Td-pur szuszpenziós injekció előretöltött fecskendőben Tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 évesnél idősebbek számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
1. A GYÓGYSZER MEGNEVEZÉSE Td-pur szuszpenziós injekció előretöltött fecskendőben Tetanusz/diftéria adszorbeált vakcina tartósítószer nélkül, 5 évesnél idősebbek számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
A Boostrix Polio diphtheria, tetanus, pertussis és poliomyelitis elleni emlékeztető oltásra javasolt 4 éves kortól (lásd 4.2 pont).
 1. A GYÓGYSZER NEVE Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett
1. A GYÓGYSZER NEVE Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Ambirix szuszpenziós injekció. Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Ambirix szuszpenziós injekció. Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1
MOST AKKOR HOGYAN OLTSUNK MENINGOCOCCUS ELLEN?? Kulcsár Andrea ESZSZK
 MOST AKKOR HOGYAN OLTSUNK MENINGOCOCCUS ELLEN?? Kulcsár Andrea ESZSZK 0-5 éves. 15-25 éves Meningitis epidemica megbetegedések korcsoportonként 0 25 éves!!!!!!!!!!!!! Forrás: OEK MEGELŐZÉSI STRATÉGIÁK
MOST AKKOR HOGYAN OLTSUNK MENINGOCOCCUS ELLEN?? Kulcsár Andrea ESZSZK 0-5 éves. 15-25 éves Meningitis epidemica megbetegedések korcsoportonként 0 25 éves!!!!!!!!!!!!! Forrás: OEK MEGELŐZÉSI STRATÉGIÁK
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Ecoporc SHIGA szuszpenziós injekció sertések számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml-es adagonként
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Ecoporc SHIGA szuszpenziós injekció sertések számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml-es adagonként
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Cervarix szuszpenziós injekció előretöltött fecskendőben Humán papillomavírus vakcina [16-os és 18-as típus] (rekombináns, adjuvánssal adszorbeált) Mielőtt
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Cervarix szuszpenziós injekció előretöltött fecskendőben Humán papillomavírus vakcina [16-os és 18-as típus] (rekombináns, adjuvánssal adszorbeált) Mielőtt
* egészséges csirkeállományból származó megtermékenyített tyúktojáson szaporított ** hemagglutinin
 1. A GYÓGYSZER NEVE Fluarix szuszpenziós injekció előretöltött fecskendőben Influenza vakcina (split-vírus, inaktivált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Influenza (inaktivált, split) vírus*, amely
1. A GYÓGYSZER NEVE Fluarix szuszpenziós injekció előretöltött fecskendőben Influenza vakcina (split-vírus, inaktivált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Influenza (inaktivált, split) vírus*, amely
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE HBVAXPRO 5 mikrogramm szuszpenziós injekció Hepatitis B vakcina (rdns) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml) tartalma: Hepatitis
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE HBVAXPRO 5 mikrogramm szuszpenziós injekció Hepatitis B vakcina (rdns) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml) tartalma: Hepatitis
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Daronrix szuszpenziós injekció előretöltött fecskendőben Pandémiás influenza vakcina (teljes virion, inaktivált, adjuvánshoz kötött) 2. MINŐSÉGI
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Daronrix szuszpenziós injekció előretöltött fecskendőben Pandémiás influenza vakcina (teljes virion, inaktivált, adjuvánshoz kötött) 2. MINŐSÉGI
Kombinált diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis adszorbeált vakcina
 1. A GYÓGYSZER NEVE Infanrix IPV szuszpenziós injekció előretöltött fecskendőben Kombinált diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis adszorbeált vakcina 2. MINŐSÉGI ÉS MENNYISÉGI
1. A GYÓGYSZER NEVE Infanrix IPV szuszpenziós injekció előretöltött fecskendőben Kombinált diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis adszorbeált vakcina 2. MINŐSÉGI ÉS MENNYISÉGI
Kombinált diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis adszorbeált vakcina. legalább 30 NE legalább 40 NE
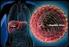 1. A GYÓGYSZER MEGNEVEZÉSE Infanrix IPV szuszpenziós injekció előretöltött fecskendőben Kombinált diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis adszorbeált vakcina 2. MINŐSÉGI ÉS
1. A GYÓGYSZER MEGNEVEZÉSE Infanrix IPV szuszpenziós injekció előretöltött fecskendőben Kombinált diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis adszorbeált vakcina 2. MINŐSÉGI ÉS
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Felnőtt szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Infanrix-IPV+Hib por szuszpenziós injekcióhoz és szuszpenziós injekció előretöltött fecskendőben
 1. A GYÓGYSZER NEVE Infanrix-IPV+Hib por szuszpenziós injekcióhoz és szuszpenziós injekció előretöltött fecskendőben Diphtheria (D), tetanus (T), acellularis pertussis (Pa), inaktivált poliomyelitis (IPV)
1. A GYÓGYSZER NEVE Infanrix-IPV+Hib por szuszpenziós injekcióhoz és szuszpenziós injekció előretöltött fecskendőben Diphtheria (D), tetanus (T), acellularis pertussis (Pa), inaktivált poliomyelitis (IPV)
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Equilis West Nile szuszpenziós injekció lovak számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A vakcina adagonként
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Equilis West Nile szuszpenziós injekció lovak számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A vakcina adagonként
Infanrix-IPV+Hib por szuszpenziós injekcióhoz és szuszpenziós injekció előretöltött fecskendőben
 1. A GYÓGYSZER NEVE Infanrix-IPV+Hib por szuszpenziós injekcióhoz és szuszpenziós injekció előretöltött fecskendőben Adszorbeált kombinált, diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis
1. A GYÓGYSZER NEVE Infanrix-IPV+Hib por szuszpenziós injekcióhoz és szuszpenziós injekció előretöltött fecskendőben Adszorbeált kombinált, diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis
1 adag (0,5 ml) tartalma: legalább 40 nemzetközi egység (NE) hidratált alumínium-hidroxidhoz adszorbeálva max. 0,7 mg Al 3+
 1. A GYÓGYSZER NEVE VACTETA 40 NE/0,5ml szuszpenziós injekció Tetanusz vakcina (adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) tartalma: Tetanusz-toxoid legalább 40 nemzetközi egység
1. A GYÓGYSZER NEVE VACTETA 40 NE/0,5ml szuszpenziós injekció Tetanusz vakcina (adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) tartalma: Tetanusz-toxoid legalább 40 nemzetközi egység
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/18
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/18 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Neocolipor szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag(ok): adagonként (2 ml):
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/18 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Neocolipor szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag(ok): adagonként (2 ml):
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Havrix 1440 szuszpenziós injekció előretöltött fecskendőben Havrix 720 Junior szuszpenziós injekció előretöltött fecskendőben Hepatitisz A vakcina (inaktivált,
Betegtájékoztató: Információk a felhasználó számára Havrix 1440 szuszpenziós injekció előretöltött fecskendőben Havrix 720 Junior szuszpenziós injekció előretöltött fecskendőben Hepatitisz A vakcina (inaktivált,
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA. Fluval P szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált)
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Fluval P szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) Mielőtt beadják Önnek ezt az injekciót, olvassa el figyelmesen
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Fluval P szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) Mielőtt beadják Önnek ezt az injekciót, olvassa el figyelmesen
A Varilrix megfelel az Egészségügyi Világszervezet (WHO) biológiai anyagokra és a varicella vakcinákra előírt követelményeinek.
 1. A GYÓGYSZER NEVE Varilrix por és oldószer oldatos injekcióhoz Élő, attenuált varicella-zoster vírus (OKA törzs) vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A Varilrix a varicella-zoster vírus élő,
1. A GYÓGYSZER NEVE Varilrix por és oldószer oldatos injekcióhoz Élő, attenuált varicella-zoster vírus (OKA törzs) vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL A Varilrix a varicella-zoster vírus élő,
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Parvoduk szuszpenzió és hígító szuszpenziós injekcióhoz pézsmakacsa részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Parvoduk szuszpenzió és hígító szuszpenziós injekcióhoz pézsmakacsa részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
A vakcina összetétele megfelel az Egészségügyi Világszervezet (WHO), valamint az EU 2015/2016- os szezonra (északi féltekére) vonatkozó ajánlásának.
 1. A GYÓGYSZER NEVE 3Fluart szuszpenziós injekció influenza vakcina (teljes vírus, inaktivált, adjuvált) (a 2015/2016-os szezonra) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) vakcina összetétele
1. A GYÓGYSZER NEVE 3Fluart szuszpenziós injekció influenza vakcina (teljes vírus, inaktivált, adjuvált) (a 2015/2016-os szezonra) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) vakcina összetétele
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Gyermek szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Twinrix Gyermek szuszpenziós injekció Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
HBVAXPRO 10 µg/ml szuszpenziós injekció előretöltött fecskendőben
 HBVAXPRO 10 µg/ml szuszpenziós injekció előretöltött fecskendőben hepatitis b antigen ATC-kód: J07BC01 Sanofi Pasteur/MSD SNC 1x előretöltött fecskendő tű nélkül V Szabadáras EU/1/01/183 / 011 TTT-kód:
HBVAXPRO 10 µg/ml szuszpenziós injekció előretöltött fecskendőben hepatitis b antigen ATC-kód: J07BC01 Sanofi Pasteur/MSD SNC 1x előretöltött fecskendő tű nélkül V Szabadáras EU/1/01/183 / 011 TTT-kód:
5. AZ ALKALMAZÁSSAL KAPCSOLATOS TUDNIVALÓK ÉS AZ ALKALMAZÁS MÓDJA(I)
 A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK {DOBOZ} 1. A GYÓGYSZER MEGNEVEZÉSE Chinofungin külsőleges oldatos spray tolnaftát 100 g 2. HATÓANYAG(OK) MEGNEVEZÉSE Hatóanyagok: 2 g tolnaftát 100 g folyadékban
A KÜLSŐ CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK {DOBOZ} 1. A GYÓGYSZER MEGNEVEZÉSE Chinofungin külsőleges oldatos spray tolnaftát 100 g 2. HATÓANYAG(OK) MEGNEVEZÉSE Hatóanyagok: 2 g tolnaftát 100 g folyadékban
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Purevax FeLV szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Minden adag (1 ml) tartalmaz: Hatóanyag
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Purevax FeLV szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Minden adag (1 ml) tartalmaz: Hatóanyag
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Gripovac 3 szuszpenziós injekció sertés részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Minden adag 2 ml tartalmaz:
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Gripovac 3 szuszpenziós injekció sertés részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Minden adag 2 ml tartalmaz:
Egy immunizáló dózis (0,5 ml) 1,5 μg inaktivált kullancsencephalitis-vírust (törzs K23; csirkeembrio fibroblast sejtkultúrán tenyésztett) tartalmaz.
 1. A GYÓGYSZER NEVE ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy immunizáló dózis (0,5 ml) 1,5 μg inaktivált
1. A GYÓGYSZER NEVE ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy immunizáló dózis (0,5 ml) 1,5 μg inaktivált
0,3 milligramm Al 3+ [Al(OH) 3 ] és alumínium-foszfáthoz (AlPO 4 ) kötött 0,2 milligramm Al 3+
![0,3 milligramm Al 3+ [Al(OH) 3 ] és alumínium-foszfáthoz (AlPO 4 ) kötött 0,2 milligramm Al 3+ 0,3 milligramm Al 3+ [Al(OH) 3 ] és alumínium-foszfáthoz (AlPO 4 ) kötött 0,2 milligramm Al 3+](/thumbs/55/36039311.jpg) 1. A GYÓGYSZER NEVE Boostrix szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus és pertussis (acelluláris összetevő) vakcina (adszorbeált, csökkentett antigén tartalmú) 2. MINŐSÉGI ÉS
1. A GYÓGYSZER NEVE Boostrix szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus és pertussis (acelluláris összetevő) vakcina (adszorbeált, csökkentett antigén tartalmú) 2. MINŐSÉGI ÉS
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Nobivac L4 szuszpenziós injekció kutyák számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Adagonként (1 ml)
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Nobivac L4 szuszpenziós injekció kutyák számára 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Adagonként (1 ml)
Szuszpenziós injekció előretöltött fecskendőben. Az Encepur Junior fehéres, zavaros szuszpenziós injekció előretöltött fecskendőben.
 1. A GYÓGYSZER NEVE Encepur Junior szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,25 ml) tartalma: 0,75 mikrogramm
1. A GYÓGYSZER NEVE Encepur Junior szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,25 ml) tartalma: 0,75 mikrogramm
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Equip WNV - emulziós injekció lovak részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1ml (1adag) tartalma:
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Equip WNV - emulziós injekció lovak részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1ml (1adag) tartalma:
A Boostrix Polio diphtheria, tetanus, pertussis és poliomyelitis elleni emlékeztető oltásra javasolt 4 éves kortól (lásd 4.2 pont).
 1. A GYÓGYSZER NEVE Előretöltött fecskendő: Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált,
1. A GYÓGYSZER NEVE Előretöltött fecskendő: Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált,
Priorix por és oldószer oldatos injekcióhoz előretöltött fecskendőben Kanyaró, mumpsz és rubeola vakcina (élő)
 1. A GYÓGYSZER NEVE Priorix por és oldószer oldatos injekcióhoz előretöltött fecskendőben Kanyaró, mumpsz és rubeola vakcina (élő) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Feloldást követően 1 adag (0,5 ml)
1. A GYÓGYSZER NEVE Priorix por és oldószer oldatos injekcióhoz előretöltött fecskendőben Kanyaró, mumpsz és rubeola vakcina (élő) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Feloldást követően 1 adag (0,5 ml)
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Twinrix Gyermek szuszpenziós injekció előretöltött fecskendőben Hepatitisz A (inaktivált) és hepatitisz B (rdns) (HAB) vakcina (adszorbeált) Mielőtt
Betegtájékoztató: Információk a felhasználó számára Twinrix Gyermek szuszpenziós injekció előretöltött fecskendőben Hepatitisz A (inaktivált) és hepatitisz B (rdns) (HAB) vakcina (adszorbeált) Mielőtt
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Purevax Rabies szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Minden adag (1 ml) tartalmaz:
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Purevax Rabies szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Minden adag (1 ml) tartalmaz:
A/California/7/2009 (H1N1)pdm09 - eredetű NYMC X-179A reasszortáns törzs...15 mikrogramm HA**
 1. A GYÓGYSZER NEVE IDflu 15 mikrogramm/törzs szuszpenziós injekció Influenza vakcina (split virion, inaktivált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az alábbi influenza vírus (inaktivált, hasított) törzsek*:
1. A GYÓGYSZER NEVE IDflu 15 mikrogramm/törzs szuszpenziós injekció Influenza vakcina (split virion, inaktivált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az alábbi influenza vírus (inaktivált, hasított) törzsek*:
hemagglutinin adjuváns: alumínium-foszfát gél 0,33 milligramm Al
 1. A GYÓGYSZER MEGNEVEZÉSE FLUVAL P szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Pandémiás törzsből előállított, inaktivált,
1. A GYÓGYSZER MEGNEVEZÉSE FLUVAL P szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Pandémiás törzsből előállított, inaktivált,
Az alábbi törzshöz tartozó influenzavírus felszíni antigénjei (haemagglutinin és neuraminidáz)*:
 1. A GYÓGYSZER MEGNEVEZÉSE Foclivia szuszpenziós injekció többadagos tartályban Pandémiás influenza elleni vakcina (felszíni antigén, inaktivált, adjuvált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az alábbi
1. A GYÓGYSZER MEGNEVEZÉSE Foclivia szuszpenziós injekció többadagos tartályban Pandémiás influenza elleni vakcina (felszíni antigén, inaktivált, adjuvált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az alábbi
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Optaflu szuszpenziós injekció előretöltött fecskendőben Influenza elleni vakcina (felszíni antigén, inaktivált, sejttenyészetben előállított)
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Optaflu szuszpenziós injekció előretöltött fecskendőben Influenza elleni vakcina (felszíni antigén, inaktivált, sejttenyészetben előállított)
B/Massachusetts/2/2012 (vad típus) min.15µg HA **
 1. A GYÓGYSZER NEVE Fluval AB szuszpenziós injekció influenza vakcina (teljes vírus, inaktivált, adjuvált) (a 2013/2014-es szezonra) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) vakcina összetétele
1. A GYÓGYSZER NEVE Fluval AB szuszpenziós injekció influenza vakcina (teljes vírus, inaktivált, adjuvált) (a 2013/2014-es szezonra) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) vakcina összetétele
Szuszpenziós injekció előretöltött fecskendőben. Az Encepur Adults fehéres, zavaros szuszpenziós injekció előretöltött fecskendőben.
 1. A GYÓGYSZER NEVE Encepur Adults szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml) tartalma: 1,5 mikrogramm
1. A GYÓGYSZER NEVE Encepur Adults szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis vakcina, inaktivált 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml) tartalma: 1,5 mikrogramm
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Fendrix szuszpenziós injekció Hepatitis B (rdns) vakcina (adjuvánshoz kötött, adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) tartalma:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Fendrix szuszpenziós injekció Hepatitis B (rdns) vakcina (adjuvánshoz kötött, adszorbeált). 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) tartalma:
0,3 milligramm Al 3+ [Al(OH) 3 ] és alumínium-foszfáthoz (AlPO 4 ) kötött 0,2 milligramm Al 3+
![0,3 milligramm Al 3+ [Al(OH) 3 ] és alumínium-foszfáthoz (AlPO 4 ) kötött 0,2 milligramm Al 3+ 0,3 milligramm Al 3+ [Al(OH) 3 ] és alumínium-foszfáthoz (AlPO 4 ) kötött 0,2 milligramm Al 3+](/thumbs/39/18583412.jpg) 1. A GYÓGYSZER NEVE Boostrix szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus és pertussis (acelluláris összetevő) vakcina (adszorbeált, csökkentett antigén tartalmú) 2. MINŐSÉGI ÉS
1. A GYÓGYSZER NEVE Boostrix szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus és pertussis (acelluláris összetevő) vakcina (adszorbeált, csökkentett antigén tartalmú) 2. MINŐSÉGI ÉS
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Purevax RC liofilizátum és oldószer szuszpenziós injekcióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml-es
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Purevax RC liofilizátum és oldószer szuszpenziós injekcióhoz 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml-es
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen
diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett antigén tartalmú)
 1. A GYÓGYSZER NEVE Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett
1. A GYÓGYSZER NEVE Boostrix Polio szuszpenziós injekció előretöltött fecskendőben diphtheria, tetanus, pertussis (acelluláris összetevő) és (inaktivált) poliomyelitis vakcina (adszorbeált, csökkentett
Ez a gyógyszer orvosi vény nélkül kapható. Az optimális hatás érdekében azonban elengedhetetlen e gyógyszer körültekintő alkalmazása.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Coldastop orrcsepp PIL új BETEGTÁJÉKOZTATÓ Coldastop orrcsepp A-vitamin-palmitát
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Coldastop orrcsepp PIL új BETEGTÁJÉKOZTATÓ Coldastop orrcsepp A-vitamin-palmitát
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/19 1
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/19 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Eurican Herpes 205 por és oldószer emulziós injekcióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/19 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Eurican Herpes 205 por és oldószer emulziós injekcióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Hatóanyag
alumínium-hidroxidhoz adszorbeálva 0,3-0,4 mg Al 3+
 1. A GYÓGYSZER NEVE Menjugate 10 mikrogramm por és oldószer szuszpenziós injekcióhoz C-csoportú meningococcus konjugált vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml,előkészített) vakcina
1. A GYÓGYSZER NEVE Menjugate 10 mikrogramm por és oldószer szuszpenziós injekcióhoz C-csoportú meningococcus konjugált vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy adag (0,5 ml,előkészített) vakcina
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Cervarix szuszpenziós injekció Humán papillomavírus vakcina [16-os és 18-as típus] (rekombináns, adjuvánssal adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Cervarix szuszpenziós injekció Humán papillomavírus vakcina [16-os és 18-as típus] (rekombináns, adjuvánssal adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI
* egészséges csirketenyészetekből származó megtermékenyített tyúktojásban elszaporítva ** haemagglutinin
 IDFLU 15 µg/törzs szuszpenziós injekcióhoz Gyártó: Sanofi Pasteur S.A. Az alábbi influenza vírus (inaktivált, hasított) törzsek*: A/California/7/2009 (H1N1) - eredetű törzs NYMC X-179A reassz:.9 mikrogramm
IDFLU 15 µg/törzs szuszpenziós injekcióhoz Gyártó: Sanofi Pasteur S.A. Az alábbi influenza vírus (inaktivált, hasított) törzsek*: A/California/7/2009 (H1N1) - eredetű törzs NYMC X-179A reassz:.9 mikrogramm
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina
Betegtájékoztató: Információk a felhasználó számára Engerix-B szuszpenziós injekció gyermekeknek Engerix-B szuszpenziós injekció előretöltött fecskendőben gyermekeknek Hepatitisz B (rekombináns DNS) vakcina
Infanrix-IPV + HIB vakcina fecskendőben por és szuszpenzió szuszpenziós injekcióhoz
 1. A GYÓGYSZERKÉSZÍTMÉNY MEGNEVEZÉSE Infanrix-IPV + HIB vakcina fecskendőben por és szuszpenzió szuszpenziós injekcióhoz Adszorbeált kombinált, diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis
1. A GYÓGYSZERKÉSZÍTMÉNY MEGNEVEZÉSE Infanrix-IPV + HIB vakcina fecskendőben por és szuszpenzió szuszpenziós injekcióhoz Adszorbeált kombinált, diphtheria, tetanus, acellularis pertussis, inaktivált poliomyelitis
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Ambirix szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Ambirix szuszpenziós injekció előretöltött fecskendőben Hepatitis A (inaktivált) és hepatitis B (rdns) (HAB) vakcina (adszorbeált). 2. MINŐSÉGI ÉS
A Mencevax ACWY megfelel a WHO biológiai készítményekre és a meningococcus meningitis vakcinákra vonatkozó előírásainak.
 1. A GYÓGYSZERKÉSZÍTMÉNY MEGNEVEZÉSE MENCEVAX ACWY135 Y egy adagos vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Összetétel dózisonként: Neisseria meningitidis poliszacharid A típusú, tisztított 50,0 μg
1. A GYÓGYSZERKÉSZÍTMÉNY MEGNEVEZÉSE MENCEVAX ACWY135 Y egy adagos vakcina 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Összetétel dózisonként: Neisseria meningitidis poliszacharid A típusú, tisztított 50,0 μg
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina
Betegtájékoztató: Információk a felhasználó számára Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina
Az állapot súlyosságától függően prekóma vagy kóma esetében 24 óra alatt az adag 8 ampulláig emelhető.
 1. A GYÓGYSZER NEVE Hepa-Merz 0,5 g/ml koncentrátum oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 db 10 ml-es ampulla 5 g L-ornitin-L-aszpartátot tartalmaz. A segédanyagok teljes listáját
1. A GYÓGYSZER NEVE Hepa-Merz 0,5 g/ml koncentrátum oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 db 10 ml-es ampulla 5 g L-ornitin-L-aszpartátot tartalmaz. A segédanyagok teljes listáját
KÜLÖN, A BETEGRENDELÉSTŐL ELKÜLÖNÍTETT
 A vakcina elérhető fél év feletti gyermekek részére, DÍJTALANUL. A védelem egyszeri, a felkar deltaizomzatába adott oltással biztosítható. A védőoltást igénylők számára az oltás beadására KÜLÖN, A BETEGRENDELÉSTŐL
A vakcina elérhető fél év feletti gyermekek részére, DÍJTALANUL. A védelem egyszeri, a felkar deltaizomzatába adott oltással biztosítható. A védőoltást igénylők számára az oltás beadására KÜLÖN, A BETEGRENDELÉSTŐL
1. A GYÓGYSZER NEVE. 1FLUART szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált)
 1. A GYÓGYSZER NEVE 1FLUART szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) vakcina összetétele: A vakcina formaldehiddel
1. A GYÓGYSZER NEVE 1FLUART szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) vakcina összetétele: A vakcina formaldehiddel
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE CYTOPOINT 10 mg oldatos injekció kutyák számára CYTOPOINT 20 mg oldatos injekció kutyák számára CYTOPOINT
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE CYTOPOINT 10 mg oldatos injekció kutyák számára CYTOPOINT 20 mg oldatos injekció kutyák számára CYTOPOINT
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Equilis Te szuszpenziós injekció lovaknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az 1 ml-es adag tartalma:
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Equilis Te szuszpenziós injekció lovaknak 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Az 1 ml-es adag tartalma:
Betegtájékoztató AVAXIM 160 EGYSÉG SZUSZPENZIÓS INJEKCIÓ ELÕRETÖLTÖTT FECSKENDÕBEN
 AVAXIM 160 EGYSÉG SZUSZPENZIÓS INJEKCIÓ ELÕRETÖLTÖTT FECSKENDÕBEN Avaxim 160 Egység szuszpenziós injekció elõretöltött fecskendõben Hepatitis A vakcina (inaktivált, adszorbeált) HATÓANYAG: Hepatitisz A
AVAXIM 160 EGYSÉG SZUSZPENZIÓS INJEKCIÓ ELÕRETÖLTÖTT FECSKENDÕBEN Avaxim 160 Egység szuszpenziós injekció elõretöltött fecskendõben Hepatitis A vakcina (inaktivált, adszorbeált) HATÓANYAG: Hepatitisz A
Megjegyzés: Ez az alkalmazási előírás, címkeszöveg és betegtájékoztató a Bizottság Határozata időpontjában érvényes verzió.
 III.Melléklet Alkalmazási előírás, címkeszöveg és betegtájékoztató Megjegyzés: Ez az alkalmazási előírás, címkeszöveg és betegtájékoztató a Bizottság Határozata időpontjában érvényes verzió. A Bizottság
III.Melléklet Alkalmazási előírás, címkeszöveg és betegtájékoztató Megjegyzés: Ez az alkalmazási előírás, címkeszöveg és betegtájékoztató a Bizottság Határozata időpontjában érvényes verzió. A Bizottság
FSME-IMMUN Junior szuszpenziós injekció előretöltött fecskendőben
 FSME-IMMUN Junior szuszpenziós injekció előretöltött fecskendőben kullancs encephalitis vírus, inaktivált ATC-kód: J07BA01 Baxter Hungary 1x0,25 ml V Szabadáras OGYI-T-9519 / 01 TTT-kód: 220176124 GRAV
FSME-IMMUN Junior szuszpenziós injekció előretöltött fecskendőben kullancs encephalitis vírus, inaktivált ATC-kód: J07BA01 Baxter Hungary 1x0,25 ml V Szabadáras OGYI-T-9519 / 01 TTT-kód: 220176124 GRAV
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Suvaxyn Circo emulziós injekció sertések részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (2 ml) tartalmaz:
1.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Suvaxyn Circo emulziós injekció sertések részére 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (2 ml) tartalmaz:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Infanrix hexa, por és szuszpenzió szuszpenziós injekcióhoz előretöltött fecskendőben Diphtheria (D), tetanus (T), pertussis (acelluláris komponens)
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Infanrix hexa, por és szuszpenzió szuszpenziós injekcióhoz előretöltött fecskendőben Diphtheria (D), tetanus (T), pertussis (acelluláris komponens)
ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben
 ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben tick-borne encephalitis vaccine, inactivated ATC-kód: J07BA01 Novartis Vaccines and Diagnostics 1x0,5 ml V 2823 Ft2117 Ft OGYI-T-8227 / 01
ENCEPUR ADULTS szuszpenziós injekció előretöltött fecskendőben tick-borne encephalitis vaccine, inactivated ATC-kód: J07BA01 Novartis Vaccines and Diagnostics 1x0,5 ml V 2823 Ft2117 Ft OGYI-T-8227 / 01
Az oldat tartalma milliliterenként: humán plazmaprotein... 200 mg (legalább 98%-os tisztaságú IgG)
 1. A GYÓGYSZER MEGNEVEZÉSE Hizentra 200 mg/ml oldatos injekció bőr alá történő beadásra 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán normál immunglobulin (SCIg). Az oldat tartalma milliliterenként: humán
1. A GYÓGYSZER MEGNEVEZÉSE Hizentra 200 mg/ml oldatos injekció bőr alá történő beadásra 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Humán normál immunglobulin (SCIg). Az oldat tartalma milliliterenként: humán
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! z alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmese BETEGTÁJÉKOZTTÓ:
FIGYELEM!!! z alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmese BETEGTÁJÉKOZTTÓ:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE IXIARO szuszpenziós injekció Japán encephalitis elleni vakcina (inaktivált, adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) IXIARO
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE IXIARO szuszpenziós injekció Japán encephalitis elleni vakcina (inaktivált, adszorbeált) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 adag (0,5 ml) IXIARO
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Pandemic influenza vaccine (H5N1) (split virion, inactivated, adjuvanted) GlaxoSmithKline Biologicals szuszpenzió és emulzió emulziós injekcióhoz.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Pandemic influenza vaccine (H5N1) (split virion, inactivated, adjuvanted) GlaxoSmithKline Biologicals szuszpenzió és emulzió emulziós injekcióhoz.
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! B BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Jumex 5 mg tabletta
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! B BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Jumex 5 mg tabletta
kullancsencephalitis (Tick-Borne Encephalitis, TBE) vakcina (inaktivált, teljes vírus)
 1. A GYÓGYSZER NEVE FSME-Immun Junior szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis (Tick-Borne Encephalitis, TBE) vakcina (inaktivált, teljes vírus) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
1. A GYÓGYSZER NEVE FSME-Immun Junior szuszpenziós injekció előretöltött fecskendőben kullancsencephalitis (Tick-Borne Encephalitis, TBE) vakcina (inaktivált, teljes vírus) 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
ENCEPUR JUNIOR szuszpenziós injekció előretöltött fecskendőben
 ENCEPUR JUNIOR szuszpenziós injekció előretöltött fecskendőben tick-borne encephalitis vaccine, inactivated ATC-kód: J07BA01 Novartis Vaccines and Diagnostics 1x0,25 ml (tűvel) V 2395 Ft1796 Ft OGYI-T-8192
ENCEPUR JUNIOR szuszpenziós injekció előretöltött fecskendőben tick-borne encephalitis vaccine, inactivated ATC-kód: J07BA01 Novartis Vaccines and Diagnostics 1x0,25 ml (tűvel) V 2395 Ft1796 Ft OGYI-T-8192
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Encepur Junior szuszpenziós injekció előretöltött fecskendőben kullancsenkefalitisz vakcina, inaktivált Mielőtt beadják gyermekének ezt az injekciót,
Betegtájékoztató: Információk a felhasználó számára Encepur Junior szuszpenziós injekció előretöltött fecskendőben kullancsenkefalitisz vakcina, inaktivált Mielőtt beadják gyermekének ezt az injekciót,
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára 3Fluart szuszpenziós injekció a 2013/2014-es szezonra Influenza vakcina (teljes vírus, inaktivált, adjuvált) Mielőtt elkezdenék Önnél alkalmazni ezt
Betegtájékoztató: Információk a felhasználó számára 3Fluart szuszpenziós injekció a 2013/2014-es szezonra Influenza vakcina (teljes vírus, inaktivált, adjuvált) Mielőtt elkezdenék Önnél alkalmazni ezt
Betegtájékoztató: Információk a felhasználó számára. 1FLUART szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált)
 Betegtájékoztató: Információk a felhasználó számára 1FLUART szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) Mielőtt beadják Önnek ezt a vakcinát, olvassa el figyelmesen
Betegtájékoztató: Információk a felhasználó számára 1FLUART szuszpenziós injekció Pandémiás influenza vakcina (teljes vírus, inaktivált, adjuvált) Mielőtt beadják Önnek ezt a vakcinát, olvassa el figyelmesen
Maprelin. Maprelin 75µg/ml oldat injekciós sertések számára A.U.V. Biotechnikai felhasználásra, csoportok vagy állományok kezelésére.
 Maprelin Maprelin 75µg/ml oldat injekciós sertések számára A.U.V Biotechnikai felhasználásra, csoportok vagy állományok kezelésére. Maprelin 75 μg/ml 1.A FORGALOMBA HOZATALI ENGEDÉLY JOOSULTJÁNAK, TOVÁBBÁ
Maprelin Maprelin 75µg/ml oldat injekciós sertések számára A.U.V Biotechnikai felhasználásra, csoportok vagy állományok kezelésére. Maprelin 75 μg/ml 1.A FORGALOMBA HOZATALI ENGEDÉLY JOOSULTJÁNAK, TOVÁBBÁ
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Címkeszöveg tervezet Külső (doboz) csomagoláson: Novascabin emulzió 70 g
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Címkeszöveg tervezet Külső (doboz) csomagoláson: Novascabin emulzió 70 g
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmesen az alábbi
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmesen az alábbi
1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE. Remacycline L.A. 200 mg/ml oldatos injekció A.U.V. Oxitetraciklin 2. HATÓ- ÉS SEGÉDANYAGOK MEGNEVEZÉSE
 A KÜLSŐ CSOMAGOLÁSON ÉS A KÖZVETLEN CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK Papírdoboz 50 ml-es, 100 ml-es, 250 ml-es és 500 ml-es injekciós üvegnek és címke 100 ml, 250 ml, 500 ml üvegre 1. AZ ÁLLATGYÓGYÁSZATI
A KÜLSŐ CSOMAGOLÁSON ÉS A KÖZVETLEN CSOMAGOLÁSON FELTÜNTETENDŐ ADATOK Papírdoboz 50 ml-es, 100 ml-es, 250 ml-es és 500 ml-es injekciós üvegnek és címke 100 ml, 250 ml, 500 ml üvegre 1. AZ ÁLLATGYÓGYÁSZATI
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Optaflu szuszpenziós injekció előretöltött fecskendőben Influenza elleni vakcina (felszíni antigén, inaktivált, sejttenyészetben előállított) (2015./2016.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Optaflu szuszpenziós injekció előretöltött fecskendőben Influenza elleni vakcina (felszíni antigén, inaktivált, sejttenyészetben előállított) (2015./2016.
