Triptofántartalom meghatározása hús és húskészítményekben
|
|
|
- Csenge Nagy
- 6 évvel ezelőtt
- Látták:
Átírás
1 Triptofántartalom meghatározása hús és húskészítményekben RÉKASINÉ SZOMBATI ÉVA, ORLANDO PRESA CABALLERO* MIHÁLYINÉ KENGYEL VILMA, DR. KÖRMENDY LÁSZLÓ Országos H úsipari K utatóintézet, B udapest Érkezett: szeptember 15. A triptofántartalom meghatározásával a hústermékekben levő fehérjék biológiai értékét állapíthatjuk meg, miután a triptofán az eszenciális aminosavak egyike és jelenléte táplálkozásélettanilag rendkívül fontos. Ismert, hogy a húsfehérjék közül a miofibrilláris- és szarkoplazmafehérjék teljes értékűek, tartalmazzák mind a 8 aminosavat, melyet az emberi szervezet nem képes szintetizálni, ugyanakkor a kötőszöveti fehérjék éppen triptofán hiányuk miatt nem tekinthetők teljes értékűnek. A termék minőségi jellemzőinek megállapításakor a víz- és zsírtartalmon kívül mérik vagy számítják az összfehérjetartalmat is. A fehérje minőségére, biológiai értékére a fent említettek értelmében az összfehérjetartalom ismerete önmagában nem nyújt felvilágosítást. Szükséges meghatároznunk, hogy az összfehérjetartalom hogyan oszlik meg a különböző fehérjefrakciók között. A kötőszöveti fehérjéket két fő frakció alkotja: a kollagén és elasztin. Mindkettőre jellemző, hogy ellentétben az izomfehérjékkel az őket felépítő aminosavak között szerepel a hidroxiprolin. Ez a különböző kollagénfrakcióknál átlagosan az össz-aminosavtartalom 12,5%-át teszi ki, az elasztin ennél lényegesen kevesebbet tartalmaz, 1-2% - ot. Szokás ezért a kötőszövettartalmat a hidroxiprolintartalom mennyiségének ismerete alapján számítani. Természetes, hogy a kollagénre és elasztinra történő pontos átszámítás különböző szorzó faktorok segítségével lehetséges csak, s mivel nem ismerjük a két kötőszövet frakció arányát a kötőszövettartalom kiszámításánál nagyot tévedhetünk. A hidroxiprolintartalom alapján számított kötőszövettartalom különösen akkor tér el jelentősen a valódi értéktől, ha elasztinban dús anyagot dolgoznak be a hústermékbe, mert az átszámítás általánosan kollagénre történik. Míg a kötőszöveti fehérjék nem, vagy alig tartalmaznak triptofánt, kreatint és N-metilhisztidint, addig a nem-kötőszöveti fehérjék jelentős menynyiségben tartalmazzák azt. így remény van arra, hogy ezek mennyiségének meghatározásával közvetve mérhetjük a kötőszövettartalmat. Mivel főzés során a kreatin nagy része a főzővízbe kerül, főtt termékek biológiai értéke ilyen módon nem becsülhető. Kísérleteink során triptofánt határoztunk meg húsból és hústermékekből. A triptofántartalom meghatározása történhet hidrolizált vagy intakt, nem hidrolizált fehérjéből. Az első esetben a szabad aminosavként jelenlévő triptofántartalmat, míg az utóbbi esetben a peptidkötésben levő triptofántartalmat kapjuk meg. Amennyiben szabad aminosavként határozzuk meg a fehérje triptofántartal- *Centro Nációnál de Investigaciones Cientificas, La H abana (Cuba) 3 Éielmiszervizsgálati Közlemények 17
2 mát a meghatározás minden esetben két lépésből áll: a fehérje hidrolízisből, majd az ezt követő kimutatási reakcióból. Nem hidrolizált fehérjéből végezve a meghatározást a reakció lényegesen rövidebb a hidrolízis idejének elmaradása miatt. A közleményekben található számos triptofán meghatározási módszer közül kísérleteinkhez olyan módszert választottunk ki, mely üzemi körülmények között is, aránylag rövid idő alatt véghezvihető. így semmiképpen nem jöhetett szóba olyan módszerek alkalmazása, amelyek komolyabb berendezést igényelnek (automata aminosavanalizátor, spektrofluorimetrás berendezés). Célszerűnek látszott a hosszú időt igénylő és triptofán veszteséget okozó fehérje-hidrolízist elhagyni. Bár számos törekvés található az irodalomban, ami arra irányul, hogy a hidrolízist olyan körülmények között vezessék be, melynek során a triptofán-veszteség elhanyagolható (1, 2, 3). Meghatározásainknál ezért nem hidrolizált fehérjéből indultunk ki és a peptidkötésben levő triptofán meghatározására két spektrofotometriás módszert választottunk ki: Spies és Chambers (1, 4) p-dimetil-amino-benzaldehides módszerét, melyet a szerzők sikeresen alkalmaztak különböző fehérjéknél a reakcióparaméterek pontos kimérése után; - Concon (5) módszerét, mely a Opienska-Blauth által módosított Adamkievich reakción alapszik, glioxálsav és triptofán reakciója során színes indofenol vegyidet képződik, melynek mennyisége spektrofotometriásán mérhető. Felhasznált anyagok: KÍSÉRLETI RÉSZ Kísérleteink során a következő fehérjetartalmú anyagok triptofántartalmát határoztuk meg: vágás után 48 óráig hűtőtárolt sertés semimembranosus- és longissimus dorsi izom, vágás után 5 napig hűtőtárolt marha semimembranosus- és longissimus dorsi izom, kereskedelemben árusított hústermékek (párizsi, lecsókolbász, füstölt kolbász és téliszalámi), sertés miofibrilláris és szarkoplazma fehérje [előállítva (6)-szerint], marha Achilles in, marha Ligamentum nuchae, marha szérum albumin (SERVA készítmény), ló szív, mioglobin (Nutritional Biochemicals Corporation készítmény), vérplazma (Pápa, kísérleti gyártás), PROMINE-D (szójafehérje izolátum, CENTRAL SOYA készítményt, EM-HV (Na-kazeinát, DMV készítmény), folyékony vérplazma (Cegléd, PENOMAH), tejpor (Hajdú megyei Tejipari Vállalat, Gyula-i Tejporgyár). Minta előkészítés A vizsgált hús és hústermék mintát húsdarálón kétszer ledaráltuk, majd négyszeres mennyiségű kloroform-metanol (3:1) elegyével zsírtalanítottuk, Ultra- Turrax (Janke-Kunkel T 45) segítségével homogenizáltuk, 1/2 órai állás után szűrtük, az oldószernyomok eltávolítása érdekében szárítottuk, a szárított mintát kávéőrlőn majd mozsárban addig aprítottuk, amíg a minta 1 mm 0-jű szitán teljesen átment. A kémiai vizsgálatok az így nyert homogén mintából történtek. T r iptofántartalom meghal árazása 1. DAB módszer (1) A módszer elve: a triptofán p-dimetil-amino-benzaldehiddel 19n kénsavas közegben színtelen kondenzációs terméket képez, mely NaNO, hatására kék színű vegyületté oxidálódik. 18
3 Reagensek' p-dimetil-amino-benzaldehid p.a. (DAB) 19n H S04 NaNO", p.a. L-triptofán, 1/14 árj. minőség (REANAL) Az eljárás leírása: 10,00 mg fehérje-mintát 20 cm:i-es, csiszolt üvegdugós kémcsőbe mérünk, majd hozzáadunk 20 cm3 frissen készített reagenst (30 mg DAB 10 cm 119n 1i.,S04- ban oldva) A kémcsövet összezárás nélkül 16,5 órán át, szobahőmérsékleten (20 25 T ), sötétben állni hagyjuk, majd hozzáadunk 0,1 cm3 frissen készített 0,045% NaN()2-et tartalmazó vizes oldatot és összerázzuk. 1 /2 órai sötétben történő állás után a kémcsőben levő folyadékot ismét összerázzuk, szűrjük (célszerű finom pórusú üvegszűrőn, vákuumban) és a kék színű oldat extinkcióját 590 nm-nél (Spektromom 204) mérjük. A vakpróba a leírtak szerint készül, DAB-reagens nélkül. A triptofántartalmat kalibrációs görbe alapján számítjuk (1. ábra). A kalibrációs görbét L-triptofánnal a fent leírt körülmények között vettük fel. 2 GL Y-módszer (5) A módszer elve: az ecetsavból FeCF hatására fokozottabban képződő glioxálsav triptofánnal színes vegyületet képez. Reagensek: A) Jégecet - FeCI3 oldat: 5,4 g FeCl3-бНХИ 10 cm3 vízben és néhány csepp jégecetben oldunk [(Fe/OH)3 képződés megakadályozása], majd ezen oldat 0,5 cm3-ét jégecettel 1 1-re hígítjuk. Barna üvegben tároljuk. В ) 25,8n H2S04-oldat C) Standard oldat: 25 mg L-triptofánt +15 cm3 0,075n NaOH-ot desztillált vízzel 250 cm3-re hígítunk. Barna üvegben tároljuk. E5901 3* 19
4 Az eljárás leírása: 10,00 mg mintát 15 cm3-es üvegdugós kémcsőbe mérünk, a várható triptofántartalomtól függően 1 x-es ( /ug Try/10 mg minta) vagy 2x-es reagens mennyiséget alkalmazunk. Hús és hústermékek esetén 2x-es reagens felesleggel dolgozva, a következőképpen járunk el: a bemért mintához hozzáadunk 2 cm3 0,075n NaOH-ot, majd 6 cm3 A reagenst és 4 cm3,,b reagenst, a kémcső tartalmát jól összerázzuk és 1 órán át a reakció elegyet 60 C-on tartjuk, 20 percenként az elegyet jól összerázzuk. Egy óra elteltével a kémcsöveket jeges vízbe helyezzük, majd centrifugáljuk (4000 ford/perc). Az extinkció értékét 545 nm-nél (Spektromom204) olvassuk le. A vakpróba minta nélkül készül, csupán a reagenseket tartalmazva. A triptofántartalom értékét kalibrációs görbéről olvassuk le (2. ábra). A kalibrációs görbét L-triptofánnal vesszük fel, a reakció körülményei csak az optimális reakcióidőben különböznek, a 60 C-on történő hőkezelés 110 percig tart. Kémiai vizsgálatok: A fehérjetartalmat roncsolás után automata analizátoron (7) határoztuk meg. A hidroxiprolin és a nem-kötőszöveti fehérjetartalmat Szeredy (8, 9) módszerével állapítottuk meg. Statisztikai analízis: Az eredményeket variancia analízissel értékeltük. A két triptofán módszerrel nyert értéket Zukál és mtsai. (10) szerint hasonlítottuk össze. A regressziós egyenesek különböző modellekkel történő lehetséges helyettesitését Mandel (11) szerint vizsgáltuk meg. EREDMÉNYEK Hús és hústermékek triptofántartalmának meghatározására két módszert alkalmaztunk. A kísérleti részben leírt reakciók számára az optimális körülményeket részben az irodalom, részben pedig saját kisérleteink alapján valósítottuk meg. A DAB-inódszer esetében a 16,5 órás reakcióidő nem a reakciót tekintve optimális, hanem a vizsgálat elvégzéséhez kedvező időtartam. (A 8-16 óra közti optimális reakció-idő rutin analizisnél csak automatikus berendezésekkel valósítható meg). Tekintve, hogy a triptofántartalmat L-triptofánnal felvett kalibrációs görbe segítségével számítjuk és várható, hogy a szabad aminosavként és peptidkötésben levő triptofán másképpen reagál p-dimetil-amino-benzaldehiddel, a módszer használhatóságának megerősitésére ismert mennyiségű szabad triptofánt (loo^g) kevertünk a húsmintába és vizsgáltuk a visszanyerhető triptofán mennyiségét. Az 5-5 párhuzamos vizsgálat számított, szabad aminosavként jelenlevő triptofán átlagértéke (101,04+4,52) nem tért el szignifikánsan a bemért értéktől. Ugyanazon húsmintából különböző mennyiségeket bemérve a mintasúly és mért extinkció érték között lineáris összefüggést kaptunk, az extinkció alapján (kalibrációs görbe) számított triptofántartalon nem különbözött szignifikánsan (3. ábra). A kísérletek ismétlése (1. és II.) során kapott triptofántartalmak t próbával való összehasonlítása a módszer jó reprodukálhatóságára utal (1. táblázat). 20
5 A DAB-módszer reprodukálhatóságának vizsgálata 7. táblázat M inta jel (parallel) Bem ért súly mg E s 1. ismétlés II. ismétlés t próba A ( 3 ) ,141+0,015 0, ,020 0,068 В ( 3 ) ,252+0,007 0, ,018 2,32 C (3)... lő 0,417+0,019 0, ,004 1,72 D (3) , ,065 0,497+0,011 0,29 E ( 3 ) , ,020 0, ,031 1,42 Jelölés: E590 = 590 nm -nél 1 cm-es küvettában m ért extinkció s = szórás A GLY módszer alkalmazásánál a kalibrációs görbét ugyancsak L-triptofánnal vettük fel, mivel azonban a szabad és kötött triptofán reakcióideje lényegesen eltér, a kalibráció felvételénél a Concon (5) ált 11javasolt és általunk is megerősített 110'-es hőkezelést alkalmaztuk, húsminták esetében meghatároztuk az optimális reakcióidőt mely 60' volt. Mivel a módszer 100,ug triptofántartalomig használható és húsminták esetében az alkalmazott bemérésnél a várható triptofán érték azt meghaladja, megvizsgáltuk az extinkció és hígítás közötti összefüggést és azt találtuk, hogy a kalibrációs görbe felvételénél megállapított extinkció tartományban (Lambert-Beer törvény érvényes) a reagens mennyiségének növelése nem befolyásolja a kapott eredményt (4. ábra). Az ismeretlen minta triptofántartalmának számítása a következő összefüggések alapján történt: DAB-módszer triptofán fig/20 cm3 = 394,63 E s 90,i cm, GYL-módszer triptofán ^g/6 cin3 = 209,56 E s45,i cm, ahol E = a megfelelő hullámhosszon, 1 cm-es küvettában mért extinkció érték. Az említett összefüggésekhez a Mandel (ll)-féle variancia analízis eredményei vezettek. 21
6 A kiválasztott két módszer segítségével 61 húsmintát (nyers hús és húskészítmény) analizáltunk. Az 5. ábrán a két módszerrel nyert triptofán értékek közötti összefüggést szemléltettük. A módszerek matematikai összehasonlítását Zukál és rntsai (10) szerint végeztük el. 5. ábra Különböző általunk előállított és kereskedelemben kapható fehérje DABmódszerrel meghatározott triptofántartalma látható a 2. táblázatban. Különböző fehérjék triptofántartalma DAB-módszerrel meghatározva 2. táblázat F E H É R JE T riptofán.. X 100 feherje Sertés m iofibrillárisfehérje... 1,63 Sertés szark o p lazm afeh érje... Album in (m arha szérum )... 2,08 0,62 ívlioglobin (ló s z ív )... 1,63 Achilles in (m a rh a )... 0,07 L igam entum nuchae ( m a r h a )... 0,06 V érplazm a-por (P ápa)... 1,28 PR Ö M IN E-D... 0,95 E M -H V... 1,75 Fagyasztott vérplazm a (Cegléd, P E N O M A H )... 1,51 T ejpor (H ajdúm eevei T ejipari V á lla la t)... 1,46 ÉRTÉKELÉS Hús- és húskészítményekben a triptofán előfordulhat szabad aminosavként és kötött állapotban, fehérjék, peptidek alkotóelemeként. A vizsgálatokhoz szükséges kis mennyiségű, homogén minta bemérése (max. 100 /ug triptofántartalom), csak megfelelő minta-előkészítés után lehetséges. Az általunk kidolgozott előkészítési művelet során, a mintákban levő szabad triptofán nagyobb része az oldószerbe került, így az alkalmazott módszerek segítségével tulajdonképpen a hús és hústermékek pepiid kötésben levő triptofántartalmát határoztuk meg. A vizsgált 61 minta triptofántartalmára, a kiválasztott két meghatározási módszer segítségével némileg eltérő értékeket kaptunk (5. ábra). Az eltérés várható 22
7 volt a mintákban jelenlevő egyéb a két reakciót különbözőképpen zavaró anyagok elenléte miatt. Brieskorn és Berg (12) szerint a glioxálsav specifikusabb triptofánja, mint a p-dimetil-amino-benzaldehid. A húskészítmények triptofántartalmát a termék összfehérjetartalmára vonatkoztattuk. Egyes készítmények esetében (pl. lecsókolbász) az összfehérje jelentős részét triptofánt nem tartalmazó kötőszöveti fehérje teszi ki. Ezért célszerűnek látszott a termékekre kapott triptofánértékeket összehasonlítani a kötőszövetmentes hús triptofántartalmával. E célból meghatároztuk marha és sertés longissimus dorsi és semimembranosus izmainak (5 5 minta) triptofántartalmát és nemkötőszöveti fehérjetartalmát, majd az utóbbira vonatkoztatott triptofánértékeket variancia analízissel értékeltük. Megállapítottuk, hogy a vizsgált minták triptofántartalma nem különbözött szignifikánsan, így a nyert értékeket átlagoltuk és a termékek triptofántartalmát ehhez az értékhez hasonlítottuk. ( triptofán 100 \ Az átlagértékek a következők voltak: Vnem-kötőszöveti fehérje ) DAB-módszerrel: 1,41+0,08% GLY-módszerrel: 1,34 + 0,08% A húskészítmények analízisénél kapott eredményekből (2. táblázat) a következőket állapítottuk meg: Húskészítmények átlagos fehérje jellemzői (átlag ± szórás) 2. táblázat Jellemzők Párizsi Lecsó- 1 F ü stö ltkolbász j kolbász Téliszalámi Összfehérje % (m intasúlvra)... 10,81 + 1,02 17,10 + 0,89 16,48+ 1,84 22,43+ 1,86 DAB (eredeti m intára).. (fe h é rjé re )... 0,154+0,016 1,44 +0,156 0,220+0,026 1,29 ± 0,147 0,207+0,030 1,27+ 0,164 0, ,032 1,36 ± 0,215 GLY (eredeti m intára).. (fe h é rjé re )... ПП Гhidroxiprolin 8 I L összfehérjére J, 00 Г trip to fá n I nem kötőszéveti I L fehérje try J 0,150+0,015 1,40 ± 0,127 0, ,030 1,23 ± 0,167 0, ,027 1,20 ± 0,10 0, ,019 1,29 ± 0,143 18,52+3,92 29,92+5,00 23,82 + 4,12 13,62+ 1,46-8,6+ 0,87 8,4+ 1,12 10,50+ 1,29 11,00 ± 0, , ,42 - A PÁRIZSI fehérjére vonatkoztatott triptofántartalma meglehetősen nagy (1,44 ill. 1,40%), egyes minták esetében meghaladja az 1,41 ill. 1,34 értéket; a nagy triptofántartalom csak a különböző fehérjeadalékok (vérplazma, tejpor, kazeinát) használatának tulajdonítható. A vizsgált PÁRIZSI minták kötőszövettartalma hidroxiprolintartalom alapján számítva, az összfehérje százalékában kifejezve 18,52% volt. A készítményt tehát nagy triptofántartalom és nagy hidroxiprolitartalom jellemzi. A LECSÓ- és FÜSTÖLT-kolbászok triptofántartalma kisebb a nemkötőszöveti fehérjékre vonatkoztatott triptofántartalomnál. A FÜSTÖLT-kol 23
8 bász triptofántartalma (1,27%) és kötőszöveti fehérjetartalma (23,82%) is kisebb, mint a LECSÓ-kolbászé, (1,29%, 29,92%) valószínű, hogy a lecsókolbászokhoz adagolt Na-kazeinát eredményezi a nagyobb triptofántartalmat. A TÉLISZALÁMI triptofántartalma kisebb (1,36+0,215%) a nemkötőszöveti fehérjék triptofántartalmánál. Hústermékek kötőszövettartalmának meghatározására legáltalánosabban használt módszer a hidroxiprolintartalom alapján történő számítás. A módszernek számos hibája van, melyek közül legjelentősebb, mint már a bevezetőben említettük a kötőszöveti fehérjék eltérő hidroxiprolintartalmából adódik. Új lehetőségként kínálkozott a kötőszövettartalom közvetett úton való számítása. Az izomfehérjék mennyiségét a kötőszövetmentes hús triptofántartalmára kapott átlagérték segítségével számítottuk a hústermék triptofántartalma alapján. A kötőszöveti fehérjetartalom a (100-izomfehérje) különbség. Az így nyert kötőszövettartalmakat összehasonlítottuk a hidroxiprolintartalom alapján számítottal és lényegesen eltérő értékeket kaptunk (2. táblázat). A triptofántartalom segítségével számított érték jóval kisebb, egyes termék (pl. párizsi) esetében olyan, mintha az nem is tartalmazna kötőszövetet. Ezen kis értékek csak részben magyarázhatók a termékekhez adagolt nagyobb triptofántartalmú adalékokkal (pl. tejpor, Na-kazeinát, vérplazma). Feltételezhető, hogy a kisszámú vizsgálat alapján (5 5) a két különböző állatra és izomcsoportra kapott, szignifikánsan nem különböző triptofán értékek nem reprezentálják az egész állatra, ennek minden egyes izomcsoportjára jellemző triptofántartalmat. Közleményekből ismert, hogy a miofibrilláris fehérjéket alkotó fő fehérjék az aktin és miozin triptofántartalma (2,1 ill. 0,82) eltérő és még nagyobb különbségek találhatók a szarkoplazmafehérjéket alkotó egyes fehérjefrakciók között, a fehérjék arányának változásával az izomban, tehát változhat a triptofántartalom is. Feltételeztük továbbá hústermékek esetében a fűszerek, nitrites só zavaró hatását, hőkezelt termékeknél a zselatinálódott kollagén kioldódását a minta előkészítése során, elképzelhető hőkezelt termékeknél a nyers állapotban maszkírozott triptofáncsoportok hozzáférhetővé válása is. Ezen hibalehetőségek megvizsgálására kísérleteket folytattunk. A vizsgált hústermékeknél nagyobb mennyiségben használt fűszer a bors és a paprika. A DAB-módszerrel meghatározott, bemért mintasúlyra vonatkoztatott triptofántartalom bors esetében 0,17%, a paprikáé 0,12% volt. A termékhez adagolt, viszonylag kis mennyiségű, nem nagy triptofántartalmú fűszer semmiképpen nem eredményezhet lényegesen nagyobb triptofán értéket. A továbbiakban megvizsgáltuk ugyanannak a húsnak (2 sertés, 2 marha) a triptofántartalmát nyers állapotban, hőkezelés, valamint nitrites só hozzáadása és hőkezelés után. Megállapítottuk, hogy sem a DAB-, sem a GLYmódszerrel nyert triptofántartalmak nem különböztek szignifikánsan. Az eddigi eredményeket összefoglalva megállapíthatjuk, hogy lehetséges a hústermékek biológiai értékére triptofántartalom alapján egy mérőszámot megadni annál is inkább, mivel a triptofán az eszenciális aminosavak egyike és jelenléte élelmiszereinkben táplálkozásélettani szempontból igen fontos, azonban a kötőszövettartalmat ily módon számítani nem lehet. A kötőszövettartalom számlására minden hibája ellenére jelenleg a hidroxiprolintartalom maghatározásán alapuló módszer marad. 24
9 IRODALOM (1) Spies, J. R., Chambers, D. C.: Anal. Chem., 21, 1249, (2) Репке, В., Ferenczi, R., Kovács, К, K.: A nal. Biochem., 60, 45, (3) M iller, E. L.: J. Sei. Fd Agric. 18, 381, (4) Spies, J. R., Chambers, D. C.: Anal. Chem., 20, 30, (5) Concon, J. M.: A nal. Biochem., 67, 206, (6) M ihälyi-kengyel, V., Zukál, E., Körmendy, L.: Acta A lim entaria, 4, 367, (7) M ihályi, Gy.-né: Élelmezési Ipar, 29, 200, (8) Szeredy, 1.: É V IR E, 16, 17, (9) Szeredy, I.: É V IR E, 3, 234, (10) Zukál, E., Fényes, T., Körmendy, L.: R ísérletügyi Rözlem ények L X III E. Élelm iszeripar, 1-3, 41, (11) M andel, J.: The S tatistical Analysis of E xperim ental D ata, Interscience Publishers, New Y ork, London, Sydney, (12) Brieskorn, C. H., Berg, H. W.: Z. U. L. 109, 302, 391, ОПРЕДЕЛЕНИЕ ТРИПТОФАНА В МЯСЕ И МЯСНЫХ ИЗДЕЛИЯХ Ржащинэ - Сомбати Э., Орландо Преса Кабалиеро, Михалинэ - Кендьел В. и др. Кёрменди Л. Для определения триптофана в пептидной связи мяса и мясных изделий авторы применяли два метода, а именно: определение из негидролизованного белка п-диметил-амино-бензалдегидом иреагентом глиоксаловой кислоты, значения триптофана полученные по этим д в у м методам отличались друг от друга. Содержание триптофана в говяжих и свинных длинных спинных п о л у - перепончатых мышцах не отличалось сигнификантно, величина триптофана отнесенной на белки несоединительных тканей с п-диметил-аминобензалдегидом 1,41%, с глиоксаловой кислотой 1,34%. Сравнивали содержание триптофана четырёх видов мясных изделий (безструктурной колбасы, колбасы, для лечо, копчённой колбасы и венгерской салями) с содержанием триптофана мяса без соединительных тканей. Установили, что в безструктурной мягкой колбасе и в колбасе для лечо высокое содержание триптофана образуется с одной части из-за применения кровянной плазмы, сухого молока и казеината, дальше количество соединительных тканей в расчете на содержание триптофана, в случае если не применяют добавочные ващества, будет меньше количества расчитанного на основании содержания гидроксипролина. Значит содержание триптофана может характеризовать биологическую стоимость одного мясного продукта, но не можно его применять для непрямого определения содержания соединительных тканей. BESTIMMUNG VON TRYPTOPHAN IN FLEISCH UND FLEISCHPRODUKTEN Rékasi - Szombati, É., Orlando Caballero, Presa V. Mihályi - Lengyel und L. Körmendy Zwei Methoden wurden zur Bestimmung des in Peptidbindung anwesenden Tryptophangehaltes von 61 Mustern von Fleisch und Fleischprodukten angewendet, die Bestimmung wurde mit unhydrolysiertem Protein mittels der Reagenzien p-dimethylaminobenzaldehyd bzw. Glyoxalsäure durchgeführt. Die mit den zwei Methoden erhaltenen Tryptophanwerte waren voneinander abweichend. Keine signifikante Unterschiede wurden zwischen den Tryptophangehalten des 4 Élelm iszervizsgálati Rözlemények 25
10 Muskel longissimus dorsi und semimembranosus von Rindvieh und Schwein beobachtbar. Der Tryptophangehalt bezüglich des nicht-bindegewebeproteins war mit p-ditnethylaminobenzaldehyd 1,41%, während mit Glyoxalsäure 1,34%. Der Tryptophangehalt von vier Fleischprodukten (Pariserwurst, Letschowurst, Rauchwurst und Wintersalami) wurde mit dem Tryptophangehalt des von Bindegewebe freien Fleisches verglichen. Es wurde dabei gefunden, dass der höhere Gehalt an Tryptophan in der Pariserwurst und in der Letschowurst zum Teil dem als Zusatzstoff angewendeten Blutplasma, Milchpulver und Caseinat zugeschrieben werden kann, ferner dass die Menge der auf Grund des Tryptophangehaltes berechneten Bindegewebe sogar in Abwesenheit von Zusatzstoffen geringer ist, als die auf Grund des Hydroxyprolingehaltes berechnete Menge. Deshalb, obwohl der biologische Wert eines Fleischproduktes durch den Wert des Tryptophangehaltes gekennzeichnet werden kann, ist dieser letztere Wert zur indirecten Bestimmung des Bindegewebegehaltes der Produkte nicht anwendbar. DETERMINATION OF TRYPTOPHAN IN MEAT AND IN MEAT PRODUCTS É. Rékasi Szombati, Orlando Presa Caballero, V. Mihályi - Lengyel and L. Körmendy Two methods were applied for the determination of the tryptophan content in peptidic bond present in 61 samples of meat and meat products. Determinations were carried out from non-hydrolyzed protein, with the use of p-dimethylaminobenzaldehyde and glyoxylic acid as reagents. Tryptophan values obtained by the two methods differed from each other. No significant deviations were found between the tryptophan contents observed in longissimus dorsi and semimembranosus muscles of cattle and pig, the tryptophan value referred to non-connective tissue protein was 1.41% with the use of p-dimethylaminobenzaldehyde whereas 1.34% with the use of glyoxalic acid. The tryptophan contents of four types of meat products ( Parisian sausage, letcho sausage, smoked sausage and winter salami) were compared with the tryptophan content of meat free of connective tissue. It was found that the higher contents of tryptophan in the Parisian and letcho sausages may be due partly to blood plasm, powdered milk and caseinate applied as additives during the manufacturing process. Besides, the amount of connective tissue calculated on the vasis of the tryptophan content was even in the absence of additives smaller than that calculated on the basis of the content of hydroxyproline. Consequently, though the value of tryptophan content may serve as a characteristic of the biological value of a meat product, it cannot be used for the indirect determination of the content of connective tissue of the products. 26
Pálinkák réztartalom meghatározási módszereinek összehasonlítása
 Pálinkák réztartalom meghatározási módszereinek összehasonlítása ВЕКЕ ÉVA és MANDEL PÁL Fővárosi Élelmiszerellenőrző és Vegyvizsgáló Intézet, Budapest A kereskedelmi és bérfőzésből származó és a forgalmazásra
Pálinkák réztartalom meghatározási módszereinek összehasonlítása ВЕКЕ ÉVA és MANDEL PÁL Fővárosi Élelmiszerellenőrző és Vegyvizsgáló Intézet, Budapest A kereskedelmi és bérfőzésből származó és a forgalmazásra
Húskészítmények kötőszöveti fehérjetartalmának vizsgálata*.
 Húskészítmények kötőszöveti fehérjetartalmának vizsgálata*. OJTOZY KRISTÓFNE Fővárosi Élelmiszerelienőrző és Vegyvizsgáló Intézet, B udapest Táplálkozásunk elengedhetetlen alapanyaga az állati eredetű
Húskészítmények kötőszöveti fehérjetartalmának vizsgálata*. OJTOZY KRISTÓFNE Fővárosi Élelmiszerelienőrző és Vegyvizsgáló Intézet, B udapest Táplálkozásunk elengedhetetlen alapanyaga az állati eredetű
MINTAJEGYZŐKÖNYV A VÉRALVADÁS VIZSGÁLATA BIOKÉMIA GYAKORLATHOZ
 MINTAJEGYZŐKÖNYV A VÉRALVADÁS VIZSGÁLATA BIOKÉMIA GYAKORLATHOZ Feladatok 1. Teljes vér megalvasztása rekalcifikálással 1.1 Gyakorlat kivitelezése 1.2 Minta jegyzőkönyv 2. Referenciasor készítése fehérjeméréshez
MINTAJEGYZŐKÖNYV A VÉRALVADÁS VIZSGÁLATA BIOKÉMIA GYAKORLATHOZ Feladatok 1. Teljes vér megalvasztása rekalcifikálással 1.1 Gyakorlat kivitelezése 1.2 Minta jegyzőkönyv 2. Referenciasor készítése fehérjeméréshez
Ecetsav koncentrációjának meghatározása titrálással
 Ecetsav koncentrációjának meghatározása titrálással A titrálás lényege, hogy a meghatározandó komponenst tartalmazó oldathoz olyan ismert koncentrációjú oldatot adagolunk, amely a reakcióegyenlet szerint
Ecetsav koncentrációjának meghatározása titrálással A titrálás lényege, hogy a meghatározandó komponenst tartalmazó oldathoz olyan ismert koncentrációjú oldatot adagolunk, amely a reakcióegyenlet szerint
1. feladat Összesen: 7 pont. 2. feladat Összesen: 16 pont
 1. feladat Összesen: 7 pont Gyógyszergyártás során képződött oldatból 7 mintát vettünk. Egy analitikai mérés kiértékelésének eredményeként a következő tömegkoncentrációkat határoztuk meg: A minta sorszáma:
1. feladat Összesen: 7 pont Gyógyszergyártás során képződött oldatból 7 mintát vettünk. Egy analitikai mérés kiértékelésének eredményeként a következő tömegkoncentrációkat határoztuk meg: A minta sorszáma:
FEHÉRJETARTALOM MEGHATÁROZÁSA NESSLER- REÁGENSSEL KIFEJLESZTETT SZÍN FOTOMETRIÁS KIÉRTÉKELÉSÉVEL HÚSIPARI TERMÉKBEN
 FEHÉRJETARTALOM MEGHATÁROZÁSA NESSLER- REÁGENSSEL KIFEJLESZTETT SZÍN FOTOMETRIÁS KIÉRTÉKELÉSÉVEL HÚSIPARI TERMÉKBEN POLÁK ARANKA* Az élelmiszeriparban táplálkozásélettani és kereskedelmi szempontból nagy
FEHÉRJETARTALOM MEGHATÁROZÁSA NESSLER- REÁGENSSEL KIFEJLESZTETT SZÍN FOTOMETRIÁS KIÉRTÉKELÉSÉVEL HÚSIPARI TERMÉKBEN POLÁK ARANKA* Az élelmiszeriparban táplálkozásélettani és kereskedelmi szempontból nagy
Forralt bor vizsgálata
 Forralt bor vizsgálata SISKA ELEMÉR, B. NÉ M A O Y A R I ÁGNES, E N G L E R T DEZSŐ Megyei Élelm iszerellenőrző és Vegyvizsgáló Intézet, Veszprém Érkezett: 1981. november 4. A forralt bor különösen a téli
Forralt bor vizsgálata SISKA ELEMÉR, B. NÉ M A O Y A R I ÁGNES, E N G L E R T DEZSŐ Megyei Élelm iszerellenőrző és Vegyvizsgáló Intézet, Veszprém Érkezett: 1981. november 4. A forralt bor különösen a téli
Víztechnológiai mérőgyakorlat 2. Klórferőtlenítés törésponti görbe felvétele. Jegyzőkönyv
 A mérést végezte: NEPTUNkód: Víztechnológiai mérőgyakorlat 2. Klórferőtlenítés törésponti görbe felvétele Jegyzőkönyv Név: Szak: Tagozat: Évfolyam, tankör: AABB11 D. Miklós Környezetmérnöki Levlező III.,
A mérést végezte: NEPTUNkód: Víztechnológiai mérőgyakorlat 2. Klórferőtlenítés törésponti görbe felvétele Jegyzőkönyv Név: Szak: Tagozat: Évfolyam, tankör: AABB11 D. Miklós Környezetmérnöki Levlező III.,
2. Fotometriás mérések II.
 2. Fotometriás mérések II. 2008 október 31. 1. Ammónia-nitrogén mérése alacsony mérési tartományban és szabad ammónia becslése 1.1. Háttér A módszer alkalmas kis ammónia-nitrogén koncentrációk meghatározására;
2. Fotometriás mérések II. 2008 október 31. 1. Ammónia-nitrogén mérése alacsony mérési tartományban és szabad ammónia becslése 1.1. Háttér A módszer alkalmas kis ammónia-nitrogén koncentrációk meghatározására;
Sajt fehérjetartalmának spektrofotometriás meghatározása az ultraibolya tartományban
 Sajt fehérjetartalmának spektrofotometriás meghatározása az ultraibolya tartományban GÁBOR MIKLÓSNÉ Élelm iszeripari Főiskola, Szeged, Kém ia Tanszék Érkezett: 1977. december 10. Az eljárás elvi alapjai
Sajt fehérjetartalmának spektrofotometriás meghatározása az ultraibolya tartományban GÁBOR MIKLÓSNÉ Élelm iszeripari Főiskola, Szeged, Kém ia Tanszék Érkezett: 1977. december 10. Az eljárás elvi alapjai
2019. április II.a, II.b
 A program részben az Emberi Erőforrások Minisztériuma a megbízásából a Nemzeti Tehetség g Program éss az Emberi Támogatáskezelő által meghirdetett NTP TMV 18 0139 azonosítószámú pályázati támogatásból
A program részben az Emberi Erőforrások Minisztériuma a megbízásából a Nemzeti Tehetség g Program éss az Emberi Támogatáskezelő által meghirdetett NTP TMV 18 0139 azonosítószámú pályázati támogatásból
Hidroxiprolin meghatározására alkalmazott módszerek összehasonlító vizsgálata
 Hidroxiprolin meghatározására alkalmazott módszerek összehasonlító vizsgálata B Á L IN T M IH Á L Y Megyei Élelmiszerellenőrző és Vegyvizsgáló Intézet, Zalaegerszeg Érkezett: 1977. szeptember 7. A húsipar
Hidroxiprolin meghatározására alkalmazott módszerek összehasonlító vizsgálata B Á L IN T M IH Á L Y Megyei Élelmiszerellenőrző és Vegyvizsgáló Intézet, Zalaegerszeg Érkezett: 1977. szeptember 7. A húsipar
CLOXACILLINUM NATRICUM. Kloxacillin-nátrium
 Cloxacillinum natricum Ph.Hg.VIII. Ph.Eur.5.7-1 04/2007:0661 CLOXACILLINUM NATRICUM Kloxacillin-nátrium C 19 H 17 ClN 3 NaO 5 S.H 2 O M r 475,9 DEFINÍCIÓ Nátrium-[(2S,5R,6R)-6-[[[3-(2-klórfenil)-5-metilizoxazol-4-il]karbonil]amino]-
Cloxacillinum natricum Ph.Hg.VIII. Ph.Eur.5.7-1 04/2007:0661 CLOXACILLINUM NATRICUM Kloxacillin-nátrium C 19 H 17 ClN 3 NaO 5 S.H 2 O M r 475,9 DEFINÍCIÓ Nátrium-[(2S,5R,6R)-6-[[[3-(2-klórfenil)-5-metilizoxazol-4-il]karbonil]amino]-
AQUA AD DILUTIONEM SOLUTIONUM CONCENTRATARUM AD HAEMODIALYSIM. Tömény hemodializáló oldatok hígítására szánt víz
 concentratarum ad haemodialysim Ph.Hg.VIII. Ph.Eur.6.3-1 01/2008:1167 javított 6.3 AQUA AD DILUTIONEM SOLUTIONUM CONCENTRATARUM AD HAEMODIALYSIM Tömény hemodializáló oldatok hígítására szánt víz Az alábbi
concentratarum ad haemodialysim Ph.Hg.VIII. Ph.Eur.6.3-1 01/2008:1167 javított 6.3 AQUA AD DILUTIONEM SOLUTIONUM CONCENTRATARUM AD HAEMODIALYSIM Tömény hemodializáló oldatok hígítására szánt víz Az alábbi
NATRII AUROTHIOMALAS. Nátrium-aurotiomalát
 Natrii aurothiomalas Ph.Hg.VIII. Ph.Eur.5.8-1 07/2007:1994 NATRII AUROTHIOMALAS Nátrium-aurotiomalát DEFINÍCIÓ A (2RS)-2-(auroszulfanil)butándisav mononátrium és dinátrium sóinak keveréke. Tartalom: arany
Natrii aurothiomalas Ph.Hg.VIII. Ph.Eur.5.8-1 07/2007:1994 NATRII AUROTHIOMALAS Nátrium-aurotiomalát DEFINÍCIÓ A (2RS)-2-(auroszulfanil)butándisav mononátrium és dinátrium sóinak keveréke. Tartalom: arany
FEHÉRJETARTALOM MEGHATÁROZÁSA FOTOMETRIÁS MÓDSZERREL BAROMFIHÚSBAN
 FEHÉRJETARTALOM MEGHATÁROZÁSA FOTOMETRIÁS MÓDSZERREL BAROMFIHÚSBAN POLÁK ARANKA* A fehérjetartalom vizsgálata rendkívül fontos probléma a minőség változásával, ellenőrzésével foglalkozó laboratóriumokban.
FEHÉRJETARTALOM MEGHATÁROZÁSA FOTOMETRIÁS MÓDSZERREL BAROMFIHÚSBAN POLÁK ARANKA* A fehérjetartalom vizsgálata rendkívül fontos probléma a minőség változásával, ellenőrzésével foglalkozó laboratóriumokban.
A raffinóztartalom meghatározása melaszokban*
 A raffinóztartalom meghatározása melaszokban* POLACSEKNÉ RÁ CZ MÁRIA, SZÉP IVÁNN É **, V Á M О S N É VIGYÁZÓ LILLY K ö zp on ti É lelm iszeripari K u ta tó Intézet, Budapest Érkezett: 1981. április 2.
A raffinóztartalom meghatározása melaszokban* POLACSEKNÉ RÁ CZ MÁRIA, SZÉP IVÁNN É **, V Á M О S N É VIGYÁZÓ LILLY K ö zp on ti É lelm iszeripari K u ta tó Intézet, Budapest Érkezett: 1981. április 2.
7. gyak. Szilárd minta S tartalmának meghatározása égetést követően jodometriásan
 7. gyak. Szilárd minta S tartalmának meghatározása égetést követően jodometriásan A gyakorlat célja: Megismerkedni az analízis azon eljárásaival, amelyik adott komponens meghatározását a minta elégetése
7. gyak. Szilárd minta S tartalmának meghatározása égetést követően jodometriásan A gyakorlat célja: Megismerkedni az analízis azon eljárásaival, amelyik adott komponens meghatározását a minta elégetése
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Fehérjealapú adalék anyagok emulziókapacitásának meghatározása
 Fehérjealapú adalék anyagok emulziókapacitásának meghatározása O R M AINÉ CSERHALMI ZSUZSANNA és KUCSORA ISTVÁN K ö zp o n ti É lelm iszerip a ri K u ta tó in té ze t É r k e z e tt: 1 9 8 6. jú n i u
Fehérjealapú adalék anyagok emulziókapacitásának meghatározása O R M AINÉ CSERHALMI ZSUZSANNA és KUCSORA ISTVÁN K ö zp o n ti É lelm iszerip a ri K u ta tó in té ze t É r k e z e tt: 1 9 8 6. jú n i u
2. Fotometriás mérések I.
 2. Fotometriás mérések I. 2008 október 17. 1. Szín mérése Pt-Co skálán[5] 1.1. Háttér A platina-kobalt színskála közel színtelen folyadékok sárga árnyalatainak meghatározására alkalmas. Eredetileg szennyvizek
2. Fotometriás mérések I. 2008 október 17. 1. Szín mérése Pt-Co skálán[5] 1.1. Háttér A platina-kobalt színskála közel színtelen folyadékok sárga árnyalatainak meghatározására alkalmas. Eredetileg szennyvizek
Titokzatos gyümölcskocsonya
 Titokzatos gyümölcskocsonya A gyümölcstorta igazán csábító édesség és elkészíteni sem olyan nagy ördöngösség. Kivéve, ha valami mégsem sikerül. Például nem dermed meg a tetején a zselé De hát miért?! Hiszen
Titokzatos gyümölcskocsonya A gyümölcstorta igazán csábító édesség és elkészíteni sem olyan nagy ördöngösség. Kivéve, ha valami mégsem sikerül. Például nem dermed meg a tetején a zselé De hát miért?! Hiszen
Tápszerek triptofántartalmának változása hőkezelés hatására
 Tápszerek triptofántartalmának változása hőkezelés hatására ÖRSI FERENC és HOLLÓSY JUDIT Budapesti Műszaki Egyetem Biokémiai és Élelmiszertechnológiai Tanszék Érkezett: 1983. június 20. A tápszerek biológiai
Tápszerek triptofántartalmának változása hőkezelés hatására ÖRSI FERENC és HOLLÓSY JUDIT Budapesti Műszaki Egyetem Biokémiai és Élelmiszertechnológiai Tanszék Érkezett: 1983. június 20. A tápszerek biológiai
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével
 5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével 5.1. Átismétlendő anyag 1. Adszorpció (előadás) 2. Langmuir-izoterma (előadás) 3. Spektrofotometria és Lambert Beer-törvény
5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével 5.1. Átismétlendő anyag 1. Adszorpció (előadás) 2. Langmuir-izoterma (előadás) 3. Spektrofotometria és Lambert Beer-törvény
ó Ó ú ó ó ó Á ó ó ó Á ó ó ó ó Á ó ú ó ó ó
 É ó ú ó ú ó Á ó ó ú ó ó ó ú ó ó ó ó ú ó ó ó ó ó ó ú ó ó ú ó ó ó ó Ó ú ó ó ó Á ó ó ó Á ó ó ó ó Á ó ú ó ó ó Ö ó ó ó ó ó ó ó ó ó ó ó ó Ü ó ű ú ú ó ó ó ó ó ó ó É ó É ó É ó ó ó ó ó ó É ó ú ó ó É ó ó ó ó É ó
É ó ú ó ú ó Á ó ó ú ó ó ó ú ó ó ó ó ú ó ó ó ó ó ó ú ó ó ú ó ó ó ó Ó ú ó ó ó Á ó ó ó Á ó ó ó ó Á ó ú ó ó ó Ö ó ó ó ó ó ó ó ó ó ó ó ó Ü ó ű ú ú ó ó ó ó ó ó ó É ó É ó É ó ó ó ó ó ó É ó ú ó ó É ó ó ó ó É ó
Ú ű É ű ű Ü Ü ű ű Ú É ű ű Ü ű ű ű ű ű ű ű Ú ű ű
 Ú ű ű ű ű ű ű ű ű Ú ű É ű ű Ü Ü ű ű Ú É ű ű Ü ű ű ű ű ű ű ű Ú ű ű É ű Ú Ú Ú Ú Ú ű Á Ú Ú Ú Ú ű Ú Ú ű É ű Ú Ú Ú Ú Ú Á ű Ó ű Ú É É Ú Ú ű É ű ű ű ű É ű Ő ű Ő ű ű ű ű ű É ű É Á ű ű Ü Á Ó ű ű ű Ú ű ű É ű ű Ú
Ú ű ű ű ű ű ű ű ű Ú ű É ű ű Ü Ü ű ű Ú É ű ű Ü ű ű ű ű ű ű ű Ú ű ű É ű Ú Ú Ú Ú Ú ű Á Ú Ú Ú Ú ű Ú Ú ű É ű Ú Ú Ú Ú Ú Á ű Ó ű Ú É É Ú Ú ű É ű ű ű ű É ű Ő ű Ő ű ű ű ű ű É ű É Á ű ű Ü Á Ó ű ű ű Ú ű ű É ű ű Ú
Ó Ó ó ö ó
 É ó ö É Á ó ó ü ó Ü ó ö ú ű ö ö ö ü ó Ó Ó ó ö ó Ó Ó ö ö ö ü Ó Ó ö ö ü ö ó ó ü ü Ó Ó Ó Ó ó ö ó ö ó ö ó ö ü ö ö ü ö ó ü ö ü ö ö ö ü ü ö ü É ü ö ü ü ö ó ü ü ü ü Ó Ó ü ö ö ü ö ó ö ö ü ó ü ó ö ü ö ü ö ü ö ó
É ó ö É Á ó ó ü ó Ü ó ö ú ű ö ö ö ü ó Ó Ó ó ö ó Ó Ó ö ö ö ü Ó Ó ö ö ü ö ó ó ü ü Ó Ó Ó Ó ó ö ó ö ó ö ó ö ü ö ö ü ö ó ü ö ü ö ö ö ü ü ö ü É ü ö ü ü ö ó ü ü ü ü Ó Ó ü ö ö ü ö ó ö ö ü ó ü ó ö ü ö ü ö ü ö ó
ü ü Ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü É ü ü
 ü ü É ű ű É É ű ü ű ü ü ü Á ü ü ü ü ü ű É ü ű É ű ü ü ü Ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü É ü ü ü Á ü ü ü ü ü Ú ü ü ű É ü ü ű ü ü ű ü ü ü ü É ü ü ü ü ü ü ü ü É ű ü Á ü ü ü ü ü Á Ö É ü ü ű Ú ü ü ü ű
ü ü É ű ű É É ű ü ű ü ü ü Á ü ü ü ü ü ű É ü ű É ű ü ü ü Ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü ü É ü ü ü Á ü ü ü ü ü Ú ü ü ű É ü ü ű ü ü ű ü ü ü ü É ü ü ü ü ü ü ü ü É ű ü Á ü ü ü ü ü Á Ö É ü ü ű Ú ü ü ü ű
ű Ö ű Ú ű ű ű Á ű
 ű ű Ó É É ű Ó ű Ü ű ű Ö ű Ú ű ű ű Á ű É ű Á ű ű ű ű ű ű ű ű ű ű ű Á ű ű Ö Ü Ö É ű ű Ü Ü ű É Á Ú É É ű ű ű Ö É ű É Ó É Á Á É ű ű Á ű ű ű Á É ű Ö Á ű ű ű Á ű Á É Ö Ó Ö ű ű ű ű ű ű ű Á É Á Á ű ű ű Á ű ű ű
ű ű Ó É É ű Ó ű Ü ű ű Ö ű Ú ű ű ű Á ű É ű Á ű ű ű ű ű ű ű ű ű ű ű Á ű ű Ö Ü Ö É ű ű Ü Ü ű É Á Ú É É ű ű ű Ö É ű É Ó É Á Á É ű ű Á ű ű ű Á É ű Ö Á ű ű ű Á ű Á É Ö Ó Ö ű ű ű ű ű ű ű Á É Á Á ű ű ű Á ű ű ű
Ó é é Ó Ó ő ű Ó Ö ü Ó é Ó ő Ó Á Ö é Ö Ó Ó é Ó Ó Ó Ó ú Ó Ó Ó Ó ű Ö Ó Ó Ó é Ó Ó ö Ö Ó Ö Ö Ó Ó Ó é ö Ö é é Ü Ó Ö Ó é Ó é ö Ó Ú Ó ő Ö Ó é é Ö ú Ó Ö ö ű ő
 É Ó Ű Á Ó É Ó Á É Ó Á ő ű Ó ú Ö ú é Ö Ó Ö ú Ó Ö ú Ó Ó Ó Ó ű é ű ű Ó Ó ú ű ű é é Ö ö Ö Ö Ó ű Ó Ö ü ű Ö Ó ő Ó ő Ó ú Ó ő Ó é Ó ű Ó Ó Ó Ó ú Ó Ó Ó Ó Ö Ó Ó ö ő ü é ü Ö é é é Á é Ó Ó ú ú ű é Ö é é é Ó é é Ó Ó
É Ó Ű Á Ó É Ó Á É Ó Á ő ű Ó ú Ö ú é Ö Ó Ö ú Ó Ö ú Ó Ó Ó Ó ű é ű ű Ó Ó ú ű ű é é Ö ö Ö Ö Ó ű Ó Ö ü ű Ö Ó ő Ó ő Ó ú Ó ő Ó é Ó ű Ó Ó Ó Ó ú Ó Ó Ó Ó Ö Ó Ó ö ő ü é ü Ö é é é Á é Ó Ó ú ú ű é Ö é é é Ó é é Ó Ó
ű ű ű Ú Ú Á ű Ö ű ű Ú Ő É
 Ü ű ű ű Ú Ú Á ű Ö ű ű Ú Ő É É ű Ö Ö Á É ű Ö Ö Á Ü Á ű ű Ó Ó Á Á É Ü É ű Ó Á Ó Á ű Ö ű ű É Ü Ö ű É Ö ű ű Ó ű ű Ú ű ű ű ű ű É ű É Ú Ö Á É ű ű Ó ű ű ű ű ű ű Ó ű Ü ű ű ű É ű ű Ü Ü ű ű Ő Á Á Á ű ű ű Ó Ó Ó ű
Ü ű ű ű Ú Ú Á ű Ö ű ű Ú Ő É É ű Ö Ö Á É ű Ö Ö Á Ü Á ű ű Ó Ó Á Á É Ü É ű Ó Á Ó Á ű Ö ű ű É Ü Ö ű É Ö ű ű Ó ű ű Ú ű ű ű ű ű É ű É Ú Ö Á É ű ű Ó ű ű ű ű ű ű Ó ű Ü ű ű ű É ű ű Ü Ü ű ű Ő Á Á Á ű ű ű Ó Ó Ó ű
Á Ó ű ű Á É ű ű ű ű Ú Ú
 Ö ű ű Ö Ü ű ű ű ű ű Ó ű Ü ű Á Ó ű ű Á É ű ű ű ű Ú Ú ű ű Á Á Á É ű ű ű ű ű ű ű ű ű ű É ű Ö Ó Ú ű ű ű ű Ü Ó Ú ű É É Ó É É Ó É É É É Ó ű ű ű ű ű Ü ű Á ű ű ű ű ű Ü ű ű ű ű ű ű Á ű Ú Á Á Ö É Á Á Ö É Ü ű ű Ü
Ö ű ű Ö Ü ű ű ű ű ű Ó ű Ü ű Á Ó ű ű Á É ű ű ű ű Ú Ú ű ű Á Á Á É ű ű ű ű ű ű ű ű ű ű É ű Ö Ó Ú ű ű ű ű Ü Ó Ú ű É É Ó É É Ó É É É É Ó ű ű ű ű ű Ü ű Á ű ű ű ű ű Ü ű ű ű ű ű ű Á ű Ú Á Á Ö É Á Á Ö É Ü ű ű Ü
É Á Á Ö Á
 É Á Á Ö Á Á É Á Ü ű Á É Ü ű Ú ű ű É É ű ű Á ű ű ű ű ű É ű ű ű Á É É É ű Á É É Á É Á É Ü Ü ű Á Á Á ű Á Á Á Á Á Á Á Á Ü ű Á ű Ü É É Á Á Á É ű ű ű ű ű ű ű ű ű ű ű ű ű Á Á É É ű É ű Ő ű É Ő Á É É ű ű Ú Á
É Á Á Ö Á Á É Á Ü ű Á É Ü ű Ú ű ű É É ű ű Á ű ű ű ű ű É ű ű ű Á É É É ű Á É É Á É Á É Ü Ü ű Á Á Á ű Á Á Á Á Á Á Á Á Ü ű Á ű Ü É É Á Á Á É ű ű ű ű ű ű ű ű ű ű ű ű ű Á Á É É ű É ű Ő ű É Ő Á É É ű ű Ú Á
é ü ó ö é Ö é ü é é ó ö é ü ü é é ó ó ó é Á é é ü ó é ó ó é ö ö ö é é ü é ü é é ö ü ü é ó é é é é é é ö é é é é é é ö é ó ö ü é é é ü é é ó é ü ó ö é
 Ó Ö é ü ó ö é é ü é é ó ö é ü ü é é ó é é é é é é ö é é é é é é é ó ö ü é é é ü ó ö é Ö é ü é é ó ö é ü ü é é ó ó ó é Á é é ü ó é ó ó é ö ö ö é é ü é ü é é ö ü ü é ó é é é é é é ö é é é é é é ö é ó ö ü
Ó Ö é ü ó ö é é ü é é ó ö é ü ü é é ó é é é é é é ö é é é é é é é ó ö ü é é é ü ó ö é Ö é ü é é ó ö é ü ü é é ó ó ó é Á é é ü ó é ó ó é ö ö ö é é ü é ü é é ö ü ü é ó é é é é é é ö é é é é é é ö é ó ö ü
Á Á ő ő Ö ő ő ö É ö ő ö ő ő ö ő ő ö ő ő ü ö
 ű É É Á Á Á É Ó É É Á ö ő ő ö ő ő ő Ó ő ö ő ö ő ú ő ü ö ő ü ö Á É ű Á É É É Ö ö Á É É ő ő ö Á Á ő ő Ö ő ő ö É ö ő ö ő ő ö ő ő ö ő ő ü ö É É Á Ö ő ú ő ű Ö ü Ő É Ó É É Á Ó É Á É Ü É Á Ó É ő ő ö ö ő ö ö ö
ű É É Á Á Á É Ó É É Á ö ő ő ö ő ő ő Ó ő ö ő ö ő ú ő ü ö ő ü ö Á É ű Á É É É Ö ö Á É É ő ő ö Á Á ő ő Ö ő ő ö É ö ő ö ő ő ö ő ő ö ő ő ü ö É É Á Ö ő ú ő ű Ö ü Ő É Ó É É Á Ó É Á É Ü É Á Ó É ő ő ö ö ő ö ö ö
ű Ú ű ű É Ú ű ű
 ű ű ű ű Ú Á É Ú ű Ú ű ű É Ú ű ű ű Á ű ű ű ű ű Ü ű Á ű ű ű Á Á ű ű ű É ű ű ű Ú É ű ű ű ű ű ű ű ű Á É Á Ö Ü ű É ű ű Ö É Ü Ú ű Ó ű É Ó Ó Ó ű É Ü Ü ű ű Ú ű ű ű ű ű ű ű ű ű ű É ű ű Á Á ű Ú ű Ú ű ű Ó ű ű Ü Ü
ű ű ű ű Ú Á É Ú ű Ú ű ű É Ú ű ű ű Á ű ű ű ű ű Ü ű Á ű ű ű Á Á ű ű ű É ű ű ű Ú É ű ű ű ű ű ű ű ű Á É Á Ö Ü ű É ű ű Ö É Ü Ú ű Ó ű É Ó Ó Ó ű É Ü Ü ű ű Ú ű ű ű ű ű ű ű ű ű ű É ű ű Á Á ű Ú ű Ú ű ű Ó ű ű Ü Ü
ó ő ő ó ő ö ő ő ó ó ó ö ő ó ó ó ö ő ó ő ő ö Ö ő ö ó ő ö ő ő ú ö ö ü ö ó ö ö ö ő ö ö Ö ú ü ó ü ő ő ő ő ó ő ü ó ü ö ő ö ó ő ö ő ö ü ö ü ő ö ö ó ö ő ő ö
 ü ö ő ö ő ó ö ő ü ü ö ő ó ó ü ő ö ő ö ő ö ü ö ő ö ő ó ö ü ü ö ő ő ő ö ő ö ü ö ő ó ő ö ü ö ő ő ű ő ö ö ő ű ő ü ö Ő ó ö ö ő ü ó ü ú ű ú ő ó ó ó ő ö ő ő ö ó ö ö ő ő ö ö ó ú ő ő ö ó ö ó ö ü ó ő ő ö ó ő ő ó
ü ö ő ö ő ó ö ő ü ü ö ő ó ó ü ő ö ő ö ő ö ü ö ő ö ő ó ö ü ü ö ő ő ő ö ő ö ü ö ő ó ő ö ü ö ő ő ű ő ö ö ő ű ő ü ö Ő ó ö ö ő ü ó ü ú ű ú ő ó ó ó ő ö ő ő ö ó ö ö ő ő ö ö ó ú ő ő ö ó ö ó ö ü ó ő ő ö ó ő ő ó
Á Ö Ö Ö Ö ú ú Ö Ö Ó Ó ú ú Ü ú Ó Ö Ö Ü Ó Ö Ö Á Ó ú ú ú ű Ö Ö Ö Ö Á Ó Ö Ó ú ú Ö
 Ó ú ú ú ú ű ű ű ú Á Ö ű Á Ö Ö Ö Ö ú ú Ö Ö Ó Ó ú ú Ü ú Ó Ö Ö Ü Ó Ö Ö Á Ó ú ú ú ű Ö Ö Ö Ö Á Ó Ö Ó ú ú Ö Ú ű ú É Á Ó Ó É Ó Ó ú ű ű ű ú Ö Ó Ö ú ú Ö ú Ü ú Ü É Ö Á Á Á Á ú Ó Ö ú ú ú Ü Ö ú ú ú ú ú ú Ö ú Ö Ó ű
Ó ú ú ú ú ű ű ű ú Á Ö ű Á Ö Ö Ö Ö ú ú Ö Ö Ó Ó ú ú Ü ú Ó Ö Ö Ü Ó Ö Ö Á Ó ú ú ú ű Ö Ö Ö Ö Á Ó Ö Ó ú ú Ö Ú ű ú É Á Ó Ó É Ó Ó ú ű ű ű ú Ö Ó Ö ú ú Ö ú Ü ú Ü É Ö Á Á Á Á ú Ó Ö ú ú ú Ü Ö ú ú ú ú ú ú Ö ú Ö Ó ű
Ó Ó ö ú ö ö ö ö ü ú ú ö ö ö ú ú ö ö ö ú ú ú ű ö ö ú ö ü ö ö ö ö ü ú Á ö ü Á ö ö ö ö ö ö
 É Ó ö É Á ű Ü Ü ö Ú ö ö ö ö ö ö ö ú ö ö ö ö ö ú ú ú ú ú ú ü ú ú ö ö ű ö ü ú ö Ó Ó ö ú ö ö ö ö ü ú ú ö ö ö ú ú ö ö ö ú ú ú ű ö ö ú ö ü ö ö ö ö ü ú Á ö ü Á ö ö ö ö ö ö Á Ó ú ö Á ö Á ö ú ú ö ö ö ö ü ü Ü ú
É Ó ö É Á ű Ü Ü ö Ú ö ö ö ö ö ö ö ú ö ö ö ö ö ú ú ú ú ú ú ü ú ú ö ö ű ö ü ú ö Ó Ó ö ú ö ö ö ö ü ú ú ö ö ö ú ú ö ö ö ú ú ú ű ö ö ú ö ü ö ö ö ö ü ú Á ö ü Á ö ö ö ö ö ö Á Ó ú ö Á ö Á ö ú ú ö ö ö ö ü ü Ü ú
ö ő ü ö ő ő ü ü ő ő ő ü ö ü ü ő ú ő ő ő ü ő ő ő ő ő ú ő ő ü ő ő ő ü ö ü ú ő ő ő ő ü ü ő ő ú
 ő ű ű ő ö ö Á ö ő ü ö ő ő ü ü ő ő ő ü ö ü ü ő ú ő ő ő ü ő ő ő ő ő ú ő ő ü ő ő ő ü ö ü ú ő ő ő ő ü ü ő ő ú ő ö Á Ó ő ő ü ú ő ő ő ő Á ő ú ű ő ő ő ü ú ő ő ő ő ő ő ő ő ö ü ú ő ő ő ő ű ű ő ő ö ű ü ő ő ő ö ö
ő ű ű ő ö ö Á ö ő ü ö ő ő ü ü ő ő ő ü ö ü ü ő ú ő ő ő ü ő ő ő ő ő ú ő ő ü ő ő ő ü ö ü ú ő ő ő ő ü ü ő ő ú ő ö Á Ó ő ő ü ú ő ő ő ő Á ő ú ű ő ő ő ü ú ő ő ő ő ő ő ő ő ö ü ú ő ő ő ő ű ű ő ő ö ű ü ő ő ő ö ö
ph-számítás A víz gyenge elektrolit. Kismértékben disszociál hidrogénionokra (helyesebben hidroxónium-ionokra) és hidroxid-ionokra :
 ph-számítás A víz gyenge elektrolit. Kismértékben disszociál hidrogénionokra (helyesebben hidroxónium-ionokra) és hidroxid-ionokra : H 2 O H + + OH -, (2 H 2 O H 3 O + + 2 OH - ). Semleges oldatban a hidrogén-ion
ph-számítás A víz gyenge elektrolit. Kismértékben disszociál hidrogénionokra (helyesebben hidroxónium-ionokra) és hidroxid-ionokra : H 2 O H + + OH -, (2 H 2 O H 3 O + + 2 OH - ). Semleges oldatban a hidrogén-ion
ú ö ö ö ö ö ö Á ö ö ö á á á ű Ü ű ö ö Á á Á
 ú ú ö ö ö ö ö ö Á ö ö ö á á á ű Ü ű ö ö Á á Á Á ú á ú á Á ö á ö ö ö ú á á ö ö ö ö á ű Ü ú ö Ü ű ö ú ű á á á ú á ú ú á ö ö ú ö ú ú ö ö ú ö ö ö á ö ö ö á á ö ú ö á á Ú á ö ö ö Ü ú Á á ű ö Ü ö ú Á á ö á ö
ú ú ö ö ö ö ö ö Á ö ö ö á á á ű Ü ű ö ö Á á Á Á ú á ú á Á ö á ö ö ö ú á á ö ö ö ö á ű Ü ú ö Ü ű ö ú ű á á á ú á ú ú á ö ö ú ö ú ú ö ö ú ö ö ö á ö ö ö á á ö ú ö á á Ú á ö ö ö Ü ú Á á ű ö Ü ö ú Á á ö á ö
Természetvédő 1., 3. csoport tervezett időbeosztás
 Természetvédő 1., 3. csoport tervezett időbeosztás 4. ciklus: 2012. március 08. Optikai mérések elmélet. A ciklus mérései: 1. nitrit, 2. ammónium, 3. refraktometriax2, mérőbőrönd. Forgatási terv: Csoport
Természetvédő 1., 3. csoport tervezett időbeosztás 4. ciklus: 2012. március 08. Optikai mérések elmélet. A ciklus mérései: 1. nitrit, 2. ammónium, 3. refraktometriax2, mérőbőrönd. Forgatási terv: Csoport
ü ú ú ü ú ú ú ú
 ú ú ú ü Ü ú ú ű ú ú ü ú ü ü ú ú ü ú ú ú ú ü ú Ö ü ü ü ú ü ú Ó ü ü ű ü Á Ü ü ű ü ű ü ű ű ü Ó ű ú ú ű ú ü ü ú ű ű ú ű ü ú ű ű ü ü ü ű ü ű ü ü ű ü ü ü ü ü ü ü ü ü ú ű ü ű Ó ü ü ü ú Á Ü ú ü ű ü Á Ü Ö Ú Á Á
ú ú ú ü Ü ú ú ű ú ú ü ú ü ü ú ú ü ú ú ú ú ü ú Ö ü ü ü ú ü ú Ó ü ü ű ü Á Ü ü ű ü ű ü ű ű ü Ó ű ú ú ű ú ü ü ú ű ű ú ű ü ú ű ű ü ü ü ű ü ű ü ü ű ü ü ü ü ü ü ü ü ü ú ű ü ű Ó ü ü ü ú Á Ü ú ü ű ü Á Ü Ö Ú Á Á
Összehasonlító vizsgálatok a LECO FP-428 gyors fehérje meghatározóval és Kjeldahl módszerrel
 Összehasonlító vizsgálatok a LECO FP-428 gyors fehérje meghatározóval és Kjeldahl módszerrel GAJZÁGÓ ILDIKÓ* és BALÁZSY ANDREA** *Központi Élelmiszeripari Kutató Intézet, Budapest **GLOBUS Konzervgyár,
Összehasonlító vizsgálatok a LECO FP-428 gyors fehérje meghatározóval és Kjeldahl módszerrel GAJZÁGÓ ILDIKÓ* és BALÁZSY ANDREA** *Központi Élelmiszeripari Kutató Intézet, Budapest **GLOBUS Konzervgyár,
2.5.33. ÖSSZES FEHÉRJE
 2.5.33. Összes fehérje Ph.Hg.VIII. - Ph.Eur.6. 2.5.33. -1 2.5.33. ÖSSZES FEHÉRJE 01/2008:20533 javított 6.0 Az alábbi meghatározási módszerek között több olyan található, amely kereskedelemből beszerezhető
2.5.33. Összes fehérje Ph.Hg.VIII. - Ph.Eur.6. 2.5.33. -1 2.5.33. ÖSSZES FEHÉRJE 01/2008:20533 javított 6.0 Az alábbi meghatározási módszerek között több olyan található, amely kereskedelemből beszerezhető
1. feladat. Versenyző rajtszáma: Mely vegyületek aromásak az alábbiak közül?
 1. feladat / 5 pont Mely vegyületek aromásak az alábbiak közül? 2. feladat / 5 pont Egy C 4 H 8 O összegképletű vegyületről a következő 1 H és 13 C NMR spektrumok készültek. Állapítsa meg a vegyület szerkezetét!
1. feladat / 5 pont Mely vegyületek aromásak az alábbiak közül? 2. feladat / 5 pont Egy C 4 H 8 O összegképletű vegyületről a következő 1 H és 13 C NMR spektrumok készültek. Állapítsa meg a vegyület szerkezetét!
GYORS MÓDSZER A FŰSZERPAPRIKA ÖSSZES PIROS ÉS ÖSSZES SÁRGA FESTÉKMENNYISÉGÉNEK MEGHATÁROZÁSÁRA
 GYORS MÓDSZER A FŰSZERPAPRIKA ÖSSZES PIROS ÉS ÖSSZES SÁRGA FESTÉKMENNYISÉGÉNEK MEGHATÁROZÁSÁRA HALÁSZNÉ, FEKETE MÁRIA* A fűszerpaprika-őrlemények festéktartalmának meghatározására ismert módszerek a gyors
GYORS MÓDSZER A FŰSZERPAPRIKA ÖSSZES PIROS ÉS ÖSSZES SÁRGA FESTÉKMENNYISÉGÉNEK MEGHATÁROZÁSÁRA HALÁSZNÉ, FEKETE MÁRIA* A fűszerpaprika-őrlemények festéktartalmának meghatározására ismert módszerek a gyors
A tehéntej hamisításának (vizezésének) vizsgálata*
 A tehéntej hamisításának (vizezésének) vizsgálata* CSAK ALÄN, KOVÁCS LÁSZLÓ és KACSKOVICS MIKLÓS Megyei Élelmiszerellenőrző és Vegyvizsgáló Intézet, Pécs A tejipar számára meghatározó jelentőségű a felvásárolt
A tehéntej hamisításának (vizezésének) vizsgálata* CSAK ALÄN, KOVÁCS LÁSZLÓ és KACSKOVICS MIKLÓS Megyei Élelmiszerellenőrző és Vegyvizsgáló Intézet, Pécs A tejipar számára meghatározó jelentőségű a felvásárolt
A rosszindulatú daganatos halálozás változása 1975 és 2001 között Magyarországon
 A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
Automata titrátor H 2 O 2 & NaOCl mérésre klórmentesítő technológiában. On-line H 2 O 2 & NaOCl Elemző. Méréstartomány: 0 10% H 2 O % NaOCl
 Automata titrátor H 2 O 2 & NaOCl mérésre klórmentesítő technológiában On-line H 2 O 2 & NaOCl Elemző Méréstartomány: 0 10% H 2 O 2 0 10 % NaOCl Áttekintés 1.Alkalmazás 2.Elemzés áttekintése 3.Reagensek
Automata titrátor H 2 O 2 & NaOCl mérésre klórmentesítő technológiában On-line H 2 O 2 & NaOCl Elemző Méréstartomány: 0 10% H 2 O 2 0 10 % NaOCl Áttekintés 1.Alkalmazás 2.Elemzés áttekintése 3.Reagensek
1. Adatok kiértékelése. 2. A feltételek megvizsgálása. 3. A hipotézis megfogalmazása
 HIPOTÉZIS VIZSGÁLAT A hipotézis feltételezés egy vagy több populációról. (pl. egy gyógyszer az esetek 90%-ában hatásos; egy kezelés jelentősen megnöveli a rákos betegek túlélését). A hipotézis vizsgálat
HIPOTÉZIS VIZSGÁLAT A hipotézis feltételezés egy vagy több populációról. (pl. egy gyógyszer az esetek 90%-ában hatásos; egy kezelés jelentősen megnöveli a rákos betegek túlélését). A hipotézis vizsgálat
Kismennyiségű fehérjetartalom meghatározása borokban a biuret reakcióval megkötött réztartalom alapján
 Kismennyiségű fehérjetartalom meghatározása borokban a biuret reakcióval megkötött réztartalom alapján M O LN Á R ISTVÁN Szőlészeti és Borászati K u ta tó Intézet, Budapest Érkezett: 1981. november 4.
Kismennyiségű fehérjetartalom meghatározása borokban a biuret reakcióval megkötött réztartalom alapján M O LN Á R ISTVÁN Szőlészeti és Borászati K u ta tó Intézet, Budapest Érkezett: 1981. november 4.
Méz diasztázaktivitásának meghatározására szolgáló módszerek összehasonlítása. Nagy István, Kiss Írisz, Kovács Józsefné NÉBIH ÉLBC Kaposvári RÉL
 Méz diasztázaktivitásának meghatározására szolgáló módszerek összehasonlítása Nagy István, Kiss Írisz, Kovács Józsefné NÉBIH ÉLBC Kaposvári RÉL 1 A mézvizsgálatok céljai Minőségellenőrzés Botanikai eredet
Méz diasztázaktivitásának meghatározására szolgáló módszerek összehasonlítása Nagy István, Kiss Írisz, Kovács Józsefné NÉBIH ÉLBC Kaposvári RÉL 1 A mézvizsgálatok céljai Minőségellenőrzés Botanikai eredet
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Főzőpoharak. Desztillált víz. Vegyszeres kanál Üvegbot Analitikai mérleg Fűthető mágneses keverő
 KÉMIA TÉMAHÉT 2015 Előzetes feladatok A projekt napokat megelőzően két alkalommal ült össze hat fős csoportunk. Az első alkalommal (márc.02.) Likerné Pucsek Rózsa tanárnő kiosztotta az elkészítendő feladatokat.
KÉMIA TÉMAHÉT 2015 Előzetes feladatok A projekt napokat megelőzően két alkalommal ült össze hat fős csoportunk. Az első alkalommal (márc.02.) Likerné Pucsek Rózsa tanárnő kiosztotta az elkészítendő feladatokat.
A nád (Phragmites australis) vizsgálata enzimes bonthatóság és bioetanol termelés szempontjából. Dr. Kálmán Gergely
 A nád (Phragmites australis) vizsgálata enzimes bonthatóság és bioetanol termelés szempontjából Dr. Kálmán Gergely Bevezetés Az úgynevezett második generációs (lignocellulózokból előállított) bioetanol
A nád (Phragmites australis) vizsgálata enzimes bonthatóság és bioetanol termelés szempontjából Dr. Kálmán Gergely Bevezetés Az úgynevezett második generációs (lignocellulózokból előállított) bioetanol
9 gyak. Acél mangán tartalmának meghatározása UV-látható spektrofotometriás módszerrel
 9 gyak. Acél mangán tartalmának meghatározása UV-látható spektrofotometriás módszerrel A gyakorlat célja: Megismerkedni az UV-látható spektrofotometria elvével, alkalmazásával a kationok, anionok analízisére.
9 gyak. Acél mangán tartalmának meghatározása UV-látható spektrofotometriás módszerrel A gyakorlat célja: Megismerkedni az UV-látható spektrofotometria elvével, alkalmazásával a kationok, anionok analízisére.
1 A TEHÉN-, JUH-, KECSKETEJ ALKOTÓRÉSZEINEK ÖSSZEHASONLÍTÓ TÁPLÁLKOZÁSÉLETTANI MEGÍTÉLÉSE
 1 A TEHÉN-, JUH-, KECSKETEJ ALKOTÓRÉSZEINEK ÖSSZEHASONLÍTÓ TÁPLÁLKOZÁSÉLETTANI MEGÍTÉLÉSE FENYVESSY JÓZSEF - CSANÁDI JÓZSEF egyetemi tanár - főiskolai tanársegéd JATE Szegedi Felsőoktatási Szövetség Szegedi
1 A TEHÉN-, JUH-, KECSKETEJ ALKOTÓRÉSZEINEK ÖSSZEHASONLÍTÓ TÁPLÁLKOZÁSÉLETTANI MEGÍTÉLÉSE FENYVESSY JÓZSEF - CSANÁDI JÓZSEF egyetemi tanár - főiskolai tanársegéd JATE Szegedi Felsőoktatási Szövetség Szegedi
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
1.1. Reakciósebességet befolyásoló tényezők, a tioszulfát bomlása
 2. Laboratóriumi gyakorlat A laborgyakorlatok anyagát összeállította: dr. Pasinszki Tibor egyetemi tanár 1.1. Reakciósebességet befolyásoló tényezők, a tioszulfát bomlása A reakciósebesség növelhető a
2. Laboratóriumi gyakorlat A laborgyakorlatok anyagát összeállította: dr. Pasinszki Tibor egyetemi tanár 1.1. Reakciósebességet befolyásoló tényezők, a tioszulfát bomlása A reakciósebesség növelhető a
THEOPHYLLINUM. Teofillin
 Theophyllinum Ph.Hg.VIII. Ph.Eur.5.0-1 04/2005:0299 THEOPHYLLINUM Teofillin C 7 H 8 N 4 O 2 M r 180,2 DEFINÍCIÓ 1,3-dimetil-3,7-dihidro-1H-purin-2,6-dion. Tartalom: 99,0 101,0% (szárított anyagra). SAJÁTSÁGOK
Theophyllinum Ph.Hg.VIII. Ph.Eur.5.0-1 04/2005:0299 THEOPHYLLINUM Teofillin C 7 H 8 N 4 O 2 M r 180,2 DEFINÍCIÓ 1,3-dimetil-3,7-dihidro-1H-purin-2,6-dion. Tartalom: 99,0 101,0% (szárított anyagra). SAJÁTSÁGOK
Méréselmélet és mérőrendszerek 2. ELŐADÁS (1. RÉSZ)
 Méréselmélet és mérőrendszerek 2. ELŐADÁS (1. RÉSZ) KÉSZÍTETTE: DR. FÜVESI VIKTOR 2016. 10. Mai témáink o A hiba fogalma o Méréshatár és mérési tartomány M é r é s i h i b a o A hiba megadása o A hiba
Méréselmélet és mérőrendszerek 2. ELŐADÁS (1. RÉSZ) KÉSZÍTETTE: DR. FÜVESI VIKTOR 2016. 10. Mai témáink o A hiba fogalma o Méréshatár és mérési tartomány M é r é s i h i b a o A hiba megadása o A hiba
AZ ŐZHÚS ZSÍRSAVÖSSZETÉTELÉNEK ÖSSZEHASONLÍTÓ ÉRTÉKELÉSE
 Szent István Egyetem Állatorvos-tudományi kar Egzotikusállat és Vadegészségügyi Tanszék AZ ŐZHÚS ZSÍRSAVÖSSZETÉTELÉNEK ÖSSZEHASONLÍTÓ ÉRTÉKELÉSE Dr. Marosán Miklós és Dr. Tóth Tamás Budapest 2015. 03.
Szent István Egyetem Állatorvos-tudományi kar Egzotikusállat és Vadegészségügyi Tanszék AZ ŐZHÚS ZSÍRSAVÖSSZETÉTELÉNEK ÖSSZEHASONLÍTÓ ÉRTÉKELÉSE Dr. Marosán Miklós és Dr. Tóth Tamás Budapest 2015. 03.
V átlag = (V 1 + V 2 +V 3 )/3. A szórás V = ((V átlag -V 1 ) 2 + ((V átlag -V 2 ) 2 ((V átlag -V 3 ) 2 ) 0,5 / 3
 5. gyakorlat. Tömegmérés, térfogatmérés, pipettázás gyakorlása tömegméréssel kombinálva. A mérési eredmények megadása. Sóoldat sőrőségének meghatározása, koncentrációjának megadása a mért sőrőség alapján.
5. gyakorlat. Tömegmérés, térfogatmérés, pipettázás gyakorlása tömegméréssel kombinálva. A mérési eredmények megadása. Sóoldat sőrőségének meghatározása, koncentrációjának megadása a mért sőrőség alapján.
Általános Kémia GY, 2. tantermi gyakorlat
 Általános Kémia GY, 2. tantermi gyakorlat Sztöchiometriai számítások -titrálás: ld. : a 2. laborgyakorlat leírásánál Gáztörvények A kémhatás fogalma -ld.: a 2. laborgyakorlat leírásánál Honlap: http://harmatv.web.elte.hu
Általános Kémia GY, 2. tantermi gyakorlat Sztöchiometriai számítások -titrálás: ld. : a 2. laborgyakorlat leírásánál Gáztörvények A kémhatás fogalma -ld.: a 2. laborgyakorlat leírásánál Honlap: http://harmatv.web.elte.hu
Bevezetés a hipotézisvizsgálatokba
 Bevezetés a hipotézisvizsgálatokba Nullhipotézis: pl. az átlag egy adott µ becslése : M ( x -µ ) = 0 Alternatív hipotézis: : M ( x -µ ) 0 Szignifikancia: - teljes bizonyosság csak teljes enumerációra -
Bevezetés a hipotézisvizsgálatokba Nullhipotézis: pl. az átlag egy adott µ becslése : M ( x -µ ) = 0 Alternatív hipotézis: : M ( x -µ ) 0 Szignifikancia: - teljes bizonyosság csak teljes enumerációra -
Szójakészítménnyel gyártott húsipari termékek szójatartalmának meghatározása
 Szójakészítménnyel gyártott húsipari termékek szójatartalmának meghatározása SZABÓ EDITH Állategészségügyi és Élelm iszer Ellenőrző K özpont Érkezett: 1984. február 7. Egyes húsipari termékek gyártásában
Szójakészítménnyel gyártott húsipari termékek szójatartalmának meghatározása SZABÓ EDITH Állategészségügyi és Élelm iszer Ellenőrző K özpont Érkezett: 1984. február 7. Egyes húsipari termékek gyártásában
Cisztein-meghatározási módszerek tanulmányozása
 Cisztein-meghatározási módszerek tanulmányozása S Í M ÖNNÉ SARKADI LÍVIA és SZERZŐ ZSOLT B udapesti M űszaki Egyetem Biokémiai és Élelm iszertechnológiai Tanszék Érkezett: 1983. december 2. Az élelmiszerek
Cisztein-meghatározási módszerek tanulmányozása S Í M ÖNNÉ SARKADI LÍVIA és SZERZŐ ZSOLT B udapesti M űszaki Egyetem Biokémiai és Élelm iszertechnológiai Tanszék Érkezett: 1983. december 2. Az élelmiszerek
Kettőnél több csoport vizsgálata. Makara B. Gábor
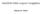 Kettőnél több csoport vizsgálata Makara B. Gábor Három gyógytápszer elemzéséből az alábbi energia tartalom adatok származtak (kilokalória/adag egységben) Három gyógytápszer elemzésébô A B C 30 5 00 10
Kettőnél több csoport vizsgálata Makara B. Gábor Három gyógytápszer elemzéséből az alábbi energia tartalom adatok származtak (kilokalória/adag egységben) Három gyógytápszer elemzésébô A B C 30 5 00 10
HEPARINA MASSAE MOLECULARIS MINORIS. Kis molekulatömegű heparinok
 01/2014:0828 HEPARINA MASSAE MOLECULARIS MINORIS Kis molekulatömegű heparinok DEFINÍCIÓ A kis molekulatömegű heparinok olyan, 8000-nél kisebb átlagos relatív molekulatömegű szulfatált glükózaminoglikánok
01/2014:0828 HEPARINA MASSAE MOLECULARIS MINORIS Kis molekulatömegű heparinok DEFINÍCIÓ A kis molekulatömegű heparinok olyan, 8000-nél kisebb átlagos relatív molekulatömegű szulfatált glükózaminoglikánok
Mangalica specifikus DNS alapú módszer kifejlesztés és validálása a MANGFOOD projekt keretében
 Mangalica specifikus DNS alapú módszer kifejlesztés és validálása a MANGFOOD projekt keretében Szántó-Egész Réka 1, Mohr Anita 1, Sipos Rita 1, Dallmann Klára 1, Ujhelyi Gabriella 2, Koppányné Szabó Erika
Mangalica specifikus DNS alapú módszer kifejlesztés és validálása a MANGFOOD projekt keretében Szántó-Egész Réka 1, Mohr Anita 1, Sipos Rita 1, Dallmann Klára 1, Ujhelyi Gabriella 2, Koppányné Szabó Erika
A vaj zsírmentes szárazanyag tartalmának meghatározásával kapcsolatos összehasonlító vizsgálatot
 A vaj zsírmentes szárazanyag tartalmának meghatározásával kapcsolatos összehasonlító vizsgálatot SZABÓ EDIT és CSÁK ALÁN MÉM ÉVK és M ÉVI Pécs** V alam int valam ennyi Élelm iszerellenőrző és V egyvizsgáló
A vaj zsírmentes szárazanyag tartalmának meghatározásával kapcsolatos összehasonlító vizsgálatot SZABÓ EDIT és CSÁK ALÁN MÉM ÉVK és M ÉVI Pécs** V alam int valam ennyi Élelm iszerellenőrző és V egyvizsgáló
Élelmiszeranalitikai körvizsgálatok III.
 Élelmiszeranalitikai körvizsgálatok III. Fűszerpaprika színezőanyag-tartalmának meghatározása SZABÓ EDITH és KÓSA KATALIN Állategészségügyi és Élelmiszerellenőrző Központ A fűszerpaprika mintát legjobban
Élelmiszeranalitikai körvizsgálatok III. Fűszerpaprika színezőanyag-tartalmának meghatározása SZABÓ EDITH és KÓSA KATALIN Állategészségügyi és Élelmiszerellenőrző Központ A fűszerpaprika mintát legjobban
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Méréselmélet és mérőrendszerek
 Méréselmélet és mérőrendszerek 6. ELŐADÁS KÉSZÍTETTE: DR. FÜVESI VIKTOR 2016. 10. Mai témáink o A hiba fogalma o Méréshatár és mérési tartomány M é r é s i h i b a o A hiba megadása o A hiba eredete o
Méréselmélet és mérőrendszerek 6. ELŐADÁS KÉSZÍTETTE: DR. FÜVESI VIKTOR 2016. 10. Mai témáink o A hiba fogalma o Méréshatár és mérési tartomány M é r é s i h i b a o A hiba megadása o A hiba eredete o
Geokémia gyakorlat. 1. Geokémiai adatok értelmezése: egyszerű statisztikai módszerek. Geológus szakirány (BSc) Dr. Lukács Réka
 Geokémia gyakorlat 1. Geokémiai adatok értelmezése: egyszerű statisztikai módszerek Geológus szakirány (BSc) Dr. Lukács Réka MTA-ELTE Vulkanológiai Kutatócsoport e-mail: reka.harangi@gmail.com ALAPFOGALMAK:
Geokémia gyakorlat 1. Geokémiai adatok értelmezése: egyszerű statisztikai módszerek Geológus szakirány (BSc) Dr. Lukács Réka MTA-ELTE Vulkanológiai Kutatócsoport e-mail: reka.harangi@gmail.com ALAPFOGALMAK:
Természetes vizek szennyezettségének vizsgálata
 A kísérlet, mérés megnevezése, célkitűzései: Természetes vizeink összetételének vizsgálata, összehasonlítása Vízben oldott szennyezőanyagok kimutatása Vízben oldott ionok kimutatása Eszközszükséglet: Szükséges
A kísérlet, mérés megnevezése, célkitűzései: Természetes vizeink összetételének vizsgálata, összehasonlítása Vízben oldott szennyezőanyagok kimutatása Vízben oldott ionok kimutatása Eszközszükséglet: Szükséges
2. Fogalom-meghatározás Erukasav-tartalom: az erukasav mennyisége a leírt módszer szerint meghatározva.
 4. melléklet a /2010. (..) VM rendelethez 33. melléklet a 152/2009. (XI. 12.) FVM rendelethez A Magyar Élelmiszerkönyv 3-1-80/891 számú előírása az étolaj, étkezési zsír, valamint ezek hozzáadásával készült
4. melléklet a /2010. (..) VM rendelethez 33. melléklet a 152/2009. (XI. 12.) FVM rendelethez A Magyar Élelmiszerkönyv 3-1-80/891 számú előírása az étolaj, étkezési zsír, valamint ezek hozzáadásával készült
6 Ionszelektív elektródok. elektródokat kiterjedten alkalmazzák a klinikai gyakorlatban: az automata analizátorokban
 6. Szelektivitási együttható meghatározása 6.1. Bevezetés Az ionszelektív elektródok olyan potenciometriás érzékelők, melyek valamely ion aktivitásának többé-kevésbé szelektív meghatározását teszik lehetővé.
6. Szelektivitási együttható meghatározása 6.1. Bevezetés Az ionszelektív elektródok olyan potenciometriás érzékelők, melyek valamely ion aktivitásának többé-kevésbé szelektív meghatározását teszik lehetővé.
SZABVÁNYMŰVELETI ELŐÍRÁS
 SEMMELWEIS EGYETEM Orvosi Biokémiai Intézet 1094 Budapest, Tű zoltó u. 37-47. SZABVÁNYMŰVELETI ELŐÍRÁS Készítette: 2009.02.04. A dokumentáció kódja: SE-OBI-OKT-MU- 05 Dr. Komorowicz Erzsébet adjunktus
SEMMELWEIS EGYETEM Orvosi Biokémiai Intézet 1094 Budapest, Tű zoltó u. 37-47. SZABVÁNYMŰVELETI ELŐÍRÁS Készítette: 2009.02.04. A dokumentáció kódja: SE-OBI-OKT-MU- 05 Dr. Komorowicz Erzsébet adjunktus
Abszorpciós fotometria
 abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
Hús és hústermék, mint funkcionális élelmiszer
 Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
ADALÉKOK A KÓ-LYUKI. KLIMATOLÓGIÁJÁHOZ RÁKOSI JÁNOS
 NME Közleményei, Miskolc, I. Sorozat, Bányászat, 33(1986) kötet, 1-4. füzet, 235-239. ADALÉKOK A KÓ-LYUKI. KLIMATOLÓGIÁJÁHOZ RÁKOSI JÁNOS Összefoglalás Megállapíthatjuk, a hőmérsékleti adatok alapján a
NME Közleményei, Miskolc, I. Sorozat, Bányászat, 33(1986) kötet, 1-4. füzet, 235-239. ADALÉKOK A KÓ-LYUKI. KLIMATOLÓGIÁJÁHOZ RÁKOSI JÁNOS Összefoglalás Megállapíthatjuk, a hőmérsékleti adatok alapján a
SZABADALMI IGÉNYPONTOK. képlettel rendelkezik:
 SZABADALMI IGÉNYPONTOK l. Izolált atorvasztatin epoxi dihidroxi (AED), amely az alábbi képlettel rendelkezik: 13 2. Az l. igénypont szerinti AED, amely az alábbiak közül választott adatokkal jellemezhető:
SZABADALMI IGÉNYPONTOK l. Izolált atorvasztatin epoxi dihidroxi (AED), amely az alábbi képlettel rendelkezik: 13 2. Az l. igénypont szerinti AED, amely az alábbiak közül választott adatokkal jellemezhető:
HÚS- ÉS HÚSKÉSZÍTMÉNYEK SZÉNHIDRÁT-, NITRÁT- ÉS FEHÉRJETARTALMÁNAK MEGHATÁROZÁSA SPEKTROSZKÓPIÁS ELJÁRÁSOKKAL^
 HÚS- ÉS HÚSKÉSZÍTMÉNYEK SZÉNHIDRÁT-, NITRÁT- ÉS FEHÉRJETARTALMÁNAK MEGHATÁROZÁSA SPEKTROSZKÓPIÁS ELJÁRÁSOKKAL^ CZEGLÉDI -JANKÓ GÉZÁNÉ ÉLIÁS Ш А -NAGY EDIT Országos Húsipari Kutatóintézet, Budapest A spektroszkópiás
HÚS- ÉS HÚSKÉSZÍTMÉNYEK SZÉNHIDRÁT-, NITRÁT- ÉS FEHÉRJETARTALMÁNAK MEGHATÁROZÁSA SPEKTROSZKÓPIÁS ELJÁRÁSOKKAL^ CZEGLÉDI -JANKÓ GÉZÁNÉ ÉLIÁS Ш А -NAGY EDIT Országos Húsipari Kutatóintézet, Budapest A spektroszkópiás
Mérési hibák 2006.10.04. 1
 Mérési hibák 2006.10.04. 1 Mérés jel- és rendszerelméleti modellje Mérési hibák_labor/2 Mérési hibák mérési hiba: a meghatározandó értékre a mérés során kapott eredmény és ideális értéke közötti különbség
Mérési hibák 2006.10.04. 1 Mérés jel- és rendszerelméleti modellje Mérési hibák_labor/2 Mérési hibák mérési hiba: a meghatározandó értékre a mérés során kapott eredmény és ideális értéke közötti különbség
Curie Kémia Emlékverseny 9. évfolyam III. forduló 2018/2019.
 A feladatokat írta: Név: Pócsiné Erdei Irén, Debrecen... Lektorálta: Iskola: Kálnay Istvánné, Nyíregyháza... Beküldési határidő: 2019. január 07. Curie Kémia Emlékverseny 9. évfolyam III. forduló 2018/2019.
A feladatokat írta: Név: Pócsiné Erdei Irén, Debrecen... Lektorálta: Iskola: Kálnay Istvánné, Nyíregyháza... Beküldési határidő: 2019. január 07. Curie Kémia Emlékverseny 9. évfolyam III. forduló 2018/2019.
HORVÁTHJÁNOS s AVASÉRCEKDÚSÍTÁSÁBAN ELÉRTEREDMÉNYEINK. Krivojvrogi vörösv
 erős AVASÉRCEKDÚSÍTÁSÁBAN ELÉRTEREDMÉNYEINK HORVÁTHJÁNOS s ZIPSZER KONRÁD A dolgozat részletesen foglalkozik a Krivojvrogi vörösv vasérc dúsítási technológiájának kialakításával, figyelembe véve a dúsítandó
erős AVASÉRCEKDÚSÍTÁSÁBAN ELÉRTEREDMÉNYEINK HORVÁTHJÁNOS s ZIPSZER KONRÁD A dolgozat részletesen foglalkozik a Krivojvrogi vörösv vasérc dúsítási technológiájának kialakításával, figyelembe véve a dúsítandó
É ú É ö ö ű ö ö ö ú ú ú ű ű ú ö ű ö ű ű ü ö ö ü ű ö ü ö ö ö ö ú ü ö ö ö ú ö ö ú ö ö ú ü ú ú ú ű ü ö ö ű ú ű ű ü ö ű ö ö ö ű ú ö ö ü ú ü ö ö ö ü ú ö ű
 É É É Ó Á É ú É ö ö ű ö ö ö ú ú ú ű ű ú ö ű ö ű ű ü ö ö ü ű ö ü ö ö ö ö ú ü ö ö ö ú ö ö ú ö ö ú ü ú ú ú ű ü ö ö ű ú ű ű ü ö ű ö ö ö ű ú ö ö ü ú ü ö ö ö ü ú ö ű ü ű ö ö ú ö ú ö ö ö ö ö ü ú ü ö ö ö ö ö ü
É É É Ó Á É ú É ö ö ű ö ö ö ú ú ú ű ű ú ö ű ö ű ű ü ö ö ü ű ö ü ö ö ö ö ú ü ö ö ö ú ö ö ú ö ö ú ü ú ú ú ű ü ö ö ű ú ű ű ü ö ű ö ö ö ű ú ö ö ü ú ü ö ö ö ü ú ö ű ü ű ö ö ú ö ú ö ö ö ö ö ü ú ü ö ö ö ö ö ü
A hús szöveti összetétele és minősége közötti összefüggések (II) *
 A hús szöveti összetétele és minősége közötti összefüggések (II) * S Z E R E D Y I D A K o n z e r v -, H ú s - é s H ű t ő i p a r i K u t a t ó I n t é z e t, B u d a p e s t Érkezeit: 1957. július 3.
A hús szöveti összetétele és minősége közötti összefüggések (II) * S Z E R E D Y I D A K o n z e r v -, H ú s - é s H ű t ő i p a r i K u t a t ó I n t é z e t, B u d a p e s t Érkezeit: 1957. július 3.







