Tartalomjegyzék FOCUS MEDICINAE
|
|
|
- Léna Nagy
- 8 évvel ezelőtt
- Látták:
Átírás
1 FOCUS MEDICINAE Felelõs szerkesztõ: Dr. Szolnoky Miklós Fõszerkesztõ: Dr. Karabélyos Csaba Szerkesztõbizottság: Dr. Bencsik Krisztina Prof. Czirják László Prof. Horváth Örs Péter Dr. Kalmár Ágnes Dr. Mátrai Zoltán Dr. Nemes László Dr. Paál Mária Dr. Pál Katalin Prof. Zeher Margit Szerkesztõbizottság tanácsadó testülete: Prof. Fekete György Prof. Kiss Attila Prof. Kiss István Prof. Komoly Sámuel Prof. Lipták József Prof. Mándi Yvette Prof. Maródi László Prof. Medgyesi György Dr. Mészner Zsófia Dr. M. Tóth Antal Dr. Nagy Kálmán Prof. Pálóczi Katalin Prof. Perner Ferenc Prof. Pénzes István Prof. Péter Ferenc Prof. Romics Imre Prof. Rozgonyi Ferenc Prof. Sas Géza Prof. Schuler Dezsõ Dr. Siklós Pál Prof. Szegedi Gyula Dr. Szita János Prof. Tekeres Miklós Prof. Tímár László Dr. Trestyánszky Zoltán Prof. Tulassay Tivadar Alapító: Biotest Hungaria Kft. Kiadja és a nyomdai munkáért felelõs: Dursusz Bt. Szerkesztõség és levelezési cím: 2045 Törökbálint, Torbágy u. 15/A ISSN: Megjelenik: évente négyszer Elõfizetési díj: évre 2011,- Ft + 5% áfa Tartalomjegyzék Focus Medicinae Bevezetés 126 éves a Tûzoltó utcai Gyermekklinika, a volt Fehér Kereszt Gyermekkórház 2 /Introduction The Pediatric Clinic earlier White Cross Children Hospital in the Tûzoltó street is 126 years old/ Prof. Szabó András A szisztémás autoimmun betegségek gyermekkori jellegzetességei 4 /Childhood characteristics of systemic autoimmune diseases/ Dr. Dérfalvi Beáta Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban 9 /Importance of new cytogenetic analyses in childhood leukemias/ Dr. Haltrich Irén, Prof. Fekete György A gyermekonkológiai kezelések aktuális problémái: terápia, szupportáció 19 /The actual problems of pediatric oncology: therapy, supportation/ Dr. Garami Miklós A gyermekkori ITP korszerû kezelése 25 /The modern therapy of childhood ITP/ Dr. Kovács Gábor, Dr. Csóka Monika Az antimüllercsõ hormon (AMH) jelentõsége és szerepe, esetleges gyermek-endokrinológiai lehetõségek 29 /The role and importance of the anti-müllerian hormone (AMH), the potential use in pediatric endocrinology/ Dr. Luczay Andrea MEGEMLÉKEZÉS Prof. Kálmánchey Rozália 32 /In memoriam Rozália Kálmánchey/ 1
2 FOCUS MEDICINAE Interdiszciplináris tudományos folyóirat Focus Medicinae Tisztelt Olvasó! A Focus Medicinae jelen száma a Semmelweis Egyetem II. sz. Gyermekgyógyászati Klinikájának munkásságát mutatja be. Bevezetésként egy rövid történeti áttekintést olvashatnak intézetünkrõl, amelyet a tudományos publikációk követnek. 126 éves a Tûzoltó utcai Gyermekklinika, a volt Fehér Kereszt Gyermekkórház A Fehér Kereszt Gyermekkórház Dr. Szalárdy Mór ( ) kezdeményezése nyomán, az júniusában létrejött Szegény Beteg Gyermek Egyesület céljainak teljesítésére jött létre. Az intézmény létrehozása a hazai gyermekvédelem és gyermekegészségügy fontos eseménye volt. Az intézmény igazgatóinak, orvosainak és ápoló nõvéreinek elkötelezettsége, hivatástudata, kiemelkedõ szakmai tevékenysége révén itt indult el hazánkban elõször a modern csecsemõ- és gyermekgyógyászat több szakterületének mûvelése. Az 1946 óta egyetemi gyermekklinikaként mûködõ intézményben létesült elõször gyermekkardiológiai- és szívsebészeti osztály, citogenetikai diagnosztika, gyermek onkológia és hematológia, és itt vette kezdetét több gyermekkori anyagcsere betegség molekuláris genetikai vizsgálata. Mint a Semmelweis Egyetem II. sz. Gyermekgyógyászati Klinikája jelenleg több szakterület országos központjának számít. Dr. Berend Miklós egyetemi magántanár között vezette a Fehér Kereszt Gyermekkórházat, majd a Pozsonyból Budapestre került egyetemi gyermekklinika igazgatójaként és a kórházat mûködtetõ egyesület elnökeként Dr. Heim Pál professzor szerzett hírnevet az intézménynek. Dr. Petényi Géza professzor 1937-tõl volt az intézmény igazgatója, majd 1946-tól haláláig, 1965-ig a II. sz. Gyermekklinika elsõ tanszékvezetõ egyetemi tanára. Iskolateremtõ egyénisége, szellemi és erkölcsi példamutatása meghatározóak voltak több évtized orvos- és gyermekgyógyász nemzedéke számára. A kitûnõ csecsemõ- és gyermekgyógyász Dr. Lóránt Imre egyetemi docens rövid igazgatói mûködése után Dr. Kerpel-Fronius Ödön professzor, akadémikus 1967 és 1976 között, 10 éven át vezette a Klinikát. A csecsemõkori sorvadás, a folyadék-és elektrolit háztartás zavarainak nemzetközileg is méltán kiemelkedõ elismertséget szerzett tudósaként új, színvonalas kutatásokat támogatott a Klinikán, és vezetésével jött létre az Országos Csecsemõ- és Gyermekegészségügyi Intézet. Dr. Schuler Dezsõ professzor 18 éven át, között irányította a Klinikát. Létrehozta az elsõ hazai cytogenetikai laboratóriumot, a gyermekkori leukémiás és daganatos betegek korszerû diagnosztikáját és kezelését megvalósító országos hálózatot, a leukémiában és rosszindulatú daganatos betegségekben szenvedõ gyermekek magyarországi regiszterét. Az Országos Csecsemõ- és Gyermekegészségügyi Intézet fõigazgatójaként számos szervezeti újítás mellett kiemelt szerepe volt a csecsemõhalálozás csökkentésében. Dr. Fekete György professzor, aki 1994-tõl 2009-ig, 15 éven át vezette a nagy múltú intézményt, az egyik elsõ hazai molekuláris genetikai diagnosztikai és tudományos kutatásokat végzõ laboratóriumot hozta létre. Jelentõs fejlesztésekkel segítette a betegellátás, a bõvülõ magyar és idegen nyelvû orvos,- fogorvosképzés, a szakorvos képzés és továbbképzés, valamint a tudományos kutatás klinikai feltételeit. Dr. Szabó András professzor július 1-tõl kapott megbízást a II. sz. Gyermekklinika vezetésére. Eddig több sikeres PhD védés és habilitációs eljárás, a betegellátás nehéz körülmények között is kiváló eredményei jelzik, hogy irányításával a Klinikának sikerült megõriznie a Semmelweis Egyetem vezetõ klinikái közötti helyét. A II. sz. Gyermekklinika 2010-ben 134 ágyon, 11 fekvõbeteg osztályon és nagyszámú, jelentõs betegforgalmú ambulancián folytatta gyógyító munkáját. Évi mintegy 9000 fekvõ és több mint járó beteg ellátását végezzük. A tartós klinikai kezelést igénylõ gyermekek, szüleikkel együtt korszerû, komfortos kórtermekben tartózkodnak. Az elmúlt évekhez hasonlóan folyamatos felújítások teszik lehetõvé, hogy a hazai betegellátó intézetek átlagához képest lényegesen jobb körülmények között tudjuk fogadni betegeinket. A gazdasági helyzet és az egészségügy súlyos helyzete ellenére eddig úgy sikerült megtartani a magas szakmai színvonalat és a stabil orvosi és ápolói gárdát, hogy dolgozóink áldozatos munkájukkal elsõdleges feladatuknak tekintik a beteg csecsemõk és gyermekek gyógyítását, az orvosképzést és a múlt nemes példáit követõ tudományos kutatást. 2
3 2011. XIII. évfolyam 1. szám Focus Medicinae Hálával tartozunk valamennyiüknek, és mindazoknak az alapítványoknak, áldozatkész magánszemélyeknek, valamint az elmúlt húsz év során Klinikánkat látogatásukkal megtisztelõ neves személyiségeknek, akik támogatták és elismerték tevékenységünket. Prof. Szabó András ÚTMUTATÓ SZERZÕINKNEK: A folyóiratban eredeti és áttekintõ jellegû közleményeket, valamint folyóiratreferátumokat jelentetünk meg. A kézirattal kapcsolatos formai követelmények (eredeti és áttekintõ /review/ jellegû közlemények) a következõk: A kézirat sorrendje: magyar nyelvû cím, szerzõvel, intézettel együtt magyar nyelvû absztrakt magyar kulcsszavak angol nyelvû absztrakt angol kulcsszavak szöveg (csak magyarul) irodalomjegyzék (max. 30) táblázat(ok) ábrá(k), ábrajegyzék Cím: a szerzõk a munkahelyük megjelölésével szerepeljenek a közlemény címét követõen. Absztrakt: maximálisan 1 oldal terjedelmû legyen, az absztraktok esetén bekezdéseket ne használjunk, folyamatosan történjen a gépelés. Kulcsszavak: 5-10 jellemzõ kulcsszót emeljünk ki a szöveg elé, mindkét nyelven. Szöveg: (az itt felsorolt követelmények természetesen az absztraktra is vonatkoznak) 1 oldal: sor 1 sor: 70 leütés Betûtípus: Arial, normál 12-es méretû, (a szöveg, amennyiben lehetséges Windows XP vagy újabb változatban készüljön). Maximális oldalszám: 10 (esetenként ettõl eltérés lehet a szerkesztõbizottság döntése alapján), kívánt oldalszám: 6-8 oldal (A/4). Helyesírás: ahol lehet, magyar kifejezéseket és magyaros írásmódot használjunk. Irodalomjegyzék: a hivatkozások száma ne haladja meg a 30-at, a szövegben az adott bekezdés végén levõ, dõlt, zárójelbe tett szám jelezze a citált publikációt, az irodalomjegyzék elsõ szerzõ szerinti ABC-rendben készüljön. Formai kérések: 1. Szerzõk megjelölése dõlt betûvel (elõl családnév, utána keresztnév elsõ betûje ponttal zárva. 3-nál több szerzõ esetén az elsõ három szerzõ után et al.: álljon. 2. A cikk teljes címe 3. A folyóirat hivatalos rövidítése (pl. N. Engl.J.Med.), kötetszáma és oldalszáma, majd legvégül az évszám (pl. 73(1), , 1986) Táblázat(ok): a táblázatok Windows XP vagy újabb verzióval készüljenek, és legyenek címmel ellátva. Ábrá(k): színes ábrákat és fotókat nem áll módunkban leközölni, az esetleges színes ábrák fekete-fehér kópiában jelennek meg. Folyóiratreferátumok: Ezek esetében csak a referáló nevét és a forrást kell feltüntetni, (felül magyarra fordított cím, alatta a forrás pontos adatai, alul a referáló neve). A folyóirat-referátum a két gépelt oldal terjedelmet ne haladja meg, az elõbbiekben valamint az eredeti közleményeknél említett követelmények megtartása mellett. Kérjük a szerzõket, hogy a cikkeket -en adják le szerkesztõségünknek, és amennyiben mód van rá, kinyomtatott formában is juttassák el azt a Biotest Hungaria Kft. irodájába. Cím: 2045 Törökbálint, Torbágy u. 15/A biotest@biotest.hu vagy karabelyos.csaba@biotest.hu 3
4 A szisztémás autoimmun betegségek gyermekkori jellegzetességei Dr. Dérfalvi Beáta Semmelweis Egyetem, II. sz. Gyermekgyógyászati Klinika, Budapest A szisztémás autoimmun betegségek gyermekkori jellegzetességei Összefoglalás: A szerzõ irodalmi áttekintés keretében hangsúlyozza a gyermekkori szisztémás autoimmun betegségek jellegzetességeit a felnõttkori formákhoz viszonyítva. A gyermekkori szisztémás autoimmun kórképek közé tartoznak a juvenilis SLE, az újszülöttkori lupus, a juvenilis dermatomyositis, scleroderma (morphea, linearis scleroderma, szisztémás sclerosis), kevert kötõszöveti betegség és a vasculitisek. Összességében elmondható, hogy ezekkel a betegségekkel ritkábban találkozunk, mint felnõttkorban. Tüneteik rendkívül változatosak. Gyakran lappangva, csak általános tünetekkel indulnak, rossz közérzet, fogyás, fejlõdésben visszamaradás, hõemelkedés, fokozott infekció hajlam képében. A diagnózis felállítását segítõ, gyermekekre vonatkoztatott PRES/PRINTO által javasolt besorolási kritériumrendszer a vasculitisek, a juvenilis dermatomyositis és juvenilis szisztémás sclerosis esetében használatosak, az SLE esetében a felnõttkori kritériumrendszer az irányadó. A Kawasaki szindróma és a neonatalis lupus kizárólagosan gyermekkori betegségek. A gyermekkori kórképeket a krónikus lefolyás és eltérõ, gyakran kedvezõtlen prognózis jellemzi. A kezelésnél jelentõs gondot jelent, hogy számos immunszuppresszív gyógyszer illetve a biológiai terápiák csak off-label indikációban alkalmazhatók gyermekkorban. A tartósan aktív betegség következtében a betegek jelentõs szervkárosodással illetve kumulatív gyógyszertoxicitással léphetnek át a felnõttkorba. A hosszantartó gyermek-immunológiai, -reumatológiai követés után átmenetileg szoros együttmûködés szükséges a felnõtteket gondozó orvosokkal. Kulcsszavak: juvenilis SLE, juvenilis dermatomyositis, linearis scleroderma, Kawasaki-szindróma, Schönlein-Henoch purpura Bevezetés Summary: The author gives a literature overview about the characteristic differences of the pediatric systemic autoimmune diseases compared with their adult forms. The pediatric systemic autoimmune diesases are the juvenile SLE, neonatal lupus, juvenile dermatomyositis, scleroderma (morphea, linear scleroderma and systemic sclerosis), mixed connective tissue disease and vasculitides. The prevalence of these diseases are lower than in adulthood. Their symptomes are very colourful. Usually the onset is insidious with general symptomes, like malaise, loss of weight, developmental delay, lowgrade temperature, increased frequency of infections. There are verifyed or provisional pediatric classification criterias, suggested by PRES/PRINTO in the vasculitides, in juvenile systemic sclerosis and juvenile dermatomyositis. The neonatal lupus and the Kawasaki syndromes are exclusively pediatric diseases. The pediatric systemic autoimmune disesaes usually show chronic course and rather unfavourable prognosis. Unfortunately in the treatment there are several immunosuppresives and biological therapies we can use only in off-label indication. Because of the organ damage due to the longlasting active chronic disease not rarely the adolescent patients enter the adulthood with remarkable organ damage or cumulative drog toxicity. There is a need for the strong cooperation with the adult immunologist/rheumatologist during the transition to the adult care of these patients. Key words: juvenile SLE, juvenile dermatomyositis, linear scleroderma, Kawasaki-syndrome, Henoch-Schonlein purpura Jelen publikációban a szisztémás autoimmun betegségek és vasculitisek gyermekkori jellegzetességeit emeljük ki. A felnõttkori kórképekkel megegyezõ patofiziológiai, klinikai és laboratóriumi jellemzõket nem részletezzük. Pontos epidemiológiai adatok nem állnak rendelkezésre, a prevalenciát csak becsülni tudjuk. Az alacsony prevalencia, így a vizsgálatokba beválasztható csekély betegszám miatt multicentrikus elemzésekre van szükség. A PRES (Pediatric Rheumatology European Society) és PRINTO (Pediatric Rheumatology Trial Organisation) által támogatott, általánosan elfogadott, gyermekekre vonatkoztatott klasszifikációs kritériumokat tettek közre a vasculitisek, a juvenilis dermatomyositis és a juvenilis szisztémás sclerosis tekintetében. A felnõttkori ACR kritériumok csak juvenilis SLE-re vannak validálva. A gyermekkori kórképeket a krónikus lefolyás és eltérõ, gyakran kedvezõtlen prognózis jellemzi. A kezelésnél jelentõs gondot jelent, hogy számos immunszuppresszív gyógyszer illetve a biológiai terápiák csak off-label indikációban alkalmazhatók gyermekkorban. A tartósan aktív betegség következtében a betegek jelentõs szervkárosodással illetve kumulatív gyógyszertoxicitással léphetnek át a felnõttkorba. A hosszantartó gyermek-immunológiai követés után átmenetileg szoros együttmûködés szükséges a felnõtteket gondozó orvosokkal. Szisztémás lupus erythematosus Az SLE prevalenciája a 18 év alatti fehér populációban 5-10/ gyermek. Az SLE egyötöde indul gyermekkorban. Serdülõkor elõtt a lány/fiú arány: 4-5:1 (felnõttkorban 8-10:1). A változatos klinikai tünetek mellett az ACR kritériumrendszere segít a betegség diagnózisának felállításában, mely gyermekkorban 96%- ban szenzitív és 100%-ban specifikus (10). 4
5 A juvenilis SLE 1/3-a atípusos tünetekkel indul, gyakori a gastrointestinalis érintettség, és általánosságban igaz, hogy korral fordítottan arányosan súlyosabb tünetekkel jelentkezik. Veseérintettség és idegrendszeri tünetek gyakoribbak, fokozott a szteroid és immunszuppresszív gyógyszer igény. Arthritis, cardiopulmonalis érintettség a felnõttekben gyakoribb. Antifoszfolipid szindróma közel egyenlõ arányban jelentkezik, az immunprofil hasonló. Discoid lupus gyermekkorban szinte nem fordul elõ (1,21,22). A juvenilis SLE súlyosabb lefolyású, mint a felnõttkori. A betegség aktívabb, a szervi érintettség kiterjedtebb, súlyosabb (magasabb SLEDAI pontszám), a betegség okozta egészségkárosodás korábban jelentkezik, a károsodási index (SLICC pontszám) magasabb. Összességében tehát nagyobb terhet ró a fiatalkorban induló betegség az érintettekre. Az általában agresszívebb lefolyás oka ismeretlen; esetleg hormonális tényezõk, az immunrendszer éretlenségébõl eredõ szabályozási zavar illetve fokozott infekcióhajlam magyarázhatja. A komplement deficiens SLE-sek tünetei is korábban indulnak és gyakoribbak az infekcióik (8,9,14,21,22). Az életkor adta gondozásbeli különbségek a növekedési elmaradás, korai gonádelégtelenség, pszichoszociális fejlõdési zavar, adherencia problémákból adódnak. Kifejezetten nehéz a lázadó adolescensek terápiás vezetése, amennyire csak lehet, az ambuláns ellátást részesítjük elõnyben. A felnõttkorba lépve az átvevõ gondozó orvosnak a hosszú betegség lefolyás következtében a korai atherosclerosis (hypertensio, cardiovascularis szövõdmények), a szteroid kezelés, illetve inaktivitás okozta osteoporosis jelenthet nehéz feladatot az alapbetegség tüneti kezelése mellett. A 10 éves túlélésben nincs különbség, az a juvenilis SLE esetében is 90% feletti (4,5,6,26). Neonatalis lupus Újszülöttek, kiscsecsemõk ritka, szerzett, átmeneti autoimmun betegsége a transplacentaris anyai immunglobulinoknak (IgG) köszönhetõ. SLE-ben, Sjögren szindrómában, vagy kevert kötõszöveti betegségben (MCTD) szenvedõ, de gyakran teljesen tünetmentes (!) anyák SS-A, SS-B antitestjei a gyermekben a következõ tüneteket okozzák: A szisztémás autoimmun betegségek gyermekkori jellegzetességei erythema annulare cytopeniák (anaemia, thrombocytopenia, neutropenia) hepatitis arrhythmia, congenitalis szívblokk A bõrtünetek, a cytopeniák és a májérintettség nem igényelnek kezelést; az anyai antitestek lebomlása után, a 4-6. hónap körül megszûnnek. A congenitalis szívblokk az ismerten SS-A/SS-B pozitív anyák újszülöttjeinél 2%- ban fordul elõ. A betegség halálozása magas, ezért gondos perinatalis követés és születés után azonnal élethosszig pacemaker beültetés szükséges (5)! Juvenilis dermatomyositis Ismeretlen eredetû krónikus autoimmun multiszisztémás vasculopathia. A juvenilis dermatomyositis klinikailag abban tér el a felnõttkori dermatomyositistõl, hogy inkább szisztémás vasculopathiaként viselkedik, mely a bõr és az izmok mellett súlyosabb formában a beleket is érinti. Gyermekkorban nem társul malignus betegségekkel. Gyakran átfedõ szindróma része, egyéb autoimmun kötõszöveti betegségek mellett. A betegség ritka, incidenciája 1-7/ gyermek, általában 4-10 éves kor között indul. Megkülönböztetjük az általában monociklikus klasszikus, az amyopathiás és a vasculopathiás formát. Gyermekkorban nagyon ritka a bõrtünet nélküli, polymyositises beteg, akik gyakran krónikus, terápia rezisztens lefolyást mutatnak. Az akár bélperforációval, pulmonalis vasculitissel, bõrfekélyekkel járó legsúlyosabb vasculopathiás forma sürgõsségi ellátást igényelhet. Ezekben az esetekben a dysphonia, dysphagia, reflux, légzési elégtelenség, carditis is jelzik a zsigeri érintettséget. A lypodystrophia, calcinosis kifejezetten rossz prognosztikai jel, krónikus lefolyást jelez elõre, relapsusokkal (7,17). Korábban a Bohan és Peters kritériumokra támaszkodtunk a diagnózis felállításánál, újabban a Rider és Targoff kritériumrendszer az irányadó (3,25)(1. táblázat). Típusos esetben egyre kevesebb centrumban végeznek invazív EMG, vagy izombiopsziás beavatkozást, inkább a T2 súlyozott képeken látott izom oedema által jelzett gyulladásra támaszkodunk (18). Az izomenzimek nem mindig jelzik megbízhatóan az izomérintettség mértékét. A gyulladásos laborparaméterek inkább csak a vasculopathiás Kritérium Bohan és Peters Rider és Targoff 1 Tipikus bõrtünet ( heliotrope rash = szemhéjak livid Igazolt jdm: 1+3 másik Igazolt jdm: 1+3 másik elszínezõdése, Gottron-papulák a feszítõ felszínek felett) teljesül a 2-5 közül teljesül a 2-6 közül 2 Szimmetrikus proximalis izomgyengeség Valószínû: 1+2 másik Valószínû: 1+2 másik 3 Izomenzim emelkedés (CPK, LDH, GOT, GPT, aldoláz) teljesül a 2-5 közül teljesül a 2-6 közül 4 Jellemzõ EMG elváltozások (polifázisos csökkent amplitúdó, Egyenlõ súllyal beleveszi a pozitív hegyes hullámok, spontán és kiváltott, magas frekvenciájú myositis specifikus antitesteket is ismétlõdõ kisülések) 5 Jellemzõ elváltozások izombiopsziás mintán (perifascicularis Pozitív MRI lelet kiváltja a 2., degeneráció / regeneráció, necrosis, phagocytosis, interstitialis vagy 3. kritériumot mononuclearis sejt infiltráció) 6 Myositis-specifikus antitestek (anti-szintetáz, Mi2, SRP) 1. táblázat: A juvenilis dermatomyositis diagnosztikai kritériumai 5
6 alcsoportban emelkednek. ANA 50%-ban pozitív. A Mi-2 antitest pozitívak jól, az SRP antitest pozitívak rosszul reagálnak a kezelésre, a Jo-1 autoantitest pozitvitás a felnõttkori dermatomyositisre jellemzõ. Gyermekkorban a PRINTO kezdeményezésére a betegség aktivitására, károsodás mértékére validált kritériumrendszer létezik (15,23). Leggyakrabban iv. bolus methylprednisolon kezelést alkalmazunk remisszió indukcióra, majd a tartós kisebb dózisú oralis szteroid kezelést MTX, illetve cyclosporin A kezeléssel egészítjük ki/váltjuk fel. Súlyos esetekben IVIg (intravénás immunglobulin) terápia, iv. cyclophosphamid, esetleg TNFα-gátló, rituximab, illetve autolog õssejt átültetés jöhet szóba. Fizioterápia elengedhetetlen. A jdm általában évek múlva kiég (17). Scleroderma Felosztás szerint megkülönböztetünk lokalizált és szisztémás formákat. A juvenilis lokalizált scleroderma becsült incidenciája 1/ , ez a forma 10-szer gyakoribb, mint a szisztémás megjelenés, és általában nem megy át szisztémás formába. A felnõttektõl eltérõen gyermekkorban bizonyos lokalizált formák sokkal gyakoribbak; ebbe a csoportba tartozik a linearis scleroderma (50-70%), a fejen megjelenõ en-coup-de sabre forma és a ritka Parry-Romberg féle hemiatrophia. A morphea elõfordulása a gyermekkori lokalizált sclerodermák között 10-20%, ez a típus felnõttkorban sem ritka. A korábban jóindulatúnak tartott lokalizált scleroderma 25%-ánál lehet extracutan manifesztációra számítani. Leggyakoraibb extracutan tünet az ízületi gyulladás, kontraktúra linearis scleroderma esetében akár 50%- ban jelentkezhet, mely a betegek negyedénél a sclerodermás bõrterülettõl távol helyezkedik el! Az en-coupde sabre formánál fontos a szemészeti kivizsgálás episcleritis, uveitis lehetõsége, neurológiai kivizsgálás (MRI, EEG) központi idegrendszeri érintettség (vasculitis, ér-malformáció, fejfájás, eclampsia) miatt. Bár a localis scleroderma zsigeri szerveket nem érint, nem életet veszélyeztetõ betegség, mégis súlyos esztétikai zavar, ízületi kontraktúra, helyi-, illetve végtag növekedési zavar, deformitás esetén a lokális szteroid tartalmú kenõcsök mellett szisztémás immunszuppresszív vagy citosztatikus kezelés (általában methotrexat, esetleg methylprednisolon) is szükséges lehet. A felnõttkorban kiterjedten alkalmazott fototerápia (UVA/PUVA) gyermek betegnél csak kivételesen jön szóba. Fontos a rendszeres gyógytorna is a kontraktúrák csökkentésére. A lokális scleroderma prognózisa jó, a betegség aktivitása 3-5 év alatt megszûnik, a laesiok atrophiával gyógyulnak (2,28). A juvenilis szisztémás sclerosis (jssc) nagyon ritka betegség, prevalenciája 1/ gyermek. A szisztémás sclerosis az esetek 10%-ában kezdõdik 16 éves kor elõtt és újabb adatok szerint akár 50%-ban 10 éves kor elõtt indul. A PRES a tüneteket major és minor tünetcsoportokba sorolta (2. táblázat). A juvenilis klasszifikációs rendszer elõnye a felnõttkori besorolási kritériumokhoz képest, hogy a belsõ szervi érintettségnél a tüdõfibrosis mellett egyéb szerveket is figyelembe vesz (29). A szisztémás autoimmun betegségek gyermekkori jellegzetességei Major tünetek 1. sclerosis/induratio 2. sclerodactylia 3. Raynaud-jelenség Felnõttekben a betegség kezdetén gyakoribb az anti-topoizomeráz (SCL-70) antitest jelenléte, és a lefolyás során gyakoribb a Raynaud-tünet, tüdõfibrózis, szívelégtelenség, oesophagus érintettség, vesekrízis. Felnõtteknél a scleroderma malignitáshoz is társulhat. Gyermekkorban inkább az arthritis gyakoribb. A jssc progresszív, gyakran letális kimenetelû megbetegedés de a mortalitása alacsonyabb, mint felnõttkorban. Multicentrikus adatelemzések szerint a jssc prognózisa lényegesen kedvezõbb, mint a felnõttkori megbetegedésé: az 5 éves túlélés 90-95% (felnõttekben 67-78%). Ebben több tényezõ is szerepet játszik: a gyermekek jobb általános egészségi állapota, a komorbiditások hiánya, az immunszuppresszív kezelések kevesebb szövõdménye, és a megbetegedés kevésbé súlyos szervérintettséggel történõ zajlása (11,12,29). Kevert kötõszöveti betegség (mixed connective tissue disease MCTD) Ritka kórkép, általában a 6 évesnél idõsebb lányokat érinti. A klinikai tünetek között láz, lymphadenopathia, hepatosplenomegalia, arthritis, myositis, Raynaud-jelenség, sclerodermára-, SLE-re vagy juvenilis dermatomyositisre jellemzõ bõrtünetek, nyelõcsõ dysmotilitás, vese-, tüdõ- és szív-érintettség, parotis duzzanat és thrombocytopenia szerepelnek. Átfedõ (overlap) szindrómaként is felfogható, amely több szisztémás autoimmun betegség (SLE, juvenilis idiopathiás arthritis, jdm, SSc, Sjögren) jellemzõit foglalja magába. Immunszerológiai jellemzõje a magas titerû anti-rnp antitest pozitivitás (100%) és RF pozitivitás (70%). Gyermekkorra validált diagnosztikus kritériumrendszer nincs (5,27). Vasculitisek Minor tünetek 1. érrendszer: kapillármikroszkópos eltérések, digitális ulcus 2. emésztõrendszer: dysphagia, gastrooesophagealis reflux 3. vese: veseelégtelenség, újonnan fellépõ hypertonia 4. szív: arrythmia, szívelégtelenség 5. légzõrendszer: pulmonalis fibrosis, diffúziós zavar, hypertonia 6. vázizomrendszer: ínsúrlódás, arthritis, myositis 7. idegrendszer: neuropathia, carpaltunnel szindróma 8. immunszerológia: ANA pozitivitás, RF pozitivitás, SSc-re specifikus antitestek (Scl-70, PM-Scl, anticentromer) 2. táblázat: Juvenilis szisztémás sclerosis PRES által javasolt klasszifikációs kritériumrendszere. A diagnózis kimondásához legalább egy major és két minor tünet megléte szükséges 16 éves kor elõtt A vasculitisek közül a Kawasaki-kór csak gyermekkorban, az arteritis temporalis pedig csak idõskorban jelentkezik. Gyermekreumatológiai betegek között a 6
7 különbözõ vasculitisek ritkán (1-6%-ban) fordulnak elõ; a két leggyakoribb kórkép a Schönlein-Henoch purpura és a Kawasaki-kór. A többi primer szisztémás vasculitis nagyon ritka gyermekkorban, de azok morbiditása és mortalitása kimagasló. A vasculitissel kezelt gyermekek 10-20%-ánál a betegség nem klasszifikálható! A heterogén gyermekkori szisztémás vasculitisek legújabb, 2005-ben egy nemzetközi gyermekreumatológiai konszenzus konferencián kidolgozott felosztása a 3. táblázatban látható. Ez tulajdonképpen a Chapel Hill-i felosztás módosított változata. A különbözõ gyermekkori vasculitisek EULAR/PRES/PRINTO által validált klasszifikációs kritériumrendszere közül csak a két leggyakoribb gyermekkori vasculitis klasszifikációs kritériumrendszerét ismertetjük (19, 20) (3. táblázat). Döntõen nagyér Takayasu arteritis vasculitis Döntõen a közepes Gyermekkori polyarteritis nodosa nagyságú ereket Cutan polyarteritis érintõ vasculitis Kawasaki betegség Döntõen kisér Granulomatosus vasculitis Wegener-granulomatosis Churg-Strauss szindróma Nem granulomatosus Mikroszkópikus polyangiitis Schönlein-Henoch purpura Izolált cutan leucocytoclasticus vasculitis Hypocomplementaemiás urticaria vasculitis Behçet kór Egyéb vasculitisek Szekunder vasculitisek infekciókhoz (Hepatitis B infekcióhoz társuló PAN is) társulva Malignus betegségekhez társulva Gyógyszer indukálta (hiperszenzitív) vasculitisek Kötõszöveti betegségekhez társuló vasculitisek (SLE, juvenilis dermatomyositis, Sjögren szindróma, scleroderma, kevert kötõszöveti betegség) Központi idegrendszer izolált vasculitise Cogan szindróma Nem besorolható vasculitisek 3. táblázat: A gyermekkori vasculitisek felosztása Schönlein-Henoch purpura (SHP) Fehér populációban ez a leggyakoribb vasculitis gyermekkorban, incidenciája 14/ , a vasculitises gyermekek 20-50%-át teszi ki. A SHP betegek 90%-a 10 év alatti. A gyermekkori SHP besorolási kritériumai a 4. táblázatban olvashatók (27). Gyermekekben felsõ légúti hurut (fõleg Streptococcus infekció), felnõttekben inkább gyógyszer, toxin, oltás, rovarcsípés, ételallergia a gyanított kiváltó tényezõ. Gyermekeknél gyakori a polimorf, felnõtteknél jellemzõ a monomorf kiütés. Hólyagos, vagy vérzéses, necroticus laesiok a kor elõrehaladtával válnak gyakoribbá. Veseérintettség is gyakrabban, 50-70%-ban észlelhetõ a felnõtteknél, míg gyermekkorban csak 20-40%-ban. Az arthritis, arthralgia inkább a gyermekeknél fordul elõ (20,24). Leucocytosis, thrombocytosis, emelkedett CRP gyermekekben; magas IgA és cryoglobulin szint felnõt- A szisztémás autoimmun betegségek gyermekkori jellegzetességei Purpura vagy petechia (döntõen az alsó végtagon) és legalább 1 tünet az alábbiak közül: 4. táblázat: A gyermekkori Schönlein-Henoch purpura kritériumai tekben gyakoribb. Amennyiben haematuria és/vagy proteinuria jelentkezik, nefrológiai gondozás szükséges! Veseelégtelenség a veseérintett gyermekek 2-10%-, felnõttek akár 30%-ánál alakulhat ki késõi szövõdményként! (13) Súlyos hasi fájdalom, bélvérzés, necrotisaló bõrjelenségek, súlyos proteinuria esetén oralis szteroid adása (1mg/ttkg/nap) javasolt, egyebekben NSAID elegendõ az arthralgia fájdalomcsillapítására. A betegség általában enyhe és monociklusos lefolyású, gyermekekben jobb indulatú, mint késõbbi életkorban. Kawasaki-betegség 1.) Hasi fájdalom 2.) Bármilyen szervbõl származó, döntõen IgA depozitumokat mutató biopsziás minta 3.) Arthritis vagy arthralgia 4.) Veseérintettség (haematuria és/vagy proteinuria) Incidenciája 6-10/ a fehér, 94/ a japán gyermekeknél, fõként 5 éven aluliak érintettek. Vasculitises gyermekek 20-65%-át teszik ki kontinensünkön. Gyakran infekció elõzi meg, szuperantigének által kiváltott poliklonalis T- és B-sejt aktivációt feltételeznek hátterében. Jellemzõen a kis- és közepes erek gyulladását okozza. A Kawasaki-betegség diagnosztikai kritériumait az 5. táblázatban mutatjuk be (27). Min. 5 napja tartó, más okkal nem magyarázható láz és legalább 4 tünet az alábbiak közül: 1.) Oropharyngealis nyálkahártya elváltozások: gyulladt torok és ajkak, vagy száraz, berepedt ajkak, epernyelv 2.) Kétoldali, nem gennyes conjunctivitis 3.) Distalis végtagrészek elváltozásai: kéz-, láboedema és/vagy erythema, általában a körmök körül kezdõdõ hámlás 4.) Polimorf exanthema (elsõsorban törzsön és nem vesicularis) 5.) Nyaki lymphadenopathia (min. 1,5 cm átmérõjû) 5. táblázat: Kawasaki-betegség diagnosztikus kritériumai Fontos a korai felismerés és kezelés. Az elsõ 10 napon belül nagydózisú intravénás immunglobulint (2 g/ttkg) kell adni a betegeknek. EKG és szív-uh vizsgálatot kötelezõ elvégezni, mert a kezeletlen esetek negyedénél jelentkezhet coronaria aneurizma! Szalicilsavat gyulladás gátló dózisban ( mg/ttkg/nap 4 részletben), majd leláztalanodás után alacsony thrombocyta aggregációt gátló adagban (3-5 mg/ttkg/nap) adjuk tovább. A Kawasaki-kóros gyermekek általános kilátásai jók, de kezeletlen esetekben 1-2%-ban jelentkezik myocardialis infarktus okozta korai halálozás! A coronaria érintettséggel járó betegeknél felnõttkori coronaria betegség veszélye fokozott, tartós kardiológiai gondozást igényelnek! 7
8 Köszönetnyilvánítás Köszönet Dr. Becker Krisztinának a tanácsaiért. Irodalomjegyzék 1. Bader-Meuner B., Armengaud J.B., Haddad E. et al.: Initial presentation of childhood-onset systemic lupus erythematosus: a French multicenter study. J. Pediatrics, 146, , Beltramelli M., Vercellesi P., Frasin A. et al.: Localized severe scleroderma: a retrospective study of 26 pediatric patients. Pediat. Dermatol., 27, , Bohan A., Peter JB.: Polymyositis és dermatomyositis. N. Eng. J. Med., 292, , , Brunner H.I., Gladman D.D., Ibanez D. et al.: Difference in disease features between childhood-onset and adult-onset systemic lupus erythematosus. Arthr. Rheum., 58, , Cassidy J.T., Petty R.E., Laxer R.M. et al.: Textbook of Pediatric Rheumatology. 5th ed. Philadelphia: Elsevier Saunders, Cimaz R., Lehman T.: Pediatrics in systemic autoimmune diseases- Volume 6 in Handbook of systemic autoimmune diseases. Amsterdam, Elsevier, Constantin T., Ponyi A, Kálovics T. et al.: Juvenilis és felnõttkori dermatomyositisben szenvedõ betegek kórlefolyásának jellegzetességei, illetve a kezelés és a késõbbi kórlefolyás kapcsolatának vizsgálata. Orv. Hetil., 148, , Descloux E., Durieu I., Cochat P. et al.: Influence of age at disease onset in the outcome of paediatric systemic lupus erythematosus. Rheumatology, 48, , Falcini F., Nacci F.: Systemic lupus erythematosus in the young:the importance of a transition clinic. Lupus, 16, , Ferraz M.B., Goldenberg J., Hilario M.O. et al.: Evaluation of the 1982 ARA lupus criteria data set in pediatric patients. Clin. Exp. Rheumatol., 12, 83-87, Foeldvari I.: Update on pediatric systemic sclerosis: similarities and differences from adult disease. Curr. Op. Rheumatol., 20, , Foeldvari I., Zhavania M., Birdi N. et al.: Favourable outcome in 135 children with juvenile systemic sclerosis: Results of a multinational survey. Rheumatology, 39, , González L.M., Janniger C.K., Schwartz R.A.: Pediatric Henoch-Schönlein purpura. Int. J. Dermatol., 48, , Hersh A.O., von Scheven E., Yazdany S. et al.: Differences in longterm disease activity and treatment of adult patients with childhood- and adult-onset systemic lupus erythematosus. Arthr. Rheum., 61, 13-20, Huber A.M., Lang B., Leblanc C.M.: Medium- and long-term functional outcomes in a multicenter A szisztémás autoimmun betegségek gyermekkori jellegzetességei cohort of children with juvenile dermatomyositis. Arthr. Reum, 43, , Kone-Paut I., Piram M., Guillaume J. et al.: Lupus in adolescens. Lupus, 16, , Lowry C.A., Pilkington C.A.: Juvenile dermatomyositis:extramuscular manifestation and their management. Curr. Opin. Rheum., 21, , Maillard S.M., Jones R., Owens C. et al.: Quantitative assessment of MRI T2 relaxation time of thigh muscles in juvenile dermatomyositis. Rheumatology, 43, , O Neil K.M.: Progress in pediatric vasculitis, Curr. Op. Rheumatol., 21, , Ozen S., Pistorio A., Iusan M.S. et al.: EULAR/ PRINTO/PRES criteria for Henoch-Schönlein purpura, childhood polyarteritis nodosa, childhood Wegener granulomatosis and childhood Takayashu arteritis. Ankara Part II: Final classification criteria. Ann. Rheum. Dis., 69, , Papadimitraki E.D., Isenberg D.A.: Childhood- and adult-onset lupus: an update of similarities and differences. Expert Rev. Clin. Immunol., 5, , Pluchinotta F.R., Schiavo V.F., Vittadello F. et al.: Distinctive clinical features of pediatric systemic lupus erythematosus in three different age classes. Lupus, 16, , Ruperto N., Ravelli A., Murray K.J. et al.: Preliminary core sets of measures for disease activity and damage assassment in juvenile systemic lupus erythematosus and juvenile dermatomyositis. Rheumatology, 42, , Ruperto N., Ozen S., Pistorio A. et al.: EULAR/ PRINTO/PRES criteria for Henoch-Schönlein purpura, childhood polyarteritis nodosa, childhood Wegener granulomatosis and childhood Takayashu arteritis. Ankara Part II:Final classification criteria. Ann. Rheum. Dis., 69, , Targoff I.N., Miller F.W., Medsger T.A. et al.: Classification criteria for the idiopathic inflammatory myopathies. Curr. Opin. Rheumatol., 9, , Tucker L.B., Uribe A.G., Fernandez M. et al.: Adolescent onset of lupus erythematosus in more aggressive disease worse outcomes: results of a nested matched case-control study within LUMINA, a multiethnic US cohort (LUMINA LVII). Lupus, 17, , Woo P., Laxer R.M., Sherry D.D.: Pediatric rheumatology in Clinical practice. London, Springer, Zulian F.: Systemic sclerosis and localized scleroderma in childhood. Rheum. Dis. Clin. North Am., 34, , Zulian F., Woo P., Althreya B.H. et al.: The Pediatric Rheumatology European Society/American College of Rheumatology/European League against Rheumatism provisional classification criteria for juvenile systemic sclerosis. Arthr. Rheum., 57, ,
9 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban Dr. Haltrich Irén, Prof. Fekete György Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban Semmelweis Egyetem, II. sz. Gyermekgyógyászati Klinika, Budapest Összefoglalás: A gyermekkori leukémiák kezelésének sikeressége az utóbbi évtizedekben folyamatosan javul, az akut limfoid leukémiák esetében az ötéves eseménymentes túlélés megközelíti a 90%-ot. Ez a siker elsõsorban a rizikó csoportok szerinti terápiás protokollok bevezetésének köszönhetõ. A gyermekkori leukémiákban a kezdeti kromoszóma rendellenesség minden más jellemzõtõl független prognosztikai tényezõ. A rizikó csoportokba történõ besorolásnál a konvencionális kockázati tényezõk (mint például az életkor, a kezdeti fehérvérsejt szám) egyre inkább elvesztik jelentõségüket és a leukémiás sejtek genetikai elváltozásai kerülnek elõtérbe. A specifikus genetikai aberrációkat a WHO felhasználja az akut leukémiák osztályozására, az eltérések alapján önálló citogenetikai entitásokat különít el. A közlemény a citogenetikai vizsgálatok jelentõségére, a betegség diagnosztizálásában, követésében, kimenetelének megítélésében és a kezelés megválasztásában betöltött szerepére összpontosít. Összefoglalja a gyermekkori akut leukémiákban elõforduló kromoszóma rendellenességek molekuláris genetikai hátterével, gyakoriságával, prognosztikai hatásával kapcsolatos ismereteket. Összehasonlítja a klinikai gyakorlatba beépült két módszert, a G-sávos és a fluoreszcens in situ hibridizációs (FISH) technikák szerepét az ismert és a rejtett rendellenességek feltárásában. Kulcsszavak: citogenetika, G-sáv, fluoreszcens in situ hibridizáció - FISH, fúziós gén, ALL, AML Rövidítések jegyzéke: ABL1 = v-abl Abelson murine leukemia viral oncogene homolog 1 gén AFF1 = AF4/FMR2 family, member 1 (AF4) gén APL = akut promyelocytas leukémia ALL = akut lymphoblastos leukémia Alu-szekvencia = nagyfokú ismétlõdést mutató genom szakasz AML = akut myeloblastos leukémia ATRA = all-transz-retinsav BCR = breakpoint cluster region CBFA = core binding factor α gén, új neve RUNX1 CBFB = core binding factor β gén CEBPA = CCAAT/enhancer binding protein (C/EBP), α gén CD10 = sejtfelszíni antigén, a common ALL markere CML = krónikus myeloid leukémiák DEK = onkogén vagy NUP214, nucleoporin 214 kda gén DI = DNS-index ELL = eleven nineteen lysin rich leukemia gén Summary: The success rate of treatment in childhood leukemia has increased significantly during the last decades, the five year event free survival rates approaching 90% in acute lymphoblasic leukemia. This success could be explained by stringent application of prognostic factors for risk directed therapy in clinical trials. Chromosomal changes are independent prognostic indicators in childhood leukemia and patients are classified into risk groups for treatment according to their genetic abnormalities. Specific genetic abnormalities have been included in the World Health Organization (WHO) classification of hematological malignancies, and are used to define distinct disease entities. Conventional risk factors such as age, initial leukocyte count have decreasing importance. This paper focuses on the significance of cytogenetic analysis in pediatric leukemia supporting its importance in the pathogenesis, diagnosis, prognosis, follow-up and choice of treatment. It reviews the type and frequencies of the most common chromosomal aberrations, their prognostic relevance and their molecular background. Conventional cytogenetics remains the gold standard methodology for the detection of specific aberrations in acute leukemia. The new, fluorescence in situ hybridization (FISH) based techniques contribute significantly to the detection of the subtle abnormalities, but both methods are used in routine evaluation of chromosomal abnormalities. Key words: cytogenetics, G-band, fluorescence in situ hybridization - FISH, fusion genes, ALL, AML E2A = E2A immunoglobulin enhancer binding factors E12/E47, vagy TCF3, transcription factor 3 gén ETO = eight twenty-one gén ETV6 = ETS like gene, régebbi nevén TEL, translocation ets leukemia gén EVI1 = ecotropic virus integration site-1 gén FAB = French-American-British FLT3 = fms-related tyrosine kinase 3 gén HLXB6 = homeo box HB9, újabban MNX1 gén HOX = homeobox típusú gén IL3 = interleukin-3 gén IGH = immunoglobulin nehézlánc gén ITD, PTD = internális, parciális tandem duplikáció JAK2 = Janus kinase 2 gén STAT5 = signal transducer and activator of transcription gén KIT = v-kit Hardy-Zuckerman 4 feline sarcoma viral oncogene homolog gén M-BCR = maior breakpoint cluster regió m-bcr = minor breakpoint cluster regió MDS = myelodysplasiás szindróma 9
10 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban MKL1 = megakaryoblastic leukemia translocation 1, vagy MAL, megakaryocyta akut leukémia gén MLL = mixed lineage leukemia vagy myeloid/ limfoid leukemia gén MLLT1 = mixed-lineage leukemia translocated to, 1 gén, ENL fehérjét kódol MLLT3 = mixed-lineage leukemia translocated to, 3 gén, AF9 fehérjét kódol MLLT4 = mixed-lineage leukemia translocated to, 4 gén, AF6 fehérjét kódol MLLT10 = mixed-lineage leukemia translocated to, 10 gén, AF10 fehérjét kódol m-rns = messenger RNS MYH11= myosin nehéz lánc 11 gén NPM1 = nucleophosmin gén N-RAS = neuroblastoma RAS viral (v-ras) oncogene homolog gén NUMA= nuclear mitotic apparatus protein 1 gén NUP214 = nucleoporin 214 kda PBX1 = pre-b-cell leukemia homeobox 1 gén Ph = Philadelphia kromoszóma PLZF = promyelocytic leukaemia zinc finger protein gén (ZBTB16 gén) PML = promyelocyta leukémia gén RARA = retinsav receptor α gén RBM15 = RNA binding motif protein 15, vagy OTT, one twenty two gén RPN1 = ribophorin gén RT-PCR = valós idejû polimeráz láncreakció RUNX1 = runt-related transcription factor 1, vagy AML 1, vagy CBFA RUNX1T1 = runt-related transcription factor 1; translocated to, 1, gén (ETO gén) STAT5B = jelátvitelért és transzkripcióért felelõs gén T-ALL = T-sejtes ALL t-aml = terápiával összefüggõ AML TCF3 = transcription factor 3 gén (E2A gén) TEL = ETV6 TKI = tirozin kináz inhibitor(sti571) v = variáns ZBTB16 = zinc finger and BTB domain containing 16 gén (PLZFgén) Bevezetés Theodor Boveri már a 20. század elején, zseniális módon megsejtette, hogy a malignus folyamatok hátterében szerzett kromoszóma rendellenességek állnak. Az elsõ közleményt a hematológiai malignitásokban elõforduló kromoszóma rendellenességrõl, a Philadelphia kromoszómáról Nowell és Hungerford publikálta 1960-ban a Science folyóiratban. Késõbb Rowley és munkatársai (32) bebizonyították, hogy a Philadelphia kromoszóma létrejötte a 9-es és 22-es kromoszómák közötti reciprok transzlokáció következménye, azonosították a töréspontokban található BCR és ABL1 géneket (15), melyeknek a fúziója egy konstitutív aktivitású tirozin-kináz fehérje termelõdését eredményezi. A molekuláris szintû eltérések feltárása lehetõvé tette egy célzott tirozin kináz inhibitor gyógyszer kifejlesztését (STI571), mely a BCR- ABL kiméra fehérje funkciót blokkolja és ezáltal a kemoterápiánál kíméletesebben gyógyítja a betegeket. Azóta a szerzett kromoszóma rendellenességek és a malignitások között számos összefüggést azonosítottak, 358 különbözõ neoplasiával kapcsolatos fúziós gént írtak le (25). A kromoszóma rendellenességek sokfélesége ellenére az akut leukémiák kórtani szempontból egységesnek tekinthetõk. Jellemzõik a kiegyensúlyozott transzlokáció és az ennek kapcsán kialakuló különbözõ fúziós gének. A transzlokációs töréspontok területén azonosított gének többnyire olyan kináz- aktivitású fehérjéket vagy transzkripciós faktorokat kódolnak, melyek a normális hemopoetikus sejtek differenciációjában játszanak szerepet. A töréspont érinthet egy vagy több transzkripciós faktort. A fúzió által generált fehérjék szerkezete és funkciója nagyfokú hasonlóságot mutat: DNS-kötõ-, homo-vagy hetero-dimerizációs-, a kromatin átformálást, illetve a génaktivitást szabályozó domént (pl. co-repressor vagy co-aktivátor) tartalmaznak. Ilyen, a leukémiával kapcsolatos transzlokációkban gyakran résztvevõ transzkripciós faktorok például a CBFA, CBFB, MLL, E2A, PBX1, melyek a HOX gének által szabályozott transzkripciós kaszkádot befolyásolják. A HOX gének a hemopoetikus õssejtek és utódsejtek képzõdéséért felelõsek. A hemopoetikus õssejtek vagy progenitor sejtek genetikai módosulásai a sejtfunkció megváltozását és végül leukémiás transzformációját eredményezik, melynek lényege minden esetben a vérképzõ sejtek folyamatos proliferációja, kóros vagy gátolt érési folyamata. A gyermekkori leukémiák utóbbi évtizedekben elért sikeres gyógyításában jelentõs szerepet játszott a betegség patomechanizmusának megértése, a leukémiás sejtekben elõforduló genetikai elváltozások molekuláris szintû feltárása. A betegség diagnosztizálásában, kimenetelének megítélésében és a kezelés megválasztásában fontos szerepet játszik a specifikus genetikai eltérés. A kezdeti kariotípus minden más jellemzõtõl független prognosztikai tényezõ, a különbözõ terápiás szerekkel szembeni érzékenységet vagy rezisztenciát is befolyásolhatja (30). A malignus hematológiai betegek citogenetikai és molekuláris genetikai vizsgálata ma már a klinikai gyakorlat fontos része. Az akut leukémiák WHO osztályozásának citogenetikai vonatkozásai A korábbi FAB osztályozás elsõsorban a sejtek differenciáltsági fokát, a morfológiai és immunfenotípus jegyeket használta fel a leukémiák osztályozására. A WHO figyelembe veszi a genetikai információkat is. Eszerint bizonyos kromoszóma rendellenességek egységes klinikai, immunfenotípus és prognózis jegyeket határoznak meg, ezért önálló entitásoknak tekinthetõk. B lymphoblastos leukémiában az alábbi citogenetikai entitásokat, önálló megjelenési formákat különíti el: 10
11 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban B lymphoblastos leukémia/limfóma t(9;22)(q34;q11.2); BCR-ABL1 B lymphoblastos leukémia/limfóma t(v;11q23); MLL átrendezõdés B lymphoblastos leukémia/limfóma t(12;21)(p13;q22); TEL-AML1(ETV6-RUNX1) B lymphoblastos leukémia/limfóma hyperdiploid kariotípussal B lymphoblastos leukémia/limfóma hypodiploid kariotípussal B lymphoblastos leukémia/limfóma t(5;14)(q31;q32); IL3-IGH B lymphoblastos leukémia/limfóma t(1;19)(q23;p13.3); TCF3-PBX1 A felsorolt ALL-specifikus rendellenességek 20%- nál alacsonyabb csontvelõi blasztszámnál is B-sejtes lymphoblastos leukémiát igazolnak. A T-lymphoblastos leukémia/lymphoma 50-70%-ában mutatható ki kromoszóma rendellenesség. A leggyakoribb visszatérõ rendellenességek töréspontjai a T-sejt receptor lokuszokat kódoló géneket érintik: a 14q11.2-ben az α és δ-, a 7q35- ben a β és a 7p14-15-ben a γ T-sejt receptort. E töréspontokat érintõ transzlokációkkal társuló klinikai kép nem egységes. A 2009-es WHO myeloid neoplasiákra vonatkozó besorolása 3 transzlokáció specifikus alcsoportot különít el, melyek blasztszámtól függetlenül diagnosztikus értékûek: AML t(8;21)(q22;q22) transzlokációval, illetve RUNX1-RUNX1T1 fúziós génnel; AML 16-os kromoszómát érintõ inverzióval vagy transzlokációval: inv(16)(p13.1q22) vagy t(16;16)(p13.1;q22), CBFb/MYH11 fúziós génnel; APL t(15;17)(q22;q12) transzlokációval, illetve PML/ RARA fúziós génnel. Az APL esetében viszont a RARA gén variáns transzlokációit, melyek esetében a PML-tõl eltérõ a partner gén (pl. 11q23-ZBTB16-, 11q13 NUMA1-, 5q35- NPM1- vagy a 17q11.2-STAT5B-töréspontú gének) kiemeli az önálló megjelenési formák sorából, tekintettel arra, hogy nem minden esetben egyezik a fenotípusuk az APL sajátságaival és ATRA kezelésre rezisztensek lehetnek. A további (az MLL átrendezõdés kivételével) újonnan bevezetett genetikai entitások esetében a perifériás vérben vagy a csontvelõben 20% vagy annál nagyobb arányú blaszt jelenléte esetén diagnosztizálható az AML: AML t(9;11)(p22;q23) transzlokációval, illetve MLLT3-MLL fúziós génnel AML t(6;9)(p23;q34) transzlokációval, illetve DEK-NUP214 fúziós génnel AML 3-as kromoszómát érintõ inverzióval vagy transzlokációval: inv(3)(q21q26.2) vagy t(3;3)(q21;q26.2); RPN1-EVI1 fúziós génnel AML (megakaryoblastos) t(1;22)(p13;q13) transzlokációval, illetve RBM15-MKL1 fúziós génnel. Az MLL gént érintõ átrendezõdések a 85 lehetséges partnernek, illetve a molekuláris színtû szerkezeti rendellenességeknek köszönhetõen igen heterogén csoportot képviselnek, ezért csak a sokat tanulmányozott, ismert prognózisú t(9;11)(p22;q23) transzlokáció képez önálló entitást. A WHO beépíti az utóbbi 10 év molekuláris genetikai vizsgálatainak eredményeit: az NPM1 illetve CEBPA mutációval jellemezhetõ AML-t ideiglenes entitásként határozza meg. Továbbá az FLT3 gén mutáció vizsgálatát elsõsorban a citogenetikailag normális AML-ben ajánlja. A gyermekkori leukémiák citogenetikai jellemzõi A gyermekkori akut leukémiák 80-82%-a lymphoid (ALL), 15-20%-a myeloid (AML), a krónikus myeloid leukémia (CML) az esetek 1%-át teszi ki. Mivel a rizikótényezõkön alapuló terápiás protokollokkal érték el a legjobb sikereket (az 5 éves esemény mentes túlélés 80-90%) (29), a pontos kockázat becslés egyre nagyobb szerephez jut a gyermek- és a serdülõkori akut leukémia kezelésében. A különbözõ rizikó csoportokba (alacsony- LR, közepes-ir, magas-hr) történõ besorolásnál a konvencionális rizikófaktorok (immunfenotípus, életkor, nem, kezdeti fehérvérsejtszám) egyre inkább elvesztik jelentõségüket és elõtérbe kerülnek a leukémiás sejtek genetikai elváltozásai (29). A gyermekkori leukémiák specifikus genetikai aberrációinak nagy része standard citogenetikai vizsgálattal kimutatható. A rejtett rendellenességek feltárásában a FISH alapú molekuláris citogenetikai technikák bevezetése jelentett áttörést, mely lehetõvé tette az alacsony sávszámú kromoszómák vagy az osztódásra nem bírható leukémiás sejtek rendellenességeinek célzott feltárását. Az akut limfoid leukémia citogenetikája A leggyakoribb gyermekkori ALL-ben elõforduló genetikai eltérések jellemzõit az 1. táblázatban foglaltuk össze. ALL-ben kétféle eltéréssel, számbeli és szerkezeti elváltozással találkozhatunk. Az ALL számbeli elváltozásai érinthetik az egész kromoszóma állományt (triploid, tetraploid), megváltoztatva annak ploiditását, vagy jelenthetik bizonyos kromoszómák többletét vagy hiányát (aneuploiditás). A modális kromoszómaszám szerint a csontvelõi kariotípus lehet: diploid, pszeudodiploid, hyperdiploid, közel-triploid, közel-tetraploid, hypodiploid és közelhaploid. Gyermekkori ALL-ben különleges prognosztikai jelentõsége van az kromoszóma számú, magas DNS-indexû (DI > 1,16) hyperdiploid B kariotípusnak, mely a gyermekkori ALL-ek 30%-ában elõforduló, jóindulatú elváltozás. A hyperdiploid B típusra jellemzõ 8 különbözõ kromoszóma non-random triszómiája, melyek gyakorisági sorrendben a következõk: 21, X, 14, 6, 18, 4, 17, 10 (16). A hyperdiploid B kariotípushoz pre- B immunfenotípus, CD10 common ALL antigén expresszió, kettõtõl tíz évig terjedõ életkor, alacsony fehérvérsejtszám és alacsony szérum laktát dehidrogenáz szint társul. Nagyszámú hyperdiploid B kariotípúsú gyermek- 11
12 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban Aberráció Prognózisa Molekuláris jellemzõi Incidenciája Ajánlott metodika t(9;22)(q34;q11) HR BCR-ABL1 fúzió 2-3% citogenetika, FISH, RT-PCR t(4;11)(q21;q23) HR MLL-AFF1 fúzió 2-5% citogenetika, FISH, RT-PCR Közel-haploid HR Haploid készlet számfeletti kromoszómája 5-6% citogenetika, FISH, DNS index iamp21 HR RUNX1 amplifikáció 2-3% FISH t(1;19)(q23;13.3) IR TCF3-PBX1 fúzió 5-6% citogenetika, FISH MLL-t érintõ transzlokációk IR-HR MLL-átrendezõdés 5-8% FISH, citogenetika, RT-PCR IGH-t érintõ transzlokáció IR-HR IGH transzlokáció 2-3% FISH, citogenetika t(12;21)(p13;q22) LR ETV6-RUNX1 fúzió 20-25% FISH, RT-PCR Hyperdiploiditás LR Ötnél több számfeletti kromoszóma 20-30% citogenetika, FISH, DNS index 1. táblázat: A leggyakoribb kiemelt prognosztikai jelentõségû genetikai eltérések vizsgálata gyermekkori ALL-ben kori ALL eset statisztikai értékelése alapján a jó prognózis inkább bizonyos jó triszómiákkal áll összefüggésben (35), mintsem önmagában az emelkedett kromoszómaszámmal. Bizonyos munkacsoportok a 4-es, 10-es, 17- es triszómia együttes elõfordulása esetén számoltak be kiemelkedõen jó terápiás sikerrõl, a legkedvezõbb prediktív értéket a 10-es triszómia esetében figyelték meg (28,37). A közötti kromoszómaszámú hyperdiploid A kariotípus (DI >1.00 és <1,16) a gyermekkori ALL 8-15%-ában elõforduló közepes prognosztikai értékû elváltozás. A beteg gyermekek klinikai értékei általában rosszabbak, a kromoszóma többlet mintázata nem annyira jellegzetes, gyakrabban találkozunk szerkezeti elváltozásokkal. A hyperdiploid kariotípus átlagosnál jobb prognózisát a 21-es kromoszómán jelen lévõ methotrexat transzportert kódoló gén emelkedett dózisával hozták összefüggésbe, mely lehetõvé teszi nagyobb mennyiségû methotrexat felhalmozódását a leukémiás blasztokban (30). A több mint 80 kromoszómával jellemezhetõ közel tetraploid kariotípus a gyermekkori ALL-ek 1%-ában fordul elõ. Bár biológiailag különbözik a hyperdiploiditástól, a retrospektív tanulmányok alapján (31) úgy tûnik, hogy a B-immunfenotípusú betegekhez hasonlóan jó prognózisúak és az alacsony rizikó csoportnak megfelelõ kezeléssel gyógyíthatók. A 45 vagy annál kevesebb számú hypodiploid kariotípus általában a kromoszóma szám csökkenésével arányosan romló prognosztikai hatású, függetlenül attól, hogy melyik kromoszómára vonatkozik a monoszómia. A kromoszóma számú közel haploid (DI < 1) kariotípus kortól, fehérvérsejtszámtól, szerkezeti elváltozás jelenlététõl függetlenül a legrosszabb prognosztikai értékû elváltozás (11,38). A hyperdiploid és a haploid kariotípust rutin citogenetikai eljárással általában nehéz diagnosztizálni, mivel gyakran gyenge morfológiájú, rosszul terülõ kromoszómákhoz jutunk, az osztódások a rövid sejttenyészetekben elõforduló poliploid osztódásokra emlékeztethetnek, a kisméretû haploid klónok hiányos metafázisoknak, preparálási mûtermékeknek tûnhetnek fel. A két ellenkezõ prognosztikai hatású klón (a hyper- és a hypodiploid) ugyanazon betegben is elõfordulhat. A centroméra specifikus FISH próbák kiválóan alkalmasak az aneuploidiák azonosítására, mivel nagyszámú interfázis sejtmagban történõ számolással lehetõséget nyújtanak az objektívebb értékelésre, az in vitro körülmények között nem osztódó populációk feltérképezésére (8,10,13). Az ALL szerkezeti elváltozásai A t(12;21)(p13;q22) a gyermekkori B-sejtes ALL esetek 15-25%-ában elõforduló rejtett transzlokáció, a WHO besorolás önálló citogenetikai entitása. A transzlokáció során a 12p22 régióban azonosított ETV6 gén a 21q22 régióba lokalizálható RUNX1 génnel egyesül és az ETV6-RUNX1 fúziós gén keletkezik (21). A hibrid génben az ETV6 promoter régió és helix-loop-helix domén kapcsolódik az RUNX1 gén DNS kötõ és transzaktivációs doménjéhez. Az ETV6 transzkripciós modulátor, a RUNX1 gén a CBFA-CBFB transzkripciós komplex α alegységét kódolja, mely több vérképzéssel kapcsolatos gén transzkripciós aktivátora. A fúziós protein a RUNX1 target gének rendellenes szabályozásával váltja ki a leukémiás folyamatot. A transzlokáció általában kedvezõ életkorral és klinikai jellemzõkkel társuló, jó prognózisú elváltozás (24). Az elsõ tanulmányok az ETV6/RUNX1-pozitív betegek tartósabb komplett remissziójáról (56 hónap versus 26), de a késõi relapszus veszélyérõl számoltak be (36). Hosszabb követésrõl szóló átfogó tanulmányok azonban csak az utóbbi években születtek. A retrospektív tanulmányok alapján az ETV6/ RUNX1-pozitív gyermekek relapszus mentes túlélése függ a rizikó csoportokba történõ besorolási szempontoktól és az alkalmazott terápiás protokolltól. A ETV6/ RUNX1-pozitív lymphoblastok rendkívül érzékenyek az L-asparaginaséra, de jól reagálnak a szteroidokra és a vincristinre is. Azok az ETV6/RUNX1-pozitív gyermekek, akiket olyan terápiás protokoll szerint kezeltek, mely az intenzifikációs kezelés alatt több L-asparaginaset tartalmazott, elérték a 97%-os ötéves össztúlélési rátát (21). A transzlokációhoz gyakran társul a homolog ETV6 gén deléciója, melynek funkció vesztése a leukémiás transzformáció folyamatában játszhat szerepet, a terápia sikerességét lényegesen nem befolyásolja (11). Ez a gyakori transzlokáció hagyományos G-sávos kromoszómákon nem látható, mivel kb. azonos nagyságú és sávmintázatú kromoszóma szegmentumok cserélõdnek ki. Kimutatása speciális FISH próba felhasználásával vagy különféle molekuláris módszerekkel lehetséges. 12
13 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban Az MLL gént érintõ 11q23 átrendezõdések gyermekkori akut leukémiákban gyakran fordulnak elõ. Általában elmondható, hogy gyakoriságuk az életkor elõrehaladtával folyamatosan csökken: leggyakoribb a csecsemõkori leukémiában (60%), míg két éves kor fölött csak 9% körüli. Az MLL-t ún. kicsapongó, promiscuus génként tartják számon: 66 különbözõ partner génnel képez reciprok transzlokációt, de deléciót, duplikációt, inverziót, amplifikációt, addiciót, a génen belüli tandem-ismétlõdéseket (ITD) és fúziót is leírtak. A jól konzervált, nagyméretû gén két ALU szekvenciát és egy topoizomeráz II-kötõhelyet is tartalmaz. Fehérje terméke nagyfokú homológiát mutat az ecetmuslica trithorax nevû proteinjével, az emlõsökben a HOX géneket szabályozza, melyek az embrionális fejlõdésben és a hemopoetikus õssejtek differenciálódásában játszanak szerepet. Az MLL génátrendezõdések a HOX gének ellenõrzése által vezérelt transzkripciós programot zavarják meg. Kialakulásukat epipodophyllotoxin hatással hozzák összefüggésbe, mely gátolja a topoizomerázok széttekerõ funkcióját és a hatás kompenzálásaként a topoizomerázokkal homológ szekvenciák törését eredményezi (5). Az MLL gén érintettség általában véve rossz prognózisú, ugyanakkor a nagyszámú transzlokációs partnernek és a rendellenesség típusnak köszönhetõen heterogén csoportot képvisel (11,38). Egypetéjû ikertanulmányok azt bizonyítják, hogy lappangási ideje rövidebb a más géneket érintõ leukémiáknál, a topo II inhibitorral történõ kezelés esetén is az átlagosnál korábban jelentkezhet a szekunder leukémia (1,5). A t(4;11)(q21;q23) MLL-AFF1(AF4) csecsemõkori leukémiában, gyermekkori limfoid, myeloid és kevert fenotípusú akut leukémiában, t- AML-ben elõforduló igen rossz prognózisú elváltozás (18). Erre és általában a többi MLL gént érintõ transzlokációra jellemzõ a pro-b sejtes immunfenotípus, magas fehérvérsejtszám, és a központi idegrendszeri érintettség. A génexpressziós vizsgálatok bebizonyították, hogy az MLL gén transzlokációt hordozó leukémia egy különálló kórforma, különbözik az akut limfoid és a myeloid leukémiától, génexpressziós profilja sajátos HOX gén és korai progenitor hemopoetikus sejtek mintázatával jellemezhetõ. Ezidáig ez az egyetlen olyan ismert transzlokáció, amelyik egységes génexpressziós programot határoz meg. Elképzelhetõ, hogy genotípus specifikus gyógyszer kifejlesztésére is hasznosíthatóak lesznek az ezirányú kutatási eredmények (2). A megfelelõen agresszív kemoterápia elkezdése, illetve a csontvelõ transzplantációra való felkészítés szempontjából a 11q23 átrendezõdések idõbeni felismerése rendkívül nagy fontosságú. Az MLL gén transzlokációinak nagy része metafázis kromoszómákon azonosítható. Azonban néhány rejtett transzlokáció, például a t(6;11) vagy a t(11;19) alacsony sávszámú csontvelõi kromoszómákon biztonsággal nem azonosítható. Hasonlóképpen az MLL gén deléció, duplikáció átlagos felbontású kromoszómákon nem látható. Az RT-PCR technikával csak abban az esetben lehet a transzlokációt kimutatni, ha ismerjük a partner kromoszómát. Az MLL gén átrendezõdéseket jelenleg legpontosabban dualcolor FISH-próbával tudjuk azonosítani, mely alkalmas a partner kromoszómától függetlenül a transzlokációk esetében keletkezõ hasadt gén, a deletált vagy az amplifikálódott MLL gén kimutatására. A FISH próba két részbõl áll: a gén 5 distalis vége pirossal, 3 proximalis vége zölddel van jelölve és a kétszínû jel eltávolodása osztódó és nem osztódó sejtekben egyaránt jelzi a transzlokációt. A t(9;22)(q34;q11) talán a legtöbbet tanulmányozott és legismertebb citogenetikai elváltozás, mely a CML-ek 99%-ában, a gyermekkori ALL 2-3%-ában fordul elõ. A transzlokáció során a 9-es kromoszómán található ABL1 gén 3 vége a 22-es kromoszómán található BCR gén 5 végéhez helyezõdik át. Attól függõen, hogy a töréspont a BCR génen belül hol található, különbözõ nagyságú m-rns, illetve fehérje termék képzõdik. ALLben leggyakrabban a minor töréspontú átrendezõdéssel (m-bcr) találkozunk, mely egy 7-kb mrns-t és egy p190 fehérjét eredményez. A major töréspontú (M-BCR) átrendezõdés, mely egy 8,5 kb mrns-t és egy p210 fehérje terméket indukál, CML-re jellemzõ, ALL-ben csak ritkán fordul elõ. Az így keletkezõ BCR/ABL fúziós gén a derivátum 22-es kromoszómán található, mely felfedezésének helyérõl a Philadelphia nevet kapta. A törésponttól függetlenül, mindkét chiméra fehérje fokozott kináz aktivitása révén a hemopoetikus õssejtek proliferációjáért, önmegújításáért felelõs cellularis jelátviteli útvonalat (RAS, CDK1) zavarja meg. A Ph+ ALL esetek 50-80%-ában különbözõ társuló citogenetikai eltérésekkel találkozunk, melyek közül a leggyakoribbak: +der(22), -7, del(7q), +8; CML-ben gyakori az i(17q). Az ALL betegek egy kisebb részében a Ph kromoszóma konvencionális citogenetikai módszerrel nem azonosítható, de RT-PCR-rel a fúziós gén kimutatható. Ennek oka lehet szubmikroszkópikus nagyságrendû elváltozás vagy ennél lényegesen gyakoribb variáns vagy/és komplex átrendezõdés, melyben a Philadelphia kromoszóma maszkírozott formában van jelen. A Ph kromoszóma azonosításának kitûnõ eszköze a kétszínû (DC, dual color), dupla fúziós (DF, dual fusion) FISH próba, mely interfázisban és metafázisban alkalmas a gén fúzió minden formájának kimutatására és a transzlokációhoz gyakran csatlakozó, rosszabb prognózist elõidézõ ABL gén delécióját is detektálja. A Ph kromoszóma prognosztikai hatása életkor függõ, a negatív hatás az életkorral nõ, gyermekeknél általában mérsékeltebb, legsikeresebb terápiás eredményt az 1-9 éves életkor közötti betegekben értek el. A közelmúltban bevezetett transzlokáció-specifikus-kezelés (imatinib mezilát) kemoterápiával kombinálva egyre hosszabb eseménymentes túlélést biztosít, az enyhébb kemoterápiás szövõdmények következtében a betegek életminõsége is javult. A tirozin-kináz inhibitor kezelés különösen a nem transzplantálható (megfelelõ donor hiányában vagy elõrehaladott életkor miatt) betegek életkilátásait változtatta meg. A nagyobb esetszámú Ph+ ALL betegek intenzív TKI-alapú kezelése bebizonyította, hogy a korábbi prognosztikai faktorok, mint például 13
14 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban a komplex kariotípus vagy a molekuláris töréspont elveszítette jelentõségét a terápia sikeressége szempontjából, azonban igazi kihívás a TKI-ral szembeni rezisztencia problémájának megoldása (17,39). A t(1;19)(q23;p13)/e2a-pbx1 önálló WHO entitás, a gyermekkori ALL 5-6%-ában fordul elõ, lehet kiegyensúlyozott vagy egy der(19)t(1;19) többlet kromoszómával rendelkezõ, kiegyensúlyozatlan elváltozás. Gyakran fordul elõ hyperdiploid kariotípusban is, társuló anomáliái közül ismertebbek: i(1q), +6, del(6q), +8, i(9q), +17, i(17q), +21. A transzlokáció során az PBX1 gén az 1-es kromoszómáról fuzionál a 19-es kromoszóma E2A nevû génjével. Az E2A a normális lymphopoesisért és a B-sejt éréséért felelõs transzkripciós faktorokat kódol. A nem-fehér népeknél jóval gyakoribb. Általában véve minden formájában rossz prognózisú elváltozás, de az utóbbi idõben intenzívebb kemoterápiás szerek alkalmazásával, elsõsorban a kiegyensúlyozatlan formák prognózisa javult (10,38). A t(8;14)(q24;q32) és variáns formái, a t(8;22)(q24;q11) és t(2;8)(p13;24) a Burkitt limfoma mellett érett B-sejtes leukémiák 5%-ában elõforduló átrendezõdés. Lényege minden esetben az, hogy a cmyc onkogén valamelyik aktívan mûködõ immunglobulin nehéz lánc gén szabályozó szekvenciáinak hatása alá kerül, melynek eredménye a cmyc fokozott expressziója, ami kontroll nélküli sejt proliferációt eredményez. Az azonnali citogenetikai diagnózis a betegek kezelésének stratégiája szempontjából kulcsfontosságú. Az elõbbihez hasonló mechanizmus eredményezi az IL3 gén fokozott mûködését a t(5;14)(q31;q32) esetében, mely JAK2/ STAT5 útvonalon keresztül az apoptózis gátló RAS útvonalat aktiválja. Ez az önálló WHO entitású transzlokáció B-sejtes leukémiákban elõforduló, hipereozinofiliával társuló rossz prognózisú elváltozás. Az új citogenetikai technikák általánosan elterjedt alkalmazása újabb rejtett rendellenességek feltárását és prognosztikai hatásának a feltérképezését tette lehetõvé. Ilyen például a RUNX1 gént érintõ 21-es kromoszóma intrakromoszómális amplifikációja, mely pre-b immunfenotípussal társuló rossz prognózisú elváltozás. Magas rizikó csoportú kezeléssel is 50% a relapszus kockázata (7). Egy másik hasonlóan rossz prognózisú elváltozás az ABL1-NUP214 fúziós gén extrakromoszomális amplifikációja T-ALL-ben, mely a tirozin kináz aktiválás közelmúltban felfedezett formája és elképzelhetõ, hogy a TKI kezeléssel a negatív prognosztikai hatása mérsékelhetõ. Az AML citogenetikai eltérései Az AML citogenetikai palettája igen gazdag, több mint 200 specifikus számbeli és szerkezeti eltérést ír le a szakirodalom. Egy részük gyakori, másokról csak néhány esetet közöltek. Gyermekkori de novo AML-ben a kóros kariotípus gyakoribb, mint a felnõtteknél és az átrendezõdések elõfordulási gyakorisága is különbözik: bizonyos átrendezõdések kizárólag gyermekkori leukémiához kapcsolódnak. A gyermekkori AML-ben elõforduló fontosabb genetikai eltérések jellemzõit a 2. táblázatban foglaltuk össze. A leggyakoribb jó prognózisú elváltozások a következõk: t(8;21), inv(16)(p13q22), t(16;16)(p13;q22), t(15;17)(q22;q11-12), t(9;11)(p22;q23) (12,23,25,42). A t(8;21) (q22;q22) önálló WHO entitás, a korábbi FAB beosztásban az AML-M2-nek felelt meg. Ez az AML-ben leggyakrabban elõforduló reciprok transzlokáció, a betegek 10-15%-a földrajzi területtõl függõen ezt a transzlokációt hordozza. Gyermekeknél kétszer gyakoribb mint felnõtteknél, de 3 éves kor alatt rendkívül ritka, csecsemõkben eddig még nem azonosították. A transzlokáció során a 21q22 régióban lokalizálható RUNX1 gén runt doménje a 8q22 régióban lokalizálódó ETO gén C-terminus maradványával fuzionál. A 8-as kromoszómán keletkezõ kiméra fehérje domináns negatív hatású a normális RUNX1 allélra és az általa vezérelt target gének transzkripciójára. Társuló rendellenességei közül a legismertebbek: -Y,-X,+8, del(7q),del(9q). A t(8;21) a szekunder rendellenességektõl vagy az esetlegesen társuló komplex kariotípustól függetlenül jó prognózisú elváltozás, jól válaszol a kemoterápiás szerekre és egyedül a magas fehérvérsejt index [fvs csontvelõi blaszt % 20] befolyásolja negatív irányba a túlélési mutatókat (27). A t(15;17)(q22;q21) az APL-nek megfelelõ önálló WHO entitás, a FAB beosztásban az AML-M3-nak felelt meg, átlagosan az AML-ek 10%-ában fordul elõ, csecsemõkben soha. A transzlokáció során a 17q12 régióban Aberráció Prognózisa Molekuláris jellemzõi Incidenciája Ajánlott metodika t(8;21)(q22;q22) LR RUNX1-RUNX1T1 fúzió 10-15% citogenetika, FISH, RT-PCR t(15;17)(q22;q12) LR PML/RARA fúzió 5-10% citogenetika, FISH, RT-PCR inv(16)(p13.1q22) LR CBFb/MYH11 fúzió 3-8% FISH, citogenetika Normális kariotípus HR + FLT3/MLL ITD, PTD 25-30% citogenetika, RT-PCR, FISH t(11q23) HR Hasadt MLL 10-15% citogenetika, FISH 7-es monoszómia HR 2-7% FISH, citogenetika 8-as triszómia önmagában IR nincs 5-10% citogenetika, RT-PCR, FISH Normális kariotípus IR nincs 25-30% citogenetika, RT-PCR, FISH t(9;11) (p22;q23) IR MLLT3-MLL fúziós génnel 5-10% citogenetika, FISH 2. táblázat: A leggyakoribb kiemelt prognosztikai jelentõségû genetikai eltérések vizsgálata gyermekkori AML-ben 14
15 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban található RARA gén fúzionál a 15q22-ben található PML génnel. A PML génnek három különbözõ töréspontja lehet a génen belül, a RARA töréspontja konstans, a gén második intronjában. A 15-ös kromoszómán keletkezõ kiméra gén domináns negatív inhibitor hatású a vad típusú RARA génre, melynek következménye a sejtek érésének gátlása és a differenciálódás promyelocyta fázisban történõ leállítása. A PML-RARA blasztok rendkívül érzékenyek a nagy dózisú ATRA kezelésre, mely képes a sejtek érését elindítani. A transzlokáció néhány ritka esetben maszkírozott lehet, ezért APL gyanú esetén célzott FISH vagy RT-PCR vizsgálat elvégzése elengedhetetlen a genotípuson alapuló specifikus kezelés tervezése érdekében. Az APL esetek 3-5%-ában variáns transzlokációk fordulhatnak elõ egy harmadik, közbeiktatódott kromoszómával, t(15;v;17), vagy egy alternatív RARA-partnergénnel [például a PLZF-, NPM1-, NUMA-génnel a t(11;17)(q23;q21), a t(5;17)(q35;q21) és a t(11;17)(q13;q21) transzlokációk esetében]. A variáns transzlokációs betegek célzott FISH vizsgálattal történõ azonosítása azért fontos, mert az ATRA-ra hatásra rezisztensek és más terápiás algoritmus szerint kell õket kezelni. A társuló rendellenességek közül leggyakoribbak: +8, del(7q), del(9q), melyek nem befolyásolják a kezelés sikerességét. A genotípus specifikus ATRA kezelés alkalmazása megváltoztatta a transzlokáció korábbi rossz prognózisát, a betegek gyógyulási aránya eléri a 70-90%-ot, azonban 10-15%-ukban súlyos, gyakran fatális vérzéssel kapcsolatos szövõdmények lépnek fel (23,42). A 16-os kromoszóma pericentrikus inverziója, inv(16)(p13.1q22) vagy a homologok közti transzlokáció, t(16;16)(p13.1;q22) során a 16q22-ben található CBFB gén a 16p13-ban található MYH11 gén mellé helyezõdik át és a CBFB/MYH11 fúziós gént eredményezi. Ez az önálló WHO entitású, második leggyakoribb átrendezõdés kóros csontvelõi eozinofiliával jellemezhetõ és a gyermekek 3-8%-át érinti, M4-es FAB típushoz társul. A fúziós fehérje csökkenti az aktív CBF mennyiségét és domináns negatív inhibitor hatású a CBFA alegységét képezõ vad típusú RUNX1 génre, amellyel dimerizációs egységet alkot. A társuló rendellenességeknek (+8, +22 (15%), del(7q), +2) általában nincs prognosztikai jelentõsége. A 16-os inverzió és transzlokáció valamennyi altípusban jobb prognózisú elváltozás, a blasztok jól reagálnak a kemoterápiás szerekre, elsõsorban cytarabine kezelésre (19,40). A 16-os kromoszóma átrendezõdése hagyományos citogenetikai technikával nehezen azonosítható, azonban többféle specifikus gyári FISH próba segítheti a szerkezeti rendellenesség pontos feltárását. Ez azért is fontos, mert a 16-os hosszúkar deléció gyenge morfológiájú G-sávos mintázata hasonlíthat az inverzióhoz, viszont prognosztikai hatása sokkal rosszabb a CBFB/MYH11 fúziós génnél. A gyakran társuló 22-es triszómia felhívhatja a figyelmet a 16-os kromoszóma szerkezeti rendellenességére. A t(9;11) (p22;q23)(mll-mllt3(af9) önálló WHO entitás, amelyben az MLL gén az MLLT3 génnel képez fúziót. A gyermekkori AML 6-11%-ában, leggyakrabban FAB M5 típusban elõforduló, a többi MLL átrendezõdésnél bizonyos terápiás protokoll szerinti kezelés esetében valamivel jobb prognózisú (20,33), közepes rizikónak megfelelõ terápiával kezelhetõ elváltozás (42). Ugyanakkor t-aml-ben és társuló anomáliák esetében a prognózisa rosszabb (33). Ez a transzlokáció alacsony sávszámú kromoszómák esetében könnyen elnézhetõ, ezért a hasadt gén kimutatására alkalmas FISH vizsgálat elvégzése ajánlott. Egy másik csecsemõ-, illetve gyermekkorban gyakrabban elõforduló transzlokáció, a t(1;11)(q21;q23) az eddigi irodalmi adatok alapján kivételesen jó prognózist jelent. A többi MLL gént érintõ ismertebb transzlokáció, illetve fúziós gén, mint például t(6;11)(q27;q23)- MLL-MLLT4, t(10;11)(p12;q23)-mll-mllt10, t(11;19) (q23;p13.3)-mll-mllt1, t(11;19)(q23;p13.1)(mll-ell) prognózisa rossz (33). A t(6;9)(p23;q34) a DEK onkogén és a NUP214 gének fúzióját eredményezi, a 2009-es WHO új citogenetikai entitása, igen rossz prognózissal. Minden életkorban elõfordulhat. Jellemzõ rá a több sejtvonalat érintõ dysplasia, bazofil érintettség. G-sávval nehezen diagnosztizálható, variáns transzlokációs formái is ismertek, szekunder anomáliák (+8, +13, +21) az esetek 20%-ában fordulnak elõ (25). A t(1;22)(p13;q13) transzlokáció a 22-es kromoszóma q13 régiójában lokalizálódó MKL1gén és az 1-es kromoszóma RBM15 gének fúzióját eredményezi. Az 1-es kromoszómán keletkezõ kiméra gén kórosan befolyásolja a HOX gének szabályozása alatt álló differenciálódást, a kromatin szervezõdést és az extracellularis jelátviteli utat zavarja meg. Szinte kizárólag a csecsemõkori akut megakaryoblastos leukémiával (FAB-M7) hozható összefüggésbe, egy évesnél nagyobb gyermekekben ritka, a leírt esetek 96%-a két éves kor alatti. Társuló rendellenességek az esetek 40%-ában fordulnak elõ, közülük legismertebb a komplex és/vagy a monomorf mintázatú hiperdiploid kariotípus (+2, +19, +der(1)t(1;22), +6, +21 leggyakoribb triszómiákkal), mely különbözik az ALL-bõl ismert hiperdiploid kariotípustól. Érdekes módon a Down szindrómás gyermekeknél nem azonosították, habár esetükben a megakaryoblastos leukémia az átlagosnál gyakoribb. A transzlokáció rossz prognózissal társul, csak a betegek fele gyógyul meg (3,6,23). Ez a transzlokáció G-sávos analízissel könnyen észrevehetõ, mégis rejtve maradhat a komplex átrendezõdés, az alacsony blasztszám vagy a társuló myelofibrosis miatt. A t(7;12)(q36;p13) a HLXB6 és a többféle leukémiával kapcsolatos ETV6 transzkripciós faktorokat kódoló gének fúzióját eredményezi, a kiméra gén a derivátum 12-es kromoszómán található. Az M3 kivételével valamennyi FAB csoportban azonosították, valamivel gyakrabban a kevésbé differenciált M0 és M1-ben, ez idáig csak 20 hónapos kor alatti csecsemõknél. A csecsemõkori leukémiák második leggyakoribb transzlokációja (41), rossz prognózisú elváltozás. Alacsony sávszámú kromoszómákon nem látható elváltozás, korábban 12p delécióként diagnosztizálták, a FISH korszak 15
16 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban elõtt alulbecsülték a gyakoriságát. A gyakran társuló 19- es triszómia csecsemõkben felhívhatja a figyelmet a rejtett transzlokációra. Hyperdiploid kariotípus lényegesen ritkább a gyermekkori AML-ben mint ALL-ben. Az AML-ben ismert triszómiák gyakorisági sorrendben a következõk: +8, +22, +13, +21, +4. Mindegyik triszómia elsõdleges vagy másodlagos aberráció is lehet. A 8-as triszómia a gyermekkori AML 5-10%-ában fordul elõ, a Down szindrómás gyermekekben incidenciája lényegesen magasabb (27%). Valamennyi FAB-típusban ismert elváltozás, lehet egyedüli anomália vagy társulhat az AML leggyakoribb transzlokációihoz. Nagyon heterogén csoportot képvisel, prognosztikai hatásának a megítélése ellentmondásos. Nagy esetszámú vizsgálatok alapján, ha a jó prognózisú AML specifikus transzlokációival társul, nem befolyásolja negatív irányban a betegség kimenetelét. Ha viszont negatív prognosztikai hatású rendellenességekhez (del(5q),-7) társul, a 8-as triszómia rontja a prognózist (12,16,42). A 8-as triszómia önmagában közepes prognosztikai értékû. Az AML-BFM 98-as protokoll szerint kezelt gyermekek 87%-a remisszióba került (42). Feltételezhetõ, hogy a korábban háttérben maradt molekuláris szintû elváltozások feltárása pontosítani fogja a 8-as triszómia jelentõségét. A többi triszómia lényegesen ritkábban (1-3%) fordul elõ és prognosztikai hatásuk megítélése a többi elváltozás függvényében igen összetett (12). A G-sávos analízis az AML-lel diagnosztizált gyermekek 25%-ában eredményez normális kariotípust. Bár a remissziós ráta alapján standard rizikónak megfelelõ prognosztikai csoportba sorolhatók, molekuláris szinten rendkívül heterogén csoportot képviselnek. Egy kisebb részük specifikus transzlokáció hordozó, de a gyenge kromoszóma morfológia nem teszi lehetõvé azonosításukat. Igen nehezen felismerhetõ aberrációk például a t(11;19), t(9;11), t(15;17), inv(16). A normális kariotípusú betegek nagyobb csoportja fénymikroszkóppal nem detektálható rejtett átrendezõdését csak célzott FISH vizsgálattal lehet identifikálni, például a PML- RARA inszerciós transzlokációt vagy a CBFb/MYH11 fúziós gént. Az esetek egy részében in vitro körülmények között a kóros elváltozást hordozó blasztok nem osztódnak és a kromoszóma aberrációk csak az interfázis magokban láthatóak. A szerzett genetikai eltérések nagy csoportja csak molekuláris genetikai vizsgálattal azonosítható. AML-re jellemzõ gyakori eltérések az FLT3 receptor tirozin kináz és MLL gének tandem duplikációi (ITD- FLT3 és PTD-MLL), az N-RAS, KIT, RUNX1, FLT3 gének pontmutációi vagy az EVI1 gén fokozott expressziója. Érthetõ, hogy a normális kariotípusú betegek FISH vagy/és RT-PCR vizsgálata elengedhetetlen (26). A rossz kórjóslattal társuló elváltozások a gyermekekben ritkábban fordulnak elõ, ezek többnyire kiegyensúlyozatlan számbeli és szerkezeti elváltozások vagy több kromoszómát érintõ komplex átrendezõdések. A legismertebbek a következõk: -7/7q-, del(12p), del(17), inv(3)(q21q26), t(3;3) (q21;q26). A hypodiploid kariotípus általában nem rosszabb prognózisú az AML prognózisának átlagánál, még akkor sem, ha több kromoszómát érint a monoszómia (23,42). Kivételt képez a gyermekkori AML 2-7%-ában elõforduló 7-es monoszómia, mely negatív prediktív értékû elváltozás valamennyi FAB típusban, az 5 éves túlélés csak 39%. A 7-es monoszómia gyakoribb sugár vagy alkiláló szerekkel történõ kezelést követõen jelentkezõ t-aml-ben és az olyan MDS/AML-ben, mely valamilyen hajlamosító szindrómával hozható összefüggésbe (Fanconi anaemia, Kostmann szindróma, I. típusú neurofibromatosis, Down szindróma, familiáris 7-es monoszómia). Azok a betegek, akikben a 7-es monoszómia más rendellenességekhez csatlakozik, mint például inv(3)/t(3;3), t(9;22), i(17q),-5/del(5q), rendkívül rosszul válaszolnak a kemoterápiás szerekre, az 5 éves túlélésük csupán 5%. A 7q deléció egyedüli anomáliaként közepes prognosztikai hatású, de a t(8;21), t(15;17), inv (16)-hoz társulva, nem rontja le ezen elváltozások jó prognosztikai kimenetelét (14). A 12-es kromoszóma rövid kar átrendezõdései valamennyi citogenetikai csoportnál rosszabb prognózisúak, náluk a legmagasabb az ismételt relapszus incidenciája (78%) (12,42). A 3q21 és 3q26 töréspontokat egy idõben érintõ szerkezeti rendellenességek [inv(3)(q21q26), t(3;3)(q21;q26), ins(3)(q26;q21q26)], melyeket 3q21q26 szindrómaként ismer a szakirodalom, igen rossz prognózissal hozhatók összefüggésbe, akárcsak más 3q26 töréspontú transzlokációk, melyek az EVI1 transzkripciós faktor fokozott expresszióját eredményezik. Ennek az átrendezõdés típusnak a kimutatása azért fontos, mert a betegek a konvencionális kemoterápiás szerekre kevéssé reagálnak, ezért õssejt-transzplantációban kell õket részesíteni (9,22). Gyermekek esetében ritkán találkozunk a három vagy annál több kromoszómát érintõ komplex kariotípussal, valamivel gyakrabban a három éves kor alatti gyermekeknél. A komplex kariotípus általában bizonytalan kimenetelû leukémiát jellemez. Különösen akkor társul rossz prognózissal, ha 5q és 17p (TP53) delécióval jár együtt és 7-es monoszómia is szerepel a rendellenességek között. Érdekes módon, ha a komplex kariotípusban a jó prognosztikai értékû AML-specifikus transzlokációk is szerepelnek, ezek hatása érvényesül (12,34,42). Összegzés Az utóbbi idõben felfedezett aberrációk alapján arra lehet számítani, hogy nemsokára valamennyi leukémiás beteget a genetikai rendellenessége alapján lehet megfelelõ rizikó csoportba sorolni, ami a kemoterápiás szövõdmények csökkenését és a betegek életminõségének a javulását eredményezi. Az új típusú rendellenességek molekuláris szintû elváltozásai terápiás célpontként is szolgálhatnak, felhasználhatók korszerûbb gyógyszerek fejlesztésére. 16
17 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban Irodalomjegyzék 1. Alexander F.E., Patheal S.L., Biondi A. et al.: Transplacental chemical exposure and risk of infant leukemia with MLL gene fusion. Cancer Res., 61, , Armstrong S.A., Staunton J.E., Silverman L.B. et al.: MLL translocations specify a distinct gene expression profile that distinguishes a unique leukemia. Nat. Genet., 30, 41-47, Balgobind B.V., Raimondi S.C., Harbott J. et al.: Novel prognostic subgroups in childhood 11q23/MLLrearranged acute myeloid leukemia: Results of an international retrospective study. Blood, 114, , Bernstein J., Dastugue N., Haas O.A. et al.: Nineteen cases of the t(1;22)(p13;q13) acute megakaryoblastic leukaemia of infants/children and a review of 39 cases: report from a t(1;22) study group. Leukemia, 14, , DiMartino J.F., Cleary M.L.: Mll rearrangements in haematological malignancies: lessons from clinical and biological studies. Br. J. Haematol., 106, , Forestier E., Izraeli S., Beverloo B. et al.: Cytogenetic features of acute lymphoblastic and myeloid leukemias in pediatric patients with Down syndrome: an ibfm-sg study. Blood, 111, , Haltrich I., Csóka M., Kovács G. et al.: AML1-gén intrakromoszomális amplifikációja gyermekkori acut lymphoid leukémiában. Orv. Hetil., 149, , Haltrich I., Csóka M., Kovács G. et al.: A hagyományos citogenetika és a FISH egymást jól kiegészítõ vizsgálatok gyermekkori akut limfoid leukémiában. Magy. Onkol., 52, , Haltrich I., Kost-Alimova M., Kovács G. et al.: A 3q21q26 szindróma azonosítása sokpontosinterfázis-fish vizsgálattal gyermekkori myeloid leukémiában. Magy. Onkol., 49, , Harrison C.J.: Cytogenetics of paediatric and adolescent acute lymphoblastic leukaemia. Br. J. Haematol., 144, , Harrison C.J., Haas O., Harbott J.: Detection of prognostically relevant genetic abnormalities in childhood B-cell precursor acute lymphoblastic leukaemia: recommendations from the Biology and Diagnosis Committee of the International Berlin- Frankfurt-Münster study group. Br. J. Haematol., 151, , Harrison C.J., Hills R.K., Moorman A.V. et al.: Cytogenetics of childhood acute myeloid leukemia: United Kingdom Medical Research Council Treatment trials AML 10 and 12. J. Clin. Oncol., 28, , Harrison C.J., Moorman A.V., Barber K.E. et al.: Interphase molecular cytogenetic screening for chromosomal abnormalities of prognostic significance in childhood acute lymphoblastic leukaemia: a UK Cancer Cytogenetics Group Study. Br. J. Haematol., 129, , Hasle H., Alonzo T.A., Auvrignon A. et al.: Monosomy 7 and deletion 7q in children and adolescents with acute myeloid leukemia: an international retrospective study.blood, 109, , Heisterkamp N., Stam K., Groffen J. et al.: Structural organization of the bcr gene and its role in the Ph translocation. Nature, 315, , Jaff N., Chelghoum Y., Elhamri M. et al.: Trisomy 8 as sole anomaly or with other clonal aberrations in acute myeloid leukemia: impact on clinical presentation and outcome. Leuk. Res., 31, 67-73, Jaso J., Thomas D.A., Cunningham K. et al.: Prognostic significance of immunophenotypic and karyotypic features of philadelphia positive B-lymphoblastic leukemia in the era of tyrosine kinase inhibitors. Cancer, 1-9, Johansson B., Moorman A.V., Haas O.A. et al.: Hematologic malignancies with t(4;11)(q21;q23) a cytogenetic, morphologic, immunophenotypic and clinical study of 183 cases. European 11q23 Workshop participants. Leukemia, 12, , Lengfelder E., Haferlach C., Saussele S. et al.: German AML Cooperative Group. High dose ara-c in the treatment of newly diagnosed acute promyelocytic leukemia: long-term results of the German AMLCG. Leukemia, 23, , Lie S.O., Abrahamsson J., Clausen N. et al.: Long-term results in children with AML: NOPHOAML Study Group-Report of three consecutive trials. Leukemia, 19, , Loh M.L., Goldwasser M.A., Silverman L.B. et al.: Prospective analysis of TEL/AML1-positive patients treated on Dana-Farber Cancer Institute Consortium Protocol Blood, 107, , Lugthart S., Gröschel S., Beverloo H.B. et al.: Clinical, molecular, and prognostic significance of WHO type inv(3)(q21q26.2)/t(3;3)(q21;q26.2) and various other 3q abnormalities in acute myeloid leukemia. J. Clin. Oncol., 28, , Manola K.N.: Cytogenetics of pediatric acute myeloid leukemia. Eur. J. Haematol., 83, , McLean T.W., Ringold S., Neuberg D. et al.: TEL/AML- 1 dimerizes and is associated with a favorable outcome in childhood acute lymphoblastic leukemia. Blood, 88, , Mitelman Database of Chromosome Aberrations and Gene Fusions in Cancer (2011). Mitelman F., Johansson B., and Mertens F. (Eds.), nih.gov/chromosomes/mitelman 26. Mrózek K., Radmacher M.D., Bloomfield C.D. et al.: Molecular signatures in acute myeloid leukemia. Curr. Opin. Hematol., 16, 64-69, Nguyen S., Leblanc T., Fenaux P. et al.: A white blood cell index as the main prognostic factor in t(8;21) acute myeloid leukemia (AML): a survey of 161 cases from the French AML Intergroup. Blood, 99, , Paulsson K., Forestier E., Lilljebjörn H. et al.: Genetic landscape of high hyperdiploid childhood acute 17
18 Korszerû citogenetikai vizsgálatok jelentõsége a gyermekkori leukémiákban lymphoblastic leukemia. Proc. Natl. Acad. Sci. USA., 107, , Pui C.H.: Recent research advances in childhood acute lymphoblastic leukemia. J. Formos. Med. Assoc., 109, , Pui C.H., Evans E.W.: Treatment of Acute Lymphoblastic Leukemia. N. Engl. J. Med., 354, , Raimondi S.C, Zhou Y., Shurtleff S.A. et al.: Neartriploidy and near-tetraploidy in childhood acute lymphoblastic leukemia: association with B-lineage blast cells carrying the ETV6-RUNX1 fusion, T- lineage immunophenotype, and favorable outcome. Cancer Genet. Cytogenet., 169, 50-57, Rowley J.D.: A new consistent chromosomal abnormality in chronic myelogenous leukaemia identified by quinacrine fluorescence and Giemsa staining. Nature, 243, , Rubnitz J.E., Raimondi S.C., Tong X. et al.: Favorable impact of the t(9;11) in childhood acute myeloid leukemia. J. Clin. Oncol., 20, , Schoch C., Kern W., Kohlmann A. et al.: Acute myeloid leukemia with a complex aberrant karyotype is a distinct biological entity characterized by genomic imbalances and a specific gene expression profile. Gen. Chrom. Cancer, 43, , Schultz K.R., Pullen D.J., Sather H.N. et al.: Risk- and response-based classification of childhood B- precursor acute lymphoblastic leukemia: a combined analysis of prognostic markers from the Pediatric Oncology Group (POG) and Children s Cancer Group (CCG). Blood, 109, , Seeger K., von Stackelberg A., Taube T. et al.: Relapse of TEL-AML1-positive acute lymphoblastic leukemia in childhood: a matched-pair analysis. J. Clin. Oncol., 19, , Sutcliffe M.J., Shuster J.J., Sather H.N. et al.: High concordance from independent studies by the Children s Cancer Group (CCG) and Pediatric Oncology Group (POG) associating favorable prognosis with combined trisomies 4, 10, and 17 in children with NCI Standard-Risk B-precursor Acute Lymphoblastic Leukemia: a Children s Oncology Group (COG) initiative. Leukemia, 19, , Szczepañski T., Harrison Ch.J., van Dongen J.J.M.: Genetic aberrations in paediatric acute leukaemias and implications for management of patients. Lancet Oncol., 11, , Thomas D.A.: Philadelphia chromosome positive acute lymphocytic leukemia: a new era of challenges. Hematol. Am. Soc. Hematol. Educ. Program, , Tosi P., Visani G., Ottaviani E. et al.: Inv(16) acute myeloid leukemia cells show an increased sensitivity to cytosine arabinoside in vitro. Eur. J. Haematol., 60, , von Bergh A.R., van Drunen E., van Wering E.R. et al.: High incidence of t(7;12)(q36;p13) in infant AML but not in infant ALL, with a dismal outcome and ectopic expression of HLXB9. Gen. Chrom. Cancer, 45, , von Neuhoff C., Reinhardt D., Sander A. et al.: Prognostic impact of specific chromosomal aberrations in a large group of pediatric patients with acute myeloid leukemia treated uniformly according to trial AML-BFM 98. J. Clin. Oncol., 28, ,
19 A gyermekonkológiai kezelések aktuális problémái: terápia, szupportáció Dr. Garami Miklós A gyermekonkológiai kezelések aktuális problémái: terápia, szupportáció Semmelweis Egyetem, II. sz. Gyermekgyógyászati Klinika, Budapest Összefoglalás: A Magyar Gyermekonkológusok és Gyermekhematológusok Társasága (MGYGYT), mint a Gyermekleukémia Terápiás Munkacsoport jogutódja, 1971 óta valósítja meg a gyermekkori leukémiás és daganatos betegek szisztematikus regisztrálását, egységes kivizsgálását, gyógykezelését, gondozását és utánkövetését. Így optimális feltételeket biztosít a korlátozott anyagi erejû, közel 10 milliós ország gyermeknépessége számára, amelyet (15 éves kor alatt) egy lassan, de szignifikánsan emelkedõ, 132/millió gyermekrák-incidencia jellemez. Az évente mintegy 250 újonnan kórismézett beteget és az egyre növekvõ számú remisszióba kerülõ, illetõleg tartós remisszióban, rosszindulatú betegségébõl gyógyultan élõ gyermeket 7 központban, 2 transzplantációs központban és 1 rehabilitációs intézményben kezeljük, gondozzuk, korszerû konszenzus-protokollok alkalmazásával. A MGYGYT számos bilaterális és multicentrikus nemzetközi tudományos és klinikai együttmûködésben vesz részt, a nemzetközi gyermekhematológiai-onkológiai társadalom integráns részévé vált. A MGYGYT tagjainak erõfeszítése révén napjainkban a rosszindulatú megbetegedésekben szenvedõ gyermekek hazánkban hasonló gyógyulási arányra, hasonló életminõségre számíthatnak, mint egyéb fejlett ipari országokban. Kulcsszavak: gyermekonkológia, Országos Gyermektumor Regiszter, szupportív terápia, életminõség Gyermekkori malignus megbetegedések epidemiológiája Európában éven aluli gyermekre mintegy újonnan diagnosztizált malignus megbetegedés jut (12,22,24,23). A gyermekkori rosszindulatú daganatos megbetegedések számos tekintetben eltérnek a felnõttkori kórképektõl. Az egyik legfeltûnõbb különbség a malignus betegségek eltérõ spektruma (1. ábra). Egyes, a felnõttkorban tömegesen elõforduló kórképek, mint például az emlõ, a hörgõ, a gyomor-bél traktus, a prostata és az uterus rosszindulatú daganatai a gyermekkorban irodalmi ritkaságnak tekinthetõk, míg más daganatos betegségek, így a retinoblastoma, a neuroblastoma, a Wilms-tumor felnõttkori manifesztációja kivételes. Gyermekkorban az agydaganatok a leggyakoribb szolid tumorok. A sajátos különbség abban is megnyilvánul, hogy azonos szövettani, citológiai megjelenés esetében is eltérõ lehet egyes kórképek kórlefolyása a gyermekkorban és a felnõttkorban. Így a két jellegzetes életkori halmozódást kora gyermekkorit és idõs felnõttkorit mutató akut lymphoblastos leukaemia kórjóslata ma már kedvezõnek tartható az ifjabb, míg továbbra is elkeserítõ az idõsebb korcsoportban. Hason- Summary: The Association of Hungarian Pediatric Oncologists and Hematologists (AHPOH) as successor of the Childhood Leukemia Working Group has systemized registration, diagnosis, treatment and follow-up of children with leukemia and solid tumors since AHPOH has developed a uniform, nation-wide pediatric oncology service in Hungary, a country with ten million inhabitants and limited economic resources characterized by a slowly but significantly growing annual cancer incidence of 132 per one million children (below the age of 15 years). The newly diagnosed about 250 patients are being treated according to contemporary protocols and they are followed-up together with the enhancing numbers of children having cured from cancer in 7 centers, 2 hematopoietic stem cell transplantation units and in 1 rehabilitation facilities. AHPOH became an integral part of the international pediatric oncology community. As a result of the coordinated efforts of the members of AHPOH, children with cancer in Hungary experience overall and event-free survival rates similar to that of other industrialized countries. Keywords: pediatric oncology, National Pediatric Cancer Registry, supportive treatment, quality of life (QoL) ló, bár kevésbé kifejezett különbséget tapasztalhatunk a lymphomák és a lágyrészsarcomák vonatkozásában. Mindezek a különbségek azt eredményezik, hogy a gyermekkor rosszindulatú betegségeinek mintegy kétharma- 1. ábra: Gyermekkori malignitások N=2260, 0-14 évesek ( ) (OSC: osteosarcoma, HD: Hodgkin kór, NHL: non-hodgkin lymphoma, KIR: központi idegrendszeri daganat, NBL: neuroblastoma, RBL: retinoblastoma) Forrás: Országos Gyermektumor Regiszter 19
20 A gyermekonkológiai kezelések aktuális problémái: terápia, szupportáció da eredményesen kezelhetõ, azaz a gyermekbetegek többsége tartós, visszaesésmentes túlélésre számíthat (2-5. ábrák)(2,3,26) Time (years) 5. ábra: Gyermekkori Wilms-tumoros betegek túlélési görbéje (N=402, ) Forrás: Országos Gyermektumor Regiszter 2. ábra: Gyermekkori agydaganatos betegek túlélési görbéje (N=1676, ) Forrás: Országos Gyermektumor Regiszter ábra: Gyermekkori leukémiás betegek túlélési görbéje (N=2662, ) Forrás: Országos Gyermektumor Regiszter Time (years) Time (years) Gyermekonkológiai ellátás szervezeti felépítése A gyermekonkológiai ellátás országosan egységes létrehozása (1971: Magyar Gyermekleukémia Terápiás Munkacsoport; jelenleg: Magyar Gyermekorvosok Társasága Gyermekonkológiai Szekciója (GYOSZ); jogi forma: Magyar Gyermekonkológusok és Gyermekhematológusok Társasága, MGYGYT) az ország korlátozott gazdasági lehetõségeinek ellenére is gyors és folyamatos javulást eredményezett a hazai gyermekkori rosszindulatú megbetegedések körében (9,18,24,23). Az MGYGYT 7 betegellátó központ, 2 transzplantációs központ és 1 rehabilitációs központ mûködését hangolja össze. Az ország földrajzi sajátosságának megfelelõen a betegellátó központok közül 2 a fõvárosban, további 1-1 Miskolcon (Észak-Magyarország), Debrecenben (Észak-Alföld), Szegeden (Dél-Alföld), Pécsett (Dél- Dunántúl) és Szombathelyen (Nyugat-Dunántúl) mûködnek. Ez a hálózat figyelembe veszi az ország egyes régióinak népsûrûségét és jól szervezett betegszállító szolgáltatók igénybevételével egy órán belül elérhetõ, teljes körû betegellátást biztosít. A centrumok egyetemi környezetben, vagy nagy kórházak gyermekgyógyászati osztályainak részeként akkreditált, minõségellenõrzött körülmények között mûködnek. A központok, illetõleg a központokat mûködtetõ intézmények rendelkeznek a korszerû kezelés feltételeivel: korszerû laboratóriumi és képalkotó diagnosztika, intenzív betegellátó osztály, sebészeti és sugárterápiás ellátás, amelyek, onko-team formájában együttmûködve, biztosítják a korszerû betegellátást (7,18). Gyermekonkológiai kezelések, szupportáció Time (years) 4. ábra: Gyermekkori Hodgkin-kóros betegek túlélési görbéje (N=404, ) Forrás: Országos Gyermektumor Regiszter A gyermekkori daganatok természete, még inkább a gyermekkor sajátosságai érthetõvé teszik, hogy a gyermekonkológia elsõdleges célja a teljes gyógyulás elõsegítése. Ezt a célt, mai tudásunk szerint, kizárólag a da- 20
Tartalomjegyzék FOCUS MEDICINAE
 FOCUS MEDICINAE Felelõs szerkesztõ: Dr. Szolnoky Miklós Fõszerkesztõ: Dr. Karabélyos Csaba Szerkesztõbizottság: Dr. Bencsik Krisztina Prof. Czirják László Prof. Horváth Örs Péter Dr. Kalmár Ágnes Dr. Mátrai
FOCUS MEDICINAE Felelõs szerkesztõ: Dr. Szolnoky Miklós Fõszerkesztõ: Dr. Karabélyos Csaba Szerkesztõbizottság: Dr. Bencsik Krisztina Prof. Czirják László Prof. Horváth Örs Péter Dr. Kalmár Ágnes Dr. Mátrai
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
Kryoglobulinaemia kezelése. Domján Gyula. Semmelweis Egyetem I. Belklinika. III. Terápiás Aferezis Konferencia, 2014. Debrecen
 Kryoglobulinaemia kezelése Domján Gyula Semmelweis Egyetem I. Belklinika Mi a kryoglobulin? Hidegben kicsapódó immunglobulin Melegben visszaoldódik (37 C-on) Klasszifikáció 3 csoport az Ig komponens
Kryoglobulinaemia kezelése Domján Gyula Semmelweis Egyetem I. Belklinika Mi a kryoglobulin? Hidegben kicsapódó immunglobulin Melegben visszaoldódik (37 C-on) Klasszifikáció 3 csoport az Ig komponens
IMMUNOLÓGIA VILÁGNAP 2012. április 26 Prof. Dr. Dankó Katalin DEOEC III. Belklinika Klinikai Immunológiai Tanszék
 A reumatológiai/gyulladásos betegségek felismerése és szövődményei IMMUNOLÓGIA VILÁGNAP 2012. április 26 Prof. Dr. Dankó Katalin DEOEC III. Belklinika Klinikai Immunológiai Tanszék Gyulladásos betegségek
A reumatológiai/gyulladásos betegségek felismerése és szövődményei IMMUNOLÓGIA VILÁGNAP 2012. április 26 Prof. Dr. Dankó Katalin DEOEC III. Belklinika Klinikai Immunológiai Tanszék Gyulladásos betegségek
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Kappelmayer János. Malignus hematológiai megbetegedések molekuláris háttere. MOLSZE IX. Nagygyűlése. Bük, 2005 szeptember
 Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Az intravénás immunglobulin hatásmechanizmusa és alkalmazási köre a klinikai immunológiában
 Az intravénás immunglobulin hatásmechanizmusa és alkalmazási köre a klinikai immunológiában Dr. Bazsó Anna ORFI Klinikai Immunológiai, Felnőtt-és Gyermekreumatológiai Osztály Haladás a reumatológia, immunológia
Az intravénás immunglobulin hatásmechanizmusa és alkalmazási köre a klinikai immunológiában Dr. Bazsó Anna ORFI Klinikai Immunológiai, Felnőtt-és Gyermekreumatológiai Osztály Haladás a reumatológia, immunológia
Prof Dr. Pajor Attila Szülész-nőgyógyász, egyetemi tanár AUTOIMMUN BETEGSÉGEK ÉS TERHESSÉG
 Prof Dr. Pajor Attila Szülész-nőgyógyász, egyetemi tanár AUTOIMMUN BETEGSÉGEK ÉS TERHESSÉG Melyik autoimmun betegség érinti a szülőképes nőket? Izületi betegségek : RA, SLE Pajzsmirigy betegségek: Kevert
Prof Dr. Pajor Attila Szülész-nőgyógyász, egyetemi tanár AUTOIMMUN BETEGSÉGEK ÉS TERHESSÉG Melyik autoimmun betegség érinti a szülőképes nőket? Izületi betegségek : RA, SLE Pajzsmirigy betegségek: Kevert
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
LUPUSZ KVÍZ. Kérdések, megoldások, ajándéksorsolás. 2012. december 1.
 LUPUSZ KVÍZ Kérdések, megoldások, ajándéksorsolás 2012. december 1. 1. kérdés: Mi történik egy lupuszos beteg immunrendszerében? A Az immunrendszer túl kevés antitestet termel. B Az immunrendszer antitesteket
LUPUSZ KVÍZ Kérdések, megoldások, ajándéksorsolás 2012. december 1. 1. kérdés: Mi történik egy lupuszos beteg immunrendszerében? A Az immunrendszer túl kevés antitestet termel. B Az immunrendszer antitesteket
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
Terhesség immunológiai vonatkozásai. Dr. Kovács László SZTE ÁOK Reumatológiai Klinika Immunológiai Alapok Tanfolyam Szeged, október 2-3.
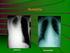 Terhesség immunológiai vonatkozásai Dr. Kovács László SZTE ÁOK Reumatológiai Klinika Immunológiai Alapok Tanfolyam Szeged, 2014. október 2-3. Az immunrendszer terhességben Magzat: szemiallograft Th1/Th2/Th17
Terhesség immunológiai vonatkozásai Dr. Kovács László SZTE ÁOK Reumatológiai Klinika Immunológiai Alapok Tanfolyam Szeged, 2014. október 2-3. Az immunrendszer terhességben Magzat: szemiallograft Th1/Th2/Th17
Dr. Bazsó Anna. Magyar Lupus Egyesület
 Autoimmun betegségek társulása Dr. Bazsó Anna Magyar Lupus Egyesület 2010.03.27. Az autoimmun betegségek evolúciója és etiopathogenesise Genetikai háttér Beningnus Patológiás Immunszerológiai Autoimmunitás
Autoimmun betegségek társulása Dr. Bazsó Anna Magyar Lupus Egyesület 2010.03.27. Az autoimmun betegségek evolúciója és etiopathogenesise Genetikai háttér Beningnus Patológiás Immunszerológiai Autoimmunitás
Szisztémás autoimmun betegségek: a kezelés és gondozás elvei Dr Szűcs Gabriella
 Szisztémás autoimmun betegségek: a kezelés és gondozás elvei Dr Szűcs Gabriella DEOEC Reumatológiai Tanszék Szisztémás autoimmun betegségek Tünetek diagnózis Szervi manifesztációk, stádium felmérése Prognosztikai
Szisztémás autoimmun betegségek: a kezelés és gondozás elvei Dr Szűcs Gabriella DEOEC Reumatológiai Tanszék Szisztémás autoimmun betegségek Tünetek diagnózis Szervi manifesztációk, stádium felmérése Prognosztikai
A DE KK Belgyógyászati Klinika Intenzív Osztályán és Terápiás Aferezis Részlegén évi közel 400 db plazmaferezis kezelést végzünk.
 A DE KK Belgyógyászati Klinika Intenzív Osztályán és Terápiás Aferezis Részlegén évi közel 400 db plazmaferezis kezelést végzünk. Az eseteink túlnyomó részét neuro-, immunológiai eredetű kórképek adják.
A DE KK Belgyógyászati Klinika Intenzív Osztályán és Terápiás Aferezis Részlegén évi közel 400 db plazmaferezis kezelést végzünk. Az eseteink túlnyomó részét neuro-, immunológiai eredetű kórképek adják.
Hepatitis C vírus és cryoglobulinaemia
 Hepatitis C vírus és cryoglobulinaemia Dr Petrovicz Edina 2012.11.10. ESZISZL Kh. és Rendelőintézet Hepatitis C vírus (HCV) Flaviviridae család Hepacivirus nemzetség egyszálú RNS vírus Choo és Kuo 1989.
Hepatitis C vírus és cryoglobulinaemia Dr Petrovicz Edina 2012.11.10. ESZISZL Kh. és Rendelőintézet Hepatitis C vírus (HCV) Flaviviridae család Hepacivirus nemzetség egyszálú RNS vírus Choo és Kuo 1989.
PDF Compressor Pro. Dr Petrovicz Edina.április.
 Dr Petrovicz Edina.április. Az immunrendszer feladata Saját és idegen felismerése Kórokozó mikroorganizmusok elleni védekezés A szervezet saját, megváltozott sejtjeinek a felismerése, eliminálása Az immunrendszer
Dr Petrovicz Edina.április. Az immunrendszer feladata Saját és idegen felismerése Kórokozó mikroorganizmusok elleni védekezés A szervezet saját, megváltozott sejtjeinek a felismerése, eliminálása Az immunrendszer
Autoimmun betegségek nefrológiai manifesztációi. Dr. Studinger Péter SEMMELWEIS EGYETEM. Általános Orvostudományi Kar
 Autoimmun betegségek nefrológiai manifesztációi Dr. Studinger Péter 2019. SEMMELWEIS EGYETEM Általános Orvostudományi Kar Semmelweis Egyetem I. sz. Belgyógyászati Klinika http://bel1.semmelweis.hu A nefrológiai
Autoimmun betegségek nefrológiai manifesztációi Dr. Studinger Péter 2019. SEMMELWEIS EGYETEM Általános Orvostudományi Kar Semmelweis Egyetem I. sz. Belgyógyászati Klinika http://bel1.semmelweis.hu A nefrológiai
KÉT ÉVTIZED EREDMÉNYEI ANCA- ASSZOCIÁLT VASCULITISBEN SZENVEDŐ BETEGEINK KOMPLEX IMMUNSZUPPRESSZÍV KEZELÉSE KAPCSÁN
 KÉT ÉVTIZED EREDMÉNYEI ANCA- ASSZOCIÁLT VASCULITISBEN SZENVEDŐ BETEGEINK KOMPLEX IMMUNSZUPPRESSZÍV KEZELÉSE KAPCSÁN Dr Haris Ágnes 1, Dr Polner Kálmán 1, Dr Arányi József 1, Dr Braunitzer Henrik 1, Bakonyvári
KÉT ÉVTIZED EREDMÉNYEI ANCA- ASSZOCIÁLT VASCULITISBEN SZENVEDŐ BETEGEINK KOMPLEX IMMUNSZUPPRESSZÍV KEZELÉSE KAPCSÁN Dr Haris Ágnes 1, Dr Polner Kálmán 1, Dr Arányi József 1, Dr Braunitzer Henrik 1, Bakonyvári
NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú
 NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú meghatározása. (Megj.: a felsorolt esetekben meghatározó
NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú meghatározása. (Megj.: a felsorolt esetekben meghatározó
BETEGTÁJÉKOZTATÓ RHEUMATOID ARTHRITISBEN SZENVEDŐ BETEGEK SZÁMÁRA I. RHEUMATOID ARTHRITIS. origamigroup. www.origami.co.hu
 BETEGTÁJÉKOZTATÓ RHEUMATOID ARTHRITISBEN SZENVEDŐ BETEGEK SZÁMÁRA I. RHEUMATOID ARTHRITIS origamigroup www.origami.co.hu I. Rheumatoid arthritis Sokat hallunk napjainkban az immunrendszernek az egészség
BETEGTÁJÉKOZTATÓ RHEUMATOID ARTHRITISBEN SZENVEDŐ BETEGEK SZÁMÁRA I. RHEUMATOID ARTHRITIS origamigroup www.origami.co.hu I. Rheumatoid arthritis Sokat hallunk napjainkban az immunrendszernek az egészség
A köpenysejtes limfómákról
 A köpenysejtes limfómákról Dr. Schneider Tamás Országos Onkológiai Intézet Lymphoma Centrum Limfóma Világnap 2014. szeptember 15. Limfómám van! Limfómám van! Igen? De milyen típusú? Gyógyítható? Nem gyógyítható?
A köpenysejtes limfómákról Dr. Schneider Tamás Országos Onkológiai Intézet Lymphoma Centrum Limfóma Világnap 2014. szeptember 15. Limfómám van! Limfómám van! Igen? De milyen típusú? Gyógyítható? Nem gyógyítható?
Semmelweis Egyetem VIII. Infektológiai Továbbképző Tanfolyam
 2015. március 20 21. Fókuszban az antibiotikum terápia PROGRAM 2015. MÁRCIUS 20. PÉNTEK 07.30 09.00 Regisztráció 09.00 09.30 Antibiotikum kezelés jelene és jövője 09.30 10.00 10.00 10.30 Prof. Dr. Ludwig
2015. március 20 21. Fókuszban az antibiotikum terápia PROGRAM 2015. MÁRCIUS 20. PÉNTEK 07.30 09.00 Regisztráció 09.00 09.30 Antibiotikum kezelés jelene és jövője 09.30 10.00 10.00 10.30 Prof. Dr. Ludwig
A TELJES SZÍV- ÉS ÉRRENDSZERI RIZIKÓ ÉS CSÖKKENTÉSÉNEK LEHETŐSÉGEI
 A TELJES SZÍV- ÉS ÉRRENDSZERI RIZIKÓ ÉS CSÖKKENTÉSÉNEK LEHETŐSÉGEI Dr. Páll Dénes egyetemi docens Debreceni Egyetem OEC Belgyógyászati Intézet A HYPERTONIA SZÖVŐDMÉNYEI Stroke (agykárosodás) Szívizom infarktus
A TELJES SZÍV- ÉS ÉRRENDSZERI RIZIKÓ ÉS CSÖKKENTÉSÉNEK LEHETŐSÉGEI Dr. Páll Dénes egyetemi docens Debreceni Egyetem OEC Belgyógyászati Intézet A HYPERTONIA SZÖVŐDMÉNYEI Stroke (agykárosodás) Szívizom infarktus
Egyénre szabott terápiás választás myeloma multiplexben
 Egyénre szabott terápiás választás myeloma multiplexben Dr. Mikala Gábor Főv. Önk. Egy. Szt István és Szent László Kórház Haematológiai és Őssejt-Transzplantációs Osztály Mit kell tudni a myelomáról? Csontvelőből
Egyénre szabott terápiás választás myeloma multiplexben Dr. Mikala Gábor Főv. Önk. Egy. Szt István és Szent László Kórház Haematológiai és Őssejt-Transzplantációs Osztály Mit kell tudni a myelomáról? Csontvelőből
Klinikai Immunológiai Interdiszciplináris Fórum II. (KIIF)
 Klinikai Immunológiai Interdiszciplináris Fórum II. (KIIF) 2011.11.10 2011.11.12. Hotel Divinus, Debrecen Főszervező: Prof. Dr. Zeher Margit A Magyar Allergológiai és Klinikai Immunológiai Társaság és
Klinikai Immunológiai Interdiszciplináris Fórum II. (KIIF) 2011.11.10 2011.11.12. Hotel Divinus, Debrecen Főszervező: Prof. Dr. Zeher Margit A Magyar Allergológiai és Klinikai Immunológiai Társaság és
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
30 év tapasztalata a TTP-HUS kezelésében
 30 év tapasztalata a TTP-HUS kezelésében Dr.Réti Marienn Egyesített Szent István és Szent László Kórház Hematológia és Őssejt-transzplantációs Osztály Thrombotikus mikroangiopathiák ENDOTHEL INFEKCIÓK:
30 év tapasztalata a TTP-HUS kezelésében Dr.Réti Marienn Egyesített Szent István és Szent László Kórház Hematológia és Őssejt-transzplantációs Osztály Thrombotikus mikroangiopathiák ENDOTHEL INFEKCIÓK:
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. szeptember 15. 1 1. Azonosítószám:
A krónikus myeloid leukémia kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. szeptember 15. 1 1. Azonosítószám:
XVI. Pécsi Reumatológus Rezidens és Szakorvosjelölt Fórum
 A Magyar Reumatológusok Egyesülete és az Immunológiai Reumatológiai és Rehabilitációs Egyesület szervezésében: XVI. Pécsi Reumatológus Rezidens és Szakorvosjelölt Fórum 2018. április 13-14. A rendezvény
A Magyar Reumatológusok Egyesülete és az Immunológiai Reumatológiai és Rehabilitációs Egyesület szervezésében: XVI. Pécsi Reumatológus Rezidens és Szakorvosjelölt Fórum 2018. április 13-14. A rendezvény
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán
 A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán Doktori értekezés tézisei Dr. Mayer László Semmelweis Egyetem Mentális Egészségtudományok
A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán Doktori értekezés tézisei Dr. Mayer László Semmelweis Egyetem Mentális Egészségtudományok
Laktózfelszívódási zavar egy gyakori probléma gyakorlati vonatkozásai
 Laktózfelszívódási zavar egy gyakori probléma gyakorlati vonatkozásai Karoliny Anna dr., B.Kovács Judit dr. Gasztroenterológiai és Nephrológiai Osztály, Heim Pál Gyermekkórház, Budapest (Igazgató: Nagy
Laktózfelszívódási zavar egy gyakori probléma gyakorlati vonatkozásai Karoliny Anna dr., B.Kovács Judit dr. Gasztroenterológiai és Nephrológiai Osztály, Heim Pál Gyermekkórház, Budapest (Igazgató: Nagy
A juvenilis idiopathias arthritis diagnosztikájának és kezelésének finanszírozási protokollja
 A juvenilis idiopathias arthritis diagnosztikájának és kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési
A juvenilis idiopathias arthritis diagnosztikájának és kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Az allergia molekuláris etiopatogenezise
 Az allergia molekuláris etiopatogenezise Müller Veronika Immunológia továbbképzés 2019. 02.28. SEMMELWEIS EGYETEM Pulmonológiai Klinika http://semmelweis.hu/pulmonologia 2017. 03. 08. Immunológia továbbképzés
Az allergia molekuláris etiopatogenezise Müller Veronika Immunológia továbbképzés 2019. 02.28. SEMMELWEIS EGYETEM Pulmonológiai Klinika http://semmelweis.hu/pulmonologia 2017. 03. 08. Immunológia továbbképzés
GYERMEK-TÜDŐGYÓGYÁSZAT
 GYERMEK-TÜDŐGYÓGYÁSZAT I. 1. Légutak és a tüdő fejlődése 2. Légzőrendszer élettani működése 3. Újszülöttkori légzészavarok 4. Bronchopulmonalis dysplasia 5. A gége veleszületett és szerzett rendellenességei
GYERMEK-TÜDŐGYÓGYÁSZAT I. 1. Légutak és a tüdő fejlődése 2. Légzőrendszer élettani működése 3. Újszülöttkori légzészavarok 4. Bronchopulmonalis dysplasia 5. A gége veleszületett és szerzett rendellenességei
Tantermi előadás. Nagy Viktor Semmelweis Egyetem, ÁOK, II. Belgyógyászati Klinika
 Tantermi előadás Nagy Viktor Semmelweis Egyetem, ÁOK, II. Belgyógyászati Klinika Glomerulonephritis acuta, nephrosis syndroma, glomerulonephritis chronica. Budapest, 2015. II. 10. Normális glomerulus
Tantermi előadás Nagy Viktor Semmelweis Egyetem, ÁOK, II. Belgyógyászati Klinika Glomerulonephritis acuta, nephrosis syndroma, glomerulonephritis chronica. Budapest, 2015. II. 10. Normális glomerulus
A myocardium infarktus különböző klinikai formáinak összehasonlítása
 A myocardium infarktus különböző klinikai formáinak összehasonlítása Infarktus Regiszter adatok Dr. Ofner Péter Cél: A STEMI és NSTEMI diagnózissal kezelt betegek demográfiai adatainak, a társbetegségeknek
A myocardium infarktus különböző klinikai formáinak összehasonlítása Infarktus Regiszter adatok Dr. Ofner Péter Cél: A STEMI és NSTEMI diagnózissal kezelt betegek demográfiai adatainak, a társbetegségeknek
Szisztémás Lupusz Eritematózusz (SLE)
 www.printo.it/pediatric-rheumatology/hu/intro Szisztémás Lupusz Eritematózusz (SLE) Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? Az SLE diagnózisa a panaszok (mint pl. fájdalom), a
www.printo.it/pediatric-rheumatology/hu/intro Szisztémás Lupusz Eritematózusz (SLE) Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? Az SLE diagnózisa a panaszok (mint pl. fájdalom), a
II. Klinikai Immunológiai Interdiszciplináris Fórum (KIIF)
 II. Klinikai Immunológiai Interdiszciplináris Fórum (KIIF) 2011.11.10 2011.11.12. Hotel Divinus, Debrecen (Debrecen, Nagyerdei krt. 1.) Főszervező: A Magyar Allergológiai és Klinikai Immunológiai Társaság
II. Klinikai Immunológiai Interdiszciplináris Fórum (KIIF) 2011.11.10 2011.11.12. Hotel Divinus, Debrecen (Debrecen, Nagyerdei krt. 1.) Főszervező: A Magyar Allergológiai és Klinikai Immunológiai Társaság
Plazmaferezis kezelések diagnózis szerinti megoszlása az elmúlt 30 évben (1983-2012) Myastenia Gravis 1353 Guillain-Barre 891 CIDP, SM, DEVIC 595
 Szemelvények a Debreceni Egyetem III. számú Belklinikáján az elmúlt 30 évben végzett plazmaferezis kezelésekből Dr. Soltész Pál Debreceni Egyetem Orvos és Egészségtudományi Centrum III. Belklinika Aferezis
Szemelvények a Debreceni Egyetem III. számú Belklinikáján az elmúlt 30 évben végzett plazmaferezis kezelésekből Dr. Soltész Pál Debreceni Egyetem Orvos és Egészségtudományi Centrum III. Belklinika Aferezis
Etanercept. Finanszírozott indikációk:
 Etanercept Finanszírozott indikációk: 1. Spondylitis ankylopoeticában, amennyiben radiológiailag legalább 2-es stádiumú bilateralis, vagy 3-as, 4-es stádiumú unilateralis sacroileitis, és legalább 3 hónapja
Etanercept Finanszírozott indikációk: 1. Spondylitis ankylopoeticában, amennyiben radiológiailag legalább 2-es stádiumú bilateralis, vagy 3-as, 4-es stádiumú unilateralis sacroileitis, és legalább 3 hónapja
Gyermekkori Dermatomiozitisz
 www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Dermatomiozitisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Más ez a gyermekeknél, mint a felnőtteknél? Felnőtteknél a dermatomiozitisz mögöttes rákbetegséget
www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Dermatomiozitisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Más ez a gyermekeknél, mint a felnőtteknél? Felnőtteknél a dermatomiozitisz mögöttes rákbetegséget
Katasztrófális antifoszfolipid szindróma (CAPS) diagnosztikája és sikeres immunmoduláns kezelése - esetbemutatás
 Katasztrófális antifoszfolipid szindróma (CAPS) diagnosztikája és sikeres immunmoduláns kezelése - esetbemutatás II. Terápiás Aferezis Konferencia Soltész Pál, Nagy-Vincze Melinda, Tarr Tünde, Győri Nikolett,
Katasztrófális antifoszfolipid szindróma (CAPS) diagnosztikája és sikeres immunmoduláns kezelése - esetbemutatás II. Terápiás Aferezis Konferencia Soltész Pál, Nagy-Vincze Melinda, Tarr Tünde, Győri Nikolett,
Katasztrófálisantifoszfolipidantifoszfolipid
 Katasztrófálisantifoszfolipidantifoszfolipid szindróma (CAPS) diagnosztikája és sikeres immunmodulánskezelése - esetbemutatás II. Terápiás Aferezis Konferencia Soltész Pál,Nagy-Vincze Melinda, Tarr Tünde,
Katasztrófálisantifoszfolipidantifoszfolipid szindróma (CAPS) diagnosztikája és sikeres immunmodulánskezelése - esetbemutatás II. Terápiás Aferezis Konferencia Soltész Pál,Nagy-Vincze Melinda, Tarr Tünde,
MHC-gének jelenléte.célkitűzésünk az volt, hogy megvizsgáljuk, hogy milyen HLA-allélek
 Az idiopathiás inflammatorikus myopathiák (IIM) szisztémás autoimmun betegségek, jellegzetességük a harántcsíkolt izomzat immunmediált gyulladása, amely progresszív izomgyengeséghez vezet. A legtöbb autoimmun
Az idiopathiás inflammatorikus myopathiák (IIM) szisztémás autoimmun betegségek, jellegzetességük a harántcsíkolt izomzat immunmediált gyulladása, amely progresszív izomgyengeséghez vezet. A legtöbb autoimmun
Újszülöttkori görcsök. Dr Szabó Miklós PhD egyetemi docens Április 7. Bókay délután
 Újszülöttkori görcsök Dr Szabó Miklós PhD egyetemi docens 2016. Április 7. Bókay délután BNO-kód : P90H0 Hivatalos név: Újszülöttkori görcsök Csoport: Újszülöttkori görcsök, A perinatális szakban keletkező
Újszülöttkori görcsök Dr Szabó Miklós PhD egyetemi docens 2016. Április 7. Bókay délután BNO-kód : P90H0 Hivatalos név: Újszülöttkori görcsök Csoport: Újszülöttkori görcsök, A perinatális szakban keletkező
Hasi tumorok gyermekkorban
 Hasi tumorok gyermekkorban Dr. Bartyik Katalin SZTE ÁOK Gyermekgyógyászati Klinika és Gyermekegészségügyi Központ, Szeged A gyermekkori tumorok a halálozási oki tényezői közül a 2. helyen állnak a balesetek,
Hasi tumorok gyermekkorban Dr. Bartyik Katalin SZTE ÁOK Gyermekgyógyászati Klinika és Gyermekegészségügyi Központ, Szeged A gyermekkori tumorok a halálozási oki tényezői közül a 2. helyen állnak a balesetek,
Esetbemutatás. Dr. Iván Mária Uzsoki Kórház 2013.11.07.
 Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
A psoriasis kezelése kórházunkban: eredményeink, céljaink. Dr. Hortobágyi Judit
 A psoriasis kezelése kórházunkban: eredményeink, céljaink Dr. Hortobágyi Judit Psoriasis vulgaris Öröklött hajlamon alapuló, krónikus, gyulladásos bőrbetegség Gyakorisága Európában 2-3% Magyarországon
A psoriasis kezelése kórházunkban: eredményeink, céljaink Dr. Hortobágyi Judit Psoriasis vulgaris Öröklött hajlamon alapuló, krónikus, gyulladásos bőrbetegség Gyakorisága Európában 2-3% Magyarországon
Védőoltásokról a célzott terápiák korszakában
 Védőoltásokról a célzott terápiák korszakában Onozó Beáta HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2014-2016. 2017. ÁPRILIS 20-21 Autoimmun betegeket fokozott infekcióhajlam jellemzi!
Védőoltásokról a célzott terápiák korszakában Onozó Beáta HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2014-2016. 2017. ÁPRILIS 20-21 Autoimmun betegeket fokozott infekcióhajlam jellemzi!
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Gyermekkori Idiopátiás Artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Idiopátiás Artritisz Verzió 2016 3. DIAGNÓZIS ÉS TERÁPIA 3.1 Milyen laboratóriumi vizsgálatok szükségesek? A diagnóziskor bizonyos laboratóriumi
www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Idiopátiás Artritisz Verzió 2016 3. DIAGNÓZIS ÉS TERÁPIA 3.1 Milyen laboratóriumi vizsgálatok szükségesek? A diagnóziskor bizonyos laboratóriumi
MI ÁLLHAT A FEJFÁJÁS HÁTTERÉBEN? Dr. HégerJúlia, Dr. BeszterczánPéter, Dr. Deák Veronika, Dr. Szörényi Péter, Dr. Tátrai Ottó, Dr.
 MI ÁLLHAT A FEJFÁJÁS HÁTTERÉBEN? Dr. HégerJúlia, Dr. BeszterczánPéter, Dr. Deák Veronika, Dr. Szörényi Péter, Dr. Tátrai Ottó, Dr. Varga Csaba ESET 46 ÉVES FÉRFI Kórelőzmény kezelt hypertonia kivizsgálás
MI ÁLLHAT A FEJFÁJÁS HÁTTERÉBEN? Dr. HégerJúlia, Dr. BeszterczánPéter, Dr. Deák Veronika, Dr. Szörényi Péter, Dr. Tátrai Ottó, Dr. Varga Csaba ESET 46 ÉVES FÉRFI Kórelőzmény kezelt hypertonia kivizsgálás
Ketogén diéta alkalmazása a gyermekepileptológiában
 TDK-munka címe Oesophagus atresia miatt operált gyermekek utógondozása Májtranszplantált gyermekek utánkövetése (szénhidrátanyagcsere, csontanyagcsere, zsíranyagcsere, cardiovascularis rizikó) különös
TDK-munka címe Oesophagus atresia miatt operált gyermekek utógondozása Májtranszplantált gyermekek utánkövetése (szénhidrátanyagcsere, csontanyagcsere, zsíranyagcsere, cardiovascularis rizikó) különös
AUTOANTITEST VIZSGÁLATOK KRITIKUS ÉRTÉKELÉSE
 AUTOANTITEST VIZSGÁLATOK KRITIKUS ÉRTÉKELÉSE Nagy Eszter Országos Reumatológiai és Fizioterápiás Intézet, Immunológiai Laboratórium Semmelweis Egyetem, Laboratóriumi Medicina Intézet Budapesti Immunológiai
AUTOANTITEST VIZSGÁLATOK KRITIKUS ÉRTÉKELÉSE Nagy Eszter Országos Reumatológiai és Fizioterápiás Intézet, Immunológiai Laboratórium Semmelweis Egyetem, Laboratóriumi Medicina Intézet Budapesti Immunológiai
Nanosomia A kivizsgálás indikációi, irányai. Dr. Halász Zita egyetemi docens Semmelweis Egyetem I. sz. Gyermekklinika, Budapest
 Nanosomia A kivizsgálás indikációi, irányai Dr. Halász Zita egyetemi docens Semmelweis Egyetem I. sz. Gyermekklinika, Budapest Az ideális növekedés alapfeltétele adequat táplálkozás, energia bevitel krónikus
Nanosomia A kivizsgálás indikációi, irányai Dr. Halász Zita egyetemi docens Semmelweis Egyetem I. sz. Gyermekklinika, Budapest Az ideális növekedés alapfeltétele adequat táplálkozás, energia bevitel krónikus
Veleszületett és szerzett immundefektusok. Decsi Tamás Gyermekgyógyászati Klinika
 Veleszületett és szerzett immundefektusok Decsi Tamás Gyermekgyógyászati Klinika Képzési célkitűzéek Alapelvek Az immundefektus klinikai gyanújelei Veleszületett immundefektusok: Szelektív IgA-hiány Primér
Veleszületett és szerzett immundefektusok Decsi Tamás Gyermekgyógyászati Klinika Képzési célkitűzéek Alapelvek Az immundefektus klinikai gyanújelei Veleszületett immundefektusok: Szelektív IgA-hiány Primér
Új könnyűlánc diagnosztika. Dr. Németh Julianna Országos Gyógyintézeti Központ Immundiagnosztikai Osztály MLDT-MIT Továbbképzés 2006
 Új könnyűlánc diagnosztika Dr. Németh Julianna Országos Gyógyintézeti Központ Immundiagnosztikai Osztály MLDT-MIT Továbbképzés 2006 1845 Bence Jones Protein vizelet fehérje 1922 BJP I-II típus 1956 BJP
Új könnyűlánc diagnosztika Dr. Németh Julianna Országos Gyógyintézeti Központ Immundiagnosztikai Osztály MLDT-MIT Továbbképzés 2006 1845 Bence Jones Protein vizelet fehérje 1922 BJP I-II típus 1956 BJP
Mevalonát-Kináz-Hiány (MKD) (vagy hiper-igd szindróma)
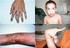 www.printo.it/pediatric-rheumatology/hu/intro Mevalonát-Kináz-Hiány (MKD) (vagy hiper-igd szindróma) Verzió 2016 1. MI AZ MKD 1.1 Mi ez? A mevalonát-kináz-hiány genetikai betegség. A szervezet veleszületett
www.printo.it/pediatric-rheumatology/hu/intro Mevalonát-Kináz-Hiány (MKD) (vagy hiper-igd szindróma) Verzió 2016 1. MI AZ MKD 1.1 Mi ez? A mevalonát-kináz-hiány genetikai betegség. A szervezet veleszületett
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA. Dr. Győrffy Balázs
 A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
Súlyos infekciók differenciálása a rendelőben. Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza
 Súlyos infekciók differenciálása a rendelőben Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza Miért probléma a lázas gyermek a rendelőben? nem beteg - súlyos beteg otthon ellátható
Súlyos infekciók differenciálása a rendelőben Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza Miért probléma a lázas gyermek a rendelőben? nem beteg - súlyos beteg otthon ellátható
Rovarméreg (méh, darázs) - allergia
 Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
2 2. O R S Z Á G O S A N T I B I O T I K U M T O V Á B B K É P Z Ô TA N F O LYA M
 PROGRAM 2016. NOVEMBER 17. CSÜTÖRTÖK 10.00 20.00 Regisztráció 13.00 Megnyitó 13.05 13.35 Lázas megbetegedés szokatlan oka: Haemophagocytosis Dr. Szombati Andrea főorvos Fővárosi Önkormányzat Egyesített
PROGRAM 2016. NOVEMBER 17. CSÜTÖRTÖK 10.00 20.00 Regisztráció 13.00 Megnyitó 13.05 13.35 Lázas megbetegedés szokatlan oka: Haemophagocytosis Dr. Szombati Andrea főorvos Fővárosi Önkormányzat Egyesített
REUMA GYERMEKKORBAN?
 REUMA GYERMEKKORBAN? Magyarországon 10 emberből 9, ha azt hallja, hogy gyermekreumatológia, akkor, talán csak magában, de felteszi a kérdést: egy gyerek is lehet reumás? Sokan úgy gondolják tehát, hogy
REUMA GYERMEKKORBAN? Magyarországon 10 emberből 9, ha azt hallja, hogy gyermekreumatológia, akkor, talán csak magában, de felteszi a kérdést: egy gyerek is lehet reumás? Sokan úgy gondolják tehát, hogy
Dr. Máthéné Dr. Szigeti Zsuzsanna és munkatársai
 Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
A Petrányi Gyula Klinikai Immunológiai és Allergológiai Doktori Iskola (PGKIADI) képzési terve 2014.
 A Petrányi Gyula Klinikai Immunológiai és Allergológiai Doktori Iskola (PGKIADI) képzési terve 2014. Az orvostudományi területen működő doktori iskolák képzésére vonatkozó alapelveket a Debreceni Egyetem
A Petrányi Gyula Klinikai Immunológiai és Allergológiai Doktori Iskola (PGKIADI) képzési terve 2014. Az orvostudományi területen működő doktori iskolák képzésére vonatkozó alapelveket a Debreceni Egyetem
PRIMER IMMUNDEFICIENCIA - KOMPLEMENT DEFEKTUS. LABORVIZSGÁLATOK BEMUTATÁSA EGY BETEGÜNK KAPCSÁN
 2014. 1. szám TESZTKÉRDÉSEI: PRIMER IMMUNDEFICIENCIA - KOMPLEMENT DEFEKTUS. LABORVIZSGÁLATOK BEMUTATÁSA EGY BETEGÜNK KAPCSÁN SZILÁGYI ÁGNES 1, VARGA LILIAN 1, PROHÁSZKA ZOLTÁN 1, DÉRFALVI BEÁTA 2 Milyen
2014. 1. szám TESZTKÉRDÉSEI: PRIMER IMMUNDEFICIENCIA - KOMPLEMENT DEFEKTUS. LABORVIZSGÁLATOK BEMUTATÁSA EGY BETEGÜNK KAPCSÁN SZILÁGYI ÁGNES 1, VARGA LILIAN 1, PROHÁSZKA ZOLTÁN 1, DÉRFALVI BEÁTA 2 Milyen
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
B-sejtek szerepe az RA patológiás folyamataiban
 B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
Az onkológiai ellátáshoz való hozzáférés esélyei
 Az onkológiai ellátáshoz való hozzáférés esélyei Garami Miklós 15 Egészség-Gazdaságtani Szimpózium Hozzáférhetőség a magyar egészségügyben ELTE TáTK, 2013 május 31 Az egészségügyi teljesítmény dimenziói
Az onkológiai ellátáshoz való hozzáférés esélyei Garami Miklós 15 Egészség-Gazdaságtani Szimpózium Hozzáférhetőség a magyar egészségügyben ELTE TáTK, 2013 május 31 Az egészségügyi teljesítmény dimenziói
Dr. SZEKANECZ Éva, dr. GONDA Andrea. DE OEC Onkológiai Intézet IV. Db. Bőrgyógyászati Napok, 2012. Október 13.
 Dr. SZEKANECZ Éva, dr. GONDA Andrea DE OEC Onkológiai Intézet IV. Db. Bőrgyógyászati Napok, 2012. Október 13. ma már a legtöbb intézetben elérhetőek a biológiai terápiák bár eredményesnek bizonyultak a
Dr. SZEKANECZ Éva, dr. GONDA Andrea DE OEC Onkológiai Intézet IV. Db. Bőrgyógyászati Napok, 2012. Október 13. ma már a legtöbb intézetben elérhetőek a biológiai terápiák bár eredményesnek bizonyultak a
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői.
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Gyermekkori Dermatomiozitisz
 www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Dermatomiozitisz Verzió 2016 1. MI A GYERMEKKORI DERMATOMIOZITISZ 1.1 Milyen betegség ez? A gyermekkori dermatomiozitisz (JDM) az izmokat és a
www.printo.it/pediatric-rheumatology/hu/intro Gyermekkori Dermatomiozitisz Verzió 2016 1. MI A GYERMEKKORI DERMATOMIOZITISZ 1.1 Milyen betegség ez? A gyermekkori dermatomiozitisz (JDM) az izmokat és a
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Kórélettan hematológiai esetek
 8. eset Középkorú nőbeteg. Két hete gyengébb, fáradékonyabb. Háziorvosa laborvizsgálatot kért, a lelet ismeretében kórházba utalta. Fehérvérsejt 62,7 G/l H 4 10 G/l Neutrophil % 40 70 % Neutrophil (abs)
8. eset Középkorú nőbeteg. Két hete gyengébb, fáradékonyabb. Háziorvosa laborvizsgálatot kért, a lelet ismeretében kórházba utalta. Fehérvérsejt 62,7 G/l H 4 10 G/l Neutrophil % 40 70 % Neutrophil (abs)
Plazmaferezis neurológiai kórképekben. Devic betegség. Dr.Simó Magdolna SE Neurológiai Klinika
 Plazmaferezis neurológiai kórképekben Devic betegség Dr.Simó Magdolna SE Neurológiai Klinika TPE neurológiai indikációi Myasthenia gravis Guillain Barre syndroma / AIDP CIDP ADEM Sclerosis multiplex PPN
Plazmaferezis neurológiai kórképekben Devic betegség Dr.Simó Magdolna SE Neurológiai Klinika TPE neurológiai indikációi Myasthenia gravis Guillain Barre syndroma / AIDP CIDP ADEM Sclerosis multiplex PPN
Citopeniák. Vérszegénységek Neutropéniák Trombocitopeniák
 Citopeniák Vérszegénységek Neutropéniák Trombocitopeniák Anémia okai Fokozott pusztulás-vvt élettartam csökkenés (
Citopeniák Vérszegénységek Neutropéniák Trombocitopeniák Anémia okai Fokozott pusztulás-vvt élettartam csökkenés (
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010. február 15. 1 1. Azonosítószám:
A krónikus myeloid leukémia kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010. február 15. 1 1. Azonosítószám:
NALP-12-Höz Társult Visszatérő Láz
 www.printo.it/pediatric-rheumatology/hu/intro NALP-12-Höz Társult Visszatérő Láz Verzió 2016 1. MI A NALP-12-HÖZ TÁRSULT VISSZATÉRŐ LÁZ 1.1 Mi ez? A NALP-12-höz társult visszatérő láz egy genetikai betegség.
www.printo.it/pediatric-rheumatology/hu/intro NALP-12-Höz Társult Visszatérő Láz Verzió 2016 1. MI A NALP-12-HÖZ TÁRSULT VISSZATÉRŐ LÁZ 1.1 Mi ez? A NALP-12-höz társult visszatérő láz egy genetikai betegség.
Együttműködési lehetőségek spondyloarthritises betegek kezelésében
 Együttműködési lehetőségek spondyloarthritises betegek kezelésében A spondyloarthritis (SpA) fogalma Hasonló tünetek: spondyloarthritis, extraartikuláris manifesztációk (EAM), sacroileitis Nem differenciált
Együttműködési lehetőségek spondyloarthritises betegek kezelésében A spondyloarthritis (SpA) fogalma Hasonló tünetek: spondyloarthritis, extraartikuláris manifesztációk (EAM), sacroileitis Nem differenciált
Az ellenanyagok szerkezete és funkciója. Erdei Anna Immunológiai Tanszék ELTE
 Az ellenanyagok szerkezete és funkciója Erdei Anna Immunológiai Tanszék ELTE Bev. 1. ábra Immunhomeosztázis A veleszületett és az adaptív immunrendszer szorosan együttműködik az immunhomeosztázis fenntartásáért
Az ellenanyagok szerkezete és funkciója Erdei Anna Immunológiai Tanszék ELTE Bev. 1. ábra Immunhomeosztázis A veleszületett és az adaptív immunrendszer szorosan együttműködik az immunhomeosztázis fenntartásáért
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
A hólyagrák aktuális kérdései a pathologus szemszögéből. Iványi Béla SZTE Pathologia
 A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
Az arthritis psoriatica diagnosztikájának és kezelésének finanszírozási protokollja
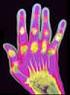 Az arthritis psoriatica diagnosztikájának és kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
Az arthritis psoriatica diagnosztikájának és kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Tünetmentes gyermek fokozott szérum transzferáz aktivitással. Mit tegyek? Szőnyi László 2012. 2012.május 11. Kávészünet. 2012.
 Tünetmentes gyermek fokozott szérum transzferáz aktivitással. Mit tegyek? Szőnyi László 2012 Miért fokozott szérum transzferáz aktivitás és nem kóros májfunkció? Szérum fokozott ALP aktivitás, fokozott
Tünetmentes gyermek fokozott szérum transzferáz aktivitással. Mit tegyek? Szőnyi László 2012 Miért fokozott szérum transzferáz aktivitás és nem kóros májfunkció? Szérum fokozott ALP aktivitás, fokozott
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. 1 adag (1 ml) tartalma: Hepatitisz B felszíni antigén 1,2. 20 mikrogramm
 1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
1. A GYÓGYSZER NEVE Engerix-B szuszpenziós injekció felnőtteknek Engerix-B szuszpenziós injekció előretöltött fecskendőben felnőtteknek Hepatitisz B (rekombináns DNS) vakcina (adszorbeált) (HBV) 2. MINŐSÉGI
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
A Brit Reumatológiai Társaság által publikált guideline a polymyalgia rheumatica (PMR) kezelésére és diagnózisára
 A Brit Reumatológiai Társaság által publikált guideline a polymyalgia rheumatica (PMR) kezelésére és diagnózisára A PMR a leggyakoribb időskori gyulladásos reumatológiai betegség és egyike a hosszú-távú
A Brit Reumatológiai Társaság által publikált guideline a polymyalgia rheumatica (PMR) kezelésére és diagnózisára A PMR a leggyakoribb időskori gyulladásos reumatológiai betegség és egyike a hosszú-távú
Gyógyításra váró pulmonológiai betegségek
 Gyógyításra váró pulmonológiai betegségek Herjavecz Irén Országos Korányi Tbc és Pulmonológiai Intézet 2009.április 20. Népbetegségek a pulmonológiában Epidemiológiai és morbiditási súlyukat tekintve a
Gyógyításra váró pulmonológiai betegségek Herjavecz Irén Országos Korányi Tbc és Pulmonológiai Intézet 2009.április 20. Népbetegségek a pulmonológiában Epidemiológiai és morbiditási súlyukat tekintve a
Jurásné Lukovics Mónika, Dr. Bohaty Ilona, Dr. Kozma László PhD OVSz Debreceni RVK
 Jurásné Lukovics Mónika, Dr. Bohaty Ilona, Dr. Kozma László PhD OVSz Debreceni RVK Az újszülöttben kialakuló trombocitopénia (
Jurásné Lukovics Mónika, Dr. Bohaty Ilona, Dr. Kozma László PhD OVSz Debreceni RVK Az újszülöttben kialakuló trombocitopénia (
Népegészségügyi Szakigazgatási Szerve. Tájékoztató Hajdú-Bihar megye lakosságának egészségi állapotáról
 Népegészségügyi Szakigazgatási Szerve Tájékoztató Hajdú-Bihar megye lakosságának egészségi állapotáról T a r t a l o m j e g y z é k 1. BEVEZETÉS... 4 2. ADATFORRÁSOK... 4 3. ELEMZÉSI MÓDSZEREK... 4 4.
Népegészségügyi Szakigazgatási Szerve Tájékoztató Hajdú-Bihar megye lakosságának egészségi állapotáról T a r t a l o m j e g y z é k 1. BEVEZETÉS... 4 2. ADATFORRÁSOK... 4 3. ELEMZÉSI MÓDSZEREK... 4 4.
Congenitalis adrenalis hyperplasia, 21-hidroxiláz defektus. Szülő- és betegtájékoztató
 Bevezetés Congenitalis adrenalis hyperplasia, 21-hidroxiláz defektus Szülő- és betegtájékoztató Minden szülő azt várja, hogy gyermeke egészséges lesz. Így azután mélyen megrázza őket, ha megtudják, hogy
Bevezetés Congenitalis adrenalis hyperplasia, 21-hidroxiláz defektus Szülő- és betegtájékoztató Minden szülő azt várja, hogy gyermeke egészséges lesz. Így azután mélyen megrázza őket, ha megtudják, hogy
IgA-glomerulonephritis
 dr. Fintha Attila 73. Patológus Kongresszus 2017. szeptember 28-30. SEMMELWEIS EGYETEM Általános Orvostudományi Kar II. sz. Pathologiai Intézet http://semmelweis.hu IgA glomerulonephritis (=IgA nephropathia)
dr. Fintha Attila 73. Patológus Kongresszus 2017. szeptember 28-30. SEMMELWEIS EGYETEM Általános Orvostudományi Kar II. sz. Pathologiai Intézet http://semmelweis.hu IgA glomerulonephritis (=IgA nephropathia)
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
