Az EMA jóváhagyta a PML nevű agyi fertőzésnek a Tysabri alkalmazásával kapcsolatos kockázata csökkentésére vonatkozó ajánlásokat
|
|
|
- Ilona Rácz
- 8 évvel ezelőtt
- Látták:
Átírás
1 25/04/2016 Az EMA jóváhagyta a PML nevű agyi fertőzésnek a Tysabri alkalmazásával kapcsolatos kockázata csökkentésére vonatkozó ajánlásokat A nagyobb kockázatnak kitett betegeknél meg kell fontolni a gyakoribb MRvizsgálatokat február 25-én az EMA befejezte a progresszív multifokális leukoenkefalopátia (PML) a szklerózis multiplex gyógyszerének, a Tysabri-nak (natalizumab) az alkalmazása melletti ismert kockázatának felülvizsgálatát, és megerősítette az ezen kockázat minimalizálását célzó kezdeti ajánlásokat. 1 A PML a John Cunningham (JC) vírus által okozott ritka agyi fertőzés. A vírus igen gyakori az általános populációban, és általában ártalmatlan, azonban PML-t eredményezhet azoknál a személyeknél, akiknek az immunrendszere legyengült. A PML leggyakoribb tünetei a progresszív gyengeség, a beszéd- és kommunikációs nehézségek, a látászavarok, és olykor a hangulat- vagy magatartásbeli változások. A PML nagyon súlyos állapot, amely súlyos rokkantságot vagy halált okozhat. Újabb vizsgálatok arra utalnak, hogy a PML korai kimutatása és kezelése, amikor a betegség tünetmentes (még a kezdeti szakaszban van, és nem mutat tüneteket), javíthatja a betegek eredményeit. A PML tünetmentes esetei MR-felvételeken kimutathatók, és az MRI és a szklerózis multiplex területének szakértői egyetértenek abban, hogy az egyszerűsített MR-protokollok (amelyek rövidebb eljárásokat engednek, és csökkentik a vizsgálatokban részt vevő betegek terhelését is) lehetővé teszik a PML elváltozások azonosítását. Minden, Tysabri-t kapó betegnél évente legalább egyszer teljes MR-vizsgálatot kell végezni, de az új adatok alapján az EMA azt javasolta, hogy a PML nagyobb kockázatának kitett betegeknél egyszerűsített protokollok szerint végzett, gyakoribb (pl. 3 6 havonkénti) MR-vizsgálatokat kell fontolóra kell venni. Ha PML-re utaló elváltozásokat fedeznek fel, az MR-protokollt ki kell terjeszteni úgy, hogy tartalmazza a kontrasztanyagos T1-súlyozott MR-t, és fontolóra kell venni a gerincvelői folyadéknak a JC vírus jelenlétére való tesztelését. Nagy klinikai vizsgálatokból származó új adatok is utalnak arra, hogy azoknál a betegeknél, akiket nem kezeltek immunszuppresszánsokkal (az immunrendszer aktivitását csökkentő gyógyszerek), a Tysabri alkalmazásának elkezdése előtt a JC vírus elleni antitestek plazmaszintje ( antitest-index ) arányos a PML kockázatának szintjével. Az új bizonyítékok figyelembevételével úgy tekintik, hogy a betegeknél az alábbiak teljesülése esetén nagyobb a PML kialakulásának veszélye: pozitív vizsgálati eredmény a JC vírusra, február 11-én kiadott PRAC ajánlások 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone +44 (0) Facsimile +44 (0) Send a question via our website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 több mint 2 évig kezelték őket Tysabri-val, valamint vagy immunszuppresszánst alkalmaztak náluk a Tysabri kezelés megkezdése előtt, vagy nem alkalmaztak náluk immunszuppresszánsokat, és magas JC vírus antitest indexszel rendelkeznek. Ezeknél a betegeknél a Tysabri-val végzett kezelés csak akkor folytatható, ha az előnyök meghaladják a kockázatokat. Ha bármikor PML gyanúja áll fenn, a Tysabri-val végzett kezelést a betegség kizárásáig fel kell függeszteni. Az EMA ajánlásai a farmakovigilanciai kockázatértékelési bizottsága (PRAC) által elvégzett kezdeti felülvizsgálaton alapulnak. A PRAC ajánlások továbbításra kerültek az emberi felhasználásra szánt gyógyszerek bizottságához (CHMP), amely megerősítette azokat, és elfogadta a végleges véleményét. A CHMP véleménye ezután továbbításra került az Európai Bizottsághoz, amely az Európai Unió egész területére érvényes, jogilag kötelező érvényű határozatot hozott. Tájékoztató a betegek számára A progresszív multifokális leukoenkefalopátia (PML, egy súlyos agyi fertőzés) a Tysabri nevű szklerózis multiplex elleni gyógyszer alkalmazásával járó ritka kockázatként ismert. Olyan új ajánlásokat adtak ki, amelyek segíthetnek a PML korai kimutatásában, és javíthatják a betegek eredményeit. A PML kialakulásának kockázata számos tényezőtől függ, például attól, hogy jelen vannak-e az Ön vérében a JC vírus elleni antitestek (annak egy jele, hogy Ön ki van téve a PML-t okozó vírusnak), és milyen a plazmaszintjük, mióta kezelik Önt Tysabri-val, valamint hogy a Tysabri alkalmazásának elkezdése előtt kezelték-e Önt olyan gyógyszerekkel, amelyek gyengítik az immunrendszerét. Ezeket a tényezőket figyelembe véve orvosa tájékoztatni tudja majd Önt arról, hogy milyen mértékű Önnél a PML kialakulásának kockázata. A Tysabri-val végzett kezelés elkezdése előtt, majd a kezelés alatt rendszeresen, orvosa vérvizsgálatokat fog végezni a JC vírus elleni antitestek szintjének méréséhez, valamint MRvizsgálatokat az Ön állapotának ellenőrzéséhez. Kezelőorvosa azt is ellenőrizni fogja, hogy nem tapasztalhatók-e Önnél PML-re utaló jelek vagy tünetek. Ezek a vizsgálatok gyakrabban is elvégezhetők, amennyiben úgy vélik, hogy Önnél fokozott a PML kockázata. Amennyiben PML gyanúja merül fel, orvosa a PML kizárásáig felfüggeszti a Tysabri-val végzett kezelést. A PML tünetei hasonlóak lehetnek a szklerózis multiplex roham alatt tapasztalhatókhoz, és a következők tartoznak közéjük: progresszív gyengeség, beszéd- és kommunikációs nehézségek, látászavarok, és olykor hangulat- vagy magatartásbeli változások. Ha úgy érzi, hogy betegsége súlyosbodik, vagy bármilyen új vagy szokatlan tünetet tapasztal a Tysabri alkalmazása során, valamint a gyógyszer alkalmazásának befejezése utáni 6 hónapon belül, a lehető leghamarabb keresse fel kezelőorvosát. A PML-nek a Tysabri alkalmazásával kapcsolatos kockázatára vonatkozó további információk a kezelőorvosától kapott betegfigyelmeztető kártyán találhatók. Fontos, hogy figyelmesen elolvassa ezt a kártyát. Tartsa ezt a kártyát magánál, és biztosítsa, hogy a partnere vagy a gondozója ismerje annak tartalmát. 2/2. oldal
3 Amennyiben kérdése vagy aggálya merülne fel, forduljon kezelőorvosához, ápolójához vagy gyógyszerészéhez. Tájékoztató az egészségügyi szakemberek számára A PML kialakulásának ismert kockázati tényezői a Tysabri-val kezelt betegeknél a JC vírus elleni antitestek jelenléte, a Tysabri-val történő, több mint két éve tartó kezelés, valamint immunszuppresszánsok korábbi alkalmazása. Nagy klinikai vizsgálatokból származó összesített adatok arra utalnak, hogy azoknál a betegeknél, akiknél korábban nem alkalmaztak immunszuppresszánsokat, a JC vírus elleni antitest-válasz szintje (index) arányos a PML kockázatának szintjével. Ezen adatok alapján a PML-re 2 vonatkozóan frissített kockázatbecslések állnak rendelkezésre a JC vírus antitestjére pozitív, Tysabri-val kezelt betegek esetében, amint az az alábbi, 1. táblázatban látható: 1. táblázat: A PML 1000 betegre számított kockázatának becslései a JC vírus elleni antitestre pozitív betegeknél* A Tysabri alkalmazásának időtartama Immunszuppresszánsok korábbi alkalmazása nélkül 1,5-nél Nincs 0,9-es vagy 0,9 és 1,5 nagyobb indexérték kisebb index közötti index index Immunszuppresszánsok korábbi alkalmazása mellett 1 12 hónap 0,1 0,1 0,1 0,2 0, hónap 0,6 0,1 0,3 0,9 0, hónap 2 0,2 0, hónap 4 0, hónap 5 0, hónap 6 0, *A Tysabri Orvosoknak szóló tájékoztató és kezelési irányelvek kiadványból A fenti, frissített kockázatbecslések azt mutatják, hogy a PML kialakulásának kockázata kicsi, és a 0,9- es vagy az alatti antitest-index érték esetén a korábban becsültnél alacsonyabb, és jelentősen megnő a Tysabri-val már több mint 2 éve kezelt betegeknél, akiknél az index értéke 1,5 felett van. Azoknál a betegeknél, akiknek a vizsgálati eredménye a JC vírus antitestjeire negatív volt, a PML 1000 betegre számított kockázatbecslése változatlanul 0,1 marad. A kockázatbesorolásra, a diagnózisra és a PML kezelésére vonatkozóan részletesebb információk a Tysabri frissített Orvosoknak szóló tájékoztató és kezelési irányelvek kiadványában lesz megtalálható. Az egészségügyi szakembereknek az alábbi ajánlásokat kell szem előtt tartani: A Tysabri-val történő kezelés megkezdése előtt a betegeket és a gondozókat tájékoztatni kell a PML kockázatáról. A betegeknek fel kell hívni a figyelmét arra, hogy forduljanak orvoshoz, ha úgy érzik, hogy a betegségük súlyosbodik, vagy ha bármilyen új vagy szokatlan tünetet tapasztalnak. 2 A PML-re vonatkozó kockázatbecslések a STRATIFY-2, TOP, TYGRIS és STRATA klinikai vizsgálatokban részt vevő beteg egyesített kohorszán alapuló élettartam-táblázat módszer alkalmazásából származtak. A PML JC vírus elleni antitestindex intervallumának további stratifikációja az olyan betegeknél, akiknél korábban nem alkalmaztak immunszuppresszánsokat, a teljes éves kockázatnak és az antitest-index eloszlásának egyesítéséből származott. 3/3. oldal
4 A kezelés megkezdése előtt referenciaként rendelkezésre kell állnia egy (általában 3 hónapon belüli) kiindulási MRI-nek, és a PML kockázatbesorolásának támogatására el kell végezni egy kiindulási vizsgálatot a JC elleni antitestekre vonatkozóan. A Tysabri-val végzett kezelés során a betegeket rendszeres időközönként ellenőrizni kell az új neurológiai diszfunkciók jeleire és tüneteire vonatkozóan, és a kezelés ideje alatt évente legalább egyszer teljes agyi MRI-t kell végezni. Azoknál a betegeknél, akiknél nagyobb a PML kockázata, fontolóra kell venni a gyakoribb (pl. 3 6 havonkénti), rövidített protokoll (pl. FLAIR, T2-súlyozott és diffúzió-súlyozott (DW) képalkotás) használatával végzett MRI-ket, mivel a PML korai kimutatása a tünetmentes betegeknél a PML kezelésének jobb eredményével jár. A neurológiai tünetekkel és/vagy az MRI-n új agyi elváltozásokkal bíró betegeknél a differenciáldiagnózis során mérlegelni kell a PML lehetőségét is. Beszámoltak az MRI alapján tünetmentes PML esetekről, valamint olyan tünetmentes esetekről, ahol a JC vírus jelen volt a gerincvelői folyadék DNS-ében. Ha PML gyanúja áll fenn, az MR-protokollt ki kell terjeszteni úgy, hogy tartalmazza a kontrasztanyagos T1-súlyozott MR-t, és fontolóra kell venni a gerincvelői folyadéknak a JC vírus DNS-e jelenlétére való tesztelését ultraszenzitív PCR segítségével. Ha bármikor PML gyanúja jelenik meg, a Tysabri-val végzett kezelést a betegség kizárásáig fel kell függeszteni. Az antitestre negatív betegeknél a JC vírus elleni antitestre vonatkozóan 6 havonta vizsgálatot kell végezni. Az alacsony indexértékekkel rendelkező, korábban immunszuppresszív kezelésben nem részesült betegeket a 2 éves kezelési pont elérését követően szintén 6 havonta újra kell tesztelni. 2 évi kezelést követően a betegeket ismét tájékoztatni kell a PML-nek a Tysabri alkalmazásával kapcsolatos kockázatáról. Fel kell hívni a betegek és a gondozók figyelmét arra, hogy a Tysabri alkalmazásának abbahagyását követően még 6 hónapig maradjanak éberek a PML kockázatával kapcsolatban. További információk a gyógyszerről A Tysabri a nagyon aktív szklerózis multiplexben (SM) szenvedő felnőtt betegek kezelésére szolgáló gyógyszer. Az SM az idegek megbetegedése, amelynek során az idegsejteket körülvevő védőhüvelyt gyulladás pusztítja el. A Tysabri-t a relapszáló-remittáló SM-ként ismert típus esetében alkalmazzák, amikor a betegnek a tünetmentes időszakok (remissziók) közötti időszakokban rohamai (relapszusai) vannak. A gyógyszert akkor alkalmazzák, amikor a betegség a béta-interferonnal vagy a glatirameracetáttal (az SM kezelésére alkalmazott más típusú gyógyszerek) végzett kezelésre nem reagál, vagy súlyos és gyorsan súlyosbodik. A Tysabri hatóanyaga, a natalizumab, egy monoklonális antitest (egy fehérjefajta), amelyet úgy alkottak meg, hogy felismerje és kötődjön az α4β1 integrin nevű fehérje egy meghatározott részéhez. Ez a fehérje a legtöbb leukocita (a vérben található fehérvérsejtek, amelyek a gyulladás folyamatában játszanak szerepet) felületén megtalálható. Az integrinhez kötődése által a natalizumab 4/4. oldal
5 leállítja a leukocitáknak a vérből az agyba történő áramlását, így enyhíti az SM által okozott gyulladást és idegkárosodást. A Tysabri-t 2006 júniusában engedélyezték az Európai Unióban. További információk az eljárásról A Tysabri felülvizsgálatát május 7-én kezdeményezték az Európai Bizottság kérésére, a 2004/726/EK rendelet 20. cikke alapján. A felülvizsgálatot a farmakovigilanciai kockázatfelmérési bizottság (PRAC), az emberi felhasználásra szánt gyógyszerek biztonságossági kérdéseinek értékeléséért felelős bizottság végezte, amely egy sor ajánlást adott ki. A PRAC ajánlások továbbításra kerültek az emberi felhasználásra szánt gyógyszerek bizottságához (CHMP), amely felelős az emberi felhasználásra szánt gyógyszereket érintő kérdésekben, és amely elfogadta az Ügynökség végleges véleményét. A CHMP véleménye továbbításra került az Európai Bizottsághoz, amely 25/04/2016 az EU minden tagállamában érvényes, végleges, jogilag kötelező érvényű határozatot adott ki. Kapcsolatfelvétel sajtóreferensünkkel Monika Benstetter Tel.: +44 (0) press@ema.europa.eu 5/5. oldal
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 38 Tudományos következtetések A progresszív multifokális leukoenkefalopátiára (PML) vonatkozó tudományos bizonyíték a Tysabrival kezelt betegek esetében rohamosan
IV. melléklet Tudományos következtetések 38 Tudományos következtetések A progresszív multifokális leukoenkefalopátiára (PML) vonatkozó tudományos bizonyíték a Tysabrival kezelt betegek esetében rohamosan
pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált)
 EMA/90006/2015 EMEA/H/C/001104 EPAR-összefoglaló a nyilvánosság számára pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált) Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő
EMA/90006/2015 EMEA/H/C/001104 EPAR-összefoglaló a nyilvánosság számára pneumococcus poliszacharid konjugált vakcina (13-valens, adszorbeált) Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő
A Pradaxa egy dabigatrán etexilát nevű hatóanyagot tartalmazó gyógyszer. Kapszula formájában kapható (75, 110 és 150 mg).
 EMEA/H/C/000829 EPAR-összefoglaló a nyilvánosság számára dabigatrán etexilát Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi felhasználásra
EMEA/H/C/000829 EPAR-összefoglaló a nyilvánosság számára dabigatrán etexilát Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi felhasználásra
Új korlátozások a szívritmusra gyakorolt hatások kockázatainak minimalizálására vonatkozóan hidroxizin tartalmú gyógyszerekkel
 2015. március 27. Új korlátozások a szívritmusra gyakorolt hatások kockázatainak minimalizálására vonatkozóan hidroxizin tartalmú gyógyszerekkel Használatuk kerülendő a legnagyobb kockázatnak kitett betegeknél,
2015. március 27. Új korlátozások a szívritmusra gyakorolt hatások kockázatainak minimalizálására vonatkozóan hidroxizin tartalmú gyógyszerekkel Használatuk kerülendő a legnagyobb kockázatnak kitett betegeknél,
Az Avastin-t más daganatellenes gyógyszerekkel kombinálva, az alábbi típusú daganatos betegségekben szenvedő felnőttek kezelésére alkalmazzák:
 EMEA/H/C/000582 EPAR-összefoglaló a nyilvánosság számára bevacizumab Ez a dokumentum az -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi felhasználásra
EMEA/H/C/000582 EPAR-összefoglaló a nyilvánosság számára bevacizumab Ez a dokumentum az -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi felhasználásra
Oktatási anyagok a Suliqua elnevezésű diabétesz gyógyszert alkalmazó egészségügyi szakemberek és betegek számára
 2017. január 19. EMA/747766/2016 Oktatási anyagok a Suliqua elnevezésű diabétesz gyógyszert alkalmazó egészségügyi szakemberek és betegek számára Két különböző hatáserősségű toll összecserélési kockázatának
2017. január 19. EMA/747766/2016 Oktatási anyagok a Suliqua elnevezésű diabétesz gyógyszert alkalmazó egészségügyi szakemberek és betegek számára Két különböző hatáserősségű toll összecserélési kockázatának
Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból
 25 January 2018 EMA/PRAC/35603/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2018. január 8-11-i ülésén
25 January 2018 EMA/PRAC/35603/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2018. január 8-11-i ülésén
Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból
 17 December 2015 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2015. november 30 december 3-i ülésén elfogadva
17 December 2015 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2015. november 30 december 3-i ülésén elfogadva
Mielóma multiplex (a fehérvérsejtek egy típusa, a plazmasejtek daganatos betegsége) esetében a Revlimid-et a következőképpen alkalmazzák:
 EMA/112959/2016 EMEA/H/C/000717 EPAR-összefoglaló a nyilvánosság számára lenalidomid Ez a dokumentum a -re vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi
EMA/112959/2016 EMEA/H/C/000717 EPAR-összefoglaló a nyilvánosság számára lenalidomid Ez a dokumentum a -re vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi
Az Opdivo nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban
 EMA/55240/2019 EMEA/H/C/003985 Az Opdivo nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban Milyen típusú gyógyszer az Opdivo és milyen betegségek esetén alkalmazható? Az Opdivo
EMA/55240/2019 EMEA/H/C/003985 Az Opdivo nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban Milyen típusú gyógyszer az Opdivo és milyen betegségek esetén alkalmazható? Az Opdivo
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 1 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
IV. melléklet Tudományos következtetések 1 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
Az Opdivo nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban
 EMA/489091/2018 EMEA/H/C/003985 Az Opdivo nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban Milyen típusú gyógyszer az Opdivo és milyen betegségek esetén alkalmazható? Az Opdivo
EMA/489091/2018 EMEA/H/C/003985 Az Opdivo nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban Milyen típusú gyógyszer az Opdivo és milyen betegségek esetén alkalmazható? Az Opdivo
HATÓANYAG: Natalizumab. 300 mg natalizumab, 15 ml koncentrátumot tartalmazó injekciós üvegenként (20 mg/ml).
 TYSABRI 300 MG KONCENTRÁTUM OLDATOS INFÚZIÓHOZ TYSABRI 300 mg koncentrátum oldatos infúzióhoz natalizumab HATÓANYAG: Natalizumab. 300 mg natalizumab, 15 ml koncentrátumot tartalmazó injekciós üvegenként
TYSABRI 300 MG KONCENTRÁTUM OLDATOS INFÚZIÓHOZ TYSABRI 300 mg koncentrátum oldatos infúzióhoz natalizumab HATÓANYAG: Natalizumab. 300 mg natalizumab, 15 ml koncentrátumot tartalmazó injekciós üvegenként
Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból
 12 October 2017 EMA/PRAC/662554/2017 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2017. szeptember 25-29-i
12 October 2017 EMA/PRAC/662554/2017 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2017. szeptember 25-29-i
Mielóma multiplex (a fehérvérsejtek egy típusa, a plazmasejtek daganatos betegsége) esetében a Revlimid-et a következőképpen alkalmazzák:
 EMA/113870/2017 EMEA/H/C/000717 EPAR-összefoglaló a nyilvánosság számára lenalidomid Ez a dokumentum a -re vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az Ügynökségnek
EMA/113870/2017 EMEA/H/C/000717 EPAR-összefoglaló a nyilvánosság számára lenalidomid Ez a dokumentum a -re vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az Ügynökségnek
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 A Keytruda nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban Milyen típusú gyógyszer a Keytruda és milyen betegségek esetén alkalmazható? A Keytruda
EMA/235911/2019 EMEA/H/C/003820 A Keytruda nevű gyógyszer áttekintése és indoklás, hogy miért engedélyezték az EU-ban Milyen típusú gyógyszer a Keytruda és milyen betegségek esetén alkalmazható? A Keytruda
Útmutató a gyógyszerekkel szembeni, feltételezett mellékhatások spontán esetjelentéseinek értelmezéséhez
 2017. január 30. Ellenőrzések, emberi felhasználásra szánt gyógyszerek farmakovigilancia és bizottságok EMA/749446/2016 Revision 1* Útmutató a gyógyszerekkel szembeni, feltételezett mellékhatások spontán
2017. január 30. Ellenőrzések, emberi felhasználásra szánt gyógyszerek farmakovigilancia és bizottságok EMA/749446/2016 Revision 1* Útmutató a gyógyszerekkel szembeni, feltételezett mellékhatások spontán
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 57 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
IV. melléklet Tudományos következtetések 57 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
MabThera. rituximab. Milyen típusú gyógyszer a MabThera? Milyen betegségek esetén alkalmazható a MabThera? EPAR-összefoglaló a nyilvánosság számára
 EMA/614203/2010 EMEA/H/C/000165 EPAR-összefoglaló a nyilvánosság számára rituximab Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi
EMA/614203/2010 EMEA/H/C/000165 EPAR-összefoglaló a nyilvánosság számára rituximab Ez a dokumentum a -ra vonatkozó európai nyilvános értékelő jelentés (EPAR) összefoglalója. Azt mutatja be, hogy az emberi
Online jelentés felhasználói útmutató
 Beteg egészségvédelem Ez az online jelentés felhasználói útmutató az online jelentés adatelemeivel, szerkezetével, értelmezésével és funkcióival kapcsolatban nyújt tájékoztatást. 1. Adatelemek... 2 2.
Beteg egészségvédelem Ez az online jelentés felhasználói útmutató az online jelentés adatelemeivel, szerkezetével, értelmezésével és funkcióival kapcsolatban nyújt tájékoztatást. 1. Adatelemek... 2 2.
Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból
 25 February 2016 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2016. február 8-11-i ülésén elfogadva Az ebben
25 February 2016 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2016. február 8-11-i ülésén elfogadva Az ebben
PRAC ajánlások a kísérőiratok frissítését igénylő szignálokkal kapcsolatban
 2015. január 22. Farmakovigilancia kockázatértékelő bizottság (Pharmacovigilance Risk Assessment Committee- PRAC) PRAC ajánlások a kísérőiratok frissítését igénylő szignálokkal kapcsolatban A PRAC 2015.
2015. január 22. Farmakovigilancia kockázatértékelő bizottság (Pharmacovigilance Risk Assessment Committee- PRAC) PRAC ajánlások a kísérőiratok frissítését igénylő szignálokkal kapcsolatban A PRAC 2015.
Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból
 15 September 2016 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2016. augusztus 30-szeptember 2-i ülésén elfogadva
15 September 2016 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2016. augusztus 30-szeptember 2-i ülésén elfogadva
Nincs egyértelmű bizonyíték a szívproblémáknak a tesztoszteront tartalmazó gyógyszerekkel kapcsolatos fokozott kockázatára
 2014. november 21. EMA/706140/2014 Nincs egyértelmű bizonyíték a szívproblémáknak a tesztoszteront tartalmazó gyógyszerekkel kapcsolatos fokozott kockázatára A CMDh 1, amely az uniós tagállamokat képviselő
2014. november 21. EMA/706140/2014 Nincs egyértelmű bizonyíték a szívproblémáknak a tesztoszteront tartalmazó gyógyszerekkel kapcsolatos fokozott kockázatára A CMDh 1, amely az uniós tagállamokat képviselő
Az Európai Gyógyszerügynökség a metoklopramid alkalmazásának módosítását javasolja
 2013. december 20. Corr. 1 Az Európai Gyógyszerügynökség a metoklopramid alkalmazásának módosítását A változtatások célja főként a neurológiai mellékhatások kockázatának csökkentése Október 24-én az Európai
2013. december 20. Corr. 1 Az Európai Gyógyszerügynökség a metoklopramid alkalmazásának módosítását A változtatások célja főként a neurológiai mellékhatások kockázatának csökkentése Október 24-én az Európai
Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból
 10 November 2016 EMA/PRAC/730045/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2016. október 24-27-i ülésén
10 November 2016 EMA/PRAC/730045/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Új kísérőirat szövegezés Kivonatok a PRAC szignálokkal kapcsolatos ajánlásaiból A PRAC 2016. október 24-27-i ülésén
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA
 III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA Az alkalmazási előírás és a betegtájékoztató módosításai a Bizottság Határozatával egyidőben lépnek érvénybe. A Bizottsági Határozat
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA Az alkalmazási előírás és a betegtájékoztató módosításai a Bizottság Határozatával egyidőben lépnek érvénybe. A Bizottsági Határozat
IV. MELLÉKLET TUDOMÁNYOS KÖVETKEZTETÉSEK
 IV. MELLÉKLET TUDOMÁNYOS KÖVETKEZTETÉSEK Tudományos következtetések A hepatitisz B vírus (HBV) és hepatitisz C vírus (HCV) társfertőzés az átfedő terjedési mód miatt nem ritka. Ismeretes, hogy a HCV fertőzés
IV. MELLÉKLET TUDOMÁNYOS KÖVETKEZTETÉSEK Tudományos következtetések A hepatitisz B vírus (HBV) és hepatitisz C vírus (HCV) társfertőzés az átfedő terjedési mód miatt nem ritka. Ismeretes, hogy a HCV fertőzés
változások az SM kezelésében: tények és remények
 változások az SM kezelésében: tények és remények Prof. Dr. Illés Zsolt Dél-Dániai Egyetem Odense az SM klinikai típusai relapszussal remisszióval szekunderprogresszív primer progresszív progresszív relapszáló
változások az SM kezelésében: tények és remények Prof. Dr. Illés Zsolt Dél-Dániai Egyetem Odense az SM klinikai típusai relapszussal remisszióval szekunderprogresszív primer progresszív progresszív relapszáló
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL
 MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
List of nationally authorised medicinal products
 11 January 2018 EMA/32390/2018 Human Medicines Evaluation Division Active substance(s): eprosartan Procedure No.: PSUSA/00001243/201704 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone
11 January 2018 EMA/32390/2018 Human Medicines Evaluation Division Active substance(s): eprosartan Procedure No.: PSUSA/00001243/201704 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone
MELLÉKLET TUDOMÁNYOS KÖVETKEZTETÉSEK ÉS AZ ELUTASÍTÁS INDOKLÁSA AZ EMEA ÖSSZEÁLLÍTÁSÁBAN
 MELLÉKLET TUDOMÁNYOS KÖVETKEZTETÉSEK ÉS AZ ELUTASÍTÁS INDOKLÁSA AZ EMEA ÖSSZEÁLLÍTÁSÁBAN A NATALIZUMAB ELAN PHARMÁRA VONATKOZÓ 2007. JÚLIUS 19-I CHMP SZAKVÉLEMÉNY FELÜLVIZSGÁLATA A CHMP a 2007. júliusi
MELLÉKLET TUDOMÁNYOS KÖVETKEZTETÉSEK ÉS AZ ELUTASÍTÁS INDOKLÁSA AZ EMEA ÖSSZEÁLLÍTÁSÁBAN A NATALIZUMAB ELAN PHARMÁRA VONATKOZÓ 2007. JÚLIUS 19-I CHMP SZAKVÉLEMÉNY FELÜLVIZSGÁLATA A CHMP a 2007. júliusi
I. melléklet. Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása
 I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása 1 Tudományos következtetések Figyelembe véve a Farmakovigilanciai Kockázatértékelő
I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása 1 Tudományos következtetések Figyelembe véve a Farmakovigilanciai Kockázatértékelő
NÉV, GYÓGYSZERFORMA, HATÁSERŐSSÉG, ALKALMAZÁSI MÓD ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME AZ EURÓPAI UNIÓ TAGORSZÁGAIN BELÜL
 I. MELLÉKLET NÉV, GYÓGYSZERFORMA, HATÁSERŐSSÉG, ALKALMAZÁSI MÓD ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME AZ EURÓPAI UNIÓ TAGORSZÁGAIN BELÜL 1 EU Tagország Olaszország JÓD-KAZEINT/TIAMINT
I. MELLÉKLET NÉV, GYÓGYSZERFORMA, HATÁSERŐSSÉG, ALKALMAZÁSI MÓD ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJÁNAK NEVE ÉS CÍME AZ EURÓPAI UNIÓ TAGORSZÁGAIN BELÜL 1 EU Tagország Olaszország JÓD-KAZEINT/TIAMINT
Az Ügynökség évi munkaprogramja: bevezetés
 7 augusztus 2015 Ügyvezető igazgatóhelyettes Andreas Pott, ügyvezető igazgatóhelyettes Az EMA prioritásai és főbb befolyások Az európai gyógyszerészeti szabályozó rendszer egy olyan hálózaton alapul, amelynek
7 augusztus 2015 Ügyvezető igazgatóhelyettes Andreas Pott, ügyvezető igazgatóhelyettes Az EMA prioritásai és főbb befolyások Az európai gyógyszerészeti szabályozó rendszer egy olyan hálózaton alapul, amelynek
Biztos abban, hogy a megfelelő intézkedéseket teszi az influenza elleni védelem tekintetében? Oltassa be magát!
 Biztos abban, hogy a megfelelő intézkedéseket teszi az influenza elleni védelem tekintetében? Oltassa be magát! Influenza Egy súlyos betegség Az influenza minden évben a népesség 5% - 15%-át érinti. Az
Biztos abban, hogy a megfelelő intézkedéseket teszi az influenza elleni védelem tekintetében? Oltassa be magát! Influenza Egy súlyos betegség Az influenza minden évben a népesség 5% - 15%-át érinti. Az
I. melléklet. Tudományos következtetések
 I. melléklet Tudományos következtetések 1 Tudományos következtetések A daklizumab béta egy humanizált IgG1 monoklonális antitest, amely az IL-2 jelátvitelt befolyásolja azáltal, hogy a CD25-függő, nagy
I. melléklet Tudományos következtetések 1 Tudományos következtetések A daklizumab béta egy humanizált IgG1 monoklonális antitest, amely az IL-2 jelátvitelt befolyásolja azáltal, hogy a CD25-függő, nagy
I. melléklet Tudományos következtetések és a forgalomba hozatali engedélyek feltételei módosításának indoklása
 I. melléklet Tudományos következtetések és a forgalomba hozatali engedélyek feltételei módosításának indoklása Tudományos következtetések Figyelembe véve a farmakovigilanciai kockázatértékelő bizottságnak
I. melléklet Tudományos következtetések és a forgalomba hozatali engedélyek feltételei módosításának indoklása Tudományos következtetések Figyelembe véve a farmakovigilanciai kockázatértékelő bizottságnak
Az Ügynökség évi munkaprogramja: bevezetés
 2016. február 8. Ügyvezető igazgató Guido Rasi, ügyvezető igazgató Az EMA prioritási területei és a főbb befolyások Az európai gyógyszer-szabályozási hálózat egy olyan hálózaton alapul, amelynek tagjai
2016. február 8. Ügyvezető igazgató Guido Rasi, ügyvezető igazgató Az EMA prioritási területei és a főbb befolyások Az európai gyógyszer-szabályozási hálózat egy olyan hálózaton alapul, amelynek tagjai
Tudományos következtetések és következtetések indoklása
 Melléklet IV. Tudományos következtetések és a forgalomba hozatali engedélyek feltételei módosításának indoklása, valamint a PRAC ajánlástól való eltérések részletes magyarázata Tudományos következtetések
Melléklet IV. Tudományos következtetések és a forgalomba hozatali engedélyek feltételei módosításának indoklása, valamint a PRAC ajánlástól való eltérések részletes magyarázata Tudományos következtetések
Tudományos következtetések. A Prevora tudományos értékelésének átfogó összegzése
 II. MELLÉKLET AZ EURÓPAI GYÓGYSZERÜGYNÖKSÉG (EMA) ÁLTAL BETERJESZTETT TUDOMÁNYOS KÖVETKEZTETÉSEK, A POZITÍV VÉLEMÉNY, AZ ALKALMAZÁSI ELŐÍRÁS, A CÍMKESZÖVEG, VALAMINT A BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSÁNAK INDOKLÁSA
II. MELLÉKLET AZ EURÓPAI GYÓGYSZERÜGYNÖKSÉG (EMA) ÁLTAL BETERJESZTETT TUDOMÁNYOS KÖVETKEZTETÉSEK, A POZITÍV VÉLEMÉNY, AZ ALKALMAZÁSI ELŐÍRÁS, A CÍMKESZÖVEG, VALAMINT A BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSÁNAK INDOKLÁSA
I. melléklet Tudományos következtetések és az Európai Gyógyszerügynökség által kiadott forgalomba hozatali engedély felfüggesztésének indoklása
 I. melléklet Tudományos következtetések és az Európai Gyógyszerügynökség által kiadott forgalomba hozatali engedély felfüggesztésének indoklása 1 Tudományos következtetések A nikotinsav/laropiprant tudományos
I. melléklet Tudományos következtetések és az Európai Gyógyszerügynökség által kiadott forgalomba hozatali engedély felfüggesztésének indoklása 1 Tudományos következtetések A nikotinsav/laropiprant tudományos
Demyelinisatios betegségek
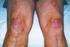 Demyelinisatios betegségek Dr. Zsigmond Ildikó MR Kutatóközpont, Mediworld Plus Kft., Mediworld Diagnosztika Kft. 2013. május 24. Székesfehérvár A fehérállomány: - Az idegsejtek velőshüvellyel borított
Demyelinisatios betegségek Dr. Zsigmond Ildikó MR Kutatóközpont, Mediworld Plus Kft., Mediworld Diagnosztika Kft. 2013. május 24. Székesfehérvár A fehérállomány: - Az idegsejtek velőshüvellyel borított
Alkalmazási előírás. 4.2 Adagolás és alkalmazás. 4.3 Ellenjavallatok
 A Strattera (atomoxetine) hatásai a vérnyomásra és a szívfrekvenciára a forgalomba hozatali engedély jogosultja (MAH) által végzett klinikai vizsgálat adatainak felülvizsgálata alapján. Végleges SPC és
A Strattera (atomoxetine) hatásai a vérnyomásra és a szívfrekvenciára a forgalomba hozatali engedély jogosultja (MAH) által végzett klinikai vizsgálat adatainak felülvizsgálata alapján. Végleges SPC és
Az Metacam-ra vonatkozó áttekintés és az EU-ban való engedélyezésének indoklása
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Az Metacam-ra vonatkozó áttekintés és az EU-ban való engedélyezésének indoklása Milyen típusú készítmény a Metacam és milyen betegségek esetén alkalmazható? A Metacam
EMA/CVMP/259397/2006 EMEA/V/C/000033 Az Metacam-ra vonatkozó áttekintés és az EU-ban való engedélyezésének indoklása Milyen típusú készítmény a Metacam és milyen betegségek esetén alkalmazható? A Metacam
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 61 Tudományos következtetések Háttér-információ A ponatinib egy tirozin-kináz inhibitor (TKI), amelyet a natív BCR-ABL, valamint minden mutáns variáns kináz beleértve
IV. melléklet Tudományos következtetések 61 Tudományos következtetések Háttér-információ A ponatinib egy tirozin-kináz inhibitor (TKI), amelyet a natív BCR-ABL, valamint minden mutáns variáns kináz beleértve
I. melléklet. Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása
 I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása 1 Tudományos következtetések Figyelembe véve a Farmakovigilancia Kockázatértékelő
I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása 1 Tudományos következtetések Figyelembe véve a Farmakovigilancia Kockázatértékelő
Az Európai Gyógyszerügynökség 2006-ban
 European Medicines Agency EMEA/2323/27/HU/VÉGLEGES Az EMEA tizenkettedik éves jelentésének összefoglalója Ez a dokumentum az EMEA 26. évi éves jelentésének összefoglalója. Az EMEA 26. évi teljes éves jelentését
European Medicines Agency EMEA/2323/27/HU/VÉGLEGES Az EMEA tizenkettedik éves jelentésének összefoglalója Ez a dokumentum az EMEA 26. évi éves jelentésének összefoglalója. Az EMEA 26. évi teljes éves jelentését
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA. Tramalgic 50 mg kemény kapszula tramadol-hidroklorid
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Tramalgic 50 mg kemény kapszula tramadol-hidroklorid Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót. -
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Tramalgic 50 mg kemény kapszula tramadol-hidroklorid Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót. -
I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása
 I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása 1 Tudományos következtetések Figyelembe véve a Farmakovigilancia Kockázatértékelő
I. melléklet Tudományos következtetések és a forgalomba hozatali engedély(ek) feltételeit érintő módosítások indoklása 1 Tudományos következtetések Figyelembe véve a Farmakovigilancia Kockázatértékelő
II. melléklet. Tudományos következtetések
 II. melléklet Tudományos következtetések 10 Tudományos következtetések A Solu-Medrol 40 mg por és oldószer oldatos injekcióhoz (a továbbiakban Solu-Medrol ) készítmény metilprednizolont és segédanyagként
II. melléklet Tudományos következtetések 10 Tudományos következtetések A Solu-Medrol 40 mg por és oldószer oldatos injekcióhoz (a továbbiakban Solu-Medrol ) készítmény metilprednizolont és segédanyagként
31/2015. (VI. 12.) EMMI rendelet egyes egészségbiztosítási és gyógyszerészeti tárgyú miniszteri rendeletek módosításáról 1
 31/2015. (VI. 12.) EMMI rendelet egyes egészségbiztosítási és gyógyszerészeti tárgyú miniszteri rendeletek módosításáról 1 hatályos: 2015.06.13-2015.06.14 Tartalom: Az egészségügyi szakellátás társadalombiztosítási
31/2015. (VI. 12.) EMMI rendelet egyes egészségbiztosítási és gyógyszerészeti tárgyú miniszteri rendeletek módosításáról 1 hatályos: 2015.06.13-2015.06.14 Tartalom: Az egészségügyi szakellátás társadalombiztosítási
ÁLLATOK KLINIKAI VIZSGÁLATAI
 ÁLLATOK KLINIKAI VIZSGÁLATAI ---------------------------------------------------------------------------------------------------- Állatokon végzett tanulmányok A CV247 két kutatásban képezte vizsgálat
ÁLLATOK KLINIKAI VIZSGÁLATAI ---------------------------------------------------------------------------------------------------- Állatokon végzett tanulmányok A CV247 két kutatásban képezte vizsgálat
Familiáris mediterrán láz
 www.printo.it/pediatric-rheumatology/hu/intro Familiáris mediterrán láz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? Általában a következő módszert követik: Klinikai gyanú: az FMF
www.printo.it/pediatric-rheumatology/hu/intro Familiáris mediterrán láz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? Általában a következő módszert követik: Klinikai gyanú: az FMF
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Flexove 625 mg Tabletta Szájon át történő alkalmazás 1327 Lysaker, Norvégia Belgium - Navamedic ASA Vollsveien 13 C 1327 Lysaker, Norvégia
 I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN 1 Tagállam Forgalomba hozatali engedély
I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN 1 Tagállam Forgalomba hozatali engedély
Tudományos következtetések
 II. melléklet Tudományos következtetések, a forgalomba hozatali engedélyek visszavonásának illetve a forgalomba hozatali engedélyek feltételeit érintő változásnak az indoklása, valamint a PRAC ajánlásaitól
II. melléklet Tudományos következtetések, a forgalomba hozatali engedélyek visszavonásának illetve a forgalomba hozatali engedélyek feltételeit érintő változásnak az indoklása, valamint a PRAC ajánlásaitól
BETEGTÁJÉKOZTATÓ RHEUMATOID ARTHRITISBEN SZENVEDŐ BETEGEK SZÁMÁRA I. RHEUMATOID ARTHRITIS. origamigroup. www.origami.co.hu
 BETEGTÁJÉKOZTATÓ RHEUMATOID ARTHRITISBEN SZENVEDŐ BETEGEK SZÁMÁRA I. RHEUMATOID ARTHRITIS origamigroup www.origami.co.hu I. Rheumatoid arthritis Sokat hallunk napjainkban az immunrendszernek az egészség
BETEGTÁJÉKOZTATÓ RHEUMATOID ARTHRITISBEN SZENVEDŐ BETEGEK SZÁMÁRA I. RHEUMATOID ARTHRITIS origamigroup www.origami.co.hu I. Rheumatoid arthritis Sokat hallunk napjainkban az immunrendszernek az egészség
III. melléklet. A kísérőiratok vonatkozó pontjaiba bevezetendő módosítások
 III. melléklet A kísérőiratok vonatkozó pontjaiba bevezetendő módosítások Megjegyzés: Ezen kísérőiratok annak a referál eljárásnak az eredményeként készültek, amelyre a Bizottság e döntése vonatkozik.
III. melléklet A kísérőiratok vonatkozó pontjaiba bevezetendő módosítások Megjegyzés: Ezen kísérőiratok annak a referál eljárásnak az eredményeként készültek, amelyre a Bizottság e döntése vonatkozik.
Méhnyakszűrés: Vizsgálati eredmények magyarázata. Frissített útmutató
 Méhnyakszűrés: Vizsgálati eredmények magyarázata Frissített útmutató Page 2 Ebben a betegtájékoztatóban a méhnyakszűrés eredményét magyarázzuk el, amely vizsgálat célja a méhnyak (a méh alsó része) sejtjeiben
Méhnyakszűrés: Vizsgálati eredmények magyarázata Frissített útmutató Page 2 Ebben a betegtájékoztatóban a méhnyakszűrés eredményét magyarázzuk el, amely vizsgálat célja a méhnyak (a méh alsó része) sejtjeiben
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ. Radiográfus szakképesítés. 2425-06 Klinikum a képalkotásban modul. 1. vizsgafeladat. 2013. május 15.
 Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az interaktív vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az interaktív vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
A sclerosis. és kezelése. A Minden nap mozgásban program elérhetőségei Információs vonal: +36 30 694 31 21. Pearl Hungary Kft.
 A sclerosis multiplex és kezelése A Minden nap mozgásban program elérhetőségei Információs vonal: +36 30 694 31 21 Pearl Hungary Kft. 1142 Budapest, Erzsébet királyné útja 112. A Minden nap mozgásban program
A sclerosis multiplex és kezelése A Minden nap mozgásban program elérhetőségei Információs vonal: +36 30 694 31 21 Pearl Hungary Kft. 1142 Budapest, Erzsébet királyné útja 112. A Minden nap mozgásban program
Neurológiai Továbbképzı Tanfolyam Pécs, 2008. Bors László PTE Neurológiai Klinika
 SCLEROSIS MULTIPLEX A GYAKORLATBAN Neurológiai Továbbképzı Tanfolyam Pécs, 2008. Bors László PTE Neurológiai Klinika NEM EGYSÉGES A KLINIKAI MEGJELENÉS NEM EGYSÉGES A PATHOLÓGIA NEM EGYSÉGES A PATHOGENETIKA
SCLEROSIS MULTIPLEX A GYAKORLATBAN Neurológiai Továbbképzı Tanfolyam Pécs, 2008. Bors László PTE Neurológiai Klinika NEM EGYSÉGES A KLINIKAI MEGJELENÉS NEM EGYSÉGES A PATHOLÓGIA NEM EGYSÉGES A PATHOGENETIKA
III. melléklet. Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteit érintő módosítások
 III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteit érintő módosítások Megjegyzés: Az alkalmazási előírás és a betegtájékoztató módosításait értelemszerűen a referencia-tagállammal
III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteit érintő módosítások Megjegyzés: Az alkalmazási előírás és a betegtájékoztató módosításait értelemszerűen a referencia-tagállammal
NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú
 NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú meghatározása. (Megj.: a felsorolt esetekben meghatározó
NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú meghatározása. (Megj.: a felsorolt esetekben meghatározó
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? A klinikai jelek és a vizsgálatok
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 Hogyan diagnosztizálható? A klinikai jelek és a vizsgálatok
A rheumatoid arthritises (RA) betegek ellátásának standard követelményei
 A rheumatoid arthritises (RA) betegek ellátásának standard követelményei Translation into: Completed by: Email: SOC 1 SOC 2 HUNGARIAN Dr. Géza BÁLINT bjd@t-online.hu Az RA tüneteivel jelentkező betegnek
A rheumatoid arthritises (RA) betegek ellátásának standard követelményei Translation into: Completed by: Email: SOC 1 SOC 2 HUNGARIAN Dr. Géza BÁLINT bjd@t-online.hu Az RA tüneteivel jelentkező betegnek
Ritka Gyermekkori Elsődleges Szisztémás Vaszkulitisz
 https://www.printo.it/pediatric-rheumatology/hu/intro Ritka Gyermekkori Elsődleges Szisztémás Vaszkulitisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 A vaszkulitisz típusai és osztályozása A gyermekkori vaszkulitiszt
https://www.printo.it/pediatric-rheumatology/hu/intro Ritka Gyermekkori Elsődleges Szisztémás Vaszkulitisz Verzió 2016 2. DIAGNÓZIS ÉS TERÁPIA 2.1 A vaszkulitisz típusai és osztályozása A gyermekkori vaszkulitiszt
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Prepandrix szuszpenzió és emulzió emulziós injekcióhoz Prepandémiás influenza (H5N1) vakcina (split virion, inaktivált, adjuvánshoz kötött) Mielőtt elkezdené
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Prepandrix szuszpenzió és emulzió emulziós injekcióhoz Prepandémiás influenza (H5N1) vakcina (split virion, inaktivált, adjuvánshoz kötött) Mielőtt elkezdené
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Cetirizin-ratiopharm 10 mg filmtabletta Cetirizin-ratiopharm 10 mg filmtabletta
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Cetirizin-ratiopharm 10 mg filmtabletta Cetirizin-ratiopharm 10 mg filmtabletta
Szklerózis Multiplex a munkahelyen: A munkaadók kézikönyve
 Szklerózis Multiplex a munkahelyen: A munkaadók kézikönyve Készült a Magyar Sclerosis Multiplex Társaság és a Sclerosis Multiplexes Betegek Országos Egyesületének szakmai útmutatása alapján Ez a kiadvány
Szklerózis Multiplex a munkahelyen: A munkaadók kézikönyve Készült a Magyar Sclerosis Multiplex Társaság és a Sclerosis Multiplexes Betegek Országos Egyesületének szakmai útmutatása alapján Ez a kiadvány
Prof Dr. Pajor Attila Szülész-nőgyógyász, egyetemi tanár AUTOIMMUN BETEGSÉGEK ÉS TERHESSÉG
 Prof Dr. Pajor Attila Szülész-nőgyógyász, egyetemi tanár AUTOIMMUN BETEGSÉGEK ÉS TERHESSÉG Melyik autoimmun betegség érinti a szülőképes nőket? Izületi betegségek : RA, SLE Pajzsmirigy betegségek: Kevert
Prof Dr. Pajor Attila Szülész-nőgyógyász, egyetemi tanár AUTOIMMUN BETEGSÉGEK ÉS TERHESSÉG Melyik autoimmun betegség érinti a szülőképes nőket? Izületi betegségek : RA, SLE Pajzsmirigy betegségek: Kevert
ÚJSÁGÍRÓ ISMERETTERJESZTŐ/PROMÓCIÓS HONLAP A MÉHNYAKRÁK MEGELŐZÉSÉÉRT
 ISMERETTERJESZTŐ/PROMÓCIÓS HONLAP A MÉHNYAKRÁK MEGELŐZÉSÉÉRT Dömötörfy Zsolt PÁLYÁZÓ Dömötörfy Zsolt Istenhegyi Géndiagnosztikai Centrum www.hpv-mehnyakrak.hu A méhnyakrák áldozatai Magyarországon napjainkban
ISMERETTERJESZTŐ/PROMÓCIÓS HONLAP A MÉHNYAKRÁK MEGELŐZÉSÉÉRT Dömötörfy Zsolt PÁLYÁZÓ Dömötörfy Zsolt Istenhegyi Géndiagnosztikai Centrum www.hpv-mehnyakrak.hu A méhnyakrák áldozatai Magyarországon napjainkban
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3,
 Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
II. melléklet. Tudományos következtetések
 II. melléklet Tudományos következtetések 74 Tudományos következtetések Az Egyesült Királyság 2016. július 7-én a 2001/83/EK irányelv 31. cikke szerint farmakovigilanciai adatokon alapuló beterjesztési
II. melléklet Tudományos következtetések 74 Tudományos következtetések Az Egyesült Királyság 2016. július 7-én a 2001/83/EK irányelv 31. cikke szerint farmakovigilanciai adatokon alapuló beterjesztési
A sclerosis multiplex diagnosztikája és kezelése
 Finanszírozási protokoll Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010. július 15. Azonosítószám: 23/2010 1. Azonosítószám: 23/2010 2. Az
Finanszírozási protokoll Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010. július 15. Azonosítószám: 23/2010 1. Azonosítószám: 23/2010 2. Az
A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat.
 A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat. A rotavírus az egyik leggyakoribb okozója a súlyos hasmenésnek csecsemő és kisdedkorban. Évente világszerte
A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat. A rotavírus az egyik leggyakoribb okozója a súlyos hasmenésnek csecsemő és kisdedkorban. Évente világszerte
Rovarméreg (méh, darázs) - allergia
 Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Beutalást igénylô állapotok. A beutalás az emlôbetegséggel foglalkozó sebészhez történjen. Minden új, körülírt csomó.
 Az emlôpanaszos nôk beutalásának irányelve (Guidelines for the referral of patients with breast problems) NHS Breast Screening Programme & The Cancer Research Campaign Elôszó Az emlôrák a nôket érintô
Az emlôpanaszos nôk beutalásának irányelve (Guidelines for the referral of patients with breast problems) NHS Breast Screening Programme & The Cancer Research Campaign Elôszó Az emlôrák a nôket érintô
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Az egészségügyi szakembereket arra kérjük,
LUPUSZ KVÍZ. Kérdések, megoldások, ajándéksorsolás. 2012. december 1.
 LUPUSZ KVÍZ Kérdések, megoldások, ajándéksorsolás 2012. december 1. 1. kérdés: Mi történik egy lupuszos beteg immunrendszerében? A Az immunrendszer túl kevés antitestet termel. B Az immunrendszer antitesteket
LUPUSZ KVÍZ Kérdések, megoldások, ajándéksorsolás 2012. december 1. 1. kérdés: Mi történik egy lupuszos beteg immunrendszerében? A Az immunrendszer túl kevés antitestet termel. B Az immunrendszer antitesteket
1. MILYEN BETEGSÉGEK ESETÉN ALKALMAZHATÓ ÉS HOGYAN FEJTI KI HATÁSÁT A LAMOTRIGINE HEXAL TABLETTA?
 LAMOTRIGINE HEXAL 25 MG TABLETTA Lamotrigine HEXAL 25 mg tabletta Lamotrigine HEXAL 50 mg tabletta Lamotrigine HEXAL 100 mg tabletta Hatóanyag: 25 mg, 50 mg, ill. 100 mg lamotrigin tablettánként. Segédanyagok:
LAMOTRIGINE HEXAL 25 MG TABLETTA Lamotrigine HEXAL 25 mg tabletta Lamotrigine HEXAL 50 mg tabletta Lamotrigine HEXAL 100 mg tabletta Hatóanyag: 25 mg, 50 mg, ill. 100 mg lamotrigin tablettánként. Segédanyagok:
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ Mielőtt elkezdené gyógyszerét alkalmazni,
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ Mielőtt elkezdené gyógyszerét alkalmazni,
Ez az alkalmazási előírás és a betegtájékoztató az előterjesztési eljárás eredménye alapján jött létre.
 II. melléklet Az alkalmazási előírás és a betegtájékoztató módosítása az Európai Gyógyszerügynökség előterjesztésére Ez az alkalmazási előírás és a betegtájékoztató az előterjesztési eljárás eredménye
II. melléklet Az alkalmazási előírás és a betegtájékoztató módosítása az Európai Gyógyszerügynökség előterjesztésére Ez az alkalmazási előírás és a betegtájékoztató az előterjesztési eljárás eredménye
Foglalkozás-egészségügyi Alapellátás
 Foglalkozás-egészségügyi Alapellátás Foglalkozás-egészségügyi alapellátás Szakmakód: 2501 Tevékenységek progresszivitási szint szerinti besorolása Foglalkozás-egészségügy Progresszivitási szint I. alapellátás
Foglalkozás-egészségügyi Alapellátás Foglalkozás-egészségügyi alapellátás Szakmakód: 2501 Tevékenységek progresszivitási szint szerinti besorolása Foglalkozás-egészségügy Progresszivitási szint I. alapellátás
I. MELLÉKLET MEGNEVEZÉSEK, GYÓGYSZERFORMÁK, HATÁSERŐSSÉGEK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
 I. MELLÉKLET MEGNEVEZÉSEK, GYÓGYSZERFORMÁK, HATÁSERŐSSÉGEK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN Tagállam Forgalomba hozatali engedély jogosultja Termék törzskönyvezett
I. MELLÉKLET MEGNEVEZÉSEK, GYÓGYSZERFORMÁK, HATÁSERŐSSÉGEK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN Tagállam Forgalomba hozatali engedély jogosultja Termék törzskönyvezett
Törzskönyvezett megnevezés. Lipophoral Tablets 150mg. Mediator 150 mg Tabletta Oralis alkalmazás. Benfluorex Qualimed
 I. MELLÉKLET A GYÓGYSZEREK FANTÁZIANEVEINEK, GYÓGYSZERFORMÁINAK ÉS ERŐSSÉGÉNEK, AZ ADAGOLÁS MÓDJÁNAK ÉS A TAGÁLLAMOKBELI (EGT) FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAINAK FELSOROLÁSA 1 Tagállam Ciprus
I. MELLÉKLET A GYÓGYSZEREK FANTÁZIANEVEINEK, GYÓGYSZERFORMÁINAK ÉS ERŐSSÉGÉNEK, AZ ADAGOLÁS MÓDJÁNAK ÉS A TAGÁLLAMOKBELI (EGT) FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAINAK FELSOROLÁSA 1 Tagállam Ciprus
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára Lamictal 25 mg tabletta Lamictal 50 mg tabletta Lamictal 100 mg tabletta Lamictal 2 mg rágótabletta/diszpergálódó tabletta Lamictal 5 mg rágótabletta/diszpergálódó
Betegtájékoztató: Információk a felhasználó számára Lamictal 25 mg tabletta Lamictal 50 mg tabletta Lamictal 100 mg tabletta Lamictal 2 mg rágótabletta/diszpergálódó tabletta Lamictal 5 mg rágótabletta/diszpergálódó
A kockázatértékelés során gyakran elkövetett hibák. Európai kampány a kockázatértékelésről
 A kockázatértékelés során gyakran elkövetett hibák Európai kampány a kockázatértékelésről Megelőzés jogi háttér A jogszabály szerint az EU-ban a munkáltatók kötelesek megakadályozni, hogy a munkavállalókat
A kockázatértékelés során gyakran elkövetett hibák Európai kampány a kockázatértékelésről Megelőzés jogi háttér A jogszabály szerint az EU-ban a munkáltatók kötelesek megakadályozni, hogy a munkavállalókat
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 1 Tudományos következtetések A nátrium-glükóz kotranszporter-2 (SGLT2) inhibitorokat 2-es típusú cukorbetegeknél alkalmazzák diéta és testmozgás mellett önmagukban
IV. melléklet Tudományos következtetések 1 Tudományos következtetések A nátrium-glükóz kotranszporter-2 (SGLT2) inhibitorokat 2-es típusú cukorbetegeknél alkalmazzák diéta és testmozgás mellett önmagukban
Jelentés az Európai Gyógyszerügynökség 2014-es pénzügyi évre vonatkozó éves beszámolójáról. az Ügynökség válaszával együtt
 Jelentés az Európai Gyógyszerügynökség 2014-es pénzügyi évre vonatkozó éves beszámolójáról az Ügynökség válaszával együtt 12, rue Alcide De Gasperi - L - 1615 Luxembourg T (+352) 4398 1 E eca-info@eca.europa.eu
Jelentés az Európai Gyógyszerügynökség 2014-es pénzügyi évre vonatkozó éves beszámolójáról az Ügynökség válaszával együtt 12, rue Alcide De Gasperi - L - 1615 Luxembourg T (+352) 4398 1 E eca-info@eca.europa.eu
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! z alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Skinoren krém Skinoren krém Mielőtt elkezdené alkalmazni ezt a gyógyszert,
FIGYELEM!!! z alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Skinoren krém Skinoren krém Mielőtt elkezdené alkalmazni ezt a gyógyszert,
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Zonegran 25 mg szájban diszpergálódó tabletta Zonegran 50 mg szájban diszpergálódó tabletta Zonegran 100 mg szájban diszpergálódó tabletta Zonegran 300
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Zonegran 25 mg szájban diszpergálódó tabletta Zonegran 50 mg szájban diszpergálódó tabletta Zonegran 100 mg szájban diszpergálódó tabletta Zonegran 300
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmesen
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 1 Tudományos következtetések A Lemtrada-ra vonatkozó (EMEA/H/C/PSUSA/00010055/201809) időszakos gyógyszerbiztonsági jelentés (PSUSA) értékelése során a következő
IV. melléklet Tudományos következtetések 1 Tudományos következtetések A Lemtrada-ra vonatkozó (EMEA/H/C/PSUSA/00010055/201809) időszakos gyógyszerbiztonsági jelentés (PSUSA) értékelése során a következő
Az RP-info (Rendeletek, Protokollok, Gyógyszer információk) szoftver bemutatása
 Az RP-info (Rendeletek, Protokollok, Gyógyszer információk) szoftver bemutatása Az RP-info egy orvosok számára kifejlesztett információs rendszer, amely a betegellátás során felmerülő szakmai kérdések
Az RP-info (Rendeletek, Protokollok, Gyógyszer információk) szoftver bemutatása Az RP-info egy orvosok számára kifejlesztett információs rendszer, amely a betegellátás során felmerülő szakmai kérdések
II. melléklet. Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása
 II. melléklet Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása 7 Tudományos következtetések A Cymevene i.v. és kapcsolódó nevek (lásd I. melléklet)
II. melléklet Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása 7 Tudományos következtetések A Cymevene i.v. és kapcsolódó nevek (lásd I. melléklet)
