< Az ásványokról
|
|
|
- Erzsébet Budainé
- 8 évvel ezelőtt
- Látták:
Átírás
1 < SZAKTÁRGYAK Soós Károlynéi Az ásványokról Mlllnsr Tivadari "Az ásványok színs" címtf cikkének /Természet Világa I.szám/ olvasása indított arra, hogy néhány gondolatot írjak az ásványok keletkezéséről, lelőhelyéről és természetesen színéről is. Úgy gondolom jól hasznosíthatjuk ezeket a kémia órákon. Már mindnyájan Jártunk a Magyar Nemzeti Múzeum Ásvány- és Kőzettani Kiállításán, és csodálkozva nézetettük mi is a szebbnél-szebb ásványokat. Kit ne ragadott volna meg Firenzében járva a Ponté Vecchio roskadásig megtelt ékszer üzleteinek kirakatában a csiszolt és a csiszolatlan kristályok, a vörös Jáspisok, a kék zafírok, a lila ametisztek vagy a sokféle más drágakő ragyogáss. Hol találjuk az ásványokat? A földkéreg felső, több kilométer vastag, 9zilérd részét kőzetek alkotják. A kőzetek ásványokból állnak, melyek hegyek szikláiban, folyók hordalékában, sivatagok homokjában vagy éppen tíüzhányó-hegyek üregeiben találhatók. Az ásványok kristályos szerkezetűek. A kristályt síklapok határolják. A lapok elrendeződése mindig bizonyos szimmetria szerint történik. A kristályok kül6ő szabályos alakja és belső felépítése között szoros kapcsolat van. A kristályt a középpontján áthaladó egy vagy több síkkal két olyan félre oszthstjuk, amelyek egymásnak tükörképei, vagyis szimmetrikusak egymással. A kristályokat szimmetria alapján 32 kristályosztályba soroljuk. A 32 kristályosztály hót kristályrendszerbe tartozik.
2 34 - így ismeretes: I. Szabályos rendszer II. Hatszögéé -"- III. Háromszöges IV. Négyzetes V. Rombos VI. Egyhajíású VII. Háromhajlású -"- A kristálylapok egymást élekben metszik, ée az élek csúcsban futnak össze. A lapok, élek, csúcsok együttvéve a kristály határoló elemei. Egy bizonyos anyag kristályainak meghatározott lapjai és élei által bezárt szög az illető anyagra jellemző, állandó érték. Ez az érték a nyomáé és a hőmérséklet hatására is csak keveset változik. Hogyan keletkeztek az ásványok? A Föld szilárd kérge alatt találjuk a magmát. A magma görög szó, tésztát jelent. Ez a szó is arra utal, hogy az izzó olvadék nagyon képlékeny. A magma az idők folyamán lehűl ós megszilárdul. A magma a Föld felszíne felé törekedve a kőzetek repedéseibe jut - miközben a mélyből a forróvizes oldatok is féltörnek - és így keletkeznek az arany és ezüst telérek. Ezek a hidrotermális eredetű ásványok. Oe keletkezhet ásvány más módon is. Például a termésekén a földkéreg legfelső réezóben, néha a felszínen jelenik meg. Vulkáni kitöréskor vagy a vulkáni utóhatás során a földfelszínre törő gázok és gőzök termékeként keletkezik. Elmondhatjuk tehát, hogy az anyag olvadékának lehüléee, túltelített oldatokból való kiválása vagy gőzökből gázokból való kicsapódás révén kerül s'zilárd, kristályos állapotba. A túlhűlt olvadékok /pl. természetes üvegek/ és a víztartalmukat lassan elveezitő kolloidok /pl.: opál/ lassan szintén szabályos belső szerkezetet nyernek és az alaktalan állapotból kristályos állapotba mennek át
3 < A márvány csupa apró, villogó kristálvszemeoskéeből áll. Az egyes szsmscskéknek sem helyük, sem idejük nem volt ahhoz, hogy lapokkal körülhatárolt kristályokká fejlődhessenek* A hirtelen kristályosodó anyagban a szemecskék egymáet akadályozták a növekedésben* Az ilyen f nem kristálylapokkal határolt, csupa egymás mellé szorult kristályszemecakékből álló anyagot kristályosnak mondjuk. Amennyiben a kristályosodó anyagnak hely és idő áll a rendelkezésére, és a kristályok nem akadályozzák egymást növekedésükben, úgy jól fejlett, sík*lapok által határolt kristályok keletkeznek, vagyis az anyag kristáiyosodott A kristályok nagysága tág határok között mozog. A nagyságot a rendelkezésre élló anyagmennyiségen kivül a kristály keletkezésekor uralkodó hőmérséklet, nyomás, ez oldat vagy olvadék viszkozitása, a rendelkezésre álló idő é* hely határozza meg. Például a kvarcból mikroszkópi kicsinységfi kristályok mell'ett több tonnás példányokat is ismerünk. Sokszor találkozunk úgynevezett zárványokkal A zárványok azok < a gáz, cseppfolyós vagy szilárd anyagok, amelyeket növekedése közben zárt körül a kristály. A gáz és a folyadékzárvány fehér színűre, a nagyobb tömegű szilárd zárvány a legkülönbözőbb színűre színezi a gazdaásványt. Tehát az ásványok általában színesek. Az átlátszó világossárga topáz,., a gyémántfényű cinóbervörös proustit, a nem átlátszó zöld smaragd, a kagylóetőrésü opál, - amelynél az alapszínből különböző színű foltok gyakran éles határral, mozaikszerűe/i válnak ki, mig máskor lágyan olvadnak egymásba - a színek és a fények változatos skáláját mutatják. Színük ezerint a tudomány az ásványokat két nagy csoportra osztja, vannak idiokromés /saját színű/ és allokromá* /idegenszínű/ ásványok.
4 36 - Idiokromás ásványoknak nevezzük azokat az ásványokat, amelyeknek színe összetételük egyik komponensétől ered Például a rodokrozit színe rózssezín. Kémiai összetétele: MnC0 3 /mangánkarbonát/. Ebben ez esetben a szép rózsaszín a mangán /II/-ionoktól ered, melyből felépül a kristály. Allokromás ásványok azok az ásványok, amelyek színe nem a fő komponenstől, hanem az ezek mellett kismértékben jelenlévő idegen atomoktól származik. Például a korund, az alumíniumoxid színtelen ásvány. Ha azonban a korund kristályrácsába o,5-2 %-ban krómoxid /Cr o0^/ épül be, a krie- tr tály égő vörös színű lesz, és rubinról beszélünk. Azokban az esetekben, amikor a színező anyag annyira finoman elosztott, hogy a színezett ásvány teljesen átlátszó marad, a ezínsző anyagot nsm lehet lótni benne, dilut színezésről beszélünk. Ilyen a rubin is. Ha magában színtelen berillbe /Be 2Al 2Si 6O 10/ króm/iii/-ionok épülnek be, akkor a krietály zöld színű lesz. Ilyenkor a berillt smaragdnak nevezzük. Az allokrómás színt tehát általábsn az idegen atom ionkörnyezete váltja ki. Már régen felismerték, hogy egyes ásványok szinét az Idegen atom vegyértéke is befolyásolja. Például a három vegyértékű vas általában sárgára, barnára Ízín$z, míg a két vegyértéké vas világoszöld ezínt okoz. Ezt láthatjuk az egyébként ezíntelen ezfelerit /ZnS/ esetében is. Ha viszont mindkét ión, vas/iii/ ós vas/ii/ ión együttesen van jelen az ásványban, mély kék színt idéz elő. Nagyon érdekes az a jelenség, hogy azonos két vegyértékű rézionok adnak zöld színt a malechitnak és kék ezínt az azuritnak. A vizsgálatok szerint a szomszédos ionok különbözősége a döntő tényező. Millner Tivadar cikkében rámutat arra, hogy a zafira kék színű korund- nyomokban sem tartalmaz kobaltot, mint azt korábban hitték. A zafir allokrómás ásvány ugyan, de
5 < A márvány csupa apró, villogó kristálvszemgoekéltböl áll. Az egyss szsmscskéknsk sem helyük, sem idejük nem volt ahhoz, hogy lapokkal körülhatárolt kristályokká fejlődhessenek* A hirtelen kristályosodó anyagban a szemecskák egymást akadályozták a növekedésben* Az ilyen, nem kristály lapokkal határolt, csupa egymás mellé szorult kristályszemecekékből álló anyagot kristályosnak mondjuk* Amennyiben a kristályosodó anyagnak hely és idő áll a rendelkezésére, és a kristályok nem akadályozzák egymást növekedésükben, úgy Jól fejlett, sík'lapok által határolt kristályok keletkeznek, vagyis az anyag kristályosodott. A kristályok nagysága tág határok között mozog. A nagyságot a rendelkezésre álló anyagmennyiségen kívül a kristály keletkezésekor uralkodó hőmérséklet, nyomás, ez oldat vagy olvadék viszkozitása, a rendelkezésre álló idő és hely határozza meg* Például a- kvarcból mikroszkópi kicsinységé kristályok mell'ett több tonnás példányokat is Ismerünk* Sokszor találkozunk úgynevezett zárványokkal* A zárványok azok. a gáz, cseppfolyós vagy szilárd anyagok, amelyeket növekedése közben zárt körül a kristály. A gáz és a folyadékzárvány fehér színűrs, a nagyobb tömegű szilárd zárvány a legkülönbözőbb színűre színezi a gézdaésványt. Tehát az ásványok általában színesek. Az átlátszó világossárga topáz,., a gyémántfényű cinóbervörös proustit, a nem átlátszó zöld smaragd, a kagylóstörósü opál, - amelynél az alapszínből különböző színű foltok gyakran éles határral, mozaikszerűe/i válnak ki, mig máékor lágyan olvadnak egymásba - a színak és a fények változatos skáláját mutatják. Színük szerint a tudomány az ásványokat két nagy csoportra osztja, vannak idiokromás /saját színű/ és allokromá* /idegenszínű/ ásványok.
6 < Idiokromás ásványoknak nevezzük azokat az ásványokat, amelyeknek színe összetételük egyik komponensétől ered Például e rodokrozit színe rózssezín. Kémiai összetétele: MnCOg /mangánkarbonát/. Ebben az esetben a szép rózsaszín a mangán /II/-ionoktól ered, melyből felépül a kristály. Allokromás ásványok azok az ásványok, amelyek színe nem a fő komponenstől, hanem az ezek mellett kiemértékben jelenlévő idegen atomoktól származik. Például a korund, az aluminiumoxid színtelen ásvány. Ha azonban a korund kristályrácsába 0,5-2 %-ban krómoxid /Cr o0 Q/ épül be, a krie- / j/ tály égő vörös színű lesz, és rubinról beszélünk. Azokban ez esetekben, amikor a színező anyag annyira finoman eloeztott, hogy a színezett ásvány teljesen átlátszó marad, a 6zínező anyagot nem lehet látni benne, dilut színezésről beszélünk* Ilyen a rubin is. Ha 0 magában színtelen berillbe /Be 2Al 2Si 6O lb/ króm/iii/-ionok épülnek be, akkor a kristály zöld színű lesz. Ilyenkor a berillt smaragdnak nevezzük. Az allokrómás színt t ehát általábsn az idegen atom ionkörnyezete váltja ki. Mér régen felismerték, hogy egyes ásványok szinét ez Idegen atom vegyértéke is befolyásolja. Például a három vsgyértékű vas általáben sárgára, barnára Ízín0z, míg a két vegyértéké vas világoszöld ezínt okoz. Ezt láthatjuk az egyébként színtelen ezfalerit /ZnS/ esetében ie. Ha viszont mindkét ión, vae/iii/ ós vas/ii/ ión együttesen van jelen az ásványban, mély kék színt idéz elő. Nagyon érdekes az a jelenség, hogy azonos két vegyértékű rézionok adnak zöld színt a malechitnak és kék ezínt az azuritnak. A vizsgálatok szerint a szomszédos ionok különbözősége a döntő tényező. Millner Tivadar cikkében rámutat arra, hogy a zafira kék színű korund- nyomokban sem tartalmaz kobaltot, mint azt korábban hitték. A zafir allokrómás áevény ugyan, de
7 - 37- színét nem sgystlsn atomfajtától nyeri. Az allokromás ásványok szint okozó idegen atomjai elnyelik az ásványon áthaladó fehér fényből a színek egy részét, és így ml az ásványt az átbocsátott maradók színben látjuk. Erre olyan idegen atomok képesek, amelyeknek atommagja körül magános /páratlan/ elektronok vannak, ugyanis csak ezek tudják a látható fényt elnyelni. Az Al 2 összetételű színtelen korundban sem az alumínium ionoknak, sem az oxigén ionoknak nincs magános elektronjuk. Azonban kristályrácsában néhol egy-egy alumínium iont egy-egy titén/iv/-ion és egy-egy vas/ii/-ion vált fel. A titán/iv/-iónban nincs magános elektron, ezért fényelnyelést nem végezhet. A vae/ii/-ionban viszont négy magános elektron van. /Ezek nyelik el a fényt./ Fénye Ínye léskor a vas/ii/-ion magános elektronjaiból egyet átad a titán/iv/- -ionnak, ezáltal a vas/ii/-ionból vas/iii/-ion, a titán/iv/rionból pedig titán/iii/-ion lesz. Fe 2+ + Ti 4+ fényelnyelés Fe 3+ + Ti 3+ Ez a folyamat a zafírban olyan színek elnyelése révén jön létre, ami által az átbocsátott fényt kéknek látjuk. A fluorit ásvány néha sárga, néha zöld vagy lila. A fluorit ásvány /CaF 2/ kalciumból és fluorionokból áll. Néhol a kristályrácsban egy-egy fluorion hiányzik. Ennek helyét egy magános elektron tölti ki. Ezt a helyet, illetve ezt a képződményt nevezzük F-centrumnak a német Farbzentren szó szimbólumaként. A magányos elektron itt ugyanolyan helyzetben van, mint az előbb tárgyalt ionoknál a fehér fényből megszabott színű fényt tud elnyelni,szint adva ezzel egy-egy ásványnak. A fluorit ásványban többféle ezincentrum fordul elő. Máe esetekben a természetes radioaktív gamma sugárzás olyan rácshibákat idéz elő a kristályban, amely lila maradékszínt okozó fényelnyelósre képes, mint például az ametiszt esetében.
8 < Nagyon érdekes, hogy az ásványtan már száz évvel ezelőtt azt állította, hogy a nemesopálok színe nem az idegen anyagoktól származik. Az ujabb vizsgálatok bizonyították, hogy a nemesopálok színét a diffrakció, a fényszórás jeleneége idézi elő. Ssnders ausztráliai kutató szerinti ha fehér fény olyan részecskék szabályos sorait tartalmazó párhuzamos rétegeinek csoportját éri, amelyben a részecskék távolsága a fény hullámhosszához esik közel, és amely elrendezésben minden részecske minden irányban ezórja a fényt, akkor tisztán jelennek meg a fehér fény összetevői egymás mellett : a vörös, narancs, sárga, zöld, kék, indigó és ibolya szinek. Még sok érdekes törvényszerűségről számol be Millner cikke sz ásványok színévsl kapcsolatban, melyből csak néhányat ragadtam ki, amelyet a kémia órákon felhasználhatunk. Az ásványok természetét ismertető rövid cikkemmel arra ezerettem volna kartársaim figyelmét felhívni, hogy hallgatóikkal múzeumi sétáik során iktassák programjukba a Magyar Nemzbti Múzeum Ásvány és Kőzettani Kiállítását is.
ÁSVÁNY vagy KŐZET? 1. Honnan származnak ásványaink, kőzeteink? Írd a kép mellé!
 ÁSVÁNY vagy KŐZET? 1. Honnan származnak ásványaink, kőzeteink? Írd a kép mellé! 2. Magmás kőzetek a hevesek A legjobb építőtársak a vulkáni kiömlési kőzetek. Hogy hívják ezt a térkövet?.. A Föld kincseskamrája
ÁSVÁNY vagy KŐZET? 1. Honnan származnak ásványaink, kőzeteink? Írd a kép mellé! 2. Magmás kőzetek a hevesek A legjobb építőtársak a vulkáni kiömlési kőzetek. Hogy hívják ezt a térkövet?.. A Föld kincseskamrája
Polimorfia Egy bizonyos szilárd anyag a külső körülmények függvényében különböző belső szerkezettel rendelkezhet. A grafit kristályrácsa A gyémánt kri
 Ásványtani alapismeretek 3. előadás Polimorfia Egy bizonyos szilárd anyag a külső körülmények függvényében különböző belső szerkezettel rendelkezhet. A grafit kristályrácsa A gyémánt kristályrácsa Polimorf
Ásványtani alapismeretek 3. előadás Polimorfia Egy bizonyos szilárd anyag a külső körülmények függvényében különböző belső szerkezettel rendelkezhet. A grafit kristályrácsa A gyémánt kristályrácsa Polimorf
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
A Föld kéreg: elemek, ásványok és kőzetek
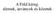 A Föld kéreg: elemek, ásványok és kőzetek A Föld szerkezete: réteges felépítés... Litoszféra: kéreg + felső köpeny legfelső része Kéreg: elemi, ásványos és kőzettani összetétel A Föld különböző elemekből
A Föld kéreg: elemek, ásványok és kőzetek A Föld szerkezete: réteges felépítés... Litoszféra: kéreg + felső köpeny legfelső része Kéreg: elemi, ásványos és kőzettani összetétel A Föld különböző elemekből
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 7 KRISTÁLYTAN VII. A KRIsTÁLYOK szimmetriája 1. BEVEZETÉs Az elemi cella és ebből eredően a térrácsnak a szimmetriáját a kristályok esetében az atomok, ionok
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 7 KRISTÁLYTAN VII. A KRIsTÁLYOK szimmetriája 1. BEVEZETÉs Az elemi cella és ebből eredően a térrácsnak a szimmetriáját a kristályok esetében az atomok, ionok
Ásványtani alapismeretek
 Ásványtani és s kőzettani k alapismeretek Előadók: Dr Molnár Ferenc, egyetemi docens, Ásványtani Tanszék Dr Ditrói Puskás Zuárd, egyetemi docens, Kőzettan-Geokémiai Tanszék Gyakorlatvezetők: Dr Molnár
Ásványtani és s kőzettani k alapismeretek Előadók: Dr Molnár Ferenc, egyetemi docens, Ásványtani Tanszék Dr Ditrói Puskás Zuárd, egyetemi docens, Kőzettan-Geokémiai Tanszék Gyakorlatvezetők: Dr Molnár
1. Mi a drágakő? a. ásványváltozat b. biogén eredetű anyag c. mindkettő lehet. 13. Mit értünk a kristályok külső szimmetriáján?
 1. Mi a drágakő? a. ásványváltozat b. biogén eredetű anyag lehet 2. Mit nevezünk ércnek? a. ásvány, amiből fémet nyerhetünk ki b. kőzet, amiből fémet nyerhetünk ki c. kőzet, amiből gazdaságosan fémet nyerhetünk
1. Mi a drágakő? a. ásványváltozat b. biogén eredetű anyag lehet 2. Mit nevezünk ércnek? a. ásvány, amiből fémet nyerhetünk ki b. kőzet, amiből fémet nyerhetünk ki c. kőzet, amiből gazdaságosan fémet nyerhetünk
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
11. előadás MAGMÁS KŐZETEK
 11. előadás MAGMÁS KŐZETEK MAGMÁS KŐZETEK A FÖLDKÉREGBEN A magmából képződnek az elő- és főkristályosodás során. A megszilárdulás helye szerint: Intruzív (mélységi) kőzetek (5-20 km mélységben) Szubvulkáni
11. előadás MAGMÁS KŐZETEK MAGMÁS KŐZETEK A FÖLDKÉREGBEN A magmából képződnek az elő- és főkristályosodás során. A megszilárdulás helye szerint: Intruzív (mélységi) kőzetek (5-20 km mélységben) Szubvulkáni
Almandin. Pirit Magnetit. Hexakiszoktaéder
 Ásványtani alapismeretek 2. előadás Jellemző kristályformák a monoklin és rombos kristályosztályokban A monoklin rendszer szimmetria ele- mei a maximális szimmetria esetén 1 digír 1 tükörsík 1 inverzíós
Ásványtani alapismeretek 2. előadás Jellemző kristályformák a monoklin és rombos kristályosztályokban A monoklin rendszer szimmetria ele- mei a maximális szimmetria esetén 1 digír 1 tükörsík 1 inverzíós
Halmazállapotok. Gáz, folyadék, szilárd
 Halmazállapotok Gáz, folyadék, szilárd A levegővel telt üveghengerbe brómot csepegtetünk. A bróm illékony, azaz könnyen alakul gázhalmazállapotúvá. A hengerben a levegő részecskéi keverednek a bróm részecskéivel
Halmazállapotok Gáz, folyadék, szilárd A levegővel telt üveghengerbe brómot csepegtetünk. A bróm illékony, azaz könnyen alakul gázhalmazállapotúvá. A hengerben a levegő részecskéi keverednek a bróm részecskéivel
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 30 Műszeres ÁSVÁNYHATÁROZÁS XXX. Műszeres ÁsVÁNYHATÁROZÁs 1. BEVEZETÉs Az ásványok természetes úton, a kémiai elemek kombinálódásával keletkezett (és ma is keletkező),
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 30 Műszeres ÁSVÁNYHATÁROZÁS XXX. Műszeres ÁsVÁNYHATÁROZÁs 1. BEVEZETÉs Az ásványok természetes úton, a kémiai elemek kombinálódásával keletkezett (és ma is keletkező),
Ásvány- és kőzettan. Kristálytan Ásványtan Kőzettan Magyarország ásványai, kőzetei Történeti áttekintés. Bidló A.: Ásvány- és kőzettan
 Ásvány- és kőzettan Kristálytan Ásványtan Kőzettan Magyarország ásványai, kőzetei Történeti áttekintés Ásványok Ásványok fogalma Az ásvány a földkéreg szilárd, homogén, természetes eredetű része kb. 4000
Ásvány- és kőzettan Kristálytan Ásványtan Kőzettan Magyarország ásványai, kőzetei Történeti áttekintés Ásványok Ásványok fogalma Az ásvány a földkéreg szilárd, homogén, természetes eredetű része kb. 4000
Modern fizika vegyes tesztek
 Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam
 A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam A feladatok megoldásához csak
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 8. évfolyam A feladatok megoldásához csak
2. előadás A KRISTÁLYTAN ALAPJAI. 1. A kristályok belső rendezettsége (kristályszerkezet) 2. A kristályok külső alakja (kristálymorfológia)
 2. előadás A KRISTÁLYTAN ALAPJAI 1. A kristályok belső rendezettsége (kristályszerkezet) 2. A kristályok külső alakja (kristálymorfológia) KRISTÁLY FOGALOM A MÚLTBAN Ókorban: jég (= krüsztallosz), a színtelen
2. előadás A KRISTÁLYTAN ALAPJAI 1. A kristályok belső rendezettsége (kristályszerkezet) 2. A kristályok külső alakja (kristálymorfológia) KRISTÁLY FOGALOM A MÚLTBAN Ókorban: jég (= krüsztallosz), a színtelen
Kondenzált anyagok csoportosítása
 Szilárdtestfizika Kondenzált anyagok csoportosítása 1. Üvegek Nagy viszkozitású olvadék állapotú anyagok, amelyek nagyon lassan szilárd állapotba mennek át. Folyékony állapotból gyors hűtéssel állíthatók
Szilárdtestfizika Kondenzált anyagok csoportosítása 1. Üvegek Nagy viszkozitású olvadék állapotú anyagok, amelyek nagyon lassan szilárd állapotba mennek át. Folyékony állapotból gyors hűtéssel állíthatók
Az ásványok rendszerezése Az ásványok osztályokba sorolásának alapelvei: - Összetétel - Kristályszerkezet - Előfordulás Összesen 9 osztályba soroljuk
 Ásványtani alapismeretek 4. előadás Az ásványok rendszerezése Az ásványok osztályokba sorolásának alapelvei: - Összetétel - Kristályszerkezet - Előfordulás Összesen 9 osztályba soroljuk az ásványokat,
Ásványtani alapismeretek 4. előadás Az ásványok rendszerezése Az ásványok osztályokba sorolásának alapelvei: - Összetétel - Kristályszerkezet - Előfordulás Összesen 9 osztályba soroljuk az ásványokat,
minden színben, sávokkal színtelen, zöld, barna vagy vörös berakódásokkal kékeszöld, vagy pirosaslila
 Achát minden színben, sávokkal Mohaachát színtelen, zöld, barna vagy vörös berakódásokkal Alexandrit kékeszöld, vagy pirosaslila Amazonit zöld, kékeszöld Ametiszt ibolyalila, halvány pirosaslila Andaluzit
Achát minden színben, sávokkal Mohaachát színtelen, zöld, barna vagy vörös berakódásokkal Alexandrit kékeszöld, vagy pirosaslila Amazonit zöld, kékeszöld Ametiszt ibolyalila, halvány pirosaslila Andaluzit
NYOMOZÁS A DRÁGAKÖVEK VILÁGÁBAN Melyik drágaköves ékszert rabolták el? 7. osztály Készítette: Bagócsi Zsuzsanna, Léki Boglárka
 NYOMOZÁS A DRÁGAKÖVEK VILÁGÁBAN Melyik drágaköves ékszert rabolták el? 7. osztály Készítette: Bagócsi Zsuzsanna, Léki Boglárka A feladat leírása: A diákok az ásványok és kőzetek témáján belül a drágakövekkel
NYOMOZÁS A DRÁGAKÖVEK VILÁGÁBAN Melyik drágaköves ékszert rabolták el? 7. osztály Készítette: Bagócsi Zsuzsanna, Léki Boglárka A feladat leírása: A diákok az ásványok és kőzetek témáján belül a drágakövekkel
7. osztály Hevesy verseny, megyei forduló, 2003.
 Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 3 AZ ÁSVÁNYTaN ÉS kőzettan TÁRGYa, alapfogalmak III. ALAPFOGALMAK 1. MI AZ ÁsVÁNY? Nem véletlen, hogy a bevezető gondolatokban a kémiai elemekkel, azok elterjedésével
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 3 AZ ÁSVÁNYTaN ÉS kőzettan TÁRGYa, alapfogalmak III. ALAPFOGALMAK 1. MI AZ ÁsVÁNY? Nem véletlen, hogy a bevezető gondolatokban a kémiai elemekkel, azok elterjedésével
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
7. osztály 2 Hevesy verseny, országos döntő, 2004.
 7. osztály 2 Hevesy verseny, országos döntő, 2004. Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő tíz feladat megoldására 90 perc áll rendelkezésedre.
7. osztály 2 Hevesy verseny, országos döntő, 2004. Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő tíz feladat megoldására 90 perc áll rendelkezésedre.
Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek. fémek
 Kémiai kötések Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek fémek Fémek Szürke színűek, kivétel a színesfémek: arany,réz. Szilárd halmazállapotúak, kivétel a higany. Vezetik az
Kémiai kötések Az elemeket 3 csoportba osztjuk: Félfémek vagy átmeneti fémek nemfémek fémek Fémek Szürke színűek, kivétel a színesfémek: arany,réz. Szilárd halmazállapotúak, kivétel a higany. Vezetik az
ÁSVÁNYOK-KİZETKÉPZİDÉS
 ÁSVÁNYOK-KİZETKÉPZİDÉS Tartalom Ásvány, kristály, kızet fogalma Elemek gyakorisága a földkéregben Kızetképzıdés folyamata Ásványok tulajdonságai Kızetalkotó ásványok Ásvány természetben elıforduló anyag
ÁSVÁNYOK-KİZETKÉPZİDÉS Tartalom Ásvány, kristály, kızet fogalma Elemek gyakorisága a földkéregben Kızetképzıdés folyamata Ásványok tulajdonságai Kızetalkotó ásványok Ásvány természetben elıforduló anyag
Milyen színűek a csillagok?
 Milyen színűek a csillagok? A fényesebb csillagok színét szabad szemmel is jól láthatjuk. Az egyik vörös, a másik kék, de vannak fehéren villódzók, sárga, narancssárga színűek is. Vajon mi lehet az eltérő
Milyen színűek a csillagok? A fényesebb csillagok színét szabad szemmel is jól láthatjuk. Az egyik vörös, a másik kék, de vannak fehéren villódzók, sárga, narancssárga színűek is. Vajon mi lehet az eltérő
ÜVEG ÉS ÜVEGMÁZ. (Fórizs István MTA Geokémiai Kutatóintézet Anyagának felhasználásával)
 ÜVEG ÉS ÜVEGMÁZ (Fórizs István MTA Geokémiai Kutatóintézet Anyagának felhasználásával) Üveg: különleges anyag Sajátos szerkezet: rövid távú rendezettség, röntgen-amorf, térhálós Oxigén atomok alkotják
ÜVEG ÉS ÜVEGMÁZ (Fórizs István MTA Geokémiai Kutatóintézet Anyagának felhasználásával) Üveg: különleges anyag Sajátos szerkezet: rövid távú rendezettség, röntgen-amorf, térhálós Oxigén atomok alkotják
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged Kálnay Istvánné, Nyíregyháza Lektorálta: .. Kozma Lászlóné, Sajószenpéter
 A feladatokat írta: Harkai Jánosné, Szeged Kálnay Istvánné, Nyíregyháza Lektorálta: Kódszám:.. Kozma Lászlóné, Sajószenpéter 2011. május 14. Curie Kémia Emlékverseny 8. évfolyam Országos döntő 2010/2011.
A feladatokat írta: Harkai Jánosné, Szeged Kálnay Istvánné, Nyíregyháza Lektorálta: Kódszám:.. Kozma Lászlóné, Sajószenpéter 2011. május 14. Curie Kémia Emlékverseny 8. évfolyam Országos döntő 2010/2011.
Minta feladatsor. Az ion képlete. Az ion neve O 4. Foszfátion. Szulfátion CO 3. Karbonátion. Hidrogénkarbonátion O 3. Alumíniumion. Al 3+ + Szulfidion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve Foszfátion Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve Foszfátion Szulfátion
1. Szimmetriák. Háromszög-szimmetria. Rubin Zafir Kalcit aluminium-oxid: Al 2 O 3 kalcium-karbonát: CaCO 3
 Egy kis reklám A Matematikatanárok Klubjának honlapja: https://www.cs.elte.hu/ miertmat/progs.html Recski András: Síkbarajzolható gráfok, rúdszerkezetek, transzformátorok. https://www.youtube.com/watch?v=iy4dzcwyf5s
Egy kis reklám A Matematikatanárok Klubjának honlapja: https://www.cs.elte.hu/ miertmat/progs.html Recski András: Síkbarajzolható gráfok, rúdszerkezetek, transzformátorok. https://www.youtube.com/watch?v=iy4dzcwyf5s
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával. www.chem.elte.hu/pr
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok március 6. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok március 6. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
Színképelemzés. Romsics Imre 2014. április 11.
 Színképelemzés Romsics Imre 2014. április 11. 1 Más néven: Spektrofotometria A színképből kinyert információkból megállapítható: az atomok elektronszerkezete az elektronállapotokat jellemző kvantumszámok
Színképelemzés Romsics Imre 2014. április 11. 1 Más néven: Spektrofotometria A színképből kinyert információkból megállapítható: az atomok elektronszerkezete az elektronállapotokat jellemző kvantumszámok
AZ ÉLETTELEN ÉS AZ ÉLŐ TERMÉSZET
 AZ ÉLŐ ÉS AZ ÉLETTELEN TERMÉSZET MEGISMERÉSE AZ ÉLETTELEN ÉS AZ ÉLŐ TERMÉSZET Az élőlények és az élettelen természet kapcsolata. Az élettelen természet megismerése. A Földdel foglalkozó tudományok. 1.
AZ ÉLŐ ÉS AZ ÉLETTELEN TERMÉSZET MEGISMERÉSE AZ ÉLETTELEN ÉS AZ ÉLŐ TERMÉSZET Az élőlények és az élettelen természet kapcsolata. Az élettelen természet megismerése. A Földdel foglalkozó tudományok. 1.
Metamorf kőzettan. Magmás (olvadék, kristályosodás, T, p) szerpentinit. zeolit Üledékes (törmelék oldatok kicsapódása; szerves eredetű, T, p)
 Metamorf kőzettan Metamorfózis (átalakulás, átkristályosodás): ha a kőzetek keletkezési körülményeiktől eltérő nyomású és/vagy hőmérsékletű környezetbe kerülve szilárd fázisban átkristályosodnak és/vagy
Metamorf kőzettan Metamorfózis (átalakulás, átkristályosodás): ha a kőzetek keletkezési körülményeiktől eltérő nyomású és/vagy hőmérsékletű környezetbe kerülve szilárd fázisban átkristályosodnak és/vagy
T I T - M T T. Hevesy György Kémiaverseny. országos döntő. Az írásbeli forduló feladatlapja. 7. osztály
 T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
Az atom- olvasni. 1. ábra Az atom felépítése 1. Az atomot felépítő elemi részecskék. Proton, Jele: (p+) Neutron, Jele: (n o )
 Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
A tudós neve: Mit tudsz róla:
 8. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
8. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Elektrokémia. A nemesfém elemek és egymással képzett vegyületeik
 Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
Elektrokémia Redoxireakciók: Minden olyan reakciót, amelyben elektron leadás és elektronfelvétel történik, redoxi reakciónak nevezünk. Az elektronleadás és -felvétel egyidejűleg játszódik le. Oxidálószer
ISMÉTLÉS, RENDSZEREZÉS
 ISMÉTLÉS, RENDSZEREZÉS A) változat 1. Egészítsd ki az ábrát a hiányzó anyagcsoportokkal és példákkal! ANYAGOK (összetétel szerint) egyszerű anyagok összetett anyagok......... oldat pl.... pl.... pl. levegő
ISMÉTLÉS, RENDSZEREZÉS A) változat 1. Egészítsd ki az ábrát a hiányzó anyagcsoportokkal és példákkal! ANYAGOK (összetétel szerint) egyszerű anyagok összetett anyagok......... oldat pl.... pl.... pl. levegő
CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapa judeţeană 5 mai 2018 Ediţia a XIV-a. I Tétel pont
 CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapa judeţeană 5 mai 2018 Ediţia a XIV-a Munkaidő: 3 óra. A feladatok megoldásához használjátok az atomtömegek kerekített értékét a csatolmányban
CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapa judeţeană 5 mai 2018 Ediţia a XIV-a Munkaidő: 3 óra. A feladatok megoldásához használjátok az atomtömegek kerekített értékét a csatolmányban
6. előadás AZ ÁSVÁNYOK RENDSZEREZÉSE OXIDOK, HIDROXIDOK, KARBONÁTOK
 6. előadás AZ ÁSVÁNYOK RENDSZEREZÉSE OXIDOK, HIDROXIDOK, KARBONÁTOK Oxidok Fémeknek oxigénnel alkotott vegyületei. Szerkezetükben főleg ionos kötés érvényesül. Az összetett oxidokban két vagy több kation
6. előadás AZ ÁSVÁNYOK RENDSZEREZÉSE OXIDOK, HIDROXIDOK, KARBONÁTOK Oxidok Fémeknek oxigénnel alkotott vegyületei. Szerkezetükben főleg ionos kötés érvényesül. Az összetett oxidokban két vagy több kation
Bútorfogantyúk. 1882-56 - fém. 1884-48 - fém. antik ezüst. antik ezüst. 1885-56 - fém. 1886-36 - fém. antik ezüst. antik ezüst.
 Bútorfogantyúk. 88- - fém 88-8 - fém antik ezüst 0000700 antik ezüst 0000700 9 9 9 8, 88- - fém 88- - fém 00007070 antik ezüst 00007080 7,,, 0 antik ezüst, 9 88-09 - fém antik ezüst 0000700 8 7 09 887-
Bútorfogantyúk. 88- - fém 88-8 - fém antik ezüst 0000700 antik ezüst 0000700 9 9 9 8, 88- - fém 88- - fém 00007070 antik ezüst 00007080 7,,, 0 antik ezüst, 9 88-09 - fém antik ezüst 0000700 8 7 09 887-
OPTIKA. Fénykibocsátás mechanizmusa fényforrás típusok. Dr. Seres István
 OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
T I T - M T T. Hevesy György Kémiaverseny. országos döntő. Az írásbeli forduló feladatlapja. 7. osztály
 T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos döntő Az írásbeli forduló feladatlapja 7. osztály A versenyző azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
KÖZSÉGI VERSENY KÉMIÁBÓL március 3.
 OKTATÁSI, TUDOMÁNYOS ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL 2018. március 3. TUDÁSFELMÉRŐ FELADATLAP A VII. OSZTÁLY SZÁMÁRA A tanuló jeligéje (három
OKTATÁSI, TUDOMÁNYOS ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL 2018. március 3. TUDÁSFELMÉRŐ FELADATLAP A VII. OSZTÁLY SZÁMÁRA A tanuló jeligéje (három
Mi a hasonlóság és mi a különbség a felsorolt kémiai részecskék között? Hasonlóság:... Különbség: atom a belőle származó (egyszerű) ion
 Kedves Versenyző! 2 Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő kilenc feladat megoldására 90 perc áll rendelkezésedre. A feladatokat a számítási feladatok
Kedves Versenyző! 2 Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő kilenc feladat megoldására 90 perc áll rendelkezésedre. A feladatokat a számítási feladatok
Labradorit. Fegyvári Tamás Ásvány- és Kőzettár
 Labradorit Fegyvári Tamás Ásvány- és Kőzettár Labradorit A labradorit kétarcú ásvány. A plagioklász- földpátok közé tartozó anortit változata. Mint kőzetalkotó ásvány nagy mennyiségben fordul elő például
Labradorit Fegyvári Tamás Ásvány- és Kőzettár Labradorit A labradorit kétarcú ásvány. A plagioklász- földpátok közé tartozó anortit változata. Mint kőzetalkotó ásvány nagy mennyiségben fordul elő például
10. előadás Kőzettani bevezetés
 10. előadás Kőzettani bevezetés Mi a kőzet? Döntően nagy földtani folyamatok során képződik. Elsősorban ásványok keveréke. Kőzetalkotó ásványok építik fel. A kőzetalkotó komponensek azonban nemcsak ásványok,
10. előadás Kőzettani bevezetés Mi a kőzet? Döntően nagy földtani folyamatok során képződik. Elsősorban ásványok keveréke. Kőzetalkotó ásványok építik fel. A kőzetalkotó komponensek azonban nemcsak ásványok,
T I T M T T. Hevesy György Kémiaverseny
 T I T M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Az atommag összetétele, radioaktivitás
 Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Jegyzet. Kémia, BMEVEAAAMM1 Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens.
 Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
A FÖLD BELSŐ SZERKEZETE
 A FÖLD BELSŐ SZERKEZETE 1) A Föld kialakulása: Mai elméleteink alapján a Föld 4,6 milliárd évvel ezelőtt keletkezett Kezdetben a Föld izzó gázgömbként létezett, mint ma a Nap A gázgömb lehűlésekor a Föld
A FÖLD BELSŐ SZERKEZETE 1) A Föld kialakulása: Mai elméleteink alapján a Föld 4,6 milliárd évvel ezelőtt keletkezett Kezdetben a Föld izzó gázgömbként létezett, mint ma a Nap A gázgömb lehűlésekor a Föld
Hevesy György Országos Kémiaverseny Kerületi forduló február 12. Munkaidő: 60 perc 8. évfolyam
 Hevesy György Országos Kémiaverseny Kerületi forduló 2014. február 12. Munkaidő: 60 perc 8. évfolyam A feladatlap megoldásához kizárólag periódusos rendszer és elektronikus adatok tárolására nem alkalmas
Hevesy György Országos Kémiaverseny Kerületi forduló 2014. február 12. Munkaidő: 60 perc 8. évfolyam A feladatlap megoldásához kizárólag periódusos rendszer és elektronikus adatok tárolására nem alkalmas
Mit tanultunk kémiából?2.
 Mit tanultunk kémiából?2. Az anyagok rendkívül kicsi kémiai részecskékből épülnek fel. Több milliárd részecske Mól az anyagmennyiség mértékegysége. 1 mol atom= 6. 10 23 db atom 600.000.000.000.000.000.000.000
Mit tanultunk kémiából?2. Az anyagok rendkívül kicsi kémiai részecskékből épülnek fel. Több milliárd részecske Mól az anyagmennyiség mértékegysége. 1 mol atom= 6. 10 23 db atom 600.000.000.000.000.000.000.000
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
KRISTÁLYOK GEOMETRIAI LEÍRÁSA
 KRISTÁLYOK GEOMETRIAI LEÍRÁSA Kristály Bázis Pontrács Ideális Kristály: hosszútávúan rendezett hibamentes, végtelen szilárd test Kristály Bázis: a kristály legkisebb, ismétlœdœ atomcsoportja Rácspont:
KRISTÁLYOK GEOMETRIAI LEÍRÁSA Kristály Bázis Pontrács Ideális Kristály: hosszútávúan rendezett hibamentes, végtelen szilárd test Kristály Bázis: a kristály legkisebb, ismétlœdœ atomcsoportja Rácspont:
4. elıadás A KRISTÁLYFIZIKA ALAPJAI
 4. elıadás A KRISTÁLYFIZIKA ALAPJAI KRISTÁLYFIZIKA ANIZOTRÓPIA IZOTRÓPIA JELENSÉGE Izotrópia (irányok szerint egyenlı): ha a fizikai sajátságok függetlenek az iránytól. Ide tartoznak a köbös rendszerbe
4. elıadás A KRISTÁLYFIZIKA ALAPJAI KRISTÁLYFIZIKA ANIZOTRÓPIA IZOTRÓPIA JELENSÉGE Izotrópia (irányok szerint egyenlı): ha a fizikai sajátságok függetlenek az iránytól. Ide tartoznak a köbös rendszerbe
Cirkon (ZrSiO4) Kis Annamária Ásvány- és Kőzettár
 Cirkon (ZrSiO4) Kis Annamária Ásvány- és Kőzettár Tudományos és múzeumi Állandó kiállításunkon megtekinthetők az egyik legidősebb földi ásvány, egy cirkonkristály Nyugat- Ausztráliából származó kortársai.
Cirkon (ZrSiO4) Kis Annamária Ásvány- és Kőzettár Tudományos és múzeumi Állandó kiállításunkon megtekinthetők az egyik legidősebb földi ásvány, egy cirkonkristály Nyugat- Ausztráliából származó kortársai.
IV.főcsoport. Széncsoport
 IV.főcsoport Széncsoport Sorold fel a főcsoport elemeit! Szén C szilárd nemfém Szilícium Si szilárd félfém Germánium Ge szilárd félfém Ón Sn szilárd fém Ólom Pb szilárd fém Ásványi szén: A szén (C) Keverék,
IV.főcsoport Széncsoport Sorold fel a főcsoport elemeit! Szén C szilárd nemfém Szilícium Si szilárd félfém Germánium Ge szilárd félfém Ón Sn szilárd fém Ólom Pb szilárd fém Ásványi szén: A szén (C) Keverék,
Tanítási tervezet Fehér András Tamás Vulkáni kőzetek Tantervi követelmények A tanítási óra oktatási célja: A tanítási óra nevelési célja:
 Tanítási tervezet Óra időpontja: 2017.10.17. - 9:00 Évfolyam/osztály: 9/A Tanít: Fehér András Tamás Témakör: A Föld, mint kőzetbolygó Tanítási egység címe: Vulkáni kőzetek Óra típusa: Új ismereteket szerző
Tanítási tervezet Óra időpontja: 2017.10.17. - 9:00 Évfolyam/osztály: 9/A Tanít: Fehér András Tamás Témakör: A Föld, mint kőzetbolygó Tanítási egység címe: Vulkáni kőzetek Óra típusa: Új ismereteket szerző
Tesztkérdések az Ásványtani és kızettani alapismeretek tárgyhoz
 Tesztkérdések az Ásványtani és kızettani alapismeretek tárgyhoz 1. Mi a drágakı? a. ásványváltozat b. biogén eredető anyag lehet 2. Mit nevezünk ércnek? a. ásvány, amibıl fémet nyerhetünk ki b. kızet,
Tesztkérdések az Ásványtani és kızettani alapismeretek tárgyhoz 1. Mi a drágakı? a. ásványváltozat b. biogén eredető anyag lehet 2. Mit nevezünk ércnek? a. ásvány, amibıl fémet nyerhetünk ki b. kızet,
Algebra2, alapszint 11. előadás 1 / 11. Algebra2, alapszint. ELTE Algebra és Számelmélet Tanszék. Előadó: Kiss Emil 11.
 Algebra2, alapszint 11. előadás 1 / 11 Algebra2, alapszint ELTE Algebra és Számelmélet Tanszék Előadó: Kiss Emil ewkiss@cs.elte.hu 11. előadás Kristályok szimmetriái Algebra2, alapszint 11. előadás 2 /
Algebra2, alapszint 11. előadás 1 / 11 Algebra2, alapszint ELTE Algebra és Számelmélet Tanszék Előadó: Kiss Emil ewkiss@cs.elte.hu 11. előadás Kristályok szimmetriái Algebra2, alapszint 11. előadás 2 /
BEFEKTETÉS S O P H I E M O L N A R D E S I G N P R E S E N T S
 GYÉMÁNT BEFEKTETÉS 2018. S O P H I E M O L N A R D E S I G N P R E S E N T S Web: www.sophiemolnardesign.com E-mail: info@sophiemolnardesign.com vagy sophie@sophiemolnardesign.com Copyright: SMDesign Kft.
GYÉMÁNT BEFEKTETÉS 2018. S O P H I E M O L N A R D E S I G N P R E S E N T S Web: www.sophiemolnardesign.com E-mail: info@sophiemolnardesign.com vagy sophie@sophiemolnardesign.com Copyright: SMDesign Kft.
 Í Í É Ó Ö Í Ó Ó ű Í Í Ó ű Ó Ó Ö Ö Ó Ö ű Ó Ó Ö ű ű ű Ö Ö Ó Ó Ó Ö Í Ö Ö Ö É Ó Ó Ö Ó Ő Ö Ó Ő Ö Í Ö ű ű Í Í ű ű É Í ű Í Ö Ö Í Í É Ö Ö Í Ö Ö Ö ű Ö Ö Ö Í ű ű Í Í ű Ő Í Ö Í Í Í Ö É Ö Ö Ű Í Ö Ó Í Í Í Í Í Ö ű Ö
Í Í É Ó Ö Í Ó Ó ű Í Í Ó ű Ó Ó Ö Ö Ó Ö ű Ó Ó Ö ű ű ű Ö Ö Ó Ó Ó Ö Í Ö Ö Ö É Ó Ó Ö Ó Ő Ö Ó Ő Ö Í Ö ű ű Í Í ű ű É Í ű Í Ö Ö Í Í É Ö Ö Í Ö Ö Ö ű Ö Ö Ö Í ű ű Í Í ű Ő Í Ö Í Í Í Ö É Ö Ö Ű Í Ö Ó Í Í Í Í Í Ö ű Ö
A vulkáni kitöréseket megelőző mélybeli magmás folyamatok
 A vulkáni kitöréseket megelőző mélybeli magmás folyamatok Jankovics M. Éva MTA-ELTE Vulkanológiai Kutatócsoport SZTE ÁGK Vulcano Kutatócsoport Szeged, 2014.10.09. ábrák, adatok forrása: tudományos publikációk
A vulkáni kitöréseket megelőző mélybeli magmás folyamatok Jankovics M. Éva MTA-ELTE Vulkanológiai Kutatócsoport SZTE ÁGK Vulcano Kutatócsoport Szeged, 2014.10.09. ábrák, adatok forrása: tudományos publikációk
Orvosi Biofizika I. 12. vizsgatétel. IsmétlésI. -Fény
 Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
A szilárd testek alakja és térfogata észrevehetően csak nagy erő hatására változik meg. A testekben a részecskék egymáshoz közel vannak, kristályos
 Az anyagok lehetséges állapotai, a fizikai körülményektől (nyomás, hőmérséklet) függően. Az anyagokat általában a normál körülmények között jellemző állapotuk alapján soroljuk be szilád, folyékony vagy
Az anyagok lehetséges állapotai, a fizikai körülményektől (nyomás, hőmérséklet) függően. Az anyagokat általában a normál körülmények között jellemző állapotuk alapján soroljuk be szilád, folyékony vagy
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
(2014. március 8.) TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA
 SZERB KÖZTÁRSASÁG OKTATÁSI, TUDOMÁNYÜGYI ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL (2014. március 8.) TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA
SZERB KÖZTÁRSASÁG OKTATÁSI, TUDOMÁNYÜGYI ÉS TECHNOLÓGIAI FEJLESZTÉSI MINISZTÉRIUM SZERB KÉMIKUSOK EGYESÜLETE KÖZSÉGI VERSENY KÉMIÁBÓL (2014. március 8.) TUDÁSFELMÉRŐ FELADATLAP A VIII. OSZTÁLY SZÁMÁRA
5. elıadás KRISTÁLYKÉMIAI ALAPOK
 5. elıadás KRISTÁLYKÉMIAI ALAPOK KRISTÁLYKÉMIAI ALAPFOGALMAK Atomok: az anyag legkisebb olyan részei, amelyek még hordozzák a kémiai elem jellegzetességeit. Részei: atommag (mely protonokból és neutronokból
5. elıadás KRISTÁLYKÉMIAI ALAPOK KRISTÁLYKÉMIAI ALAPFOGALMAK Atomok: az anyag legkisebb olyan részei, amelyek még hordozzák a kémiai elem jellegzetességeit. Részei: atommag (mely protonokból és neutronokból
7. osztály 2 Hevesy verseny, megyei forduló, 2004.
 7. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
7. osztály 2 Hevesy verseny, megyei forduló, 2004. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 17 KRISTÁLYFIZIkA XVII. Hőtani, MÁGNEsEs, ELEKTROMOs, RADIOAKTÍV TULAJDONsÁGOK 1. Hőtani TULAJDONsÁGOK A hősugarak a színkép vörös színén túl lépnek fel (infravörös
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 17 KRISTÁLYFIZIkA XVII. Hőtani, MÁGNEsEs, ELEKTROMOs, RADIOAKTÍV TULAJDONsÁGOK 1. Hőtani TULAJDONsÁGOK A hősugarak a színkép vörös színén túl lépnek fel (infravörös
Szilárdtestek sávelmélete. Sávelmélet a szabadelektron-modell alapján
 Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
 é ö é Ö é ü é é ö ö ö ü é é ö ú ö é é é Ő ö é ü é ö é é ü é é ü é é é ű é ö é é é é é é é ö ö í é ü é ö ü ö ö é í é é é ö ü é é é é ü ö é é é é é é é é é é é é é é é ö é Í ö í ö é Í í ö é Í é í é é é é
é ö é Ö é ü é é ö ö ö ü é é ö ú ö é é é Ő ö é ü é ö é é ü é é ü é é é ű é ö é é é é é é é ö ö í é ü é ö ü ö ö é í é é é ö ü é é é é ü ö é é é é é é é é é é é é é é é ö é Í ö í ö é Í í ö é Í é í é é é é
Hevesy György Kémiaverseny. 8. osztály. megyei döntő 2003.
 Hevesy György Kémiaverseny 8. osztály megyei döntő 2003. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
Hevesy György Kémiaverseny 8. osztály megyei döntő 2003. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
ÁSVÁNYTANI ÉS KİZETTANI ALAPISMERETEK
 ÁSVÁNYTANI ÉS KİZETTANI ALAPISMERETEK Elıadó: Szakáll Sándor Gyakorlatvezetık: Mádai Ferenc, Mádai Viktor, Szakáll Sándor Ásvány- és Kızettani Tanszék Tel.: 565-111 / 1211 E-mail: askszs@uni-miskolc.hu
ÁSVÁNYTANI ÉS KİZETTANI ALAPISMERETEK Elıadó: Szakáll Sándor Gyakorlatvezetık: Mádai Ferenc, Mádai Viktor, Szakáll Sándor Ásvány- és Kızettani Tanszék Tel.: 565-111 / 1211 E-mail: askszs@uni-miskolc.hu
OPTIKA. Hullámoptika Diszperzió, interferencia. Dr. Seres István
 OPTIKA Diszperzió, interferencia Dr. Seres István : A fény elektromágneses hullám A fehér fény összetevői: Seres István 2 http://fft.szie.hu : A fény elektromágneses hullám: Diszperzió: Különböző hullámhosszúságú
OPTIKA Diszperzió, interferencia Dr. Seres István : A fény elektromágneses hullám A fehér fény összetevői: Seres István 2 http://fft.szie.hu : A fény elektromágneses hullám: Diszperzió: Különböző hullámhosszúságú
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam
 A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam A feladatok megoldásához csak
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam A feladatok megoldásához csak
Szabadentalpia nyomásfüggése
 Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Általános Kémia, BMEVESAA101
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Kémiai alapismeretek 14. hét
 Kémiai alapismeretek 14. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2011. december 6. 1/9 2010/2011 I. félév, Horváth Attila c 1785 Cavendish:
Kémiai alapismeretek 14. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2011. december 6. 1/9 2010/2011 I. félév, Horváth Attila c 1785 Cavendish:
CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN. etapajudeţeană 13mai 2017 Ediţia a XIII-a I. Tétel...40 pont A...20 pont
 CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapajudeţeană 13mai 217 Ediţia a XIII-a I. Tétel...4 pont A....2 pont Az első periódusos rendszert 1869 publikálták, egy orosz kémikus Mendeleev,
CONCURSUL DE CHIMIE PENTRU CLASA a VII-a RALUCA RIPAN etapajudeţeană 13mai 217 Ediţia a XIII-a I. Tétel...4 pont A....2 pont Az első periódusos rendszert 1869 publikálták, egy orosz kémikus Mendeleev,
feladatmegoldásai K É M I Á B Ó L
 A 2006/2007. tanévi ORSZÁGOS KÖZÉPISKOLAI TANULMÁNYI VERSENY első (iskolai) fordulójának Az értékelés szempontjai feladatmegoldásai K É M I Á B Ó L Egy-egy feladat összes pontszáma a részpontokból tevődik
A 2006/2007. tanévi ORSZÁGOS KÖZÉPISKOLAI TANULMÁNYI VERSENY első (iskolai) fordulójának Az értékelés szempontjai feladatmegoldásai K É M I Á B Ó L Egy-egy feladat összes pontszáma a részpontokból tevődik
KÉSŐ AVAR ÜVEGGYÖNGYÖK ÖSSZETÉTEL- VIZSGÁLATA
 . BUDAPESTINENSIS DE EÖTVÖS NOM. * KÉSŐ AVAR ÜVEGGYÖNGYÖK ÖSSZETÉTEL- VIZSGÁLATA különös tekintettel a mállási jelenségek kimutatására Készítette: Király Csilla: Környezettudomány MSc. I. évf. Mácsai Cecília:
. BUDAPESTINENSIS DE EÖTVÖS NOM. * KÉSŐ AVAR ÜVEGGYÖNGYÖK ÖSSZETÉTEL- VIZSGÁLATA különös tekintettel a mállási jelenségek kimutatására Készítette: Király Csilla: Környezettudomány MSc. I. évf. Mácsai Cecília:
Magyar vagyok. Legszebb ország hazám az öt világrész nagy terűletén.
 7. osztály 2 Hevesy verseny, megyei forduló, 2006. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
7. osztály 2 Hevesy verseny, megyei forduló, 2006. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár. Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár,
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
3. feladat. Állapítsd meg az alábbi kénvegyületekben a kén oxidációs számát! Összesen 6 pont érhető el. Li2SO3 H2S SO3 S CaSO4 Na2S2O3
 10. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
10. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
Múzeumpedagógiai feladat. Látogatás az ELTE Ásványtárában
 Múzeumpedagógiai feladat Látogatás az ELTE Ásványtárában A feladatlapot összeállította: Csintalan Lilian, 2013 Az ELTE Ásványtárába (Budapest, 1117, Pázmány Péter sétány 1/C.) tervezett tárlatvezetést
Múzeumpedagógiai feladat Látogatás az ELTE Ásványtárában A feladatlapot összeállította: Csintalan Lilian, 2013 Az ELTE Ásványtárába (Budapest, 1117, Pázmány Péter sétány 1/C.) tervezett tárlatvezetést
Meteorit becsapódás földtani konzekvenciái a Sudbury komplexum példáján
 Meteorit becsapódás földtani konzekvenciái a Sudbury komplexum példáján Készítette : Gregor Rita Környezettan BSc. Témavezető: Dr. Molnár Ferenc egyetemi docens Tartalomjegyzék o A Sudbury szerkezet elhelyezkedése
Meteorit becsapódás földtani konzekvenciái a Sudbury komplexum példáján Készítette : Gregor Rita Környezettan BSc. Témavezető: Dr. Molnár Ferenc egyetemi docens Tartalomjegyzék o A Sudbury szerkezet elhelyezkedése
Összeadó színkeverés
 Többféle fényforrás Beépített meghajtás mindegyik fényforrásban Néhány fényforrásban beépített színvezérlő és dimmer Működtetés egyszerűen 12V-ról Színkeverés kézi vezérlővel Komplex vezérlés a DkLightBus
Többféle fényforrás Beépített meghajtás mindegyik fényforrásban Néhány fényforrásban beépített színvezérlő és dimmer Működtetés egyszerűen 12V-ról Színkeverés kézi vezérlővel Komplex vezérlés a DkLightBus
T I T - M T T. Hevesy György Kémiaverseny
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Kémia Fizika 7-8. osztály. I. Nobel-díjasok (kb. 25 perc)
 OM 037757 NÉV: IX. Tollforgató 2017.04.01. Monorierdei Fekete István Általános Iskola : 2213 Monorierdő, Szabadság út 43. : 06 29 / 419-113 : feketeiskola.monorierdo@gmail.com : http://www.fekete-merdo.sulinet.hu
OM 037757 NÉV: IX. Tollforgató 2017.04.01. Monorierdei Fekete István Általános Iskola : 2213 Monorierdő, Szabadság út 43. : 06 29 / 419-113 : feketeiskola.monorierdo@gmail.com : http://www.fekete-merdo.sulinet.hu
Ásvány- és kzettan. Történeti áttekintés Kristálytan Ásványtan Kzettan Magyarország ásványai, kzetei. Bidló A.: Ásvány- és kzettan
 Ásvány- és kzettan Történeti áttekintés Kristálytan Ásványtan Kzettan Magyarország ásványai, kzetei Ásványok Ásványok fogalma Az ásvány a földkéreg (a Hold és más égitestek) szilárd, homogén, természetes
Ásvány- és kzettan Történeti áttekintés Kristálytan Ásványtan Kzettan Magyarország ásványai, kzetei Ásványok Ásványok fogalma Az ásvány a földkéreg (a Hold és más égitestek) szilárd, homogén, természetes
