Ismét a paracetamolról
|
|
|
- Hanna Katona
- 9 évvel ezelőtt
- Látták:
Átírás
1 AKTUÁLIS KÉRDÉSEK Ismét a paracetamolról Hazai Eszter 1, Monostory Katalin dr. 1, Bakos Ágnes dr. 2, Zacher Gábor dr. 2 és Vereczkey László dr. 1 Magyar Tudományos Akadémia, Budapest, Kémiai Kutatóközpont, Farmakobiokémiai Osztály (igazgató: Pálinkás Gábor dr.) 1 Péterfy Sándor utcai Kórház Erzsébet Kórháza, Budapest, Sürgősségi Belgyógyászati és Klinikai Toxikológiai Osztály (osztályvezető főorvos: Kárteszi Mihály dr.) 2 A szerzõk a paracetamol (acetaminophen) okozta májtoxicitás mechanizmusát és a mérgezettek terápiáját tekintik át. A paracetamol széles körben alkalmazott, vény nélkül is kapható láz- és fájdalomcsillapító. Terápiás dózisban biztonságosnak tekinthetõ, azonban az elmúlt évek során a túladagolásból vagya gondatlan alkalmazásból fakadó mérgezéses esetek száma megnövekedett. A hepatotoxicitásért a paracetamol egyik metabolitja, az N-acetil-p-benzokinonimin felelõs. Ma még nem rendelkezünk hatékonyterápiás stratégiával a paracetamol okozta májkárosodások kezelésére; a mérgezettek kezelése során a tápcsatorna-dekontaminációt, N-acetilcisztein antidotum adagolását és az elimináció fokozását tartalmazó protokollt alkalmazzák. Súlyos májkárosodás és idegrendszeri szimptómák esetén azonban szóba jöhet a nekrotikus máj eltávolítása és a májtranszplantáció is. Kulcsszavak: paracetamol-túladagolás, hepatotoxicitás, N-acetil-pbenzokinonimin About hepatotoxicity of paracetamol overdose. The mechanism of hepatotoxicitycaused byparacetamol (acetaminophen) overdose and the treatment of patients is reviewed. Paracetamol is widelyused over-the-counter drug with analgesic and antipyretic properties. Although it is considered to be safe at therapeutic doses, the incidence of hepatotoxicitycaused byoverdose or inadvertent application has been increasing lately. N-acetyl-p-benzoquinonimine, one of the metabolites formed from paracetamol is responsible for the hepatotoxicity. Until now there is no complete therapeutic strategyfor the effective treatment of hepatotoxicitycaused byparacetamol. Gut decontamination, N-acetylcystein antidote administration and enhancement of elimination is used for the management of paracetamol overdose. Those with severe hepatotoxicity and neurological symptomes can benefit from removal of necrotic liver and undergo transplantation. Key words: paracetamol overdose, hepatotoxicity, N-acetyl-pbenzoquinonimine A paracetamol (4 -hidroxi-acetanilid, acetaminophen) évtizedek óta széles körben használt, vény nélkül is kapható láz- és fájdalomcsillapító. Megfelelően alkalmazva biztonságos, terápiás dózisban kevés mellékhatást mutat, azonban túladagolása az egyik leggyakoribb oka a gyógyszeres májkárosodásoknak és a fulmináns májelégtelenségeknek, amelyek gyakran halálos kimenetelűek (3, 10, 14, 30, 32, 37, 47, 50). Magyarországon az első paracetamol-tartalmú készítményt, a Scutamil-C-t (EGIS Gyógyszergyár Rt., Budapest) 1967-ben, majd a Rubophent (Chinoin Gyógyszer és Vegyészeti Termékek Gyára Rt., Budapest) 1989-ben törzskönyvezték (az Országos Gyógyszerészeti Intézet adatai). Felhasználása hazánkban is folyamatosan növekszik (1. ábra), különösen 1996 óta a médiában történő szabad reklámozásnak köszönhetően. A mérgezéses esetek, főként a könnyű hozzáférhetőség miatt Magyarországon is egyre szaporodnak, a Péterfy Sándor utcai Kórház adatai szerint évente paracetamol okozta gyógyszermérgezés fordul elő. Különösen tanulságos annak a férfinak az esete, aki panaszaival 24 órán belül először a háziorvosához, később a patikához, végül az éjszakai ügyelethez fordult, majd ezek tanácsára mindháromszor paracetamol-tartalmú készítményt szedett (3 1 g). Szerencsére a paracetamol kiváltotta májkárosodásból a beteg maradéktalanul gyógyult. A véletlen túladagolás mellett gyógyszeres öngyilkossági kísérletek gyakori eszköze elsősorban a fiatalok, azon belül is a nők körében (13). A sikeres suicid-esetek hátterében meglehetősen eltérő paracetamol-dózis állhat. A magyarországi esetleírások tanulmányozása során találkozhattunk 9 g és 45 g okozta halálos kimenetelű kísérletekkel is. Az irodalomban azonban egyre többször találkozunk olyan esetleírásokkal, ahol a paracetamol-kezelés bizonyos körülmények között (tuberculosis miatt alkalmazott izoniazid-kezelés, alkoholizmus vagy rossz tápláltsági állapot miatt) a terápiás alkalmazás mellett is súlyos következményekkel járt (4, 12, 17, 21, 36, 48). Szerencsés véget ért egy 37 éves nőbeteg esete, akit szubakut májelégtelenséggel szállítottak a Szent László Kórházba ez év elején. Korábban lázcsillapításul terápiás dózisban két héten keresztül kapott paracetamolt, majd ezt követően amoxycillin (Augmentin)-kezelésben részesült (szintén terápiás dózisban). Mivel a máj nem mutatott regenerációs készséget, májtranszplantációra volt szükség. A beteg azóta felépült és elhagyta a Transzplantációs Klinikát. A paracetamol-mérgezés klinikai jellemzõi Kockázatbecslés akut mérgezés esetén Ma elfogadott toxikus dózis felnőttek esetén 7,5 g-nál (250 mg/kg, illetve gyerekeknél 150 mg/kg-nál magasabb dózis (2, 47, 50). A paracetamol-mérgezés korai időszakában (az első 24 órában) gasztrointesztinális tünetek jelentkeznek: étvágytalanság, hányinger, hányás, hastáji Orvosi Hetilap 2001, 142 (7),
2 1. ábra: Paracetamolfogyasztás-változása hazánkban 2. ábra: A paracetamol hepatotoxicitásának megítélése fájdalom, izzadás, általános gyengeség, rossz közérzet, amelyek általában enyhülnek a órára. Azonban ebben a második szakaszban is megmarad a hastáji fájdalom (a has jobb felső negyedében), amelyhez csatlakoznak a kezdeti májtoxicitás tünetei: emelkedett szérumbilirubin- és transzamináz-szint (GOT, GPT akár 100-szoros emelkedése), megnövekedett protrombinidő, valamint az artériás ph csökkenése (ph < 7,3) és a hypoglykaemia (13, 43). A 72. óra után a toxicitástól függő súlyosságú tünetek várhatók: fulmináns májelégtelenség, encephalopathia, esetleg kóma. Igen súlyos esetben a 3 5. nap táján bekövetkezhet a halál. Azoknál a mérgezetteknél, akik túljutnak ezen a harmadik szakaszon, a klinikai tünetek enyhülnek, a szérum-transzaminázok szintje normalizálódik és szerencsés esetben nem alakul ki krónikus májdiszfunkció (47). A paracetamol-mérgezés korai felismerése rendkívül fontos a halálesetek elkerülésében. Mivel a paracetamolmérgezés kezdeti tünetei általánosak (nem specifikusak) és emiatt nehezen felismerhetők, a mérgezett aktuális állapotának legbiztosabb meghatározása a paracetamolvérszint alapján történik. A Rumack-Matthew nomogram néven elterjedt koncentráció-idő görbe alapján becsülhető a májkárosodás kialakulásának valószínűsége és meghatározható a szükséges terápia. A gyógyszer bevétele után 4 órával mérhető 200 mg/l, illetve 15 órával kapott 30 mg/l paracetamol-vérszint által meghatározott egyenes alapján felmérhető a toxicitási kockázat mértéke (2. ábra, szaggatott vonal). Ezt a nomogramot használják ma is Nagy-Britanniában, míg Kanadában és az Egyesült Államokban a nagyobb érzékenység végett 25%-kal csökkentették a toxicitási kockázatot, valamint a kezelést meghatározó görbe lefutási magasságát (2. ábra, folyamatos vonal). A görbe alapján, következtetni lehet arra, hogy a májkárosodást jelző szérum-transzaminázszint (glutamát oxálacetát transzamináz [GOT], ill. glutamát piruvát transzamináz [GPT]) meghaladja-e az 1000 U/l-t. A nomogram nem ad közvetlen becslést a túlélési esélyekre, de segítséget nyújt a kezelés tervezésében (47). Amennyiben a beteg paracetamol-vérszintje a bevételtől számított 4 óra múlva a Rumack-Matthew nomogram 150-es görbéje (folyamatos vonal) felett van, a májkárosodás kockázata igen magas és a terápia azonnali megkezdése létfontosságú. Ha a 4. órában mért paracetamol-koncentráció az egyenes alatt található, akkor 6 órával később ismételten meg kell mérni a vérszintet, amely eldönti a kezelés szükségességét. A módszer azonban egy az egyben nem alkalmazható a következő esetekben: májműködési zavarokban szenvedő betegeknél, például alkoholistáknál; alultáplált egyéneknél, illetve krónikus betegség miatt fennálló, általánosan gyenge állapotú betegeknél; egyes gyógyszerek egyidejű adása esetén (például isoniazid). A toxicitás mechanizmusa A paracetamol felszívódása terápiás dózisban teljes és gyors. Biológiai hasznosíthatósága 75%, fehérjekötődése 30 50%-os, a csúcskoncentráció 0,5 2 óra között mérhető, a plazma felezési idő 1,5 2,5 óra, míg a plazma clearance értéke 400 ml/perc (2). A paracetamol terápiás adagolása esetén kb. 96%-ban a májban metabolizálódik, 4%-a változatlan formában a vizelettel ürül (2). A metabolizmus fő útja az UDP-glükuronil-transzferáz (kb. 60%) és szulfotranszferáz (kb. 30%) enzimeken keresztül valósul meg. Az így képződő paracetamol-glükuronid és paracetamol-szulfát konjugátumok elsősorban a vizelettel és kis mennyiségben az epével (paracetamol-glükuronid) ürülnek (2). További 4 5% a máj citokróm P450 enzimrendszeren keresztül alakul át 3-hidroxi-paracetamollá, illetve a reaktív N-acetil-para-benzokinoniminné (NAPQI) (8, 9, 34, 40). Terápiás dózisban csak nyomnyi mennyiségű NAPQI képződik, amely a sejtekben jelenlevő redukált glutation hatására vagy paracetamollá redukálódik, vagy glutationnal konjugálódva 3-glutation-S-il-paracetamolt képez (2). A 3-hidroxi-paracetamol szintén glutationnal való konjugáció után ürül (2, 8) (3. ábra). A paracetamol túladagolása esetén az UDP-glükuronil- és szulfotranszferáz enzimek működéséhez szükséges anyagok (UDP-glükuronsav, foszfoadenozil-foszfoszulfát) elfogynak és a metabolizmus egyre inkább a citokróm P450 enzimrendszer irányába terelődik (2, 38). Mivel a sejtek glutationkészlete is véges, a termelődő oxidált metabolitok (NAPQI, 3-hidroxi-paracetamol) felhalmozódnak a sejtben. A paracetamol túladagolás esetén fellépő toxikus hatásért a reaktív NAPQI a felelős (2, 9, 34, 40). A NAPQI, toxicitásának oka elsősorban az, hogy a fehérjék ciszteinjének SH-csoportjához kovalensen kötődik, fehérjeadduktot képez (2, 15, 16, 19, 28). Megjegyeznénk, hogy a cisztein mellett kismértékben a lizin és hisztidin aminosavakhoz is képes kapcsolódni (2). Ennek következtében a fehérjék működésképtelenné válnak, ami a májsejt pusztulásához vezet, végül súlyos májnekrózis alakulhat ki. Párhuzamosan renalis tubularis nekrózis is bekövetkezhet, de a vesetoxicitás mechanizmusa kevésbé tisztázott (2). Magas, de még terápiás dózisú paracetamol hosszú távú alkalmazása esetén a krónikus vesekárosodás kockázata megnő (2, 18). 346
3 szén alkalmazásának is csak a bevételtől számított egy órán belül van értelme. Gyomormosás legfeljebb akkor javallott, ha a beteg igen nagy (halálos) mennyiséget vett be és a gyógyszer bevétele után 1 órán belül elvégezhető. A 4. órán túl a gastricus dekontaminációs eljárásoknak azonban már nincs értelme (47). 3. ábra: A paracetamol metabolizmusa Gyermekek esetén ritkábban fordul elő paracetamol-mérgezés. A gyermekek szervezetében a paracetamol elsősorban a szulfotranszferáz enzimeken keresztül metabolizálódik. Feltételezhető, hogy a gyermekeknél a májsejtek glutationkészlete is gyorsabban regenerálódik paracetamol-túladagolás esetén (47). Paracetamol-mérgezés esetén használatos kezelés Tápcsatorna-dekontamináció A tápcsatornából történő további felszívódás megakadályozása érdekében korábban ipecacuanaval végzett hánytatást ma már nem alkalmazzák, inkább gyomormosás használatos a mérgezés korai stádiumában. A tápcsatorna további dekontaminációját szolgálja az aktív szén adagolása. Underhill és munkatársai egy vizsgálatban összehasonlították az ipecacuanaval végzett hánytatás, illetve gyomormosás és az aktív szén adagolásának hatását paracetamol-mérgezés esetén (45). A vizsgálatok eredménye azt mutatta, hogy az aktív szén használata 52,2%-kal csökkentette a paracetamol vérplazmában mért koncentrációját, míg az ipecacuana használata vagy gyomormosás esetén ez az érték 40,7% és 39,3% volt. De az aktív N-acetilcisztein A paracetamol legfontosabb antidotuma az N-acetilcisztein (2, 5, 20). Egyrészt a sejt glutationkészletének pótlását segíti elő, így a túladagolás során nagy mennyiségben képződő NAPQI inaktiválását végzi. Az N-acetilciszteinből a májsejtben cisztein képződik, amely glutaminsavval és glicinnel kapcsolódva hozza létre a glutationt. Ugyanakkor az N-acetilcisztein prekurzora a foszfo-adenozilfoszfoszulfátnak is, amely a még át nem alakult paracetamol szulfát-konjugációjához szükséges. Ezek mellett az N-acetilcisztein tiolcsoportja közvetlenül is kapcsolódhat a képződött N-acetil-p-benzokinoniminhez (20). Kanadában és Nagy-Britanniában 20 órán át 300 mg/kg iv. dózisban kapják a betegek az N-acetilciszteint, míg az Egyesült Államokban az alkalmazott dózis 1330 mg/kg p.o. 72 órán át. Egyes szerzők úgy gondolják, hogy az N-acetilciszteint a paracetamol bevételétől számított 15 órán belül lehet csak hatékonyan alkalmazni, de a tapasztalatok azt mutatják, hogy még 24 órán belül is lehet hatást elérni (20, 47). Több szerző (7, 11, 29, 41) megkérdőjelezte az N-acetilcisztein és az aktív szén együttadásának a hasznosságát. (Megjegyzendő, hogy van olyan vélemény is, amely pont ezen vizsgálatok érvényességét kérdőjelezi meg [42].) Mivel az aktív szén fizikailag köti a molekulákat, az N-acetilcisztein együttes orális adagolásával csökkenhet a hatás. In vivo és in vitro kísérletekkel bebizonyították, hogy az N-acetilcisztein csak 10 50%-ban kötődik az aktív szénhez, míg ez az arány 50 90% paracetamol esetén (24). Ugyanakkor az aktív szén egyidejű alkalmazása csökkenti az acetilcisztein felszívódását (47), amely esetlegesen kivédhető magasabb (40%-kal) dózisú acetilcisztein adagolásával, vagy a kezelési protokoll módosításával, miszerint az aktív szén beadása után kétórás különbséggel kerüljön sor az N-acetilciszteinnel történő kezelésre. Ez utóbbi azonban nem biztos, hogy célra vezető, mivel a terápia során lényeges szempont, hogy az N-acetilciszteint minél hamarabb megkapja a beteg. A fentieket megfontolva Magyarországon intravénásan juttatják be az N-acetilciszteint a következő protokoll szerint: az első 15 perc során 150 mg/kg-ot (200 ml 5%-os dextrózban), majd 4 órán belül 50 mg/kg-ot (500 ml 5%-os dextrózban), végül a következő 16 óra alatt 100 mg/kg-ot (2000 ml 5%-os dextrózban) adagolnak. Az orális N-acetilcisztein-kezeléssel szemben az intravénás terápia előnyei között említhető, hogy kisebb mennyiség szükséges, az aktív szén nem befolyásolja az abszorpcióját és eszméletlen, vagy hányó betegeknél is alkalmazható. Cimetidin A paracetamol toxikus metabolitja, az N-acetil-p-benzokinonimin (NAPQI) a citokróm P450 enzimrendszeren keresztül keletkezik (2, 8). A citokróm P450 géncsaládba rendkívül heterogén, eltérő, ugyanakkor átfedő szubsztrátspecifitással rendelkező enzimek tartoznak. Az enzimek átfedő szubsztrátspecifitásának köszönhetően egy metabolit képződésének hátterében több enzim is állhat (27). A NAPQI képződésében bizonyítottan szerepe van CYP1A2, a CYP2A6, CYP2E1 és a CYP3A4 enzi- 347
4 meknek (2, 8, 22, 31, 49). Ezen enzimek közül terápiás dózisban a CYP3A4, míg túladagolás esetén a CYP2E1 és CYP1A2 enzimeknek van kitüntetett szerepe (2). A cimetidint a citokróm P450 enzimekre kifejtett gátló hatása miatt használják. A cimetidin valóban gátolja a citokróm P450 enzimek közül a CYP2C9-et (33), de ez az enzim bizonyítottan nem vesz részt a paracetamol toxikus metabolitjának képzésében. Ezért paracetamol-túladagolás esetén mint azt klinikai vizsgálatok is megállapították a cimetidinnek nincsen jelentősége a mérgezés kezelésében (6). Egyéb teendők, lehetőségek Toxikus vérszintek esetén a paracetamol eliminációjának fokozására hemoperfúzió szintén alkalmazható, sőt a Rumack-Matthew nomogram 150-es vonala (a paracetamol-bevételt követő 4. órában mért 150 mg/ml-es vérszint a 2. ábrán folyamatos vonal jelzi ) feletti vérszintek esetén minden esetben alkalmazzák. A legsúlyosabb mérgezéses esetekben, ahol már nincs remény a máj megfelelő regenerációjára, májtranszplantáció javasolható a következő szigorú kritériumok mellett: az artériás ph < 7,3 vagy a 3 4. fokozatú encephalopathia, a 300 µmol/l feletti szérumkreatinin-szint, illetve a 100 s-nál magasabb protrombinidő (INR 7,5) együttes jelentkezése (13). A májátültetés esetén azonban a magas költségigény mellett komoly problémát jelenthet az időben elérhető megfelelő donorszerv hiánya. A problémát súlyosbítja, hogy számos paracetamol-tartalmú készítmény van forgalomban (Magyarországon több mint 30) (43), amelyeket a média igen nagy hatékonysággal reklámoz, a veszélyekre való figyelmeztetés pedig vagy hiányzik, vagy korántsem megfelelő. Habár a mérgezettek száma emelkedett, az elmúlt években Magyarországon szociológiai szempontból messze nem olyan súlyos a helyzet, mint Angliában vagy az USA-ban. A paracetamol okozta mérgezéses esetek csökkentését célzó intézkedések is jelenthetnek némi változást a jelenlegi helyzethez képest. Nagy-Britanniában 1998-tól 8 g-ra korlátozták az 1 dobozban lévő paracetamol mennyiségét (39, 44, 46) (100 tablettánál nagyobb mennyiséget csak receptre adnak ki). Egy 1999 augusztusában végzett felmérés szerint a könnyen hozzáférhető paracetamol mennyiségének korlátozása csökkentette a hepatotoxicitás előfordulását (39, 44). A paracetamol-mérgezések kiküszöbölését célzó kutatási irányok A paracetamol toxicitásának megakadályozására több irányban folynak világszerte kutatások. A szervezet glutationkészletének mihamarabbi regenerációját (így a detoxikációt) glutationprekurzorok adásával próbálják elősegíteni (2). A NAPQI fehérjékkel való adduktképzését megelőzendő redukáló hatású vegyületekkel (például ebselen) paracetamollá történő visszaalakítást célzó vizsgálatok (2, 25). A toxicitás másik lehetséges kezelése a NAPQI képződéséért felelős citokróm P450 enzimek gátlása (2, 23, 26, 35). Mivel a NAPQI kovalens kötődése a fehérjékhez 3,5 helyzetben történik, próbálkozások történnek a paracetamol 3,5 helyzetben szubsztituált változatainak előállításával (vizsgálva, hogy a szubsztituált vegyület megtartja-e farmakológiai hatását) (1, 2). IRODALOM: 1. Bessems, J. G. M.: Hepatoxicity of paracetamol and structural analogues. Thesis Vrije Universiteit Amsterdam, Bessems, J. G. M., Te Koppele, P. A., van Dijk, P. A. és mtsai: Rat liver cytochrome P450-dependent oxidation of 3,5 disubstitued analogues of paracetamol. Xenobiotica, 1996, 26, Black, M.: Acetaminophen hepatotoxicity. Ann. Rev. Med., 1984, 35, Bonkovsky, H. L., Kane, K. E., Jones, D. P. és mtsai: Acute hepatic and renal toxicity from low doses of acetaminophen in the absence of alcohol abuse or malnutrition: evidence for increased susceptibility to drug toxicity due to cardiopulmonary and renal insufficiency. Hepatol., 1994, 19, Bruno, M. K., Cohen, S. D., Khairallah, E. A.: Antidotal effectiveness of N-acetylcysteine in reversing acetaminophen-induced hepatotoxicity. Bio. Pharm., 1988, 37, Burkhart, K. K., Janco, N., Kulig, K. W.: Cimetidine as adjunctive treatment for acetaminophen overdose. Hum. Exp. Toxicol. (England), 1995, 14, Chamberlain, J. M., Gorman, R. L., Oderda, G. M. és mtsai: Use of activated charcoal in a simulated poisoning with acetaminophen: a new loading dose for N-acetylcysteine? Ann. Emerg. Med. (United States), 1993, 22, Chen, W., Koenigs, L. L., Thompson, S. J. és mtsai: Oxidation of acetaminophen to its toxic quinone imine and nontoxic cathecol metabolites by baculovirus-expressed and purified human cytochromes P4502E1 and P4502A6. Chem. Res. Toxicol., 1998, 11, Dahlin, D. C., Miwa, G. T., Lu, A. Y. H. és mtsa: N-acetyl-p-benziquinone imine: A cytochrome P450 mediated oxidation product of acetaminophen. Proc. Natl. Acad. Sci. USA, 1984, 81, Elek, S.: Paracetamol. Gyógyszereink, 1997, 47, Ekins, B. R., Ford, D. C., Thompson, M. I.: The effect of activated charcoal on N-acetylcysteine absorption in normal subjects. Am. J. Em. Med., 1987, 5, Gabriel, R.: Paracetamol induced acute renal failure in the absence of fulminant liver damage. Br. Med. J., 1982, 284, O Grady, J. G.: Paracetamol hepatoxicity: how to prevent. J. R. Soc. Med., 1997, 90, Hinson, J. A.: Biochemical toxicology of acetaminophen. Rev. Bioch. Toxicol., 1980, 2, Hinson, J. A., Pumford, N. R., Roberts, W.: Mechanisms of acetaminophen toxicity. immunochemical detection of drug-protein adducts. Drug. Metab. Rev., 1995, 27, Holtzmann, J. L.: The role of covalent binding to microsomal proteins in the hepatoxicity of acetaminophen. Drug. Metab. Rev., 1995, 27, JákóJ., AratóG.: Amidazophen. Igen vagy nem? Orv. Hetil., 1995, 136, Johnson, G. K., Tolman, K. G.: Chronic liver disease and acetaminophen. Ann. Int. Med., 1977, 87, Jollow, D. J., Mitchell, J. R., Potter, W. Z. és mtsai: Acetaminophen-induced hepatic necrosis. II. Role of covalent binding in vivo. J. Pharm. Exp. Ther. (United States), 1973, 187, Jones, A. L.: Mechanism of action and value of N-acetylcysteine in the treatment of early and late acetaminophen poisoning: a critical review. Clin. Toxicol., 1998, 36, Kádas I., Könczöl F., Illés T.: Terápiás dózisban alkalmazott paracetamol okozta heveny fatális májkárosodás. Orv. Hetil., 1998, 139, Kostrubsky, V. E., Szakacs, J. G., Jeffery, E. H. és mtsai: Role of CYP3A in ethanol-mediated increases in acetaminophen hepatotoxicity. Toxicol. Appl. Pharm., 1997, 143, Chen, L., Mohr, N. R., Yang, C. S.: Decrease of plasma and urinary oxidative metabolites of acetaminophen after consumption of watercress by human volunteers. Clin. Pharm. Ther., 1996, 60, Lewis, R. K., Paloucek, F. P.: Assessement and treatment of acetaminophen overdose. Clin. Pharm., 1991, 10, Li, Q. J., Bessems, J. G. M., Commandeur, B. A. és mtsai: Mechanism of protection of ebselen against paracetamol-induced toxicity in rat hepatocytes. Bioch. Pharm., 1994, 48, Li, Y., Wang, E. J., Chen, L. és mtsai: Effects of phenetyl isothiocyanate on acetaminophen metabolism and hepatotoxicity in mice. Toxicol. Appl. Pharm., 1997, 144, Monostory K., Lakatos B., Vereczkey L.: Citokróm P450 enzimek: szerkezet, aktivitás, 348
5 indukció és gyakorlati jelentőségek. Act. Pharm. Hung., 1992, 62, Nelson, S. D.: Mechanism of the formation and disposition of reactive metabolites that can cause acute liver injury. Drug Metab. Rev., 1995, 27, North, D. S., Peterson, R. G., Krenzelok, E. P.: Effect of activated charcoal administration on acetylcysteine serum levels in humans. Am. J. Hosp. Pharm., 1981, 38, Olsson, R.: Increased hepatic sensitivity to paracetamol. Lancet, 1978, 2, Patten, C. J., Thomas, P. E., Guy, R. L. és mtsai: Cytochrome P450 enzymes involved in acetaminophen activation by rat and human liver microsomes and their kinetics. Chem. Res. Toxicol., 1993, 6, Pár A.: A paracetamol toxicitásáról. Orv. Hetil., 1998, 139, Pichard, L., Fabre, I., Fabre, G. és mtsai: Cyclosporin A drug interactions. Screening for inducers and inhibitors of cytochrome P450 in primary cultures of human hepatocytes and in liver microsomes. Drug Metab. Dispos., 1990, 18, Potter, W. Z., Davis, D. C., Mitchell, J. R. és mtsai: Acetaminophen induced hepatic necrosis III. Cytochrome P450-mediated covalent binding in vitro. J. Pharm. Exp. Ther., 1973, 187, Prasad, J. S., Chen, N. Q., Liu, Z. X. és mtsai: Effects of ethanol and inhibitors on the binding and metabolism of acetaminophen and N-acetyl-p-benzoquinone imine by hepatic microsomes from control and ethanol-treated rats. Bioch. Pharm., 1990, 40, Prescott, L. F., Proudfoot, A. T., Cregeen, R. J.: Paracetamol induced acute renal failure in the absence of fulminant liver damage. Br. J. Med., 1982, 284, Prescott, L. F.: Paracetamol overdosage- Pharmacological considerations and clinical management. Drugs (Australia), 1983, 25, Prescott, L. F.: Paracetamol critical bibliograhic review. Taylor and Francis Ltd., Prince, M. I., Thomas, S. H. L., James, O. F. W. és mtsai: Reduction in incidence of severe paracetamol poisoning. Lancet, 2000, 355, Raucy, J. L., Lasker, J. M., Lieber, C. S. és mtsai: Acetaminophen activation by human liver cytochromes P450IIE1 and P450IA2. Arch. Bioch. Biophys., 1989, 271, Renzi, F. P., Donovan, J. W., Martin, T. G. és mtsai: Concomitant use of activated charcoal and N-acetylcysteine. Ann. Em. Med., 1985, 14, Spiller, H. A., Krenzelok, E. P., Grande, G. A. és mtsai: A prospective evaluation on the effect of activated charcoal before oral N-acetylcysteine is acetaminophen overdose. Ann. Em. Med., 1994, 23, Szendei K.: Gyógyszer a családban. Springer Hungarica Kft., Turvill, J. L., Burroughs, A. K., Moore, K. P.: Change in occurrence of paracetamol overdose in UK after introduction of blister packs. Lancet, 2000, 355, Underhill, T. J., Greene, M. K., Dove, A. F.: A comparison of the efficacy of gastric lavage, ipecacuanha and activated charcoal in the emergency management of paracetamol overdose. Arch. Em. Med., 1990, 7, Wise, J.: Restriction of paracetamol planned. Br. J. Med., 1996, 313, Zed, P. J., Krenzelok, E. P.: Treatment of acetaminophen overdose. Am. J. Health-Syst. Pharm., 1999, 56, Zezulka, A., Wright, N.: Severe metabolic acidosis early in paracetamol poisoning. Br. J. Med., 1982, 285, Zhou, L., Erickson, R. R., Hardwick, J. P. és mtsai: Catalysis of the cysteine conjugation and protein binding of acetaminophen by microsomes from human lymphoblast line transfected with cdnas of various forms of human cytochrome P450. J. Pharm. Exp. Ther., 1997, 281, Zacher G., Faddi P.: Valóban segít az elefánt? Egy gyógyszerreklám margójára. Gyógyszereink, 1997, 47, (Hazai Eszter, Budapest, Pf ) SPRINGER TUDOMÁNYOS KIADÓ KÖNYVAJÁNLATA Cserhalmi Lívia: Szívelégtelenség A szívelégtelenséget, mely a legkülönbözőbb cardialis elváltozások következményeként alakulhat ki, ma a legjelentősebb cardiovascularis szindrómának tekintik. A krónikus szívelégtelenségben szenvedő betegek kezelésének, gondozásának és gyakori kórházi ápolásának igénye világszerte egyre nagyobb társadalom-egészségügyi probléma, a halálozás ennek ellenére a malignus betegségekével egyezik. A patofiziológia és a terápiás lehetőségek kutatása ma a kardiológia egyik centrális kérdése és az elmúlt évtizedben új, korszerű szemlélethez vezetett. Eszerint a szívelégtelenség multiszisztémás kórkép, melyet a szívizom strukturális és funkcionális elváltozásán alapuló cardialis funkciózavar mellett elsősorban a neuroendokrin-szabályozás rendellenességei jellemeznek. Ennek megfelelően változtak a terápiás elvek is. A szemléleti változásokat összefoglaló kézikönyv hazánkban eddig még nem jelent meg. A hazánkban e területen kiemelkedő széles körű klinikai tapasztalattal és tudományos munkássággal bíró belgyógyász kardiológus szerző igen nehéz feladatra, a hatalmas nemzetközi szakirodalom rövid, magyar nyelvű összefoglalására vállalkozott. A könyv tömör és didaktikus áttekintést nyújt a szívelégtelenségnek az elmúlt évtizedben kialakult modern patofiziológiai, klinikai és terápiás vonatkozásairól, valamint a gondozás elveiről, a témában már alapismeretekkel rendelkező belgyógyászoknak, kardiológusoknak, valamint szakorvos-jelölteknek és családorvosoknak. Terjedelem: 163 oldal Ár: Ft Springer Tudományos Kiadó Cím: 1088 Budapest, Múzeum u. 9. fszt. Levélcím: 1463 Budapest, Pf Telefon: , fax: sprinkia@mail.matav.hu 349
A Kockázatkezelési Terv Összefoglalója
 1 A Kockázatkezelési Terv Összefoglalója Hatóanyag/hatóanyagcsoport paracetamol ATC N02BE01 Érintett készítmény(ek) Magyarországon Paracetamol Teva 10 mg/ml oldatos infúzió (MAH: Teva Gyógyszergyár Zrt.,
1 A Kockázatkezelési Terv Összefoglalója Hatóanyag/hatóanyagcsoport paracetamol ATC N02BE01 Érintett készítmény(ek) Magyarországon Paracetamol Teva 10 mg/ml oldatos infúzió (MAH: Teva Gyógyszergyár Zrt.,
Nemekre szabott terápia: NOCDURNA
 Nemekre szabott terápia: NOCDURNA Dr Jaczina Csaba, Ferring Magyarország Kft. Magyar Urológus Társaság XXI. Kongresszusa, Debrecen Régi és új megfigyelések a dezmopresszin kutatása során 65 év felett megnő
Nemekre szabott terápia: NOCDURNA Dr Jaczina Csaba, Ferring Magyarország Kft. Magyar Urológus Társaság XXI. Kongresszusa, Debrecen Régi és új megfigyelések a dezmopresszin kutatása során 65 év felett megnő
GYÓGYSZER MÉRGEZÉSEK ELŐADÓLŐADÓ DR. R. LEHEL EHEL JÓZSEFÓZSEF 2006.11.16. 1
 GYÓGYSZER MÉRGEZÉSEK ELŐADÓLŐADÓ DR. R. LEHEL EHEL JÓZSEFÓZSEF 2006.11.16. 1 GYÓGYSZERMÉRGEZÉSEK PARACETAMOL SZALICILÁTOK/NSAID KOFFEIN/XANTINSZÁRMAZÉKOK 2006.11.16. 2 PARACETAMOL MÉRGEZÉS 2006.11.16.
GYÓGYSZER MÉRGEZÉSEK ELŐADÓLŐADÓ DR. R. LEHEL EHEL JÓZSEFÓZSEF 2006.11.16. 1 GYÓGYSZERMÉRGEZÉSEK PARACETAMOL SZALICILÁTOK/NSAID KOFFEIN/XANTINSZÁRMAZÉKOK 2006.11.16. 2 PARACETAMOL MÉRGEZÉS 2006.11.16.
III. melléklet. Az Alkalmazási előírás és a Betegtájékoztató vonatkozó fejezeteiben szükséges módosítások
 III. melléklet Az Alkalmazási előírás és a Betegtájékoztató vonatkozó fejezeteiben szükséges módosítások Megjegyzés: Ezen alkalmazási előírás, betegtájékoztató és cimkeszöveg a referál eljárás eredményeként
III. melléklet Az Alkalmazási előírás és a Betegtájékoztató vonatkozó fejezeteiben szükséges módosítások Megjegyzés: Ezen alkalmazási előírás, betegtájékoztató és cimkeszöveg a referál eljárás eredményeként
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ Mielőtt elkezdené gyógyszerét alkalmazni,
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ BETEGTÁJÉKOZTATÓ Mielőtt elkezdené gyógyszerét alkalmazni,
Add, amid van dilemmák súlyos digoxin-mérgezésben
 Add, amid van dilemmák súlyos digoxin-mérgezésben Pap Csaba Zsolt 1, Elek István 1 BallaginéSzabó Klára 2, Kovács Dóra 2, LeczkiKrisztina 2, Mező Nikoletta 2 1 Sürgősségi Betegellátó Osztály és Klinikai
Add, amid van dilemmák súlyos digoxin-mérgezésben Pap Csaba Zsolt 1, Elek István 1 BallaginéSzabó Klára 2, Kovács Dóra 2, LeczkiKrisztina 2, Mező Nikoletta 2 1 Sürgősségi Betegellátó Osztály és Klinikai
Gyógyszeres kezelések
 Gyógyszeres kezelések Az osteogenesis imperfecta gyógyszeres kezelésében számos szert kipróbáltak az elmúlt évtizedekben, de átütő eredménnyel egyik se szolgált. A fluorid kezelés alkalmazása osteogenesis
Gyógyszeres kezelések Az osteogenesis imperfecta gyógyszeres kezelésében számos szert kipróbáltak az elmúlt évtizedekben, de átütő eredménnyel egyik se szolgált. A fluorid kezelés alkalmazása osteogenesis
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1/33 1. A GYÓGYSZER MEGNEVEZÉSE Resolor 1 mg-os filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 mg prukaloprid filmtablettánként (prukaloprid-szukcinát formájában).
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1/33 1. A GYÓGYSZER MEGNEVEZÉSE Resolor 1 mg-os filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 mg prukaloprid filmtablettánként (prukaloprid-szukcinát formájában).
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai
 Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Új orális véralvadásgátlók
 Új orális véralvadásgátlók XI. Magyar Sürgősségi Orvostani Kongresszus Lovas András, Szegedi Tudományegyetem, Aneszteziológiai és Intenzív Terápiás Intézet Véralvadásgátlók alkalmazási területei posztoperatív
Új orális véralvadásgátlók XI. Magyar Sürgősségi Orvostani Kongresszus Lovas András, Szegedi Tudományegyetem, Aneszteziológiai és Intenzív Terápiás Intézet Véralvadásgátlók alkalmazási területei posztoperatív
40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban).
 1. A GYÓGYSZER NEVE Zovirax 40 mg/ml belsőleges szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban). Ismert hatású segédanyagok:
1. A GYÓGYSZER NEVE Zovirax 40 mg/ml belsőleges szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban). Ismert hatású segédanyagok:
3 sz. Gyógyszertudományok Doktori Iskola.sz. Program. és kurzuscím Óra
 3 sz. Gyógyszertudományok Doktori Iskola.sz. Program Kód Kurzusvezetö és kurzuscím Óra 2012-13/1 2012-13/2 2013-14/1 2013-14/2 2014-15/1 2014-15/2 0032- KV Dr. Tóthfalusi László 3208 Dr. Farsang Csaba
3 sz. Gyógyszertudományok Doktori Iskola.sz. Program Kód Kurzusvezetö és kurzuscím Óra 2012-13/1 2012-13/2 2013-14/1 2013-14/2 2014-15/1 2014-15/2 0032- KV Dr. Tóthfalusi László 3208 Dr. Farsang Csaba
III. melléklet. Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak ezen módosításai a referral eljárás eredményeként jöttek létre.
 III. melléklet Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak módosításai Megjegyzés: Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak ezen módosításai a referral
III. melléklet Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak módosításai Megjegyzés: Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak ezen módosításai a referral
Olvassa el figyelmesen az alábbi betegtájékoztatót, mely az Ön számára fontos információkat tartalmaz.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmesen az alábbi
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmesen az alábbi
A krónikus veseelégtelenség kardio-metabolikus kockázata
 A krónikus veseelégtelenség kardio-metabolikus kockázata Dr. Kiss István Fıv. Önk. Szent Imre Kórház, Belgyógyászati Mátrix Intézet, Nephrologia-Hypertonia Profil 1 2 SZÍV ÉS ÉRRENDSZERI KOCKÁZAT ÉS BETEGSÉG
A krónikus veseelégtelenség kardio-metabolikus kockázata Dr. Kiss István Fıv. Önk. Szent Imre Kórház, Belgyógyászati Mátrix Intézet, Nephrologia-Hypertonia Profil 1 2 SZÍV ÉS ÉRRENDSZERI KOCKÁZAT ÉS BETEGSÉG
PPI VÉDELEM A KEZELÉS SORÁN
 75 mg diclofenák-nátrium, 20 mg omeprazol módosított hatóanyag-leadású kemény kapszula PPI VÉDELEM A KEZELÉS SORÁN Jelentős fájdalom- és gyulladáscsökkentő hatás 1 Savkontroll az omeprazol segítségével
75 mg diclofenák-nátrium, 20 mg omeprazol módosított hatóanyag-leadású kemény kapszula PPI VÉDELEM A KEZELÉS SORÁN Jelentős fájdalom- és gyulladáscsökkentő hatás 1 Savkontroll az omeprazol segítségével
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
(11) Lajstromszám: E 006 093 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000093T2! (19) HU (11) Lajstromszám: E 006 093 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 749886 (22) A bejelentés napja:
!HU0000093T2! (19) HU (11) Lajstromszám: E 006 093 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 749886 (22) A bejelentés napja:
Helyi érzéstelenítők farmakológiája
 Helyi érzéstelenítők farmakológiája SE Arc-Állcsont-Szájsebészeti és Fogászati Klinika BUDAPEST Definíció Farmakokinetika: a gyógyszerek felszívódásának, eloszlásának, metabolizmusának és kiürülésének
Helyi érzéstelenítők farmakológiája SE Arc-Állcsont-Szájsebészeti és Fogászati Klinika BUDAPEST Definíció Farmakokinetika: a gyógyszerek felszívódásának, eloszlásának, metabolizmusának és kiürülésének
Új terápiás lehetőségek helyzete. Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály
 Új terápiás lehetőségek helyzete Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály Mucopolysaccharidosisok MPS I (Hurler-Scheie) Jelenleg elérhető oki terápiák Enzimpótló kezelés
Új terápiás lehetőségek helyzete Dr. Varga Norbert Heim Pál Gyermekkórház Toxikológia és Anyagcsere Osztály Mucopolysaccharidosisok MPS I (Hurler-Scheie) Jelenleg elérhető oki terápiák Enzimpótló kezelés
A PET szerepe a gyógyszerfejlesztésben. Berecz Roland DE KK Pszichiátriai Tanszék
 A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
A tabletta csaknem fehér színű, ovális és UCY 500 kódjelzéssel van ellátva.
 1. A GYÓGYSZER MEGNEVEZÉSE AMMONAPS 500 mg tabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 500 mg nátrium-fenil-butirát tablettánként. Minden AMMONAPS tabletta 62 mg nátriumot tartalmaz. A segédanyagok teljes
1. A GYÓGYSZER MEGNEVEZÉSE AMMONAPS 500 mg tabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 500 mg nátrium-fenil-butirát tablettánként. Minden AMMONAPS tabletta 62 mg nátriumot tartalmaz. A segédanyagok teljes
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Magnesium 250 mg Pharmavit pezsgőtabletta Magnesium Pharmavit 250 mg pezsgőtabletta
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Magnesium 250 mg Pharmavit pezsgőtabletta Magnesium Pharmavit 250 mg pezsgőtabletta
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-8/1/A-29-11 Az orvosi biotechnológiai
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-8/1/A-29-11 Az orvosi biotechnológiai
Diabéteszes redox változások hatása a stresszfehérjékre
 Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola Pathobiokémia Program Doktori (Ph.D.) értekezés Diabéteszes redox változások hatása a stresszfehérjékre dr. Nardai Gábor Témavezeto:
Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola Pathobiokémia Program Doktori (Ph.D.) értekezés Diabéteszes redox változások hatása a stresszfehérjékre dr. Nardai Gábor Témavezeto:
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Tabletta Magnesii Citrici 500 mg Fono VII. Parma Mielőtt elkezdené gyógyszerét
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Tabletta Magnesii Citrici 500 mg Fono VII. Parma Mielőtt elkezdené gyógyszerét
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
A prokalcitonin prognosztikai értéke
 A prokalcitonin prognosztikai értéke az első 24 órában Dr. Tánczos Krisztián SZTE Aneszteziológiai és Intenzív Terápiás Intézet Carlet et al. Antimicrobial Resistance and Infection Control 2012, 1:11 Carlet
A prokalcitonin prognosztikai értéke az első 24 órában Dr. Tánczos Krisztián SZTE Aneszteziológiai és Intenzív Terápiás Intézet Carlet et al. Antimicrobial Resistance and Infection Control 2012, 1:11 Carlet
Mérgezések. A mérgezés jellege Véletlen Suicid Szándékos. Mérgezések Sirák 1
 Mérgezések Fogorvosi körülmények között előfordul, bár nem gyakori Felismerésben fontos, hogy gondoljunk rá Méreg bekerülése a szervezetbe: Orálisan (leggyakoribb) Belélegezve Ép bőrön át felszívódva Parenterálisan
Mérgezések Fogorvosi körülmények között előfordul, bár nem gyakori Felismerésben fontos, hogy gondoljunk rá Méreg bekerülése a szervezetbe: Orálisan (leggyakoribb) Belélegezve Ép bőrön át felszívódva Parenterálisan
Az autonómia és complience, a fogyatékosság elfogadtatásának módszerei
 Az autonómia és complience, a fogyatékosság elfogadtatásának módszerei Dr. Kollár János egyetemi adjunktus Debreceni Egyetem Orvos- és Egészségtudományi Centrum, Népegészségügyi Kar Magatartástudományi
Az autonómia és complience, a fogyatékosság elfogadtatásának módszerei Dr. Kollár János egyetemi adjunktus Debreceni Egyetem Orvos- és Egészségtudományi Centrum, Népegészségügyi Kar Magatartástudományi
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! z alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmes Mielőtt elkezdené
FIGYELEM!!! z alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené szedni ezt a gyógyszert, olvassa el figyelmes Mielőtt elkezdené
1. A GYÓGYSZER NEVE 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL. Requip 0,5 mg filmtabletta
 1. A GYÓGYSZER NEVE Requip 0,25 mg filmtabletta Requip 0,5 mg filmtabletta Requip 1 mg filmtabletta Requip 2 mg filmtabletta Requip 5 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Requip 0,25 mg
1. A GYÓGYSZER NEVE Requip 0,25 mg filmtabletta Requip 0,5 mg filmtabletta Requip 1 mg filmtabletta Requip 2 mg filmtabletta Requip 5 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Requip 0,25 mg
A helyi érzéstelenítés szövődményei. Semmelweis Egyetem, Budapest Szájsebészeti és Fogászati Klinika
 A helyi érzéstelenítés szövődményei Semmelweis Egyetem, Budapest Szájsebészeti és Fogászati Klinika A helyi érzéstelenítés szövődményeinek okai Általános szövődmények: az érzéstelenítés anyaga Helyi szövődmények:
A helyi érzéstelenítés szövődményei Semmelweis Egyetem, Budapest Szájsebészeti és Fogászati Klinika A helyi érzéstelenítés szövődményeinek okai Általános szövődmények: az érzéstelenítés anyaga Helyi szövődmények:
A flavonoidok az emberi szervezet számára elengedhetetlenül szükségesek, akárcsak a vitaminok, vagy az ásványi anyagok.
 Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
A direkt hatású orális anticoagulánsok (DOAC) laboratóriumi vonatkozásai
 A direkt hatású orális anticoagulánsok (DOAC) laboratóriumi vonatkozásai Dr. Skrapits Judit Központi Laboratórium Markusovszky Oktató Kórház Szombathely MAÉT Kongresszus Szombathely, 2017.06.16. Prof.
A direkt hatású orális anticoagulánsok (DOAC) laboratóriumi vonatkozásai Dr. Skrapits Judit Központi Laboratórium Markusovszky Oktató Kórház Szombathely MAÉT Kongresszus Szombathely, 2017.06.16. Prof.
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA
 III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA Az alkalmazási előírás és a betegtájékoztató módosításai a Bizottság Határozatával egyidőben lépnek érvénybe. A Bizottsági Határozat
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA Az alkalmazási előírás és a betegtájékoztató módosításai a Bizottság Határozatával egyidőben lépnek érvénybe. A Bizottsági Határozat
változások az SM kezelésében: tények és remények
 változások az SM kezelésében: tények és remények Prof. Dr. Illés Zsolt Dél-Dániai Egyetem Odense az SM klinikai típusai relapszussal remisszióval szekunderprogresszív primer progresszív progresszív relapszáló
változások az SM kezelésében: tények és remények Prof. Dr. Illés Zsolt Dél-Dániai Egyetem Odense az SM klinikai típusai relapszussal remisszióval szekunderprogresszív primer progresszív progresszív relapszáló
PTE ÁOK Gyógyszerésztudományi Szak
 PTE ÁOK Gyógyszerésztudományi Szak Alapfogalmak 2017. 09. 22. 14:59 2 Biofarmácia tankönyv 2017. 09. 22. 14:59 3 Hogyan és mikor kell bevenni? Szedhetik-e várandósok? Szedhetik-e szoptató anyukák? Mikor
PTE ÁOK Gyógyszerésztudományi Szak Alapfogalmak 2017. 09. 22. 14:59 2 Biofarmácia tankönyv 2017. 09. 22. 14:59 3 Hogyan és mikor kell bevenni? Szedhetik-e várandósok? Szedhetik-e szoptató anyukák? Mikor
Az oszteoporosis nem gyógyszeres terápiája. Dr. Brigovácz Éva SMKMOK 2015.01.21.
 Az oszteoporosis nem gyógyszeres terápiája Dr. Brigovácz Éva SMKMOK 2015.01.21. Az orvoslás s a bizonytalanságok tudománya és s a valósz színűségek művészete. szete. William Osler Tények/ adatok Gyógyszeres
Az oszteoporosis nem gyógyszeres terápiája Dr. Brigovácz Éva SMKMOK 2015.01.21. Az orvoslás s a bizonytalanságok tudománya és s a valósz színűségek művészete. szete. William Osler Tények/ adatok Gyógyszeres
Az Ames teszt (Salmonella/S9) a nemzetközi hatóságok által a kémiai anyagok minősítéséhez előírt vizsgálat, amellyel az esetleges genotoxikus hatás
 Az Ames teszt (Salmonella/S9) a nemzetközi hatóságok által a kémiai anyagok minősítéséhez előírt vizsgálat, amellyel az esetleges genotoxikus hatás kockázatát mérik fel. Annak érdekében, hogy az anyavegyületével
Az Ames teszt (Salmonella/S9) a nemzetközi hatóságok által a kémiai anyagok minősítéséhez előírt vizsgálat, amellyel az esetleges genotoxikus hatás kockázatát mérik fel. Annak érdekében, hogy az anyavegyületével
Magisztrális gyógyszerkészítés a Wilson kór terápiájában. Dr. Birinyi Péter Mikszáth Gyógyszertár 1088 Budapest, Mikszáth Kálmán tér 4.
 Magisztrális gyógyszerkészítés a Wilson kór terápiájában Dr. Birinyi Péter Mikszáth Gyógyszertár 1088 Budapest, Mikszáth Kálmán tér 4. A Wilson kór mérföldkövei 1912. Wilson: Progressive lenticular degeneration:
Magisztrális gyógyszerkészítés a Wilson kór terápiájában Dr. Birinyi Péter Mikszáth Gyógyszertár 1088 Budapest, Mikszáth Kálmán tér 4. A Wilson kór mérföldkövei 1912. Wilson: Progressive lenticular degeneration:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Mixtard 30 40 nemzetközi egység/ml szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 injekciós üveg 10 ml-t tartalmaz, ami 400 NE-gel egyenértékű.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Mixtard 30 40 nemzetközi egység/ml szuszpenziós injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 injekciós üveg 10 ml-t tartalmaz, ami 400 NE-gel egyenértékű.
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! B BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Jumex 5 mg tabletta
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! B BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Jumex 5 mg tabletta
Gyorsítható-e a véralkoholszint csökkentése? Egy klinikai vizsgálat eredményei
 EREDETI KÖZLEMÉNYEK Gyorsítható-e a véralkoholszint csökkentése? Egy klinikai vizsgálat eredményei MÁTYUS MÁRIA DR.¹ HORVÁTH ISTVÁN DR.² FEHÉR JÁNOS DR.³ FARKAS RÓBERT¹ WOLF VERONIKA¹ GALÁNTAI RITA DR.¹
EREDETI KÖZLEMÉNYEK Gyorsítható-e a véralkoholszint csökkentése? Egy klinikai vizsgálat eredményei MÁTYUS MÁRIA DR.¹ HORVÁTH ISTVÁN DR.² FEHÉR JÁNOS DR.³ FARKAS RÓBERT¹ WOLF VERONIKA¹ GALÁNTAI RITA DR.¹
II. melléklet. Az EMA által beterjesztett tudományos következtetések és az alkalmazási előírás és a betegtájékoztató módosításának indoklása
 II. melléklet Az EMA által beterjesztett tudományos következtetések és az alkalmazási előírás és a betegtájékoztató módosításának indoklása 41 Tudományos következtetések A szisztémásan alkalmazandó, nimeszulidot
II. melléklet Az EMA által beterjesztett tudományos következtetések és az alkalmazási előírás és a betegtájékoztató módosításának indoklása 41 Tudományos következtetések A szisztémásan alkalmazandó, nimeszulidot
A klinikai vizsgálatokról. Dr Kriván Gergely
 A klinikai vizsgálatokról Dr Kriván Gergely Mi a klinikai vizsgálat? Olyan emberen végzett orvostudományi kutatás, amely egy vagy több vizsgálati készítmény klinikai, farmakológiai, illetőleg más farmakodinámiás
A klinikai vizsgálatokról Dr Kriván Gergely Mi a klinikai vizsgálat? Olyan emberen végzett orvostudományi kutatás, amely egy vagy több vizsgálati készítmény klinikai, farmakológiai, illetőleg más farmakodinámiás
Szkizofrénia. Bitter István Semmelweis Egyetem Pszichiátriai és Pszichoterápiás Klinika
 Szkizofrénia Bitter István Semmelweis Egyetem Pszichiátriai és Pszichoterápiás Klinika 2014.10.02.. Translációs kutatás Cognitive Neuroscience and Schizophrenia: Translational Research in Need of a Translator
Szkizofrénia Bitter István Semmelweis Egyetem Pszichiátriai és Pszichoterápiás Klinika 2014.10.02.. Translációs kutatás Cognitive Neuroscience and Schizophrenia: Translational Research in Need of a Translator
1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil.
 1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil. Magyarországon egyedi gyógyszerrendelés alapján két éve adható (MODASOMIL,
1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil. Magyarországon egyedi gyógyszerrendelés alapján két éve adható (MODASOMIL,
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 1 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
IV. melléklet Tudományos következtetések 1 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
Gyógyszerbiztonság a klinikai farmakológus szemszögéből
 Gyógyszerbiztonság a klinikai farmakológus szemszögéből Prof. dr. Kovács Péter Debreceni Egyetem Klinikai Központ, Belgyógyászati Intézet, Klinikai Farmakológiai Részleg BIZONYÍTÉKON ALAPULÓ ORVOSLÁS (EBM=
Gyógyszerbiztonság a klinikai farmakológus szemszögéből Prof. dr. Kovács Péter Debreceni Egyetem Klinikai Központ, Belgyógyászati Intézet, Klinikai Farmakológiai Részleg BIZONYÍTÉKON ALAPULÓ ORVOSLÁS (EBM=
A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat.
 A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat. A rotavírus az egyik leggyakoribb okozója a súlyos hasmenésnek csecsemő és kisdedkorban. Évente világszerte
A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat. A rotavírus az egyik leggyakoribb okozója a súlyos hasmenésnek csecsemő és kisdedkorban. Évente világszerte
FELNŐTT ANESZTEZIOLÓGIAI ÉS INTENZÍV SZAKÁPOLÓ SZAK ÓRAREND Helye: Centrumelnöki Hivatal Földszint Nagytanácsterem 2013. március 19.
 2013. március 18. Ápolás lélektani ismeretek az intenzív betegellátásban Ápolás lélektani ismeretek az intenzív betegellátásban Ea:Gál Lászlóné Az intenzív szakápolók mentálhigiénéje Ea:Gál Lászlóné Folyadék
2013. március 18. Ápolás lélektani ismeretek az intenzív betegellátásban Ápolás lélektani ismeretek az intenzív betegellátásban Ea:Gál Lászlóné Az intenzív szakápolók mentálhigiénéje Ea:Gál Lászlóné Folyadék
Hogyan lesznek új gyógyszereink? Bevezetés a gyógyszerkutatásba
 Hogyan lesznek új gyógyszereink? Bevezetés a gyógyszerkutatásba Keserű György Miklós, PhD, DSc Magyar Tudományos Akadémia Természettudományi Kutatóközpont A gyógyszerkutatás folyamata Megalapozó kutatások
Hogyan lesznek új gyógyszereink? Bevezetés a gyógyszerkutatásba Keserű György Miklós, PhD, DSc Magyar Tudományos Akadémia Természettudományi Kutatóközpont A gyógyszerkutatás folyamata Megalapozó kutatások
A pulzáló és folyamatos norfloxacin itatás összehasonlító vizsgálata csirkében és pulykában. Sárközy Géza
 A pulzáló és folyamatos norfloxacin itatás összehasonlító vizsgálata csirkében és pulykában Sárközy Géza Gyógyszertani és Méregtani tanszék Állatorvos-tudományi fakultás Szent István Egyetem Budapest 2002
A pulzáló és folyamatos norfloxacin itatás összehasonlító vizsgálata csirkében és pulykában Sárközy Géza Gyógyszertani és Méregtani tanszék Állatorvos-tudományi fakultás Szent István Egyetem Budapest 2002
Adhezív tabletta szájszárazság esetén
 ORAHEA LTH 13434 SE 27 th Pl Bellevue WA 98005 425-451-9876 Adhezív tabletta szájszárazság esetén Az OraHealth-ről Székhely: Bellevue, Washington Világelső a korszakalkotó orális adhezív tabletta technológiában
ORAHEA LTH 13434 SE 27 th Pl Bellevue WA 98005 425-451-9876 Adhezív tabletta szájszárazság esetén Az OraHealth-ről Székhely: Bellevue, Washington Világelső a korszakalkotó orális adhezív tabletta technológiában
A gyógyszer-metabolizáló enzimek fenokonverziója, avagy a személyre szabott terápia nehézségei
 A gyógyszer-metabolizáló enzimek fenokonverziója, avagy a személyre szabott terápia nehézségei Monostory Katalin MTA Természettudományi Kutatóközpont Személyre szabott gyógyítás one treatment, one size
A gyógyszer-metabolizáló enzimek fenokonverziója, avagy a személyre szabott terápia nehézségei Monostory Katalin MTA Természettudományi Kutatóközpont Személyre szabott gyógyítás one treatment, one size
Betegtájékoztató: Információk a felhasználó számára
 Betegtájékoztató: Információk a felhasználó számára PARAMAX Junior 250 mg tabletta PARAMAX Rapid 500 mg tabletta PARAMAX Forte 1 g tabletta paracetamol Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa
Betegtájékoztató: Információk a felhasználó számára PARAMAX Junior 250 mg tabletta PARAMAX Rapid 500 mg tabletta PARAMAX Forte 1 g tabletta paracetamol Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa
Tudományos következtetések
 II. melléklet Tudományos következtetések, a forgalomba hozatali engedélyek visszavonásának illetve a forgalomba hozatali engedélyek feltételeit érintő változásnak az indoklása, valamint a PRAC ajánlásaitól
II. melléklet Tudományos következtetések, a forgalomba hozatali engedélyek visszavonásának illetve a forgalomba hozatali engedélyek feltételeit érintő változásnak az indoklása, valamint a PRAC ajánlásaitól
Szénhidrát-anyagcsere kontroll pajzsmirigy betegségekben
 Szénhidrát-anyagcsere kontroll pajzsmirigy Dr. Putz Zsuzsanna Újdonságok a pajzsmirigy betegségek gyakorlatában 2018. október 6. SEMMELWEIS EGYETEM Általános Orvostudományi Kar Semmelweis Egyetem Pajzsmirigy
Szénhidrát-anyagcsere kontroll pajzsmirigy Dr. Putz Zsuzsanna Újdonságok a pajzsmirigy betegségek gyakorlatában 2018. október 6. SEMMELWEIS EGYETEM Általános Orvostudományi Kar Semmelweis Egyetem Pajzsmirigy
Ez a gyógyszer orvosi vény nélkül kapható. Az optimális hatás érdekében azonban elengedhetetlen e gyógyszer körültekintő alkalmazása.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Coldastop orrcsepp PIL új BETEGTÁJÉKOZTATÓ Coldastop orrcsepp A-vitamin-palmitát
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Coldastop orrcsepp PIL új BETEGTÁJÉKOZTATÓ Coldastop orrcsepp A-vitamin-palmitát
I.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/35
 I.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/35 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Acticam 1,5 mg/ml orális szuszpenzió kutyának 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml Acticam 1,5
I.sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1/35 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE Acticam 1,5 mg/ml orális szuszpenzió kutyának 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 ml Acticam 1,5
Legyünk agresszívek - A betegmenedzselés sarokpontjai etilénglikol-mérgezésben
 Legyünk agresszívek - A betegmenedzselés sarokpontjai etilénglikol-mérgezésben Pap Csaba Zsolt dr., Elek István dr., Bakos Ágnes dr., Ballaginé Szabó Klára dr. Sürgősségi Betegellátó Osztály és Klinikai
Legyünk agresszívek - A betegmenedzselés sarokpontjai etilénglikol-mérgezésben Pap Csaba Zsolt dr., Elek István dr., Bakos Ágnes dr., Ballaginé Szabó Klára dr. Sürgősségi Betegellátó Osztály és Klinikai
Hiperbár oxigénkezelés a toxikológiában. dr. Ágoston Viktor Antal Péterfy Sándor utcai Kórház Toxikológia
 Hiperbár oxigénkezelés a toxikológiában dr. Ágoston Viktor Antal Péterfy Sándor utcai Kórház Toxikológia physiological effects of carbon monoxide could be mitigated considerably by increasing the partial
Hiperbár oxigénkezelés a toxikológiában dr. Ágoston Viktor Antal Péterfy Sándor utcai Kórház Toxikológia physiological effects of carbon monoxide could be mitigated considerably by increasing the partial
Nem-szteroid gyulladáscsökkentők használata a kisállatpraxisban Pre-,és posztoperatív fájdalomcsillapítás
 Nem-szteroid gyulladáscsökkentők használata a kisállatpraxisban Pre-,és posztoperatív fájdalomcsillapítás dr.márton Kinga társállat-egészségügyi szakmai vezető Alpha-Vet Állategészségügyi Kft. Nem-szteroid
Nem-szteroid gyulladáscsökkentők használata a kisállatpraxisban Pre-,és posztoperatív fájdalomcsillapítás dr.márton Kinga társállat-egészségügyi szakmai vezető Alpha-Vet Állategészségügyi Kft. Nem-szteroid
Endokrin betegek perioperatív ellátása Továbbképző tanfolyam
 Endokrin betegek perioperatív ellátása Továbbképző tanfolyam Célcsoport: endokrinológia, aneszteziológia-intenzív terápia, családorvos, belgyógyászat, sebészet, gyermeksebészet, gyermekgyógyászat, idegsebészet,
Endokrin betegek perioperatív ellátása Továbbképző tanfolyam Célcsoport: endokrinológia, aneszteziológia-intenzív terápia, családorvos, belgyógyászat, sebészet, gyermeksebészet, gyermekgyógyászat, idegsebészet,
Ez a gyógyszer orvosi rendelvény nélkül kapható. Mindemellett az optimális hatás érdekében elengedhetetlen e gyógyszer körültekintő bevétele.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Repaglinide Krka 0,5 mg tabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg repaglinid tablettánként. A segédanyagok teljes listáját lásd a 6.1 pontban.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Repaglinide Krka 0,5 mg tabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg repaglinid tablettánként. A segédanyagok teljes listáját lásd a 6.1 pontban.
PAJZSMIRIGY HORMONOK ÉS A TESTSÚLY KONTROLL
 PAJZSMIRIGY HORMONOK ÉS A TESTSÚLY KONTROLL SEMMELWEIS EGYETEM Általános Orvostudományi Kar Semmelweis Egyetem Energia bevitel Mozgás Nyugalmi energiafogyasztás Thermogenesis Spontán motoros aktivitás
PAJZSMIRIGY HORMONOK ÉS A TESTSÚLY KONTROLL SEMMELWEIS EGYETEM Általános Orvostudományi Kar Semmelweis Egyetem Energia bevitel Mozgás Nyugalmi energiafogyasztás Thermogenesis Spontán motoros aktivitás
Alkohol és máj. Lengyel Gabriella. Semmelweis Egyetem, ÁOK, II.Belklinika Budapest. Hepatológia Továbbképzés, Balatonfüred, 2011.
 Alkohol és máj Lengyel Gabriella Semmelweis Egyetem, ÁOK, II.Belklinika Budapest Hepatológia Továbbképzés, Balatonfüred, 2011. március Májcirrhosis és HCC előfordulása a világ összlakosságában Májcirrhosis,
Alkohol és máj Lengyel Gabriella Semmelweis Egyetem, ÁOK, II.Belklinika Budapest Hepatológia Továbbképzés, Balatonfüred, 2011. március Májcirrhosis és HCC előfordulása a világ összlakosságában Májcirrhosis,
III. MELLÉKLET. Az Alkalmazási előírások és Betegtájékoztatók vonatkozó részeiben szükséges módosítások
 III. MELLÉKLET Az Alkalmazási előírások és Betegtájékoztatók vonatkozó részeiben szükséges módosítások Megjegyzés: A későbbiekben szükség lehet arra, hogy adott esetben a Referencia-tagállammal együttműködve,
III. MELLÉKLET Az Alkalmazási előírások és Betegtájékoztatók vonatkozó részeiben szükséges módosítások Megjegyzés: A későbbiekben szükség lehet arra, hogy adott esetben a Referencia-tagállammal együttműködve,
HÁZTARTÁSI VEGYI ANYAGOK
 HÁZTARTÁSI VEGYI ANYAGOK OKOZTA MÉRGEZÉSEK ELİADÓ DR. LEHEL JÓZSEF 2008.04.23. 1 HÁZTARTÁSI VEGYI ANYAGOK MARÓSZERMÉRGEZÉS Savak - lúgok lefolyó/tőzhely/fémtisztító szerek Detergensek Parfümök, kölnivizek
HÁZTARTÁSI VEGYI ANYAGOK OKOZTA MÉRGEZÉSEK ELİADÓ DR. LEHEL JÓZSEF 2008.04.23. 1 HÁZTARTÁSI VEGYI ANYAGOK MARÓSZERMÉRGEZÉS Savak - lúgok lefolyó/tőzhely/fémtisztító szerek Detergensek Parfümök, kölnivizek
A NEMSZTEROID TERÁPIA VÁLASZTÁS KRITÉRIUMAI DR. HITTNER GYÖRGY ORSZÁGOS REUMATOLÓGIAI ÉS FIZIOTERÁPIÁS INTÉZET, BUDAPEST
 A NEMSZTEROID TERÁPIA VÁLASZTÁS KRITÉRIUMAI DR. HITTNER GYÖRGY ORSZÁGOS REUMATOLÓGIAI ÉS FIZIOTERÁPIÁS INTÉZET, BUDAPEST A GYULLADÁSGÁTLÓ- ÉS FÁJDALOMCSILLAPÍTÓ KÉSZÍTMÉNYEK FELFEDEZÉSE 1897 aspirin 1963
A NEMSZTEROID TERÁPIA VÁLASZTÁS KRITÉRIUMAI DR. HITTNER GYÖRGY ORSZÁGOS REUMATOLÓGIAI ÉS FIZIOTERÁPIÁS INTÉZET, BUDAPEST A GYULLADÁSGÁTLÓ- ÉS FÁJDALOMCSILLAPÍTÓ KÉSZÍTMÉNYEK FELFEDEZÉSE 1897 aspirin 1963
Fehér kapszula, felső részén fekete OGT 918, alsó részén fekete 100 jelzéssel.
 1. A GYÓGYSZER MEGNEVEZÉSE Zavesca 100 mg kemény kapszula. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mg miglusztát kapszulánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Kemény
1. A GYÓGYSZER MEGNEVEZÉSE Zavesca 100 mg kemény kapszula. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mg miglusztát kapszulánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Kemény
Anamnézis, fizikális vizsgálat májbetegségekben
 Anamnézis, fizikális vizsgálat májbetegségekben Dr. Vincze Áron egyetemi docens PTE KK I.sz. BelgyógyászaA Klinika Hepatológia szakvizsga- előkészítő tanfolyam, Balatonfüred 2011. március 8-10. Májbetegségek
Anamnézis, fizikális vizsgálat májbetegségekben Dr. Vincze Áron egyetemi docens PTE KK I.sz. BelgyógyászaA Klinika Hepatológia szakvizsga- előkészítő tanfolyam, Balatonfüred 2011. március 8-10. Májbetegségek
Beutalást igénylô állapotok. A beutalás az emlôbetegséggel foglalkozó sebészhez történjen. Minden új, körülírt csomó.
 Az emlôpanaszos nôk beutalásának irányelve (Guidelines for the referral of patients with breast problems) NHS Breast Screening Programme & The Cancer Research Campaign Elôszó Az emlôrák a nôket érintô
Az emlôpanaszos nôk beutalásának irányelve (Guidelines for the referral of patients with breast problems) NHS Breast Screening Programme & The Cancer Research Campaign Elôszó Az emlôrák a nôket érintô
III. melléklet. Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteinek módosításai. Megjegyzés:
 III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteinek módosításai Megjegyzés: Az alkalmazási előírás, a címke és a betegtájékoztató a referál eljárás eredménye. Lehetséges,
III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteinek módosításai Megjegyzés: Az alkalmazási előírás, a címke és a betegtájékoztató a referál eljárás eredménye. Lehetséges,
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót!
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmesen az alábbi
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Mielőtt elkezdené gyógyszerét alkalmazni, olvassa el figyelmesen az alábbi
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Terbigen 250 mg-os tabletta terbinafin
 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Terbigen 250 mg-os tabletta terbinafin Mielott elkezdené gyógyszerét szedni, olvassa el figyelmesen az alábbi betegtájékoztatót. Tartsa meg a betegtájékoztatót,
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Terbigen 250 mg-os tabletta terbinafin Mielott elkezdené gyógyszerét szedni, olvassa el figyelmesen az alábbi betegtájékoztatót. Tartsa meg a betegtájékoztatót,
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS A BETEGTÁJÉKOZTATÓ VONATKOZÓ PONTJAI
 III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS A BETEGTÁJÉKOZTATÓ VONATKOZÓ PONTJAI Megjegyzés: Ezek az alkalmazási előírásnak és a betegtájékoztatónak a bizottsági határozat idején érvényes módosításai. A bizottsági
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS A BETEGTÁJÉKOZTATÓ VONATKOZÓ PONTJAI Megjegyzés: Ezek az alkalmazási előírásnak és a betegtájékoztatónak a bizottsági határozat idején érvényes módosításai. A bizottsági
és biztonságoss Prof. Dr. János J CHMP member Hungary
 Gyógyszerek hatásoss sossága és biztonságoss gosságaga Prof. Dr. János J Borvendég CHMP member Hungary A ma gyógyszerkutat gyszerkutatásának legfontosabb célbetegségei: gei: malignus betegségek gek cardiovascularis
Gyógyszerek hatásoss sossága és biztonságoss gosságaga Prof. Dr. János J Borvendég CHMP member Hungary A ma gyógyszerkutat gyszerkutatásának legfontosabb célbetegségei: gei: malignus betegségek gek cardiovascularis
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL
 MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA
 I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE FORTEKOR PLUS 1,25 mg/2,5 mg tabletta kutyáknak FORTEKOR PLUS 5 mg/10 mg tabletta kutyáknak 2. MINŐSÉGI
I. sz. MELLÉKLET A KÉSZÍTMÉNY JELLEMZŐINEK ÖSSZEFOGLALÓJA 1 1. AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNY NEVE FORTEKOR PLUS 1,25 mg/2,5 mg tabletta kutyáknak FORTEKOR PLUS 5 mg/10 mg tabletta kutyáknak 2. MINŐSÉGI
Új terápiás lehetőségek (receptorok) a kardiológiában
 Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
KETTŐS EREJÉVEL GYULLADÁSCSÖKKENTO JÓL TOLERÁLHATÓ ORRDUGULÁS ORRFOLYÁS IBUPROFÉN ÉS PSZEUDOEFEDRIN A MEGFÁZÁS TÜNETEI ELLEN FEJFÁJÁS TOROKGYULLADÁS
 IBUPROFÉN ÉS PSZEUDOEFEDRIN KETTŐS EREJÉVEL A MEGFÁZÁS TÜNETEI ELLEN GYULLADÁSCSÖKKENTO JÓL TOLERÁLHATÓ FEJFÁJÁS ORRFOLYÁS IZOMFÁJDALMAK Vény nélkül kapható gyógyszerkészítmény. LÁZ ORRDUGULÁS TOROKGYULLADÁS
IBUPROFÉN ÉS PSZEUDOEFEDRIN KETTŐS EREJÉVEL A MEGFÁZÁS TÜNETEI ELLEN GYULLADÁSCSÖKKENTO JÓL TOLERÁLHATÓ FEJFÁJÁS ORRFOLYÁS IZOMFÁJDALMAK Vény nélkül kapható gyógyszerkészítmény. LÁZ ORRDUGULÁS TOROKGYULLADÁS
Májátültetés és veleszületett anyagcsere betegségek. Dezsőfi Antal
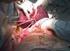 Májátültetés és veleszületett anyagcsere betegségek Dezsőfi Antal Öröklődő anyagcsere betegségek Az öröklődő anyagcsere betegségek döntő többsége a ritka betegségek közé tartozik. Ritka betegség, prevalencia
Májátültetés és veleszületett anyagcsere betegségek Dezsőfi Antal Öröklődő anyagcsere betegségek Az öröklődő anyagcsere betegségek döntő többsége a ritka betegségek közé tartozik. Ritka betegség, prevalencia
A TELJES SZÍV- ÉS ÉRRENDSZERI RIZIKÓ ÉS CSÖKKENTÉSÉNEK LEHETŐSÉGEI
 A TELJES SZÍV- ÉS ÉRRENDSZERI RIZIKÓ ÉS CSÖKKENTÉSÉNEK LEHETŐSÉGEI Dr. Páll Dénes egyetemi docens Debreceni Egyetem OEC Belgyógyászati Intézet A HYPERTONIA SZÖVŐDMÉNYEI Stroke (agykárosodás) Szívizom infarktus
A TELJES SZÍV- ÉS ÉRRENDSZERI RIZIKÓ ÉS CSÖKKENTÉSÉNEK LEHETŐSÉGEI Dr. Páll Dénes egyetemi docens Debreceni Egyetem OEC Belgyógyászati Intézet A HYPERTONIA SZÖVŐDMÉNYEI Stroke (agykárosodás) Szívizom infarktus
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ. Ápoló szakképesítés Szakápolás modul. 1. vizsgafeladat szeptember 7.
 Emberi Erőforrások Minisztériuma Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. elnökhelyettes JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
Emberi Erőforrások Minisztériuma Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. elnökhelyettes JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
Az állapot súlyosságától függően prekóma vagy kóma esetében 24 óra alatt az adag 8 ampulláig emelhető.
 1. A GYÓGYSZER NEVE Hepa-Merz 0,5 g/ml koncentrátum oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 db 10 ml-es ampulla 5 g L-ornitin-L-aszpartátot tartalmaz. A segédanyagok teljes listáját
1. A GYÓGYSZER NEVE Hepa-Merz 0,5 g/ml koncentrátum oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 db 10 ml-es ampulla 5 g L-ornitin-L-aszpartátot tartalmaz. A segédanyagok teljes listáját
Biobiztonság 6. Dr. Szatmári István
 Biobiztonság 6. Dr. Szatmári István Pharmacokinetics and Metabolism Study of the fate of the drugs Absorption, Distribution, Metabolism and Excretion ABSORPTION: reaching the circulation after oral, transdermal,
Biobiztonság 6. Dr. Szatmári István Pharmacokinetics and Metabolism Study of the fate of the drugs Absorption, Distribution, Metabolism and Excretion ABSORPTION: reaching the circulation after oral, transdermal,
Mit nyerünk a gyógyulással? Dr.Werling Klára VIMOR Elnöke Semmelweis Egyetem II. sz Belgyógyászati Klinika
 Mit nyerünk a gyógyulással? Dr.Werling Klára VIMOR Elnöke Semmelweis Egyetem II. sz Belgyógyászati Klinika 1. Meggyógyítunk egy fertőző betegséget HBV prevalencia 2006 Hepatitis B vírus terjedése - szexuális
Mit nyerünk a gyógyulással? Dr.Werling Klára VIMOR Elnöke Semmelweis Egyetem II. sz Belgyógyászati Klinika 1. Meggyógyítunk egy fertőző betegséget HBV prevalencia 2006 Hepatitis B vírus terjedése - szexuális
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Resolor 1 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 mg prukaloprid filmtablettánként (szukcinát formájában). Ismert hatású segédanyagok:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Resolor 1 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 1 mg prukaloprid filmtablettánként (szukcinát formájában). Ismert hatású segédanyagok:
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Aktív életerő HU/KAR/0218/0001
 Aktív életerő HU/KAR/0218/0001 A bizonyítottan javítja az idősödő kutyák életminőségét: élénkebbé teszi az állatokat és ezáltal aktívabb életmódot tesz lehetővé számukra. Az oxigenizáció mellett a szív-
Aktív életerő HU/KAR/0218/0001 A bizonyítottan javítja az idősödő kutyák életminőségét: élénkebbé teszi az állatokat és ezáltal aktívabb életmódot tesz lehetővé számukra. Az oxigenizáció mellett a szív-
Tudásmenedzsment és gyógyszerinnováció
 Tudásmenedzsment és gyógyszerinnováció Ipari szükségletek / elvárások Dr. Bátori Sándor Sanofi-aventis Innovatív Gyógyszerek Kutatása, MAGYOSZ, 2009.01.07. Alapvető együttm ttműködések Hosszútávú elhatározás:
Tudásmenedzsment és gyógyszerinnováció Ipari szükségletek / elvárások Dr. Bátori Sándor Sanofi-aventis Innovatív Gyógyszerek Kutatása, MAGYOSZ, 2009.01.07. Alapvető együttm ttműködések Hosszútávú elhatározás:
B. BETEGTÁJÉKOZTATÓ 1
 B. BETEGTÁJÉKOZTATÓ 1 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Busilvex 6 mg/ml koncentrátum oldatos infúzió készítéséhez buszulfán Mielőtt elkezdené gyógyszert alkalmazni, olvassa el figyelmesen
B. BETEGTÁJÉKOZTATÓ 1 BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA Busilvex 6 mg/ml koncentrátum oldatos infúzió készítéséhez buszulfán Mielőtt elkezdené gyógyszert alkalmazni, olvassa el figyelmesen
- MARSMájelégtelenség kezelésére szolgáló eljárás. Általános leírás, és alkalmazás. A MARS monitor az egyszerhasználatos szerelékkel
 Haemobil Egészségügyi Szolgáltató Közhasznú Nonprofit Korlátolt Felelősségű Társaság 1025. Budapest Vend u. 20 1255. PF: 45. Tel: 224-00-44 Fax: 213-77-48 Akut dialízis és plazmaferezis: 30/ 400 92 00
Haemobil Egészségügyi Szolgáltató Közhasznú Nonprofit Korlátolt Felelősségű Társaság 1025. Budapest Vend u. 20 1255. PF: 45. Tel: 224-00-44 Fax: 213-77-48 Akut dialízis és plazmaferezis: 30/ 400 92 00
A KOCZÁZAT-KEZELÉSI TERV ÖSSZEFOGLALÁSA
 NIMEZULID SZISZTÉMÁS ALKALMAZÁSRA (100 mg-os TABLETTA és GRANULÁTUM, 200 mg-os KÚP) (Magyarországon törzskönyvezve: Xilox 50 mg/g granulátum belsőleges szuszpenzióhoz) A KOCZÁZAT-KEZELÉSI TERV ÖSSZEFOGLALÁSA
NIMEZULID SZISZTÉMÁS ALKALMAZÁSRA (100 mg-os TABLETTA és GRANULÁTUM, 200 mg-os KÚP) (Magyarországon törzskönyvezve: Xilox 50 mg/g granulátum belsőleges szuszpenzióhoz) A KOCZÁZAT-KEZELÉSI TERV ÖSSZEFOGLALÁSA
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ. Ápoló szakképesítés Szakápolás modul. 1. vizsgafeladat június 14.
 Emberi Erőforrások Minisztériuma Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Dr. Páva Hanna A minősítő beosztása: főigazgató-helyettes JAVÍTÁSI-ÉRTÉKELÉSI
Emberi Erőforrások Minisztériuma Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Dr. Páva Hanna A minősítő beosztása: főigazgató-helyettes JAVÍTÁSI-ÉRTÉKELÉSI
