Endoplazmás retikulum stressz skorbutban
|
|
|
- Jakab Szekeres
- 8 évvel ezelőtt
- Látták:
Átírás
1 Endoplazmás retikulum stressz skorbutban Doktori értekezés Dr. Margittai Éva Semmelweis Egyetem Doktori Iskola Molekuláris Orvostudományok Tudományági Doktori Iskola Témavezető: Készítés helye: Dr. Csala Miklós egyetemi adjunktus, PhD Semmelweis Egyetem, Orvosi Vegytani, Molekuláris Biológiai és Pathobiokémiai Intézet Szigorlati bizottság elnöke: Szigorlati bizottság tagjai: Dr. Machovich Raymund egyetemi tanár, az MTA doktora Dr. Monostory Katalin tudományos főmunkatárs, Ph.D. Dr. Gróf Pál egyetemi docens, a biológiai tudomány kandidátusa Budapest 2006
2 Tartalomjegyzék 1. Bevezető A C-vitamin szerepe az állati szervezetben Történelmi áttekintés C-vitamin és oxidatív stressz A C-vitamin mint antioxidáns Más antioxidáns rendszerek Az aszkorbinsav mint kofaktor Aszkorbátfüggő monooxigenázok Aszkorbátfüggő dioxigenázok A C-vitamin napi igénye és szerepe egyes betegségekben Antioxidánsok szerepe az endoplazmás retikulumban Az aszkorbát oxidáz aktivitása a mikroszómában A fehérjék tiolcsoportjainak oxidációja aszkorbát hatására Az E-vitamin szerepe a fehérje tiolok aszkorbát által kiváltott 21 oxidációjában A citokróm b561, egy alternatív transzmembrán elektronszállító molekula Az antioxidánsok oxidatív foldingban betöltött szerepének összegzése Diszulfid kötések keletkezése A diszulfid hidak kialakulása prokariótákban A diszulfid hidak kialakulása eukariótákban A protein diszulfid izomeráz Az Ero1 fehérje A FAD szerepe A glutation szerepe Egy alternatív szereplő, az Erv A diszulfid híd kialakításához kapcsolt elektrontranszfer összegzése Unfolded protein response (UPR) és ER-függő apoptózis Az UPR fogalma és kiváltó okai 31 1
3 Az UPR mechanizmusa Az ER stressz által indukált apoptózis Hipotézis és célkitűzések Módszerek Aszkorbáthiány előidézése tengerimalacokban E-vitaminhiány előidézése patkányokon Sejtfrakciók preparálása májszövetből Sima és durva felszínű endoplazmás retikulum frakciók elválasztása A májak aszkorbáttartalmának mérése E-vitamin mennyiségi meghatározása Lipidperoxidáció vizsgálata Western blot analízis Egyes fehérjék tiol/diszulfid redox állapotának vizsgálata (redox Western 42 blot) Apoptózis vizsgálata májban Statisztikai módszerek Eredmények Aszkorbát, illetve E-vitamin megvonásának hatása az állatokra A lipidperoxidáció változása a diéta során Az állatok súlygyarapodása Endoplazmás retikulum chaperonok és foldázok indukciója Endoplazmás retikulum foldázok redox állapotának vizsgálata Apoptózis indukciója a májban Citokróm b561 jelenléte az endoplazmás retikulumban Megbeszélés Összefoglalás Summary 60 Köszönetnyilvánítás 61 Saját közlemények jegyzéke 62 Irodalomjegyzék 63 2
4 Rövidítésjegyzék AMS 4-acetamide-4 -maleimidylstilbene-2,2 -disulfonic acid ANOVA analysis of variance ASK1 apoptosis signal-regulating kinase 1 ATF activating transcription factor BiP binding protein BH3 Bcl2-homology CGcytb kromaffin granulumra jellemző citokróm b561 CHOP CCAAT-box enhancer binding protein-homologous protein CRE camp response element Dcytb duodenális citokróm b561 DER durva felszínű endoplazmás retikulum Dsb disulfide bond DTT ditiotreitol EDTA ethylene diamine tetraacetic acid EGF epidermal growth factor eif2 eukarióta iniciációs faktor 2 ER endoplazmás retikulum ERAD endoplazmás retikulum asszociált degradáció Ero1 endoplazmás retikulum oxidáz, ERP72 endoplazmás retikulum protein 72 Erv2 essential for respiration and vegetative growth FIH-1 factor inhibiting HIF-1 GADD growth arrest and DNA damage-inducible protein GLO gulonolakton oxidáz GRP glucose-regulated protein HEPES 4-(2-hydroxyethyl) piperazine-1-ethanesulfonic acid HIF-1 hipoxia által indukált faktor 1 HPLC high pressure liquid chromatography 3
5 IMP inner membrane potential IRE1 inositol requiring 1 Lcytb lizoszómális citokróm b561 MOPS 3-(N-morpholino) propanesulfonic acid PAGE poliakrilamid gélelektroforézis PAL peptidil-α-hidroxi-glicin α-amidáló liáz PDI protein-diszulfid izomeráz PERK RNA-dependent protein kinase-like ER-kinase PHM peptidil-glicin α-hidroxiláló monooxigenáz PUFA polyunsaturated fatty acid (többszörösen telítetlen zsírsav) PVDF polyvinylidene fluoride ROS reactive oxygene species SDS sodium dodecyl sulfate SEM standard error of mean SER sima felszínű endoplazmás retikulum S1P site-1 protease S2P site-2 protease UGGT UDP-glukóz glikoprotein glukoziltranszferáz uorfs upstream open reading frames UPR unfolded protein response UV-VIS ultra violet-visiable TBARS tiobarbiturate reactive substance TRAF2 tumor necrosis factor receptor-associated factor 2 TUNEL terminális dezoxinukleotidil transzferáz dutp nick-end labeling XBP cis-acting X-box binding protein 4
6 1. Bevezető 1.1. A C-vitamin szerepe az állati szervezetben Történelmi áttekintés Már régtől fogva ismert, hogy friss növények fogyasztása elengedhetetlen az egészség megőrzése szempontjából. Amikor az ember raktározott, konzerv élelmiszereket volt kénytelen fogyasztani, a skorbut felbukkanása mindig veszélyeztette az egészségét. Ez elsősorban a hosszú felfedező hajóutak idején volt jellemző, és gyakran fatális következményekkel járt a hajók személyzete körében, akik sokszor hónapokon keresztül nem jutottak friss élelmiszerhez. Elsőként Krámer János György magyar katonaorvos jött rá a friss élelmiszerek fogyasztásának fontosságára. Ő a török hadjáratok idején savanyúkáposztát osztatott a hadseregnek, amivel sikerült megelőznie a csapatok körében egyébként járványszerűen pusztító skorbutot (Kramer 1739). James Lindt, egy skót hajósebész végzett először kontrollált kísérleteket a skorbut gyógykezelésével kapcsolatban, és igazolta a citrusfélék fontosságát a skorbut megelőzésében, majd 1753-ban publikálta megfigyeléseit A Treatise of the Scurvy címmel megjelent könyvében (Lind 1753). Az ezekben a növényekben fellelhető rejtélyes hatóanyagot azonban csak jóval később, 1932-ben azonosították, amikor Svirbely és Szent-Györgyi, valamint ezzel párhuzamosan King és Waugh egy hexuronsavat izolált növényi és állati szervezetből, melynek ráismertek skorbutellenes hatásaira, ezért aszkorbinsavnak, illetve C-vitaminnak nevezték el. A C-vitamin molekuláris szerkezetének és bioszintézisének kutatásában Sir Walter Norman Haworth járt az élen, aki munkájáért 1937-ben kémiai Nobel-díjat kapott (King 1953). A C-vitamin hatásmechanizmusa, metabolizmusa és transzportja élő szervezetekben már a kezdetektől nagyfokú érdeklődésre tartott számot és máig intenzív kutatás tárgya. A hosszú évek munkája rengeteg eredményt szült e tárgyban, de számos kérdés ma is megoldásra vár, amelyhez további vizsgálatokra van szükség. 5
7 C-vitamin és oxidatív stressz A C-vitamin mint antioxidáns A C-vitamin (L-aszkorbát) összes eddig ismert fiziológiás és biokémiai funkcióját redukáló képességének köszönheti. A kettes és hármas szénatomot tartalmazó dienol struktúra hidroxil csoportjai savas disszociációra képesek, pk értékeik 4,17 és 11,57; ezért fiziológiás ph mellett az aszkorbát monovalens anion formában fordul elő (Rose és Bode 1993). Az aszkorbát monoanion formája könnyedén ad le két elektront két egymást követő reverzibilis lépésben (1. ábra). Az első elektron leadása aszkorbil szabadgyök (szemidehidro-aszkorbát vagy monodehidro-aszkorbát) képződéshez vezet. 1. ábra. Az aszkorbinsav redox-metabolizmusa Az aszkorbil gyök egy erősen delokalizált párosítatlan elektronnal rendelkezik, ezért - a többi szabadgyökkel összevetve - viszonylag stabil (T ½ 10-5 s) és nem reaktív (Padayatty és mtsai 2003). Ezek a tulajdonságok az aszkorbátot hatásos redukáló, vagyis elektrondonor antioxidáns szerré teszik: az aszkorbát ugyanis, miközben a reaktív, és legtöbbször igen 6
8 veszélyes szabadgyököket redukálja, jóval kevésbé veszélyes aszkorbil gyökké alakul (1. egyenlet). Ezt a folyamatot általában gyökfogásnak nevezik. Az aszkorbil gyök ezután diszproporcionálódhat (2. egyenlet), ami általában jóval gyorsabb ( 10 5 M -1 s -1, ha ph = 7,0) (Wells és Xu 1994), ezért gyakoribb, mint az aszkorbil gyök reakciója oxigénnel vagy biológiailag aktív vegyületekkel (3. egyenlet) (Coassin és mtsai 1991). Az aszkorbil gyök tovább-oxidációja, akár diszproporcionálódással, akár egy másik vegyülettel történő reakció során, dehidroaszkorbát képződéséhez vezet, ami hidrolízissel irreverzibilisen bomlik, hacsak alkalmas redukálószer hatására nem alakul vissza aszkorbáttá. AH 2 + R AH + RH AH + AH AH 2 + A AH + R A + RH (1. egyenlet) (2. egyenlet) (3. egyenlet) A redox reakciók és köztük a szabadgyökös reakciók irányát a termodinamika szabályai szerint a résztvevő vegyületek kulcsfontosságú elektrokémiai paramétere, a redox potenciál határozza meg. Buettner (1993) közzétett egy összefoglalást a szabadgyökök standard egyelektronos redox potenciáljáról élő szervezetben. A biológiai rendszerekben előforduló legerősebben oxidáló gyök a hidroxil gyök, HO. A hidroxil gyök egyik lehetséges forrása a jól ismert Fenton reakció, vagyis a H 2 O 2 reduktív hasítása egy fémion (pl. Fe 2+ ) által: Fe 2+ + H 2 O 2 Fe 3+ + HO + HO Az aszkorbát azonban termodinamikailag a sor alján helyezkedik el az oxidáló szabadgyökök között. Az összes olyan szabadgyök, amelynek nagyobb a redox potenciálja, beleértve a hidroxil gyököt, továbbá az alifás alkoxil és peroxil gyököket, aszkorbát segítségével eliminálhatók. Ráadásul a glutation gyök, valamint az urátból és α- tokoferolból keletkező szabadgyökök az aszkorbát segítségével az antioxidáns glutationná, uráttá, illetve α-tokoferollá regenerálhatók. Továbbá ezek az elektron (hidrogén atom) transzfer reakciók igen gyorsan zajlanak le (Buettner és Jurkiewicz 1996), vagyis az aszkorbát mind termodinamikai, mind kinetikai szempontból kiváló antioxidáns. Rose és 7
9 Bode 1993-ban felállított egy kritériumrendszert, mely alapján egy molekulát a fiziológiásan hatékony antioxidánsok közé sorolnak, és megállapítást nyert, hogy az aszkorbát számos olyan tulajdonsággal rendelkezik, mely elengedhetetlen a hatékony gyökfogáshoz az emberi szervezetben. A fent említett körülmények (az aszkorbil gyök viszonylagos stabilitása; az aszkorbil gyök / aszkorbát monoanion redox pár kedvező termodinamikai paraméterei, a releváns reakciók kedvező kinetikája) mellett az aszkorbát kiváló antioxidáns szerepét támasztja alá in vivo: 1) a különböző szövetekben lévő magas aszkorbát koncentráció; 2) számos transzport mechanizmus jelenléte, melyek lehetővé teszik az aszkorbát megfelelő eloszlását a szervezetben; 3) a legtöbb állatban fellelhető de novo aszkorbát szintézis, illetve az aszkorbát előfordulása a növényi eredetű táplálékokban és gyors abszorpciója a bélrendszerből, melyek biztosítják az emlős szervezet számára az aszkorbát könnyű hozzáférését; 4) egy olyan recirkulációs mechanizmus létezése, mely lehetővé teszi az aszkorbát számára, hogy oxidált alakja újból visszaalakuljon az antioxidánsként működő redukált formává; 5) a vese C-vitamint konzerváló szerepe renális reabszorpció révén; 6) a C-vitamin redukált formájának minimális toxicitása. Mióta Rose és Bode kritériumrendszerével alátámasztást nyert a C-vitamin ideális fiziológiás antioxidáns volta, a fent felsorolt mechanizmusok kutatásában is jelentős fejlődés ment végbe, különösen a recirkuláció és a transzport területén. Az aszkorbát toxicitásával kapcsolatban röviden meg kell említeni, hogy bizonyos körülmények között, paradox módon a vitamin prooxidáns hatással is rendelkezik. Ez a kiváló redukáló ágens ugyanis képes bizonyos fémionokat is redukálni, pl. Fe 3+ és Cu 2+ ionokat Fe 2+ és Cu + ionokká, melyek ezután oxidációs láncreakciókat idézhetnek elő (Buettner és Jurkiewicz 1996). Az ilyen katalitikus fémek nagyon alacsony koncentrációja mellett az aszkorbát szinte mindig antioxidánsként működik, azonban ha a hozzáférhető fémionok koncentrációja megemelkedik, az aszkorbát veszélyessé válhat. 8
10 Más antioxidáns rendszerek Az aszkorbát mellett az állati sejt számos enzimatikus és nem-enzimatikus faktorral rendelkezik az oxidatív hatások elleni védekezéshez (Chaudiere és Ferrari-Iliou 1999). Az enzimatikus antioxidánsok (szuperoxid-dizmutáz, kataláz, glutation-peroxidáz) főleg a reaktív oxigén származékok intracelluláris hatástalanításában játszanak fontos szerepet. A nem-enzimatikus antioxidánsok direkt módon reagálhatnak a reaktív molekulákkal mind a sejten belül, mind az extracelluláris térben. A vízoldékony (aszkorbát, glutation, urát) és lipidoldékony (tokoferol, karotin) antioxidánsok egymással redox potenciáljuknak megfelelően elektronátvivő láncot alkotnak (2. ábra), melynek fontos szerepe van a membránok lipidperoxidáció elleni védelmében. A rendszerhez kapcsolódnak más, táplálkozással a szervezetbe kerülő, általában növényi eredetű antioxidánsok is (fenolok, flavonoidok, antocianidok stb.). 2. ábra. Az antioxidánsok redox lánca (Halliwell-Asada ciklus) 9
11 A lipidek (membránlipidek és lipoptoteinek lipid komponensei) hajlamosak a peroxidációra. A folyamat leginkább a többszörösen telítetlen zsírsavakat (PUFA) érinti, mivel a kettős kötések között elhelyezkedő metilén csoportok (-CH 2 -) hidrogénjei különösen reaktívak. A lipidperoxidáció a (-CH 2 -) csoport hidrogénjének egy szabadgyök (általában hidroxil gyök) által történő elvonásával kezdődik (Reiter 1995). A keletkező lipidgyök konjugált diénné történő átrendeződés után molekuláris oxigénnel reagál, peroxil gyököt (ROO ) kialakítva. Ez utóbbi szintén képes hidrogén atomot elvonni egy másik PUFA molekulából, mely láncreakciószerűen a membrán valamennyi PUFA molekulájának oxidációjához vezetne. A lipidperoxidáció veszélyes, mivel megváltoztatja a membrán permeabilitását és befolyásolja a membránfehérjék (receptorok, transzporterek) működését. Az aszkorbát gátolja a lipidperoxidációt egyrészt a prooxidánsok szintjének csökkentése révén, másrészt a tokoferil gyök visszaredukálásával. A tokoferil gyök a lipidperoxidáció láncletörő lépésében keletkezik: a tokoferol képes a lipid-peroxil gyök redukálására (Buettner és Schafer 2000). Az interakció a vízoldékony aszkorbinsav és a hidrofób tokoferol között azért lehetséges, mert az E-vitamin fenolos hidroxil csoportja a membránvíz határfelületen található (Buettner 1993). A C- és E-vitamin ilyen kölcsönhatása különösen fontos az endoplazmás retikulum (ER) membránjában, ahol számos enzim (pl. citokróm P450 izoenzimek) termelhet reaktív intermediereket. A fehérjék szintén oxidatív módosulásokat szenvedhetnek, melyek részben fiziológiásak (bizonyos aminosavak olalláncainak enzimatikus hidroxilációja, diszulfid hidak képződése), részben patológiásak, és krónikus degeneratív betegségek patomechanizmusának elemei lehetnek. Érdekes módon az aszkorbát elősegíti a fehérjék fiziológiás oxidációját (pl. hidroxilázok kofaktoraként, ld. később), ugyanakkor véd a patológiás prooxidáns hatások ellen (antioxidánsként) Az aszkorbinsav mint kofaktor Az aszkorbinsav egyik sajátos funkciója, hogy kofaktorként működhet fémionfüggő oxigenázok által katalizált reakciókban. Az ide tartozó enzimek Cu + tartalmú monoxigenázok ( ), illetve Fe 2+ - és α-ketoglutarát-függő dioxigenázok ( ). Az 10
12 enzimek prosztetikus fémionját kell redukált formában tartani, ami kísérletes rendszerekben egyéb antioxidánsokkal is megoldható, de általában az aszkorbát a leghatékonyabb, és fiziológiás körülmények között a feladat rá hárul. Jól mutatja e szerep fontosságát, hogy a skorbutban észlelhető tünetek nagy része összefüggésbe hozható az ilyen aszkorbátfüggő enzimek funkciójának kiesésével Aszkorbátfüggő monooxigenázok Azok a monooxigenázok, melyek aszkorbát jelenlétét igénylik, az aminosav eredetű és peptidhormonok szintézisében vesznek részt. Nevüknek megfelelően a molekuláris oxigénből egy atomot építenek be a szubsztrátba. a) Peptidil-glicin α-amidáló monooxigenáz A bioaktív peptidek több mint felének eredetileg szabad karboxil csoportot tartalmazó vége amiddá módosul, ami biológiai aktivitásukhoz is szükséges. A gerincesek α-amidált peptidjei között hormonok (oxitocin, vazopresszin, gasztrin, kalcitonin) és neurotranszmitterek (substance P, neuropeptid Y) egyaránt előfordulnak. A prekurzor peptidek C-terminálisán található glicin amino-nitrogénje és α-szénatomja közötti kötés oxidatívan hasad. Mindezt egy peptidilglicin α-amidáló monooxigenáznak nevezett bifunkcionális enzim katalizálja, mely peptidil-glicin α-hidroxiláló monooxigenáz (PHM) és peptidil-α-hidroxi-glicin α-amidáló liáz (PAL) aktivitásokkal bír (Prigge és mtsai 2000). A PHM aktivitásban van szerepe a réztartalmú enzim aszkorbátfüggésének. Az enzim alapállapotban két oxidált Cu 2+ iont tartalmaz, melyeket két aszkorbát molekula redukál. Az aktív enzim Cu + ionjai aktiválják a molekuláris oxigént a hidroxilációhoz. A katalítikus ciklus végén a rézionok ismét oxidált állapotban vannak, és újabb aszkorbát molekulákra van szükség az aktiválódáshoz. Egy mól amidált termék kialakulásához tehát egy mól aszkorbát használódik fel (Murthy és mtsai 1987). Az aszkorbát a leghatékonyabb reduktáns mind in vitro (Eipper és mtsai 1983), mind sejtkultúrában (May és mtsai 1989). Ezzel függ össze a bioaktív amidált peptideket szintetizáló szövetek (mellékvese, agyalapi mirigy) jellegzetesen magas aszkorbáttartalma (Englard és Seifter 1986). 11
13 b) Dopamin β-hidroxiláz A dopamin β-hidroxiláz a tirozin-noradrenalin átalakulás utolsó lépését katalizáló réztartalmú monooxigenáz. Az enzim jelen van a központi idegrendszer katekolamintároló vezikuláiban és a mellékvesevelő kromaffin sejtjeiben, melyek magas aszkorbáttartalmukról ismertek (Englard és Seifter 1986). Ebben az esetben is az aszkorbát bizonyult az enzim leghatékonyabb reduktánsának (Levin és mtasi 1960) Aszkorbátfüggő dioxigenázok Az aszkorbát közreműködését igénylő dioxigenázok a kollagén és a karnitin bioszintézisében, valamint a tirozin katabolizmusában vesznek részt. Jellegzetességük, hogy koszubsztrátként α-ketoglutarátot használnak, amely a molekuláris oxigén egyik atomját felvéve, oxidatív dekarboxileződéssel szukcináttá alakul. a) Prolil- és lizil-hidroxilázok A kollagén-bioszintézis zavara skorbutban nyilvánvaló. Az érett kollagén normális hármas hélix szerkezetének kialakulásához elengedhetetlen a prokollagén prolil- és liziloldalláncainak poszttranszlációs módosítása. A hidroxilált prolil csoportok elsősorban a láncok közötti hidrogénkötésekhez kellenek, míg a hidroxi-lizin feltételezett szerepe a további poszttranszlációs módosítások elősegítése. A folyamatban szerepet játszó enzimek közül legalaposabban a prolil-4-hidroxilázt jellemezték (Myllyharju 2003). Az α2β2 tetramer szerkezetű enzim α alegysége tartalmazza a katalítikus helyet, míg a β alegység a protein diszulfid izomerázzal azonos. Az enzim az endoplazmás retikulum lumenében helyezkedik el. Működése során az α-ketoglutarát dekarboxilálásakor egy vas ion oxidálódik, az aszkorbát pedig azáltal stimulálja az enzim működését, hogy ezt a vas iont visszaredukálja. Ezt a következő megfigyelések támasztják alá: 1) a hidroxiláció során az aszkorbát fogyása nem sztöchiometrikus; 2) aszkorbát hiányában a prolil-4-hidroxiláz enzim aktivitásának elvesztése előtt még számos hidroxiláxiót képes katalizálni (Myllyla és mtsai 1978); 3) a reakció szétkapcsolásakor, 12
14 amikor is az α-ketoglutarát dekarboxilációja nem jár következményes prolil hidroxilációval, az aszkorbát a dekarboxilálással sztöchiometrikusan megegyező mennyiségben használódik fel (Myllyla és mtsai 1984). A katalízis során átmenetileg reaktív ferri-oxo komplex képződik, amely a prolil-hidroxilációhoz vezető oxigéntranszfer során keletkező aktív intermedier. Ha a reakció valamilyen okból szétkapcsolódik, és ferrioxo komplex Fe 3+ és O - ionokra bomlik, akkor a prolil-4-hidroxiláz inaktiválódása csak úgy kerülhető el, ha az enzimhez kötött Fe 3+ ion visszaredukálódik Fe 2+ ionná (Kivirikko és Myllyharju 1998). Mivel a reakció gyakran szétkapcsolódik fiziológiás körülmények között is (pl. más hidroxilálódó szubsztrátok jelenléte esetén), a prolil-4-hidroxiláz működése erősen függ egy megfelelő redukálószer jelenlététől, és ezt a protektív szerepet leghatékonyabban az aszkorbát tölti be. A prolil-4-hidroxiláz asszociációja a protein-diszulfid izomerázzal, illetve az a tény, hogy a protein-diszulfid izomeráz képes katalizálni a glutationfüggő dehidroszkorbát-redukciót, arra a következtetésre vezette Meister-t (1994), hogy az aszkorbát és a glutation között valószínűleg kapcsolat áll fenn a prolil-4-hidroxiláz enzim szintjén: a protein-diszulfid izomeráz szerepe az hidroxilációs reakció során keletkező dehidroaszkorbát visszaredukálása, vagyis az aszkorbát regenerálása lehetne. Kimutatták, hogy az aszkorbát képes indukálni a kollagén-bioszintézist. Sejtkultúrákban bizonyítást nyert, hogy aszkorbát adása a médiumhoz stimulálta a prokollagén szekrécióját és transzlációját, valamint a prokollagén mrns transzkripcióját és stabilitását (Schwarz ás mtsai 1987). Ezek a hatások valószínűleg részben az aszkorbát hatására fokozódó kollagénhidroxilációnak tudhatók be. b) Karnitin bioszintézisében szereplő hidroxilázok A karnitin, illetve a belőle képződő az acetil- és más acilkarnitin származékok jelentős szerepet játszanak a zsírsav-metabolizmusban. A karnitinhez való kapcsolódás célja a mitokondriális, illetve bizonyos esetkben a peroxiszómális membránon keresztül történő zsírsavtranszport. A karnitin lizinből keletkezik, melynek korai lépése az ε-ntrimetillizin képződése. A későbbiekben a bioszintézis két hidroxilációs lépést tartalmaz: az ε-n-trimetillizin β-hidroxiláció során β-hidroxi-ε-n-trimetillizinné alakul, a második 13
15 hidroxilációs lépés a γ-n-trimetil-aminobutirát β-hidroxilációja karnitinné. Ezeket a reakciókat két különböző α-ketoglutarát- és Fe 2+ -függő dioxigenáz katalizálja, melyek működését redukálószerek leghatékonyabban az aszkorbát fokozzák (Hulse és mtsai 1978; Lindstedt és Lindstedt 1970). Skorbutos állatmodellekben kimutatták a karnitinhiányt (Rebouche 1991), és feltételezhető, hogy a skorbut korai stádiumában jelentkező fáradékonyságot a karnitinhiány miatt csökkent zsírsavfelhasználás okozza. c) 4-hidroxi-fenilpiruvát dioxigenáz A tirozin-katabolizmus második lépése a 4-hidroxi-fenilpiruvát átalakítása homogentizinsavvá 4-hidroxi-fenilpiruvát dioxigenáz által. Az enzim abban különbözik más aszkorbát- és Fe 2+ függő dioxigenázoktól, hogy nem igényel α-ketoglutarátot, és így az oxigén molekula mindkét atomját ugyanabba a termékbe építi be. Valóban, az enzim által katalizált reakcióban az α-ketosav (piruvát), amely oxidatívan dekarboxilálódik, a hidroxilálódó szubsztrát része (Moran 2005). Az aszkorbát stimulálja ezt a reakciót, de a reduktáns specificitása nem annyira igazolt, mint más aszkorbátfüggő dioxigenázok esetében (Zannoni és La Du 1959). Skorbutos tengerimalacokban tirozin hatására tirozinémia alakul ki és vizeletükben megjelenik a 4-hidroxi-fenilpiruvát és 4-hidroxifenillaktát (Englard és Seifter 1986). d) EGF β-hidroxiláz Egy aszparaginil-β-hidroxilázt tisztítottak marha májból (Gronke és mtsai 1990; Wang és mtsai 1991), mely szintén α-ketoglutarát- és Fe 2+- függő, aszkorbátot is igénylő dioxigenáz. β-hidroxilált aszpartil és aszparaginil csoportokat mutattak ki EGF-like doméneken számos K-vitamin-dependens fehérjében (pl. VII. IX. X. véralvadási faktorok). Az EGF (epidermal growth factor) hidroxiláció fiziológiás szerepe még feltárandó; a jelátvitelben és a sejtmigráció szabályozásában vehet részt (Dinchuk és mtsai 2002; Maeda és mtsai 2003). e) Aszparaginil és prolil hidroxilázok a HIF-1 szabályozásában A hipoxia által indukált faktor 1 (HIF-1) egy két alegységből (α és β) álló transzkripciós faktor, mely az emlős sejtek hipoxiához való alkalmazkodását biztosítja több gén 14
16 expressziójának fokozásával. A HIF-1α mennyisége és aktivitása aszparaginil és prolil oldalláncainak hidroxilációján keresztül szabályozódik a lokális oxigénkoncentrációnak megfelelően. Egy specifikus aszparaginil csoportját a FIH-1 (factor inhibiting HIF-1) oxigenálja, ami egy aszparaginil-β-hidroxiláz, mely különbözik az EGF β-hidroxiláztól (Lando és mtsai 2002). A HIF-1α specifikus prolil csoportjait a citoszólban található prolil- 4-hidroxiláz család tagjai hidroxilálják, melyek különböznek az endoplazmás retikulumban található, a kollagén módosításában résztvevő enzimektől. A két enzimcsalád között nincs homológia, de a katalízisben szerepet játszó fontos csoportok konzerváltak (Myllyharju 2003). Az aszparaginil-hidroxiláció gátolja a HIF-1 kapcsolatát a p300 transzkripciós koaktivátorral, míg a prolil hidroxiláció a transzkripciós faktor proteaszómális lebontásához vezet (Lancaster és mtsai 2004). Hipoxia esetén a HIF-1α nem hidroxilálódik, mert a hidroxilázok csak viszonylag magas oxigéntenzió mellett működnek, így a HIF-1 mennyisége és aktivitása nő. A normoxiás állapot visszaállása után a hidroxilázok inaktiválják a jelpályát. Számos transzformált sejtvonal viszont emelkedett HIF-1 szintet mutat normoxiás körülmények között is. Érdekes, hogy az aszkorbát fiziológiás koncentrációi különösen ezekben a transzformált sejtvonalakban csökkentik a HIF-1 proteinszintet és a HIF-1 transzkripciós targetjeinek szintjét (Knowles és mtsai 2003). Az aszkorbát hatása az EGF és HIF-1α hidroxilázaira azt mutatja, hogy a molekula fontos szerepet játszhat a jelátvitelben és a génexpresszióban. Ezekben a folyamatokban való részvételét gyakran pro- vagy antioxidáns hatásainak tulajdonítják (Duarte és Lunec 2005). Valóban jól ismert a reaktív oxigénszármazékok szerepe a jelátvitelben és a génexpresszióban. Az aszkorbát befolyásolhatja ezeket a jelpályákat a sejt redox viszonyainak megváltoztatása révén. A hidroxilázok kofaktoraként betöltött funkciója viszont azt mutatja, hogy az aszkorbátnak a pro- és antioxidáns hatásokon túlmenően specifikus szerepe is lehet a biológiai szabályozásban A C-vitamin napi igénye és szerepe egyes betegségekben Az aszkorbát a legtöbb állat számára nem vitamin, mivel májsejtjeik képesek az előállítására (Bánhegyi és mtsai 1997). A szintézis UDP-glukózból indul ki; aktivitása a 15
17 glikogenolízis függvénye, így közvetve a glutation redoxstátusza által is szabályozott (Braun és mtsai 1996). Emellett a gulonolakton oxidáz (GLO), a szintézis utolsó lépését katalizáló enzim, génexpresszió szintjén is szabályozódik (Braun és mtsai 1999; Braun és mtsai 1999). Az endoplazmás retikulum membránjához kötött GLO hidrogén-peroxidot is termel, ezért az aszkorbáttermelést glutationoxidáció kíséri (Bánhegyi és mtsai 1996; Puskás és mtsai 1998). Ám a GLO néhány fajban pl. az emberben és a tengerimalacokban is hiányzik, így e szervezeteknek az aszkorbinsav vitamin (C-vitamin), melyet a táplálékkal szükséges felvenniük (Bánhegyi és mtsai 1998). A C-vitaminhiányos táplálkozás az avitaminózis egyik formájához, skorbuthoz vezet, mely egy általános anyagcsere betegség igen széles tünetskálával. Legfontosabb jellemzői a korán jelentkező fáradtság és letargia, amit a fogak kihullása, vérző íny és bőrvérzések követnek. Jellemző továbbá a meglassult sebgyógyulás, csökkent immunvédekező képesség, végtagfájdalmak és enyhe anaemia. A skorbut megelőzéséhez minimális dózisú C-vitamin bevitel elégséges (kb. 10 mg/nap), azonban ha a táplálékkal bejuttatott C-vitamin mennyisége kevesebb, mint mg/nap, a klinikai skorbutot megelőző és azt előrejelző fáradtság már jelentkezhet (Padayatty és mtsai 2003). A C-vitamin emberek számára optimális dózisával kapcsolatban máig folyamatos viták folynak. A jelenleg ajánlott napi C- vitamin-fogyasztás a UK Food Standards Agency által 40 mg/nap, míg a US Food and Nutrition Board mg-ot ajánl naponta. Néhány kutató azonban azzal érvel, hogy ha a skorbut megelőzéséhez szükséges C-vitamin mennyisége ilyen nagyságrendű, akkor az optimális közérzet elérése érdekében a C-vitamin ajánlott adagja 1 vagy több gramm kellene, hogy legyen naponta (Pauling 1970). Erre az eredményre különböző megfontolások vezették őket. Bourne érvelése emberszabású majmokon végzett kísérletein alapult, melyek az emberhez hasonlóan nem képesek C-vitamin szintézisére. Stone a patkányok által naponta termelt C-vitamin mennyisége alapján következtetett az emberek szükséges napi vitamindózisára. Pauling kiindulópontja a C-vitamin optimális dózisának (naponta 2,3 g vagy több) megállapítására az a tény volt, hogy az aszkorbát szintézis képessége csak néhány fajban szűnt meg (ami szerinte azt jelenti, hogy az étkezési növények kevesebb C-vitamint tartalmaznak, mint az optimális egészség megőrzéséhez szükséges napi mennyiség). Itt érdemes megjegyezni, hogy naponta 5db zöldség vagy 16
18 gyümölcs elfogyasztása (amit egy megfelelő étrend egyébként is tartalmaz) kb. 220 mg C- vitamin bevitelt jelent (Lachance és Langseth 1994). Az aszkorbát előnyös volta azonban a különböző betegségekben különösen rákban vita tárgya, amint azt a következő példa is mutatja. Cameron és Pauling (1976) kimutatta, hogy naponta 10 g aszkorbát fogyasztása megnöveli a túlélési időt a végső stádiumban lévő rákos betegeknél. Ezt és ehhez hasonló tanulmányokat azonban számtalanszor erős kritikával illettek a megfelelő kontrollok vagy a randomizáció hiánya miatt. Később Creagan és mtsai (1979) végeztek egy randomizált placebo-kontroll vizsgálatot magas dózisú C-vitaminnal, melyben semmilyen előnyös hatást nem sikerült kimutatni az előrehaladott állapotú rákos betegek túlélésében vagy egyéb paramétereiben. Azonban Padayatty és Levine (2001) lényeges különbségre mutatott rá a két kísérlet között: az elsőben a C-vitamint intravénásan adták, míg a másodikban orálisan, mely valószínűleg sokkal alacsonyabb plazmaszintet eredményezett. Így tehát a két vizsgálatot lehetetlen összehasonlítani, és a C-vitamin esetleges rákellenes hatása továbbra is nyitott kérdés maradt. Összegezve tehát, számos állapot van, mely emelkedett oxidatív stresszel és alacsonyabb C-vitamin szinttel jár mind a vérplazmában, mind a szövetekben (pl. rák, diabetes mellitus, cataracta és dohányzás), továbbá számos tanulmány támasztja alá a C viatmin szerepét az érrendszeri betegségekben, magasvérnyomás betegségben, vasfelszívódásban és a gyomorrák megelőzésében. Azonban míg in vitro számos bizonyíték van a C-vitamin hatékony antioxidáns működésére, az emberekben betöltött antioxidáns szerepe még nem nyert közvetlen alátámasztást epidemiológiai tanulmányokkal vagy olyan klinikai tanulmányokkal, melyek az oxidatív károsodás biomarkereit mérik. Nem bizonyított, hogy a zöldségekben és gyümölcsökben lévő C-vitamin védő hatást fejtene ki a kardiovaszkuláris betegségekben és a rákban. Napjainkig a C-vitamin egyetlen előnyös hatásaként a skorbut megelőzését tartják számon Antioxidánsok szerepe az endoplazmás retikulumban Emlőssejtekben számos fehérje (köztük a Golgi-apparátusba, a lizoszómába, a plazmamemránba, illetve a szekrécióra szánt fehérjék) a durva felszínű endoplazmás 17
19 retikulum riboszómáin szintetizálódik. Ezek a polipeptidláncok az endoplazmás retikulum lumenébe kerülnek, ahol harmadlagos szerkezetük kialakul, valamint átesnek az egyik legfontosabb ko/poszttranszlációs módosuláson, a diszulfidhíd képződésén (Tu és Weissman 2004). A fehérjék tiolcsoportjainak diszulfiddá alakításához, vagyis a citoplazmáénál jóval magasabb tiol-redoxpotenciál kialakításához oxidáló környezetre van szükség (Hwang és mtsai 1992). Ennek kialakulásában és fenntartásában szerepet játszó folyamatok azonban teljesen nem ismertek. Egy feltételezett mikroszómális elektrontranszfer-lánc továbbíthatja az újonnan szintetizált fehérjék tiolcsoportjairól az elektronokat a végső elektronfelvevőre, az oxigénre. Ennek az elektrontranszfer-láncnak a fehérje komponenseit már régóta kutatják. Leírták egy FAD-tartalmú enzim (endoplazmás retikulum oxidáz, Ero1) és a protein-diszulfid izomeráz (PDI) funkcionális kapcsolatát, mely szerint az oxigén, mint végső elektronakceptor, oxidálja az Ero1-et, ami oxidálja a PDI-t; a PDI pedig végül az újonnan szintetizált fehérjékben alakítja ki a diszulfidkötéseket (Tu és Weissman 2004). Azonban az Ero1 oxidációjának mechanizmusát részleteiben kevésbé ismerték. Feltételezhető volt, hogy a FAD és a molekuláris oxigén közötti elektronátadásban más, kis molekulatömegű elektronszállítók is részt vesznek. Leginkább a C-vitamin (aszkorbát) és az E-vitamin (tokoferol) résztvételét lehetett valószínűsíteni, ezek lévén a legnagyobb mennyiségben előforduló vízoldékony és zsíroldékony antioxidáns molekulák az endoplazmás retikulumban. Munkacsoportunk az elmúlt években számos kísérletet végzett ezen antioxidánsok szerepének tisztázására az endoplazmás retikulumban Az aszkorbát-oxidáz aktivitása a mikroszómában Intakt sejtekben az endoplazmás retikulumban lévő oxidatív környezet lehetővé teszi, hogy az újonnan szintetizált fehérjékben diszulfidhidak alakuljanak ki. Ez azonban nincs így az endoplazmás retikulum eredetű izolált mikroszómában, ami arra utal, hogy a folyamat egy citoplazmában lévő faktor vagy egy membránpermeábilis összetevő részvételét igényli, mely a mikroszómák preparálása során elvész. Felvetődött tehát a legnagyobb koncentrációban jelen lévő vízoldékony antioxidáns, az aszkorbát szerepe. Az aszkorbát prooxidáns funkciója a dehidroaszkorbát képződéséhez kapcsolódik. Ez az aszkorbát 18
20 oxidált formája, amely két elektron leadásával rendszerint két lépésben keletkezik (Van der Zee és Van den Broek 1998). Növényekben ismertek aszkorbát oxidáz enzimek, amelyek aszkorbil szabadgyököt képeznek az aszkorbátból (Horemans és mtsai 2000). Ez az intermedier aztán a második elektron leadásával akár egy másik aszkorbil szabadgyöknek (diszproporcionálódás) alakul dehidroaszkorbáttá. Állati szervezetben azonban jóval kevésbé volt ismert a folyamat, sőt, általában ezt nem enzimatikus reakcióként tartották számon, amit például fémionok vagy szabadgyökök katalizálhatnak. Patkánymáj mikroszóma jelenlétében az aszkorbát folyamatosan átalakul aszkorbilgyökké majd dehidroaszkorbáttá. A citoszóléval megegyező aszkorbátkoncentrációval (0,1 mm) indulva 37 C-on az aszkorbát koncentrációja egyenletes sebességgel, folyamatosan csökken (Szarka és mtsai 2002). A keletkező dehidroaszkorbát már néhány perc után detektálható, és szintje állandó marad egészen addig, amíg az aszkorbát el nem fogy. Az aszkorbilgyök jelenlétét is kimutattuk elektronspin-rezonancia-spektroszkópia segítségével. Mikroszóma nélküli pufferben inkubálva az aszkorbátot, autooxidáció révén detektálható mennyiségű aszkorbilgyök keletkezik. Mikroszóma jelenlétében azonban lényegesen nagyobb aszkorbilgyökszint mérhető, és ez az inkubáció teljes ideje alatt állandó marad. Mivel mind az aszkorbilgyök, mind a dehidroaszkorbát nagyon instabil, állandó szintjüket csak a folyamatos aszkorbátoxidáció tarthatja fenn. A mikroszóma jelenlétében többszörösére fokozódó aszkorbátoxidáció egy mikroszómális aszkorbát-oxidáz enzim aktivitására utal. A mikroszómák előkezelése akár hővel, akár proteázzal az aszkorbilgyök keletkezését jelentősen csökkenti, s az aszkorbátoxidáz aktivitását akár meg is szünteti, jelezve, hogy valóban enzimatikus, fehérjemediált folyamatról van szó (Szarka és mtsai 2002). Az azonosítatlan mikroszómális aszkorbát-oxidázról további információkat nyertünk gátlószerek felhasználásával. Sem gyökfogók, sem antioxidáns enzimek nem befolyásolják az aszkorbilgyök képződését. Ugyancsak hatástalanok a flavoprotein- és a hemoprotein-gátlószerek is. Ezzel szemben a citokróm inhibitorai jelentősen gátolják az aszkorbilgyök képződését, de az autooxidációt (mikroszóma nélkül) is, így feltehetőleg nem az enzimre hatnak, hanem közvetlenül reagálnak az aszkorbilgyökkel (redukálják azokat). A megvizsgált fémkelátorok (dipiridil, 1,10-fenantrolin, neokuproin) közül a 19
21 legerősebb gátlást a rézspecifikus neokuproin váltja ki. Ez mikroszóma nélkül, vagy hőinaktivált mikroszóma esetén hatástalan, csak ép mikroszóma jelenlétében hat, és szinte az autooxidáció szintjére csökkenti az aszkorbilgyökök keletkezését (Szarka és mtsai 2002). Ez a megfigyelés különösen azért érdekes, mert a növényi aszkorbát-oxidáz enzim is rezet tartalmaz (Dawson és mtsai 1975) A fehérjék tiolcsoportjainak oxidációja aszkorbát hatására A mikroszómához adott aszkorbát fogyása mellett megfigyeltük a fehérjék tioljainak kifejezett oxidációját is, ami aszkorbát nélkül elhanyagolható volt. Az aszkorbát és a tiol oxidációja korrelál egymással. A citokróm P450 inhibitorai (ekonazol, quercetin) vagy neokuproin jelenlétében mind az aszkorbátfogyás, mind a tioloxidáció csökken (Csala és mtsai 1999). Mivel a tioloxidáció az aszkorbátoxidációhoz kötött, feltételeztük, hogy a dehidroaszkorbát is részt vesz a folyamatban. A dehidroaszkorbát valóban kiváltja a fehérjék tioljainak oxidációját, bár kisebb mértékben, mint az aszkorbát (Csala és mtsai 1999). Ez különösen azért fontos, mert az endoplazmás retikulum membránja nem egyformán permeábilis az aszkorbát/dehidroaszkorbát redoxpár két tagjára nézve. Míg az oxidált alak jól mérhető sebességgel halad át a membránon, addig a redukált forma transzportja elhanyagolható (Bánhegyi és mtsai 1998). Ennek megfelelően, az aszkorbát transzportját az aszkorbátoxidáz gátlása akadályozza, azaz csak dehidroaszkorbáttá alakulva képes bejutni a lumenbe (Csala és mtsai 2000). A lumenbe jutott dehidroaszkorbát lévén a protein-diszulfid izomeráz enzim egyik szubsztrátja mint kis molekulatömegű elektronakceptor, részt tud venni a fehérjéknek ebben a kompartimentumban zajló oxidatív hajtogatódásában ( folding ) (Wells és mtsai 1990). A PDI a dehidroaszkorbátot redukálja, miközben az enzimen lévő tiolcsoportok oxidálódnak. Az immár oxidált protein-diszulfid izomeráz reagál a tiolcsoportokat tartalmazó fehérjékkel, azokon diszulfidhidakat hozva létre, miközben az enzim regenerálódik és visszaalakul katalízisre képes állapotába. Ennek az enzimreakciónak az eredményeként aszkorbát keletkezik (és felhalmozódik) a lumenben. A folyamat végbemenetelének bizonyítéka, hogy diabéteszes állat májából készült 20
22 mikroszómában, amelynek lumenében nem hajtogatott ( unfolded ) fehérje vagyis sok redukált tiolcsoport halmozódik fel (Nardai és mtsai 2003), az aszkorbát intraluminális akkumulálódása jelentősen megnő (Nardai és mtsai 2001) Az E-vitamin szerepe a fehérje tiolok aszkorbát által kiváltott oxidációjában Az a megfigyelés, hogy az aszkorbát a dehidroaszkorbátnál hatékonyabban fokozta a fehérjék tiolcsoportjainak oxidációját a mikroszómában, arra utalt, hogy az aszkorbát oxidációja valamilyen közvetett módon is kifejtette hatását. Ez egy lipidoldékony, az endoplazmás retikulum membránjában elhelyezkedő molekula jelenlétére utalt, mely a két folyamatot a membrán külső felszínén lejátszódó aszkorbátoxidációt és a lumenben végbemenő protein-tioloxidációt összekapcsolja. Az E-vitamin az endoplazmás retikulum legnagyobb mennyiségben előforduló membránhoz kötött antioxidánsa. Szerepe E- vitaminhiányos patkányok májából preparált mikroszómákon végzett kísérletekben igazolódott be. Az ilyen mikroszóma α-tokoferol-tartalma rendkívül alacsony, de in vitro körülmények között utólag szinte teljesen visszaállítható (Csala és mtsai 2001). Az E- vitamin hiánya részlegesen szétkapcsolja az extra- és intraluminális redoxfolyamatokat, vagyis az aszkorbát- és a fehérjetiolok oxidációját. Ez azt jelenti, hogy az ilyen mikroszómában jelentősen csökken az aszkorbát által kiváltott diszulfidképződés, holott az aszkorbát maga gyorsabban oxidálódik. Ezt a szétkapcsolást a membránlipidek fokozott peroxidációja is kíséri, ami nyilván az aszkorbát oxidációjakor keletkező ROS hatása. A különböző vízoldékony gyökfogók csak nagyon kis mértékben vagy egyáltalán nem védik ki a lipidperoxidációt, ami arra utal, hogy a ROS a membrán közvetlen közelében keletkezik lipidkörnyezetben ami leginkább lipofil antioxidánsok számára hozzáférhető. Vagyis feltételezzük, hogy az E-vitamin közvetlenül ennek a ROS-nak az oxidáló hatását közvetíti a lumenbe; ami így nem a membrán lipidjeit, hanem végső soron a fehérjék tiolcsoportjait oxidálja. A tokoferol utólagos pótlására a két folyamat kapcsolata újra helyreáll és a lipidperoxidáció mértéke is lecsökken (Csala és mtsai 2001). 21
23 A citokróm b561, egy alternatív transzmembrán elektronszállító molekula Az elmúlt évek során azonosítottak egy aszkorbát által redukálható, b típusú citokrómot a növényi sejtek plazmamenbránjában. A citokróm abszorpciós spektrumára jellemző az 561 nm fényelnyelési maximumnál megjelenő α hullám, amely alapján a fehérje a citokróm b561 nevet kapta. A citokróm b561 fehérjecsalád jellemzője a magas redoxpotenciál, az aszkorbát hatására való redukció és a membránon keresztüli elektronszállítás képessége. Az igen hidrofób fehérje hat transzmembrán hélixből áll, négy erősen konzervált hisztidint és a membrán két oldalán 1-1 hem prosztetikus csoportot tartalmaz. A membrán egyik felszínén található hem csoport szerepe az elektronok átvétele az aszkorbáttól, míg a membrán másik felszínén található hem csoport az így felvett elektronokat a monodehidroaszkorbátra (aszkorbil gyökre) transzportálja, ezzel regenerálva az aszkorbátot. Az aszkorbát ezután tovább tudja adni a felvett elektronokat az aszkorbát kofaktorral működő enzimek számára, így a transzmembrán elektronszállító citokróm képes fenntartani egy állandó aszkorbátszintet, és ezáltal biztosítani az aszkorbát fiziológiás funkcióinak ellátását (Tsubaki és mtsai 2005). Újabban a citokróm b561 családhoz tartozó fehérjéket számos állati szövetben is leírtak, a plazmamembránban és különböző organellumok membránjában egyaránt. A citokróm b561 eddig azonosított három izoformája: a kromaffin granulumokban található CGcytb, melynek szerepe a katekolamin szintézishez szükséges aszkorbát szint fenntartása a neuroendokrin szövetekben (Fleming és Kent 1991), a duodenális Dcytb, mely a ferri iont a könnyebben felszívódó ferro ionná redukálja (McKie és mtsai 2001), illetve a lizoszómális Lcytb, mely a lebontott hemoproteinek eloxidálódott vas ionjainak visszaredukálásában játszik szerepet (Zhang és mtsai 2006). Citokróm b561 enzimek jelenlétét endoplazmás retikulumban eddig nem vizsgálták, de az E-vitamin mellett ez a fehérje is szerepet játszhat az endoplazmás retikulum membránon keresztül történő elektronszállításban Az antioxidánsok oxidatív foldingban betöltött szerepének összegzése A leírt megfigyelések alapján a következő modellt állítottuk fel az 22
24 aszkorbát/dehidroaszkorbát és az E-vitamin oxidatív fehérje hajtogatódásban betöltött szerepére (3. ábra). A citoplazmában az aszkorbát aszkorbilgyökké alakul enzimatikus folyamat segítségével, ami az endoplazmás retikulum membránjának külső felszínén játszódik le. Ezt a folyamatot reaktív oxigéngyökök keletkezése kíséri. Ezután az aszkorbilgyök oxidációval vagy diszproporcionálódással továbbalakul dehidroaszkorbáttá. A dehidroaszkorbát bejut az endoplazmás retikulum lumenébe, ahol a PDI szubsztrátjaként részt vesz a fehérjék ciszteinjein lévő tiolcsoportok oxidálásában. Ilymódon a dehidroaszkorbát ismét aszkorbáttá alakul, amely nem tud több diszulfidhidat létrehozni, hacsak le nem ad két elektront, és vissza nem alakul dehidroaszkorbáttá. Erre ad lehetőséget a membránban jelen lévő tokoferol, amely összeköttetést teremt a membrán külső felszínén lévő oxigénszabadgyökök és a lumenben lévő aszkorbát között. A membrán közvetlen közelében keletkező reaktív oxigéngyökök oxidálják az E-vitamint E- vitamingyökké. Ez pedig képes visszaoxidálni az aszkorbátot dehidroaszkorbáttá a lumenben. Ennek a reakcióláncnak a végső eredménye az elektronok folyamatos áramlása a ciszteincsoportoktól, mint primer elektrondonoroktól az oxigénig, mint végső elektronakceptorig (Margittai 2004; Bánhegyi és mtsai 2002; Bánhegyi és mtsai 2003). Az E-vitamin hiányában az elektrontranszfer-lánc egy fontos komponense esik ki, ami azért okoz megnövekedett lipidperoxidációt, mert a ROS E-vitamin helyett a közeli membránban lévő egyéb lipidekkel reagál; azért okoz megnövekedett aszkorbátfogyást, mert hiányzik az E-vitamingyök, amely az aszkorbátot újraoxidálja; és ugyanezért okoz csökkent tioloxidációt. Fontos megjegyezni, hogy az aszkorbát az E-vitaminhiányos mikroszómákban is kivált némi tioloxidációt. Így valószínű, hogy más lipidoldékony antioxidánsok, mint a K-vitamin vagy az ubikinon, hasonló funkciót töltenek be az endoplazmás retikulum membránjában. 23
25 3. ábra. Antioxidánsok szerepe az oxidatív fehérje foldingban az endoplazmás retikulumban. (Margittai 2005) 1.3. Diszulfid kötések keletkezése A protein folding egyik legfontosabb lépése a diszulfid hidak kialakulása. A diszulfid hidak alapvetően szükségesek a szekrécióra kerülő és a membránban elhelyezkedő fehérjék 24
26 stabilitásához, megfelelő működéséhez mind prokariótákban, mind eukariótákban (Sevier és Kaiser 2002). A diszulfid hidak kialakulása két elektron átvitelével járó folyamat. In vitro megtörténhet spontán, a ciszteinek tiol csoportjainak elektronleadásával egy elektron akceptorra, mint pl. a molekuláris oxigén. In vivo a tiol-diszulfid-kicserélődés révén jönnek létre a fehérjék diszulfid hídjai. Ez a reakció megtörténhet bármely tiol csoportot tartalmazó molekula (pl. glutation) és egy fehérje között. A folyamat során minden esetben kimutatható az átmenetileg jelen lévő kevert diszulfid a két molekula között, majd végeredményként az eredetileg oxidált állapotban lévő tiol csoportok redukálódnak, a redukáltak pedig oxidálódnak. Ezt a kicserélődési reakciót tiol-diszulfid-oxidoreduktázok katalizálják. Ezen enzimek legfontosabb jellemzője, hogy tartalmaznak legalább egy Cys-X-X-Cys motívumot, aminek alapvető szerepe van a diszulfid hidak kialakításában vagy felbontásában a tiol-diszulfid-kicserélődési reakció során A diszulfid hidak kialakulása prokariótákban A prokariótákban a diszulfid hidak a periplazmában jönnek létre (Collet és Bardwell 2002; Ritz és Beckwith 2001), ahol a DsbA ( disulfide bond A ) nevű tiol-diszulfidoxidoreduktáz található. A DsbA tioljainak visszaoxidálódását a belső membránban elhelyezkedő DsbB biztosítja. Ez a fehérje az elektronokat aerob körülmények között egy ubikinon kofaktoron keresztül szállítja a molekuláris oxigénre, míg anaerob viszonyoknál a menakinon közreműködésével juttatja különböző szubsztrátokra, mint a nitrát vagy a fumarát. A prokariótákban a fent leírt DsbA-DsbB rendszer mellett létezik egy másik útvonal, amely a helytelenül kialakult diszulfid hidak izomerizációját katalizálja. Itt a periplazmában található DsbC (ami szintén egy tiol-diszulfid-oxidoreduktáz) vesz részt közvetlenül a fehérjében lévő diszulfidok átrendezésében. A DsbC redukált állapotát egy DsbD nevű fehérje tartja fenn, amely szintén a belső membránban elhelyezkedő integráns protein. Ezt pedig egy citoplazmában elhelyezkedő tioredoxin redukálja, mely a NADPH-ról vesz fel elektronokat a tioredoxin reduktáz segítségével. 25
27 A diszulfid hidak kialakulása eukariótákban Az eukariótákban a diszulfid hidak kialakulásának helyszíne az endoplazmás retikulum lumene. Ezt a sejtorganellumot oxidatív környezet, egyben a citoplazmáénál negatívabb redox potenciál jellemzi, mely a redukált és oxidált glutation arányában (GSH/GSSG) is megmutatkozik. Ez az arány a citoplazmában :1, míg az endoplazmás retikulum lumenében 1-3:1. Feltételezték, hogy ez az arány egy szelektív GSSG transzportnak köszönhető, és ezáltal a GSSG biztosítja az endoplazmás retikulumban a fehérjék diszulfid hídjainak kialakulásához szükséges oxidatív környezetet (Hwang és mtsai 1992) A protein diszulfid izomeráz A PDI negyven évvel ezelőtti izolálása rávilágított, hogy a fehérjékben előforduló diszulfid kötések létrejötte enzimatikus folyamat (Venetianer és Straub 1964; Venetianer és Straub 1965). A PDI alapvető szerepét nyilvánvalóvá teszi, hogy az egyik legnagyobb mennyiségben előforduló enzim emlős és élesztő sejtek endoplazmás retikulumának lumenében; a sejt teljes fehérjetartalmának mintegy 0,8 %-át teszi ki (Freedman és mtsai 1994). Funkciója nélkülözhetetlen, így nem véletlen, hogy különböző fajokban leírt változatai nagyfokú konzervativitást mutatnak (Ferrari és Söling 1999). Az 55 kda-os fehérjelánc tipikus C-terminális endoplazmás retikulumban tartó szekvenciát hordoz. A PDI a diszulfid kötések kialakulását, izomerizációját, továbbá redukcióját katalizálja, s emellett chaperon aktivitással is bír. Az aktív enzim négy tioredoxin-szerű doménből (a, b, b és a ), valamint egy c részből áll, így a PDI a tioredoxin szupercsalád tagja. Az oxidált állapotú PDI közvetlen tiol-diszulfid kicserélődési reakcióba léphet a szubsztrátfehérjékkel, melynek köztiterméke a két fehérje között kialakuló diszulfid Az Ero1 fehérje Élesztőben megtalálták az Ero1 gént, amelyről bebizonyosodott, hogy kulcsszerepet játszik a diszulfid hidak kialakulásában, így a megfelelő fehérje-tekeredésben (Frand és Kaiser 1998; Pollard és mtsai 1998). Szerepét alátámasztják az Ero1-1 mutánsokkal végzett 26
28 kísérletek; ilyen sejtek endoplazmás retikulumában felhalmozódnak azok a fehérjék, melyekben az esszenciális diszulfid hidak kialakulása és így a megfelelő tekeredés elmarad, ugyanakkor az esszenciális diszulfidot nem tartalmazó fehérjék megfelelő időben elhagyják az endoplazmás retikulumot és betöltik funkciójukat. Ez hasonlít ahhoz a folding-zavarhoz, amit vad típusú sejtek redukálószeres (DTT) kezelése után lehet megfigyelni. A mutáns sejtek tioloxidálószer diamiddal való kezelése a foldingot és a sejtek életképességét helyreállítja. Ez arra utal, hogy az Ero1 gén termékének legfontosabb szerepe az endoplazmás retikulumban lévő oxidatív környezet fenntartása. Az a megfigyelés, hogy a hibásan feltekeredett fehérjék által kiváltott endoplazmás retikulum stressz fokozza az Ero1 gén expresszióját, jól mutatja, hogy az endoplazmás retikulum stressz válasz egyik legfontosabb feladata a fehérjefolding helyreállítása. Az Ero1-1 mutáns sejtek életképességét nem sikerült visszaállítani a PDI gén túlexpresszáltatásával (Frand és Kaiser 1998), tehát ez Ero1 és a PDI funkciója egyaránt szükséges, de önmagában egyik sem elégséges a diszulfid hidak helyes kialakulásához. Ma már az is ismert, hogy az Ero1 és a PDI között funkcionális kapcsolat áll fenn, amennyiben az elektronok a PDI-től az Ero1 felé vándorolnak, így biztosítva a PDI oxidált állapotát, ami szubsztrát fehérjékben diszulfidképződéshez vezet (Frand és Kaiser 1999). Ezt a vegyes PDI-Ero1 diszulfid izolálásával bizonyították, amely a direkt tiol-diszulfid kicserélődés obligát köztiterméke. Az emlősökben is megtalálhatók az Ero1 szerepét betöltő fehérjék, az Ero1-Lα és az Ero1- Lβ (Cabibbo és mtsai 2000; Pagani és mtsai 2000; Mezghrani és mtsai 2001). Normál körülmények között az Ero1-Lα katalizálja a diszulfid képződés sebesség-meghatározó lépését. Az Ero1-Lβ PDI oxidáló hatása nagyobbnak tűnik, de normál körülmények között nem expresszálódik. Szerepe elsősorban a nagy fehérjeterhelés következményeként kialakuló endoplazmás retikulum stresszben jelentős, ugyanis ekkor ez a molekula veszi át az irányítást az Ero1-Lα-tól, így hatékonyabbá válik a proteinfolding. 27
Antioxidánsok szerepe a fehérje diszulfid kötések kialakulásában SZARKA ANDRÁS
 Semmelweis Egyetem, Molekuláris Orvostudományok Doktori Iskola PATHOBIOKÉMIA DOKTORI PROGRAM Antioxidánsok szerepe a fehérje diszulfid kötések kialakulásában Doktori (Ph.D.) értekezés tézisei SZARKA ANDRÁS
Semmelweis Egyetem, Molekuláris Orvostudományok Doktori Iskola PATHOBIOKÉMIA DOKTORI PROGRAM Antioxidánsok szerepe a fehérje diszulfid kötések kialakulásában Doktori (Ph.D.) értekezés tézisei SZARKA ANDRÁS
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban
 A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban PhD értekezés tézisek Varsányi Marianne 2005 Témavezető: Dr. Bánhegyi Gábor Semmelweis Egyetem Orvosi Vegytani, Molekuláris
A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban PhD értekezés tézisek Varsányi Marianne 2005 Témavezető: Dr. Bánhegyi Gábor Semmelweis Egyetem Orvosi Vegytani, Molekuláris
A téma címe: Antioxidáns anyagcsere és transzportfolyamatok az endo/szarkoplazmás retikulumban A kutatás időtartama: 4 év
 Témavezető neve: Dr. Csala Miklós A téma címe: Antioxidáns anyagcsere és transzportfolyamatok az endo/szarkoplazmás retikulumban A kutatás időtartama: 4 év Háttér A glutation (GSH) és a glutation diszulfid
Témavezető neve: Dr. Csala Miklós A téma címe: Antioxidáns anyagcsere és transzportfolyamatok az endo/szarkoplazmás retikulumban A kutatás időtartama: 4 év Háttér A glutation (GSH) és a glutation diszulfid
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
1b. Fehérje transzport
 1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
Diabéteszes redox változások hatása a stresszfehérjékre
 Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola Pathobiokémia Program Doktori (Ph.D.) értekezés Diabéteszes redox változások hatása a stresszfehérjékre dr. Nardai Gábor Témavezeto:
Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola Pathobiokémia Program Doktori (Ph.D.) értekezés Diabéteszes redox változások hatása a stresszfehérjékre dr. Nardai Gábor Témavezeto:
A légzési lánc és az oxidatív foszforiláció
 A légzési lánc és az oxidatív foszforiláció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet intermembrán tér Fe-S FMN NADH mátrix I. komplex: NADH-KoQ reduktáz
A légzési lánc és az oxidatív foszforiláció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet intermembrán tér Fe-S FMN NADH mátrix I. komplex: NADH-KoQ reduktáz
Endoplazmás retikulum stressz skorbutban. Doktori értekezés. Dr. Margittai Éva
 Endoplazmás retikulum stressz skorbutban Doktori értekezés Dr. Margittai Éva Semmelweis Egyetem Doktori Iskola Molekuláris Orvostudományok Tudományági Doktori Iskola Témavezető: Dr. Csala Miklós egyetemi
Endoplazmás retikulum stressz skorbutban Doktori értekezés Dr. Margittai Éva Semmelweis Egyetem Doktori Iskola Molekuláris Orvostudományok Tudományági Doktori Iskola Témavezető: Dr. Csala Miklós egyetemi
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont
 Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori tézisek Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori tézisek Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
A flavonoidok az emberi szervezet számára elengedhetetlenül szükségesek, akárcsak a vitaminok, vagy az ásványi anyagok.
 Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
Dr. Csala Miklós OTKA NN 75275
 Az endoplazmás retikulum piridin-nukleotid rendszerének redox változásai: összefüggés az elhízással, a 2-es típusú diabetes-szel és a metabolikus szindrómával Bevezetés A prohormonnak tekinthető kortizon
Az endoplazmás retikulum piridin-nukleotid rendszerének redox változásai: összefüggés az elhízással, a 2-es típusú diabetes-szel és a metabolikus szindrómával Bevezetés A prohormonnak tekinthető kortizon
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont
 Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori értekezés Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori értekezés Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Teaflavanolok hatása az endoplazmás retikulum fehérjeérési és minőségellenőrzési folyamataira
 Teaflavanolok hatása az endoplazmás retikulum fehérjeérési és minőségellenőrzési folyamataira Doktori értekezés Magyar Éva Judit Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Teaflavanolok hatása az endoplazmás retikulum fehérjeérési és minőségellenőrzési folyamataira Doktori értekezés Magyar Éva Judit Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
A téma címe: Mikroszómális glukóz-6-foszfát szerepe granulocita apoptózisában
 Témavezető neve: Dr. Kardon Tamás Zoltán A téma címe: Mikroszómális glukóz-6-foszfát szerepe granulocita apoptózisában A kutatás időtartama: 2004-2007 Tudományos háttér A glukóz-6-foszfatáz multienzim-komplex
Témavezető neve: Dr. Kardon Tamás Zoltán A téma címe: Mikroszómális glukóz-6-foszfát szerepe granulocita apoptózisában A kutatás időtartama: 2004-2007 Tudományos háttér A glukóz-6-foszfatáz multienzim-komplex
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből.
 Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Hús és hústermék, mint funkcionális élelmiszer
 Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK
 POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
BIOKÉMIA. A Magyar Biokémiai Egyesület tájékoztatója Quarterly Bulletin of the Hungarian Biochemical Society
 BIKÉMIA A Magyar Biokémiai Egyesület tájékoztatója Quarterly Bulletin of the Hungarian Biochemical Society Szerkesztôbizottság: ALKNYI ISTVÁN, BÁNFALVI GÁSPÁR, FALUS ANDRÁS, FÉSÜS LÁSZLÓ, GERGELY PÁL,
BIKÉMIA A Magyar Biokémiai Egyesület tájékoztatója Quarterly Bulletin of the Hungarian Biochemical Society Szerkesztôbizottság: ALKNYI ISTVÁN, BÁNFALVI GÁSPÁR, FALUS ANDRÁS, FÉSÜS LÁSZLÓ, GERGELY PÁL,
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Mire költi a szervezet energiáját?
 Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
6. Zárványtestek feldolgozása
 6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
Glikolízis. emberi szervezet napi glukózigénye: kb. 160 g
 Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
A pályázat keretében a következő kérdéseket kívántuk részleteiben vizsgálni:
 A glikogenolízis és glukoneogenezis utolsó, közös lépését katalizáló glukóz-6-foszfatáz egy enzimrendszer, melyben a katalitikus alegység kevéssé specifikus, különböző foszfátésztereket tud hasítani és
A glikogenolízis és glukoneogenezis utolsó, közös lépését katalizáló glukóz-6-foszfatáz egy enzimrendszer, melyben a katalitikus alegység kevéssé specifikus, különböző foszfátésztereket tud hasítani és
A FAD transzportjának szerepe. az oxidatív fehérje foldingban. patkány máj mikroszómákban
 A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban PhD értekezés Varsányi Marianne 2005 Témavezető: Dr. Bánhegyi Gábor Semmelweis Egyetem Orvosi Vegytani, Molekuláris
A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban PhD értekezés Varsányi Marianne 2005 Témavezető: Dr. Bánhegyi Gábor Semmelweis Egyetem Orvosi Vegytani, Molekuláris
TRANSZPORTFOLYAMATOK 1b. Fehérjék. 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS
 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen
1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
A nitrogén körforgalma. A környezetvédelem alapjai május 3.
 A nitrogén körforgalma A környezetvédelem alapjai 2017. május 3. A biológiai nitrogén körforgalom A nitrogén minden élő szervezet számára nélkülözhetetlen, ún. biogén elem Részt vesz a nukleinsavak, a
A nitrogén körforgalma A környezetvédelem alapjai 2017. május 3. A biológiai nitrogén körforgalom A nitrogén minden élő szervezet számára nélkülözhetetlen, ún. biogén elem Részt vesz a nukleinsavak, a
VÁLASZ. Dr. Virág László bírálatára
 VÁLASZ Dr. Virág László bírálatára Köszönöm, hogy Professzor úr vállalta értekezésem bírálatát. Hálás vagyok az értékelésében foglalt méltató szavakért, és a disszertáció vitára bocsátásának támogatásáért.
VÁLASZ Dr. Virág László bírálatára Köszönöm, hogy Professzor úr vállalta értekezésem bírálatát. Hálás vagyok az értékelésében foglalt méltató szavakért, és a disszertáció vitára bocsátásának támogatásáért.
Az eukarióta sejt energiaátalakító organellumai
 A mitokondrium és a kloroplasztisz hasonlósága Az eukarióta sejt energiaátalakító organellumai mitokondrium kloroplasztisz eukarióta sejtek energiaátalakító és konzerváló organellumai Működésükben alapvető
A mitokondrium és a kloroplasztisz hasonlósága Az eukarióta sejt energiaátalakító organellumai mitokondrium kloroplasztisz eukarióta sejtek energiaátalakító és konzerváló organellumai Működésükben alapvető
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése
 Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Patobiokémia Szarka András, Bánhegyi Gábor
 Patobiokémia Szarka András, Bánhegyi Gábor Patobiokémia Szarka András, Bánhegyi Gábor Szerzői jog 2014 Szarka András, Bánhegyi Gábor, Budapesti Műszaki és Gazdaságtudományi Egyetem, Semmelweis Egyetem
Patobiokémia Szarka András, Bánhegyi Gábor Patobiokémia Szarka András, Bánhegyi Gábor Szerzői jog 2014 Szarka András, Bánhegyi Gábor, Budapesti Műszaki és Gazdaságtudományi Egyetem, Semmelweis Egyetem
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
A sokoldalú L-Karnitin
 A sokoldalú L-Karnitin Az L-Karnitint két orosz kutató Gulewits és Krimberg izolálta először emlősállatok húsából. Száz évvel e Kémiai szintézissel az L-Karnitin ipari gyártása az 1970-es évek végén kezdödött
A sokoldalú L-Karnitin Az L-Karnitint két orosz kutató Gulewits és Krimberg izolálta először emlősállatok húsából. Száz évvel e Kémiai szintézissel az L-Karnitin ipari gyártása az 1970-es évek végén kezdödött
A KOLESZTERIN SZERKEZETE. (koleszterin v. koleszterol)
 19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Táplálék. Szénhidrát Fehérje Zsír Vitamin Ásványi anyagok Víz
 Étel/ital Táplálék Táplálék Szénhidrát Fehérje Zsír Vitamin Ásványi anyagok Víz Szénhidrát Vagyis: keményítő, élelmi rostok megemésztve: szőlőcukor, rostok Melyik élelmiszerben? Gabona, és feldolgozási
Étel/ital Táplálék Táplálék Szénhidrát Fehérje Zsír Vitamin Ásványi anyagok Víz Szénhidrát Vagyis: keményítő, élelmi rostok megemésztve: szőlőcukor, rostok Melyik élelmiszerben? Gabona, és feldolgozási
Zárójelentés. Gabonafélék stresszadaptációját befolyásoló jelátviteli folyamatok tanulmányozása. (K75584 sz. OTKA pályázat)
 Zárójelentés Gabonafélék stresszadaptációját befolyásoló jelátviteli folyamatok tanulmányozása (K75584 sz. OTKA pályázat) A tervezett kísérletek célja, hogy jobban megértsük a növények változó környezetre
Zárójelentés Gabonafélék stresszadaptációját befolyásoló jelátviteli folyamatok tanulmányozása (K75584 sz. OTKA pályázat) A tervezett kísérletek célja, hogy jobban megértsük a növények változó környezetre
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
Az aszkorbinsav koncentráció és redox státusz szabályozása növényi sejtekben bioszintézis és intracelluláris transzport révén
 Az aszkorbinsav koncentráció és redox státusz szabályozása növényi sejtekben bioszintézis és intracelluláris transzport révén Témavezető neve: Szarka András A kutatás időtartama: 4 év Tudományos háttér
Az aszkorbinsav koncentráció és redox státusz szabályozása növényi sejtekben bioszintézis és intracelluláris transzport révén Témavezető neve: Szarka András A kutatás időtartama: 4 év Tudományos háttér
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A tápláléknövények legfontosabb biológiai hatásai; az optimális étrend jellemzői tápláléknövények bevitele szempontjából.
 A tápláléknövények legfontosabb biológiai hatásai; az optimális étrend jellemzői tápláléknövények bevitele szempontjából Farkas Ágnes Williams K. A., Patel H. (2017): Healthy Plant-Based Diet. Journal
A tápláléknövények legfontosabb biológiai hatásai; az optimális étrend jellemzői tápláléknövények bevitele szempontjából Farkas Ágnes Williams K. A., Patel H. (2017): Healthy Plant-Based Diet. Journal
sejt működés jovo.notebook March 13, 2018
 1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
A koenzim Q10 fél évszázados története
 A koenzim Q10 fél évszázados története A koenzim Q10 a sejtek optimális működéséhez nélkülözhetetle A koenzim Q10 (KoQ10) vitaminszerű vegyület. Az ubikinonok k 1 / 8 A Nobel-díjas Dr. Peter Mitchell Kémiailag
A koenzim Q10 fél évszázados története A koenzim Q10 a sejtek optimális működéséhez nélkülözhetetle A koenzim Q10 (KoQ10) vitaminszerű vegyület. Az ubikinonok k 1 / 8 A Nobel-díjas Dr. Peter Mitchell Kémiailag
DER (Felületén riboszómák találhatók) Feladata a biológiai fehérjeszintézis Riboszómák. Az endoplazmatikus membránrendszer. A kódszótár.
 Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az élő szervezetek menedzserei, a hormonok
 rekkel exponálunk a munka végén) és azt utólag kivonjuk digitálisan a képekből. A zajcsökkentés dandárját mindig végezzük a raw-képek digitális előhívása során, mert ez okozza a legkevesebb jelvesztést
rekkel exponálunk a munka végén) és azt utólag kivonjuk digitálisan a képekből. A zajcsökkentés dandárját mindig végezzük a raw-képek digitális előhívása során, mert ez okozza a legkevesebb jelvesztést
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
Táplálkozás. SZTE ÁOK Biokémiai Intézet
 Táplálkozás Cél Optimális, kiegyensúlyozott táplálkozás - minden szükséges bevitele - káros anyagok bevitelének megakadályozása Cél: egészség, jó életminőség fenntartása vagy visszanyerése Szükséglet és
Táplálkozás Cél Optimális, kiegyensúlyozott táplálkozás - minden szükséges bevitele - káros anyagok bevitelének megakadályozása Cél: egészség, jó életminőség fenntartása vagy visszanyerése Szükséglet és
A MITOKONDRIÁLIS ENERGIATERMELŐ FOLYAMATOK VIZSGÁLATA
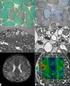 Biokémiai és Molekuláris Biológiai Intézet Általános Orvostudományi Kar Debreceni Egyetem BIOKÉMIA GYAKORLAT A MITOKONDRIÁLIS ENERGIATERMELŐ FOLYAMATOK VIZSGÁLATA Elméleti háttér Dr. Kádas János 2015 A
Biokémiai és Molekuláris Biológiai Intézet Általános Orvostudományi Kar Debreceni Egyetem BIOKÉMIA GYAKORLAT A MITOKONDRIÁLIS ENERGIATERMELŐ FOLYAMATOK VIZSGÁLATA Elméleti háttér Dr. Kádas János 2015 A
Grilla Stúdiója - gyógytorna, szülésfelkészítés
 Az éltetõ vitaminok A vitaminok olyan szerves vegyületek, amelyek feltétlenül szükségesek testünk kifogástalan mûködéséhez. A vitamin elnevezés a vita (élet) és az amin (NH2-tartalmú kémiai gyök) szavakból
Az éltetõ vitaminok A vitaminok olyan szerves vegyületek, amelyek feltétlenül szükségesek testünk kifogástalan mûködéséhez. A vitamin elnevezés a vita (élet) és az amin (NH2-tartalmú kémiai gyök) szavakból
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
T-2 TOXIN ÉS DEOXINIVALENOL EGYÜTTES HATÁSA A LIPIDPEROXIDÁCIÓRA ÉS A GLUTATION-REDOX RENDSZERRE, VALAMINT ANNAK SZABÁLYOZÁSÁRA BROJLERCSIRKÉBEN
 T-2 TOXIN ÉS DEOXINIVALENOL EGYÜTTES HATÁSA A LIPIDPEROXIDÁCIÓRA ÉS A GLUTATION-REDOX RENDSZERRE, VALAMINT ANNAK SZABÁLYOZÁSÁRA BROJLERCSIRKÉBEN Mézes Miklós a,b, Pelyhe Csilla b, Kövesi Benjámin a, Zándoki
T-2 TOXIN ÉS DEOXINIVALENOL EGYÜTTES HATÁSA A LIPIDPEROXIDÁCIÓRA ÉS A GLUTATION-REDOX RENDSZERRE, VALAMINT ANNAK SZABÁLYOZÁSÁRA BROJLERCSIRKÉBEN Mézes Miklós a,b, Pelyhe Csilla b, Kövesi Benjámin a, Zándoki
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Ferrotone 100% természetes forrásvízből nyert vastartalmú étrendkiegészítő
 Ferrotone 100% természetes forrásvízből nyert vastartalmú étrendkiegészítő Miért fontos a szervezetnek a vas? A vas számos enzim összetevője, így fontos kémiai reakciókban vesz részt. A hemoglobin és a
Ferrotone 100% természetes forrásvízből nyert vastartalmú étrendkiegészítő Miért fontos a szervezetnek a vas? A vas számos enzim összetevője, így fontos kémiai reakciókban vesz részt. A hemoglobin és a
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Tények a Goji bogyóról:
 Tények a Goji bogyóról: 19 aminosavat (a fehérjék építőkövei) tartalmaz, melyek közül 8 esszenciális, azaz nélkülözhetelen az élethez. 21 nyomelemet tartalmaz, köztük germániumot, amely ritkán fordul elő
Tények a Goji bogyóról: 19 aminosavat (a fehérjék építőkövei) tartalmaz, melyek közül 8 esszenciális, azaz nélkülözhetelen az élethez. 21 nyomelemet tartalmaz, köztük germániumot, amely ritkán fordul elő
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Jelutak. 2. A jelutak komponensei Egy tipikus jelösvény sémája. 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
AZ OXIDATÍV STRESSZ ÉS AZ ANTIOXIDÁNS VÉDELMI
 PH.D. ÉRTEKEZÉS AZ OXIDATÍV STRESSZ ÉS AZ ANTIOXIDÁNS VÉDELMI RENDSZER VIZSGÁLATA NEHÉZFÉM KEZELÉST KÖVETŐEN PONTYBAN ÉS STREPTOZOTOCIN-INDUKÁLTA DIABÉTESZES PATKÁNY MODELLBEN JANCSÓ ZSANETT TÉMAVEZETŐ:
PH.D. ÉRTEKEZÉS AZ OXIDATÍV STRESSZ ÉS AZ ANTIOXIDÁNS VÉDELMI RENDSZER VIZSGÁLATA NEHÉZFÉM KEZELÉST KÖVETŐEN PONTYBAN ÉS STREPTOZOTOCIN-INDUKÁLTA DIABÉTESZES PATKÁNY MODELLBEN JANCSÓ ZSANETT TÉMAVEZETŐ:
Apoptózis. 1. Bevezetés 2. Külső jelút 3. Belső jelút
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Növényélettani Gyakorlatok A légzés vizsgálata
 Növényélettani Gyakorlatok A légzés vizsgálata /Bevezető/ Fotoszintézis Fény-szakasz: O 2, NADPH, ATP Sötétszakasz: Cellulóz keményítő C 5 2 C 3 (-COOH) 2 C 3 (-CHO) CO 2 Nukleotid/nukleinsav anyagcsere
Növényélettani Gyakorlatok A légzés vizsgálata /Bevezető/ Fotoszintézis Fény-szakasz: O 2, NADPH, ATP Sötétszakasz: Cellulóz keményítő C 5 2 C 3 (-COOH) 2 C 3 (-CHO) CO 2 Nukleotid/nukleinsav anyagcsere
Nyilvános Értékelő Jelentés. C-vitamin Béres. 1000 mg filmtabletta. (aszkorbinsav)
 Nyilvános Értékelő Jelentés Gyógyszernév: (aszkorbinsav) Nemzeti eljárás A forgalomba hozatali engedély jogosultja: Béres Gyógyszergyár Zrt. Kelt: 2016. március 10. TARTALOM NEM EGÉSZSÉGÜGYI SZAKEMBEREKNEK
Nyilvános Értékelő Jelentés Gyógyszernév: (aszkorbinsav) Nemzeti eljárás A forgalomba hozatali engedély jogosultja: Béres Gyógyszergyár Zrt. Kelt: 2016. március 10. TARTALOM NEM EGÉSZSÉGÜGYI SZAKEMBEREKNEK
nyomelem, étrendi forrásainak vizsgálata Dr. Gergely Valéria Bükfürdő 2010.
 A Szelén, mint esszenciális nyomelem, étrendi forrásainak vizsgálata Dr. Gergely Valéria Bükfürdő 2010. A Szelén előfordulása a környezetünkben A szelén esszenciális mikroelem, azonban élettani hatása
A Szelén, mint esszenciális nyomelem, étrendi forrásainak vizsgálata Dr. Gergely Valéria Bükfürdő 2010. A Szelén előfordulása a környezetünkben A szelén esszenciális mikroelem, azonban élettani hatása
A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN. Somogyi János -- Vér Ágota Első rész
 A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN Somogyi János -- Vér Ágota Első rész Már több mint 200 éve ismert, hogy szöveteink és sejtjeink zöme oxigént fogyaszt. Hosszú ideig azt hitték azonban, hogy
A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN Somogyi János -- Vér Ágota Első rész Már több mint 200 éve ismert, hogy szöveteink és sejtjeink zöme oxigént fogyaszt. Hosszú ideig azt hitték azonban, hogy
A -tól Z -ig. Koleszterin Kisokos
 A -tól Z -ig Koleszterin Kisokos A SZÍV EGÉSZSÉGÉÉRT Szívügyek Magyarországon Hazánkban minden második ember szív- és érrendszerrel kapcsolatos betegség következtében veszíti életét*, ez Magyarországon
A -tól Z -ig Koleszterin Kisokos A SZÍV EGÉSZSÉGÉÉRT Szívügyek Magyarországon Hazánkban minden második ember szív- és érrendszerrel kapcsolatos betegség következtében veszíti életét*, ez Magyarországon
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az Etanol Metabolizmusa és az Alkoholos Májkárosodás Biokémiája
 Az Etanol Metabolizmusa és az Alkoholos Májkárosodás Biokémiája A) Az etanol metabolizmusa emberben A metabolizmus átlagos sebessége: 10 g etanol/óra Az etanol energiatartalma: 30 kj/g (7,1 kcal/g) Az
Az Etanol Metabolizmusa és az Alkoholos Májkárosodás Biokémiája A) Az etanol metabolizmusa emberben A metabolizmus átlagos sebessége: 10 g etanol/óra Az etanol energiatartalma: 30 kj/g (7,1 kcal/g) Az
A citoszolikus NADH mitokondriumba jutása
 A citoszolikus NADH mitokondriumba jutása Energiaforrásaink Fototróf: fotoszintetizáló élőlények, szerves vegyületeket állítanak elő napenergia segítségével (a fényenergiát kémiai energiává alakítják át)
A citoszolikus NADH mitokondriumba jutása Energiaforrásaink Fototróf: fotoszintetizáló élőlények, szerves vegyületeket állítanak elő napenergia segítségével (a fényenergiát kémiai energiává alakítják át)
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
A koleszterin-anyagcsere szabályozása (Csala Miklós)
 A koleszterin-anyagcsere szabályozása (Csala Miklós) A koleszterin fontos építőeleme az emberi sejteknek, fontos szerepe van a biológiai membránok fluiditásának szabályozásában. E mellett hormonok és epesavak
A koleszterin-anyagcsere szabályozása (Csala Miklós) A koleszterin fontos építőeleme az emberi sejteknek, fontos szerepe van a biológiai membránok fluiditásának szabályozásában. E mellett hormonok és epesavak
Az endomembránrendszer részei.
 Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
A koleszterin és az epesavak bioszintézise
 A koleszterin és az epesavak bioszintézise Koleszterin A koleszterin a biológia legkitüntetettebb kis molekulája. Tizenhárom Nobel-díjat ítéltek oda azon tudósoknak, aki karrierjük legnagyobb részét a
A koleszterin és az epesavak bioszintézise Koleszterin A koleszterin a biológia legkitüntetettebb kis molekulája. Tizenhárom Nobel-díjat ítéltek oda azon tudósoknak, aki karrierjük legnagyobb részét a
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Fejezet a Gulyás Méhészet által összeállított Méhészeti tudástár mézfogyasztóknak (2015) ismeretanyagból. A méz. összetétele és élettani hatása
 A méz összetétele és élettani hatása A méz a növények nektárjából a méhek által előállított termék. A nektár a növények kiválasztási folyamatai során keletkezik, híg cukortartalmú oldat, amely a méheket
A méz összetétele és élettani hatása A méz a növények nektárjából a méhek által előállított termék. A nektár a növények kiválasztási folyamatai során keletkezik, híg cukortartalmú oldat, amely a méheket
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Endokrinológia. Közös jellemzők: nincs kivezetőcső, nincs végkamra - hámsejt csoportosulások. váladékuk a hormon
 Közös jellemzők: Endokrinológia nincs kivezetőcső, nincs végkamra - hámsejt csoportosulások váladékuk a hormon váladékukat a vér szállítja el - bő vérellátás távoli szervekre fejtik ki hatásukat (legtöbbször)
Közös jellemzők: Endokrinológia nincs kivezetőcső, nincs végkamra - hámsejt csoportosulások váladékuk a hormon váladékukat a vér szállítja el - bő vérellátás távoli szervekre fejtik ki hatásukat (legtöbbször)
OTKA ZÁRÓJELENTÉS
 NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
Az Oxidatív stressz hatása a PIBF receptor alegységek összeszerelődésére.
 Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Stressz és a reaktív oxigénformák
 Stressz és a reaktív oxigénformák Oxigénformák A földi élet egyik paradoxonja: Az oxigén, amely az aerob életfolyamatokhoz szükséges, és a az energia termelés és légzés alapvetı feltétele, sok betegség
Stressz és a reaktív oxigénformák Oxigénformák A földi élet egyik paradoxonja: Az oxigén, amely az aerob életfolyamatokhoz szükséges, és a az energia termelés és légzés alapvetı feltétele, sok betegség
Anaerob fermentált szennyvíziszap jellemzése enzimaktivitás-mérésekkel
 Eötvös Loránd Tudományegyetem Természettudományi Kar Környezettudományi Centrum Anaerob fermentált szennyvíziszap jellemzése enzimaktivitás-mérésekkel készítette: Felföldi Edit környezettudomány szakos
Eötvös Loránd Tudományegyetem Természettudományi Kar Környezettudományi Centrum Anaerob fermentált szennyvíziszap jellemzése enzimaktivitás-mérésekkel készítette: Felföldi Edit környezettudomány szakos
Integráció. Csala Miklós. Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet
 Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
