3. fejezet. A nyelôcsô betegségei Szerkesztette Wittmann Tibor. Rövid tartalomjegyzék
|
|
|
- György Rezső Vincze
- 8 évvel ezelőtt
- Látták:
Átírás
1 1. fejezet 2. A nyelôcsô betegségei Szerkesztette Wittmann Tibor Rövid tartalomjegyzék A nyelőcső anatómiája, élettana, fejlődési rendellenességei és strukturális eltérései Gastrooesophagealis refluxbetegség A nyelőcső egyéb motilitászavarai A nyelőcső funkcionális betegségei A nyelőcső egyéb betegségei A nyelőcső daganatai
2 108 A nyelôcsô betegségei 109 A nyelôcsô anatómiája, élettana, fejlôdési rendellenességei és strukturális eltérései Bevezetés A nyelőcső dinamikus működése révén jut el a táplálék a garatból a gyomorba; böfögés és hányás esetén viszont a levegő, illetve a gyomortartalom gyors kiürítését szolgálja. Anatómiailag nyaki, mellkasi és hasi szakaszát különböztetjük meg. Proximalis és distalis végének anatómiailag összetett struktúrái sphincterfunkciót látnak el, és megakadályozzák, hogy légvételek alkalmával a mellkasban keletkező vákuum hatására gyomortartalom, illetve levegő kerüljön a nyelőcsőbe. A klinikai gyakorlatban leggyakoribb nyelőcsőbetegségek is a hasi és nyaki szakaszt alkotó elemek strukturális károsodásainak vagy működési elégtelenségeinek következtében alakulnak ki. A nyelőcső anatómiája A nyelőcső fejlődésanatómiája Az embrionális fejlődés 12. hetére már kialakul a primitív gasztrointesztinális traktus elő-, közép- és utóbélformában. A mesoderma és az endoderma által termelt növekedési faktorok vezérlik azokat az epithelomesenchymalis kölcsönhatásokat, amelyek következtében a dúcléceredetű sejtek meghatározott tengelyek mentén a primordiális nyelőcsőbe vándorolnak. Az előbél ventralis felszínén az első 4 hétben kialakuló tracheobronchialis diverticulum a későbbiek során megnyúlik, és a benne képződő septum leválasztja a primitív respirációs traktust. A gyorsan fejlődő luminális epithelium vakuolizációs folyamata során a 10. hétre kialakul a ciliaris hámmal 3-1. ábra. A nyelôcsô tájanatómiája fedett nyelőcsőlumen. A csillószőrös hám átalakulása laphámmá az embrionális fejlődés 4. hónapjában kezdődik, és a születésig tart. A csillószőrös hám reziduális elemeiből a nyelőcső proximalis és distalis részén a nyelőcső mirigyei fejlődnek ki. A 9. hétre az előbélben a mesenchymából kifejlődik a körkörös és hosszanti simaizomzat és az alsó nyelőcsősphincter (LES: lower esophageal sphincter). A dúcléceredetű sejtek a 4-7. embrionális héten rostrocaudalis, a 6. héttől pedig centripetális irányban is vándorolva, kialakítják a myentericus, illetve submucosus plexusokat. Kolinészteráz-aktivitás a héten már kimutatható, de differenciálódott ganglionsejtek csak a 1 héten láthatók. A 7. héten a submucosában megjelennek a vérerek. A nyelőcső felső harmadát képező harántcsíkolt izom és a felső oesophagealis sphincter a 4-6. brachialis ívek mesenchymájából fejlődik ki. Fejlődéstanilag érthető, hogy a beidegzést is az ugyancsak a brachialis ívekből származó vagus ágai biztosítják. A gyakorlati szempontból igen kritikus gastrooesophagealis junkció embrionális eredete továbbra is vitatott, de valószínűleg a gyomorfundusból származik. A nyelőcső középső, kevert, sima és harántcsíkolt izomzata két eltérő differenciálódási folyamat eredményeként jön létre. A pacemakerfunkcióval rendelkező mesenchymalis eredetű Cajal-féle intersticialis sejtek (ICC) a hét között hozzák létre a myentericus plexusban a hálózatukat. Primitív perisztaltikus aktivitás már az első trimeszterben is regisztrálható, illetve ultrahangvizsgálattal is látható, de propulzív perisztaltika az alsó és felső záróizom szimultán működésével csak a második trimeszterben mutatható ki. Megjegyzendő azonban, hogy a nyelőcső perisztaltikus aktivitása újszülöttkorban is éretlen, gyakoriak a regurgitációk, alacsony a LES-nyomás, amely a felnőttkori értéket 3-6 hetes korban éri el. A nyelőcső tájanatómiája Nyaki, mellkasi és hasi nyelőcsőszakaszt különböztetünk meg, amelyek funkcionális szempontból megfelelnek a felső nyelőcsősphincternek, a nyelőcsőtestnek és a cardiának (3-1. ábra). A nyelőcső nyaki szakasza Izbéki Ferenc A 4-5 cm hosszú cervicalis szakasz a trachea mögött, a carotisartériák között helyezkedik el, az 5-6. nyakcsigolyák közötti rés magasságában, a pharyngooesophagealis junkcióval kezdődik, és a manubrium sterni magasságáig tart. A nyelőcső cervicalis szakaszának anatómiailag összetett, funkcionális zónáját nevezzük felső nyelőcsősphincternek (UES), amely a fiziológiai folyamatok igénye szerint lezárja vagy egybenyitja a nyelőcső lumene és a garat által létrehozott anatómiai kompartmenteket. Az UES-t zárva tartó, folyamatos izomtónus lényegében megfelel a felső oesophagealis magasnyomású zónának (UEHPZ), amelynek anatómiai alapját elsősorban a musculus cricopharyngeus képezi, de jelentősen hozzájárul a nyelőcső cervicális szakaszának izomzata és a musculus constrictor pharyngis inferior, valamint a környező struktúrák is. Az UEHPZ nyomásának csúcsa a m. constrictor pharyngis inferior caudalis szélénél detektálható. Az UES nyitódása az izomtónust létrehozó izmok ellazulásának, a gége és a nyelőcső egymástól történő eltávolodásának, valamint az áthaladó bolus mechanikus hatásának az eredménye. A gége és a nyelőcső egymástól való eltávolítását elsősorban az UEHPZ-t képező izmok végzik. A m. constrictor pharyngis inferior ferdén futó rostjai és a m. cricopharyngeus harántrostjai között kialakuló nevezetes háromszögalakú területet Killian-féle háromszögnek nevezzük, ahol a Zenker-féle diverticulum képződik. Másik potenciálisan gyenge terület a cricopharyngeus izom alatt lévő Laimer Haeckermann-féle háromszög, ahol a Laimer-féle diverticulum keletkezik. A nyelőcső mellkasi szakasza A mellkasi szakasz a manubrium sterni felső részétől a bal főhörgő mögött, az aortaívtől jobbra, majd az aorta előtt halad a 10. hátcsigolya magasságában lévő hiatus oesophageushoz, amelynek peremét a rekeszszárak képezik. Endoszkóppal a metszőfogaktól mérve, a nyelőcsőtest cm-re kezdődik, és férfiakban átlagosan 40 cm-nél, nőkben 37 cm-nél ér véget. Férfiakban a metszőfogak és a cardia közötti távolság cm, nőkben cm között változhat. Radiológiailag vizsgálva, a cardia helyzete a 11. hátcsigolya alsó szélének bal oldalán meglehetősen állandó. A nyelőcső és a rekeszszárak közötti dinamikus összeköttetést a phrenooesophagealis membrán elasztikus kollagénrostjai biztosítják. A phrenooesophagealis membrán a laphám-hengerhám átmenet magasságában kapcsolódik a nyelőcsőhöz, tehát a Z- vonal axiális pozíciója a hiatus diaphragmaticusban vagy kissé distalisan található. Megjegyzendő azonban, hogy a Z-vonal helyzete nem állandó, így például perisztaltikus kontrakciók (nyelés) alkalmával jelentős orális irányú elmozdulás figyelhető meg (fiziológiás herniáció). A nyelőcső hasi szakasza A cardia a nyelőcső és gyomor találkozásánál azt a funkcionális egységet alkotó struktúrát jelenti, amelyet alsó nyelőcsősphincternek (LES) is nevezünk. Anatómiai alapját a nyelőcső distalis végének körkörös és hosszanti izomrétegei (intrinsic sphincter) és a rekeszszárak (extrinsic sphincter; diaphragma sphincter) képezik. A cardia sajátos izomelrendeződésében a belső izomréteg rostjainak bizonyos mértékű megvastagodása kimutatható, de hagyományos értelemben vett körkörös sphinctert nem alkotnak. Az itt lévő izomsejtek elektronmikroszkóppal vizsgálva nagyobbak, több mitochondriumot és endoplazmatikus reticulumot tartalmaznak; kevesebb a gap juntion, de a sejtek között több kötőszövet található, mint a nyelőcsőtestben. Továbbá strukturális fehérje-összetételük is eltér a nyelőcsőtest körkörös izomzatáétól, mivel több α-aktint, bázikus, esszenciális könnyű láncot (LC17b) és kevesebb caldesmont tartalmaznak. A kisgörbületi oldalon az intrinsic sphinctert alkotó rövidebb izomkötegek egy része (clasp fibers) nem zárul gyűrűkké, hanem C-betűt formázva ventralisan, illetve dorsalisan nyitottak. Az intrinsic sphinctert alkotó rostok másik részét a cardia nagygörbületi oldalán lovagló, hosszabb, parittyaszerű izomkötegek (sling fibers) képezik, amelyek ferdén lefelé haladva belevegyülnek a gyomor elülső és hátulsó falának belső izomrétegébe. A parittyaszerű rostok hozzák létre a nyelőcső és a gyomorfundus közötti behúzódást, az ún. His-szöget. Ennek megfelelően, a cardiának az intraabdominalis szakasza billentyűszerűen funkcionál (Gubaroff-féle billentyű; flap valve), és akadályozza a gyomortartalom regurgitációját. A C-alakú és a parittyaszerű rostok két egymásra merőlegesen álló U-formátumot hoznak létre, és ez a térbeli elrendeződés képezi a LES-ben a nyomásprofil radiális aszimmetriájának egyik alapját. Megjegyzendő, hogy a cardia ezen két ferde irányú izomcsoportja, valamint a gyomor ferde izomrostjainak a motoros beidegzése és neurohumoralis reaktivitása is eltérő. Az intrinsic sphinctert parittyaszerűen veszik körül a rekeszszárak harántcsíkolt izomkötegei, amelyet diaphragma sphincternek nevezünk. A nyelőcső mikroszkópos anatómiája A nyelőcső fala négy rétegből áll: mucosa, submucosa, muscularis propria és adventitia. Serosaborítása tehát nincs. A vastag nyálkahártya hosszanti redőket alkot. Többrétegű, nem elszarusodó laphámborításának proximalisan élénkebb gyöngyházfénye distalisan halványabb árnyalatúvá válik, és a Z-vonalban élesen elhatárolódik a gyomorhengerhám lazacvörös színétől. A μ vastag epitheliumot réteg lapos sejt alkotja, amelyek a legalsó rétegben elhelyezkedő bazofil sejtekből, mintegy 10 nap ciklusidővel, folyamatosan megújulnak. Az epitheliumot vékony kötőszöveti réteg (lamina propria) kapcsolja a nyálkahártya saját izomrétegéhez, a muscularis mucosae-hoz. Ez a vékony (100 μ), túlnyo-
3 110 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 111 móan hosszanti, distalisan kissé vastagabb, helyenként szabálytalan elrendeződésű simaizomrostokból álló réteg elválasztja a mucosát a submucosától. A nyelőcső lamina propriájában lévő, az epitheliumon áttűnő, sövényszerű elrendeződésű ereket palisad vénáknak nevezik, amelyek a gyomor és a nyelőcső határának endoszkópos meghatározását is szolgálják. A submucosa (400 μ) kötőszövete idegi és vaszkuláris plexusokat, limfocitákat, plazmasejteket, valamint mirigyeket tartalmaz. A szőlőfürtszerű mirigyek által termelt nyák védi a nyelőcsövet. A nyelőcső izomzata a külső hosszanti és a belső körkörös rétegből áll. A körkörös 500 μ, a hosszanti 400 μ vastag. A felső 5-33%-nyi szakasz kizárólag harántcsíkolt izomból, az alsó egyharmad tisztán simaizomból áll, a köztes átmeneti zóna vegyesen tartalmaz harántcsíkolt és simaizomrostokat. A nyelőcső külső, hosszanti izomrétegét lateralisan a garatizmok, ventralisan pedig a pajzsporchoz tapadó izomkötegek egyesülésének folytatódása képezi. A körkörös izomréteg a hypopharynx alsó konstriktor izmából indul ki, és kezdeti szakaszán haránt, majd a nyelőcsőtestben ferde irányban haladó rostjai a rekeszizom magasságában létrehozzák az alsó nyelőcsősphinctert. A harántcsíkolt és a simaizmot tartalmazó nyelőcsőszakaszok találkozásánál levő területet átmeneti zónának nevezzük. A külső, laza kötőszövetből álló, ereket, idegeket és nyirokelvezetést tartalmazó fibrotikus réteg (adventitia) borítja és kapcsolja a nyelőcsövet a környezetéhez. A 300 μ vastag adventitiával együtt a nyelőcső falvastagsága mintegy 2,2 mm. A nyelőcső vérellátása és nyirokkeringése A nyelőcső bőséges, szegmentális, sokszoros anasztomózissal rendelkező vérellátását az a. thryroidea inferiortól, a páros aortaágaktól, az arteria gastrica sinistratól és a bal arteria phrenicától kapja. A vénás elvezetés szintén szegmentális; a proximalis és distalis rész vénás vére az azygosrendszerbe ömlik, de a vena portae-ba ömlő vena gastrica sinistra aminek jelentősége portalis hypertensio esetén különösen nagy a nyelőcső középső harmadától is kap vénás vért. A nyelőcső nyirokelvezetése az endothelialis szövetközti terek hálózatában kezdődik, és elektronmikroszkóppal a nyálkahártya alsóbb rétegeiben és a submucosában azonosíthatók nyirokkapillárisok. A nyelőcső harántcsíkolt és simaizomzatának nyirokelvezetése eltérő: az előbbi a mély nyaki nyirokcsomókon keresztül a ductus thoracicusba, az utóbbi a superior és posterior mediastinalis nyirokcsomókba vezet. A nyelőcső alsó harmadából a gyomor és coeliacus nyirokcsomók felé is történik nyirokelvezetés. A három nyirokelvezetés között számos összeköttetés áll fenn. A nyelőcső beidegzése A nyelőcső intrinsic beidegzése A nyelőcső intrinsic beidegzését az egymással összeköttetésben álló myentericus (Auerbach) és submucosus (Meissner) plexusok ganglionokba szerveződő neuronjai alkotják. A submucosus plexus a nyelőcsőben gyér. A körkörös és hosszanti izomréteg motoros beidegzését a közöttük elhelyezkedő myentericus plexus biztosítja. A simaizomzatban a myentericus plexus ganglionjainak száma lényegesen nagyobb, mint a harántcsíkolt izomzat területén, és az innervációban is elsődleges szerepet játszanak. A harántcsíkolt izomzatban található myentericus ganglionok szerepe jórészt tisztázatlan (a harántcsíkolt izomzatot a n. vagus a motoros véglemezek nikotinos receptorai révén idegzi be). A myentericus plexusban számos neurotranszmitter kimutatható, de a főszerepet az M 3 -receptorok által közvetített, serkentő hatású kolinerg, valamint a nitrogén-monoxid (NO) által közvetített gátló hatás játssza. Az acetilkolin a körkörös simaizomzatban kalcium-beáramlást okoz, és így aktíválja a kalmodulin-, miozinkönnyűlánc-kinázokat, ami kontrakciót eredményez. Az elsődleges gátló transzmitter a nnos által termelt NO, amely cgmp-dependens mechanizmus révén fejti ki hatását. A vazoaktív intesztinális peptid (VIP) szabályozó szerepe azáltal jut érvényre, hogy simaizom-relaxáló hatása mellett fokozza az NO szintézisét is. A nyelőcsőben az ATP nem szerepel gátló transzmitterként. Az intrinsic afferens idegek a specializált mechano-, kemo- vagy termoreceptoraikkal felvett információt az interneuronokhoz közvetítik, amit azok oralis vagy aboralis irányba továbbvezetnek. A sav a nyelőcső intrinsic primer afferens neuronjain lévő ioncsatornákat (TRPV1: transiens receptor potential vanilloid 1, ASIC: acid sensing ion channels) aktíválja. A nyelőcső Cajal-féle intersticiális sejtjei gap junction - nal kapcsolódnak az idegekhez és a simaizomzathoz egyaránt, de szerepük az ingerületképzésben és vezetésben kevéssé tisztázott, mint a tápcsatorna egyéb szakaszaiban. A nyelőcső extrinsic beidegzése Az extrinsic beidegzést a n. vagus és a spinalis idegek biztosítják. A motoros beidegzés túlnyomó részét a n. vagus adja. A felső sphinctert és a harántcsíkolt izmot beidegző idegrostok a nucleus ambiguusból, míg a simaizomzatot és az alsó sphinctert ellátó rostok a dorsalis vagusmagból származnak. A simaizmot a vagusrostok a ganglionokban lévő neuronok közvetítésével indirekt módon idegzik be, ellentétben a harántcsíkolt izommal, amelyek a motoros véglemezeken direkt innervációban részesülnek. Az extrinsic afferens beidegzést biztosító vagusrostok sejttestjei a ganglion nodosumban találhatók, és a simaizmokból a nucleus solitariushoz a feszülés, a nyálkahártyából az ozmotikus, kémiai, hő- és mechanikus ingerek által keltett ingerületet szállítják; a viscerális fájdalom közvetítésében nincs jelentős szerepük, csupán a feszülésreceptorokra gyakorolt nyomás okozhat fájdalomérzetet. Ezeket a polimodális természetű ingereket a vagalis afferens idegek specializált intraganglionalis, laminalis (IGLE) és intramuscularis array (IMA) végződéseikkel érzékelik; az utóbbiak elsősorban a sphincterekben helyezkednek el. A savérzékelés az intrinsic primer afferens idegekhez hasonlóan a vagalis és spinalis afferenseken is a TRPV1 és ASIC révén történik. A spinalis extrinsic szenzoros idegek sejtestjei a gerincvelőben találhatók, a hátsó gyöki ganglionokban, ily módon az agytörzsi gracilis és cuneatus magvakban átkapcsolódva a thalamusba, az insularis és kérgi érzőközpontokhoz szállítanak nociceptív információt. A cervicalis és thoracalis (T1-T10) szimpatikus láncból származó spinalis motoros beidegzés a nyelőcső ereit és a sphinctereket kontrahálja. A nyelőcső simaizomzata direkt szimpatikus beidegzésben szinte egyáltalán nem részesül, de a myentericus plexus ganglionjainak közvetítésével hatásukra a nyelőcsőfal izomzata ellazul. A cardia beidegzése és neurohumoralis szabályozása Az alsó oesophagealis sphincter beidegzése különös jelentőségű. A LES extrinsic motoros beidegzését is a n. vagus dorsalis motoros magjából származó rostok biztosítják. A kolinerg rostok aszimmetrikus eloszlásában tükröződik a LES aszimmetrikus nyomásprofilja: az atropinérzékeny nyugalmi nyomás 80%-a bal oldalon (a parittyarostoknak megfelelően), míg 50%-ban jobb oldalon detektálható. Az intrinsic serkentő myentericus neuronok aktíválódása acetilkolin és P-anyag (SP) közvetítésével kontrakciót okoz, míg az NO és VIP által közvetített inhibítoros hatás relaxációt eredményez. A felső és alsó nyaki ganglionokból származó szimpatikus beidegzés a LES motoros működésére nem hat direkt módon; moduláló hatása révén elsősorban az izomtónust befolyásolja. Így szimpatikus hatásra az α-adrenerg receptorok közvetítésével LES-kontrakció, míg β-adrenerg ingerre LES-ellazulás következik be. Ez utóbbi hatást β1-, β2- és β3-receptorok közvetítik. A LESrégió Cajal-féle sejtjei is fokozzák a tónust. A serkentő és gátló neuronok közvetítésével és/vagy közvetlenül a körkörös izomzatra hatva számos egyéb transzmitter és neuroenterohormon is kiválthat LESkontrakciót vagy relaxációt. Így a dopamin közvetlenül a simaizomzatra gyakorolt közvetlen hatással D 1 -receptoron kontrakciót, D 2 -receptoron relaxációt okoz. Szintén közvetlenül a simaizomzatra hatva a hisztamin (H 1 ), a PGF 2α, a gasztrin, a CCK, a szerotonin, a neurotenzin és a galanin kontrakciót, a PGE 1,2, a glukagon, a szekretin, az NO, a VIP és indirekt hatásmód révén a CCK is relaxációt okoz. Részben direkt, részben neurális közvetítéssel okoz LES-relaxációt a CGRP és kontrakciót a motilin és az SP. A GIP LES-relaxációt és a somatostatin LES-kontrakciót kiváltó hatásának mechanizmusa még nem ismert. A LES szabályozását végző agytörzsi központok szoros kapcsolatban állnak a formatio reticularisban lévő nyelési központtal (SPG: swallowing pattern generator). A vagus dorsalis motoros magjában azonosítható a LES topografikus reprezentációja; rostralisan serkentő, caudalisan gátló hatású neuronok találhatók, amelyek acetilkolint, NO-ot, dopamint és adrenalint tartalmaznak. Ide az afferens információ a nucleus tractus solitariusból (NTS) interneuronok közvetítésével jut el. A perisztaltika nélkül bekövetkező tranziens alsó oesophagealis sphincter relaxációnak (TLESR) nevezett LES-ellazulás a gátló GA- BA-B- vagy CB 1 -agonista hatására a NTS-ban és a dorsalis motoros vagusmagvakban (DMNV) lévő neuronok útján érvényesül. A nyelőcsőben keltett ingerület az agytörzsön és thalamuson át az agykéregbe jut, és különböző agyi területeken, mint pl. a másodlagos érző és mozgató kérgi areákban, a parietooccipitalis kéregben, az elülső és hátulsó gyrus cingulatusban, az insulában és a prefrontalis kérgi területekben PET- és fmri-vizsgálatokkal is kimutatható aktíválódást vált ki. A diaphragmaticus sphincter izomrostjait a nervus phrenicus idegzi be, de gátló motoros innervációt kap a nyelőcső nitrerg myentericus ganglionjaitól is. A nyelőcső élettana A nyelés szorosan szabályozott folyamatában valósul meg a nyelőcső elsődleges élettani feladata, amelyet a nyúltvelőben lévő nyelésmintázat-generátornak (SPG) nevezett központ vezérel, az agykéreg pedig moduláló hatást gyakorol. Ez az agytörzsi neuronhálózat a szájból és garatból kiinduló ingerek hatására kezdeményezi a nyelést, időzíti a nyelési szekvenciákat, és biztosítja a nyelés ritmusosságát. A nyelés mechanizmusa A nyelés összerendezett reflexes folyamatának részei: az oralis fázis, a pharyngealis perisztaltika, az UES-relaxáció, a nyelőcső-perisztaltika és a LES-relaxáció. A nyelés kezdetét az elődleges nyelésizomnak is nevezett musculus myohyoideus összehúzódása jelzi. A nyelőcső fiziológiás motoros működése a nyelések alatti és a nyelések közötti időszakokra osztható. A nyelés során a nyelőcső felső sphinctere nyílik, az alsó ellazul, és a nyelőcsőtest szekvenciális, perisztaltikus kontrakciói továbbítják a falatot.
4 112 Gaszt ro en te ro ló Gia A nyelôcsô betegségei ábra. Nyelôcsô-manometria folyadékperfúziós regisztrátuma A nyelőcsőben keletkező nyeléshullámok következő típusait különböztetjük meg: Primer perisztaltikának a garatban kezdődő, nyelés által kiváltott, progresszív kontraktilis aktivitást nevezzük. Szekunder perisztaltikának nevezzük a nyelőcsőtest körkörös izomzatának bármely okból bekövetkező tágulása (feszülése) által keltett progresszív kontrakciós hullámokat, amelyeket nyelés, azaz pharyngealis kontrakció nem előz meg. Tercier hullámoknak viszont a szimultán fellépő, nem perisztaltikus kontrakciókat nevezzük, amelyek a nyelőcső különböző pontjain spontán vagy nyelés hatására, izoláltan vagy repetitív módon jelenhetnek meg. A tercier kontrakciók fogalma eredetileg dugóhúzó-nyelőcsőben báriumos nyeletés során látott összehúzódásokra vonatkozott fiziológiás körülmények között nem létező jelenség. A nyelőcső-perisztaltika vizsgálatának arany standard módszere a nyelőcső-manometria. A nyelőcső működésének megítélésére elsősorban a kontrakciók amplitúdóját (Hgmm), tartamát (másodperc), haladási sebességét (cm/másodperc), a sphincterekben az alapnyomást (Hgmm), a relaxáció mértékét (%) és tartamát (másodperc) vesszük figyelembe. A mérés történhet szilárd intraluminalis, nyomásérzékelő transzducerek alkalmazásával vagy folyadékperfúziós katéter használatával, amikor a nyomást a nyelőcsövön kívül lévő transzducerek érzékelik. A nyomásgörbék értékelése számítógép segítségével történik. A mért nyomásértékek normálértékei jelentős mértékben függenek az alkalmazott metodikától. A mérési pontok számának növelése lehetővé teszi a nyelőcső fiziológiás és kóros kontrakcióinak pontosabb jellemzését; az erre kifejlesztett módszert a nagy felbontású manometriának (HRM: high resolution manometry) nevezzük. Folyadékperfúziós technikával készített regisztrátum látható a 3-2. ábrán. A fentebb ismertetett anatómiai jellegzetesség miatt az UES nyugalmi nyomásmegoszlása jelentősen aszimmetrikus, Hgmm között változhat. Az UES nyílásához a záróizmok folyamatos idegi aktíválásának a megszűnése és a nyitó izmok aktíválódása szükséges, ami a nyelés kezdetekor 0,2-0,3 másodpercen belül bekövetkezik; a gége megemelkedésével az UES-nyomás csökken, és a falat 1 másodperc múlva eléri a nyelőcsőtestet. Az UES-ben a falat áthaladását követően egy rövid neurogén utókontrakció jelentkezik. A simaizomzatban a primer perisztaltika intrinsic módon jön létre, de kezdeményezheti a központi idegrendszer is, amely egyébként módosíthatja is a perisztaltikus tevékenységet. Nyugalmi helyzetben a nyelőcsőtest tónusa csekély, az intrathoracalis nyomástól függően a lumenben valamennyi levegő is lehet. Álló helyzetben történő radiológiai vizsgálat során a báriumos nyeletés alkalmával a folyadék, lényegében a gravitáció hatására, gyorsan lejut a gyomorba, de a falra tapadó maradék báriumot csak az ismétlődő perisztaltikus kontrakciók tisztítják le; a szolid bolus viszont lassan, aktív perisztaltikus kontrakciók által jut a gyomorba. Fekvő helyzetben a folyadék gyomorba jutása is lassúbb, lényegében aktív perisztaltika révén következik be. A körkörös izomzat összehúzódása lument elzáró perisztaltikus kontrakciót eredményez, amelynek időtartama a nyelőcső proximalis részén 2, distalisan 5 7 másodperc között változik. A perisztaltikus kontrakció terjedési sebessége is változik: a proximalis részen 3 cm/ sec, a középsőn 5 cm/sec és distalisan 2,5 cm/sec; tehát egy perisztaltikus hullám a nyelőcsövön 5-10 másodperc alatt halad végig. Standard körülmények között, kortól függetlenül, egy egyénben a perisztaltikus hullámok karaktere meglehetősen állandó. Ugyanakkor az amplitúdóját, időtartamát és haladási sebességét számos körülmény befolyásolja: függ az adott nyelőcsőszakasz helyzetétől, a testhelyzettől, a bolus konzisztenciájától, méretétől, hőmérsékletétől és attól is, hogy mekkora ellenállással szemben halad végig a nyelőcsőben. A nyeléshullámok amplitúdója a nyelőcső proximalis és középső harmadának határán az úgynevezett átmeneti zónában a legalacsonyabb (kb Hgmm). Ettől mind proximálisabban (40-60 Hgmm), mind distalisan magasabb értékek mérhetők. Distalis irányba haladva az amplitúdó a cardiáig fokozatosan növekszik, legmagasabb értéke közvetlenül a záróizom felett, átlagosan Hgmm között van. A kontrakciós hullámok időtartama distalis irányban növekvő, a terjedési sebességük pedig fokozatosan csökken. Fekvő helyzetben, illetve folyadéknyelés esetén a kontrakciók ereje nagyobb, mint amekkorát a száraz nyelés eredményez. A nagyobb volumenű bolus szintén erősebb kontrakciót vált ki. Az abdominalis nyomás növekedése (Valsalva) vagy a kimeneti obstrukció lassítja a nyelőcső-kontrakció terjedési sebességét. A primer perisztaltika általában hatékonyan továbbítja az ételt a nyelőcsőből a gyomorba. A 30 Hgmm-nél alacsonyabb kontrakciós nyomás esetén a perisztaltika ineffektív, ételmaradék maradhat a nyelőcsőben, ami szekunder perisztaltikát indukálhat. A szekunder perisztaltikát a nyelőcső afferens neuronjai kezdeményezik, a teljes nyelési reflex általában nem vesz benne részt, nem okoz pharyngealis kontrakciót és UES-relaxációt sem, de terjedése distalis irányban lényegében azonos a primer perisztaltikus hullámokéval. A nyelőcsőfal ballon által kiváltott feszülése következtében kialakuló szekunder perisztaltika karaktere ettől eltérő lehet. A perisztaltikus kontrakciós hullámot követően a nyelőcső refrakter állapotba kerül, amikor az izomzat nem, vagy csökkent mértékben képes excitátoros ingerekre válaszolni. Újabb szabályos perisztaltikus kontrakció csak ezen látenciaperiódus után keletkezik, és propulzívvá válásához el kell érnie a küszöbamplitúdót. A nyelés után kialakuló látencia oka a myentericus plexus gátló neuronjaiból felszabaduló NO. A kontrakció az excitátoros neuronokból felszabaduló acetilkolin hatására következik be. A kontrakció létrejötte e két neuronfajta közötti együttműködés eredménye. Amikor a nyelések között eltelt idő hosszabb, mint a refrakter periódus, akkor a nyelőcsőben komplett perisztaltikus hullám halad végig. Az egymást gyorsan követő nyelések esetén úgynevezett deglutitív gátlás lép fel. Ilyenkor a nyelésreflex pharyngealis iniciálását követően a garatban és az UES-ben megjelenő kontrakciók a nyelőcsőben primer perisztaltikát nem váltanak ki; primer perisztaltika csak a sorozatnyelés befejeződése után jelenik meg (3- ábra). A deglutitív gátlás ideje alatt a nyelőcsőizomzaton hullámszerűen végighaladó, hiperpolarizált állapot gátolja a nyelőcső-kontrakciókat, és ellazítja a LES-t. A hiperpolarizációban az SPG által közvetített centrális hatások (DMN caudalis rész) és lokális neuromuscularis mediátorok (NO) egyaránt szerepet játszanak, mindazonáltal mechanizmusa nem teljesen tisztázott. A nyelőcső cervicalis szakaszán a deglutitív gátlás a nucleus ambiguus alsó motoros neuronjainak gátlása következtében jön létre. Amint előbb olvasható, egy nyeléshullám végighaladása a nyelőcsövön 5-10 másodpercig tart, és ez alatt a nyelőcső lumene zárt, vagyis ezen időn belül újabb bolus továbbhaladása akadályozott. A deglutitív gátlás lehetővé teszi, hogy folyadékiváskor a nyelések mégis 1-2 másodpercenként követhessék egymást. A nyelések ilyen gyors egymásutánja esetén a nyelőcső az utolsó nyelésig gátolt állapotban marad, és csak ezt követően jelentkezik teljes perisztaltikus kontrakció. A deglutitív gátlást deglutitív excitáció követi, ami kontrakcióban nyilvánul meg, és kolinerg, illetve nonkolinerg, rebound hatásra következik be. A folyamatban a DMN rostralis részéből induló preganglionális vagusrostok és a 3- ábra. Nyelôcsô-manometria Deglutitív gátlás myentericus plexus postganglionalis kolinerg neuronjai vesznek részt. A vagalis pályák aktíválódása craniocaudalis irányban szekvenciális, ami időzíti a perisztaltikus kontrakció lezajlását. Ezeknek következtében a kolinerg antagonista hatások (atropin) nem a nyelőcső distalis, hanem a proximalis szakaszán növelik a kontrakciók latenciáját, és csökkentik azok amplitúdóját. Ezzel szemben a NOS-antagonisták a nyelőcső distalis szakaszán csökkentik a kontrakciók latenciáját, és szimultán kontrakciókat okoznak. Az alsó oesophagealis magasnyomású zónaként (LE- HPZ) definiált, 2-4 cm hosszú LES jellegzetes tónusos izom. Szemben a nyelőcsőtest inger által kiváltott gyors és rövid ideig tartó összehúzódásaival, a LES-régió izomtónusa spontán alakul ki, összehúzódása lassú, de tartós, miáltal a nyelőcsövet zárva tartja, értéke mintegy 20 Hgmm (10-30 Hgmm). A tónus fenntartásában, illetve az izom összehúzódásában vagy ellazulásában a fentebb leírt miogén, idegi és neurohormonális tényezők egyaránt szerepet játszanak. Elektrofiziológiai szempontból a LES-t alkotó izom depolarizáltsági foka nagyobb, mint a nyelőcsőizomé, ami a klorid-csatornák eltérő működésével magyarázható. Az időközönként észlelhető spike-aktivitás fokozza a depolarizációt, ami szintén növeli az izomtónust. Az MMC első fázisa során a LES tónusa nem változik, de a késői második fázisban és a harmadik fázisban fázikus kontrakciók jelentkeznek anélkül, hogy a bazális nyomás érdemben változna. Nyelés vagy a nyelőcsőfal feszülése LES-relaxációt okoz. Fokozza a LES-nyomást az intraabdominalis nyomás növekedése is, amelyet vagus reflex közvetít. A diaphragmaticus sphincter tónusos kontrakciója, különösen a belégzés idején, szintén hozzájárul a LES bazális nyomásának létrehozásához. Nyeléskor a LES-ellazulás már a nyelés
5 114 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 115 kezdete után, 1,5-2,5 másodpercen belül bekövetkezik, és 6-8 másodpercig tart. A relaxáció a perisztaltikus hullám LES-hez érkezésével szűnik meg. Nyelés kapcsán a LESellazulás akkor is bekövetkezik, ha a nyelés nem indukál perisztaltikát a nyelőcsőben. A nyelésektől függetlenül a TLERS alkalmával is teljes mértékben ellazul a LES, ami 15 másodpercig tart, és óránként hatszor következik be normális estben. A nyelőcső fejlődési rendellenességei és strukturális eltérései Tracheooesophagealis fisztula és nyelőcső-atresia A tracheooesophagealis fisztula és a nyelőcső-atresia a nyelőcső két leggyakoribb veleszületett fejlődési rendellenessége, újszülött közül egyben fordul elő. Az esetek 7%-ában egyedül és 93%-ában más fejlődési rendellenességekhez társulva jelenik meg. A társuló fejlődési rendellenességek vertebralis, anorectalis, cardialis, trachealis, oesophagealis, renalis és végtagi megnyilvánulásúak lehetnek. Előfordulási gyakoriságuk az elmúlt harminc év során nem változott, de a túlélés jelentősen javult. A tracheooesophagealis fisztula a respiratorikus traktus és az előbél szétválasztódási folyamata során keletkezik. A nyelőcső-atresia a primitív bél rekanalizációjának az elégtelensége, ami a 8. embrionális hét során alakul ki. A veleszületett nyelőcső-atresia gyakran társul tracheooesophagealis fisztulával, és ez alapján 5 csoportját (A-E) különböztetjük meg: A-típus tiszta nyelőcső-atresia (7,6%) B-típus nyelőcső-atresia proximalis tracheooesophagealis fisztulával (0,8%) C-típus nyelőcső-atresia distalis tracheooesophagealis fisztulával (86,5%) D-típus nyelőcső-atresia proximalis és distalis tracheooesophagealis fisztulával (0,7%) E-típus H-alakú tracheooesophagealis fisztula nyelőcső-atresia nélkül (4,4%) A leggyakoribb forma a C-típus, amelyben a nyelőcső vak tasakban végződik, és a tracheával, többnyire a carina magasságában, fisztulát képez. Az atresiás nyelőcső vak tasak formájában végződik, és a trachea a nyelőcsőnek az elzáródástól distalis szakaszával közlekedik, emiatt a tápcsatornába levegő kerül. Klinikai gyanúját a terhesség során a polyhydramnion, születés után pedig a nyálfolyás vetheti fel. Az első táplálás köhögést és fulladást válthat ki. A nyelőcső-atresiát a nazogasztrikus szondalevezetés sikertelensége megerősíti. Enyhébb esetekben az ismétlődő pneumonia hívhatja fel a figyelmet tracheooesophagealis fisztulára. Az atresia és fisztula jelenléte, illetve típusa oesophagográfiával és bronchoszkópiával azonosítható. A nyelőcső-atresiával felnőtt korban nem találkozunk. Tracheoesophagealis fisztulával felnőttkorban elvétve találkozunk asztma, visszatérő tüdőgyulladások, refluxbetegség hátterében, de kialakulhat a nyelőcső sérülése, korrozív károsodása vagy a nyelőcsövet, a tüdőt és a mediastinumot érő traumás behatás következtében is. Kezelése sebészi. Congenitalis nyelőcsőstenosis Az oesophagus veleszületett szűkületei ritka rendellenességek, mintegy élve születésre esik egy. A nyelőcső bármelyik szakaszán előfordulhat, a distalis harmadban a leggyakoribb. A membránszerű képződménnyel járó forma rendszerint rövid szakaszra korlátozódik, míg a fibromuscularis forma hosszú szakaszt érint. A stenosist okozó forma a fisztulákhoz hasonlóan a 8. embrionális hét során a primitív béllumen kialakulásának elégtelensége. Előfordul, hogy a vérerek nem fejlődnek ki, és ez vezet a szűkülethez. A szűkült területekben gyakran található légutakat alkotó szövet. Szövettanilag három csoportot különböztetünk meg: I. csoport: tracheobronchialis eredetű szövetet tartalmazó (hengerhám, porc, csillószőrös hám, légúti nyáktermelő mirigyek) II. csoport: membránképződéssel járó forma III. csoport: fibromuscularis stenosis Congenitalis nyelőcsőstenosissal felnőtteknél elvétve találkozhatunk. Endoszkópos vizsgálattal, többnyire a nyelőcső középső részén lévő szűkület környezetében gyakran tracheára emlékeztető porcgyűrűket láthatunk. Endoszkópos ultrahangvizsgálat a tisztázatlan nyelőcsőszűkületek esetén diagnosztikus segítséget jelenthet. Indokolt továbbá mellkas CT elvégzése is. Mint a nyelőcsőszűkületek esetében általában, fontos a betegek megnyugtatása és ellátása táplálkozási tanácsokkal. A ballonos nyelőcsőtágítással a betegek többsége sikeresen tünetmentessé tehető, műtéti beavatkozás ritkán szükséges. A congenitalis nyelőcső-duplikátumok és ciszták Az előbél-duplikátumok nyelőcsőcisztákat (tubuláris duplikátum) és bronchogen cisztákat képezhetnek. A primitív előbél elégtelen vakuolizálódása következtében cisztózus vagy tubuláris képződmények a nyelőcső teljes hossza mentén kialakulhatnak, és rendszerint más malformációkkal társulnak, mint pl. fisztulák, a gerinc vagy a gasztrointesztinális traktus egyéb részeinek fejlődési rendellenességei. A ciszták a nyelőcső jóindulatú daganatainak mintegy 0,5-2,5%-át teszik ki. A mediastinumban jobb oldalon hátul találhatók leggyakrabban, falukban rendszerint simaizom van, és alimentáris eredetű hám borítja őket. A nyelőcső veleszületett duplikátumai lehetnek teljesen szeparáltak, vagy rendelkezhetnek közös fallal, előfordul, hogy gyomornyálkahártya-szigeteket tartalmaznak. Szintén társulhat hozzájuk gerincfejlődési rendellenesség vagy vékonybél-duplikátum is. Felnőttkorban dysphagia vagy rutin mellkasröntgenen megjelenő mediastinalis térfoglaló folyamat kivizsgálása során találkozunk ezekkel a fejlődési rendellenességekkel. Endoszkópiával ép nyálkahártyát látunk; mellkas CT és endoszkópos ultrahangvizsgálat megbízható diagnózist biztosít. Pungálásuk diagnosztikus célból is ellenjavallt, a megoldást és a végső diagnózist a sebészi eltávolítás képezi. Veleszületett nyelőcsőgyűrűkű (oesophageal rings) A nyelőcsőben található veleszületett, gyűrűszerű, normál nyálkahártyával fedett bedomborodások bárhol előfordulhatnak, de leggyakrabban a distalis nyelőcsőben találhatók. Három típust (A, B és C) különböztetünk meg. Fejlődéstani okokra visszavezethető keletkezésük az embrionális nyelőcső hengerhámja hibás vakuolizációjának következménye. Keletkezésüket összefüggésbe hozták azonban immunbetegségekkel, gyulladással és refluxbetegséggel is. Az A-típusú gyűrű a legritkábban előforduló forma. A squamocolumnaris határtól 2 cm-rel proximálisan található, muscularis formának is nevezik, mivel a LES proximalis határának proliferációja okozza. Három rétege van: mucosa, submucosa és muscularis propria. A C-típusú gyűrűt a rekeszszárak benyomatai hozzák létre. Tünetet nem okoz, többnyire a nyelőcső báriumos radiológiai vizsgálata során látható elváltozás. A Schatzki-féle gyűrű (B-típusú gyűrű) a leggyakoribb gyűrűforma, az endoszkóppal vizsgált személyek 6 14%- ában megtalálható, mindkét nemben egyaránt, de negyven év felett gyakrabban fordul elő. A laphám és a hengerhám határán található, ahhoz való viszonya továbbra sem tisztázott. Többnyire a hiatus hernia proximalis határát képezi, két rétegből áll: mucosa (laphám a nyelőcső felőli, hengerhám a gyomor felőli felszínén) és submucosa. Keletkezését refluxbetegséggel is kapcsolatba hozták, de az egyértelmű klinikai összefüggés nem bizonyított. Gyermekekben eosinophil oesophagitisszel járhat együtt. Tüneteket, elsősorban dysphagiát és falatelakadást akkor okoz, ha következtében a reziduális lumen 13 mm-nél kisebb. A betegek gyakran refluxos tünetekről (pyrosis, regurgitáció) is beszámolnak. A diagnosztika legérzékenyebb módszere a báriumos nyelésvizsgálat, endoszkópiával többnyire a jelentős szűkülettel járó forma ismerhető fel könnyen. Társuló eosinophil oesophagitis igazolására nyelőcső-biopszia indokolt. Ha falatelakadást okoz, nyelőcsőtágítást kell alkalmazni. Ballonos vagy bougie-s nyelőcsőtágítás a választandó kezelés. A tágítás után a betegek kétharmada egy évig, egyharmada két évig tünetmentes, és három év múlva a betegek 90%-ánál visszatérnek a tünetek. Ez esetben a tágítás ismétlése javasolt. A tágítást követően tartós fenntartó protonpumpagátló kezelés alkalmazása indokolt. Nyelőcsőhártyák (esophageal webs) Vékony, többnyire excentrikus, haránt irányú, hártyaszerű képződmények a nyelőcsőben. Két rétegét (mucosa, submucosa) kötőszövet rögzíti a szabályos nyelőcsőhámhoz. Elhelyezkedése változó, leggyakrabban a cervicalis szakaszon található, gyakran heterotóp gyomornyálkahártya kíséretében, ez utóbbit cervical inlet patch-nek (CIP) is nevezik az angol irodalomban. Veleszületett és szerzett formáját különböztetjük meg. A veleszületett forma rendkívül ritka, többnyire a nyelőcső középső és alsó harmadában található. A nyelőcső lumenének embrionális fejlődése során a vakuolizációs folyamat zavarának következménye. A szerzett forma etiológiája igen változatos lehet. Dysphagiát okozhat. Nőkben gyakrabban fordul elő. Vashiányos anaemiával, glossitisszel és koilonychiával társuló formáját Plummer Vinson-szindróma (Peterson Kellyszindróma) neveken is számon tartjuk, és ezekben a betegekben gyakoribb a nyelőcső- vagy gégerák előfordulása. Társulhat epidermolysis bullosával is. A betegek többségének a nyelőcsőhártyák nem okoznak panaszt, ha igen, akkor a tünetek gyermekkorban kezdődnek. Leggyakrabban falatelakadást okoz, de aspirációval vagy refluxszerű tünetekkel is járhat. Kimutatásuk legérzékenyebb módszere a radiológiai vizsgálat. Gasztroszkóppal a nyelőcső proximális szakaszának gondos vizsgálata során látható ectopiás nyálkahártya is felhívhatja rá a figyelmet. A tüneteket okozó hártyákat bouginage-zsal kezeljük, ritkán transzendoszkópos bemetszésre vagy sebészi reszekcióra is szükség lehet. Heterotrop gyomornyálkahártya a nyelőcsőben A heterotrop gyomornyálkahártya-szigetek a tápcsatorna területén bárhol előfordulhatnak, de leggyakrabban a
6 116 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 117 nyelőcső nyaki szakaszán találhatók (CIP). Endoszkópos vizsgálatok során az észlelés gyakorisága igen változó (0,1 10%), aminek az oka az, hogy a felső sphincter alatti nyálkahártya megítélése nem könnyű, és csak az endoszkóp lassú visszahúzásával észlelhető. Mérete 1-2 mm-től 3-4 cm-ig változhat. Szövettanilag nem mindig lelhető fel benne a gyomornyálkahártya összes jellegzetes eleme. A nyelőcső embrionális hámosodási folyamatának zavara következtében alakul ki. A refluxbetegség ezekben a betegekben gyakoribb, és a heterotop nyálkahártya metaplasiás eredetét is felvetették, ez azonban nem nyert bizonyítást. Dysplasia, malignitás is előfordul benne, de jelenleg nem tartjuk precarcinomatosisnak. A tünetmentes, illetve tünetekkel jelentkező, továbbá a heterotop nyálkahártyához társuló morfológiai eltérések (stenosis, fekély, fisztula, hártya), illetve a dysplasia vagy az ectopiás gyomornyálkahártyában malignus daganat fennállása alapján a betegek öt csoportja különböztethető meg. A tünetmentes betegeket nem kell kezelni. A kezelés a refluxos tünetek kezelésére irányul, indokolt a tartós protonpumpagátló kezelés. A stenosissal szövődött esetekben a malignus folyamat kizárása rendkívül fontos. A nyelőcsőtágítás ezekben az esetekben különös óvatossággal végzendő. Malignus folyamat esetén műtéti megoldás szükséges. A nyelőcső diverticulumai A nyelőcső-diverticulumok a nyelőcsőfal egy vagy több rétegének kitüremkedését jelentik, amelyek a nyelőcső bármely szakaszán megjelenhetnek. A valódi diverticulumokat a nyelőcsőfal összes rétegének, míg a pseudodiverticulumokat csak a mucosának vagy a submucosának a kitüremkedése hozza létre. Ebben az értelemben a cricopharyngeus izomtól proximalisan kialakuló Zenkerféle diverticulum pseudodiverticulum. A nyelőcső-diverticulumok csoportosíthatók keletkezési mechanizmusuk vagy lokalizációjuk szerint. A keletkezésük szerint pulziós és trakciós diverticulumokat különböztetünk meg. A pulziós diverticulumok a nyálkahártya kitüremkedései, amelyek a nyelőcső bármely szakaszán, a lumen organikus vagy funkcionális természetű, tartós obstrukciói következtében jönnek létre. Többségük diffúz nyelőcsőspazmus vagy achalasia következménye. A nyelőcső középső részén keletkező trakciós diverticulumok tradicionálisan a mediastinalis gyulladásos folyamatok (tbc, gombás fertőzések) okozta fibrózis vagy centrális malignus tüdődaganatok következményei. A Zenker-féle diverticulum ritka, az átlag populáció 0,01 0,11%-ában, a dysphagia miatt radiológiailag vizsgált betegek 2-3%-ában fordul elő, és általában az idősebbekben. Kialakulásában szerepet tulajdonítanak a cricopharyngeus izom fibroadiposus elfajulása következtében csökkent izomcompliance-nak; emiatt nyelés alkalmával megnő az intrabolus nyomás, ami a garatfal hátsó, potenciálisan kiboltosulásra hajlamos hátsó részén (Killian-féle háromszög) a nyálkahártya herniálódását okozza. A nyelőcső felső szakaszán még ennél is ritkább diverticulum a Laimer-féle diverticulum, amely hasonló mechanizmussal a cricopharyngeus izom alatt keletkezik. A Zenker-féle diverticulum a betegek többségénél éves korban derül ki. A tünetek globusérzés és a teljes nyelésképtelenséggel járó dysphagia között oszlanak meg. A klasszikus tünet az étel regurgitációjával járó oropharyngealis dysphagia, aminek kialakulása független a diverticulum méretétől. Ennek az az oka, hogy a Zenker-féle diverticulum nyílása gyakran a garat tengelyébe esik, tehát a táplálék elsősorban ide jut, és a feltelődő gurdély komprimálja a nyelőcsőlument. Gyakori panasz a rossz szájszag, rekedtség, esetleg tapintható nyaki terime megjelenése. A Zenker-féle diverticulum leggyakoribb szövődménye a visszatérő aspiráció, a pneumonia. A dysphagia miatt testsúlycsökkenés is bekövetkezhet. Vérzés és perforáció is előfordul. A nyelőcsőtest diverticulumait lokalizációjuk alapján parabronchialis és epiphrenicus elnevezéssel illetjük. A nyálkahártya-kitüremkedés intramuralis formája is ismeretes, amikor kicsiny (1-3 mm) psseudodiverticulumok jönnek létre a nyálkahártya gyulladása és megvastagodása következtében. Ezek endoszkópia során többnyire nem, de báriumos nyelés alkalmával jól láthatók. A parabronchialis és epiphrenicus diverticulumok rendszerint enyhe dysphagiás tüneteket okoznak, gyakran a tünetektől függetlenül, radiológiai vizsgálat során derülnek ki. Panaszokkal főleg a diffúz nyelőcsőspazmus okozta diverticulumok járnak. Szövődményként bezoárképződés, szívritmuszavar és ritkán a tasakban kialakuló carcinoma fordulhat elő. A nyelőcső-diverticulumok diagnosztikájában a báriumos nyelésvizsgálatot, az endoszkópiát, a nyelőcső-manometriát és CT-vizsgálatot, illetve ezek kombinációját alkalmazzuk. A báriumos nyelésvizsgálat minden diverticulum gyanúja esetén hasznos és biztonságos, elsőként választandó vizsgáló módszer. A CT-vizsgálat különösen a trakciós diverticulum esetében hasznos, mivel egyben információt szolgáltat az anatómiai környezetről is. Az endoszkópia főleg a malignus folyamatok kizárása szempontjából fontos, de rendkívüli óvatossággal kell végezni a vizsgálatot. A Zenker-féle diverticulum nyílásának öszszetévesztése a nyelőcsőlumennel könnyen perforációhoz vezethet. Emiatt is érdemes minden dysphagiás beteg esetén első lépésben a radiológiai vizsgálatot elvégezni. A nyelőcső-manometria a diverticulum kialakulásához vezető motoros okok feltárásán túl a sebészi megoldás tervezésében is segítséget nyújt. A tüneteket okozó Zenker-féle diverticulumot kezelni kell. Kis diverticulum esetén cricopharyngealis myoto- mia is elegendő lehet, nagyobbak esetében ehhez diverticulectomia is társul. A műtét a betegek közel 80%-ában tünetmentességet eredményez, a Zenker-féle diverticulum recidívája kisebb, mint 5%. Újabban endoszkópos diverticulumreszekciós technikákat is alkalmaznak. A tünetmentes epiphrenicus és peribronchialis diverticulumokat nem kell kezelni. A tüneteket okozó betegek ellátásának a nyelőcsőszűkület vagy a háttérben álló diszmotilitás kezelésére kell irányulnia. A sebészi megoldás kiterjesztett myotomia, diverticulectomia és antireflux műtét együttes alkalmazását jelenti. Hiatus hernia A hiatus hernia azt az állapotot jelenti, amikor a rekesz hiatus oesophageusán k eresztül a gyomor egy része vagy a teljes gyomor a mellüregbe kerül. A rekeszszárakat és a nyelőcsövet tágulékony, laza kötőszövet, illetve a phrenooesophagealis membrán kapcsolja össze. Ennek gyengesége, illetve a benne felszaporodó zsírszövet (obesitas), valamint az intraabdominalis nyomás növekedése következtében a sagittalis rés megnagyobbodik, és kerek vagy ovális nyílássá, sérvkapuvá alakul, amelyen a cardia már a fiziológiást meghaladó mértékben csúszik át a rekesz fölé. A kórfolyamat súlyossága alapján történik a rekeszsérvek osztályozásai is, amelyet a 3-4. ábra mutat be. Az I-es típus esetében a membrándiszfunkció körkörös, ezért a cardia axiális irányba teljes egészében átcsúszik (sliding mechanizmus) a hiatuson. Amikor a membrán meggyengülése részleges (lokalizált), akkor csak a gyomorfundus egy része kerül a nyelőcső és a rekesz közé. Ezt II-es vagy paraoesophagealis típusnak nevezzük, ami ún. rolling mechanizmussal alakul ki. Ez a típus nem jár a nyelőcső és a gyomor átmenetének orális irányú áthelyeződésével, és az enyhébb esetekben nincs állandó hiatuszsák sem, hanem csak légzéskor vagy az intraabdominalis nyomás fokozódásakor képződik hiatuszsák. A III-as típus kialakulásában mindkét mechanizmus szerepet játszik, ilyenkor a nyelőcső-gyomor átmenet a mediastinumba vándorol (axialis típus), és a hiatuszsák tovább növekedvén, a mediastinum alsó részébe 3-4. ábra. A rekeszsérvek osztályozása türemkedik; összenövések is kialakulhatnak a pleurával vagy a pericardiummal. A II-es és III-as típusok természetes lefolyása progresszív. A sérvképződés legsúlyosabb formája az ún. upside-down-stomach, azaz a IV-es típus, amikor a gyomor a bal rekeszszárat és a kisgörbületen, az angulust összekötő tengely mentén rotálódva, a hatalmas hiatuson át a mellüregbe kerül. A pylorus és a cardia a sérvkapuban egymás mellett helyezkedik el. Ilyenkor a phrenooesophagealis membrán is elszakad, és a gyomrot a léphez és a vastagbélhez rögzítő szalagok megnyúlnak. Súlyos esetben a colon, a lép vagy a hasnyálmirigy is herniálódik. A leggyakrabban, mintegy 85%-ban, az I-es típussal találkozunk, és a fennmaradó 15% a II-es és IVes típusok között oszlik meg. A paraoesophagealis hiatus hernia általában idősebb korban jelentkezik, és valamelyest gyakoribb nőkben. A cardiadiszfunkció következtében a rekeszsérvek mindegyik típusa okozhat refluxbetegséget, de jellemzően a klasszikus tünetekkel ez az I-es típusú hiatus hernia esetén szokott előfordulni. A paraoesophagealis hiatus hernia tünettana ettől eltérő. A II-es típus lehet tünetmentes, vagy többnyire intermittáló jelleggel az ischaemia miatt epigastrialis fájdalmat, étkezés utáni teltségérzetet, hányingert vagy böfögést okoz. A III-as típusban ezek a tünetek állandósulhatnak. A paraoesophagealis hiatus hernia gyakran idős betegek vashiányos anaemiájának kivizsgálása során derül ki, ami többnyire ulceratio (Cameron-féle fekély) és következményes vérzés miatt alakulhat ki. A IV-es típus pedig akut gyomorvolvulushoz vezethet, elzáródást, incarceratiót, gyomorgangrénát vagy perforációt is okozhat. A volvulus gyakran hányás vagy köhögés kapcsán lép fel, de az is előfordul, hogy a gyomornak a mellkasból a hasüregbe történő visszatérésekor következik be. A rekeszsérv gyakran egyszerű mellkasfelvételen is azonosítható. A paraoesophagealis hiatus hernia báriumos nyelésvizsgálattal általában könnyen igazolható, bár a II-es és III-as típus elkülönítése nem mindig egyszerű. A báriumos nyelésvizsgálat az I-es típusú rekeszsérv diagnosztikájában meglehetősen szubjektív, ezt jelzik a gyakoriságára vonatkozó adatok szélsőséges értékei (10 80%). Az I-es típus kimutatásánál figyelembe kell venni
7 118 Gaszt ro en te ro ló Gia A nyelôcsô betegségei ábra. Axiális hiatus hernia radiológiai képének vázlata az oesophagogastricus junktio és a hiatus oesophagicus egymáshoz viszonyított fiziológiás elmozdulását. Ennek megfelelően a hiatus és a B-gyűrű (a Z-vonalnak megfelelő benyomat) közötti elmozdulás 2 cm-t meghaladó mértékét tekintjük diagnosztikusnak. Mivel a B-gyűrű csak ritkán látható, ezért azt többnyire a nyelés során, a nyelőcső distalis végén a radiológiai képen látható vestibulummal, illetve rekeszsérv esetén a rekeszbenyomat által létrehozott ampulla phrenica aljával helyettesíthetjük. Az axiális hiatus hernia radiológiai képének vázlatát mutatja a 3-5. ábra. A hiatus oesophageuson áthaladó gyomornyálkahártya-redők a rekeszsérv jelenlétét jelzik. A hiatuszsák nagyságának meghatározását az is nehezíti, hogy a perisztaltika kezdetén és végén mért értékek 1 cm-rel is eltérhetnek, továbbá az intraabdominalis nyomás növekedése is jelentősen befolyásolja a meghatározást. Így a 3 cm-nél kisebb axialis hiatus hernia radiológiai meghatározása meglehetősen bizonytalan. Endoszkóppal az I-es típusú rekeszsérvet akkor állapíthatjuk meg, ha a Z-vonal és rekeszszárak által okozott benyomat távolsága nagyobb, mint 2 cm. Ez a meghatározás azonban számos tényező által nehezített, pl. az endoszkópon öt centiméterenként elhelyezkedő jelölések, vagy a nagyon laza, benyomatot nem okozó rekesz, levegővel túlságosan felfújt gyomor, esetlegesen Barrett-nyelőcső. Megjegyzendő, hogy a hiatus hernia nagyságának az endoszkópos vizsgálat kezdetén és végén mért értékei közötti eltérés (inherens hiba) 2 cm. A cardia vizsgálatának másik lehetősége az alulról (retroflexióban) történő megtekintés, amely lehetővé teszi a Gubaroff-féle billentyű (flap valve) integritásának az értékelését (Hill I-IV. súlyossági stádium). Mint látható, a radiológiai diagnosztikához hasonlóan a hiatus hernia endoszkópos diagnosztikája szintén korlátozott. A paraoesophagealis hiatus hernia esetén nyelőcsőszűkület észlelhető, és a deformált gyomorból nem mindig lehet a duodenumba jutni, továbbá a fundus sem vizsgálható. A cardia funkcionális vizsgálómódszere a nyelőcsőmanometeria. A hagyományos áthúzásos technikával végzett vizsgálat során a rekeszszárakat általában a belégzésre bekövetkező nyomásváltozások irányának megfordulása (respiratorikus inverziós pont) jelzi. Mivel azonban a LES-nyomás, a rekeszszárak nyomása, az intraabdominalis nyomás és az intraoesophagealis nyomás különbsége, valamint a nyelőcső intrinsic sphinctere és a cruralis diaphragma közötti távolság individuális variabilitása igen jelentős, a hagyományos manometria nem megbízható módszer a hiatus hernia diagnosztikájára. A gastrooesophagealis junkció nyomásprofiljának térbeni és időbeni dinamikájának feltérképezésére kifejlesztett egyik új módszer a HRM. Ezzel a módszerrel vált lehetővé a nyelőcső intrinsic sphinctere és a rekeszszárak szeparálódásának fiziológiás és kóros mértékének megbízható elkülönítése. A módszerrel végzett vizsgálatok kimutatták, hogy 2 cm-t meghaladó szeparáció gyakori a refluxbetegségben, megerősítve a hiatus hernia szerepét a GERD patogenezisében. Szintén a cardia kompetenciájának vizsgálatára szolgáló új diagnosztikus eljárás az EndoFlip (endolumenal functional lumen imaging probe) technika, amely impedancia planimetriás elven működik, és általa háromdimenziós, körkörös képen lehet a záróizom kontrakciós, illetve relaxációs képességét vizsgálni. A hiatus hernia terápiája a tüneteket okozó refluxbetegség kezelését jelenti. A reflux okozta tünetek kezelésére a tartós protonpumpagátló adása vagy a hiatus hernia műtéti megoldása egyaránt hatékony módszer. A sebészi kezelés a reflux okozta szövődmények megelőzése tekintetében hatékonyabbnak mutatkozik, ugyanakkor a műtéti kezelés gyakrabban okoz dysphagiát, gázosságot (flatulenciát) és böfögésképtelenséget. A ritka paraoesophagealis sérvek esetében sebészi megoldás az előnyben részesítendő kezelésmód. Ajánlott irodalom Achkar, E: Zenker s diverticulum. Dig Dis, : DeVault, KR: Lower esophageal (Schatzki s) ring: pathogenesis, diagnosis and therapy. Dig Dis Sci, : Kahrilas, PJ, Kim, HC, Pandolfino, JE: Approaches to the diagnosis and grading of hiatal hernia. Best Practice & Research Clin Gastroenterol, : Liebermann-Meffert, D, Allgöwer, M, Schmid, P et al.: Muscular equivalent of the lower esophageal sphincter. Gastroenterology, : Mulder, CJ, Costamagna, G, Sakai, P: Zenker s diverticu- Gastrooesophagealis refluxbetegség Kulcsfontosságú megállapítások A gastrooesophagealis refluxbetegség (legelterjedtebb rövidítése a GERD) a felső gasztrointesztinum komplex motilitási zavarán alapuló kórkép, amelynek következtében a gyomorbennék (refluxátum) a nyelőcsőbe és a légutakba kerülve klinikai tüneteket és/vagy makroszkópos eltéréseket okozhat. A GERD három klinikai fenotípusa a nem erozív refluxbetegség (NERD), az erozív refluxbetegség (ERD) és a Barrett-oesophagus. A NERD olyan refluxbetegség-forma, amelyben a típusos vagy atípusos tünetek hátterében, a nyelőcsőben makroszkópos eltérés nem észlelhető Az ERD diagnosztikus kritériuma az ún. mucosal brake, azaz a nyálkahártya-folytonosság megszakadásának jelenléte. Az erozív oesophagitis endoszkópos megítélésére a Los Angeles klasszifikációt használjuk, amely a nyálkahártya-károsodás súlyosságától függően 4 stádiumot (A, B, C és D) különít el. A GERD típusos tünetei a gyomorégés és a savas regurgitáció, legfontosabb atípusos tünetei a mellkasi fájdalom, a respiratórikus tünetek és az alvászavarok. A GERD tüneteinek és szövődményeinek gyógyszeres terápiájában a protonpumpagátlók (PPI) jelentik a leginkább költséghatékony kezelést. A gyógyszeres kezelés iniciális és fenntartó kezelési szakaszból áll, a kezelést a step-down stratégia elvei szerint kell végezni. Bizonyos jól megválogatott esetekben a sebészi antirefluxműtétek reális terápiás alternatívát jelenthetnek. lum: treatment using a flexible endoscope. Endoscopy, : Oláh T: A nyelőcső sebészete. Magyar Sebészet, : Rahden, BHA von, Stein, HJ, Becker, K et al.: Heterotopic Gastric Mucosa of the Esophagus: Literature-Review and Proposal of a Clinicopathologic Classification. Am J Gastroenterol, : Richter, JE, Wu, WC, Johns, DN et al.: Esophageal manometry in 95 healthy adult volunteers. Variability of pressures with age and frequency of abnormal contractions. Dig Dis Sci, : Rosztóczy A, Vadászi K, Németh I et al.: Increased incidence of gastroesophageal reflux disease and Barrettesophagus in patients with cervical inlet patch. Gut, (Suppl2): A140. Siafakas, CG, Ryan, CK, Brown, MR, Miller, TL: Multiple esophageal rings: an association with eosinophilic esophagitis: case report and review of the literature. Am J Gastroenterol, : Skandalakis, JE, Ellis, H: Embryologic and anatomic basis of esophageal surgery. Surg Clin N America, : Tobin, RW: Esophageal rings, webs, and diverticula. J Clin Gastroenterol, : Younes, Z, Johnson, DA: Congenital esophageal stenosis: clinical and endoscopic features in adults. Dig Dis, : Definíció, klasszifikáció, patogenezis Lonovics János Bevezetés Wittmann Tibor A gastrooesophagealis refluxbetegség (legelterjedtebb nem zetközi rövidítése a GERD) klinikai jelentőségét rendkívüli elterjedtsége, az életminőséget jelentősen ron tó klinikai tünetei, a szövődményráta relatív magas volta és a klinikai kép sokszínűsége, heterogenitása adja. Tekintettel arra, hogy a GERD a felnőtt populáció 10 30%-át érintheti, valamint arra, hogy a klinikai tünetek típusos és atípusos megjelenése miatt a betegekkel az orvosi szakma szinte valamennyi szegmense kapcsolatba kerülhet, a családorvostól kezdve, a belgyógyász és gasztroenterológus szakorvosokon keresztül a legkülönbözőbb egyéb specialistáig (sebész, kardiológus, pulmonológus, fül-orr-gégész, pszichiáter, szomnológus, fogszakorvos stb.), rendkívül fontos ennek a betegségnek a felismerése. Ez típusos tünetek jelentkezése esetén nem okoz nehézséget, viszont az atípusos tünetek képében jelentkező GERD-ben a betegség sokszor egyáltalán nem kerül felismerésre, vagy indokolotlanul hosszú ideig késik a helyes diagnózis felállítása. Fentiek miatt rendkívül fontos a kórkép patogenezisének, sokszor megtévesztő tüneteinek, az extraoesophagealis (supraoesophagealis) manifesztációknak és a modern diagnosztikus és terápiás lehetőségeknek a társszakmákkal való megismertetése.
8 120 Gaszt ro en te ro ló Gia A nyelôcsô betegségei táblázat. A GERD elsô modern klasszifikációja GERD ELSÔ KLASSZIFIKÁCIÓJA NERD (60%) ERD (35%) Szövôdményes ERD (5%) Nem erozív refluxbetegség erozív refluxbetegség Ulcus (Endoszkóposan negatív strictura refluxbetegség) Barrett-oesophagus Adenocarcinoma Definíció A GERD a felső gasztrointesztinum komplex motilitási zavarán alapuló kórkép, amelynek következtében a gyomorbennék (dominálóan savas refluxátum) a nyelőcsőbe vagy a légutakba kerülve klinikai tüneteket (típusos és atípusos) és az esetek egy részében makroszkóposan is észlelhető elváltozásokat, erozív oesophagitist és Barrettoesophagust okozhat. A 2006-os Gasztroenterológiai Világkongresszuson ismertették a GERD egyszerűsített, ún. Montreáli definicióját, amely szerint a refluxbetegség egy olyan kórkép, amelyben a gyomortartalom refluxa a betegnek az életminőséget jelentősen rontó, kellemetlen tüneteket és komplikációkat okoz. Klasszifikáció A refluxbetegséget és a refluxoesophagitist hosszú ideig az orvostársadalom a mindennapi klinikai gyakorlatban szinonim fogalomként kezelte, annak ellenére, hogy hamar nyilvánvalóvá vált, hogy a refluxbetegség képezi azt a motilitászavaron alapuló klinikai entitást, amelynek egyik részjelensége lehet a refluxoesophagitis. A paradigmaváltást nagyban elősegítette az a felismerés, hogy a refluxoesophagitis nehezen kvantifikálható terminológiáját felváltotta az eróziók jelenlétén alapuló Los Angeles-féle endoszkópos klasszifikáció, amely a refluxbetegség erozív formáival járó csoportját négy súlyossági fokozatra osztotta (lásd később). Ennek alapján került sor a GERD első modern klasszifikációjának felállítására, amely a refluxbetegség három formáját különíti el: 1. Nem erozív refluxbetegség (NERD) vagy endoszkóposan negatív refluxbetegség, amelyben endoszkópiával makroszkópos elváltozás nem mutatható ki. 2. Erozív refluxbetegség (ERD), amelyben nyálkahártyakárosodások (mucosal brake) különböző súlyossági formái detektálhatók endoszkópiával. Szövődményes ERD, amelyben strictura, perforáció, vérzés, Barrett-metaplasia vagy adenocarcinoma fejlődik ki. Az epidemiológiai felmérések szerint a refluxbetegek mintegy 60%-a tartozik a NERD-, 35%-a az ERD- és csupán 5%-a a szövődményes ERD-csoportba (3-1. táblázat) táblázat. A GERD spektrumkoncepciója Enyhe forma Közepesen Súlyos forma súlyos forma NERD Erozív Strictura és oesophagitis Barrett-oesophagus Adenocarcinoma A refluxtevékenység létrejöttét lehetővé tevő közös patogenetikai mechanizmus (a motilitászavar és a döntően savas refluxátum szerepe) teremtette meg az alapját a GERD ún. spektrumkoncepciója kialakulásának. A spektrumkoncepció alapján a GERD különböző megnyilvánulási formái (NERD, ERD, szövődményes ERD) egy, a fenti, azonos patogenetikai alapokon nyugvó betegség különböző súlyosságú spektrumát képezik: a spektrum egyik végén helyezkedik el az ép oesophagus nyálkahártyával bíró NERD-betegek csoportja, amelyet a refluxbetegség enyhe formájának tartottak. A tünetek súlyosbodásával és a nyálkahártya-léziók megjelenésével a betegek a spektrum következő fokozatába, a súlyosabb ERD-csoportba kerülnek. A spektrum másik végén található a refluxbetegség legsúlyosabb formája, a szövődményekkel, Barrett-metaplasiával vagy adenocarcinomával járó, szövődményes ERD-betegek csoportja (3-2. táblázat). A spektrumkoncepció azt sugallja, hogy a felsorolt formák idővel egymásba átmennek, a NERD-ből ERD, majd szövőményes ERD alakul ki, és ezáltal ad abszurdum a refluxbetegség bármely formája adenocarcinomába torkollhat, ami nyilvánvalóan a felesleges és eredménytelen szűrőprogramok beindításához vezetett. Hamar nyilvánvalóvá vált, hogy a GERD különböző alcsoportjaiban a közös denominátornak tartható refluxtevékenység mellett az egyéb patogenetikai faktorokban (motilitászavar, refluxátum kémhatása, oesophagus nyálkahártya szenzitívitása stb.) mutatkozó eltérések, a PPI-re adott eltérő terápiás válasz, valamint a csoportok közötti átmenet ritkasága alapján a spektrumkoncepció nem tartható fenn. A GERD spektrumkoncepció fentiekben részletezett kritikáját követően került sor amerikai szerzők (Fass és Ofman) részéről egy új alcsoport-koncepció kidolgozására, amely szerint a GERD különböző megnyilvánulási formái patofiziológiai, diagnosztikai, terápiás válaszkészség és prognosztikai következmények szempontjából három, egymástól elkülöníthető önnálló alcsoportra oszthatók: 1. Nem erozív refluxbetegség, 2. Erozív refluxbetegség és Barrett oesophagus (3- táblázat). A három alcsoport közül az ERD- és a Barrettoesophagus-alcsoport a klasszifikációs és patogenetikai szempontok alapján aránylag homogén alcsoportnak bizonyult, míg a NERD meglehetősen heterogén alcsoportnak tartható (lásd később). A GERD legújabb csoportosítását igyekezett meghatározni a Montreáli klasszifikáció, amely tiszteletben tartja ugyan a NERD, ERD és Barrett-oesophagus csoportosítást, azonban a klinikai tünetek szindrómákba való tömörítésével ugyanakkor meg is zavarja a klinikusokat (3-4. táblázat). A klasszifikáció mentségére hozható fel az a családorvosoknak adresszált üzenet, amellyel az ún. tünetorientált diagnosztikát és az empirikus kezelést helyezi előtérbe (ezt szolgálja a klasszifikáció), és csak az empirikus terápia sikertelensége esetén irányítja a beteget a szakorvosok felé, ahol már az ERD, a NERD és Barrettklasszifikáció szerint történik a további diagnosztikus tevékenység és terápia. Epidemiológia 3-4. táblázat. A GERD Montreáli klasszifikációja 3- táblázat. A GERD új alcsoport-klasszifikációja és a fô komplikációk NERD ERD Barett-oesophagus Oesophagealis és Strictura Adenocarcinoma extraoesophagealis Fekély manifesztációk Vérzés A GERD-re vonatkozó epidemiológiai adatok a klinikai tünetek elemzése alapján kerültek meghatározásra. A prevalenciaadatok attól függően változnak, hogy az epidemiológiai adatgyüjtés a típusos vagy az atípusos tünetek alapján történik. A típusos tünetek alapján a lakosság mintegy 20%-ának vannak hetente jelentkező gyomorégéssel járó panaszai, ez a szám meghaladja a 40%-ot, ha a havonta jelentkező gyomorégés-frekvenciával számolunk. A típusos tünetek prevalenciája férfiakban valamivel magasabb, a férfi-nő arány durván 1,5:1-re tehető. Amennyiben az atípusos tünetek alapján gyűjtünk epidemiológiai adatokat, a prevalencia szintén elérheti a 20%-ot, a krónikus köhögés hátterében pl %-ban, az asthma bronchiale eseteiben 30 80%-ban mutatható ki a GERD-el való kapcsolat. Az epidemiológiai adatok helyes értékelését tovább nehezítik azok a tények, amelyek szerint az atípusos tünetek gyakran típusos tünetek nélkül jelentkeznek: az asztmások 40 60%-ában, a krónikus köhögésben szenvedők 43 75%-ában, a refluxeredetű mellkasi fájdalomban szenvedő betegek 10 20%-ában nincsenek gyomorégéses tünetek. A betegek ezen csoportját, amelyekben az epidemiológiai felmérések döntő többségében alkalmazott indikátortünetek, a gyomorégés és savas regurgitáció hiányoznak, joggal nevezik gyomorégés szempontjából ún. néma refluxbetegeknek. A mindennapi gyakorlatban ezek az új adatok azt jelentik, hogy a típusos tünetek alapján megadott epidemiológiai adatok jelentősen alulbecsülik a refluxbetegség valódi prevalenciáját. A fenti epidemiológiai eszmefuttatás további gyakorlati következménye az, hogy a néma refluxbetegekben az atípusos tünetek és a refluxbetegség közötti oki összefüggés gyakran rejtve marad, ami nehezíti a refluxbetegség időben történő diagnózisát. A refluxoesophagitissel járó refluxbetegség prevalenciáját a korábbi években jelentősen túlbecsülték. A legújabb vizsgálatok szerint a refluxbetegek csupán mintegy 35 40%-ában lehet a nyelőcsőben makroszkópos elváltozást (ERD, szövődményes ERD, Barrett-metaplasia stb.) kimutatni, míg a betegek nagy többsége, mintegy 60%-a tartozik a NERD-csoportba. Az ERD betegek 5%-ában fekély, 8 20%-ában strictura alakulhat ki. Jelentős vérzés csak az esetek kevesebb, mint 2%-ában jelentkezik, a nyelőcső-perforáció extrém ritkaság. A Barrett-epithelium az erozív refluxbetegség 8 20%- ában jelenik meg, strictura esetén a Barrett-metaplasia kockázata 40%-ra növekszik. A Barrett-oesophagus kli- A GERD olyan kórkép, amelyben a gyomortartalom refluxa a betegeknek kellemetlen tüneteket és komplikációt okoz. Ezek a következôk: Oesophagealis szindrómák Extraoesophagealis szindrómák Tüneti szindrómák oesophagus károsodással Ismert Feltételezett járó szindrómák komplikációk komplikációk Típusos reflux refluxoesophagitis refluxköhögés Pharyngitis szindróma Reflux-strictura Refluxlaryngitis Sinusitis Mellkasi fájdalom Barrett oesophagus refluxasthma tüdôfibrosis szindróma Adenocarcinoma Dentalis erózió otitis media rec.
9 122 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 123 A refluxátum eltérő jellegzetességei Amikor az agresszív faktorok tünetképzésben és nyálkahártya-károsító hatásban játszott szerepéről beszélünk, fontos elkülöníteni a savas, az alkaliás, a volumen- és a gázreflux fogalmát. Savas refluxról beszélünk akkor, ha a refluxátum kémhatása < ph 4. A savas refluxon belül elkülönítendő a patológiás és a fiziológiás savas reflux fogalma. Patológiás savas refluxról beszélünk akkor, ha a refluxepizódok frekvenciája és időtartama egy bizonyos numerikus értéket (DeMeester-score) meghalad, a jelentősen megnyúlt sósav-nyelőcső nyálkahártya-konnikai jelentőségét az adja, hogy precancerosus elváltozásnak tartható, az adenocarcinoma gyakorisága Barrettmetaplasia esetén 10 15%. Amennyiben az epidemiológiai adatokat az orvoshoz fordulás arányában vizsgáljuk, akkor az arányokat a GERD-jéghegy hasonlattal lehet legjobban kifejezni: a lakosságnak csak mintegy 2%-a tartozik abba a súlyos csoportba (jéghegy csúcsa), akik a krónikus és permanens tünetek miatt rendszeresen orvoshoz fordulnak. A betegek egy következő csoportjában aránylag gyakran jelentkező tünetek miatt szintén gyakori az orvoshoz fordulás (a jéghegy víz feletti része). A refluxbetegek többsége (a jéghegy víz alatti részének döntő hányada) azonban egyáltalán nem fordul orvoshoz, általában az öngyógyítás valamilyen formáját választja, vagy egyáltalán nem részesül kezelésben. Régóta vita folyik a GERD-prevalencia emelkedésének okairól. Az irodalom megegyezik abban, hogy a diagnosztika fejlődése önmagában nem magyarázza a GERD-betegség frekvenciájának növekedését. Mivel a GERD gyakoribb a fejlett nyugati országokban, a gyorséttermekben felszolgált ételek etiológiai szerepe már korán felmerült. Epidemiológiai adatok igazolták, hogy a gyorséttermi ételek fűszertartalma (chili, stb.) szoros korrelációt mutat a refluxepizódok számának növekedésével. Az italok közül a cola- és citrusfélék, valamint a fehér bor fokozzák a refluxepizódok számát. Manometriás vizsgálatokkal kimutatták, hogy a fehér bor szignifikánsan csökkenti az alsó oesophagus sphincter nyomását, míg a vörös bor azt nem befolyásolja. Az etiológiai faktorok sorában a magasabb életkor és a testtömegindex növekedése szintén fontos szerepet játszik a GERD-prevalenciaemelkedésben, bár ezzel ellentmondó adatok is találhatók. A Helicobacter pylori infekció az általa okozott corpus gastritis és az ammóniaprodukció pufferkapacitása miatt bizonyos védő szerepet fejt ki a refluxbetegség ellen. Epidemiológiai adatok igazolták, hogy a Helicobacter pylori infekció prevalenciája szignifikánsan alacsonyabb GERD-betegekben, mint a normál populációban. Különösen feltűnő negatív korrelációt mutattak ki a virulens, caga + Helicobacter pylori törzsek okozta infekció és a GERD súlyossága között. Az erozív GERDformákban a caga + törzsek prevalenciája jelentősen lecsökkent, a dysplasiával/adenocarcinomával szövődött Barrett-oesophagus esetekben pedig kimutathatatlan volt a virulens törzsek jelenléte. Ezek az adatok alátámasztják a Helicobacter pylori infekció védőszerepét, egyben igazolják azt, hogy a nyugati civilizációban a Helicobacter infekció prevalenciájának drámai csökkenése etiológiai szereppel bír a GERD-prevalencia növekedésében. A GERD etiológiájában szereplő ismert faktorok fűszeres ételek, testsúlynövekedés, életkor, dohányzás, alkoholfogyasztás, simaizom-relaxáló gyógyszerek stb. mellett a legújabb vizsgálatok a genetikai faktorok szerepét hangsúlyozzák. Halmozott előfordulású GERDcsaládokban sikerült lokalizálni a putatív GERD-gént a 13q14 kromoszómán, a vizsgálatok szerint a GERD az autoszomális domináns öröklésmintát követi. Patogenezis A GERD patogenezise komplex: a refluxbetegség alapvetően az oesophagust védő (antireflux-barrier, a nyelőcső savclearance tevékenysége, a nyálkahártya integritása mint szöveti rezisztencia) és a gyomorból a nyelőcsőbe jutó agresszív faktorok (gyomorsósav, duodenumtartalom) egyensúlyának megbomlása következtében alakul ki. A refluxátum nyelőcsőbe jutásában a legfőbb patogenetikai faktor az alsó oesophagus sphincter zárófunkciójának meggyengülése, addicionális faktorok a nyelőcsőclearance csökkenése és a betegek egy csoportjánál az elhúzódó gyomorürülés. Protektív faktorok Antireflux barrier A reflux elleni első védelmi vonalat az antireflux-barrier képezi. Az antireflux-barrier egy komplex anatómiai struktúra, amelynek komponensei az intraabdominalis térbe is terjedő alsó oesophagus sphincter (LES), a rekeszszárak, a phrenooesophagealis ligamentum és a megfelelő His-szög. Refluxtevékenység három módon következhet be az antireflux-barrieren keresztül: 1. a postprandialis tranziens LES-relaxációk (TLESR), 2. a nyelés indukálta LESrelaxációk és a LES-nyomás csökkenése következtében. A patológiás reflux létrejöttében a fiziológiás refluxban is szerepet játszó TLESR-k frekvenciájának növekedése a döntő faktor. A TLESR-k létrejöttéért egy vagalis reflexív a felelős, amelyet a gyomorfundus feszülése aktívál. A stimulus a nucleus tractus solitariusban átkapcsolódva vezet az alsó oesophagus sphincter relaxációjához. A legújabb kutatások szerint a reflexív működésében résztvevő, eddig ismert mediátorok nitrogén-monoxid, acetilkolin, enkefalinok, glutamát, kolecisztokinin mellett az inhibitoros neurotranszmitter, a gamma-aminovajsav (GABA) a GABA B -receptorok stimulálása révén szignifikánsan gátolja a TLESR-t, amelynek klinikai jelentőségét az adja, hogy a GABA B -agonisták új terápiás alternatívát jelenthetnek a refluxbetegség kezelésében. A GABA B - agonista baclofennel végzett klinikai vizsgálatokban a szer szignifikánsan fokozta az alsó oesophagus sphincter nyomását, és csökkentette a TLESR-k számát. A nyelésindukálta LES-relaxációk a refluxtevékenység 5-10%-áért felelősek, és főleg egyidejű hiatus hernia esetén vezetnek refluxhoz. A LES-nyomás csökkenése szintén szerepet játszhat a reflux létrejöttében, különösen akkor, ha az intraabdominális nyomás megnő. A LES-nyomás < 5 Hgmm esetén ún. szabad refluxról beszélünk, amely súlyos refluxoesophagitis esetén következhet be. A csuszamlásos hiatus hernia komplex módon járulhat hozzá a refluxtevékenység fokozódásához. A LES anatómiai támasztékának áthelyeződése önmagában rontja a sphincter kompetenciáját és az oesophagus clearance tevékenységét, a legújabb vizsgálatok szerint ezekben a betegekben is a TLESR-k frekvenciájának a fokozódása az egyik legjelentősebb patogenetikai faktor. A gyomorürülési zavar, mint egy fontos motilitási komponens szintén szerepet játszhat a patológiás refluxtevékenység kialakulásában, bár ennek patogenetikai jelentősége a legújabb vizsgálatok szerint csökkent, csupán az esetek 6 38%-ában tehető felelőssé a gyomorürülési zavar. Nyelőcső-savclearence A reflux elleni védelem második vonala az oesophagus volumen- és savclearance tevékenysége. Az oesophagus perisztaltikája a nyelőcsőbe jutott refluxátumot és savat a gyomorba juttatja. A nyelés indukálta primer perisztaltika sokkal hatékonyabb, mint a reflux indukálta szekunder perisztaltika. A refluxátum clearance-ében a gravitáció is jelentős szerepet játszik, éjszaka ez a mechanizmus kiesik. A másik komponens a lenyelt nyál és a nyelőcsőmirigyek lúgos szekrétuma, amely a még nyelőcsőben maradó savat neutralizálja. Éjszaka a nyálképződés csökken. A nyelőcső-savclearance tevékenységét a kifejlődő refluxoesophagitis másodlagosan súlyosan károsíthatja. Szöveti rezisztencia A reflux elleni védelem harmadik vonalát a nyelőcsőnyálkahártya szöveti rezisztenciája képezi, amely az oesophagusba jutó sósav rediffúziója ellen próbál védelmet nyújtani. A védelmi struktúra három rétegből áll: 1. preepithelialis, 2. epithelialis és postepithelialis védelmi réteg. A preepithelialis réteg gyakorlatilag egy gyengén fejlett nyákréteg, amelynek alig van pufferkapacitása. Az epithelialis réteg strukturális és funkcionális komponensből áll. A többrétegű epithelialis sejteket intercellularis tight junction -ok teszik ellenállóvá a H + -rediffúzióval szemben. A sósav az intercellularis rések kiszélesítése és a tight junction -ok pusztítása révén képes a nyálkahártyába hatolni. A bejutott savat az epithelialis réteg funkcionális komponense bikarbonát-ionok, foszfát- és fehérje-molekulák elválasztásával próbálja pufferelni. Az agresszív refluxátum okozta nyálkahártya-károsodás első jele az intercellularis rések kiszélesedése, amelyet ma a sósavkárosító hatás egyértelmű markerének tartják. NERD-betegekben csupán ez a marker mutatható ki szövettani vizsgálatokkal, a klinikai tünetek képződésében a tágult intercelluláris réseken bejutó sósav a felelős. A postepithelialis védelmet a nyálkahártya vérellátása jelenti, amely oxigén, tápanyagok és bikarbonát biztosítása, valamint a H + eltávolítása révén próbálja biztosítani a sav-bázis egyensúlyt és a nyálkahártya integritását. A sósav károsító hatására az epithelsejtek proliferációja indul meg, azonban ez a repair mechanizmus, összehasonlítva a gyomorral, rendkívül lassú, órák helyett napokban mérhető. Agresszív faktorok Gyomorsósav A gyomorsósav és az általa aktívált pepszin a legfontosabb agresszív tényező, amely a nyelőcső-károsodásban a fő szerepet játsza. A gyomorban termelt sósav mennyisége fontos tényező ugyan, de a döntő az antireflux-barrier károsodása. Normális motilitási viszonyok mellett hiperacid betegekben sem kerül olyan mennyiségű sósav a nyelőcsőbe, hogy klinikai tüneteket okozzon. A sósav patogenetikai szerepére utalnak azok az adatok, amelyek igazolták a sósavtermelést csökkentő (PPI, H2RA) vagy közömbösítő (antacidák) szerek terápiás hatását. Megfigyelték azt is, hogy a Helicobacter pylori infekció (különösen a caga-pozitív törzsek) bizonyos védő hatást fejt ki refluxbetegség ellen, feltehetőleg az által, hogy a baktérium által termelt ammónia puffereli a sósavat, másrész az infekció okozta corpus gastritis és atrophia jelentősen csökkenti a sósavszekréciót. A nyelőcsőbe jutott sósav és a pepszin a mucosalis barrier diszrupciójához, a H + -ion rediffúziójához, mikroszkópos (az intercellularis rések kiszélesedéséhez, a tight junction -ok sérüléséhez) és makroszkópos (erózió, gyulladás, vérzés, strictura, Barrett-metaplasia) nyálkahártya-károsodáshoz vezet. Duodenogastricus reflux A duodenumtartalom szintén károsítja a nyelőcső-nyálkahártyát. A konjugált epesavak sósav és pepszin jelenlétében okoznak súlyos nyálkahártya-károsodást, míg a tripszin és a dekonjugált epesavak a savtól függetlenül is kifejthetik hatásukat. A sósav és az epesavak szinergista módon súlyosbítják az oesophagitist, és jelentős szerepet játszanak a Barrett-metaplasia kialakulásában.
10 124 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 125 taktusidő hatására klinikai tünetek és makroszkópos elváltozások jönnek létre a nyelőcsőben. A fiziológiás savas reflux élettani jelenség, amely egészséges egyénekben semmilyen tünetet nem okoz, viszont a nyelőcső hiperszenzitívitása esetén gyomorégést generálhat. A klinikai tünetek és a savas refluxepizódok között ezekben az esetekben pozitív korreláció áll fenn, ez magyarázza a sósavszekréció-gátló szerek kitűnő terápiás hatásosságát. Gyengén savas reflux esetén a refluxátum ph-ja 4 és 7, nem savas (alkaliás) reflux esetén > 7,4 feletti tartományba esik. Volumen- vagy gázrefluxról beszélünk, amikor nem a kémhatás, hanem a refluxátum volumene vagy a regurgitált gáz által létrehozott disztenzió váltja ki a klinikai tüneteket. A klinikai tünetképződés mechanizmusa Az általános patogenetikai hasonlóságokon túl a GERDalcsoportok patogenezisében lényeges különbségek is felfedezhetők, amelyek különösen markánsan nyilvánulnak meg a klinikai tünetek létrejöttében. Az ERD patogenezisében a döntő etiológiai faktor az excesszív sósav- és pepszinexpozíció, a patológiás savas reflux az esetek 75%-ában áll fenn, NERD esetében csak a betegek mintegy 50%-ában igazolható patológiás savas reflux. A fennmaradó esetekben fiziológiás savas, gyengén savas, alkaliás, volumen- vagy gázreflux váltja ki a gyomorégést. A klinikai tünetek létrejöttében ezekben az esetekben az érzőidegek perifériás és centrális szenzitizációja játszik szerepet, amelynek következtében a nyelőcsőbe jutó refluxátum akár savas vegyhatás hiányában is gyomorégést vált ki. Oesophagus ballondisztenziós vizsgálatokkal igazolták, hogy ezen betegek oesophagusa szignifikánsan szenzitívebbnek bizonyult a kontrollcsoporténál. Az atípusos tünetek képződésének patomechanizmusa szintén komplex. A reggeli rekedtségért a reflux okozta, krónikus laryngeális irritáció a felelős. A globus pharyngeus kiváltásában a reflux okozta felső oesophagus sphincter spazmusának szerepét feltételezik. A respiratórikus tünetek közül a krónikus köhögés létrejöttében az esetek egy részében a reflux okozta laryngitis a felelős, a laryngitissel nem járó esetekben csökkent köhögési ingerküszöb volt igazolható kapszaicininhaláció során, a köhögést feltehetőleg az ún. oesophagotracheobronchiális reflex triggereli. Asthma bronchialéban a bronchospazmus kiváltásában a főleg éjszaka jelentkező mikroaspirációk mellett szintén a fenti reflexmechanizmus játszik szerepet. A nyelőcsőeredetű mellkasi fájdalom (nem kardiális mellkasi fájdalom) prevalenciája a felnőtt átlagpopulációban meghaladhatja a 20%-ot. Klinikai jelentőségét az adja, hogy a fenti panaszokkal jelentkező betegekben mellkasi fájdalomnak csupán 15 34%-a bizonyul szíveredetűnek, a betegek döntő többségében a fájdalom a refluxbetegség következménye. A nyelőcsőeredetű mellkasi fájdalom mechanizmusa szintén komplex, számos részletében feltáratlan. A savas reflux okozta tartós oesophaguskontrakció magyarázhatja a fájdalmat az ERD-es betegek egy csoportjánál. A betegek másik csoportjánál (x-szindrómás betegek: típusos anginás panaszok, pozitív terheléses EKG, normális koronária angiogram), a nyelőcső sósav-instillációja (Bernsteinteszt) oesophagocardialis reflexmechanizmussal valódi koronáriaspazmust provokálhat következményes anginával, amit a szakirodalom linked anginának nevez. Nyelőcsőeredetű mellkasi fájdalom jelentkezhet azonban azon NERD-betegeknél is, akiknél patológiás reflux nem igazolható. A római kritériumok szerint a funkcionális mellkasi fájdalom keletkezésének mechanizmusa hasonló a többi funkcionális kórképben észlelhető fájdalom keletkezési mechanizmusához: a fiziológiás savas reflux eddig még nem ismert mechanizmussal a nociceptív C-rostok és a szenzoafferens pályák hiperszenzitizációját idézik elő szekunder allodynia kialakulásával. A visceralis hiperszenzitívitás mellett abnormális centrális percepció is szerepet játszik a tünetek létrejöttében, amelyet az oesophagus elektromos stimulációja kapcsán EEG-vel regisztrált kortikális kiváltott potenciálmérésekkel igazoltak. A szenzoafferens pályák hiperszenzitívitása kialakulásának mechanizmusa jelenleg pontosan nem ismert. Azt tudjuk, hogy a nyelőcső szenzoros innervációjában vagus (paraszimpatikus) és spinalis (szimpatikus) rostok vesznek részt. A vagus izomrétegek között elhelyezkedő receptív végkészülékei a mechanikus disztenzió közvetítésében, a submucosában elhelyezkedő receptorai a polymodalis vagusafferenseken keresztül közvetítik a különböző kémiai és mechanikai intraluminális impulzusokat. Normális esetben ezek a rostok nem játszanak szerepet a visceralis fájdalom percepciójában, bár kétségtelenül van fájdalommoduláló hatásuk. A spinalis afferensek receptorai (visceralis nociceptorok) mechano- és kemoszenzitívek, a disztenzió és az intraluminális sav által kiváltott fájdalom közvetítésében játszanak szerepet. A savas és nem savas ingerek, a volumen okozta disztenzió és a motoros történés okozta stimulus a gerincvelő hátsó szarván keresztül jut el a kérgi struktúrákhoz, ahol a stimulusok tünetként (gyomorégés, mellkasi fájdalom stb.) jelenítődnek meg. A stimulusok közvetítésében szerepet játszó neurotranszmitterek közül a kalcitonin génkapcsolt peptid és a substance P emelhető ki. A szenzoafferens pályák hiperszenzitizációja következtében az egyébként normális körülmények között tünetet nem okozó stimulus (fiziológiás savas reflux, ph-változás, kisfokú volumendisztenzió vagy motoros történés) is klinikai tünetet vált ki, míg normoszenzitív vagy hiposzenzitív, szenzoafferens pályák esetén a patológiás, savas refluxtörténések sem okoznak pl. gyomorégést. Ez a jelenség a magyarázata az ún. silent GERD fogalomnak, amely különösen megnehezíti az olyan, extraoesophagealis tüneteket okozó GERD diagnózisát, ahol a gyomorégés mint jelzőrendszer, éppen ezen pályák hiposzenzitívitása miatt, hiányzik. Mivel a tüneti percepcióban a központi idegrendszer szerepe döntő tényező, minden, a központi idegrendszert érintő pszichológiai komorbiditás (anxietas, stressz, depresszió stb.) tünetamplifikáló tényezőként szerepelhet. Ezen betegek hajlamosak arra, hogy túlzott (excesszív) figyelmet fordítanak a normál egyének által nem is észlelt oesophageális történésekre (a jelenséget hipervigilanciának nevezi az irodalom), amelyeket a fenti komplex mechanizmus révén drámai klinikai tünetként élnek meg. Ajánlott irodalom Fass, R, Ofmann, JJ: Gastroesophageal reflux disease Should we adopt a new conceptual framework? Am J Gastroenterol, : Lonovics J, Simon L, Wittmann T: A GERD patogenezisének modern szemlélete, erozív és nem erozív formák (ERD és NERD). Háziorv Továbbk Szle 7: ; Quigley, E: Non-erosive reflux disease: part of the spectrum of gastro-oesophageal reflux disease, a component of functional dyspepsia, or both? Eur J Gastroenterol Hepatol, : S13 S18. Richter, JE: Gastroesophageal reflux disease and its complications. In Feldman M, Friedman LS, Brandt LJ (eds): Sleisenger and Fordtrans s Gastrointestinal and Liver Disease. Philadelphia, 2006, Saunders Elsevier, Vakil, N, van Zanten, SV, Kahrilas, P et al.: The Montreal definition and classification of gastroesophageal reflux disease: A global evidence-based consensus. Am J Gastroenterol, : A refluxbetegség klinikai tünetei Rosztóczy András Bevezetés A gastrooesophagealis refluxbetegség tünettanában megkülönböztetünk típusos és atípusos tüneteket; az utóbbiak származhatnak a nyelőcsőből (oesophagealis) vagy lehetnek nyelőcsövön kívüli (extraoesophagealis) eredetűek. A GERD diagnosztikájában a klinikai tünetek helyes értékelése kiemelt jelentőségű, mivel típusos tünetek fennállása esetén alarmtünet hiányában első lépésben eszközös vizsgálatok végzése nem szükséges. Ilyen esetekben a diagnózist felállíthatjuk a klinikai tünetek és/ vagy a pozitív PPI terápiás teszt alapján. Külön figyelmet érdemelnek az úgynevezett alarm vagy vészjelző tünetek, amelyek fennállása esetén mindig gondolni kell az alapbetegség szövődményeire vagy egyéb organikus (malignus) betegségre. Ilyen esetekben a beteg részletes gasztroenterológiai kivizsgálása szükséges (3-5. táblázat). Típusos tünetek Gyomorégés (pyrosis, heartburn) A gastrooesophagealis refluxbetegség típusos tünete a szegycsont mögött, a mellkas középvonalában a gyomorszájtól a garat felé terjedő meleg, égő, maró érzés. Kisugározhat a nyak, az áll, a lapockák és a karok felé. Ez az enyhe forma fájdalomba is átcsaphat, ilyenkor vizsgálatok nélkül nem mindig lehet elkülöníteni a szívkoszorúerek keringési zavara által okozott anginás fájdalomtól. Kiváltásában a nyelőcső-nyálkahártyát érő sósav-, illetve epesav-expozíciónak van szerepe. Jellemzi kialakulását, hogy étkezés után, laposan fekvő helyzetben, illetve a hasi nyomás fokozódásakor (pl. lehajlás, emelés) jelentkezik. Savközömbösítő szer (antacidum) bevétele jellemzően azonnal enyhíti vagy szünteti. Gyakran társul regurgitációval vagy respiratorikus tünetekkel. Elkülönítése egyes atípusos esetekben nehézséget okozhat a gyomor-, 3-5. táblázat. A GERD tünettana Típusos tünetek Gyomorégés Savas felböfögés Atípusos tünetek Nyelôcsô eredetû (oesophagealis) Dysphagia Odynophagia Mellkasi fájdalom (NCCP) Nyelôcsövön kívüli eredet (extraoesophagealis) Kardiális tünetek: mellkasi fájdalom (linked-angina), ritmuszavarok, vezetési zavarok Légúti (felsô/alsó) tünetek: globusérzés, torokégés/kaparás, garatfalon váladékérzés, rekedtség, hangfáradékonyság, laryngospasmus, krónikus köhögés, asztma Szájüregi tünetek: nyáladzás, szájszag, fogérzékenység, fogeróziók Alvászavarok: elalvási zavar, felriadás, mikroébredés, fáradékonyság, nappali álmosság Alarmtünetek Dysphagia/Odynophagia Hányás Fogyás Vérszegénység Okkult vagy manifeszt vérzés
11 126 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 127 a nyombélfekély, illetve a diszpepsziák által okozott hasonló panasztól. Regurgitáció Tipikusan a nyelőcső betegségeire jellemző tünet, folyamata során a gyomor/duodenumbennék visszajut a nyelőcsőbe vagy akár a szájüregbe. A gastrooesophagealis refluxbetegséghez társuló savas vagy esetenként epés regurgitáció gyakran okoz jellegzetes, maró, égő érzést a nyelőcsőben. Szájüregig terjedése keserű, savas szájízt okoz. Elsősorban a postprandialis időszakban vagy testhelyzetváltozásra (lehajlás, lefekvés, nehéz tárgy emelése) jelentkezik. Differenciáldiagnosztikai szempontból lényeges, hogy megjelenési formája sok esetben utal valószínű okára. Súlyos nyelőcsőszűkületet okozó peptikus vagy korrozív strictura, illetve tumor esetén a regurgitáció gyakran társul dysphagiával, ilyenkor a lenyelt étel rövid időn belül szinte változatlan formában regurgitál. Előrehaladott stádiumban levő achalasia, illetve nagyobb diverticulum jelenlétekor a regurgitáció kevésbé szorosan kötődik az étkezés folyamatához. A lenyelt étel hoszszabb időn át (akár napokig) panghat a tágult nyelőcsőben, illetve a diverticulumban. A regurgitáció ezen fajtájához így nem ritkán társul foetor ex ore. Dysphagia A dysphagia fájdalmatlan nyelési nehezítettséget jelent, amelyet a beteg általában a lenyelt falat elakadásaként él meg. Mindig alarmtünetként értékelendő, hiszen súlyos szövődményt (strictura) vagy egyéb organikus eltérést (carcinoma) jelezhet. Az esetek többségében azonban a refluxbetegség jelenlétekor nem találunk organikus okot hátterében. Gyakran társulhat a GERD egyéb oesophagealis és extraoesophagealis tüneteivel. Intermittáló, enyhe formája jelenthet lassult tranzitot, progresszivitása azonban organikus eltérésre utal. Ilyenkor egyre gyakrabban és egyre kisebb falatok nyelése is nehezített, majd végül már a folyadék lenyelése is akadályozott. El kell különíteni a fájdalmas nyelést jelentő odynophagiától, amely inkább a gyulladásos megbetegedések, illetve a spasztikus motilitászavarok kísérő tünete. Sok, elsősorban idősebb beteg hosszú időn át hajlamos elhanyagolni kisebb-nagyobb fokú nyelési nehezítettségét, mert azt az öregedés természetes velejárójának tartja. Differenciáldiagnosztikai szempontból lényeges, hogy a dysphagia jelentkezhet szilárd, folyékony vagy mindkét típusú étel nyelésekor. A mechanikus obstrukció típusos esetben szilárd étel nyelésekor okoz panaszt. Ilyenek leggyakrabban a hús, a friss fehérkenyér vagy az alma. A folyamat jellemzően progresszív, intra- és extraluminalis obstrukció egyaránt létrehozhatja. Intraluminalisan obstrukciót elsősorban peptikus, gyulladásos vagy korrozív stricturák, jó- és rosszindulatú daganatok, nyálkahártyagyűrűk (pl. Plummer Vinson-szindróma, Schatzki-gyűrű), illetve idegentest okozhatnak. Extraluminalis kompresszió hátterében nyaki vagy mediastinalis tumorok, megnagyobbodott nyirokcsomók, feltelődött nagy diverticulum (leggyakrabban Zenker-féle), pajzsmirigymegnagyobbodás vagy vaszkuláris rendellenesség (pl. aortaaneurysma, rendellenes lefutású jobb arteria subclavia) jelenlétére kell gondolni. A dysphagia progresszivitása esetén alapvető fontosságú a malignus térszűkítő folyamat mielőbbi kizárása. A falat elakadási helyének szubjektív megítélése organikus ok esetén általában jól egyezik annak tényleges lokalizációjával. Átlagos méretű szilárd bolus lenyelése esetén 13 mm alatti nyelőcsőátmérőnél mindig, mm közt gyakran, míg 20 mm felett igen ritkán fordul elő a falat elakadása. Dysphagia esetén az endoszkópia az elsődlegesen választandó vizsgálat! A szilárd és folyékony étel által egyaránt kiváltott nem progresszív dysphagia elsősorban motilitási zavarok következménye. Oropharyngealis dysphagia esetén elsősorban szekunder (neurogén, muszkuláris) eredetre kell gondolni. A magas dysphagia elkülönítése a pharynx régiójában manifesztálódó egyéb tünetektől (pl. globusérzés, postnasalis drip) gondos anamnézisfelvételt igényel, mert a betegek ezeket is gyakran említik nyelési panaszként. Jellemző különbség azonban, hogy utóbbiak étkezéstől függetlenül, általában az egész nap folyamán, szinte változatlanul jelen vannak. A distalis esetekben nyelőcső (cardia) tumor, achalasia cardiae, diffúz nyelőcsőspazmus, diótörő-nyelőcső, hipertenzív alsó nyelőcsősphincter lehetősége merül fel. Odynophagia Az odynophagia fájdalmas nyelést jelent, ami típusos esetben gyulladásos folyamatot valószínűsít, de spasztikus jellegű motilitási zavarok (cricopharyngealis hypertensio, diffúz nyelőcsőspazmus, diótörő-nyelőcső, achalasia cardiae, alsó nyelőcsősphincter-hypertonia) vagy idegentest jelenléte is teljesen hasonló panaszt okozhat. Atípusos vagy extraoesophagealis tünetek Mellkasi fájdalom Mellkasi fájdalom gyakran jelentkezik gastrooesophagealis refluxbetegségben, mégsem sorolható annak típusos tünetei közé, hiszen egyrészt más nyelőcső-motilitási zavarokban (diótörő-nyelőcső, diffúz oesophagusspazmus, achalasia) is előfordul, másrészt jellege teljesen hasonló lehet a kardiális eredetű mellkasi fájdalomhoz. Éppen ezért első lépésben mindig kizárandó a mellkasi fájdalom kardiális eredete, majd ezt követően indokolt lehet egyéb (pulmonalis, mozgásszervi) okok kizárása is. A differenciáldiagnosztikát tovább nehezíti, hogy a savas reflux, az úgynevezett oesophagocardialis reflex révén maga is képes koronáriaspazmust, következményes myocardialis ischaemiát és mellkasi fájdalmat előidézni (linked-angina). A fájdalom nyelőcsőeredetét (esophageal chest pain, non-cardiac chest pain) támogathatja az étkezéssel, testhelyzetváltozással (lehajlás, lefekvés) való összefüggés, illetve, ha más nyelőcsőbetegségre jellemző tünettel együtt fordul elő (3-6. ábra). Légúti tünetek A különböző légúti tünetek önmagukban csak részletes, negatív eredményű pulmonológiai és laryngológiai kivizsgálás után utalhatnak refluxbetegségre. Bár a refluxbetegség egyéb tüneteihez (pl. regurgitáció, gyomorégés, mellkasi fájdalom, dysphagia) is társulhatnak, előfordul, hogy egyedüli tünetként jelentkezve jelentősen megnehezítik a háttérben megbújó refluxbetegség felismerését. Jellemző lehet napszaki megoszlásuk, például éjszaka jelentkező fulladás, reggeli köhögés. Patogenezisükben a sav krónikus mikroaspirációja által okozott direkt irritatív hatás és vagovagalis reflexmechanizmusok (pl. oesophagobronchialis reflex) játsszák a főszerepet. A savas refluxnak inkább az alsó léguti (pl. asztma), míg a gyengén savas epizódoknak a laryngealis tünetek kiváltásában tulajdonítanak jelentőséget. Globusérzés A GERD gyakori extraoesophagealis tünete. Globusérzés alatt a garatban jelentkező, fájdalmatlan, de a beteget zavaró csomó vagy gombóc érzését értjük. Szemben a dysphagiával, étkezéskor javul vagy megszűnik. A tünetképződés mechanizmusa nem ismert, mindössze annyi bizonyos, hogy az esetek többségében nem igazolható súlyos fokú proximalis savas reflux jelenléte. Ezért ma elsősorban a gyengén savas refluxepizódok, illetve reflexmechanizmus szerepét feltételezik létrejöttében. A tünet általános jellegzetességeit részletesen lásd A nyelőcső funkcionális megbetegedései című alfejezetben. Szájüregi tünetek cím 3-6. ábra. A mellkasi fájdalom etiológiája Ábramagyarázat. GERD: gastrooesophagealis refluxbetegség; ISZB: ischaemiás szívbetegség; AP: angina pectoris; NCCP: nem szíveredetû mellkasi fájdalom. A szájüregi tünetek jelentkezhetnek a fogakhoz, illetve a lágyrészekhez kapcsolódóan. A fogakon megjelenő tünet az erózió, amely GERD esetén dominálóan a felső fogsort érinti, és a fogak belső palatinalis, illetve occlusalis felszínén jelenik meg. A lágyrészekhez kapcsolható tünetek a szájégés, savas szájíz, nyáladzás, kellemetlen szájszag. A jellegzetes lokalizációjú fogeróziók kiváltásáért a masszív, proximális savas reflux a felelős. Differenciáldiagnosztikai szempontból a GERD mellett a ruminatio-szindróma, illetve a krónikusan fennálló, ismétlődő hányással járó kórképek (pl. anorexia, bulimia) jönnek szóba. Jóval bonyolultabb a helyzet a lágyrésztünetek vonatkozásában, amelyek oka számos egyéb kórkép is lehet, így krónikus gyulladások, szisztémás betegségek (pl. Sjögrenszindróma), sőt a megváltozott szenzitivitás és percepció (pl. szájégés esetén). Alvászavarok A reflux okozta alvászavarok egyrészt felébredéshez köthető oesophagealis (pl. gyomorégés, regurgitáció) és légúti (pl. köhögés, fulladás) tünetekben, másrészt felébredéssel nem járó, kóros alvás alatti eseményekben (mikroarousal, repetitív obstruktív alvási apnoe, horkolás) nyilvánulnak meg. Mindkét tünetcsoport eredménye a csökkent nappali vigilancia és teljesítőképesség. Alarmtünetek Hányinger, hányás Aspecifikus tünet, ami refluxbetegségben a szövődményként kialakuló strictura vagy malignizálódás következménye. Elkülönítése a regurgitációtól fontos, de gyakran nem könnyű feladat. Az erős hányás ugyanakkor oka lehet a nyelőcső sérüléseinek (pl. Mallory Weiss-szindróma, Boerhaave-szindróma) vagy nyelőcső-varicositas esetén varix ruptúrához is vezethet. Vérzés, vérszegénység A GERD tünettanában ritka a vérzés előfordulása, azonban az minden esetben súlyos erozív oesophagitisre, illetve nyelőcsőfekélyre utal. Más gasztrointesztinális vérzésekhez hasonlóan lehet manifeszt vagy okkult, és következményes vérszegénységet, illetve gyengeséget vonhat
12 128 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 129 maga után. Ha van mód az anamnézis felvételére, akkor a társuló tünetek alapján általában valószínűsíthető a vérzés oka, de pontos választ sokszor csak az endoszkópos vizsgálat elvégzése után kapunk. Masszív akut vérzés obligát velejárója a haematemesis, majd a nem sokkal később megjelenő melaena. Az okkult vérzés és a hozzá társuló vashiányos anaemia a nyelőcső esetében is főleg malignus tészűkítő folyamatra utal, még akkor is, ha nem társul hozzá dysphagia vagy más tünet. Gyengeség, fogyás Legtöbbször más tünetekkel együtt fordulnak elő a refluxbetegségben. Megjelenése a betegség előrehaladott stádiumát, oesophagealis szövődmény (fekély, strictura, adenocarcinoma) jelenlétét valószínűsíti. A refluxbetegség diagnózisa Rosztóczy András A GERD diagnózisa, illetve a betegnek a GERD adott alcsoportjába történő besorolása egyrészt a tünetek értékelésén, másrészt eszközös vizsgálatok eredményén alapul. A ma alkalmazott diagnosztikus stratégia kialakulása egyrészt a kórképet jellemző epidemiológiai tényezőkre, másrészt a tünettan jellegzetességeire vezethető vissza. Tekintettel arra, hogy a GERD rendkívül gyakori, kiemelt jelentősége van az eszköz nélküli diagnosztikának. Ebben a kórképre jellemző fizikális vizsgálattal igazolható eltérés híján a kulcsfontosságú az anamnézis, a betegség tüneteinek értékelése. Anamnézis Az anamnézis felvétele a GERD rendkívül színes tünettana (oesophagealis és extraoesophagealis szimptomák) miatt nem könnyű feladat, ráadásul a típusos tünetek szubjektív súlyossága önmagában nem prediktív sem az oesophagealis, sem az extraoesophagealis manifesztációk jelenlétére. Mivel a GERD diagnosztikus algoritmusai a kórképre jellemző típusos és atípusos tünetek, illetve szövődmények jelenlétén vagy hiányán alapulnak, ezért kiemelt fontossága van az anamnézisfelvétel során a pontos és lehetőség szerint standardizált adatgyűjtésnek, hiszen ez dönti majd el, hogy kinek van szüksége az eszközös diagnosztika elemeinek igénybevételére. Az anamnézis felvételét, standardizálását segítő validált kérdőívek (pl. ReQuest) segíthetik a GERD diagnózisának felállítását, azonban szerepük inkább a kontrollált klinikai vizsgálatokban a kezelés hatékonyságának lemérésében, a kórlefolyás nyomonkövetésében van. Protonpumpainhibitor-teszt (PPI-teszt) Szintén a tünetek értékelésén alapszik a GERD eszköznélküli diagnosztikájának másik fontos eleme a PPIteszt. Ennek során a beteg meghatározott időn keresztül, adott dózisú (alap vagy emelt adag) PPI-kezelést kap. A klinikai tünetek változása alapján állítható fel a diagnózis. Amennyiben a vizsgált típusos vagy atípusos tünet(ek) a terápiás teszt időtartama alatt megszűnnek, vagy a beteg megítélése alapján jelentősen mérséklődnek, a teszt pozitív, és az adott tünet(ek) kiváltásában a savas reflux kóroki szerepe bizonyítottnak tekinthető. Negatív esetben (nem változó tünetek) ennek megfelelően a savas reflux etiológiai szerepe valószínűtlen. Nem a PPI-teszt része ugyan, de a PPI-kezelés kapcsán merülhet fel a volumenrefluxnak nevezett jelenség gyanúja, amikor a beteg arról számol be, hogy a terápia hatására a pyrosis vagy a fájdalom megszűnt, de a regurgitáció fennmaradt. Típusos tünetek (gyomorégés, savas felböfögés) jelenlétekor amennyiben sem szövődményre utaló jele, sem alarmtünete nincs a betegnek első lépésben nincs szükség eszközös vizsgálatok végzésére. A diagnózis ilyenkor felállítható kéthetes időtartamú, alapdózisban alkalmazott PPI-teszt elvégzésével. Ennek során a típusos refluxos tünet megszűnése, illetve jelentős regressziója bizonyítja a savas reflux kóroki szerepét (3-7. ábra). Atípusos tünetek esetében a terápiás teszt ideje hoszszabb. Mellkasi fájdalom (non-cardiac chest pain) esetében 8 hét; krónikus köhögés, asztmás légzészavar, illetve egyéb légúti tünet esetében 12 hét. A teszt elvégzéséhez emelt dózisú (alapdózis naponta 2-szer) PPI adása szükséges (MGT konszenzus 2002.). Szövődmény gyanúja, illetve alarmtünet fennállása esetén az első lépésben kötelező az endoszkópos vizsgálat, szükség esetén szövettani mintavétellel kiegészítve (3-8. ábra). Endoszkópia Endoszkópos vizsgálattal dönthető el, hogy a refluxbetegség erozív vagy nem erozív formájáról van-e szó, felderítheti a hiatus hernia jelenlétét, illetve ezzel a vizsgálattal lehetséges a Barrett-metaplasia felismerése is. Ezért javasolt a refluxbetegek gondozása során legalább egyszer az endoszkópia ( once-in-a-life-endoscopy ) elvégzése. Nyelőcsőfunkciós vizsgálatok A refluxbetegség és elsősorban a NERD színes patofiziológiai háttere miatt előtérbe kerültek a nyelőcsőfunkció diagnosztikai eszköztárának elemei, amelyek segítségével igazolhatók és tipizálhatók az adott esetet jellemző rendellenességek. E vizsgálatok elsődleges célja a gastrooesophagealis reflux jelenlétének, formájának (savas, nem savas, epés, folyadék, gáz), kiterjedésének (distalis, proximalis), illetve a panaszokkal való ok-okozati összefüggésének a bizonyítása. A nyelőcsövet érő reflux megjelenési formájának leírására a nyelőcső 24 órás ph-metriás, Bilitec és impedanciaméréses vizsgálatai szolgálnak, míg a motilitászavar tipizálása a nyelőcső-manometriával lehetséges. Mivel az egyes módszerek részletes leírása a 11. fejezetben olvasható, ebben a fejezetben csak a módszerek legfontosabb ismérveit említjük táblázat. Diagnosztikus algoritmus típusos tünetekkel járó, szövôdménymentes GERD esetén 3-8. táblázat. Diagnosztikus algoritmus a GERD atípusos, illetve szövôdményes eseteiben
13 130 Gaszt ro en te ro ló Gia A nyelôcsô betegségei órás intraoesophagealis ph-metria, impedancia, illetve a bilirubin monitorozása A 24 órás ph-metriás vizsgálat a nyelőcső savexpozíciójának mérésére szolgál. Segítségével meghatározható a ph < 4 alatti savas reflux mértéke, napszaki megoszlása, tünetekkel való összefüggése, illetve többcsatornás mérés esetén proximális kiterjedése (3-9. ábra, ábra). Nem informál viszont a gyengén savas, nem savas és biliáris reflux jelenlétéről. A ph-mérő kapszulás formája a Bravo-rendszer, amely 24 órát meghaladó (max. 96 órás) méréseket is lehetővé tesz. A gyengén savas és nem savas reflux mértéke a 24 órás kombinált nyelőcső-ph--impedanciaméréses vizsgálattal határozható meg. E módszer segítségével különbség tehető folyadék- és gázhalmazállapotú refluxátum között is (3-11 ábra) ábra. Gyengén savas reflux 3-9. ábra. 24 órás intraoesophagealis ph-metria fiziológiás reflux ábra. 24 órás intraoesophagealis ph-metria patológiás reflux ábra. Biliáris reflux
14 132 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 133 Az epés reflux kimutatására csak a 24 órás bilirubinmonitorozás (Bilitec 2000) használható, amely fotometriás úton azonosítja a nyelőcsőbe regurgitáló epét (3-12. ábra). Fontos megjegyezni, hogy az epés reflux ritka kivételtől eltekintve nem alkalikus, mivel a regurgitáló epe enyhén lúgos kémhatását az erősen savas karakterű és volumenében is jelentősebb gyomorszekrétum savassá változtatja, mielőtt az a nyelőcsőbe jut. Nyelőcső-manometria A nyelőcső manometriás vizsgálata nem tartozik a GERD-diagnosztika alapelemei közé. Elsősorban atípusos tünetek, terápiára rosszul reagáló esetek, illetve az antirefluxműtétet megelőző kivizsgálás részeként alkalmazzák. Refluxbetegségre jellemző tipikus manometriás eltérések a rövidült, proximalis irányban diszlokált alsó nyelőcsősphincter, amelynek nyomása csökkent és relaxációja megnyúlt. A nyelőcsőtestben pedig, elsősorban a distalis szakaszon, csökken a perisztaltikus hullámok amplitúdója. Lényeges, hogy a standard, éhomi állapotban végzett manometriás vizsgálat negatív eredménye nem zárja ki refluxbetegség fennállását, hiszen a betegség egyik fontos patofiziológiai tényezőjéről, a postprandialis időszak tranziens relaxációiról nem kapunk információt. Egyelőre nem tisztázott, hogy a közelmúltban bemutatott új vizsgálóeljárások a nagy felbontású manometria (HRM), illetve az alsó nyelőcsősphincter kompetenciáját vizsgálni képes endofliptechnika mennyiben változtatják meg a diagnosztikát, illetve a klinikai döntéshozatal menetét gastrooesophagealis refluxbetegségben. Báriumnyeletéses röntgenvizsgálat A nyelőcső radiológiai vizsgálata gastrooesophagealis refluxbetegségben fontos kiegészítő adatokkal szolgálhat. Segítségével információ nyerhető a volumenreflux jelenlétéről, valamint minden egyéb módszernél pontosabban írja le a GERD fontos patogenetikai faktorát jelentő hiatus herniát. A módszer a dysphagiával járó nyelőcső-motilitási zavarok felismerésében is segítséget jelenthet, megfelelő kivitelezés esetén. Ilyenkor a nyelési próbát érdemes többféle (folyékony, félfolyékony, illetve szilárd) kontrasztanyaggal is elvégezni. Segítséget jelenthet a testhelyzet változatása is, hiszen a motilitási zavarok egy része (gastrooesophagealis reflux, nyelőcsőtest aperistalsis) fekvő vagy Trendelenburg-helyzetben könnyebben ábrázolható. A vizsgálat értékelése videóval, cinematográffal vagy újabban számítógépes digitális sorozatkép-rögzítéssel tehető pontosabbá. A GERD diagnosztikájában korábban viszonylag széles körben alkalmazott izotópnyeletéses technikák szerepe marginális, a gyakorlatban jelenleg csak elvétve használatosak. Bernstein-teszt A refluxdiagnosztika egyik legrégebbi eleme, amelyet a névadó szerző első, 1958-as közlése óta többször is módosítottak, de a vizsgálat alapja mindmáig változatlan. A nyelőcső középső harmadába orron át levezetett szondán keresztül felváltva 0,1 N sósavat és fiziológiás sóoldatot perfundálunk oly módon, hogy sem az orvos, sem a beteg nem tudja, melyik oldat perfúziója zajlik. A vizsgálat pozitív, ha a beteg típusos panasza (gyomorégés, mellkasi fájdalom) a sósav perfúziójával kiváltható. A teszt specificitása 90% körüli. Segítségével igazolható a nyelőcső hiperszenzitivitása, a savas reflux és a tünetképződés közti ok-okozati összefüggés. Új, továbbfejlesztett változatainak (Bernstein-teszt + echocardiográfiás koronária-véráramlásmérés, illetve Bernstein-teszt + metakolin provokációs légzésfunkció-vizsgálat) a reflexmechanizmusokon alapuló extraoesophagealis manifesztációk (oesophagocardialis, illetve osophagobronchialis reflex) jelenlétének bizonyításában van szerepe. A refluxbetegség terápiája Rosztóczy András Bevezetés A refluxbetegség kezelésében háromféle terápiás modalitás alkalmazása jön szóba: a refluxbetegség enyhébb formáiban életmódbeli változtatások segíthetnek a tünetek enyhítésében, azonban ezek hatékonyságát kontrollált klinikai vizsgálatokkal eddig még nem ellenőrizték. A hatékony terápia alapját a gyógyszeres kezelés jelenti, amelyek közül legköltséghatékonyabbnak a PPI-szerek bizonyultak. Bizonyos jól megválogatott esetekben a sebészi antirefluxműtétek reális terápiás alternatívát jelenthetnek. Életmódi javaslatok Fiziológiai vizsgálatok igazolták, hogy az életmódbeli változtatások az ágyfej megemelése, súlycsökkentés, dohányzás, szoros ruházat, alkohol, zsíros ételek, szénsavas italok, citrusfélék kerülése, vacsora utáni lefekvés vagy éjszakai nassolás elhagyása javíthatják a nyelőcső savclearance-ét, csökkenthetik a savas refluxepizódokat és a gyomorégést. Bár hatékonyságukat kontrollált klinikai vizsgálatokkal nem ellenőrizték, a tapasztalatok alapján önmagukban csak az enyhe esetek fenntartó kezelésére elégségesek. Egyéb esetekben pedig a gyógyszeres terápia kiegészítéseként alkalmazhatók. Fontos felhívni a refluxbetegek figyelmét, hogy kerüljék az olyan gyógyszerek alkalmazását, amelyek a LES-nyomást csökkentik (α-adrenerg bénítók, antikolinerg szerek, kalcium-antagonisták, teofillin, diazepam, barbiturátok stb.). Amennyiben mégis szükséges ilyen szereket alkalmazni, azt effektív PPI-védelemben kell megtenni. Gyógyszeres kezelés A refluxbetegség a felső gasztrointesztinum komplex motilitászavarán alapuló kórkép, ezért elvileg a GERD oki terápiáját a motilitászavar normalizálása jelentené. A motilitászavar rendezésére hosszú ideig a prokinetikumok (metoclopramid, domperidon, cisaprid), újabban a baclofen és származékai adásával kísérleteztek, azonban nem megfelelő hatékonyságuk és mellékhatásaik miatt jelentőségük háttérbe szorult. Ma már monoterápiában egyáltalán nem alkalmazzuk őket, a GERD bizonyos extraoesophagealis manifesztációinak (légúti tünetek) kezelésében szóba jöhet PPI-kal való kombinációjuk (a cisaprid kivételével). Tekintettel arra, hogy a refluxbetegség patogenezisében a savas refluxátum döntő tényező, ezért ma a refluxbetegség típusos és atípusos tüneteinek, a morfológiai eltéréseknek és szövődményeinek terápiájában a PPI (omeprazol, pantoprazol, lanzoprazol, esomeprazol, rabeprazol) kezelés vált egyeduralkodóvá, gyakorlatilag kiszorítva a korábban alkalmazott H 2 -receptor-antagonistákat. Mivel a refluxbetegség alcsoportjainak (NERD, ERD, Barrett-oesophagus) tárgyalásánál részletesen ismertetjük a kezelési stratégiákat, ebben a fejezetben csupán a refluxbetegség kezelésének általános szabályairól szólunk. Iniciális és fenntartó kezelés A GERD kezelésében megkülönböztetünk egy iniciális és egy fenntartó kezelési szakot. Az iniciális kezelési szakasz időtartama változó attól függően, hogy a típusos vagy atípusos tünetek megszüntetése a cél, vagy a morfológiai elváltozások és szövődményeinek kezelésére irányul. A típusos tünetek, mint a gyomorégés és savas regurgitáció PPI-kezelés hatására napok alatt megszűnnek. Amennyiben NERD-ről van szó, általában 4-6 hetes iniciális szakasz után lehet áttérni a fenntartó kezelésre. Ez csak a kórkép enyhe formái esetén lesz sikeres. Atípusos tünetek esetén az iniciális szakasz lényegesen hosszabb, pl. mellkasi fájdalom esetén 8 hét, légúti tünetek esetén legalább 12 hét, és mindig emelt PPI-dózisok alkalmazása szükséges. Erozív oesophagitis esetén az iniciális szakasz átlagosan nyolc hét, az időtartam és a dózis nagyban függ az erozív elváltozások (Los Angeles A-D) súlyosságától. Step-down stratégia Fenntebb említettük, hogy a GERD legköltséghatékonyabb kezelését a megfelelő dózisban alkalmazott PPI-k adása jelenti. Ez vonatkozik a fenntartó kezelésre is. A fenntartó kezelési dózisok meghatározása a step-down stratégia elvei szerint történik. Típusos tünetekkel járó szövődménymentes esetekben alap dózisú, iniciális PPIterápiát (omeprazol 20 mg, pantoprazol 40 mg, lanzoprazol 30 mg, esomeprazol 40 mg, rabeprazol 20 mg) követően a fenntartó kezelést a dózis megfelezésével indítjuk. Kititráljuk azt a dózist, amellyel a tünetmentesség fenntartható. Az esetek egy részében ritkán jelentkező típusos tünetek elérhető a gyógyszeres kezelés elhagyása is. Ebben a periódusban az ún. igény szerinti (on demand) kezelés végezhető. Ez a visszatérő, enyhe panaszok megszüntetésére irányuló, átmeneti gyógyszeres kezelést jelenti, amelynek során a beteg a legkisebb biztosan hatékony gyógyszeradagot használja a tünetek megszűnéséig. Ez elérhető PPI-k, H 2 -receptor-antagonisták, illetve a legenyhébb esetekben antacidumok adagolásával is. Atípusos tünetek vagy szövődmények esetén (oesophagealis és extraoesophagealis tünetek, strictura stb.) az induló terápia mindig emelt PPI (2-szer alapdózis) kezelést jelent. A fenntartó kezelés során itt is a stepdown-stratégia követendő, de a lépcsőfokok az aktuális szövődmény jellegének megfelelően hosszabbak. Szövődmények és extraoesophagealis manifesztáció esetén a PPI-kezelés elhagyása biztosan recidívához és a kórkép súlyosbodásához fog vezetni. A légúti tünetek esetén ritkán csökkenthető az emelt dózisú PPI adagja. Mellkasi fájdalom esetén a PPI fenntartó kezelés triciklikus antidepresszánsokkal, légúti tünetek esetén prokinetikumokkal kombinálható. Erozív refluxbetegségben a relapszus és a szövődmények kialakulása szintén csak PPI fenntartó kezeléssel védhető ki. Nyelőcsőtágítást követő stratégia Bármely okból (achalasia, strictura, stb.) végzett nyelőcsőtágítás refluxra hajlamosító állapotot teremt. Ezekben a betegekben a savas reflux károsító hatásának kivédése céljából megfelelő dózisban alkalmazott PPI-kezelést kell kezdeni. Achalasia esetén, ha a tágítás szövődményeként nem alakul ki másodlagos reflux, akkor PPI-kezelés nem indokolt. Strictura miatt végzett tágítás esetén azonban legtöbbször csak emelt dózisú PPI-kezeléssel tartható fenn a tünetmentesség, míg a kezelés abbahagyása szinte kivétel nélkül súlyos relapszushoz vezet! Az öngyógyítás problémája OTC-szerek Régóta ismeretes a refluxbetegséggel kapcsolatos, úgynevezett jéghegyhasonlat, amely jól érzékelteti, hogy a be-
15 134 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 135 A refluxbetegség típusos vagy atípusos tünetei hátterében akkor merül fel a NERD-entitás diagnózisa, amikor az elvégzett endoszkópos vizsgálattal a nyelőcsőben makroszkópos elváltozások (eróziók) nem igazolhatók. Folyton visszatérő dilemma, hogy valóban NERD-ről van-e szó, vagy a gyógyult ERD-et minősítjük NERD-nek. A választ a gondos anamnézisfelvétel és a betegek hosszú távú követése döntheti el. A mindennapi gyakorlatban a következő diagnosztikus modalitás a PPI-teszt: gyomorégés és savas regurgitáció esetén alapdózisú PPI 2 hetes, mellkasi fájdalom és extraoesophagealis tünetek esetén dupla dózisú PPI 8, illetve 12 hetes adagolásából áll. A pozitív teszt azt jelenti, hogy a klinikai tünetek és a savas reflux között oksági összefüggés áll fenn. Gyomorégésben szenvedő NERD-betegek mintegy 70%-ában a pozitív teszt igazolja a savas reflux etiopatogenetikai szerepét. A PPI-teszt negativitása esetén nem savas refluxról van szó, és mivel ezek a betegek nem, vagy nem megfelelően reagálnak a PPI-kezelésre, további diagnosztikus lépések szükségesek (Bilitec, impedanciavizsgálat, mategek csak egy kisebb része (a jéghegy csúcsa és a jéghegy víz feletti része ) kerül orvoshoz, a betegek jelentős hányada egyáltalán nem jut el orvoshoz, a betegségről az információkat vagy az írott vagy a vetített médiákon keresztül, vagy más betegektől szerzi be, és ennek alapján kezdeményezett, legtöbbször inadekvát kezelésben részesül. A betegek legtöbbje nem vényköteles (OTC: over the counter) készítményeket (antacidumok, H 2 -receptorantagonisták) használ, a szerencsésebbek megkérdezik a gyógyszerészt, aki legújabban már a PPI-kezelést hazánkban is ajánlhatja. Hazánkban az OTC-szerek közül egy PPI-készítmény pantoprazol (20 mg) kapható vény nélkül, amelynek utasítási leiratában szigorúan kéthetes kezelést javasolnak, ezt követően ajánlják, hogy a betegek forduljanak családorvosukhoz. A nem savas vagy gyengén savas, a volumen- vagy gázreflux okozta problémák kezelésére a további fejezetrészekben térünk ki. Az antirefluxműtét indikációi Az antirefluxműtét a refluxbetegség sebészi kezelését jelenti, amelyben a sebész a cardia zárófunkciójának helyreállítását műtéti úton biztosítja. A Nissen-féle fundoplikáció a leghatásosabb cardiazárófunkció-helyreállító eljárás, amelyet ma laparoszkópos technikával végeznek. A műtét lényege, hogy az intraabdominalis pozícióba visszahúzott distalis nyelőcsőszegment körül a gyomor fundusából laza, körkörös mandzsettát képeznek. A refluxbetegek döntő többsége kitűnően reagál protonpumagátló kezelésre, azonban különösen olyan fiatal betegekben, akik egész életükben PPI-kezelésre szorulnak, az antirefluxműtét költséghatékony megoldást jelent. Ugyanez vonatkozik bármely életkorú, ún. PPI-dependens betegekre, akiknél a tünetmentesség csak tartós PPI-adagolással oldható meg. További műtéti indikációt képeznek azok a betegcsoportok, akiknél a PPI-kezelés különböző okokból (volumenreflux, biliáris reflux, hiatus hernia) nem kellő hatékonyságú. Barrett-oesophagus (savas és biliáris reflux, hiatus hernia) és extraoesophagealis, főleg respiratórikus tünetek (PPI-kezelés mellett jelentős volumenreflux) esetén különösen kiválóak az antirefluxműtétek eredményei. Fontos megjegyezni, hogy az ilyen műtéteket csak a megfelelő nyelőcsőfunkciós vizsgálatok eredményei alapján, megfelelő műtéti tapasztalatokkal rendelkező centrumokban szabad végezni. Az endoszkópos antireflux-eljárások, amelyekben különböző módszerekkel (radiófrekvenciás ablatio, endoszkópos varratvonalképzés, endoszkópos injekciózási technikák stb.) próbálták az antireflux-barriert helyreállítani, nem váltották be a hozzájuk fűzött reményeket. A refluxbetegség alcsoportjainak sajátságai A nem erozív refluxbetegség (NERD) Lonovics János Bevezetés A nem erozív refluxbetegség a GERD olyan alcsoportja, amelynél a nyelőcsőben eróziók, illetve makroszkópos elváltozások nem mutathatók ki, ezért a NERD-et endoszkóposan negatív refluxbetegségnek is nevezik. A makroszkóposan ép nyelőcső ellenére a NERD-betegeknek az életminőséget súlyosan befolyásoló típusos és atípusos refluxtüneteik lehetnek. A GERD-alcsoportokat összehasonlítva a nyelőcső szenzitivitása a NERD-betegekben a legmagasabb, az extraoesophagealis tünetek prevalenciája is feltűnően magas. A klinikai tünetek szempontjából tehát súlyos hiba a NERD-et a refluxbetegség enyhe formájának tartani. Ez különösen igaz a terápia vonatkozásában, a NERD kezelése a patogenetikai heterogenitás miatt ma az egyik legnagyobb kihívást jelenti a gyakorló orvos számára. Epidemiológia A nem erozív refluxbetegség alcsoport a GERD-betegek mintegy 60-70%-át foglalja magában. A NERD-prevalencia az összlakosság 12%-ára tehető. Egy hazai felmérés alapján a NERD- és ERD-esetek megoszlása 69, illetve 31%-nak bizonyult. A NERD-betegek 75%-ának voltak típusos tünetei, 25%-ukban az extraoesophagealis tünetek domináltak. Nemzetközi felmérések szerint az extraoesophagealis tünetek gyakorisága közel azonos a refluxbetegség erozív (34,9%) és nem erozív (30,5%) formáiban. A NERD-betegek többsége nő, a betegek általában vékonyak, a fiatalabb korosztályból kerülnek ki, és nincs hiatus herniájuk Patogenezis A heterogenitás a patogenetikai tényezőket illetően a legkifejezettebb ebben az alcsoportban. Az antireflux-barrier károsodásban a TLESR-k frekvenciájának fokozódása szintén a legdöntőbb tényező. Az agresszív faktorok vonatkozásában azonban megjegyzendő, hogy a klinikai tünetek (gyomorégés) kiváltásában csak az esetek mintegy 50%-ában tehető felelőssé a patológiás savas reflux, az esetek másik 50%-ában a gyomorégés fiziológiás savas refluxtörténések mentén jön létre. Az utóbbi betegcsoportban maguk a fiziológiás savas refluxepizódok (17%) váltják ki a hiperszenzitív oesophagussal rendelkező betegekben a gyomorégést. Mivel ezekben az esetekben a savas refluxepizódok és a klinikai tünetek között szoros korreláció mutatható ki, érthető, hogy ezek a betegek jól reagálnak PPI-kezelésre. A betegek fennmaradó csoportjában (33%) gyengén savas vagy nem savas refluxtörténések, vagy azok volumenhatásai következtében létrejött disztenzió vagy motoros tevékenység vált ki gyomorégést. Természetesen ezekben az esetekben a savas refluxepizódokkal való tüneti korreláció hiánya miatt a PPI-kezelés többnyire hatástalan. Vannak olyan megfigyelések, hogy nyelőcső-ph minuciózus változásai is, azaz olyan phesés, amelynek során a ph nem csökken a 4 alatti értékre, is képes gyomorégést kiváltani. Martinez összefoglalaló elemzése alapján gyomorégést kiváltó patogenetikai tényezők alapján a NERD három alegységre osztható: 1. Patológiás savas NERD-alegység 2. Fiziológiás savas NERD-alegység Nem savas NERD-alegység (3-6. táblázat) Az utóbbi két csoportban a hiperszenzitív nyelőcső fontos szerepet játszik a tünetképződésben. Tack nevezéktana a patológiás savas refluxcsoportot nevezi valódi NERD -nek, a fiziológiás savas reflux által kiváltott tünetek esetén savérzékeny hiperszenzitív oesophagusról beszél, míg a savval nem korreláló tünetek esetén funkcionális gyomorégés elnevezést használ. A Martinez-féle nem savas refluxalegységet a Róma III. konszenzuskonferencia is funkcionális gyomorégés névvel illeti, amelynek fő kritériuma a savas reflux hiánya a gyomorégés létrejöttében, és a PPI-tesztre adott negatív válasz. A Róma III. konszenzuskonferencia szerint a NERD-betegek kb. 10%-a tartozik a funkcionális gyomorégéscsoportba, azzal a megjegyzéssel, hogy ez az arány a családorvosi környezetben valószínűleg nagyobb. A makroszkópos elváltozások (eróziók) hiányában sokáig nehéz volt magyarázni a klinikai tünetek patomechanizmusát. A legújabb vizsgálatok szerint NERD-ben az oesophagus nyálkahártya-rezisztencia károsodott, a sósav a tágult intercellularis réseken (DIS) keresztül, az érzőidegvégződéseket elérve aktiválja a kemoszenzitív nociceptorokat (feltehetőleg savérzékelő ioncsatornákat). Mindez, részben a gerincvelő hátsó szarván keresztül a központi idegrendszerbe juttatva az információt, gyomorégést vált ki, részben egy rövid reflexíven keresztül, a nyelőcső hosszanti rostjainak kontrakciója (SEC: sustained esophageal contraction) miatt vált ki fájdalmat vagy gyomorégést. A fiziológiás savas refluxepizódok, a minuciózus ph-változások, a nem savas (duodenogastricus) refluxepizódok a kemo- vagy mechanoszenzitív nociceptorokon keresztül csak akkor képesek klinikai tüneteket generálni, ha a senzoafferens pályák hiperszenzitívvé válnak. Az oesophagus visceralis hiperszenzitivitás és hyperalgesia mechanizmusa pontosan nem ismert, a legújabb vizsgálatok szerint a szubklinikus gyulladás az idegrostokban fokozza a kapszaicinszenzitív vanilloid (TRPV1) receptorok expresszióját. Diagnózis 3-6. táblázat. NERD-alegységek numerikus megoszlása gyomorégés-jelzôrendszer alapján Patológiás savas NERD-alegység 50% Fiziológiás savas NERD-alegység 17% Nem savas NERD-alegység 33% Patológiás savas Fiziológiás savas reflux Gyengén savas reflux reflux ph-változás, nem savas reflux plusz Volumenreflux hiperszenzitív oesophagus Gázreflux plusz hiperszenzitív oesophagus Martinez SD et al.: Aliment. Pharm. Ther. 2003
16 136 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 137 nometria) a nem savas refluxesemények, a hiperszenzitív oesophagus vagy nyelőcső primer motilitászavarai (diótörő-oesophagus, nem specifikus motilitászavarok, diffúz nyelőcsőspazmus, LES-hypertensio, achalasia) etiopatogenetikai szerepének tisztázására. Terápia Gyomorégés és savas regurgitáció, valamint pozitív PPI diagnosztikus tesztet követően folytatjuk a PPI-adagolást. Amennyiben az iniciális 4 hetes kezelés sikeresnek bizonyult, fenntartó kezelésre térünk át a step-down stratégia elvei szerint: a mindennapi gyakorlatban ez vagy féldózisú PPI tartós adagolását jelenti, vagy akár on demand kezelés is elegendő lehet standard dózisú PPI alkalmi adagolásával. A H2-receptor-antagonisták szerepe a fenntartó kezelésben is háttérbe szorult. A probléma akkor jelentkezik, ha a 4 hetes terápiás PPI-teszt eredménytelen, ekkor további 4 hetes emelt dózisú PPI adásával próbálkozhatunk, amely tisztán savas reflux esetén feltehetően eredményes lesz. Különösen fontos megjegyezni, hogy szintén emelt dózisú PPI adagolásra van szükség magas vagy éjszakai savas reflux, a rövid 1-2 perces savas refluxesemények vagy fiziológiás savas reflux esetén, mivel ezek tünetképző hatásait sokkal nehezebb befolyásolni. Kevert savas és biláris reflux estén a kezelést prokinetikumok (domperidon, metoclopramid), hiperszenzitív nyelőcső esetén fájdalommoduláló, kis dózisú triciklikus antidepresszánsok (TCA) adásával egészíthetjük ki. Az atípusos tünetek (nyelőcsőeredetű mellkasi fájdalom, respiratórikus tünetek stb.) iniciális kezelése szintén dupla dózisú PPI adásából áll, amelyet legalább 3 hónapon át kell folytatnunk. A PPI-kezelést respiratorikus tünetek esetén prokinetikumokkal, nyelőcső eredetű mellkasi fájdalom esetén kisdózisú TCA-val célszerű kiegészíteni. Tüneti remisszió esetén fenntartó kezelés tartós PPI (alap, majd féldózis) plusz prokinetikum vagy TCA kombinált adásával folytatandó. Gyakori relapszusok, a kórképek progressziója esetén, vagy amikor a remisszió csak emelt dózisú PPI adásával biztosítható, reális terápiás alternatíva a laparoszkópos antirefluxműtét. Erozív refluxbetegség (ERD) Izbéki Ferenc Bevezetés Az erozív oesophagitis leggyakrabban refluxbetegség következtében alakul ki, amikor a gyomorból a nyelőcsőbe regurgitáló emésztőnedveket tartalmazó gyomortartalom a nyálkahártyán felmaródásokat okoz. A nyálkahártya-sérülések nyelőcsőtükrözéssel állapíthatók meg, és ezen alapul a refluxbetegség erozív (ERD) és nem erozív (NERD) formáinak az elkülönítése is. Az endoszkópos vizsgálatok alapján derült ki, hogy az ERD és a NERD a refluxbetegség két egymástól elkülönülő megnyilvánulási formája (fenotípusa), és egymásba való átalakulásuk az esetek csak kevesebb, mint 10%-ában fordul elő. Ezért a betegség természetes lefolyása és kezelése során kialakuló recidíva is valószínűleg a korábban észlelt formában fog bekövetkezni. Epidemiológia A refluxbetegség tünetei havonta egyszer a népesség 40%-ában, hetente egyszer mintegy 20%-ában előfordulnak. Nyálkahártya-erózió a típusos tünetekkel jelentkező refluxbetegek kevesebb, mint felében mutatható ki. Az erozív forma idősebb fehér férfiakban és obezitásban gyakoribb. Patogenezis A nyelőcsőbe regurgitáló, emésztőenzimeket, savat és epét tartalmazó gyomorbennék nyálkahártya-károsodást okozó hatása alapvetően három tényezőtől függ: a cardia antireflux-mechanizmusainak hatékonyságától, a behatás időtartamától és a nyálkahártya ellenálló képességétől. A GERD erozív formájának patogenezisében a döntő szerepet a savas refluxepizódok száma, a savas reflux proximalis kiterjedésének mértéke (patológiás savas reflux!), valamint a nyelőcsőben a savclearance károsodása játssza. A reflux megelőzésében fontos a cardia működése, amely gyakran károsodik hiatus hernia, intraabdominális nyomásfokozódás (obesitas), lassú gyomorürülés (pl. cukorbaj) vagy a LES ellazulását okozó táplálkozási és neurohumorális tényezők (nagy mennyiségű étel, szénhidrátok, zsírok, koffein, alkohol) következtében. A cardiadiszfunkció következtében növekszik a nyelőcső-nyálkahártyát érő savhatás időtartama. Refluxbetegségben a fiziológiásan is előforduló, tranziens alsó nyelőcsősphincter-relaxációhoz (TLESR) kapcsolódó savas reflux mértéke is fokozott. A regurgitáló gyomortartalom tovább fejtheti ki nyálkahártyát emésztő hatását akkor is, amikor a nyelőcső perisztaltikus aktivitása (nyelőcsőclearance) károsodott. A nyelőcső-nyálkahártya emésztőhatásokkal szembeni ellenállását számos tényező biztosítja, amelyeket szintén három csoportba sorolhatunk. A preepithelialis védekezést a nyák, a bikarbonát és az ún. nyugodt vízréteg (unstirred water layer), a postepithelialist a vérkeringés és a szöveti sav-bázis egyensúly képezi. A védekezés legjelentősebb komponensei magában a nyálkahártyában vannak, amelyek részben az alkotósejtek közötti kapcsolatokból (tight junctions), intra- és extracellularis pufferekből és az intracellularis ph biztosításáért felelős ioncserélő csatornákból (Na + -H + ; Na + -dependens Cl - ) tevődnek össze. A nyálkahártya-gyulladás során felszabaduló mediátorok (IL-6, IL- 8, PAF, PGE2) tovább károsítják a LES-funkciót és a simaizom kontraktilitását, ezáltal a nyelőcsőclearence-t. Klinikai tünetek és szövődmények Az erozív oesophagitis tünetei megegyeznek a refluxbetegség korábban tárgyalt típusos és atípusos tüneteivel. A nyálkahártya-károsodás pyrosist (gyomorégés, epigastrialis fájdalom), nyelési fájdalmat, nyelőcső eredetű mellkasi fájdalmat okozhat. A nyálkahártya-léziók jelenléte vagy hiánya a tünetek alapján nem mondható meg, az csak endoszkópos vizsgálattal állapítható meg. A dysphagia szövődményt vagy egyéb betegséget jelez. A tünetek másik csoportját az erozív oesophagitis szövődményei (vérzés, nyelőcsőfekély, perforáció, peptikus nyelőcsőszűkület) okozzák. Ritkán, de előfordul, hogy a refluxbetegség első megnyilvánulási formája okkult vagy manifeszt gasztrointesztinális vérzés. A kezeletlen vagy nem megfelelően kezelt erozív oesophagitis következtében vashiányos anaemia is kialakulhat. Az erozív oesophagitis súlyosabb formái nyelőcsőfekély kialakulásához vezethetnek, amelyek mintegy harmada manifeszt vérzést okoz, és 3%-ban perforáció is bekövetkezhet. A kezeletlen erozív oesophagitis az esetek mintegy 10%-ában peptikus nyelőcsőstricturák kialakulásához vezet, amelyek idősebb korban, hiatus hernia és epés reflux esetében gyakoribbak. A PPI-k bevezetése óta azonban ezeket a szövődményeket ritkábban látjuk, a stricturák ballonos tágítását követő recidívák számának csökkenése is a PPI-kezelésnek köszönhető. A peptikus nyelőcsőszűkület vezető tünete a dysphagia, amihez fájdalom, gyakori aspiráció és testsúlycsökkenés társulhat. Kezdetben szilárd ételek fogyasztásakor nehezített a nyelés, időnként elakad a falat, később a folyadéknyelés is nehezítetté válik. Dysphagia esetén a kivizsgálást mindig endoszkópia végzéséval kezdjük. A 2 cm-nél hosszabb, kanyargós vagy megtöretést mutató szűkületek esetén a malignitás tisztázására további vizsgálatok szükségesek (nyelésröntgen, CT). Az erozív oesophatitis szövődményeként kialakuló Barrett-nyelőcső részletes leírásával a fejezet következő része foglalkozik. Diagnózis Endoszkópos vizsgálattal történik a refluxbetegség erozív és nem erozív formáinak elkülönítése, továbbá a nyálkahártya-károsodás kiterjedtségének mértéke alapján a súlyossági fokozatainak megállapítása. A refluxoesophagitis súlyossági fokának megállapítására számos endoszkópos klasszifikációs rendszert fejlesztettek ki, amelyek közül a Savary Miller-féle, a Hetzel Dent-féle és a MUSE (Metaplasia, Ulcer, Stricture, Erosion) voltak a legismertebbek. A különböző klasszifikációrendszerek hiányosságaik, túlzott bonyolultságuk folytán, illetve a napi endoszkópos gyakorlatban nehezen alkalmazható voltuk következtében nem tették lehetővé az adatok öszszehasonlíthatóságát, ezért 1994-ben Los Angelesben a Gasztroenterológiai Világkongresszuson új klasszifikációs rendszert vezettek be, ami azóta általánosan elfogadottá vált a mindennapi klinikai gyakorlatban. A Los Angeles klasszifikáció a mucosal break (nyálkahártya-sérülés) fogalmát vezette be, amely magában foglalja a körülírt, éles szélű hyperaemiás foltokat, eróziókat és fekélyeket egyaránt. Mivel endoszkóppal a nyálkahártya-sérülés mélysége egyértelműen nem állapítható meg, ezért az erózió és az ulcus között nem tesz különbséget. Nem tér ki továbbá olyan, gyakran szubjektív jellegű minorjelenségek értékelésére sem, mint az erythema, az ödéma vagy a nyálkahártya sérülékenysége. Ez utóbbi eltéréseket a NERD részjelenségének tekinti. A nyálkahártya-sérülések először mindig a redők lumenbe domborodó felszínén (a redők tetején) alakulnak ki, endoszkóppal kevés levegőbefújásnál észlelhetők legpontosabban. A Los Angeles klasszifikáció a nyálkahártya-sérüléseket 4 súlyossági fokozatba (A-D) sorolja (3-1 ábra). Az A-fokozatba azok a nyálkahártya-sérülések tartoznak, amelyek 5 mm-nél kisebbek, és a nyálkahártyaredők tetején helyezkednek el. A B-fokozatban a nyálkahártya-sérülések közül legalább egy hosszabb, mint 5 mm, de a redők közé nem terjednek be. A C-fokozatban legalább egy nyálkahártya-sérülés beterjed a redők közötti területre is, de nem körkörös, és a nyálkahártya-felület kevesebb mint 75%-át érinti. A D-fokozatban az összefolyó nyálkahártya-defektusok a nyálkahártya felületének több mint 75%-ára kiterjednek. 3-1 ábra. A GERD Los Angeles klasszifikációja
17 138 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 139 A korábbi beosztásokkal ellentétben a Los Angeles klasszifikációban nem szerepelnek a refluxoesophagitis szövődményei sem. Így a strictura vagy a Barrett-nyelőcső leírására az endoszkópos szakvéleményben külön ki kell térni. Az endoszkópos differenciáldiagnosztika fontos szempontja, hogy eróziókkal járó nyálkahártya-károsodás a nyelőcsőben bekövetkezhet gyógyszerek, kémiai behatások által okozott sérülés és fertőzések következtében is. Az eróziók elhelyezkedése utalhat a kiváltó okra is. Refluxbetegségre a cardia magasságában megjelenő, illetve az attól proximális irányba fokozatosan enyhülő erozív elváltozások jellemzőek. A gyógyszer okozta, kontakt eróziók vagy fekélyek leggyakrabban a fiziológiás vagy a szerzett szűkületek magasságában, illetve a nyelőcső úgynevezett átmeneti zónájában (a simaizommal és harántcsíkolt izommal borított területek közti határ) fordulnak elő. A fertőzéses oesophagitisekre általában diffúz erozív elváltozások jellemzők, a gyulladásos bélbetegség (Crohn-betegség) nyelőcső-manifesztációja esetén pedig típusos esetben aftózus fekélyek láthatók. A nyelőcsőfekélyek makroszkópos képe alapján mindezen információk ellenére sok esetben nem zárható ki biztonsággal malignus alapbetegség jelenléte, így a léziók szövettani vizsgálata szükséges, adott esetben immunohisztokémiai vizsgálatokkal is kiegészítve. Az erozív oesophagitisben manometriával a betegek felében kimutatható perisztaltikus diszfunkció és alacsony LES-nyomás. Hasonló módon, a 24 órás ph-metria az erozív oesophagitises betegek háromnegyedében kóros értékeket (patológiás savas reflux) mutat, és jellemzőek az éjszakai elhúzódó refluxepizódok. Az eróziók kialakulásában a duodenogastrooesophagealis refluxnak is fontos szerepe lehet, mivel a betegek jelentős részében epés reflux is kimutatható. Terápia A terápia egyrészt magának az erozív oesophagitisnek, másrészt a szövődményeinek kezelésére, illetve megelőzésére irányul. A kezelés célja a beteg tüneteinek a megszüntetése. Erre gyógyszeres, endoszkópos és sebészi megoldások állnak rendelkezésre. Az életmód-változtatás, a testsúlycsökkentés és a diéta fontos kiegészítő szerepet játszik a refluxbetegség kezelésében. Az erozív oesophagitis gyógyszeres kezelésének leghatékonyabb módszere a PPI-k alkalmazása. PPI-kezeléssel az ERD tünetei általában rövidebb idő alatt szüntethetők meg, mint a NERD tünetei. Az endoszkópos képtől (Los Angeles stádiumok) függően a kezelést alap vagy emelt dózisú PPI-vel indítjuk, és 8-12 hétig folytatjuk (H 2 -receptor-blokkolókat ma már az erozív esophagitis kezelésére nem alkalmazunk). PPI-kezelésre a betegek napok alatt tünetmentessé válnak, az eróziók a betegek több mint 80%-ában 2 hónap alatt meggyógyulnak. Panaszmentesség esetén térünk rá a fenntartó kezelésre a stepdown stratégia elvei szerint, mivel fenntartó kezelés nélkül a betegek 80%-ában az erozív oesophagitis egy éven belül recidivál. A fenntartó gyógyszeradagot úgy állítjuk be, hogy a beteg tünetmentes maradjon, és az életminősége stabilizálódjon. Erozív oesophagitis esetén tehát tartós gyógyszeres kezelés szükséges. A gyakorlatban ez azt jelenti, hogy a súlyosabb LA-C/D oesophagitisek esetében általában tartósan szükséges alap vagy emelt dózisú PPI adása, míg az enyhébb formákban elegendő lehet a feles dózisú vagy ritkán az on demand PPI fenntartó kezelés. ERD esetén a beteg számára alternatív kezelési lehetőséget az antirefluxműtét jelent. A laparoszkópos fundoplicatio hatékony terápiás lehetőség a visszatérő makacs refluxbetegség esetén, különösen fiatalabb betegek számára, vagy ha rekeszsérv áll a hátérben. Az ERD szövődményeit illetően az erozív oesophagitis ritkán okoz masszív vérzést; ez endoszkópos kezelést általában nem igényel, a gyógyszeres kezelés elegendő. A peptikus nyelőcsőszűkület tágítására alapvetően a ballonos és a mechanikus (bouginage) módszerek állnak rendelkezésre. Mivel a peptikus nyelőcsőszűkületek általában rövidek, a két technika közötti választás elsősorban az endoszkópos laboratórium lehetőségétől és az endoszkópos gyakorlatától függ. A beavatkozáshoz, különösen a bonyolultabb szűkületek esetén, röntgenellenőrzésre szükség lehet. A tágító eszközt többnyire vezetődrót segítségével juttatjuk a szűkületbe. A kisebb tágítóballonokat az endoszkóp munkacsatornáján keresztül vezetjük be. A tágítást a szűkület átmérőjének megfelelő fokozatú tágítóeszközzel kezdjük, és a cél az, hogy a lumen legalább 2 mm-rel növekedjék, de egy ülésben háromnál több, egymást követő fokozatú tágítóeszköz nem használható (hármas szabály). A tágítás célja a szilárdétel-dysphagia megszüntetése, ami általában 12 mm-es szabad lumen esetében érhető el, de ez egyénenként változó lehet. Lehetőség szerint mm szabad lumen eléréséig folytassuk a tágítást. A beavatkozás szövődményeként kisebb vérzés jelentkezhet. Perforáció 0,2-0,4%-ban fordulhat elő. Mellkasi fájdalom és bacteriaemia is előfordulhat, ez utóbbi miatt a fokozott kockázatnak kitett betegekben megfelelő antibiotikummal endocarditis profilaxis szükséges. A beavatkozást követően a beteg tartós, emelt dózisú PPI-kezelést kapjon, ami csökkenti a recidíva előfordulását. A betegek mintegy 30-40%-ában a szűkület okozta panaszok még így is egy éven belül visszatérnek. Ez esetben a tágítás ismételt elvégzése javasolt. A makacs, tágítással nem uralható esetekben nyelőcsőstentek átmeneti alkalmazása jelenthet megoldást. Sebészi megoldásra ritkán, többnyire a bonyolult, többszörös szűkülettel járó esetekben kerül sor. Barrett-oesophagus (BE) Rosztóczy András Bevezetés A Barrett-nyelőcső alatt a gastrooesophagealis refluxbetegség speciális alcsoportját értjük, amelyre jellemző, hogy az oesophagogastricus junkció felett normál esetben jelen levő többrétegű, el nem szarusodó laphám helyét rövidebb-hosszabb szakaszon specializált intesztinális hengerhám-metaplasia foglalja el. A kórforma klinikai jelentőségét az adja, hogy az utóbbi két évtizedben a nyugati fejlett országokban gyorsan növekvő incidenciát mutató nyelőcső-adenocarcinoma precancerosus elváltozását jelenti. A kórkép definíciója Norman Barrett által történt első leírása (1950) óta többször változott. Az eredeti megfogalmazás szerint Barrett-nyelőcső alatt az oesophagogastricus junkció fölé legalább 3 cm hosszan terjedő columnaris metaplasiát értették (columnar lined esophagus, CLE) függetlenül az elváltozás szövettani típusától ben az amerikai gasztroenterológiai társaság (AGA) javaslatára módosították a megfogalmazást, úgy hogy az oesophagogastricus junkció felett elhelyezkedő, bármilyen kiterjedésű specializált intesztinális metaplasia Barrett-nyelőcsőnek értékelendő. Ennek kapcsán megkülönböztettek rövid (< 3 cm) és hosszú ( 3 cm) szegmenst érintő Barrett-metaplasiákat. A GERD jelenleg érvényes Montreáli definíciója (2006) elhagyja a Barrett-nyelőcső kritériumrendszeréből a specializált intesztinális metaplasia jelenlétének szükségességét, és bevezeti az endoszkóposan feltételezett oesophagealis metaplasia fogalmát (ESEM: endoscopically suspected esophageal metaplasia). A Barrett-metaplasia jelenléte csak biopszia és a szövettani vizsgálat alapján mondható ki! Az új klaszszifikációs rendszernek a létjogosultságát az adja, hogy a distalis nyelőcsőben megjelenő hengerhám-metaplasiák különösen a rövid szegmenst érintőek nagyfokú szövettani változatosságot mutatnak, és nem pontosan ismert, hogy az egyes formák milyen sajátosságokkal rendelkeznek (3-14. ábra). Epidemiológia, természetes lefolyás, etiológia A Barrett-metaplasia előfordulási gyakorisága körülbelül 1%-os a teljes lakosság körében. Míg a jelenleg rendelkezésre álló európai populációvizsgálatok (Olaszország, Svédország) ennél kissé magasabb (1,3-1,6%-os), addig az Egyesült Államokban a Mayo Klinika patológiai adatai ennek megfelelő (1%-os), Ázsiában (Dél-Korea) pedig valamelyest alacsonyabb (0,8%) prevalenciát tapasztaltak. Figyelembe véve a GERD átlagosan 20%-os gyakoriságát, ez azt jelenti, hogy a refluxbetegek 5%-ában kell számolni jelenlétével. Életkori megoszlását tekintve a betegek többsége az éves korosztályból kerül ki, incidenciája az életkorral növekszik. Jelentős a férfinem dominanciája, átlagosan 2-3:1, és a súlyosabb szövettani formákban kifejezettebb. Etnikai megoszlását tekintve az USA-ban leggyakoribb a fehérek között, míg a legritkább az afro-amerikaiak körében. A kórkép természetes lefolyását tekintve a folyamat lassú progressziót mutat, 0,5-0,6%-os (1/200 betegév) gyakorisággal alakul ki adenocarcinoma. A metaplasia-dysplasia-carcinoma folyamat előrehaladtával azonban egyre nő a carcinoma kialakulási valószínűsége. A dysplasia súlyosságát illetően a ben publikált bécsi klasszifikáció (Vienna classification) stádiumbeosztása az általánosan elfogadott. Ez megkülönböztet dysplasiamentes, dysplasiára nézve nem definitív és dysplasiás állapotot. Ez utóbbit pedig két súlyossági osztályba enyhe, illetve súlyos dysplasia sorolja. Súlyos dysplasia esetén az invazív carcinoma kialakulásának aránya 1 év alatt elérheti az 50%-ot. Súlyos dysplasia miatt végzett nyelőcső-reszekátumok feldolgozása bizonyította sok esetben a korai carcinoma párhuzamos, metakron jelenlétét. A nyelőcsőben előforduló metaplasiák többségét, különösen a rövid (< 3 cm) szakaszra kiterjedőket, jelentős szövettani változatosság jellemzi. Legtöbbször gyomorhám (cardia/fundus típusú mucosa) alkotja a domináns mintázatot, és ebben fordulnak elő fokálisan az egyéb metaplasztikus struktúrák, mint például intestinalis metaplasia, pancreas acinaris és ductalis metaplasia, Schaffer-mirigyek, Paneth-sejtek, ciliált sejtek. A hosszú szegmenst érintő metaplasiák esetében viszont az intestinalis metaplasia a jellemző domináns mintázat, és emellett ritkábban forulnak elő egyéb struktúrák. A Barrett-nyelőcső reverzibilitását illetően eltérőek a vélemények. Bár időről-időre találkozhatunk közlésekkel, amelyek a metaplasztikus hámterület visszahúzódását írják le, a valóságban nem áll rendelkezésre olyan adat, amely hosszú szegmens Barrett-nyelőcső ablációs terápia nélküli restitúcióját bizonyítaná. A remissziót illetően további kérdés az intesztinális metaplasia és a ábra. Barrett-metaplasiatípusok
18 140 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 141 A Barrett-nyelőcső kezelése többszintű. A terápia alapja, a gastrooesophagealis refluxbetegség kezelése, amely ez esetben mindig tartós emelt dózisú PPI-terápiát vagy antirefluxműtét végzését jelenti. A terápia második szintje a dysplasia progressziójának megakadályozása, illetve a malignus transzformáció kialakulásának megelőzése. Ennek elérésére a tápcsatorna egyéb területein sikerrel alkalmazott COX-2-gátlók és az acetil-szalicilsav kemoprofilaktikus hatása Barrett-nyelőcsőben ma még nem kellően bizonyított. Bár több retrospektív analízis támogatja a hipotézis helyességét, de a nagy esetszámú, randomizált, placebokontrollált vizsgálatok (pl. AspECT) eredményei még nem állnak rendelkezésre. Mivel jelenleg nem áll rendysplasiás eltérések visszafejlődése, illetve eltűnése. Noha a különböző refluxgátló terápiák (emelt dózisú PPI, antirefluxműtét) esetében egyaránt állnak rendelkezésre ezt támogató adatok, azonban ezekben nincs szó arról, hogy fokális vagy metaplasiás terület egészét érintő, generalizált jelenség volt-e az, aminek regresszióját igazolták. A kórforma etiológiáját illetően nem különbözik a refluxbetegség egyéb formáitól. Kiemelendő azonban a gasztrointesztinális karcinogenezis szempontjából fontos rizikótényezők, úgymint a dohányzás, az obesitas, illetve a gyümölcsökben és rostokban szegény étrend szerepe. Ugyanakkor az alkohol káros hatására e tekintetben nincs egyértelmű bizonyíték. A progresszivitást mutató esetekben a fehér férfiak dominanciája felveti genetikai faktorok szerepét is, amelyet részletesen a patofiziológiai részben tárgyalunk. Patofiziológia A kórforma patofiziológiája tekintetében egyre inkább elfogadott nézet, hogy Barrett-nyelőcső esetén a proximalis tápcsatorna motilitási zavara súlyosabb fokú. A nyelőcsőfunkciós vizsgálatok e kórformában bizonyították a legsúlyosabb mértékű savas és biliaris reflux jelenlétét. Az alsó nyelőcsősphincter zárófunkciójának károsodása, illetve a nyelőcsőtest motilitási zavara is kifejezettebb, és gyakrabban fordul elő e betegekben hiatus hernia és erozív oesophagitis is. Az a korábbi feltételezés azonban, amely szerint a Barrett-metaplasia a súlyosabb, erozív nyelőcsőgyulladások oki következménye, azaz, hogy e két kórforma a GERD spektrumának egymást követő lépése, mára megdőlt. Ennek bizonyítéka, hogy jelentős azon Barrett-nyelőcsöves betegek aránya, akiknek nincs az anamnézisében erozív nyelőcsőgyulladás. Részben ennek kapcsán, részben az epidemiológiai vizsgálatok által mutatott szembetűnő etnikai és nemi különbségek, valamint az iker- és családvizsgálatok eredményei alapján valószínű a genetikai prediszpozíció szerepe is. Az intestinalis metaplasia kialakulásának folyamatát ma inkább a nyelőcső adaptív védekezési mechanizmusának gondolják. Ennek során az irritatív tényezőknek (sósav, pepszin, epesavak, pancreas enzimek) jobban ellenálló hámszerkezet váltja fel a nyelőcső többrétegű laphámborítását. Ezt az elméletet több tényező is támogatja. Egyrészt a metaplasztikus hám típusos esetben az irritációnak leginkább kitett területen, a redőéleken alakul ki először, másfelől az intestinalis metaplasia jelentős anion (bikarbonát) szekréciós kapacitással bír, ami legalább ötszöresen meghaladja a laphámét. Emellett az intestinalis metaplasia által termelt viszkózus mucin is segíti a hám védelmét. Vizsgálatok igazolták, hogy a mucintermelés károsodása fokozza a malignus progreszszió kialakulásának rizikóját. Szintén a védelmet segítik a specializált intestinalis metaplasia sejtjei között megtalálható claudin-18 pozitív tight junctionok, amelyek jobban ellenállnak a gyomorsav károsító hatásának. Végül, de nem utolsósorban bizonyított több olyan gén fokozott expressziója, amely a hámrestitúcióban játszik szerepet. A rizikófaktorok (GER, dohányzás, obesitas) által a nyelőcsőben kiváltott elváltozás jelenléte után a karcinogenezis következő fontos mozzanata a krónikus gyulladás fennállása. Ebben a proinflammatorikus citokinek (IL-6, TNFα) és gyulladásos mediátorok (pl. COX-2) mellett adipokinek (leptin, adiponectin) proliferációt serkentő hatása is szerepet játszik. A meginduló sejtproliferáció eredménye lesz azután a sejtek genomikai változása szintén egy többlépcsős, biomarkerekkel nyomonkövethető folyamat, ami végül elvezet az invazív carcinoma kialakulásához. Klinikai tünetek A Barrett-nyelőcső tünettanát a refluxbetegségre jellemző (oesophagealis és extraoesophagealis) tünetek alkotják. Specifikus tünete nincs, így felismerése csak endoszkópos vizsgálattal lehetséges. A tünettannal kapcsolatosan több publikáció is kiemeli a kórforma tünetszegénységét. Van olyan vizsgálat, amelyben közel 50%-os volt azon betegek aránya, akik nem rendelkeztek típusos refluxos tünetekkel (néma GERD). Diagnózis A diagnózishoz az endoszkópos vizsgálattal vett minta szövettani értékelése szükséges. A kórismézés szempontjából alapvető fontosságú, hogy az endoszkópos megfelelően azonosítani tudja a gyomor és a nyelőcső közti határt (az oesophagogastricus junkciót), hiszen az ettől proximalisan elhelyezkedő, hengerhámmal borított terület a Barrett-metaplasia. Definíció szerint az oesophagogastricus junkciót a gyomorredők proximális csúcsa, illetve a nyelőcső palisad vénáinak distalis vége jelzi. A metaplasztikus hámterület kiterjedését a 2004-ben bevezetett Prága C&M kritériumrendszer szerint ítéljük meg (3-15. ábra). Ez a metaplasia körkörös (C) és maximális (M) kiterjedését adja meg centiméterben. Ennek megfelelően a 2 cm körkörös kiterjedésű, maximálisan 5 centiméterre felterjedő metaplasiás területet C2M5-nek jelöljük. A klasszifikációs módszer nagy előnye, hogy egyszerű, kvantifikált, és ennél fogva megkönnyíti a betegek utánkövetését. Hátránya, hogy sem az izolált metaplasztikus hámszigeteket, sem pedig a metaplasiás területben megjelenő izolált laphámszigeteket nem értékeli. Az endoszkópos vizsgálat egyik buktatója a hiatus hernia téves értékelése, ezért a vizsgálat során mind előre tekintve a ábra. A Barrett-metaplasia endoszkópos lokalizációja a Prága C & M kritériumrendszer alapján nyelőcső felől, mind inverzióban nézve a gyomor felől, lényeges a régió alapos vizsgálata. A Barrett-nyelőcső kórélettani jellegzetességei között már említettük, hogy az intestinalis metaplasia az esetek nagyobb részében fokálisan jelenik meg, és igaz ez a dysplasiás jelenségekre is. A hagyományos, fehér fényű endoszkópia segítségével azonban csak a metaplasia ténye állapítható meg, annak szövettani szerkezete nem. Még jelentősebb probléma, hogy a dysplasia jelenléte sem ismerhető fel, és a korai malignus elváltozásokat csak akkor látjuk, ha a felszíni hám egyenetlensége vagy az érstruktúra szabálytalansága már szabad szemmel észrevehető. Emiatt alkalmazzák azt a szövettani mintavételi szabályt, hogy a metaplasztikus hám minden 2 cm-es szakaszának 4 kvadránsából kell venni randombiopsziákat. Szükséges ezen kívül minden metaplasztikus nyúlvány és szigetszerű hámterület vizsgálata is. Amennyiben malignitásra van gyanú (pl. hámegyenetlenség, színbeli eltérés), akkor az adott területből célzott mintavétel is szükséges. Ha végiggondoljuk, hogy mit jelent ez egy hosszú (C10M13) metaplasiás terület esetén, akkor könnyen érthető, hogy miért jelennek meg újabb és újabb technikák, amelyek célja a pontosabb, célzott mintavétel megvalósítása. Időrendben először a kromoendoszkópiás vizsgálatok vagy másnéven vitális festési eljárások jelentek meg. Megkülönböztettünk ezek között abszorptív (a festék kémiai kötéssel kötődik a hámhoz) és kontrasztfokozó (a festék csak kiemeli a hámrajzolatot) eljárásokat. Előbbire példa a lugol (a laphámot festi) és a metilénkék (az intestinális metaplasia hengerhámsejtjeihez kötődik), utóbbira pedig az indigókármin, a kristályibolya, illetve az ecetsavas kontrasztfokozás módszere. A gyakorlatban azonban e módszereknek számos hátránya mutatkozott, mint például az egyenetlen festődés, a nem megfelelő nyákoldás kapcsán kialakuló buborékképződés, illetve, hogy a mélyben levő elváltozások nem váltak láthatóvá. A fejlődés további állomásai a nagyfelbontású és a nagyító (zoom) endoszkópia voltak. Az utóbbi tette lehetővé a metaplasztikus hám rajzolatának vizsgálatát, majd megjelentek a különböző optikai festési eljárások, mint a Narrow Band Imaging (NBI, Olympus), az intelligens kromoendoszkópia (FICE, Fujinon) és az I-Scan (Pentax)), amelyek a megvilágítás módjának megváltoztatásával értek el kontrasztosabb képet és tették lehetővé a felszíni struktúrák részletesebb vizsgálatát. Összeségében azonban e módszerek egyelőre nem haladják meg a nagy felbontású (nem nagyító!), fehér fényű endoszkópia találati arányát a malignus struktúrák felismerésében Barrett-nyelőcső esetén. E tekintetben előrelépést jelent az autofluoreszcencia endoszkópia, amely jó negatív prediktív értékével csökkenteni tudja a vizsgálatkor vett biopsziák számát. A mélyben levő dysplasiás mirigystruktúrák felismerését szolgálja a konfokális lézer-endomikroszkópia megjelenése, amely gyakorlatilag in vivo szövettani vizsgálatot tesz lehetővé. E módszer nagy hátránya, hogy nagy nagyítása miatt nem lehetséges vele nagyobb egybefüggő hámterület átvizsgálása, azaz valahogyan előbb ki kell választani a részletesen vizsgálandó területet a metaplasiás nyelőcsőben. További hátránya, hogy a nyelőcső szívtől, aortától átvett mozgása jelentősen nehezíti a képalkotást. A szövettani vizsgálat elsődleges célja a metaplasia típusának azonosítása mellett a dysplasia jelenlétének és súlyosságának a megítélése. Erre a célra a hagyományos hematoxilin-, eozinfestés mellett kehelysejteket azonosító festési eljárásokat (PAS-alciánkék, Gömöri aldehid-fukszin) alkalmaznak. Dysplasia gyanúja esetén a proliferatív aktivitás megítélésére immunohisztokémiai vizsgálatok (pl. Ki67, p53) végzése szükséges. A diagnózis speciális kérdésköre a szövettanilag azonosított súlyos dysplasia, illetve korai carcinoma további vizsgálata. A lokális invázió kiterjedésének és a nyirokcsomó-metasztázisok jelenlétének megítélésére szolgáló képalkotó módszerek értékelése (endoszonográfia, CT, MRI) részletesen A nyelőcső daganatai című fejezetben olvasható. Terápia, endoszkópos követés
19 142 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 143 direkt központi idegrendszeri szabályozás alatt állnak. Cricopharyngealis diszfunkcióban a nyelőcső felső záróizmának relaxációs zavara egyrészt nehezíti, vagy súlyosabb esetben teljesen meg is akadályozza a falat továbbhaladását a nyelőcsőbe, másrészt következményesen elősegíti annak a tracheába vagy a nasopharynxba való jutását, ami alsó és felső légúti tüneteket, illetve szövődményeket okoz. A betegség congenitalis formája többnyire már néhány hónapos korban manifesztálódik, és az oropharyngealis régió fejlődési rendellenességeivel (nyúlajak, farkastorok stb.) társulhat. A felnőtt korban jelentkező motilitási zavar kórélettani háttere nem teljesen tisztázott. Ritka, de bizonyított kóroki tényező a cricopharyngealis izom izolált miogén dystrophiája. Felvetik emellett a magasra is terjedő gastrooesophagealis reflux szerepét, amely fokozza a záróizom spazmuskészségét. Ennek indirekt bizonyítéka a pharyngooesophagealis diverticulumok magasabb előfordulási aránya ebben a betegcsoportban. A cricopharyngealis működészavar jellegzetes felnőttkori szövődményeként tartják számon a pharyngooesophagealis diverticulumok (Zenker, Killian Jamieson, pharyngeal pouch) kialakuládelkezésünkre olyan gyógyszeres kezelési eljárás, amely biztonsággal megállítja a Barrett-hámban a metaplasia-dysplasia-carcinoma szekvencia progresszióját, ezért a carcinoma kialakulására nézve magas rizikót jelentő, súlyosan dysplasiás hámterületek eltávolítása az egyetlen megoldás. Ennek módszerei ma az endoszkópos mucosectomia és a radiofrekvenciás ablatio. Kisebb, izolált léziók eltávolíthatók ezeken kívül argonplazma-koaguláció (APC) segítségével is. A különböző ablatiós technikák közül ma a leghatékonyabbnak a radiofrekvenciás technikát tartjuk. Ez esetében a legkisebb a szövődmények (vérzés, strictura) aránya, és gyakorlatilag nem maradnak vissza reziduális, metaplasztikus mirigyek, amelyek később a rájuk növő neosquamosus epithelium miatt láthatatlanok lesznek a nyomonkövetés számára ( buried-gland ). Korai carcinoma esetén alapvető fontosságú a kiterjedés megítélése (staging). A nyirokcsomó-metasztázisok aránya már a legkisebb fokú submucosainvázió (sm1) esetén is meghaladja a 10%-ot. Ez a gyakorlatban azt jelenti, hogy ha a szövettani vizsgálat a submucosa invázióját bizonyítja, akkor sebészi megoldás (distalis nyelőcső-reszekció + nyirokcsomó-abláció) végzése szükséges. Speciális, jelenleg sokat vitatott kérdés az enyhe dysplasiát mutató metaplasztikus hámterületek terápiájának problémaköre. Jelenleg e hámterületek ablációjának hasznossága nem kellően bizonyított, így ma az ilyen betegek endoszkópos követése javasolt. Az endoszkópos ellenőrzés (surveillance) tekintetében a Magyar Gasztroenterológiai Társaság szakmai ajánlása dysplasiamentes esetekben háromévenkénti, enyhe dysplasia esetén évenkénti kontrollt ír elő, a fenti elvek szerinti szövettani mintavétellel. Súlyos dysplasia és korai carcinoma esetén mielőbbi rebiopszia javasolt, majd, amennyiben az eltérés megerősítést nyer, ablatio végzendő. Ezt követően endoszkópos kontroll három hónap múlva szükséges. Ajánlott irodalom Armstrong D, Bennett JR, Blum AL et al.: The endoscopic assessment of esophagitis: a progress report on observer agreement. Gastroenterology, : El Seraq HB: Epidemiology of non-erosive reflux disease. Digestion, : Fass R, Ofmann JJ: Gastroesophageal reflux disease Should we adopt a new conceptual framework? Am J Gastroenterol, : Galmiche JP, Clouse RE, Bálint A et al.: Functional esophageal disorders. Gastroenterology, : Jaspersen D, Kulig M, Labenz J et al.: Prevalence of extraoesophageal manifestations in gastroesophageal reflux disease: an analysis based on the ProGERD study. Aliment Pharmacol Ther, , Labenz J, Jaspersen D, Kulig M et al.: Risk factors for erosive esophagitis: a multivariate analysis based on the ProGERD study initiative. Am J Gastroenterol, : Lonovics J, Simon L, Tulassay Zs, Wittmann T (szerk.): A gastrooesophagealis refluxbetegség (GERD) emésztőszervi és más megjelenési formák. Budapest, 2003, Magyar Gasztroenterológiai Társaság, AstraZeneca. Lonovics J, Simon L, Tulassay Zs, Wittmann T (szerk.): A nem erozív refluxbetegség (NERD). Budapest, 2005, Magyar Gasztroenterológiai Társaság, AstraZeneca. Martinez SD, Malagon IB, Garewal HS et al.: Non-erosive reflux disease (NERD) acid reflux and symptom patterns. Aliment Pharmacol Ther, : Pregun I, Hritz I, Tulassay Z, Herszényi L: Peptic esophageal stricture: medical treatment. Dig Dis, : Reid BJ, Li X, Galipeau PC, Vaughan TL: Barrett s oesophagus and oesophageal adenocarcinoma: time for a new synthesis. Nat Rev Cancer, : Riccardolo FLM, Rado V, Fabbri LM et al.: Bronchoconstriction induced by citric acid inhalation in guinea pigs: role of tachykinins, bradykinin, and nitric oxide. Am J Respir Crit Care Med, : Richter JE: Gastroesophageal reflux disease and its complications. In Feldman M, Friedman LS, Brandt LJ (eds): Sleisenger and Fordtrans s Gastrointestinal and Liver Disease. Philadelphia, 2006, Saunders Elsevier, Sharma P, Dent J, Armstrong D et al.: The development and validation of an endoscopic grading system for Barrett s esophagus: the Prague C & M criteria. Gastroenterology, : Sifrim D, Dupont L, Blondeau K et al.: Weakly acidic reflux in patients with chronic unexplained cough during 24 hour pressure, ph, and impedance monitoring. Gut : Sontag SJ, Sonnenberg A, Schnell TG et al.: The longterm natural history of gastroesophageal reflux disease. J Clin Gastroenterol, : Tack J: Is there a unifying role for visceral hypersensitivity and irritable bowel syndrome in non-erosive reflux disease? Digestion, : Vaezi MF, Richter JE: Role of acid and duodenogastroesophageal reflux in gastroesophageal reflux disease. Gastroenterology, : Vakil N, van Zanten SV, Kahrilas P et al.: Global Consensus Group. The Montreal definition and classification of gastroesophageal reflux disease: a global evidencebased consensus. Am J Gastroenterol, : Wright RA, Miller SA, Corsello BF: Acid-induced esophago-bronchial-cardiac reflexes in humans. Gastroenterology, : 71 7 A nyelôcsô egyéb motilitási zavarai Kulcsfontosságú megállapítások A nyelőcső motilitási zavarainak primer és szekunder formáit különböztetjük meg. A nyelőcső motilitási zavarainak legfontosabb vezető tünetei a nyelészavarok (következményes fogyás) és a mellkasi fájdalom. A differenciáldiagnosztikai szempontból fontos alarm tünetek azonnali szakorvosi kivizsgálást tesznek szükségessé. A primer motilitási zavarok terápiájában a gyógyszeres kezelés, az endoszkópos tágítás vagy a sebészi myotomia jön szóba. A gyógyszeres kezelés (nitrátok, kalciumcsatorna-blokkolók, triciklikus antidepreszszánsok, prokinetikumok) hatásossága kérdéses. Endoszkópos tágítás vagy sebészi myotomiát követően a következményes reflux miatt protonpumpagátlókezelés válhat szükségessé. A szekunder motilitászavarok esetében az alapbetegség kezelése alapvető fontosságú. Bevezetés A nyelőcső motilitási zavarait a 3-7. táblázat foglalja össze. Ezek közé az előző fejezetben tárgyalt gastrooesophagealis reflux-betegségen kívül olyan elsődleges vagy másodlagos kórképek tartoznak, amelyek során a nyelőcső egy vagy több szakaszának a motoros működése károsodik. A nyelőcső motilitási zavarainak osztályozása nem egységes. A mindennapi gyakorlat számára a legegyszerűbb és leghasznosabb felosztási mód az elsődleges és másodlagos formák közti különbségtétel. Az elsődleges motilitási zavarokat ezt követően azok patofiziológiai jellemzői alapján osztályozzuk tovább. Cricopharyngealis diszfunkció A primer cricopharyngealis diszfunkció (régebbi nevén cricopharyngealis achalasia) lényege, hogy nyeléskor a nyelőcső felső záróizmát alkotó m. cricopharyngeus elégtelenül lazul el. Patofiziológia A cricopharyngealis régió izomzatát eltérően a nyelőcső egyéb területeitől harántcsíkolt izmok alkotják, amelyek Rosztóczy András 3-7. táblázat. A nyelôcsô-motilitási zavarok osztályozása Primer motilitási zavarok: 1. Gastrooesophagealis refluxbetegség 2. Elégtelen záróizom-relaxációval járó kórképek: Cricopharyngealis diszfunkció Achalasia cardiae A LES-relaxáció atípusos zavarai Inkoordinált kontrakciók: Diffúz nyelôcsô spazmus 4. Fokozott kontraktilitás: Diótörô (nutcracker) nyelôcsô Izolált LES hypertonia 5. Csökkent kontraktilitás: Ineffektív nyelôcsô-motilitás (nem specifikus nyelôcsômotilitási zavar) Szekunder motilitási zavarok: 1. Diabetes mellitus 2. Autoimmun betegségek (progresszív szisztémás sclerosis, CREST-szindróma, Sjögren-szindróma, polymyositisdermatomyositis, kevert kötôszöveti betegség) Neuromuscularis betegségek (cerebrovaszkuláris, motoneuron és demielinizációs-betegségek, Parkinson-kór, izomdisztrófiák, myasthenia gravis) 4. Chagas-kór (Trypanosoma cruzi) 5. Amyloidosis
20 144 Gaszt ro en te ro ló Gia A nyelôcsô betegségei 145 sát, amiben a motilitási zavar mellett a nyelőcsőfal kötőszöveti gyengeségének is szerepe van. Tünettan, epidemiológia A primer cricopharyngealis diszfunkció ritka betegség. Jellemző tünetei a fokozott nyáladzás, a köhögés, az étel regurgitációja, a fuldoklás, illetve a visszatérő súlyos légúti infekciók (legtöbbször tüdőgyulladás). Diagnózis A cricopharyngealis diszfunkcióra jellemző motilitási zavar manometriával bizonyítható, de csecsemőkorban ennek nehéz kivitelezhetősége miatt szinte kizárólag csak indirekt módon, nyelésvizsgálat alapján állítják fel a diagnózist. Differenciáldiagnosztikai szempontból az egyéb anatómiai rendellenességektől kell elkülöníteni (pl. kongenitális nyelőcső szűkület, tracheooesophagealis fisztula stb.). Terápia A cricophayngealis diszfunkció kezelésének az egyetlen, hosszú távon is sikeres módja a sebészi myotomia végzése. A ballonos vagy bougie-tágítás nem hatékony, a botulinumtoxin injiciálása pedig e kórképben is csak átmeneti eredménnyel jár. Achalasia cardiae A nyelőcső primer motilitási zavarai közül a legismertebb. Lényege a nyelőcső alsó záróizmának és a simaizmot tartalmazó tubuláris szakaszának a működészavara, ábra. A nyelôcsôplexus myentericus stimulátoros (ACh) és inhibitoros (NO/VIP) neuronjainak megoszlása Ábramagyarázat. UES: felsô nyelôcsôsphincter, LES: alsó nyelôcsôsphincter, ACh: acetilkolin, NO: nitrogén-monoxid, VIP: vazoaktív intesztinális peptid. amelyet a záróizomban nyelés után jelentkező inkomplett relaxáció, a nyelőcsőtestben pedig a progresszív perisztaltika hiánya jellemez. A legújabb, nagy felbontású manometriás vizsgálat bevezetésével módosult a kórkép klasszifikációja. A korábbi két alcsoport (klasszikus, vigorózus) helyett három forma (klasszikus, kompressziós és spasztikus) különíthető el. Patofiziológia Az achalasiára jellemző motilitási eltérések patofiziológiai hátterét a nyelőcsőfalban levő myentericus plexus inhibitoros, nitrerg, illetve kisebb részben VIP-erg neuronjainak a pusztulása jelenti. Ezek az idegsejtek felelősek a nyelésre kialakuló primer perisztaltikus hullám relaxációs komponenséért, valamint az alsó nyelőcső-záróizom időbeni koordinált ellazulásáért. Hisztológiai vizsgálatok alapján ismert, hogy e sejtek legnagyobb denzitása normál esetben éppen az alsó záróizomban található, majd a nyelőcsőtestben proximális irányban haladva egyre csökken előfordulásuk (3-16. ábra). E megoszlás ismeretében könnyen érthető a fent leírt motilitási zavar kialakulása. Bár a kórkép etiológiáját tekintve ma éppúgy nincs általánosan elfogadott magyarázat, mint 1674-ben, a Sir Thomas Willis által leírt eset kapcsán, az inhibitoros, dominálóan nitrerg myentericus ganglionsejtek pusztulásának okait illetően az utóbbi években számos fontos adatra derült fény. Szövettani vizsgálatok igazolták a myentericus ganglionok CD3/CD8 pozitív T-limfocitás infiltrációját, az achalasiás betegek szérumából pedig myentericus neuronokkal szemben termelt autoantitesteket izoláltak, és magasabbnak találták e betegek szérum IL-8-szintjét. Nincs egyértelmű bizonyíték azonban az autoimmun ganglionitis kialakulásának kiváltó tényezőjére. Leírták egyes HLA-genotípusok (DQA1*0103 és DQB1*0603) szerepét, és visszatérően felvetik különböző vírusok, mindenekelőtt a HSV-1 patogenetikai szerepét. Bár az anti-hsv-ellenanyag és a HSV-DNS pozitivitás aránya nem tér el szignifikánsan a kontrollokétól, az achalasiás betegek nyelőcsövének myentericus ganglionja mellől izolált citotoxikus T-sejtek több mint háromszor magasabb proliferációs indexet mutattak HSV-1 hatására. Másfelől a rendelkezésre álló adatok azt a nézetet is támogatják, hogy heterogén etiológiájú betegségről van szó, azaz több út is vezethet a myentericus sejtek pusztulásához és a jellegzetes klinikai kép kialakulását jelentő végső állapothoz. Erre utal, hogy az idősebb korcsoportban manifesztálódó achalasiás betegekben a VIP receptor 1 gén polimorfizmusa jelentős eltérést mutat mind a kontrollokhoz, mind a fiatalabb achalasiás betegcsoportokhoz képest. Epidemiológia A betegség ritka, átlagosan ezer lakosra jut egy új eset évente. A férfiakat és a nőket egyformán érinti. Bármely életkorban előfordulhat, de leggyakrabban a harmadik-ötödik életévtizedben jelenik meg. Veleszületett formái igen ritkák, alig 5%-át teszik ki a betegeknek, ilyenkor általában egyéb fejlődési anomáliákkal együtt fordul elő. A legismertebb kórkép az autoszomális receszszív öröklődésű Allgrove-szindróma (másnéven Tripla- A-szindróma), mely achalasia, alacrimia, és ACTH-rezisztencia fennállását jelenti. Emellett leírták előfordulását Alport- és Down-szindrómás betegekben is. A szekunder formák közül ki kell emelni a poszttraumás eseteket, amelyek műtéti trauma (coronaria bypass, fundoplikáció, gyomorszűkítő műtétek), illetve nem műtéti trauma (legtöbbször gépkocsibaleset) következményei. A kórkép időskori manifesztációjakor mindig gondolni kell pseudoachalasia lehetőségére, amikor a kórkép valójában szekunder módon megjelenő paraneopláziás tünet. Legtöbbször gyomor-, cardia-, tüdő- és hasnyálmirigy-carcinomához, illetve lymphomákhoz asszociáltan írták le előfordulását. Az achalasia idiopathiás formájával megegyező motilitási zavar jellemzi a Dél-Amerikában endémiás parazitózist, a Trypanosoma cruzi által okozott Chagas-kórt is. A betegség egyéb jellemzőit, diagnózisát és kezelését a vékony- és vastagbelek motilitási zavarai című fejezetben tárgyaljuk. Tünettan, természetes lefolyás A kórkép korai és vezető tünete a dysphagia (nyelési nehezítettség), amely előbb a szilárd, majd folyékony ételek fogyasztásakor is jelentkezik, végül a betegség végstádiumában, a nyelőcső nagyfokú kitágulása idején, akár el is tűnhet. A korai stádiumban a betegek jellegzetesen hideg folyadékkal juttatják le a gyomrukba a nyelőcsőben megakadt ételt. A falat megakadását mellkasi fájdalom kísérheti, amely a nyelőcső kiürülésével oldódik. A betegség tünettanát tekintve szembetűnő, hogy a vezető tünetek közt több úgynevezett vészjelző (alarm) tünet dysphagia, fogyás, hányás található. Ezek jelentőségét az adja, hogy malignus nyelőcsőbetegséget is jelezhetnek, így előfordulásuk esetén nem halasztható a beteg intézeti kivizsgálása. Az achalasia kórlefolyása során a nyelőcsőben megrekedő szekrétum és étel a nyelőcsőfal folyamatos feszülését eredményezi. Ennek következtében a nyelőcső fokozatosan kitágul, rezervoárrá alakul. A benne felgyülemlett emésztetlen baktériumok, gombák által fermentált étel gyakran regurgitál, és egyrészt kellemetlen szájszagot (foetor ex ore), másrészt súlyos szövődményeket (pl. visszatérő légúti infekciókat) okoz. Nagyobb mennyiségű étel fogyasztásakor nem ritka, hogy a beteg percen belül kihányja az emésztetlen táplálékot. Bár a nyelőcsőben végbemenő fermentáció révén ez lehet enyhén savas karakterű, de fontos elkülöníteni a gastrooesophagealis reflux betegségben előforduló savas regurgitációtól és hányástól. Az achalasiás betegek testsúlyának változása a betegség stádiumától függ. A korai szakaszban általában csökken a testsúly, majd a nyelőcső kitágulásakor létrejöhet egy többé-kevésbé kompenzált állapot, amikor a beteg tartja a súlyát, sőt esetleg gyarapodhat is. A végső stádiumban pedig progresszív súlyvesztés jelentkezik. A kezeletlen achalasiás beteg ennek megfelelően krónikusan alultáplált, aminek szövődményeként polyneuropathia és mentális hanyatlás alakulhat ki. Az achalasia természetes lefolyását a nyelőcső fent bemutatott fokozatos kitágulása jellemzi. Ez hosszú távon extrém fokot akár 8-10 cm-es átmérőt is elérhet, miközben a nyelőcső kanyargós, sigmoid alakot vesz fel. Ez az úgynevezett dolichomegaoesophagus, amely kompressziós tünetet (pl. szív esetében) okozhat. A folyamat során a cardia magasságában szifonszerű tágulat alakulhat ki. Így a gastrooesophagealis junkció elkerül a nyelőcső legalsó pontjáról, ami mechanikailag tovább rontja az egyébként is akadályozott nyelőcsőürülést. A tág nyelőcsőben pangó étel krónikus nyálkahártya-irritációt, diffúz oesophagitist okoz, nem ritkán gombás felülfertőződéssel. Ez az állapot jelentősen, mintegy szorosára növeli meg a nyelőcsőlaphámrák kialakulásának kockázatát a normál populációhoz képest. Azokban az esetekben pedig, ahol a kezelés eredményeként szekunder gastrooesophagealis reflux alakul ki, hosszú távon fokozott a Barrett-metaplasia és az adenocarcinoma rizikója. A betegek követését illetően nemzetközileg elfogadott ajánlások még nem állnak rendelkezésre, de a régóta fennálló, előrehaladott stádiumú esetek gasztroenterológiai (nyelésröntgen, endoszkópia) követése indokoltnak tartható. Diagnózis Noha az achalasia cardiae tünetei könnyen felismerhetőnek tűnnek, a kórismézés mégsem egyszerű, hiszen a tünetek első megjelenésétől kezdve a diagnózis felállításáig nem ritkán 5 évnél is hosszabb idő telik el. A diagnosztikus stratégia elsődleges célja az organikus betegségek (pl. tumor, peptikus strictura, anatómiai rendellenességek) kizárása. Az eszközös diagnosztika első lépése ennél fogva dysphagiás panaszok esetén a nyelőcső endoszkópos vizsgálata, amelyet kiegészít a kontrasztanyag-nyeletéses radiológiai vizsgálat. E vizsgálómódszerek azonban a specifikus diagnózis felállítására kevéssé alkalmasak, hiszen a betegség korai stádiumában a nyelőcsőtest még nem tágult, és ezért a cardia relaxációs zavara sem annyira szembetűnő.
Az emésztôrendszer károsodásai. Lonovics János id. Dubecz Sándor Erdôs László Juhász Ferenc Misz Irén Irisz. 17. fejezet
 Az emésztôrendszer károsodásai Lonovics János id. Dubecz Sándor Erdôs László Juhász Ferenc Misz Irén Irisz 17. fejezet Általános rész A fejezet az emésztôrendszer tartós károsodásainak, a károsodások
Az emésztôrendszer károsodásai Lonovics János id. Dubecz Sándor Erdôs László Juhász Ferenc Misz Irén Irisz 17. fejezet Általános rész A fejezet az emésztôrendszer tartós károsodásainak, a károsodások
Systema digestorium
 Systema digestorium 2 2016 A lágyszájpad izmai A lágyszájpad mozgásainak iránya a felsorolt izmok működése következtében (nyilak). Palatopharyngealis sphincter: a felső garatfűző izom és az aponeurosis
Systema digestorium 2 2016 A lágyszájpad izmai A lágyszájpad mozgásainak iránya a felsorolt izmok működése következtében (nyilak). Palatopharyngealis sphincter: a felső garatfűző izom és az aponeurosis
Nyelőcső manometria, ph-metria, Bilitec- Impedancia vizsgálatok
 Nyelőcső manometria, ph-metria, Bilitec- Impedancia vizsgálatok Dr. Czimmer József, Ph.D. Pécsi Tudományegyetem I. sz. Belgyógyászati Klinika Diagnosztikus módszerek a gasztroenterológia és hepatológiában
Nyelőcső manometria, ph-metria, Bilitec- Impedancia vizsgálatok Dr. Czimmer József, Ph.D. Pécsi Tudományegyetem I. sz. Belgyógyászati Klinika Diagnosztikus módszerek a gasztroenterológia és hepatológiában
GYERMEKGYÓGYÁSZAT Gastrooesophagealis reflux betegség
 Gastrooesophagealis reflux betegség Csecsemõ- és Gyermekgyógyászati Szakmai Kollégium Definíció és patomechanizmus A gastrooesophagealis reflux (GOR) alatt azt az elváltozást értjük, amikor a gyomortartalom
Gastrooesophagealis reflux betegség Csecsemõ- és Gyermekgyógyászati Szakmai Kollégium Definíció és patomechanizmus A gastrooesophagealis reflux (GOR) alatt azt az elváltozást értjük, amikor a gyomortartalom
I, A nyelőcső nyálkahártya sérülés (lézió) és vérbő, gyulladásos elváltozás (erythema) nem összefüggő, csak foltokban látható.
 Fiziológiás Reflux Fiziológiás körülmények között, azaz normál élettani körülmények között a savanyú vagy ritkábban a lúgos gyomornedv tartalom időnként a nyelőcsőbe jut (ezt hívjuk Reflux -nak), és annak
Fiziológiás Reflux Fiziológiás körülmények között, azaz normál élettani körülmények között a savanyú vagy ritkábban a lúgos gyomornedv tartalom időnként a nyelőcsőbe jut (ezt hívjuk Reflux -nak), és annak
A táplálkozás és energiaháztartás neuroendokrin szabályozása 1.
 A táplálkozás és energiaháztartás neuroendokrin szabályozása 1. A mechanikai és kémiai tevékenység koordinációja a GI rendszerben A gatrointestinalis funkciók áttekintése. A mechanikai tevékenység formái
A táplálkozás és energiaháztartás neuroendokrin szabályozása 1. A mechanikai és kémiai tevékenység koordinációja a GI rendszerben A gatrointestinalis funkciók áttekintése. A mechanikai tevékenység formái
KERINGÉS, LÉGZÉS. Fejesné Bakos Mónika egyetemi tanársegéd
 KERINGÉS, LÉGZÉS Fejesné Bakos Mónika egyetemi tanársegéd Az erek általános felépítése Tunica intima: Endothel sejtek rétege, alatta lamina basalis. Subendothel réteg : laza rostos kötőszövet, valamint
KERINGÉS, LÉGZÉS Fejesné Bakos Mónika egyetemi tanársegéd Az erek általános felépítése Tunica intima: Endothel sejtek rétege, alatta lamina basalis. Subendothel réteg : laza rostos kötőszövet, valamint
Emészt rendszer szövettana 2. Dobó Endre
 Emészt rendszer szövettana 2 Dobó Endre Oesophagus > tunica mucosa (nyálkahártya) > tela submucosa / tunica submucosa > tunica muscularis > tunica adventitia > kivéve a pars abdominalis oesophagei-t, mert
Emészt rendszer szövettana 2 Dobó Endre Oesophagus > tunica mucosa (nyálkahártya) > tela submucosa / tunica submucosa > tunica muscularis > tunica adventitia > kivéve a pars abdominalis oesophagei-t, mert
Autonóm idegrendszer
 Autonóm idegrendszer Az emberi idegrendszer működésének alapjai Október 26. 2012 őszi félév Vakli Pál vaklip86@gmail.com Web: http://www.cogsci.bme.hu/oraheti.php Szomatikus és autonóm idegrendszer Szomatikus:
Autonóm idegrendszer Az emberi idegrendszer működésének alapjai Október 26. 2012 őszi félév Vakli Pál vaklip86@gmail.com Web: http://www.cogsci.bme.hu/oraheti.php Szomatikus és autonóm idegrendszer Szomatikus:
Az Egészségügyi Minisztérium szakmai protokollja A gastrooesophagealis reflux betegség diagnózisa, terápiája
 Az Egészségügyi Minisztérium szakmai protokollja A gastrooesophagealis reflux betegség diagnózisa, terápiája Készítette: A Gasztroenterológiai Szakmai Kollégium I. Alapvető megfontolások A gastrooesophagealis
Az Egészségügyi Minisztérium szakmai protokollja A gastrooesophagealis reflux betegség diagnózisa, terápiája Készítette: A Gasztroenterológiai Szakmai Kollégium I. Alapvető megfontolások A gastrooesophagealis
A nyelőcső és a gyomor betegségei Herszényi László Semmelweis Egyetem, Budapest II. sz. Belgyógyászati Klinika
 A nyelőcső és a gyomor betegségei Herszényi László Semmelweis Egyetem, Budapest II. sz. Belgyógyászati Klinika 2012. szeptember 12. Gyomorégés = Reflux Normál Reflux Gyomorsav Nyelőcső reflux betegség
A nyelőcső és a gyomor betegségei Herszényi László Semmelweis Egyetem, Budapest II. sz. Belgyógyászati Klinika 2012. szeptember 12. Gyomorégés = Reflux Normál Reflux Gyomorsav Nyelőcső reflux betegség
Légzés 4. Légzésszabályozás. Jenes Ágnes
 Légzés 4. Légzésszabályozás Jenes Ágnes Spontán légzés: - idegi szabályzás - automatikus (híd, nyúltvelı) - akaratlagos (agykéreg) A légzés leáll, ha a gerincvelıt a n. phrenicus eredése felett átvágjuk.
Légzés 4. Légzésszabályozás Jenes Ágnes Spontán légzés: - idegi szabályzás - automatikus (híd, nyúltvelı) - akaratlagos (agykéreg) A légzés leáll, ha a gerincvelıt a n. phrenicus eredése felett átvágjuk.
Az erek simaizomzatának jellemzői, helyi áramlásszabályozás. Az erek működésének idegi és humorális szabályozása. 2010. november 2.
 Az erek simaizomzatának jellemzői, helyi áramlásszabályozás. Az erek működésének idegi és humorális szabályozása 2010. november 2. Az ér simaizomzatának jellemzői Több egységes simaizom Egy egységes simaizom
Az erek simaizomzatának jellemzői, helyi áramlásszabályozás. Az erek működésének idegi és humorális szabályozása 2010. november 2. Az ér simaizomzatának jellemzői Több egységes simaizom Egy egységes simaizom
FEJEZETCÍM: A nasogastricus diagnosztikus, terápiás és tápláló szonda valamint a Sengstaken-Blakemore szonda behelyezése. A fejezet célja...
 FEJEZETCÍM: A nasogastricus diagnosztikus, terápiás és tápláló szonda valamint a Sengstaken-Blakemore szonda behelyezése A fejezet célja... 2 Alapfogalmak/fogalomtár... 2 A nasogastricus szonda levezetése...
FEJEZETCÍM: A nasogastricus diagnosztikus, terápiás és tápláló szonda valamint a Sengstaken-Blakemore szonda behelyezése A fejezet célja... 2 Alapfogalmak/fogalomtár... 2 A nasogastricus szonda levezetése...
A nyelıcsı motilitási zavarai
 Gasztroenterológia: nyelıcsıbetegsé A nyelıcsı motilitási zavarai Rosztóczy András SZTE I.sz. Belgyógy gyászati Klinika 2008. A nyelıcs csı betegségei gei Organikus betegsé Funkcionális betegsé Egyéb betegsé
Gasztroenterológia: nyelıcsıbetegsé A nyelıcsı motilitási zavarai Rosztóczy András SZTE I.sz. Belgyógy gyászati Klinika 2008. A nyelıcs csı betegségei gei Organikus betegsé Funkcionális betegsé Egyéb betegsé
Az érdeklődés középpontjába éve került Az ismeretek tárháza gyarapodik Kevés hasznosul a napi gyakorlatban Gyakori a fel nem ismert, vagy nem
 Dr. Póka László Az érdeklődés középpontjába 15-20 éve került Az ismeretek tárháza gyarapodik Kevés hasznosul a napi gyakorlatban Gyakori a fel nem ismert, vagy nem megfelelően kezelt eset A friss megbetegedések
Dr. Póka László Az érdeklődés középpontjába 15-20 éve került Az ismeretek tárháza gyarapodik Kevés hasznosul a napi gyakorlatban Gyakori a fel nem ismert, vagy nem megfelelően kezelt eset A friss megbetegedések
Légzőszervi megbetegedések
 Orrmelléküreg-gyulladás (sinusitis) Légzőszervi megbetegedések Az orr melléküregeinek gyulladása, melyet leggyakrabban baktériumok okoznak. Orrnyálkahártya-gyulladás (rhinitis) Különböző típusú gyulladások
Orrmelléküreg-gyulladás (sinusitis) Légzőszervi megbetegedések Az orr melléküregeinek gyulladása, melyet leggyakrabban baktériumok okoznak. Orrnyálkahártya-gyulladás (rhinitis) Különböző típusú gyulladások
Az autonóm idegrendszer
 Az autonóm idegrendszer Enterális idegrendszer Szimpatikus idegrendszer Paraszimpatikus idegrendszer HYPOTHALAMUS AGYTÖRZS agyidegek PERIFÉRIÁS GANGLIONOK EFFEKTOR GERINCVELŐ Gerincvelői idegek PERIFÉRIÁS
Az autonóm idegrendszer Enterális idegrendszer Szimpatikus idegrendszer Paraszimpatikus idegrendszer HYPOTHALAMUS AGYTÖRZS agyidegek PERIFÉRIÁS GANGLIONOK EFFEKTOR GERINCVELŐ Gerincvelői idegek PERIFÉRIÁS
Mi a GERD? - Tények. Motilitási zavarok. GERD - Tünetek. GERD - Leletek. Gastroesophageal Reflux (GER) Tárnok András
 Mi a GERD? Tények Motilitási zavarok Tárnok András Gastroesophageal Reflux (GER) A gyomortartalom a nyelőcsőbe jut Normális, élettani jelenség 02. hó: csecsemők 50%a 36 hó: 25% 1012 hó: 5% A refluxepizódok
Mi a GERD? Tények Motilitási zavarok Tárnok András Gastroesophageal Reflux (GER) A gyomortartalom a nyelőcsőbe jut Normális, élettani jelenség 02. hó: csecsemők 50%a 36 hó: 25% 1012 hó: 5% A refluxepizódok
Semmelweis Egyetem, Általános Orvostudományi Kar, I. sz. Sebészeti Klinika A nyelőcső és rekesz sebészete
 A nyelőcső és rekesz sebészete Dr. Balázs Ákos NYELŐCSŐ ANATOMIÁJA - TOPOGRÁFIA - PHYSIOLÓGIÁS SZŰKÜLETEK - SPHINCTEREK - KONTAKTUSOK - IZOMAPPARÁTUS - ÉRELLÁTÁS (ARTERIÁS, VENÁS) - BEIDEGZÉS - NYIROKRENDSZER
A nyelőcső és rekesz sebészete Dr. Balázs Ákos NYELŐCSŐ ANATOMIÁJA - TOPOGRÁFIA - PHYSIOLÓGIÁS SZŰKÜLETEK - SPHINCTEREK - KONTAKTUSOK - IZOMAPPARÁTUS - ÉRELLÁTÁS (ARTERIÁS, VENÁS) - BEIDEGZÉS - NYIROKRENDSZER
VEGETATIV IDEGRENDSZER AUTONOM IDEGRENDSZER
 VEGETATIV IDEGRENDSZER AUTONOM IDEGRENDSZER A szervezet belső környezetének_ állandóságát (homeostasisát) a belső szervek akaratunktól független egyensúlyát a vegetativ idegrendszer (autonóm idegrendszer)
VEGETATIV IDEGRENDSZER AUTONOM IDEGRENDSZER A szervezet belső környezetének_ állandóságát (homeostasisát) a belső szervek akaratunktól független egyensúlyát a vegetativ idegrendszer (autonóm idegrendszer)
Az anamnézis felvétel sajátosságai tüdıbetegségek esetén
 Az anamnézis felvétel sajátosságai tüdıbetegségek esetén Dr. Szőcs Gabriella, Dr. Szabó Zoltán DE OEC Belgyógyászati Intézet Anamnézis Jelen panaszok Családi anamnézis Elızı betegségek Foglalkozás Szociális
Az anamnézis felvétel sajátosságai tüdıbetegségek esetén Dr. Szőcs Gabriella, Dr. Szabó Zoltán DE OEC Belgyógyászati Intézet Anamnézis Jelen panaszok Családi anamnézis Elızı betegségek Foglalkozás Szociális
Gyógyszerészeti neurobiológia Idegélettan 3. A gerincvelő szerepe az izomműködés szabályozásában
 Gyógyszerészeti neurobiológia Idegélettan 3. A gerincvelő szerepe az izomműködés szabályozásában A szomatomotoros szabályozási központok hierarchiája A hierarchikus jelleg az evolúciós adaptáció következménye
Gyógyszerészeti neurobiológia Idegélettan 3. A gerincvelő szerepe az izomműködés szabályozásában A szomatomotoros szabályozási központok hierarchiája A hierarchikus jelleg az evolúciós adaptáció következménye
az a folyamat, amikor egy élőlény a szerves anyagok átalakításához oxigént vesz fel, illetve az átalakításkor keletkező szén-dioxidot leadja.
 Légzés az a folyamat, amikor egy élőlény a szerves anyagok átalakításához oxigént vesz fel, illetve az átalakításkor keletkező szén-dioxidot leadja. Az életet biztosító, egymással szorosan összefüggő két
Légzés az a folyamat, amikor egy élőlény a szerves anyagok átalakításához oxigént vesz fel, illetve az átalakításkor keletkező szén-dioxidot leadja. Az életet biztosító, egymással szorosan összefüggő két
III./2.2.: Pathologiai jellemzők, etiológia. III./2.2.1.: Anatómiai alapok
 III./2.2.: Pathologiai jellemzők, etiológia Ez az anyagrész az önálló fejfájások pathomechanizmusát foglalja össze. A tüneti fejfájások kóreredetét terjedelmi okokból nem tárgyaljuk. III./2.2.1.: Anatómiai
III./2.2.: Pathologiai jellemzők, etiológia Ez az anyagrész az önálló fejfájások pathomechanizmusát foglalja össze. A tüneti fejfájások kóreredetét terjedelmi okokból nem tárgyaljuk. III./2.2.1.: Anatómiai
Jóga anatómia és élettan
 Jóga anatómia és élettan Fábián Eszter (eszter.fabian@aok.pte.hu) 2017.05.06. orrmelléküregek garat gége légcső Tüdő hörgők hörgőcskék Felső légutak: Orrüreg: Az orrüreget és az egész légzőrendszert csillószőrös
Jóga anatómia és élettan Fábián Eszter (eszter.fabian@aok.pte.hu) 2017.05.06. orrmelléküregek garat gége légcső Tüdő hörgők hörgőcskék Felső légutak: Orrüreg: Az orrüreget és az egész légzőrendszert csillószőrös
A légzőrendszer felépítése, a légzőmozgások
 A légzőrendszer felépítése, a légzőmozgások A légzőrendszer anatómiája felső légutak: orr- és szájüreg, garat - külső orr: csontos és porcos elemek - orrüreg: 2 üreg (orrsövény); orrjáratok és orrmandula
A légzőrendszer felépítése, a légzőmozgások A légzőrendszer anatómiája felső légutak: orr- és szájüreg, garat - külső orr: csontos és porcos elemek - orrüreg: 2 üreg (orrsövény); orrjáratok és orrmandula
A táplálkozás, kiválasztás és a légzés szervrendszerei
 A táplálkozás, kiválasztás és a légzés szervrendszerei Emésztőrendszer felépítése: Nyálkahártya (mucosa): 1 epithelium: hámréteg 2 lamina propria: kötőszöveti réteg: 3 lamina muscularis mucosa: nyálkahártya
A táplálkozás, kiválasztás és a légzés szervrendszerei Emésztőrendszer felépítése: Nyálkahártya (mucosa): 1 epithelium: hámréteg 2 lamina propria: kötőszöveti réteg: 3 lamina muscularis mucosa: nyálkahártya
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Tüdőszűrés CT-vel, ha hatékony szűrővizsgálatot szeretnél! Online bejelentkezés CT vizsgálatra. Kattintson ide!
 Tüdőszűrés CT-vel, ha hatékony szűrővizsgálatot szeretnél! Nap mint nap, emberek millió szenvednek valamilyen tüdőbetegség következtében, ráadásul a halálokok között is vezető szerepet betöltő COPD előfordulása
Tüdőszűrés CT-vel, ha hatékony szűrővizsgálatot szeretnél! Nap mint nap, emberek millió szenvednek valamilyen tüdőbetegség következtében, ráadásul a halálokok között is vezető szerepet betöltő COPD előfordulása
A vizeletürítés zavarai: diagnózis, kezelés, rehabilitáció
 A vizeletürítés zavarai: diagnózis, kezelés, rehabilitáció dr. Péley Iván PTE ÁOK KK Idegsebészeti klinika Súlyos agykárosodottak rehabilitációs osztálya Forrás: az EüM szakmai irányelv neurogén eredetű
A vizeletürítés zavarai: diagnózis, kezelés, rehabilitáció dr. Péley Iván PTE ÁOK KK Idegsebészeti klinika Súlyos agykárosodottak rehabilitációs osztálya Forrás: az EüM szakmai irányelv neurogén eredetű
IZOMSÉRÜLÉS AZ IZOMSÉRÜLÉSEK LEGGYAKORIBB OKA A TÚLTERHELÉS, ILLETVE EBBŐL ADÓDÓAN AZ IZOMLÁZ, IZOMGÖRCS ÉS IZOMKONTRAKTÚRA RÉVÉN KIALAKULÓ IZOMSZAKAD
 A SPORTOLÓK IZOMSÉRÜLÉSÉVEL SZERZETT TAPASZTALATAINK UH VIZSGÁLATTAL DR. KARDOS LÁSZLÓ, DR. BARTEK PÉTER PAMOK GYŐR, RADIOLÓGIA OSZTÁLY MRT XXVIII. KONGRESSZUS BUDAPEST, 2016.06.23-25 IZOMSÉRÜLÉS AZ IZOMSÉRÜLÉSEK
A SPORTOLÓK IZOMSÉRÜLÉSÉVEL SZERZETT TAPASZTALATAINK UH VIZSGÁLATTAL DR. KARDOS LÁSZLÓ, DR. BARTEK PÉTER PAMOK GYŐR, RADIOLÓGIA OSZTÁLY MRT XXVIII. KONGRESSZUS BUDAPEST, 2016.06.23-25 IZOMSÉRÜLÉS AZ IZOMSÉRÜLÉSEK
Gasztrointesztinális fiziológia II.
 Gasztrointesztinális fiziológia II. 62. A felső gasztrointesztinális rendszer funkciói: rágás, nyálelválasztás, nyelés. 63. A gyomor motoros funkciói. Hányás. Prof. Sáry Gyula 1 A GI RENDSZER MOTOROS MŰKÖDÉSEI
Gasztrointesztinális fiziológia II. 62. A felső gasztrointesztinális rendszer funkciói: rágás, nyálelválasztás, nyelés. 63. A gyomor motoros funkciói. Hányás. Prof. Sáry Gyula 1 A GI RENDSZER MOTOROS MŰKÖDÉSEI
A modern radiológiai képalkotó eljárások lehetőségei a gyulladásos bélbetegségek diagnosztikájában
 A modern radiológiai képalkotó eljárások lehetőségei a gyulladásos bélbetegségek diagnosztikájában Dr. Kardos Lilla SZTE ÁOK Radiológiai Klinika, Szeged 1. diapár Bélbetegségek gyanúja esetén a hagyományos
A modern radiológiai képalkotó eljárások lehetőségei a gyulladásos bélbetegségek diagnosztikájában Dr. Kardos Lilla SZTE ÁOK Radiológiai Klinika, Szeged 1. diapár Bélbetegségek gyanúja esetén a hagyományos
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az emésztırendszer betegségeinek legfontosabb tünetei csecsemıés gyermekkorban
 1 Az emésztırendszer betegségeinek legfontosabb tünetei csecsemıés gyermekkorban Dysphagia (nyelészavar) Regurgitáció Reflux Hányás Anorexia Diarrhea Székrekedés Haspuffadás Hasfájás Globus érzés Rumináció
1 Az emésztırendszer betegségeinek legfontosabb tünetei csecsemıés gyermekkorban Dysphagia (nyelészavar) Regurgitáció Reflux Hányás Anorexia Diarrhea Székrekedés Haspuffadás Hasfájás Globus érzés Rumináció
A somatomotoros rendszer
 A somatomotoros rendszer Motoneuron 1 Neuromuscularis junctio (NMJ) Vázizom A somatomotoros rendszer 1 Neurotranszmitter: Acetil-kolin Mire hat: Nikotinos kolinerg-receptor (nachr) Izom altípus A parasympathicus
A somatomotoros rendszer Motoneuron 1 Neuromuscularis junctio (NMJ) Vázizom A somatomotoros rendszer 1 Neurotranszmitter: Acetil-kolin Mire hat: Nikotinos kolinerg-receptor (nachr) Izom altípus A parasympathicus
A szív élettana. Aszív élettana I. A szív pumpafunkciója A szívciklus A szívizom sajátosságai A szív elektrofiziológiája Az EKG
 A szív élettana A szív pumpafunkciója A szívciklus A szívizom sajátosságai A szív elektrofiziológiája Az EKG prof. Sáry Gyula 1 Aszív élettana I. A szívizom sajátosságai A szívciklus A szív mint pumpa
A szív élettana A szív pumpafunkciója A szívciklus A szívizom sajátosságai A szív elektrofiziológiája Az EKG prof. Sáry Gyula 1 Aszív élettana I. A szívizom sajátosságai A szívciklus A szív mint pumpa
5% 30% Az extraesophagealis reflux betegség. Extraoesophagealis Légúti - alsó légúti < Oesophagealis. reflux indukálta. asthma. reflux.
 Gasztroenterológia: nyelıcsıbetegségek Az extraesophagealis reflux betegség Rosztóczy András SZTE I.sz. Belgyógy gyászati Klinika 2008. A GORB szövıdm dményei Oesophagealis Barrett Fekély Strictura Extraoesophagealis
Gasztroenterológia: nyelıcsıbetegségek Az extraesophagealis reflux betegség Rosztóczy András SZTE I.sz. Belgyógy gyászati Klinika 2008. A GORB szövıdm dményei Oesophagealis Barrett Fekély Strictura Extraoesophagealis
Gastrointestinalis betegségek szövettana. Felső GI tractus
 Gastrointestinalis betegségek szövettana Felső GI tractus Barrett oesophagus Reflux oesophagitishez társul, de lehet tünetmentes is Emelkedett rizikó oesophagus adenocarcinomára (különösen dysplásiával
Gastrointestinalis betegségek szövettana Felső GI tractus Barrett oesophagus Reflux oesophagitishez társul, de lehet tünetmentes is Emelkedett rizikó oesophagus adenocarcinomára (különösen dysplásiával
Az akciós potenciál (AP) 2.rész. Szentandrássy Norbert
 Az akciós potenciál (AP) 2.rész Szentandrássy Norbert Ismétlés Az akciós potenciált küszöböt meghaladó nagyságú depolarizáció váltja ki Mert a feszültségvezérelt Na + -csatornákat a depolarizáció aktiválja,
Az akciós potenciál (AP) 2.rész Szentandrássy Norbert Ismétlés Az akciós potenciált küszöböt meghaladó nagyságú depolarizáció váltja ki Mert a feszültségvezérelt Na + -csatornákat a depolarizáció aktiválja,
A légzési gázok szállítása, a légzőrendszer szerveződése, a légzés szabályozása
 A légzési gázok szállítása, a légzőrendszer szerveződése, a légzés szabályozása A levegő összetétele: N 2 78.09% O 2 20.95% CO 2 0.03% argon 0.93% Nyomásviszonyok: tengerszinten 760 Hg mm - O 2 159 Hg
A légzési gázok szállítása, a légzőrendszer szerveződése, a légzés szabályozása A levegő összetétele: N 2 78.09% O 2 20.95% CO 2 0.03% argon 0.93% Nyomásviszonyok: tengerszinten 760 Hg mm - O 2 159 Hg
2354-06 Nőgyógyászati citodiagnosztika követelménymodul szóbeli vizsgafeladatai
 1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
Végtagfájdalom szindrómák
 www.printo.it/pediatric-rheumatology/hu/intro Végtagfájdalom szindrómák Verzió 2016 1. Bevezetés Számos gyermekkori betegség okozhat végtagfájdalmat. A végtagfájdalom szindróma" egy általános kifejezés
www.printo.it/pediatric-rheumatology/hu/intro Végtagfájdalom szindrómák Verzió 2016 1. Bevezetés Számos gyermekkori betegség okozhat végtagfájdalmat. A végtagfájdalom szindróma" egy általános kifejezés
VIRTUALIS COLONOSCOPIA. Dr. Kiss Ildikó 2005.
 VIRTUALIS COLONOSCOPIA Dr. Kiss Ildikó 2005. ANATOMIA I. Colon ascendens Colon transversum Colon descendens Colon sigmoideum Rectum Anus víz és folyadék szabályozás ANATOMIA II. Alakja: tágabb mint a vékonybél,
VIRTUALIS COLONOSCOPIA Dr. Kiss Ildikó 2005. ANATOMIA I. Colon ascendens Colon transversum Colon descendens Colon sigmoideum Rectum Anus víz és folyadék szabályozás ANATOMIA II. Alakja: tágabb mint a vékonybél,
VII./2. Veleszületett fejlődési rendellenességek
 VII./2. Veleszületett fejlődési rendellenességek A térd veleszületett rendellenességei összességében ritka kórképek, előfordulhatnak önálló elváltozásként, de időnként komplex fejlődési rendellenességek
VII./2. Veleszületett fejlődési rendellenességek A térd veleszületett rendellenességei összességében ritka kórképek, előfordulhatnak önálló elváltozásként, de időnként komplex fejlődési rendellenességek
A mellkasi betegségek diagnosztikus lehetőségei. Dr. Miheller Pál Semmelweis Egyetem, II.sz. Belgyógyászati Klinika
 A mellkasi betegségek diagnosztikus lehetőségei Dr. Miheller Pál Semmelweis Egyetem, II.sz. Belgyógyászati Klinika Fizikálsi status inspectio, palpatio, percussio, auscultatio Funkcionális vizsgálatok
A mellkasi betegségek diagnosztikus lehetőségei Dr. Miheller Pál Semmelweis Egyetem, II.sz. Belgyógyászati Klinika Fizikálsi status inspectio, palpatio, percussio, auscultatio Funkcionális vizsgálatok
G-B.J. fiú 4 éves. Védıoltásokat megkapta.
 1 G-B.J. fiú 4 éves Családi anamnézis: anyai nagymama Crohn betegség Geszt. anamnézis: eltérés nélkül Születési anamnézis: kóros eltérés nélkül Fejlıdés: fiziológiás Elızı betegségek: 1 ½ év. Lázgörcs
1 G-B.J. fiú 4 éves Családi anamnézis: anyai nagymama Crohn betegség Geszt. anamnézis: eltérés nélkül Születési anamnézis: kóros eltérés nélkül Fejlıdés: fiziológiás Elızı betegségek: 1 ½ év. Lázgörcs
A harántcsíkolt izom struktúrája általános felépítés
 harántcsíkolt izom struktúrája általános felépítés LC-2 Izom LC1/3 Izom fasciculus LMM S-2 S-1 HMM rod Miozin molekula S-1 LMM HMM S-2 S-1 Izomrost H Band Z Disc csík I csík M Z-Szarkomér-Z Miofibrillum
harántcsíkolt izom struktúrája általános felépítés LC-2 Izom LC1/3 Izom fasciculus LMM S-2 S-1 HMM rod Miozin molekula S-1 LMM HMM S-2 S-1 Izomrost H Band Z Disc csík I csík M Z-Szarkomér-Z Miofibrillum
A DE KK Belgyógyászati Klinika Intenzív Osztályán és Terápiás Aferezis Részlegén évi közel 400 db plazmaferezis kezelést végzünk.
 A DE KK Belgyógyászati Klinika Intenzív Osztályán és Terápiás Aferezis Részlegén évi közel 400 db plazmaferezis kezelést végzünk. Az eseteink túlnyomó részét neuro-, immunológiai eredetű kórképek adják.
A DE KK Belgyógyászati Klinika Intenzív Osztályán és Terápiás Aferezis Részlegén évi közel 400 db plazmaferezis kezelést végzünk. Az eseteink túlnyomó részét neuro-, immunológiai eredetű kórképek adják.
Gyógyszerészeti neurobiológia. Idegélettan 4. Spinalis shock. Agytörzs, kisagy, törzsdúcok, agykéreg szerepe a mozgásszabályozásban.
 Gyógyszerészeti neurobiológia. Idegélettan 4. Spinalis shock. Agytörzs, kisagy, törzsdúcok, agykéreg szerepe a mozgásszabályozásban. Gerincvelői shock A gerincvelő teljes harántsérülését követően alakul
Gyógyszerészeti neurobiológia. Idegélettan 4. Spinalis shock. Agytörzs, kisagy, törzsdúcok, agykéreg szerepe a mozgásszabályozásban. Gerincvelői shock A gerincvelő teljes harántsérülését követően alakul
A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat.
 A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat. A rotavírus az egyik leggyakoribb okozója a súlyos hasmenésnek csecsemő és kisdedkorban. Évente világszerte
A rotavírus a gyomor és a belek fertőzését előidéző vírus, amely súlyos gyomor-bélhurutot okozhat. A rotavírus az egyik leggyakoribb okozója a súlyos hasmenésnek csecsemő és kisdedkorban. Évente világszerte
VIII./1. fejezet: A láb fejlődési rendellenességei
 VIII./1. fejezet: A láb fejlődési rendellenességei A fejezetben a lábat alkotó csontok számbeli többletét és hiányát, valamint méretbeli túl-, illetve alulnövekedését részletezzük. Az e fejezetben található
VIII./1. fejezet: A láb fejlődési rendellenességei A fejezetben a lábat alkotó csontok számbeli többletét és hiányát, valamint méretbeli túl-, illetve alulnövekedését részletezzük. Az e fejezetben található
A simaizmok szerkezete
 A simaizmok szerkezete simaizomsejtek: egymagvúak, orsó alakúak többegységes simaizom egyegységes simaizom Ø nincsenek réskapcsolatok (gap junction-ök) minden izomsejt külön működik v nincs akciós potenciál
A simaizmok szerkezete simaizomsejtek: egymagvúak, orsó alakúak többegységes simaizom egyegységes simaizom Ø nincsenek réskapcsolatok (gap junction-ök) minden izomsejt külön működik v nincs akciós potenciál
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
MI ÁLLHAT A FEJFÁJÁS HÁTTERÉBEN? Dr. HégerJúlia, Dr. BeszterczánPéter, Dr. Deák Veronika, Dr. Szörényi Péter, Dr. Tátrai Ottó, Dr.
 MI ÁLLHAT A FEJFÁJÁS HÁTTERÉBEN? Dr. HégerJúlia, Dr. BeszterczánPéter, Dr. Deák Veronika, Dr. Szörényi Péter, Dr. Tátrai Ottó, Dr. Varga Csaba ESET 46 ÉVES FÉRFI Kórelőzmény kezelt hypertonia kivizsgálás
MI ÁLLHAT A FEJFÁJÁS HÁTTERÉBEN? Dr. HégerJúlia, Dr. BeszterczánPéter, Dr. Deák Veronika, Dr. Szörényi Péter, Dr. Tátrai Ottó, Dr. Varga Csaba ESET 46 ÉVES FÉRFI Kórelőzmény kezelt hypertonia kivizsgálás
Áttörésükben visszamaradt bölcsességfogak diagnosztikája. Semmelweis Egyetem, Budapest Szájsebészeti és Fogászati Klinika
 Áttörésükben visszamaradt bölcsességfogak diagnosztikája Semmelweis Egyetem, Budapest Szájsebészeti és Fogászati Klinika Ambulancia műtéti profiljának változása 1999 2004 2008 Műtéti fogeltávolítás 4427
Áttörésükben visszamaradt bölcsességfogak diagnosztikája Semmelweis Egyetem, Budapest Szájsebészeti és Fogászati Klinika Ambulancia műtéti profiljának változása 1999 2004 2008 Műtéti fogeltávolítás 4427
AZ ELŐADÁS CÍME. Stromájer Gábor Pál
 AZ ELŐADÁS CÍME Stromájer Gábor Pál 2 Idegrendszer Az idegrendszer felosztása Anatómiai felosztás Központi idegrendszer: Agyvelő Gerincvelő Környéki idegrendszer: Gerincvelői idegek Agyidegek Perifériás
AZ ELŐADÁS CÍME Stromájer Gábor Pál 2 Idegrendszer Az idegrendszer felosztása Anatómiai felosztás Központi idegrendszer: Agyvelő Gerincvelő Környéki idegrendszer: Gerincvelői idegek Agyidegek Perifériás
Légúti idegentestek. Réti Csaba dr. MRE Bethesda Gyermekkórház Budapest. Kávészünet Siófokon 2012. május 11.
 Légúti idegentestek Réti Csaba dr. MRE Bethesda Gyermekkórház Budapest Kávészünet Siófokon 2012. május 11. Nyelés mechanizmusa Szájpad emelkedése Epiglottis megdőlése Hangrés záródása Nyelőcső primer perisztaltikája
Légúti idegentestek Réti Csaba dr. MRE Bethesda Gyermekkórház Budapest Kávészünet Siófokon 2012. május 11. Nyelés mechanizmusa Szájpad emelkedése Epiglottis megdőlése Hangrés záródása Nyelőcső primer perisztaltikája
MELLKASI ULTRAHANGVIZSGÁLATOK. KIS ÉVA Semmelweis Egyetem ÁOK Budapest I. sz. Gyermekklinika
 MELLKASI ULTRAHANGVIZSGÁLATOK KIS ÉVA Semmelweis Egyetem ÁOK Budapest I. sz. Gyermekklinika MELLKASI ULTRAHANGVIZSGÁLATOK A legtöbb mellkasi kórkép diagnosztizálásához elegendı a röntgenfelvétel Néha az
MELLKASI ULTRAHANGVIZSGÁLATOK KIS ÉVA Semmelweis Egyetem ÁOK Budapest I. sz. Gyermekklinika MELLKASI ULTRAHANGVIZSGÁLATOK A legtöbb mellkasi kórkép diagnosztizálásához elegendı a röntgenfelvétel Néha az
Csigolyatörések konzervativ és műtéti kezelése. Kasó Gábor Pécsi Tudományegyetem, Idegsebészeti Klinika
 Csigolyatörések konzervativ és műtéti kezelése Kasó Gábor Pécsi Tudományegyetem, Idegsebészeti Klinika Csigolyatörések konzervativ és műtéti kezelése traumás poroticus pathologias craniocervicalis, cervicalis,
Csigolyatörések konzervativ és műtéti kezelése Kasó Gábor Pécsi Tudományegyetem, Idegsebészeti Klinika Csigolyatörések konzervativ és műtéti kezelése traumás poroticus pathologias craniocervicalis, cervicalis,
M E G O L D Ó L A P. Emberi Erőforrások Minisztériuma. Korlátozott terjesztésű!
 Emberi Erőforrások Minisztériuma Érvényességi idő: az írásbeli vizsga befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes M E G O L D Ó L A P szakmai írásbeli
Emberi Erőforrások Minisztériuma Érvényességi idő: az írásbeli vizsga befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes M E G O L D Ó L A P szakmai írásbeli
KOLLOKVIUMI TÉTELEK ANATÓMIA, SZÖVET- ÉS FEJLŐDÉSTAN I. ÉVFOLYAM, II. FÉLÉV
 Szegedi Tudományegyetem, Általános Orvostudományi Kar Anatómiai, Szövet- és Fejlődéstani Intézete Igazgató: Dr. Mihály András egyetemi tanár 6724 Szeged, Kossuth L. sgt. 40. Telefon: (62)-545-665 6701
Szegedi Tudományegyetem, Általános Orvostudományi Kar Anatómiai, Szövet- és Fejlődéstani Intézete Igazgató: Dr. Mihály András egyetemi tanár 6724 Szeged, Kossuth L. sgt. 40. Telefon: (62)-545-665 6701
2355-06 Egyéb citológiai vizsgálatok követelménymodul szóbeli vizsgafeladatai
 1. feladat Tájékoztassa a munkahelyére érkező vendégeket a különféle szervekből nyert citológiai anyagok feldolgozásáról, diagnosztikára való előkészítéséről! Tájékoztatója során az alábbi szempontokra
1. feladat Tájékoztassa a munkahelyére érkező vendégeket a különféle szervekből nyert citológiai anyagok feldolgozásáról, diagnosztikára való előkészítéséről! Tájékoztatója során az alábbi szempontokra
Microcytaer anaemiák
 Microcytaer anaemiák Herszényi László MTA doktora Semmelweis Egyetem II. sz. Belgyógyászati Klinika 2015. február 19. I. Fokozott vvt-pusztulás a. Haemolysis II. Csökkent vvt-képzés a. Hgb-szintézis zavara
Microcytaer anaemiák Herszényi László MTA doktora Semmelweis Egyetem II. sz. Belgyógyászati Klinika 2015. február 19. I. Fokozott vvt-pusztulás a. Haemolysis II. Csökkent vvt-képzés a. Hgb-szintézis zavara
Hámszövet, mirigyhám. Dr. Katz Sándor Ph.D.
 Hámszövet, mirigyhám Dr. Katz Sándor Ph.D. HÁMSZÖVET A hámsejtek a bazális membránon helyezkednek el. Oldalai: bazális, laterális és apikális. HÁMSZÖVET Szorosan egymás mellett helyezkednek el és speciális
Hámszövet, mirigyhám Dr. Katz Sándor Ph.D. HÁMSZÖVET A hámsejtek a bazális membránon helyezkednek el. Oldalai: bazális, laterális és apikális. HÁMSZÖVET Szorosan egymás mellett helyezkednek el és speciális
Jegyzőkönyv. dr. Kozsurek Márk. A CART peptid a gerincvelői szintű nociceptív információfeldolgozásban szerepet játszó neuronális hálózatokban
 Jegyzőkönyv dr. Kozsurek Márk A CART peptid a gerincvelői szintű nociceptív információfeldolgozásban szerepet játszó neuronális hálózatokban című doktori értekezésének házi védéséről Jegyzőkönyv dr. Kozsurek
Jegyzőkönyv dr. Kozsurek Márk A CART peptid a gerincvelői szintű nociceptív információfeldolgozásban szerepet játszó neuronális hálózatokban című doktori értekezésének házi védéséről Jegyzőkönyv dr. Kozsurek
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Az anus atresia diagnosztikája, kezelése és gondozása. Dr. Máttyus István SE I. sz. Gyermekklinika
 Az anus atresia diagnosztikája, kezelése és gondozása Dr. Máttyus István SE I. sz. Gyermekklinika Bevezető kérdés-1: melyik szerv rendellenessége nem szokott társulni anus atresiával? A. szív B. vese C.
Az anus atresia diagnosztikája, kezelése és gondozása Dr. Máttyus István SE I. sz. Gyermekklinika Bevezető kérdés-1: melyik szerv rendellenessége nem szokott társulni anus atresiával? A. szív B. vese C.
GERIÁTRIA. Fertőző betegségek SEMSEI IMRE. Debreceni Egyetem Orvos- és Egészségtudományi Centrum Egészségügyi Kar
 GERIÁTRIA Időskori elváltozások, betegségek és kezelésük VI Fertőző betegségek SEMSEI IMRE Debreceni Egyetem Orvos- és Egészségtudományi Centrum Egészségügyi Kar FERTŐZÉSEK IDŐSKORBAN Régen vezető halálok
GERIÁTRIA Időskori elváltozások, betegségek és kezelésük VI Fertőző betegségek SEMSEI IMRE Debreceni Egyetem Orvos- és Egészségtudományi Centrum Egészségügyi Kar FERTŐZÉSEK IDŐSKORBAN Régen vezető halálok
Elakadt falat - akadozó diagnosztika Nyelőcső idegentest gasztroenterológiai vonatkozásai
 Elakadt falat - akadozó diagnosztika Nyelőcső idegentest gasztroenterológiai vonatkozásai Dr. Karoliny Anna, Dr. Gombos Eszter, Dr.Lásztity Natália, Dr.Nagy Anikó, Dr.Lőrincz Margit Heim Pál Gyermekkórház
Elakadt falat - akadozó diagnosztika Nyelőcső idegentest gasztroenterológiai vonatkozásai Dr. Karoliny Anna, Dr. Gombos Eszter, Dr.Lásztity Natália, Dr.Nagy Anikó, Dr.Lőrincz Margit Heim Pál Gyermekkórház
NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú
 NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú meghatározása. (Megj.: a felsorolt esetekben meghatározó
NOAC-kezelés pitvarfibrillációban. Thrombolysis, thrombectomia és kombinációja. Az ischaemiás kórképek szekunder prevenciója. A TIA új, szöveti alapú meghatározása. (Megj.: a felsorolt esetekben meghatározó
Allergia immunológiája 2012.
 Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
Max. inger. Fotopikus ERG. Szkotopikus ERG. Oscillatorikus potenciál Flicker (30Hz) ERG
 ERG, VEP vizsgálatok. Elektrofiziológiai eto oógamódszerek e a látópálya funkcionális állapotának vizsgálatára Janáky Márta Jelentőségük nem invazív módszerek minimális kooperációt igényelnek objektív
ERG, VEP vizsgálatok. Elektrofiziológiai eto oógamódszerek e a látópálya funkcionális állapotának vizsgálatára Janáky Márta Jelentőségük nem invazív módszerek minimális kooperációt igényelnek objektív
Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz
 www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
www.printo.it/pediatric-rheumatology/hu/intro Reumás láz és sztreptokokkusz-fertőzés utáni reaktív artritisz Verzió 2016 1. MI A REUMÁS LÁZ 1.1 Mi ez? A reumás láz nevű betegséget a sztreptokokkusz baktérium
 IRRITÁBILIS BÉL SZINDRÓMA Dr. Vitális Zsuzsa DEOEC II. Belklinika Gasztroenterológia Tanszék A RÓMAI III KLASSZIFIKÁCIÓ A. FUNKCIONÁLIS NYELŐCSŐ RENDELLENESSÉGEK B. FUNKCIONÁLIS GASTRODUODENALIS RENDELLENESSÉGEK
IRRITÁBILIS BÉL SZINDRÓMA Dr. Vitális Zsuzsa DEOEC II. Belklinika Gasztroenterológia Tanszék A RÓMAI III KLASSZIFIKÁCIÓ A. FUNKCIONÁLIS NYELŐCSŐ RENDELLENESSÉGEK B. FUNKCIONÁLIS GASTRODUODENALIS RENDELLENESSÉGEK
GYERMEK-TÜDŐGYÓGYÁSZAT
 GYERMEK-TÜDŐGYÓGYÁSZAT I. 1. Légutak és a tüdő fejlődése 2. Légzőrendszer élettani működése 3. Újszülöttkori légzészavarok 4. Bronchopulmonalis dysplasia 5. A gége veleszületett és szerzett rendellenességei
GYERMEK-TÜDŐGYÓGYÁSZAT I. 1. Légutak és a tüdő fejlődése 2. Légzőrendszer élettani működése 3. Újszülöttkori légzészavarok 4. Bronchopulmonalis dysplasia 5. A gége veleszületett és szerzett rendellenességei
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai
 Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
III./2.3. Vékonybél tumorok
 III./2.3. Vékonybél tumorok Herszényi László A fejezet célja egy esetbemutatáson keresztül a vékonybél tumorok epidemiológiájának, tüneteinek, diagnosztikájának, terápiájának és szűrésének áttekintése.
III./2.3. Vékonybél tumorok Herszényi László A fejezet célja egy esetbemutatáson keresztül a vékonybél tumorok epidemiológiájának, tüneteinek, diagnosztikájának, terápiájának és szűrésének áttekintése.
2423-06 Anatómiai, élettani, metszetanatómiai ismeretek alkalmazása követelménymodul szóbeli vizsgafeladatai
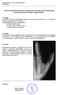 1. feladat Munkahelyi vezetője megbízásából anatómiai kiscsoportos gyakorlatot tart. Az ön feladata az anatómiai bevezető rész ismertetése. Az előadásában térjen ki a következőkre: - az emberi test fő
1. feladat Munkahelyi vezetője megbízásából anatómiai kiscsoportos gyakorlatot tart. Az ön feladata az anatómiai bevezető rész ismertetése. Az előadásában térjen ki a következőkre: - az emberi test fő
Anisocoria. Anisocoria
 Anisocoria Orvosa anisocoriát állapít meg. Ebben az esetben a jobb és a bal szem pupillája nem azonos nagyságú. Kisfokú anisocoria, azaz a pupillák méretének különbözősége, fiziológiás. Előfordul, hogy
Anisocoria Orvosa anisocoriát állapít meg. Ebben az esetben a jobb és a bal szem pupillája nem azonos nagyságú. Kisfokú anisocoria, azaz a pupillák méretének különbözősége, fiziológiás. Előfordul, hogy
Kéz- és lábápoló, műkörömépítő. 31 815 01 0000 00 00 Kéz- és lábápoló, műkörömépítő 2/43
 A /07 (II. 27.) SzMM rendelettel módosított 1/06 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A /07 (II. 27.) SzMM rendelettel módosított 1/06 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
Magyarországon több mint 2 millió hypertoniás él. 2025-re az előrejelzések szerint további 60 százalékkal megnő az érintettek száma.
 Magyarországon több mint 2 millió hypertoniás él. 2025-re az előrejelzések szerint további 60 százalékkal megnő az érintettek száma. A magasvérnyomásos populációban emelkedett vércukor értéket (5,6 mmol/l
Magyarországon több mint 2 millió hypertoniás él. 2025-re az előrejelzések szerint további 60 százalékkal megnő az érintettek száma. A magasvérnyomásos populációban emelkedett vércukor értéket (5,6 mmol/l
Neurobiológia - III. blokk Idegélettan # 12/4. A vázizomműködés gerincvelői kontrollja - II
 Neurobiológia - III. blokk Idegélettan # 12/4 A vázizomműködés gerincvelői kontrollja - II Gamma-rostok aktiválódásának következménye γ aktiválódás hossznövekedés A gamma-aktiválódás következménye ugyanaz,
Neurobiológia - III. blokk Idegélettan # 12/4 A vázizomműködés gerincvelői kontrollja - II Gamma-rostok aktiválódásának következménye γ aktiválódás hossznövekedés A gamma-aktiválódás következménye ugyanaz,
2. ATP (adenozin-trifoszfát): 3. bazális (vagy saját) miogén tónus: 4. biológiai oxidáció: 5. diffúzió: 6. csúszó filamentum modell:
 Pszichológia biológiai alapjai I. írásbeli vizsga (PPKE pszichológia BA); 2017/2018 I. félév 2017. december 24.; A csoport név:... Neptun azonosító:... érdemjegy:... (pontszámok.., max. 120 pont, 60 pont
Pszichológia biológiai alapjai I. írásbeli vizsga (PPKE pszichológia BA); 2017/2018 I. félév 2017. december 24.; A csoport név:... Neptun azonosító:... érdemjegy:... (pontszámok.., max. 120 pont, 60 pont
A NEOADJUVÁNS KEZELÉS SZEREPE A LOKÁLISAN ELŐREHALADOTT STÁDIUMÚ NYELŐCSŐRÁKOK SEBÉSZI KEZELÉSÉBEN
 A NEOADJUVÁNS KEZELÉS SZEREPE A LOKÁLISAN ELŐREHALADOTT STÁDIUMÚ NYELŐCSŐRÁKOK SEBÉSZI KEZELÉSÉBEN PhD értekezés Dr. Papp András PTE KK Sebészeti Klinika Programvezető: Program: Témavezető: Prof. Dr. Horváth
A NEOADJUVÁNS KEZELÉS SZEREPE A LOKÁLISAN ELŐREHALADOTT STÁDIUMÚ NYELŐCSŐRÁKOK SEBÉSZI KEZELÉSÉBEN PhD értekezés Dr. Papp András PTE KK Sebészeti Klinika Programvezető: Program: Témavezető: Prof. Dr. Horváth
Savval kapcsolatos betegségek osztályozása
 Savval kapcsolatos betegségek osztályozása Gastrooesophageális reflux betegség NERD, ERD, Barrett s oesophagus Peptikus fekélyek HP +, HP fekélyek Nem HP Nem NSAID fekélyek Fekély-szerű dyspepsia Peptikus
Savval kapcsolatos betegségek osztályozása Gastrooesophageális reflux betegség NERD, ERD, Barrett s oesophagus Peptikus fekélyek HP +, HP fekélyek Nem HP Nem NSAID fekélyek Fekély-szerű dyspepsia Peptikus
III./2.3.: Klinikai jellegzetességek, tünetek. III./2.3.1.: Migrén
 III./2.3.: Klinikai jellegzetességek, tünetek III./2.3.1.: Migrén Egyes felmérések szerint a migrén az orvosok által leggyakrabban látott neurológiai kórkép. Nagy epidemiológiai vizsgálatok szerint a migrén
III./2.3.: Klinikai jellegzetességek, tünetek III./2.3.1.: Migrén Egyes felmérések szerint a migrén az orvosok által leggyakrabban látott neurológiai kórkép. Nagy epidemiológiai vizsgálatok szerint a migrén
Az ultrahang szerepe az abdominálisretineált here diagnosztikájában
 Az ultrahang szerepe az abdominálisretineált here diagnosztikájában Dr. Polovitzer Mária (1), Dr. Sulya Bálint (2), Dr. Bartók Márta (1), Dr. Morvai Zsuzsanna (1) Heim Pál Gyermekkórház Röntgen/Ultrahang
Az ultrahang szerepe az abdominálisretineált here diagnosztikájában Dr. Polovitzer Mária (1), Dr. Sulya Bálint (2), Dr. Bartók Márta (1), Dr. Morvai Zsuzsanna (1) Heim Pál Gyermekkórház Röntgen/Ultrahang
Élettan írásbeli vizsga (PPKE BTK pszichológia BA); 2014/2015 II. félév
 Élettan írásbeli vizsga (PPKE BTK pszichológia BA); 2014/2015 II. félév 2015. május 35. A csoport név:... Neptun azonosító:... érdemjegy:... (pontszámok.., max. 120 pont, 60 pont alatti érték elégtelen)
Élettan írásbeli vizsga (PPKE BTK pszichológia BA); 2014/2015 II. félév 2015. május 35. A csoport név:... Neptun azonosító:... érdemjegy:... (pontszámok.., max. 120 pont, 60 pont alatti érték elégtelen)
Prenatalis MR vizsgálatok
 Prenatalis MR vizsgálatok Prof. Dr. Lombay Béla Borsod A.Z. Megyei Kórház és s Egyetemi Oktatókórház Miskolci Egyetem, Egészségtudományi gtudományi Kar, Képalkotó Diagnosztikai Tanszék Miskolc Múlt - jelen
Prenatalis MR vizsgálatok Prof. Dr. Lombay Béla Borsod A.Z. Megyei Kórház és s Egyetemi Oktatókórház Miskolci Egyetem, Egészségtudományi gtudományi Kar, Képalkotó Diagnosztikai Tanszék Miskolc Múlt - jelen
Nehéz intubációs helyzetek és megoldások
 Nehéz intubációs helyzetek és megoldások Dr. Tóth Krisztina, Dr Fent Zoltán, Dr. Branovics Judit, Dr. Visnyei Orsolya, Prof. Dr. Gál János SE Aneszteziológiai és Intenzív Terápiás Intézet SE Fül-Orr-Gége,
Nehéz intubációs helyzetek és megoldások Dr. Tóth Krisztina, Dr Fent Zoltán, Dr. Branovics Judit, Dr. Visnyei Orsolya, Prof. Dr. Gál János SE Aneszteziológiai és Intenzív Terápiás Intézet SE Fül-Orr-Gége,
2390-06 Masszázs alapozás követelménymodul szóbeli vizsgafeladatai
 1. feladat Ön azt a feladatot kapta a munkahelyén, hogy készítsen kiselőadást a sejtek működésének anatómiájáról - élettanáról! Előadása legyen szakmailag alátámasztva, de a hallgatók számára érthető!
1. feladat Ön azt a feladatot kapta a munkahelyén, hogy készítsen kiselőadást a sejtek működésének anatómiájáról - élettanáról! Előadása legyen szakmailag alátámasztva, de a hallgatók számára érthető!
FEJEZETEK AZ ÉLETTAN TANTÁRGYBÓL
 Eke András, Kollai Márk FEJEZETEK AZ ÉLETTAN TANTÁRGYBÓL Szerkesztette: Ivanics Tamás Semmelweis Kiadó www.semmelweiskiado.hu B u d a p e s t, 2 0 0 7 Szerkesztette: Ivanics Tamás egyetemi docens, Semmelweis
Eke András, Kollai Márk FEJEZETEK AZ ÉLETTAN TANTÁRGYBÓL Szerkesztette: Ivanics Tamás Semmelweis Kiadó www.semmelweiskiado.hu B u d a p e s t, 2 0 0 7 Szerkesztette: Ivanics Tamás egyetemi docens, Semmelweis
Mediastinális betegségek CT diagnosztikája
 Mediastinális betegségek CT diagnosztikája Grexa Erzsébet Pécsi Diagnosztikai Központ Mediastinum anatómia Mediastinum - gátorüreg A mellüreg középső részén, a két tüdő által közrefogott üreg. Határai:
Mediastinális betegségek CT diagnosztikája Grexa Erzsébet Pécsi Diagnosztikai Központ Mediastinum anatómia Mediastinum - gátorüreg A mellüreg középső részén, a két tüdő által közrefogott üreg. Határai:
ANATÓMIA KOLLOKVIUMI TÉTELEK II. ÉVFOLYAM 2010/2011. TANÉV 1. FÉLÉV
 Szegedi Tudományegyetem, Általános Orvostudományi Kar Anatómiai, Szövet- és Fejlődéstani Intézete Igazgató: Dr. Mihály András egyetemi tanár 6724 Szeged, Kossuth L. sgt. 40. Telefon: (62)-545-665 6701
Szegedi Tudományegyetem, Általános Orvostudományi Kar Anatómiai, Szövet- és Fejlődéstani Intézete Igazgató: Dr. Mihály András egyetemi tanár 6724 Szeged, Kossuth L. sgt. 40. Telefon: (62)-545-665 6701
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ INTERAKTÍV VIZSGAFELADATHOZ. Szonográfus szakasszisztens szakképesítés
 Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az interaktív vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az interaktív vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
