Készítette: Sándor Gyula Kaposvár 2006
|
|
|
- Barnabás Péter
- 7 évvel ezelőtt
- Látták:
Átírás
1 Készítette: Sándor Gyula Kaposvár 2006
2 Tartalom Atom Molekula Szilárd testek Elemi cella Rácshibák Színfémek Fém ötvözetek Vas szén ötvözetek Izotermikus átalakulás
3 Az atom a kémiai elemek legkisebb része, amely még rendelkezik az elemek tulajdonságaival. Az atom felépítése: Kifelé semleges, az atommagból és a körülötte keringő negatív töltésű elektronokból áll. Az atommag a pozitív töltésű protonokból, valamint a semleges töltésű neutronokból tevődik össze. A rendszám Z, azonos az elem protonszámával, de mivel az atom kifelé semleges, így az elektronok számával is. A tömegszám A, a protonok és neutronok összege, A = Z+N.
4 Vas - és szénatom Fe Ø 2,876 A Ø 1,54 A 0 C Fe ++ Ø 1,66 A 0 1 A 0 = 10-7 mm Ø 0,4 A 0 C ++++ Atomsúly: 56, elektron szám: 26 Atomsúly: 12, elektron szám: 6 Atommag: 26 proton és 30 neutron Atommag: 6 proton és 6 neutron Elektron: 9, gr, proton: 1, gr, neutron: 1, gr Külső héj leadása, vas ion (Fe ++ ) Külső héj leadása, szén ion (C ++++ )
5 Az atomok által létrehozott vegyületek legkisebb része, amely még rendelkezik a vegyület tulajdonságaival. Két, vagy több atom között kialakult kötés eredménye. Az atomok és molekulák a nyomástól és hőmérséklettől függően három állapotban fordulhatnak elő: Rendezetlen állapot (gáz): amelyben sem rövid, sem hosszú távon rendezettség nem tapasztalható, az alak és a térfogat változó.
6 Rövid távú rendezettség állapota (folyékony): amelyben néhány atomnyi, vagy molekulányi távolságban rendezettség tapasztalható, az alak változó míg a térfogat változatlan. Hosszú távú rendezettség állapota (szilárd): amelyben az atomok, vagy molekulák nagy távolságon szabályos rendben helyezkednek el, az alak és a térfogat változatlan. Az energia állapota alacsonyabb.
7 A szilárd testek két nagy csoportba sorolhatók az amorf és a kristályos szerkezetűek közé. Amorf: a rövid távú rendezettségű, nagy viszkozitású folyadékok, határozott olvadásponttal. Fizikai és kémiai tulajdonságaik iránytól függetlenek ezért izotrópok. (üveg, kátrány, viasz) Kristályos: az atomok szabályos rácspontokban helyezkednek el, a köztük kialakuló összetartó kötések alapján megkülönböztetünk elsődleges kötésű és másodlagos kötésű kristályos anyagokat. Elsődleges kötések nagy energiájú, erős: ionos, kovalens, fémes Másodlagos kötés kis energiájú, gyenge: Van der Waals erők, mágneses dipólus (műanyagok). Kötések összefoglalása
8 Ionos kötés NaCl Na F C Na + Cl - Cl Fémes és nemfémes anyagok között jön létre úgy, hogy az egyik atom könnyen leadja az elektront, míg a másik könnyen felveszi, így (+) és ( ) ionok jönnek létre. (NaCl, MgO) Az ionrácsot a Coulomb erők (F C ) tartják össze. Az elektromos áramot és a hőt gyengén vezetik, hőre és alakításra nő a vezetőképesség. Rideg viselkedés, bizonyos síkokban hasíthatók.
9 Kovalens kötés Cl 2 Cl Cl Egymás melletti vagy egymáshoz közeli elemek között jön létre (H 2 O, Cl 2 ) A telített közös külső héj úgy jön létre, hogy mindkét atom ugyanannyi elektront ad a közös pályára így molekulát alkotnak Irányított erős kötés, nem alakíthatók, szigetelők illetve félvezetők lehetnek.
10 ha egy elektront adnak be egy molekula jön létre (Cl2, H2) ha két - két szomszédjukkal kapcsolódva érik el a telítettséget lánc vagy gyűrű molekulát alkotnak (S; Se; láncpolimerek) ha három szomszédjával kapcsolódva érik el a telítettséget, akkor az atomok síkot hoznak létre, az ilyen anyag könnyen hasítható (Bi) a metalloidoknál négy szomszédos atomhoz kapcsolódik, így térbeli kristályrács alakul ki, igen erős irányított kötés (C; Si; Ge)
11 Fémes kötés Olyan atomok között jön létre, amelyek le tudnak adni egy elektront a közös elektronfelhőbe, míg pozitív fémionjaik hosszútávon térbeli rácsrendszerbe rendeződnek. Iránytól független, pozitív fémionokból és a közöttük mozgó elektron felhőből áll. Mivel a kötésük nem irányított így képlékenyen alakíthatóak, amely a kristálysíkok elcsúszásában realizálódik. Az elektromosságot és hőt jól vezetik.
12 Kötések összefoglalása
13 Azt a több atomból álló, legkisebb szabályos geometriai idomot, amely ismétlődéséből épül fel a kristályszerkezet, elemi cellának (rácselemnek) nevezzük. kristálytani sík rácspont kristálytani irány elemi cella rács
14 Elemi cella felépítése Az atomok az elemi cella csúcsaiban (rácspontokban) rezgő mozgást végeznek. A rezgő mozgás nagysága a hőmérséklettől függ (magasabb hőmérsékleten gyorsabb). Azokat a síkokat, amelyeken a szabályosan ismétlődő atomok középpontjai vannak, kristálytani síkoknak nevezzük. Az egymást követő atomok középpontjait összekötő irányt kristálytani irányoknak nevezzük. Az elemi cellákat geometriai alakja és a cellát felépítő atomok száma alapján különböző típusokba soroljuk.
15 Elemi cella típusok I. Köbös: egyszerű köbös (Po) a=b=c, α=β=γ=90 0 térközepes köbös a=b=c, α=β=γ=90 0 lapközepes köbös a=b=c, α=β=γ=90 0
16 Elemi cella típusok II. Tetragonális: egyszerű (Sn) a=b c α=β=γ=90 0 térben középpontos a=b c, α=β=γ=90 0 Ortorombos: a b c α=β=γ=90 0 (Ga, U)
17 Elemi cella típusok III. Hexagonális: a=b=c d, α=β=γ=90 0, δ=120 0 (Mg) legsűrűbb illeszkedésű hexagonális Romboéderes: a=b=c, α 90 0, β 90 0, γ 90 0 (Hg, Bi) Monoklin: a b c, α 90 0, β 90 0, γ=90 0 (S) Triklin: a b c, α 90 0, β 90 0, γ 90 0 (Se)
18 A cellák geometriai jellemzői Az alakváltozások megértéséhez ismerni kell a rácstípusok felépítésétől függő geometriai jellemzőket, amelyek: a koordinációs szám az elemi cellához tartozó atomok száma az atomok átmérője a térkitöltési tényező a síkkitöltési tényező a legnagyobb hézag helye a rácsban
19 Koordinációs szám I. A koordinációs szám (N): a rácsban elhelyezkedő bármely atomot körülvevő legközelebbi szomszédos atomok száma, amelyeket az atom érint. egyszerű köbös A három irány mentén két-két szomszédos atomja van a cella kiválasztott atomjának, így: N = 3x2 = 6
20 Koordinációs szám II. térközepes köbös A kocka közepén lévő atom legközelebbi szomszédjai a nyolc sarokatom, így: N = 8
21 Koordinációs szám III. lapközepes köbös A két rács vízszintes lapja középen lévő atom legközelebbi szomszédjai a vele egy síkon lévő négy sarokatom valamint a felette és alatta lévő négy-négy lapközépen elhelyezkedő atom, így: N = 12
22 A cella atomszáma I. A cellához tartozó atomok száma (A): az atomok térkitöltésének meghatározásához szükséges adat. egyszerű köbös Minden cella csúcsában nyolc atom helyezkedik el. Mindegyik csúcsban lévő atom tagja a nyolc szomszédos cellának. Így A = 8/8 = 1 atom/cella A = 1
23 A cella atomszáma II. térközepes köbös A csúcsokban lévő nyolc atomra ugyan az érvényes mint az egyszerű köbös esetén, tehát egy darab atom tartozik hozzá. Ugyanakkor minden ilyen típusú cella közepén pedig újabb egy atom található. Így A = 8/8 + 1 = 2 atom/cella A = 2
24 A cella atomszáma III. lapközepes köbös A csúcsokban lévő nyolc atomra ugyan az érvényes mint az egyszerű köbös esetén, tehát egy darab atom tartozik hozzá. A lapközepeken lévő hat atom pedig kétkét szomszédos cellával érintkezik, emiatt még három atom tartozik a cellához. A = 8/8 + 6/2 = = 4 atom/cella A = 4
25 Atomátmérő Az atomok nem pontszerűek, ezért az atomok átmérője (d) és a cella mérete (a) között geometriai kapcsolat van. d/2 d/2 a egyszerű köbös d a a d/2 d d/2 a 2 lapközepes köbös d a 2 2 a a d/2 d d/2 a 3 térközepes köbös a d 2 3 a
26 Térkitöltés A térkitöltés T megmutatja a cellához tartozó atomok térfogatának V a és a teljes cella térfogatának V c viszonyszámát. T V V a c 100 % V a a cellához tartozó atomok számának (A) és az egy atom térfogatának szorzata. Egyszerű köbösnél A = 1 és d = a, így: V a 1 3 a 6 V c a cella térfogata Vc a 3 3 a 6 a Tek % T lkk = 74 % T tkk = 68 %
27 Síkkitöltés A síkkitöltés S megmutatja, hogy a cella síkjának A c, hány százalékát takarják le a cellához tartozó atomok A a. S A A a c 100 A legszorosabban illeszkedő síkokban a legnagyobb a kitöltés. % e. k. a l. k. k. a 2 t. k. k. a a a 2 a 2 Sek 2 2 a a ,54% S lkk = 55,48 %
28 A legnagyobb hézag A rácsba illeszthető legnagyobb idegen atom méretét adja meg. Az ötvözeteknél megmutatja, hogy az adott elem, milyen elemmel ötvözhető. Eldönthető, hogy torzul-e a rács vagy nem. a 2 a a 3 a a e. k. r ( 3 1) 0,365 a Egyszerű köbös: Lapközepes köbös: Térközepes köbös r = 0,365 a r = 0,145 a r = 0,126 a
29 Kristályos testek alakváltozása Az atomok a rácspontokban egyensúlyi helyzetben vannak, ezért a rácspontokból történő elmozdításukhoz energiát kell közölni. Az atomok elmozdulása lehet: rugalmas (reverzibilis), maradó (irreverzibilis), vagy más szóval képlékeny. A rugalmas alakváltozást létrehozhatja a húzóerő hatására fellépő húzófeszültség (ζ), vagy a nyíróerő hatására fellépő nyírófeszültség (η). Az alakváltozás akkor lesz képlékeny, ha a nyíróerő hatására fellépő nyírófeszültség (η) nagyobb lesz mint az elméleti szilárdsági érték (η max ).
30 Rugalmas alakváltozás ζ ζ ζ = E ε E G Anyag GPa GPa Al 72 27,6 η Hooke törvény Cu ,5 Szénacél Krómacél ,5 η η = G γ Titán Volfram E = rugalmassági modulusz ε = fajlagos nyúlás G = rugalmassági modulusz γ = szögelforduláás
31 Képlékeny alakváltozás alap rugalmas rugalmas + képlékeny képlékeny csúszási sík Elméleti szilárdság a köbös rendszerben Τ max = G 2 π Az elméleti és a kísérleti szilárdsági értékek között eltérés van, amelynek okai a rácsrendezetlenségek Anyag G (GPa) T elm (GPa) T kís (MPa) T elm / T kis Fe 81, Al 26,4 4,2 0,
32 Tökéletes felépítésű, hibamentes rács nincs! A hibák keletkezésének okai: Szabálytalan kristálynövekedés: A dermedés során kristályosodási középpontok (elemi cellák) alakulnak ki, majd ezek körül jönnek létre a szabályos elrendezésű, de különböző irányú krisztallitok. A krisztallitok gátolják egymást a növekedésben, ezért a szemcsehatárok rendezetlenek lesznek. Idegen atom jelenléte a rácsban (ötvöző, szennyező) Saját atom a szokásostól eltérő helyen Hőkezelés és képlékeny alakítás
33 Rácshibák jelentősége, típusai Miért fontosak a rácshibák? A rácshibák nagyon kis koncentrációban is gyökeresen megváltoztatják az anyagok tulajdonságait. A rácshibák nélkül : a félvezetők nem működnének a fémek szilárdsága sokkal nagyobb lenne a kerámiák szívóssága sokkal nagyobb lenne a kristályoknak nem lenne színük A rácshibákat a kiterjedésük alapján három csoportba soroljuk: Pontszerű hibák (nullméretű hiba) Vonalszerű hibák (egyméretű hiba, diszlokációk) Felületszerű hibák (kétméretű hiba, határhiba) Térfogati hibák
34 Pontszerű hibák I. A hiba pontszerű, ha az ideális kristály geometriai szerkezetében az egyedi atomok rendje megváltozik. Ez a változás a rácsszerkezet néhány atomátmérőnyi részére korlátozódik, itt torzul a rács. Típusai: Üres rácshely (vakcina): a fémkristályban mindig jelen van, hő hatására számuk növekszik (szobahőmérsékleten 1018 atomra jut egy). A kialakulási mechanizmusa: hőre kiszakad egy atom, és diffúziós úton halad a kristályrács belseje felé. Cementálásnál van jelentősége. Előidézheti még: képlékeny alakváltozás, neutron becsapódás.
35 Pontszerű hibák II. Saját atom intersztíciós (beékelt) helyzetben: a kialakulási mechanizmusa, egy atom kilép a megszokott helyéről (A) és a diffúziós folyamat végén más helyen beékelődik egy elemi cellába (B). Körülötte torzul a rács. Idegen atom szubsztituciós (helyettesítés) helyzetben: egy adott rácspontban valamilyen idegen atom (kisebb vagy nagyobb lehet) a rács egy atomját helyettesíti. A rács mindegyik esetben torzul!
36 Pontszerű hibák III. Idegen atom intersztíciós (beékelt) helyzetben: A kialakulási mechanizmusa: a fémrácsban lévő atomok nem töltik ki teljesen a rendelkezésükre álló teret, így az idegen atom a rács atomjai közötti hézagokban tud elhelyezkedni. Csak kis atomátmérőjű elemeknél van erre lehetőség (C, H, O).
37 Vonalszerű rácshibák I. Olyan kristályhiba, amely a rács atomjainak egész sorára kiterjed ki és a kristály elcsúszott és el nem csúszott részének a határát adják. A fémek alakíthatóságában döntő szerepet játszik. Típusai: Éldiszlokáció: csúszási sík extrasík
38 Vonalszerű rácshibák I. Csavardiszlokáció: Vegyes diszlokáció
39 Felületszerű rácshibák Kétdimenziós határok, amelyek olyan tartományokat választanak el, amelyek két oldalán különböző orientációjú, illetve különböző rácsszerkezetű részek találhatók. A felületre merőleges kiterjedése néhány atomátmérőnyi. A hiba lehet kristályszerkezettől független és függő. Rácstól független: Kristályfelület Szemcsehatár Szubszemcsehatár Általános fázishatár Rácstól függő: Rétegződési hiba Összefüggő fázishatár Ikerkristály határ ikerkristály szemcsehatár
40 Az atomok a rácsszerkezetben rezgő mozgást végeznek. Olvadáskor a hő hatására mozgásuk amplitúdója annyira megnő, hogy kiszakadnak a rácsból és az anyag folyékonnyá válik. Q = c m (t 2 t 1 ) Q = az a hőmennyiség, amely az adott tömeget t 1 ről, t 2 re hevíti c = az anyag fajhője m = a test tömege Dermedéskor a mozgás lelassul és néhány atom összekötődéséből kristálycsírák (kristályosodási középpontok) alakulnak ki. Körülöttük elkezdenek duzzadni a kristályok, amelyek szabálytalan határfelülettel összeérnek. Az így kialakult tovább már nem növekvő kristályokat krisztallitoknak nevezzük.
41 ömledék pépes szilárd Színfém lehűlési görbéje T, C 0 dermedés kezdete dermedés vége T D Δt Az olvadás és dermedés azonos hőmérsékleten, T D és Δt idő alatt megy végbe. Gyors hűtéssel finom, míg lassú hűtéssel durva szemcseszerkezet keletkezik. T SZ t, s krisztallit határ krisztallit
42 A színfémeket mechanikai, fizikai és kémiai tulajdonságainak javítása érdekében ötvözik. Egy új tulajdonságokkal rendelkező anyagot állítanak elő. Az ötvözet legalább látszatra egynemű, fémtermészetű anyag, amelyet két vagy több anyag összeolvasztásával nyerünk. A legnagyobb mennyiségben előforduló elem az alapfém. Alkotó elemei többnyire fémek (Fe, Cu, Cr), de lehetnek fémekhez közelálló elemek (C, Si), vagy nemfémes elemek (S, P), sőt gázok (H, N) is. Az ötvözet lehet: szilárd oldat, fémes vegyület és eutektikum.
43 ömledék pépes szilárd Ötvözetek lehűlési görbéje T, C 0 dermedés kezdete dermedés vége T Dk T Dv Δt Az olvadás és dermedés nem azonos hőmérsékleten, hanem ΔT hőmérséklet közben és Δt idő alatt megy végbe. T SZ t, s alapfém ötvözőfém
44 Szilárd oldat I. Rendszerint kétalkotós kristályos fázis, amelynek alkotói közös rácsszerkezetbe illeszkednek a megszilárdulás után úgy, hogy az alkotók nem különböztethetők meg egymástól, homogén krisztallitokat alkotnak. A közös rácsszerkezet az alapfém rácsszerkezetével lesz azonos: Cu (lapközepes) Al (lapközepes) = akkor az ötvözet lapközepes Cu (lapközepes) Sn (tetragonális) = akkor az ötvözet lapközepes A dermedés meghatározott hőközben történik, nem azonos hőmérsékleten mint a színfémeknél.
45 Szilárd oldat II. Kétféle módon jöhet létre: helyettesítéssel vagy beékelődéssel: helyettesítéssel (szubsztituciós): az alapfém elemi cellájának egyes atomjait az ötvöző fém atomjai helyettesítik korlátlan oldódás: azonos rácstípus, az elektrokémiai sorozatba ne álljanak messze egymástól, atomsugár különbség kisebb mint 15%, azonos számú elektront adjanak le korlátolt oldódás: ha az előző feltételek csak részben teljesülnek beékelődéssel (interszticiós): az alapfém elemi cellájának atomjai közötti térben helyezkednek el az ötvöző fém atomjai korlátlan oldódás: 0 100%, kis rendszámú elemek (H, B, O, N), r<10-10 korlátolt oldódás: az oldóképesség felső határát telített oldatnak nevezzük
46 Fémes vegyület Két vagy többalkotós kristályos fázisok, amelynek alkotói közös kristályrács szerkezetbe illeszkednek, de ez a szerkezet független az alkotók rácsszerkezetétől. Az alkotók aránya már állandó és jellemző a vegyületre. Megszilárdulásuk a színfémekhez hasonlóan állandó hőmérsékleten történik. Típusai: ionvegyület: az olvadáspont magas, kismértékben vagy egyáltalán nem oldódnak egymásban az összetevők elektronvegyület: az olvadáspont az alkotók olvadáspontjai közé esik, nagyobb mennyiségben is képesek oldani egymást intersztíciós vegyület: oldóképességük igen kicsi, gyakorlatilag állandó
47 Állapotábra szerkesztés C C 0 A likvidusz pépes olvadék 1083 szilárd szolidusz B Cu Ni 0% 100% 25% 75% 50% 50% 75% 25% 100% 0% t 0% 50% 100% %
48 Jellegzetes állapotábrák I. Ömledék és szilárd állapotban korlátlanul oldódnak, a kialakult ötvözet kizárólag szilárd oldatot alkot. C ömledék szilárd pépes Ni 100% Cu 100% %
49 Jellegzetes állapotábrák II. Ömledék állapotban korlátlanul oldódnak, míg szilárd állapotban nem oldódnak. C H C primer Sn E primer Bi G F Sn 100% Bi 58% Bi 100% 100% 0% 100% 0% 100% 0% Sn ömledék Bi Sn Bi Sn kristály eutektikum Bi kristály % fázisdiagram 200 C 0 fázisdiagram 0 C 0 szövetdiagram
50 Jellegzetes állapotábrák III. ömledék + Ag Ömledék állapotban korlátlanul oldódódnak, míg szilárd állapotban korlátozottan. C 0 H 950 ömledék G α C E Ge 6,5% ömledék + Ge F Ge 18,5% Ag + Ge Ge 4% D Ag 100% α = szilárd oldat mező Ge 100% %
51 Vas - szén ötvözetek A vas (Fe) legfontosabb ötvözője a szén (C), amellyel ömledék állapotban korlátlanul oldódik, míg szilárd állapotban korlátozottan oldódik. Az ötvözéshez a szenet a nagyolvasztóban a kokszból veszi fel. Az ötvözet mindig több szenet tartalmaz, mint amennyivel szobahőmérsékleten szilárd oldatot képezne. A szén kétféle formában fordulhat elő: szabad tiszta szén = grafit: kis szilárdságú, lágy anyag, képlékenyen nem alakítható kötött fémes vegyület = vaskarbid (Fe 3 C), neve cementit: kemény, rideg Az egyensúlyi diagram vizsgálatánál ezért meg kell különböztetni a karbidrendszert (Fe - Fe 3 C) és a karbonrendszert (Fe - C).
52 Fe Fe 3 C egyensúlyi diagram 1538 δ 1394 C 0 A N 0,3% B I H 1,2% 3% 5% D ,3% 1,2% 1148 γ E C F 3% M P G O S A cm A 3 A 1 K 5% α Q 0,02 0,77 2,11 4,3 6,67 Fe % Szövetelemek Fe 3 C %
53 Egyensúlyi diagram elemzése I. A likvidusz az A, B, C, D pontokon áthaladó görbe. A szolidusz az A, H, I, E, C, F, D pontokon áthaladó görbe. A tiszta vas lehűlése során a rácsszerkezet átalakul, ezért szilárd állapotban három egyfázisú (homogén) szövetelem található: az A, H, N pontok között, C 0 hőmérséklet tartományban térközepes köbös δ vas, a szénoldóképessége max. 0,09 % az N, I, E, S, G pontok közötti allotróp átalakulás révén C 0 hőmérséklet tartományban lapközepes köbös ausztenit (γ vas) szilárd oldat jön létre, a szénoldóképessége max. 2,11 % 1148 C 0 -on, lágy jól alakítható, nem mágnesezhető a G, P, Q pontok között ez az állapot nem marad meg, ugyanis 911 C 0 hőmérséklet alatt ismét térközepes köbös szilárd oldat ferrit (α vas) lesz, a szénoldóképessége maximum 0,0218% 727 C 0 -on
54 Egyensúlyi diagram elemzése II. a 770 C 0 - on található M, O vonalig (Curie hőmérséklet) a ferrit mágnesezhető (ferromágneses), ennél magasabb hőmérsékleten nem mágnesezhető (paramágneses) negyedik szilárd fázis lehetne az Fe 3 C, de csak 6,67% széntartalomnál ad homogén ötvözetet Ha C < 2,11 % - nál vas - szén ötvözeteket acéloknak, míg a nagyobbakat nyersvasnak (öntöttvas) nevezzük. A C pont két likvidusz ág találkozási pontja 4,3% C tartalomnál és 1148 C 0 hőmérsékleten, itt ledeburit elnevezésű eutektikum képződik, amely vaskarbidból (FeC 3 ) és ausztenitből (γ) áll, kemény képlékenyen nem alakítható ötvözet ha a széntartalom 2,11-4,3 % között van hipoeutektikus öntötvasról ha a széntartalom 4,3 6,67 % között van hipereutektikus öntötvasról
55 Egyensúlyi diagram elemzése III. Az S pont két korlátozott oldóképességet jelölő görbe találkozási pontja 0,77 % C tartalomnál és 727 C 0 hőmérsékleten, itt perlit elnevezésű eutektoid képződik, amely ferritből (α) és cementitből áll, képlékenyen alakítható, szilárdsága nagyobb mint a ferrité ha a széntartalom 0,0218 0,77 % között van hipoeutektoidos ötvözet ha a széntartalom 0,77 2,11 % között van hipereutektoidos ötvözet eutektoid eutektikum
56 0,3% C tartalmú acél lehűlése 1. a likvidusz felett ömledék 2. a likvidusz és a szolidusz között γ kiválás: γ + ömledék 3. a szolidusztól a GOS (A 3 ) vonalig tisztán γ található 4. a GOS (A 3 ) vonal alatt megkezdődik a γ α átalakulás, amely során ferrit válik ki és tart egyensúlyt az ausztenittel A 1 hőmérsékletig: ferrit + ausztenit 5. az A 1 (727 C 0 ) hőmérséklettől a maradék ausztenit perlitté alakul, a további lehűtés során alacsony karbonkoncentrciójú tercier cementit válik ki A hipoeutektoidos acélok: ferrit, perlit és tercier cementit szövetelemekből állnak.
57 1,2% C tartalmú acél lehűlése 1. a likvidusz felett ömledék 2. a likvidusz és a szolidusz között γ kiválás: γ + ömledék 3. a szolidusztól az ES (A cm ) vonalig tisztán γ található 4. az ES (A cm ) vonaltól secunder cementit válik ki, így itt γ + secunder cementit található 5. az A 1 hőmérséklettől lefelé megindul a γ α átalakulás további secunder cementit kiválás közben, eredménye: perlit + secunder cementit A hipereutektoidos acélok: perlit és secunder cementit szövetelemekből állnak.
58 3% C tartalmú nyersvas lehűlése 1. a likvidusz felett ömledék 2. a likvidusz és az 1147 C 0 között γ kiválás: γ + ömledék C 0 és az A 1 hőmérséklet között ledeburit ledeburit: telített ausztenit és eutektikum eutektikum: ausztenit és cementit 4. az A 1 hőmérséklettől lefelé megindul a γ α átalakulás, nagyobb karbontartalmú cementit kiválás közben, eredménye: perlit + secunder cementit A hipoeutektikus öntöttvasak: perlit, ledeburit és secunder cementit szövetelemekből állnak.
59 5% C tartalmú nyersvas lehűlése 1. a likvidusz felett ömledék 2. a likvidusz és a szolidusz (1147 C 0 ) között diffúzió révén primer cementit válik ki: ömledék + primer cementit 3. az 1147 C 0 és az A 1 hőmérséklet között ledeburit és primer cementit alakul ki 4. A 1 hőmérséklet alatt már változás nem történik A hipereutektikus öntöttvasak: ledeburit és primer cementit szövetelemekből állnak.
60 α+perlit+terc.cem. Szövetelemek elhelyezkedése 1538 δ P α C 0 A N M G H γ B O S I γ + ömledék E γ + sec. cem. perlit + sec. cem. γ + ledeburit + sec. cem. perlit + ledeburit + sec. cem. ömledék C D primer cem. + öml. primer cem. + ledeburit primer cem. + ledeburit 1227 F K Q 0,02 0,77 2,11 4,3 6,67
61 Szövetelemek tulajdonságai Ausztenit (γ) lapközepes, intersztíciós szilárd oldat lágy, jól alakítható, nem mágnesezhető Ferrit (α) térközepes köbös intersztíciós szilárd oldat lágy, jól alakítható adott hőmérsékleti mágnesezhető (774 C 0 ) Cementit (Fe 3 C) Perlit Fe 3 C intersztíciós vegyület kemény, rideg, nem alakítható ferritbe ágyazott cementit lemezkék képlékenyen alakítható
62 Izotermikus átalakulás Az egyensúlyi diagram szövetelemei lassú hűtéssel alakulnak ki, a gyártásban ez költséges lenne. Évszázadok óta a vastárgyak tulajdonságait úgy változtatták meg, hogy C 0 közé hevítették, majd gyorsan lehűtötték. Ezzel az eljárással merőben más tulajdonságú szövetelemeket lehetett előállítani (bainit, martenzit). Izotermikus átalakulási diagram szerkesztése: azonos próbatesteket különböző hőmérsékletekre hűtöttek és ott hőn tartották így megkapták az ausztenit átalakulásának kezdő és végpontját a pontokat összekötve C alakot kaptak, innen az elnevezés a hűtéskor két jelenség játszódik le: diffúzió és γ α átalakulás
63 C görbe szerkesztése C 0 A 3 A 1 P k P v B k B v M k M v log t
64 Lehűlési sebesség C 0 A 3 A 1 v hűtés < v krit. alsó ausztenit perlit v hűtés > v krit. felső ausztenit martenzit v krit. alsó < v hűtés < v krit. felső mindkettő M k M v v krit. felső v krit. alsó log t
65 Mag és felszín hűlése C 0 belső rész lehűlési sebessége A 3 A 1 Más szövetszerkezet alakulhat ki a magban a kéreghez képest! M K M V külső rész lehűlési sebessége log t
66 Perlites átalakulás A perlit kialakulása az A 1 és 550 C 0 között megy végbe. Diffúziós folyamat, elsődleges az Fe 3 C diffúziója és másodlagos a γ α átalakulás. Cementit csírák alakulnak ki az ausztenit határain, a diffúzió révén cementit korongokká válnak, ezért lemezes szerkezetű kétfázisú szövetelem lesz a perlit. Minél alacsonyabb hőmérsékleten megy végbe annál nagyobb lesz a szilárdsága. Gyors hűtéssel finomítani lehet a szemcseméretet, így nő a szilárdság, de csökken a nyúlás (sorbit, troostil). Fe 3 C lemezek ferrit (α) lemezek
67 Bainites átalakulás A bainit kialakulása 550 C 0 és 250 C 0 között játszódik le. Szintén diffúziós folyamat, de ebben a γ α átalakulás az elsődleges és az Fe 3 C diffúziója a másodlagos. Az ausztenit szemcsék határán ferritcsírák jelennek meg és belőlük tűs kristályszerkezet és cementit korongok halmaza alakul ki, amely kétfázisú szövetelem. Szilárdsága nagyobb, nyúlása kisebb mint a perlité. Minél alacsonyabb hőmérsékleten megy végbe annál nagyobb lesz a keménység.
68 Martenzites átalakulás A gyors lehűlés miatt csak γ α átalakulás van, mert ennek az átalakulásnak igen kicsi az időszükséglete, a diffúzió ilyen rövid idő alatt nem tud végbemenni, ezért ez az átalakulás diffúzió mentes. Az átalakulás során beékelődő szén atomok tetragonálissá torzítják a térközepes köbös rácsot, az így kialakult feszültséget az M k alatti hőntartással lehet csökkenteni az anyagban. Ez a szövetelem egyfázisú, keménysége a széntartalomtól függ. Igen kemény, rideg nem alakítható. durvaszemcsés finomszemcsés
69 Diagramok A torzítás mértéke az ausztenit C tartalmának függvénye A torzulás nagy belső feszültséget eredményez, ami a martenzitet nagyon keménnyé, rideggé teszi.
70
Vas- karbon ötvözetrendszer. Összeállította: Csizmazia Ferencné dr.
 Vas- karbon ötvözetrendszer Összeállította: Csizmazia Ferencné dr. 1 Vas- Karbon diagram 2 Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Vas- karbon ötvözetrendszer Összeállította: Csizmazia Ferencné dr. 1 Vas- Karbon diagram 2 Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Vas- karbon ötvözetrendszer
 Vas- karbon ötvözetrendszer Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos, és szaggatott vonallal is fel vannak
Vas- karbon ötvözetrendszer Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos, és szaggatott vonallal is fel vannak
Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások.
 Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások. dr. Fábián Enikő Réka fabianr@eik.bme.hu BMEGEMTAGM3-HŐKEZELÉS 2016/2017 Kétalkotós ötvözetrendszerekkel kapcsolatos alapfogalmak Az alkotók
Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások. dr. Fábián Enikő Réka fabianr@eik.bme.hu BMEGEMTAGM3-HŐKEZELÉS 2016/2017 Kétalkotós ötvözetrendszerekkel kapcsolatos alapfogalmak Az alkotók
Szilárdság (folyáshatár) növelési eljárások
 Képlékeny alakítás Szilárdság (folyáshatár) növelési eljárások Szemcseméret csökkentés Hőkezelés Ötvözés allotróp átalakulással rendelkező ötvözetek kiválásos nemesítés diszperziós keményítés interstíciós
Képlékeny alakítás Szilárdság (folyáshatár) növelési eljárások Szemcseméret csökkentés Hőkezelés Ötvözés allotróp átalakulással rendelkező ötvözetek kiválásos nemesítés diszperziós keményítés interstíciós
A nagytermi gyakorlat fő pontjai
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2008/09 Fe-C állapotábra Dr. Reé András ree@eik.bme.hu Fe-C 1 A nagytermi gyakorlat fő pontjai A Fe-C állapotábra felépítése Stabil (grafit) rendszer Metastabil
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2008/09 Fe-C állapotábra Dr. Reé András ree@eik.bme.hu Fe-C 1 A nagytermi gyakorlat fő pontjai A Fe-C állapotábra felépítése Stabil (grafit) rendszer Metastabil
Az atomok elrendeződése
 Anyagtudomány 2015/16 Kristályok, rácshibák, ötvözetek, termikus viselkedés (ismétlés) Dr. Szabó Péter János szpj@eik.bme.hu Az atomok elrendeződése Hosszú távú rend (kristályok) Az atomok elhelyezkedését
Anyagtudomány 2015/16 Kristályok, rácshibák, ötvözetek, termikus viselkedés (ismétlés) Dr. Szabó Péter János szpj@eik.bme.hu Az atomok elrendeződése Hosszú távú rend (kristályok) Az atomok elhelyezkedését
A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram)
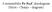 A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram) A vas-karbon egyensúlyi diagram alapvető fontosságú a vasötvözetek tárgyalásánál. Az Fe-C ötvözetekre vonatkozó ismereteket általában kettős
A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram) A vas-karbon egyensúlyi diagram alapvető fontosságú a vasötvözetek tárgyalásánál. Az Fe-C ötvözetekre vonatkozó ismereteket általában kettős
Színfémek és ötvözetek egyensúlyi lehőlése
 Színfémek és ötvözetek egyensúlyi lehőlése 1 Színfém lehőlési görbéje (nincs allotróp átalakulás) F + Sz = K + 1. K = 1 1. Szakasz F=1 olvadék Sz =1 T változhat 2. Szakasz F=2 olvadék + szilárd Sz= 0 T
Színfémek és ötvözetek egyensúlyi lehőlése 1 Színfém lehőlési görbéje (nincs allotróp átalakulás) F + Sz = K + 1. K = 1 1. Szakasz F=1 olvadék Sz =1 T változhat 2. Szakasz F=2 olvadék + szilárd Sz= 0 T
A fémek egyensúlyi viselkedése. A fémek kristályos szerkezete
 A fémek egyensúlyi viselkedése A fémek kristályos szerkezete Kristályos szerkezet A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. Azt a legkisebb - több atomból álló -
A fémek egyensúlyi viselkedése A fémek kristályos szerkezete Kristályos szerkezet A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. Azt a legkisebb - több atomból álló -
Reális kristályok, rácshibák. Anyagtudomány gyakorlat 2006/2007 I.félév Gépész BSC
 Reális kristályok, rácshibák Anyagtudomány gyakorlat 2006/2007 I.félév Gépész BSC Valódi, reális kristályok Reális rács rendezetlenségeket, rácshibákat tartalmaz Az anyagok tulajdonságainak bizonyos csoportja
Reális kristályok, rácshibák Anyagtudomány gyakorlat 2006/2007 I.félév Gépész BSC Valódi, reális kristályok Reális rács rendezetlenségeket, rácshibákat tartalmaz Az anyagok tulajdonságainak bizonyos csoportja
Anyagszerkezet és vizsgálat. 4. Előadás: Vas-karbon ötvözetrendszer
 SZÉCHENYI ISTVÁN EGYETEM Anyagismereti és Járműgyártási Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 4. Előadás: Vas-karbon ötvözetrendszer 2010. 10. 11. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
SZÉCHENYI ISTVÁN EGYETEM Anyagismereti és Járműgyártási Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 4. Előadás: Vas-karbon ötvözetrendszer 2010. 10. 11. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ
 TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ Vas-karbon diagram: A vas olvadáspontja: a) 1563 C. b) 1536 C. c) 1389 C. Mennyi a vas A1-el jelölt hőmérséklete? b) 1538 C. Mennyi a vas A2-el jelölt hőmérséklete?
TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ Vas-karbon diagram: A vas olvadáspontja: a) 1563 C. b) 1536 C. c) 1389 C. Mennyi a vas A1-el jelölt hőmérséklete? b) 1538 C. Mennyi a vas A2-el jelölt hőmérséklete?
Mérnöki anyagok Járműszerkezeti anyagok. Vas-karbon ötvözetrendszer Egyensúlyi átalakulások
 SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Mérnöki anyagok Járműszerkezeti anyagok Vas-karbon ötvözetrendszer Egyensúlyi átalakulások Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Mérnöki anyagok Járműszerkezeti anyagok Vas-karbon ötvözetrendszer Egyensúlyi átalakulások Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
Egyensúlyitól eltérő átalakulások
 Egyensúlyitól eltérő átalakulások Egyensúlyitól eltérő átalakulások Az előzőekben láttuk, hogy az egyensúlyi diagramok alapján meg lehet határozni a kristályosodás, a fázis átalakulások stb. hőmérsékleteit.
Egyensúlyitól eltérő átalakulások Egyensúlyitól eltérő átalakulások Az előzőekben láttuk, hogy az egyensúlyi diagramok alapján meg lehet határozni a kristályosodás, a fázis átalakulások stb. hőmérsékleteit.
Fémek és ötvözetek termikus viselkedése
 Anyagtudomány és Technológia Tanszék Fémek és ötvözetek termikus viselkedése Dr. Szabó Péter János szpj@eik.bme.hu Anyagszerkezettan és anyagvizsgálat BMEGEMTBGA1 2018/2019/2 Az előadás során megismerjük
Anyagtudomány és Technológia Tanszék Fémek és ötvözetek termikus viselkedése Dr. Szabó Péter János szpj@eik.bme.hu Anyagszerkezettan és anyagvizsgálat BMEGEMTBGA1 2018/2019/2 Az előadás során megismerjük
41. ábra A NaCl rács elemi cellája
 41. ábra A NaCl rács elemi cellája Mindkét rácsra jellemző, hogy egy tetszés szerint kiválasztott pozitív vagy negatív töltésű iont ellentétes töltésű ionok vesznek körül. Különbség a közvetlen szomszédok
41. ábra A NaCl rács elemi cellája Mindkét rácsra jellemző, hogy egy tetszés szerint kiválasztott pozitív vagy negatív töltésű iont ellentétes töltésű ionok vesznek körül. Különbség a közvetlen szomszédok
Anyagismeret. 3. A vas- karbon ötvözet
 Anyagismeret 3. A vas- karbon ötvözet A fémek és ötvözetek szerkezete Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Anyagismeret 3. A vas- karbon ötvözet A fémek és ötvözetek szerkezete Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Fogorvosi anyagtan fizikai alapjai 5. Általános anyagszerkezeti ismeretek Fémek, ötvözetek
 Fémek törékeny/képlékeny nemesémek magas/alacsony o.p. Fogorvosi anyagtan izikai alapjai 5. Általános anyagszerkezeti ismeretek Fémek, ötvözetek ρ < 5 g cm 3 könnyűémek 5 g cm3 < ρ nehézémek 2 Fémek tulajdonságai
Fémek törékeny/képlékeny nemesémek magas/alacsony o.p. Fogorvosi anyagtan izikai alapjai 5. Általános anyagszerkezeti ismeretek Fémek, ötvözetek ρ < 5 g cm 3 könnyűémek 5 g cm3 < ρ nehézémek 2 Fémek tulajdonságai
Fe-C állapotábra ábra A Fe-C ötvözetek állapotábrája
 41 Fe-C állapotábra Nagy ipari jelentőségük miatt a Fe C ötvözetek állapotábrája volt az első, amit a XX. század elején megszerkesztettek. Azóta az anyagszerkezeti ismeretek jelentősen bővültek, a mérőeszközök
41 Fe-C állapotábra Nagy ipari jelentőségük miatt a Fe C ötvözetek állapotábrája volt az első, amit a XX. század elején megszerkesztettek. Azóta az anyagszerkezeti ismeretek jelentősen bővültek, a mérőeszközök
A fémek egyensúlyi viselkedése. A fémek kristályos szerkezete
 A fémek egyensúlyi viselkedése A fémek kristályos szerkezete Kristályos szerkezet A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. Azt a legkisebb - több atomból álló -
A fémek egyensúlyi viselkedése A fémek kristályos szerkezete Kristályos szerkezet A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. Azt a legkisebb - több atomból álló -
5 előadás. Anyagismeret
 5 előadás Anyagismeret Ötvözet Legalább látszatra egynemű fémes anyag, amit két vagy több alkotó különböző módszerekkel való egyesítése után állítunk elő. Alapötvöző minden esetben fémes anyag. Ötvöző
5 előadás Anyagismeret Ötvözet Legalább látszatra egynemű fémes anyag, amit két vagy több alkotó különböző módszerekkel való egyesítése után állítunk elő. Alapötvöző minden esetben fémes anyag. Ötvöző
Tematika. Az atomok elrendeződése Kristályok, rácshibák
 Anyagtudomány 2013/14 Kristályok, rácshibák Dr. Szabó Péter János szpj@eik.bme.hu Tematika 1. hét: Bevezetés. 2. hét: Kristályok, rácshibák. 3. hét: Ötvözetek. 4. hét: Mágneses és elektromos anyagok. 5.
Anyagtudomány 2013/14 Kristályok, rácshibák Dr. Szabó Péter János szpj@eik.bme.hu Tematika 1. hét: Bevezetés. 2. hét: Kristályok, rácshibák. 3. hét: Ötvözetek. 4. hét: Mágneses és elektromos anyagok. 5.
American Society of Materials. Szilárdtestek. Fullerének (C atomok, sokszögek) zárt gömb, tojás cső (egy és többrétegű)
 Szilárdtestek Fullerének (C atomok, sokszögek) zárt gömb, tojás cső (egy és többrétegű) csavart alakzatok (spirál, tórusz, stb.) egyatomos vastagságú sík, grafén (0001) Amorf (atomok geometriai rend nélkül)
Szilárdtestek Fullerének (C atomok, sokszögek) zárt gömb, tojás cső (egy és többrétegű) csavart alakzatok (spirál, tórusz, stb.) egyatomos vastagságú sík, grafén (0001) Amorf (atomok geometriai rend nélkül)
Anyagtudomány. Ötvözetek egyensúlyi diagramjai (állapotábrák)
 Anyagtudomány Ötvözetek egyensúlyi diagramjai (állapotábrák) Kétkomponensű fémtani rendszerek fázisai és szövetelemei Folyékony, olvadék fázis Színfém (A, B) Szilárd oldat (α, β) (szubsztitúciós, interstíciós)
Anyagtudomány Ötvözetek egyensúlyi diagramjai (állapotábrák) Kétkomponensű fémtani rendszerek fázisai és szövetelemei Folyékony, olvadék fázis Színfém (A, B) Szilárd oldat (α, β) (szubsztitúciós, interstíciós)
Anyagszerkezet és vizsgálat. 2. Előadás
 SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 2. Előadás 2012. 09. 17. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr. előadásanyagai alapján) 1
SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 2. Előadás 2012. 09. 17. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr. előadásanyagai alapján) 1
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK. Anyagismeret 2016/17. Szilárdságnövelés. Dr. Mészáros István Az előadás során megismerjük
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2016/17 Szilárdságnövelés Dr. Mészáros István meszaros@eik.bme.hu 1 Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2016/17 Szilárdságnövelés Dr. Mészáros István meszaros@eik.bme.hu 1 Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Acélok nem egyensúlyi átalakulásai
 Acélok nem egyensúlyi átalakulásai Acélok egyensúlyitól eltérő átalakulásai Az ausztenit átalakulásai lassú hűtés Perlit diffúziós átalakulás α+fe 3 C rétegek szilárdság közepes martensit bainit finom
Acélok nem egyensúlyi átalakulásai Acélok egyensúlyitól eltérő átalakulásai Az ausztenit átalakulásai lassú hűtés Perlit diffúziós átalakulás α+fe 3 C rétegek szilárdság közepes martensit bainit finom
Ötvözetek, állapotábrák. Az előadás során megismerjük: Ötvözetek szerkezete Homogén?
 Anyagismeret 2017/18 Ötvözetek, állapotábrák Dr. Mészáros István meszaros@eik.bme.hu Az előadás során megismerjük: Az ötvözetek szerkezetét; Az állapotábrák termodinamikai alapjait; Az alapvető állapotábrákat
Anyagismeret 2017/18 Ötvözetek, állapotábrák Dr. Mészáros István meszaros@eik.bme.hu Az előadás során megismerjük: Az ötvözetek szerkezetét; Az állapotábrák termodinamikai alapjait; Az alapvető állapotábrákat
Bevezetés a lézeres anyagmegmunkálásba
 Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 6. Anyagcsaládok Fémek Kerámiák, üvegek Műanyagok Kompozitok A családok közti különbségek tárgyalhatóak: atomi szinten
Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 6. Anyagcsaládok Fémek Kerámiák, üvegek Műanyagok Kompozitok A családok közti különbségek tárgyalhatóak: atomi szinten
Réz és ötvözetei. Katt ide! Technikusoknak
 Réz és ötvözetei Katt ide! Technikusoknak Tartalomjegyzék Réz Sárgaréz Ónbronz Alumíniumbronz Bemutató vége Réz tulajdonságai Hidegen jól alakítható, nagy gázoldó képessége miatt rosszul önthető. Kémiailag
Réz és ötvözetei Katt ide! Technikusoknak Tartalomjegyzék Réz Sárgaréz Ónbronz Alumíniumbronz Bemutató vége Réz tulajdonságai Hidegen jól alakítható, nagy gázoldó képessége miatt rosszul önthető. Kémiailag
Anyagszerkezet és vizsgálat. 2. Előadás
 SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 2. Előadás 2013. 09. 10. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr. előadásanyagai alapján) 1
SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 2. Előadás 2013. 09. 10. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr. előadásanyagai alapján) 1
Anyagszerkezet és vizsgálat Fémtan, anyagvizsgálat
 SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat Fémtan, anyagvizsgálat Dr. Hargitai Hajnalka hargitai@sze.hu www.sze.hu/~hargitai B 403. (L316) (Csizmazia Ferencné
SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat Fémtan, anyagvizsgálat Dr. Hargitai Hajnalka hargitai@sze.hu www.sze.hu/~hargitai B 403. (L316) (Csizmazia Ferencné
Fogászati anyagok fajtái. Fogorvosi anyagtan fizikai alapjai 5. Általános anyagszerkezeti ismeretek Anyagcsaládok: fémek, kerámiák.
 Fogászati anyagok fajtái Fémes kötés FÉMEK KERÁMIÁK Fémes és nemfémes elemek vegyületei. Fogorvosi anyagtan fizikai alapjai 5. Általános anyagszerkezeti ismeretek Anyagcsaládok: fémek, kerámiák Kiemelt
Fogászati anyagok fajtái Fémes kötés FÉMEK KERÁMIÁK Fémes és nemfémes elemek vegyületei. Fogorvosi anyagtan fizikai alapjai 5. Általános anyagszerkezeti ismeretek Anyagcsaládok: fémek, kerámiák Kiemelt
Anyagszerkezet és vizsgálat
 SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 Dr. Hargitai Hajnalka hargitai@sze.hu www.sze.hu/~hargitai B 403. (L316) (Csizmazia Ferencné dr.
SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 Dr. Hargitai Hajnalka hargitai@sze.hu www.sze.hu/~hargitai B 403. (L316) (Csizmazia Ferencné dr.
Atomerőművi anyagvizsgálatok 4. előadás: Fémtan
 Budapesti Műszaki- és Gazdaságtudományi Egyetem (BME) Nukleáris Technikai Intézet (NTI) Atomerőművi anyagvizsgálatok 4. előadás: Fémtan Tárgyfelelős: Dr. Aszódi Attila Előadó: Kiss Attila 2012-2013. ősz
Budapesti Műszaki- és Gazdaságtudományi Egyetem (BME) Nukleáris Technikai Intézet (NTI) Atomerőművi anyagvizsgálatok 4. előadás: Fémtan Tárgyfelelős: Dr. Aszódi Attila Előadó: Kiss Attila 2012-2013. ősz
ANYAGSZERKEZETTAN II.
 ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK BSc KÉPZÉS (levelező munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET
ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK BSc KÉPZÉS (levelező munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET
KRISTÁLYHIBÁK. Rácsot összetartó erők
 KRISTÁLYHIBÁK Azokat a helyeket, tartományokat a kristályban, amelyekben az anyagi részecskék rendje nem olyan tökéletes, mint a térrácsban a rácspontoké, kristályhibának nevezzük. A kristályok felülete
KRISTÁLYHIBÁK Azokat a helyeket, tartományokat a kristályban, amelyekben az anyagi részecskék rendje nem olyan tökéletes, mint a térrácsban a rácspontoké, kristályhibának nevezzük. A kristályok felülete
Fázisátalakulás Fázisátalakulások diffúziós (egyedi atomi mozgás) martenzites (kollektív atomi mozgás, diffúzió nélkül)
 ázisátalakulások, P, C változása új (egyensúlyi) állapot Új fázis(ok): stabil, metastabil ázisátalakulás: folyamat, amelynek során a régi fázis(ok)ból új, más szerkezetű (rács, szövet) vagy halmazállapotú
ázisátalakulások, P, C változása új (egyensúlyi) állapot Új fázis(ok): stabil, metastabil ázisátalakulás: folyamat, amelynek során a régi fázis(ok)ból új, más szerkezetű (rács, szövet) vagy halmazállapotú
Az atom- olvasni. 1. ábra Az atom felépítése 1. Az atomot felépítő elemi részecskék. Proton, Jele: (p+) Neutron, Jele: (n o )
 Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
ANYAGSZERKEZETTAN II.
 ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR ANYAGTUDOMÁNYI INTÉZET Miskolc, 2008. 1. TANTÁRGYLEÍRÁS Anyagszerkezettan II. kommunikációs
ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR ANYAGTUDOMÁNYI INTÉZET Miskolc, 2008. 1. TANTÁRGYLEÍRÁS Anyagszerkezettan II. kommunikációs
HŐKEZELÉS 2016/2017 ősz BMEGEMTAGM3
 HŐKEZELÉS 2016/2017 ősz BMEGEMTAGM3 Dr. Fá Fábiá bián Enikő Enikő Réka fabianr@eik.bme.hu fabianr@eik.bme.hu Mechanikai tulajdonságok hőkezelés után- jegyzőkönyv Fénymikroszkópos labor jegyzőkönyv Felületi
HŐKEZELÉS 2016/2017 ősz BMEGEMTAGM3 Dr. Fá Fábiá bián Enikő Enikő Réka fabianr@eik.bme.hu fabianr@eik.bme.hu Mechanikai tulajdonságok hőkezelés után- jegyzőkönyv Fénymikroszkópos labor jegyzőkönyv Felületi
ANYAGSZERKEZETTAN II.
 ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK BSc KÉPZÉS (nappali munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET Miskolc,
ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK BSc KÉPZÉS (nappali munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET Miskolc,
Szilárdságnövelés. Az előadás során megismerjük. Szilárdságnövelési eljárások
 Anyagszerkezettan és anyagvizsgálat 2015/16 Szilárdságnövelés Dr. Szabó Péter János szpj@eik.bme.hu Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti alapjait; Technológiai
Anyagszerkezettan és anyagvizsgálat 2015/16 Szilárdságnövelés Dr. Szabó Péter János szpj@eik.bme.hu Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti alapjait; Technológiai
(C) Dr. Bagyinszki Gyula: ANYAGTECHNOLÓGIA II.
 HŐKEZELÉS Hőkezelés az anyagok ill. a belőlük készült fél- és készgyártmányok meghatározott program szerinti felhevítése hőntartása lehűtése a mikroszerkezet ill. a feszültségállapot megváltoztatása és
HŐKEZELÉS Hőkezelés az anyagok ill. a belőlük készült fél- és készgyártmányok meghatározott program szerinti felhevítése hőntartása lehűtése a mikroszerkezet ill. a feszültségállapot megváltoztatása és
Folyadékok. Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok.
 Folyadékok folyékony nincs saját alakja szilárd van saját alakja (deformálás után úgy marad, nem (deformálás után visszaalakul, mert ébrednek benne visszatérítő nyíróerők) visszatérítő nyíróerők léptek
Folyadékok folyékony nincs saját alakja szilárd van saját alakja (deformálás után úgy marad, nem (deformálás után visszaalakul, mert ébrednek benne visszatérítő nyíróerők) visszatérítő nyíróerők léptek
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
ACÉLOK MÉRNÖKI ANYAGOK
 ACÉLOK MÉRNÖKI ANYAGOK 80%-a (5000 kg/fő/év) kerámia, kő, homok... Ebből csak kb. 7% a iparilag előállított cserép, cement, tégla, porcelán... 14%-a (870 kg/fő/év) a polimerek csoportja, melynek kb. 90%-a
ACÉLOK MÉRNÖKI ANYAGOK 80%-a (5000 kg/fő/év) kerámia, kő, homok... Ebből csak kb. 7% a iparilag előállított cserép, cement, tégla, porcelán... 14%-a (870 kg/fő/év) a polimerek csoportja, melynek kb. 90%-a
Anyagszerkezettan vizsgajegyzet
 - 1 - Anyagszerkezettan vizsgajegyzet Előadástémák: 1. Atomszerkezet 1.1. Atommag 1.2. Atomszám 1.3. Atomtömeg 1.4. Bohr-féle atommodell 1.5. Schrödinger-egyenlet 1.6. Kvantumszámok 1.7. Elektron orbitál
- 1 - Anyagszerkezettan vizsgajegyzet Előadástémák: 1. Atomszerkezet 1.1. Atommag 1.2. Atomszám 1.3. Atomtömeg 1.4. Bohr-féle atommodell 1.5. Schrödinger-egyenlet 1.6. Kvantumszámok 1.7. Elektron orbitál
KRISTÁLYOK GEOMETRIAI LEÍRÁSA
 KRISTÁLYOK GEOMETRIAI LEÍRÁSA Kristály Bázis Pontrács Ideális Kristály: hosszútávúan rendezett hibamentes, végtelen szilárd test Kristály Bázis: a kristály legkisebb, ismétlœdœ atomcsoportja Rácspont:
KRISTÁLYOK GEOMETRIAI LEÍRÁSA Kristály Bázis Pontrács Ideális Kristály: hosszútávúan rendezett hibamentes, végtelen szilárd test Kristály Bázis: a kristály legkisebb, ismétlœdœ atomcsoportja Rácspont:
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK
 NYGTUDOMÁNY ÉS TECHNOLÓGI TNSZÉK nyagismeret 2008/09 célok hőkezelése dr. Németh Árpád arpinem@eik.bme.hu Törköly Tamás torkoly@gmail.com Ötvözetlen acélok 3 f.k.k. c3 1 t.k.k. hipoeutektoidosl EUTEKTOIDOS,
NYGTUDOMÁNY ÉS TECHNOLÓGI TNSZÉK nyagismeret 2008/09 célok hőkezelése dr. Németh Árpád arpinem@eik.bme.hu Törköly Tamás torkoly@gmail.com Ötvözetlen acélok 3 f.k.k. c3 1 t.k.k. hipoeutektoidosl EUTEKTOIDOS,
ANYAGISMERET I. ACÉLOK
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK ANYAGISMERET I. ACÉLOK Dr. Palotás Béla Dr. Németh Árpád Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus Hipereutektikus
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK ANYAGISMERET I. ACÉLOK Dr. Palotás Béla Dr. Németh Árpád Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus Hipereutektikus
Diffúzió 2003 március 28
 Diffúzió 3 március 8 Diffúzió: különféle anyagi részecskék (szilárd, folyékony, gáznemű) anyagon belüli helyváltozása. Szilárd anyagban való mozgás Öndiffúzió: a rácsot felépítő saját atomok energiaszint-különbség
Diffúzió 3 március 8 Diffúzió: különféle anyagi részecskék (szilárd, folyékony, gáznemű) anyagon belüli helyváltozása. Szilárd anyagban való mozgás Öndiffúzió: a rácsot felépítő saját atomok energiaszint-különbség
Folyadékok. Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok
 Folyadékok víz Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok 1 saját térfogat nincs saját alak/folyékony nincsenek belső nyíróerők
Folyadékok víz Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok 1 saját térfogat nincs saját alak/folyékony nincsenek belső nyíróerők
Anyagismeret tételek
 Anyagismeret tételek 1. Iparban használatos anyagok csoportosítása - Anyagok: - fémek: - vas - nem vas: könnyű fémek, nehéz fémek - nemesfémek - nem fémek: - műanyagok: - hőre lágyuló - hőre keményedő
Anyagismeret tételek 1. Iparban használatos anyagok csoportosítása - Anyagok: - fémek: - vas - nem vas: könnyű fémek, nehéz fémek - nemesfémek - nem fémek: - műanyagok: - hőre lágyuló - hőre keményedő
A testek részecskéinek szerkezete
 A testek részecskéinek szerkezete Minden test részecskékből, atomokból vagy több atomból álló molekulákból épül fel. Az atomok is összetettek: elektronok, protonok és neutronok találhatók bennük. Az elektronok
A testek részecskéinek szerkezete Minden test részecskékből, atomokból vagy több atomból álló molekulákból épül fel. Az atomok is összetettek: elektronok, protonok és neutronok találhatók bennük. Az elektronok
A szilárd testek alakja és térfogata észrevehetően csak nagy erő hatására változik meg. A testekben a részecskék egymáshoz közel vannak, kristályos
 Az anyagok lehetséges állapotai, a fizikai körülményektől (nyomás, hőmérséklet) függően. Az anyagokat általában a normál körülmények között jellemző állapotuk alapján soroljuk be szilád, folyékony vagy
Az anyagok lehetséges állapotai, a fizikai körülményektől (nyomás, hőmérséklet) függően. Az anyagokat általában a normál körülmények között jellemző állapotuk alapján soroljuk be szilád, folyékony vagy
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS
 Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
MÉRNÖKI ANYAGISMERET AJ002_1 Közlekedésmérnöki BSc szak Csizmazia Ferencné dr. főiskolai docens B 403. Dr. Dogossy Gábor Egyetemi adjunktus B 408
 MÉRNÖKI ANYAGISMERET AJ002_1 Közlekedésmérnöki BSc szak Csizmazia Ferencné dr. főiskolai docens B 403 Dr. Dogossy Gábor Egyetemi adjunktus B 408 Az anyag Az anyagot az ember nyeri ki a természetből és
MÉRNÖKI ANYAGISMERET AJ002_1 Közlekedésmérnöki BSc szak Csizmazia Ferencné dr. főiskolai docens B 403 Dr. Dogossy Gábor Egyetemi adjunktus B 408 Az anyag Az anyagot az ember nyeri ki a természetből és
Bevezetés az anyagtudományba III. előadás
 Bevezetés az anyagtudományba III. előadás 2010. február 18. Kristályos és s nem-krist kristályos anyagok A kristályos anyag atomjainak elrendeződése sok atomnyi távolságig, a tér mindhárom irányában periodikusan
Bevezetés az anyagtudományba III. előadás 2010. február 18. Kristályos és s nem-krist kristályos anyagok A kristályos anyag atomjainak elrendeződése sok atomnyi távolságig, a tér mindhárom irányában periodikusan
ANYAGSZERKEZETTAN II.
 ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET Miskolc, 2013. 1. TANTÁRGYLEÍRÁS
ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET Miskolc, 2013. 1. TANTÁRGYLEÍRÁS
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Halmazállapotok. Gáz, folyadék, szilárd
 Halmazállapotok Gáz, folyadék, szilárd A levegővel telt üveghengerbe brómot csepegtetünk. A bróm illékony, azaz könnyen alakul gázhalmazállapotúvá. A hengerben a levegő részecskéi keverednek a bróm részecskéivel
Halmazállapotok Gáz, folyadék, szilárd A levegővel telt üveghengerbe brómot csepegtetünk. A bróm illékony, azaz könnyen alakul gázhalmazállapotúvá. A hengerben a levegő részecskéi keverednek a bróm részecskéivel
Kondenzált anyagok csoportosítása
 Szilárdtestfizika Kondenzált anyagok csoportosítása 1. Üvegek Nagy viszkozitású olvadék állapotú anyagok, amelyek nagyon lassan szilárd állapotba mennek át. Folyékony állapotból gyors hűtéssel állíthatók
Szilárdtestfizika Kondenzált anyagok csoportosítása 1. Üvegek Nagy viszkozitású olvadék állapotú anyagok, amelyek nagyon lassan szilárd állapotba mennek át. Folyékony állapotból gyors hűtéssel állíthatók
GEMTT001-B ANYAGTUDOMÁNY ALAPJAI
 GEMTT001-B ANYAGTUDOMÁNY ALAPJAI c. tantárgy követelményei a 2018/19. tanév I. félévében Gépészmérnöki és Informatikai Kar, Gépészmérnöki Szak, BSc képzés Tantárgy órakimérete: 2 ea + 2 gy Félév elismerésének,
GEMTT001-B ANYAGTUDOMÁNY ALAPJAI c. tantárgy követelményei a 2018/19. tanév I. félévében Gépészmérnöki és Informatikai Kar, Gépészmérnöki Szak, BSc képzés Tantárgy órakimérete: 2 ea + 2 gy Félév elismerésének,
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV.
 TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
BUDAPESTI MŰSZAKI FŐISKOLA
 Fémtan Segédlet az Anyagszerkezettan I című tárgyhoz 1/35 Tartalomjegyzék 1. A fémek általános jellemzői... 3 1.1. Kristályos szerkezetek... 3 1.2. Halmazállapot változások fémeknél... 5 2. Az alakváltozás
Fémtan Segédlet az Anyagszerkezettan I című tárgyhoz 1/35 Tartalomjegyzék 1. A fémek általános jellemzői... 3 1.1. Kristályos szerkezetek... 3 1.2. Halmazállapot változások fémeknél... 5 2. Az alakváltozás
1. SI mértékegységrendszer
 I. ALAPFOGALMAK 1. SI mértékegységrendszer Alapegységek 1 Hosszúság (l): méter (m) 2 Tömeg (m): kilogramm (kg) 3 Idő (t): másodperc (s) 4 Áramerősség (I): amper (A) 5 Hőmérséklet (T): kelvin (K) 6 Anyagmennyiség
I. ALAPFOGALMAK 1. SI mértékegységrendszer Alapegységek 1 Hosszúság (l): méter (m) 2 Tömeg (m): kilogramm (kg) 3 Idő (t): másodperc (s) 4 Áramerősség (I): amper (A) 5 Hőmérséklet (T): kelvin (K) 6 Anyagmennyiség
Reaktortechnika. Anyagismeret
 Reaktortechnika Anyagismeret Bevezetés Atomerımővek bonyolult mérnöki létesítmények a berendezések és azok anyagai igen nehéz, esetenként szélsıséges feltételek között (nagy nyomás és hımérséklet, erıs
Reaktortechnika Anyagismeret Bevezetés Atomerımővek bonyolult mérnöki létesítmények a berendezések és azok anyagai igen nehéz, esetenként szélsıséges feltételek között (nagy nyomás és hımérséklet, erıs
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését!
 I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
Diffúzió. Diffúzió. Diffúzió. Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
 Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Fogászati anyagok fajtái. Fogorvosi anyagtan fizikai alapjai 4. Általános anyagszerkezeti ismeretek Anyagcsaládok: fémek és kerámiák KERÁMIÁK FÉMEK
 Fogászati anyagok fajtái Fémes kötés FÉMEK KERÁMIÁK Fémes és nemfémes elemek vegyületei. Fogorvosi anyagtan fizikai alapjai 4. Általános anyagszerkezeti ismeretek Anyagcsaládok: fémek és kerámiák ankönyv
Fogászati anyagok fajtái Fémes kötés FÉMEK KERÁMIÁK Fémes és nemfémes elemek vegyületei. Fogorvosi anyagtan fizikai alapjai 4. Általános anyagszerkezeti ismeretek Anyagcsaládok: fémek és kerámiák ankönyv
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
Diffúzió. Diffúzió sebessége: gáz > folyadék > szilárd (kötőerő)
 Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Az elektronpályák feltöltődési sorrendje
 3. előadás 12-09-17 2 12-09-17 Az elektronpályák feltöltődési sorrendje 3 Az elemek rendszerezése, a periódusos rendszer Elsőként Dimitrij Ivanovics Mengyelejev és Lothar Meyer vette észre az elemek halmazában
3. előadás 12-09-17 2 12-09-17 Az elektronpályák feltöltődési sorrendje 3 Az elemek rendszerezése, a periódusos rendszer Elsőként Dimitrij Ivanovics Mengyelejev és Lothar Meyer vette észre az elemek halmazában
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Reális kristályok, kristályhibák
 Reális kristályok, kristályhibák Gyakorlati fémek szilárdsága kevesebb, mint 1 %-a az ideális modell alapján számítható szilárdságnak Tiszta Si villamos vezetőképességét 10-8 tömegszázalék bór adalékolása
Reális kristályok, kristályhibák Gyakorlati fémek szilárdsága kevesebb, mint 1 %-a az ideális modell alapján számítható szilárdságnak Tiszta Si villamos vezetőképességét 10-8 tömegszázalék bór adalékolása
Kristályos szilárd anyagok
 Általános és szervetlen kémia 4. hét Elızı héten elsajátítottuk, hogy a kovalens kötés hogyan jön létre, milyen elméletekkel lehet leírni milyen a molekulák alakja melyek a másodlagos kötések Mai témakörök
Általános és szervetlen kémia 4. hét Elızı héten elsajátítottuk, hogy a kovalens kötés hogyan jön létre, milyen elméletekkel lehet leírni milyen a molekulák alakja melyek a másodlagos kötések Mai témakörök
Mérnöki anyagismeret. Szerkezeti anyagok
 Mérnöki anyagismeret Szerkezeti anyagok 1 Szerkezeti anyagok Fémek Vas, acél, réz és ötvözetei, könnyűfémek és ötvözeteik Műanyagok Hőre lágyuló és hőre keményedő műanyagok, elasztomerek Kerámiák Kristályos,
Mérnöki anyagismeret Szerkezeti anyagok 1 Szerkezeti anyagok Fémek Vas, acél, réz és ötvözetei, könnyűfémek és ötvözeteik Műanyagok Hőre lágyuló és hőre keményedő műanyagok, elasztomerek Kerámiák Kristályos,
ELLENŐRZŐ KÉRDÉSEK. Anyagtudomány c. tantárgyból a 2009/10. tanév I. félévében Gépészmérnöki és Informatikai Kar, Gépészmérnöki Szak, BSc képzés
 ELLENŐRZŐ KÉRDÉSEK Anyagtudomány c. tantárgyból a 2009/10. tanév I. félévében Gépészmérnöki és Informatikai Kar, Gépészmérnöki Szak, BSc képzés 1. Sorolja fel a szilárd halmazállapotú kristályos anyagokban
ELLENŐRZŐ KÉRDÉSEK Anyagtudomány c. tantárgyból a 2009/10. tanév I. félévében Gépészmérnöki és Informatikai Kar, Gépészmérnöki Szak, BSc képzés 1. Sorolja fel a szilárd halmazállapotú kristályos anyagokban
ÖNTÖTTVASAK HEGESZTÉSE
 Budapesti Műszaki és Gazdaságtudományi Egyetem ÖNTÖTTVASAK HEGESZTÉSE Dr. Palotás Béla Mechanikai Technológia és Anyagszerkezettani Tanszék Öntöttvasak??? Hipoeutektikus öntöttvasak Hipereutektikus öv.-k
Budapesti Műszaki és Gazdaságtudományi Egyetem ÖNTÖTTVASAK HEGESZTÉSE Dr. Palotás Béla Mechanikai Technológia és Anyagszerkezettani Tanszék Öntöttvasak??? Hipoeutektikus öntöttvasak Hipereutektikus öv.-k
KÉRDÉSEK - MŰSZAKI (TECHNIKAI) ANYAGOK-TKK-2016
 KÉRDÉSEK - MŰSZAKI (TECHNIKAI) ANYAGOK-TKK-2016 1. A szén tartalmának növelésével növekszik (keretezd be a pontos válaszokat): 2 a) a szívósság b) keménység c) hegeszthetőség d) szilárdság e) plasztikusság
KÉRDÉSEK - MŰSZAKI (TECHNIKAI) ANYAGOK-TKK-2016 1. A szén tartalmának növelésével növekszik (keretezd be a pontos válaszokat): 2 a) a szívósság b) keménység c) hegeszthetőség d) szilárdság e) plasztikusság
Acélok és öntöttvasak definíciója
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája ACÉLOK ÉS ALKALMAZÁSUK Dr. Palotás Béla palotasb@eik.bme.hu Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája ACÉLOK ÉS ALKALMAZÁSUK Dr. Palotás Béla palotasb@eik.bme.hu Acélok és öntöttvasak definíciója A 2 A 4 Hipereutektoidos acélok A 3 A cm A 1 Hipoeutektikus
Anyagtudomány. Kristálytani alapismeretek
 Anyagtudomány Kristálytani alapismeretek 1 Szilárd szerkezeti formák szilárd anyagok megjelenési formái: amorf: nincs szabályos kristályszerkezet, megszilárdult folyadékok polikristályos anyagok: szabályos
Anyagtudomány Kristálytani alapismeretek 1 Szilárd szerkezeti formák szilárd anyagok megjelenési formái: amorf: nincs szabályos kristályszerkezet, megszilárdult folyadékok polikristályos anyagok: szabályos
Vezetési jelenségek, vezetőanyagok. Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék:
 nyagtudomány 2014/15 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők fémek ötvözetek elektrolitok
nyagtudomány 2014/15 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők fémek ötvözetek elektrolitok
5. elıadás KRISTÁLYKÉMIAI ALAPOK
 5. elıadás KRISTÁLYKÉMIAI ALAPOK KRISTÁLYKÉMIAI ALAPFOGALMAK Atomok: az anyag legkisebb olyan részei, amelyek még hordozzák a kémiai elem jellegzetességeit. Részei: atommag (mely protonokból és neutronokból
5. elıadás KRISTÁLYKÉMIAI ALAPOK KRISTÁLYKÉMIAI ALAPFOGALMAK Atomok: az anyag legkisebb olyan részei, amelyek még hordozzák a kémiai elem jellegzetességeit. Részei: atommag (mely protonokból és neutronokból
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
Öntöttvasak. Öntöttvasak
 MECHANIKAI TECHNOLÓGIA ÉS ANYAGSZERKEZETTANI TANSZÉK Fémek technológiája Öntöttvasak Dr. Palotás Béla palotasb@eik.bme.hu Öntöttvasak??? Hipoeutektikus öntöttvasak Hipereutektikus öv.-k Öntöttvasak Szerzo:
MECHANIKAI TECHNOLÓGIA ÉS ANYAGSZERKEZETTANI TANSZÉK Fémek technológiája Öntöttvasak Dr. Palotás Béla palotasb@eik.bme.hu Öntöttvasak??? Hipoeutektikus öntöttvasak Hipereutektikus öv.-k Öntöttvasak Szerzo:
Vezetési jelenségek, vezetőanyagok
 Anyagszerkezettan és anyagvizsgálat 2015/16 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők
Anyagszerkezettan és anyagvizsgálat 2015/16 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők
Bevezetés a lézeres anyagmegmunkálásba
 Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 13. A lézeres l anyagmegmunkálás szempontjából l fontos anyagi tulajdonságok Optikai tulajdonságok Mechanikai tulajdonságok
Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 13. A lézeres l anyagmegmunkálás szempontjából l fontos anyagi tulajdonságok Optikai tulajdonságok Mechanikai tulajdonságok
Anyagismeret 2016/17. Diffúzió. Dr. Mészáros István Diffúzió
 Anyagismeret 6/7 Diffúzió Dr. Mészáros István meszaros@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd Diffúzió Diffúzió -
Anyagismeret 6/7 Diffúzió Dr. Mészáros István meszaros@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd Diffúzió Diffúzió -
Fogorvosi anyagtan fizikai alapjai 2.
 Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok Kiemelt témák: Viszkozitás Víz és nyál Kristályok - apatit Polimorfizmus Kristályhibák
Fogorvosi anyagtan fizikai alapjai 2. Általános anyagszerkezeti ismeretek Folyadékok, szilárd anyagok, folyadékkristályok Kiemelt témák: Viszkozitás Víz és nyál Kristályok - apatit Polimorfizmus Kristályhibák
Fogorvosi anyagtan fizikai alapjai 8. Képlékeny viselkedés. Terhelési diagram. Mechanikai tulajdonságok 2. s sz (Pa) Tankönyv fejezetei: 16-17
 rugalmas B mn 1. A rá ható erő következtében megváltozott alakját a hatás megszűntével visszanyerő. Vmihez hozzáütődve róla visszapattanó. merev B mn 1. Nem rugalmas, nem hajlékony . Rugalmasságát,
rugalmas B mn 1. A rá ható erő következtében megváltozott alakját a hatás megszűntével visszanyerő. Vmihez hozzáütődve róla visszapattanó. merev B mn 1. Nem rugalmas, nem hajlékony . Rugalmasságát,
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
AZ ATOMIUM. Ezt a kilencelemű képzeletbeli kockát térben sokszor egymáshoz fűzve kapjuk a kristályrácsot.
 AZ ATOMIUM Az Európai Unió gyökerei hat állam - Belgium, Franciaország, Hollandia, Luxemburg, Nyugat-Németország, Olaszország - által 1951-ben létrehozott Európai Szén- és Acélközösségig és az 1957-ben
AZ ATOMIUM Az Európai Unió gyökerei hat állam - Belgium, Franciaország, Hollandia, Luxemburg, Nyugat-Németország, Olaszország - által 1951-ben létrehozott Európai Szén- és Acélközösségig és az 1957-ben
Fogorvosi anyagtan fizikai alapjai 7. Képlékeny viselkedés. Terhelési diagram. Mechanikai tulajdonságok 2. s sz (Pa) Tankönyv fejezetei: 16-17
 rugalmas B mn 1. A rá ható erő következtében megváltozott alakját a hatás megszűntével visszanyerő. Vmihez hozzáütődve róla visszapattanó. merev B mn 1. Nem rugalmas, nem hajlékony . Rugalmasságát,
rugalmas B mn 1. A rá ható erő következtében megváltozott alakját a hatás megszűntével visszanyerő. Vmihez hozzáütődve róla visszapattanó. merev B mn 1. Nem rugalmas, nem hajlékony . Rugalmasságát,
Fogorvosi anyagtan fizikai alapjai 7.
 Fogorvosi anyagtan fizikai alapjai 7. Mechanikai tulajdonságok 2. Kiemelt témák: Szilárdság, rugalmasság, képlékenység és szívósság összefüggései A képlékeny alakváltozás mechanizmusa kristályokban és
Fogorvosi anyagtan fizikai alapjai 7. Mechanikai tulajdonságok 2. Kiemelt témák: Szilárdság, rugalmasság, képlékenység és szívósság összefüggései A képlékeny alakváltozás mechanizmusa kristályokban és
Fogorvosi anyagtan fizikai alapjai 7. Képlékeny viselkedés. Terhelési diagram. Mechanikai tulajdonságok 2. s sz (Pa) Tankönyv fejezetei: 16-17
 rugalmas B mn 1. A rá ható erő következtében megváltozott alakját a hatás megszűntével visszanyerő. Vmihez hozzáütődve róla visszapattanó. merev B mn 1. Nem rugalmas, nem hajlékony . Rugalmasságát,
rugalmas B mn 1. A rá ható erő következtében megváltozott alakját a hatás megszűntével visszanyerő. Vmihez hozzáütődve róla visszapattanó. merev B mn 1. Nem rugalmas, nem hajlékony . Rugalmasságát,
