Epigenetikai szabályozó mechanizmusok és zavaraik leukémiában
|
|
|
- Jázmin Deákné
- 8 évvel ezelőtt
- Látták:
Átírás
1 Összefoglaló közlemény 99 Epigenetikai szabályozó mechanizmusok és zavaraik leukémiában Gaál Zsuzsanna, Oláh Éva Debreceni Egyetem Orvos- és Egészségtudományi Centrum, Általános Orvostudományi Kar, Gyermekgyógyászati Intézet, Klinikai Genetikai Központ, Debrecen A vizsgálatot finanszírozó pályázatok: A kutatás az Európai Unió és Magyarország támogatásával, az Európai Szociális Alap társfinanszírozásával a TÁMOP A/ azonosító számú Nemzeti Kiválóság Program Hazai hallgatói, illetve kutatói személyi támogatást biztosító rendszer kidolgozása és működtetése konvergencia program című kiemelt projekt keretei között valósult meg. A közlemény az Astellas Pharma Kft. Debreceni Egyetem Orvos- és Egészségtudományi Centrum pályázati támogatásával készült. Az epigenetika a génexpressziót a DNS szekvenciájának megváltozása nélkül szabályozó mechanizmusokkal foglalkozik. Tárgykörébe tartozik a DNS-metiláció, a hisztonmodifikáció és a kis, nem kódoló RNS-ek csoportja. A DNS-metiláció a génexpresszió repressziójához vezet. A hisztonmodifikáció a módosítás típusától és az érintett oldallánctól függően a transzkripció aktivációját és gátlását egyaránt eredményezheti. E szabályozó mechanizmusok zavarai igazoltan szerepet játszanak a leukémia kialakulásában. A leukémia különböző altípusaiban a DNSmetilációs mintázat, a hisztonkód és a mikro-rns expressziós szintek jellegzetes eltéréseit figyelték meg, melyek jelentősége lehetséges klinikai alkalmazásukban rejlik. A terápiás eredmények javításához a prognosztikai klasszifikációs rendszer pontosítása szükséges. Az epigenetikai eltérések segítségével egy adott prognosztikai csoporton belül további alcsoportok elkülönítése válhat lehetségessé. A DNS metilációs mintázatában, a hisztonkódban, illetve a mikro-rns-ek expressziós szintjében bekövetkező változások sok esetben korrelálnak az alkalmazott terápia eredményességével, bizonyos esetekben pedig segítséget nyújthatnak a kemorezisztencia előrejelzésében vagy a kemoterápiát követően a minimális reziduális betegség felismerésében. A kromatin szerkezetét befolyásoló, az epigenetikai módosításokért felelős enzimek potenciális terápiás célpontokként szolgálhatnak. Előzetes eredmények szerint az epigenetikai terápia különböző típusai egymással és a konvencionális kemoterápiával egyaránt sikeresen kombinálhatók lehetnek a jövőben a leukémia terápiájában. Kulcsszavak: epigenetika, leukémia, DNS-metiláció, hisztonmodifikáció, prognózis The term epigenetics includes regulatory mechanisms that influence gene expression without any changes in the sequence of the DNA, namely DNA methylation, histone modification and small, non-coding RNAs. Methylation of the DNA leads to the repression of gene expression, while histone modification can result in both activation and inhibition of the transcription depending on the type and site of modification. These mechanisms are confirmed to have important pathogenetic role during the process of leukemogenesis. In distinct subtypes of leukemia specific alterations of the DNA methylation profile, histone code and typical changes of the microrna expression levels have been observed. The importance of them is inhered in their promising potential clinical applications. In order to achieve further improvement in the therapeutic results of leukemia, prognostic classification has to be further improved. With the help of the epigenetic alterations, subgroups could be differentiated within the known prognostic groups. Changes in the DNA methylation pattern, histone code and microrna expression levels correlate with the success of the treatment in many cases, moreover they could provide help to predict chemoresistance or detect the minimal residual disease following chemotherapy. Enzymes influencing the structure of chromatin form a wide variety of new potential therapeutic targets. Based on preliminary results, sorts of epigenetic therapy may be combined successfully either with each other or with conventional chemotherapeutic drugs in the treatment of leukemia. Gaál Z, Oláh É. Epigenetic regulatory mechanisms and their disorders in leukemia. Hungarian Oncology 58:99 107, 2014 Keywords: epigenetics, leukemia, DNA methylation, histone modification, prognosis Levelezési cím: Prof. Dr. Oláh Éva, 4032 Debrecen, Nagyerdei krt. 98. Tel.: , fax: , eolah@med.unideb.hu Közlésre érkezett: november 20. Elfogadva: január 3.
2 100 Gaál és Oláh BEVEZETÉS Az epigenetika azon mechanizmusokkal foglalkozik, melyek a génexpressziót a DNS szekvenciájának megváltozása nélkül szabályozzák. Ide tartozik a DNS-metiláció, a hiszton modifikáció és a kis, nem kódoló RNS-ek csoportja (1). A nem kódoló RNS-ek közül a mikro-rns-ek és azok malignus hematológiai kórképek kialakulásában betöltött szerepe egy korábban benyújtott közlemény témáját képezi (2), funkciójuk zavarait ezért itt nem tárgyaljuk részletesen. A sejtek tulajdonságait specifikus génexpressziós mintázatok hozzák létre (3), melyek biztosítják a sejtfunkciók zavartalan ellátását. Mindezt a DNS szekvenciájának módosulása és a benne kódolt információ érvényre jutását szabályozó rendszer hibája egyaránt lehetetlenné teheti, hasonlóan ahhoz, ahogyan a kottában szereplő hangjegyek sem elegendőek önmagukban egy zenemű tökéletes megszólalásához, hanem ahhoz számos más tényező (hangszerek, előadóművészek, karmester ) összhangja is nélkülözhetetlen. Az epigenetikai mechanizmusok a jelenleg ismert összes biológiai folyamatot befolyásolják (4). Kisiklásuk következményeit a különböző betegségekben egyre szélesebb körben kutatják. Közülük az egyik legintenzívebben fejlődő terület az onkohematológiai kórképekben előforduló szabályozási zavarok tanulmányozása. A rák kialakulásának többlépcsős folyamata során genetikai és epigenetikai változások együttesen vezetnek a betegség kialakulásához (1). Az epigenetikai szabályozás kisiklása a genetikai változásokhoz hasonlóan a karcinogenezis bármely szakaszában bekövetkezhet (5). A genetikai és epigenetikai mechanizmusok közötti további hasonlóság, hogy a környezeti tényezők mutációt és a génexpresszió szabályozásának zavarát egyaránt kiválthatják. Míg azonban a DNS-metilációs mintázat és a hisztonkód eltérései visszafordíthatók, a genetikai változások jóllehet egy részüket a reparációs mechanizmusok kijavítják jelen tudásunk szerint irreverzibilisek. Ugyanakkor fontos, hogy az epigenetikai eltérések öröklődhetnek, így az egyedet ért környezeti ártalmak hatása következményes mutációk nélkül is generációkon keresztül érvényesülhet. A szekvencia változásai, amennyiben szomatikus sejtekben következnek be, nem örökítődnek át az utódokba. Mára elfogadott nézetté vált, hogy a leukémia patogene zi sé nek a genetikai eltérések mellett a DNS-metilációs A szövegben előforduló rövidítések: ALL: akut limfoid leukémia, AML: akut mieloid leukémia, CLL: krónikus limfoid leukémia, CML: krónikus mieloid leukémia, DNMT: DNSmetiltranszferáz, HAT: hiszton-acetiltranszferáz, HDAC: hisztondeacetiláz, HDM: hiszton-demetiláz, HMT: hiszton-metiltranszferáz mintázat és a hisztonkód megváltozása, valamint a mikro- RNS-expressziós szintek eltérései is elengedhetetlenül fontos elemei (6). Egyre több összefüggést fedeznek fel a betegség típusa és stádiuma, illetve az epigenetikai szabályozási zavarok természete között. Ezek ismerete fontos lehet a differenciáldiagnózisban és a betegség prognosztikai megítélésében, emellett új terápiás célpontokként is szolgálhatnak. A DNS-METILÁCIÓ FOLYAMATA A DNS-metiláció fontos szerepet játszik a szövetspecifikus és differenciációs stádiumnak megfelelő génexpressziós mintázat fenntartásában, az imprinting folyamatában, illetve az X kromoszóma inaktivációja során. Emellett védi a genomot a mobilis és a repetitív elemek reaktivációjával szemben (7). A DNS-metiláció során DNS-metiltranszferáz (DNMT) enzimek a citozin 5-ös pozícióban lévő szénatomjához kapcsolnak metilcsoportot az ún. CpG-szigetekben. A CpGszigetek a gének mintegy felének promoter régiójában megtalálhatók (8). Metilációjuk a génexpresszió gátlását eredményezi, ugyanakkor bizonyos esetekben a transzkripció más okból bekövetkező inaktivációja is előidézheti a CpG-szigetek metilációját (9). Gerincesekben a DNS-metilációt katalizáló enzimeknek két fő családja van (10). A DNMT1 a fenntartó metilációért felelős a replikáció során, a DNMT3A és a DNMT3B pedig a de novo metiláció enzimjei (4). A DNMT3L fehérje a DNMT3A és a DNMT3B enzimek katalitikus aktivitását stimulálja (10). A DNMT2 enzim, bár rendelkezik gyenge DNS-metiltranszferáz-aktivitással, alapvetően trnsmetiltranszferázként funkcionál a sejtekben (11). A különböző szabályozó fehérjék számára a metilált, illetve nem metilált CpG-szigetek felismerését meghatározott szerkezetű domének teszik lehetővé. A CXXC domént tartalmazó fehérjék a nem metilált CpG-szigeteket tartalmazó DNS-szakaszokhoz kötődnek. A metilált CpG-szigetekhez kötődő, ún. MBD domént tartalmazó fehérjék családjának öt tagja van, ezek a MeCP2, MBD1, MBD2, MBD3 és az MBD4 (12, 13). A DNS-metiláció folyamatának reverzibilis voltát a demetiláció lehetősége biztosítja. Demetiláció létrejöhet a szénatomok közötti kötés felszakadásával vagy egy repairhez hasonló mecha nizmus révén, melynek során az 5-metil-cito zin-tar talmú nukleozid citozintartalmúra cserélődik (3). PATOLÓGIÁS VÁLTOZÁSOK A DNS METILÁCIÓS MINTÁZATÁBAN LEUKÉMIÁS MEGBETEGEDÉSBEN A DNS globális hipometilációja volt az első, malignusan elfajult sejtekben leírt epigenetikai eltérés (7). Következménye a genom instabilitása, mobilis elemek reaktivációja Professional Publishing Hungary
3 Epigenetikai szabályozási zavarok leukémiában táblázat. Hisztonacetilációért és -deacetilációért felelős enzimek HAT enzimek HDAC enzimek GNAT család MYST család p300/cbp I-es család IIa család IIb család ELP3, GCN5, HAT1, HPA2, PCAF MOZ, Ybf2/Sas3, Sas2, Tip60, ESA1 p300, CBP HDAC1, HDAC2, HDAC3, HDAC8 HDAC4, HDAC5, HDAC7, HDAC9 HDAC6, HDAC10 III-as család sirtuin -ok SIRT1-7 IV-es család HDAC11 és az imprinting mintázat elvesztése is lehet (8). CLL-ben számos onkogén, például a bcl-2, a ras és a TCL1 promoter hipometiláció általi aktiválódását megfigyelték (6). A globális hipometiláció mellett bizonyos gének, főleg a tumorszuppresszorok promoterének hipermetilációja szintén gyakori eltérés (14). Leukémiákban a p15, limfómákban pedig a p16 fehérje hipermetiláció általi down-regulációja jellegzetes (8). A HIC1 tumorszuppresszor gén a CML krónikus fázisában a betegek 50%-ában, blasztos krízisben pedig a betegek közel 100%-ában hipermetilált (6). Egyéb malignus betegségekhez hasonlóan, leukémiában a DNMT enzimek expressziós szintje a betegség típusára és stádiumára jellemző módon változik meg (6). AML-ben és a CML blasztos krízisében a DNMT1, DNMT3A és a DNMT3B enzimek expressziós szintje egyaránt emelkedett (9, 15). CLL-ben a DNMT3B down-regulációját tapasztalták (16). A MeCP2 és az MBD2 fehérjék expressziós szintjének párhuzamos megnövekedését a B-sejtek fokozott proliferációjával hozták összefüggésbe (16). CLL-ben néhány gén metilációs mintázatának és az immunglobulin nehézlánc mutációs státuszának korrelációját igazolták (6). HISZTONMODIFIKÁCIÓ ÉS A HISZTONKÓD ISMERT ELTÉRÉSEI LEUKÉMIÁBAN A hisztonfehérjéknek két nagy csoportját különböztetjük meg a szintetizálódás jellemző ideje, a kódoló régióik elhelyezkedése és az mrns szerkezete alapján. A replikációfüggő hisztonok expressziója közvetlenül az S-fázis előtt fokozódik, majd a replikációt követően lecsökken. Kódoló régióik klasztereket alkotnak, az mrns 3 végén pedig egy stemloop -nak nevezett struktúrát találunk. A replikációfüggő hisztonok közé az oktamerekben két-két példányban megtalálható H2A, H2B, H3 és H4, valamint a nukleoszómák között elhelyezkedő linker H1 hisztonfehérje tartozik. A másik nagy csoportot a replikációfüggetlen hisztonok képezik, melyek a sejtciklus aktuális fázisától függetlenül, konstitutív módon expresszálódnak. Kódoló génjeik elszórtan helyezkednek el a genomban. Az mrns 3 végén a hagyományos poli-a farokszerkezet található. A replikációfüggetlen csoportba a H3.3, H2AX, H2AZ és a makroh2a hisztonfehérjék tartoznak (1, 17, 18). A sejtek kromatinállományának alapegysége a nukleoszóma, amely egy hiszton oktamerből és a köré csavarodó, átlagosan 147 bázispár hosszúságú kettős szálú DNS-szakaszból épül fel (19). Az oktamereket alkotó hisztonok N-terminális végén elhelyezkedő aminosav változatos kovalens módosítások színteréül szolgál 1, amelyek összességét hisztonkódnak nevezzük (20). A hisztonmodifikációnak a következő típusai ismeretesek: acetiláció, metiláció, foszforiláció, ubikvitináció, szumoiláció, ADP-riboziláció, prolinizomerizáció és biotiniláció (21). Ezek a módosítások a kromatinállomány struktúráját és hozzáférhetőségét szabályozzák, továbbá kötőhelyet jelentenek transzkripciós faktorok és egyéb, hisztonmodifikációt végző enzimek számára (22). Az elmúlt években számos összefüggést fedeztek fel a hisztonmodifikációban szerepet játszó enzimek expressziós szintjének kóros eltérései és a leukémia különböző típusai között (6). Acetiláció Az acetiláció során semlegesítődik a hisztonfehérjék lizin oldalláncainak pozitív töltése. Ennek következtében gyengül a DNS és a hisztonfehérjék közötti elektrosztatikus kapcsolat, ami a transzkripció aktivációjának irányában hat (1). A folyamatot hiszton-acetiltranszferáz (HAT) enzimek katalizálják. Az acetilációval szemben a deacetiláció a transzkripció represszióját eredményezi. A deacetilációért a hiszton-deacetiláz (HDAC) enzimek felelősek (19). A HAT és a HDAC enzimek jellemzően multiprotein komplexek alkotóelemeiként fejtik ki aktivitásukat (7, 20). Mindkét enzimcsaládon belül több alcsoport különíthető el (1. táblázat). 1 A hiszton oldalláncok jelölésében a hisztonfehérje nevét az adott aminosav egybetűs rövidítése és a hisztonfehérjén belüli sorszáma követi. Pl.: H3K4=a H3 hisztonfehérje 4-es pozícióban található lizin oldallánca.
4 102 Gaál és Oláh A HAT enzimek többféle szempont szerint is csoportosíthatóak. Sejten belüli elhelyezkedésük alapján megkülönböztetünk a sejtmagban található, A típusú, illetve a citoplazmában jelen lévő, B típusú enzimeket. Elterjedtebb a fehérjék doménszerkezet szerinti rendszerezése, ami alapján a HAT enzimek a GNAT, MYST és a p300/cbp nevű alcsoportokba oszthatók (7, 23). Az emberben azonosított, összesen tizennyolc HDAC enzim négy csoportba sorolható, melyeket római számokkal jelölünk. Az I-es csoport tagjai ubikviter módon, minden szövetben expresszálódnak. Ide tartozik a HDAC1, 2, 3 és 8. A II-es csoport a IIa (HDAC4, 5, 7, 9) és a IIb (HDAC6, 10) alcsoportokra tagolódik. A csoport tagjaira szövetspecifikus kifejeződés jellemző. A III-as csoportba az ún. sirtuin enzimek (SIRT1-7) tartoznak, melyeknek jellegzetes megoszlását figyelték meg a különböző celluláris kompartmentek között. A IV-es csoportnak mindössze egyetlen tagja ismert, a HDAC11 (6, 24, 25). ALL-ben az egészséges csontvelőmintákhoz viszonyítva emelkedett HDAC2, -3, -6 és -8 szinteket találtak, ezenkívül T-sejtes ALL-ben a HDAC1 és -4, B-sejtes ALL-ben pedig a HDAC5 szintje is magasabbnak bizonyult (6). CLLben a tumorszuppresszor tulajdonságú E-cadherin gén hipoacetiláció miatt bekövetkező funkcióvesztésének jelentőségét igazolták (26). A HDAC3 deléciója vérképző rendszeri őssejtekben hipocelluláris csontvelőhöz és anémiához vezet (27). Metiláció A hisztonfehérjék metilációja végbemehet lizin és arginin oldalláncokon, mely a génexpressziót aktiváló és gátló hatású egyaránt lehet. A lizin oldalláncokon mono-, di- és trimetiláció lehetséges. Arginin oldalláncokon a módosítás mono- és dimetiláció formájában mehet végbe (1, 6). A hiszton-metiltranszferáz (HMT) és a hiszton-demetiláz (HDM) enzimeknek számtalan képviselőjét ismerjük (2. táblázat). Az arginin-metiltranszferázok mellett meg külön böztetjük az ún. SET domént tartalmazó, illetve nem tartalmazó lizin-metiltranszferáz enzimeket. A hisztondemetilációért felelős fehérjék szintén több különböző családba sorolhatók (1, 6, 19, 28 30). Néhány jellegzetes eltérést akut és krónikus leukémiában is megfigyeltek a hiszton oldalláncok metilációs szintjében és a módosításokért felelős enzimek aktivitásában. Primer akut leukémiában a H3K4 oldalláncok mérhetetlenül alacsony, míg a H3K9 oldalláncok szignifikánsan megnövekedett metilációs szintjét észlelték (31). Az EZH2 overexpresszióját B-sejtes ALL-ben a betegség progressziójával hozták összefüggésbe a p21 és PTEN tumorszuppresszor gének inaktivációjában betöltött szerepe miatt (32). Az MLL hiszton-metiltranszferáz aktivitásáért felelős SET domént az MLL fehérje génjének transzlokációja révén képződő fúziós proteinek nem tartalmazzák (33). Az izocitrát-dehidrogenáz enzim mutációja a JHDM1 nevű lizin-demetiláz gátlásához vezet, ami az AML-es betegek 15 30%-ában megfigyelhető (6, 34). Ubikvitináció, szumoiláció, foszforiláció, ADP-riboziláció, prolinizomerizáció, biotiniláció Ubikvitináció során a 76 aminosav hosszúságú ubikvitin fehérje C-terminális része kovalensen kapcsolódik a hiszton fehérjék lizin oldalláncainak ε-aminocsoportjához (19). Egy adott oldallánc ubikvitinációja a génexpresszió aktivációjához és repressziójához is vezethet (19). Erre feltehetően a hisztonmetilációért és az ubikvitinációért felelős enzimek későbbi fejezetben részletezett kölcsönhatása szolgáltat magyarázatot. A SUMO körülbelül 100 aminosav hosszúságú, az ubikvitin hez hasonló fehérje, mely számos hiszton oldallánchoz hozzákapcsolódhat. Az esetek többségében a szumoiláció a transzkripció repressziójához vezet, amit részben HDAC enzimek toborzásán keresztül idéz elő (19, 35). Foszforiláció a hisztonfehérjék szerin, treonin és tirozin oldalláncain lehetséges (19, 33, 36). A transzkripció szabályozásában betöltött szerepéről ellentmondásos eredményeket közöltek. Annyi bizonyos, hogy a hisztonfehérjék oldalláncainak megfelelő foszforiláltsági állapota szükséges a DNS-repair folyamatok zavartalan végbemeneteléhez (20). 2. táblázat. Hisztonmetilációért és -demetilációért felelős enzimek Arginin- metiltranszferáz CARM1, PRMT1, PRMT2, PRMT5, PRMT6 Lizin-metiltranszferáz SET-domént tartalmazó EZH2, G9a, MLL1, SUV39H1 SET-domént nem tartalmazó DOT1L, NSD1 Hiszton-lizin-demetiláz JMD2 család JARID1 család Egyéb JHDM3A/JMJD2A, JMJD2C/GASC1, JMJD2B, JMJD2D, JHDM1, UTX PLU1, RBP2, SMCX, SMCY KDM1A, LSD1, PHF8 Hiszton- arginindemetiláz JMJD6, Pad4 Professional Publishing Hungary
5 Epigenetikai szabályozási zavarok leukémiában 103 Az ADP-riboziláció ismert funkciója a sejtek különböző károsodásokra adott megfelelő válaszának elősegítése. Poli- ADP-ribozilációt követően először rövid időre kompaktabbá válik a kromatinállomány, mely feltehetőleg a sejtek védelmét szolgálja a további károsodásokkal szemben. Ezt a szerkezet fellazulása követi, ami hozzáférhetővé teszi az adott kromatinszakaszt a DNS-repair folyamatok számára (19, 37). Az izomerizáció spontán is végbemenő folyamat. A prolin-izomerázok felgyorsítják az oldalláncok cisz és transz konformációs állapota közötti átmenetet. A hisztonfehérjék biotinilációjában részt vevő enzimek a biotinidáz és a holokarboxiláz-szintetáz (20). A módosítás biológiai jelentősége nem ismert. Poszttranszlációs hisztonmódosítások közötti összefüggések A modifikációs helyek közötti kis távolságok következtében egy-egy oldallánc kovalens módosítása gyakran hatással van más enzimek által katalizált folyamatokra is (20). A hiszton-metiltranszferáz MLL fehérje génje fuzionálhat a HAT-aktivitású CBP és p300 fehérjék génjével, továbbá a nukleoszómákat pozicionáló Swi/Snf komplex valamelyik tagjával is (33). A H3P38 prolin oldallánc bizonyos konformációja meggátolja a H3K36 oldallánc meti lá cióját. A H2BK123 oldallánc ubikvitinációja a H3K4 és a H3K79 oldalláncok metilációjának szükséges feltétele. A hisztonmodi fikációban fontos szerepet játszó ún. PRC komplexek különböző típusai között is leírtak kölcsönhatást. A H3K27 oldallánc PRC2 általi metilációja a PRC1-es komplex toborzásához és a H2A hisztonfehérje következményes ubikvitinációjához vezet (19). Nemcsak különböző, hanem azonos típusú hisz tonmódo sí tások is befolyásolhatják egymás végbemenetelét. Például a H3R2 és H3K4 oldalláncok metilációja egymást kölcsönösen kizárja (38). EPIGENETIKAI SZABÁLYOZÓ MECHANIZMUSOK KÖZÖTTI KÖLCSÖNHATÁSOK A DNS-metiláció, hisztonmodifikáció és a mikro-rns-ek egymást kölcsönösen befolyásoló mechanizmusok, melyek a génexpressziós mintázatot együttesen, közös szabályozó hálózatként határozzák meg (1. ábra). A következőkben e kölcsönhatások közül ismertetünk néhányat. A különböző típusú hisztonmodifikációk közötti összefüggésekről egy korábbi fejezetben számoltunk be, így ezekre itt nem térünk ki. Leukémiában gyakori a tumorszuppresszor tulajdonságú mikro-rns-ek expressziós szintjének lecsökkenése a kódoló régió promoterének hipermetilációja következtében. 1. ábra. Epigenetikai szabályozó mechanizmusok közötti kölcsönhatások Mikro-RNS-ek DNS-metiláció GÉNEXPRESSZIÓ Hisztonmodifikáció A mir-124 down-regulációja a limfoid és mieloid eredetű hematológiai malignus betegségek közös jellemzője (21, 39). Bizonyos hiszton oldalláncok módosítása változásokat idéz elő a DNS metilációs mintázatában (13), emellett ismert a metilált CpG-szigetekhez kötődő fehérjék hisztonmodi fiká cióra kifejtett hatása is (9). A köl csön hatások jelentőségét tükrözi, hogy az EZH2 hiszton-metil transz feráz interakcióját a DNMT enzimek valamennyi típusával leírták (34). Számos, a hisztonmodifikáció és a mikro-rns-ek közötti kapcsolat ismert. Például ALL-ben a mir-22 down-regulációjához a H3K27 oldallánc represszív hatású metilációja jelentősen hozzájárul (40). További érdekesség, hogy a HDAC enzimek és a mikro-rns-ek kölcsönösen befolyásolják egymás szintjét. CLL-ben a HDAC enzimek overexpressziója is elősegíti a tumorszuppresszor tulajdonságú mir-15, mir-16 és mir-29b szintjének lecsökkenését (41). A DNS-metiltranszferáz enzimek és a mikro-rns-ek szintén kölcsönösen befolyásolják egymás kifejeződését. Például a DNMT1 szabályozza a mir-370 expresszióját (11), a mir-152-nek pedig a DNMT1 az egyik targetje (42). EPIGENETIKAI SZABÁLYOZÓ MECHANIZMUSOK ÉS FÚZIÓS ONKOPROTEINEK KÖZÖTTI INTERAKCIÓK Az epigenetikai mechanizmusok közötti számtalan kölcsönhatás mellett a genetikai eltérések is eredményezhetnek változásokat az epigenomban. Bizonyítékok növekvő sora igazolja, hogy a leukémiában transzlokáció révén képződő fúziós fehérjék a betegség kialakulását részben különböző epigenetikai szabályozási zavarok előidézésével okozzák. A PML/RARα fúziós fehérje kromatinremodelláló enzimek toborzása által a DNS metilációs mintázatára és a hisztonkódra egyaránt hatással van, és a target gének
6 104 Gaál és Oláh kife jeződését konstitutív transzkripciós represszorként működve gátolja meg (14, 43). A RARB2 génnek az említett mechanizmussal megvalósuló, PML/RARα általi inak ti vá ciója volt az első bizonyíték genetikai eltérés által előidézett epigenetikai változásra malignusan transzformálódott sejtekben (8). Az AML1/ETO fúziós protein kromatin remo delláló fehérjék toborzásán keresztül járul hozzá a mir-223 szintjének lecsökkenéséhez (44, 45). A H3K79 oldallánc metilációját katalizáló DOT1L szerepét a közelmúltban igazolták az MLL/AF9 transzlokációval járó leukémia iniciációjában és progressziójában (46). A TEL/ AML1 fúziós protein közvetve a hisztondeacetilációra és a hisztonmetilációra is hatást gyakorol (33). Az E2A/PBX1 fúziós fehérje direkt interakciója a p300/cbp nevű HATcsalád tagjaival a fúziós fehérje onkogén hatását erősíti (47). A CML-ben képződő BCR/ABL fúziós fehérje transzaktiváció révén megnöveli a mir klaszter expressziós szintjét (48). A mikro-rns-ek egy másik típusa, a mir-203 viszont éppen a BCR/ABL kifejeződését szabályozza (44). ÖSSZEFÜGGÉSEK A KEMOTERÁPIA EREDMÉNYESSÉGÉVEL ÉS A BETEGSÉG PROGNÓZISÁVAL A leukémia prognosztikai klasszifikációs rendszerének újabb szempontokkal való bővítése a betegség kimenetelének pontosabb előrejelzésében és a legmegfelelőbb terápia kivá lasz tásában nyújt segítséget. Az epigenetikai eltérések alapján a jelenleg ismert prognosztikai csoportokon belül további alcsoportok különíthetők el, bizonyos esetekben pedig előrejelezhető lehet a kemoterápiás szerekkel szembeni rezisztencia is. Az utóbbi években sikerrel azonosítottak a genetikai eltérésekkel korreláló DNS-metilációs mintázatokat. A t(8;21), inv(16), illetve t(15;17) szerkezeti eltérésekkel társuló AML-ben specifikus DNS-metilációs profilokat mutattak ki, az NPM1 gén mutációját hordozó csoport tagjait pedig az eltérő metilációs mintázatok alapján négy külön alcsoportba sorolták (49, 50). Mielodiszpláziás szindrómában és szekunder AML-ben a DNMT3A enzim mutációja, ALLben a CALC1 gén promoterének hipermetilációja a betegség kedvezőtlen kimenetelével társul (6, 34). Bizonyos gének hiper meti lá ciójának kimutatása segítheti a minimális reziduális betegség felismerését az akut leukémia kemoterápiáját követően (9). A hisztonmodifikációban részt vevő enzimek megváltozott expressziós szintje szintén összefügghet a leukémia prognózisával. CLL-ben a HDAC7 és HDAC10 enzimek szintjének megemelkedése, valamint a HDAC6 és a SIRT3 down-regulációja kedvezőtlen kimenetellel társul (51). A mielo disz pláziás szindrómában szenvedő, EZH2- mutációt hordozó betegek prognózisa rosszabbnak bizonyult a mutációt nem hordozó csoporthoz képest (34). Korrelációt igazoltak bizonyos epigenetikai eltérések és a kemo rezisz tencia között is. Előzetes eredmények szerint a PHF8 hiszton-demetiláz enzim expressziós szintjének növekedése az ATRA-rezisztens sejtek reszen zitizá cióját eredményezi promielocitás leukémiában (29). CML-ben az imatinibrezisztenciát összefüggésbe hozták a proapoptotikus BID és BIM gének promoterének hipermeti lációjával, továbbá a hiszton-metiltranszferáz EZH2 és a deacetiláz aktivitású SIRT enzimek megváltozott expressziós szintjével is (6, 52). A H2AXS139 oldallánc foszfa tidil-inozitol-3-kináz általi foszforilációjának gátlása in vitro kísérletek során a sejtek adriamicinnel szembeni érzékenységének fokozódásához vezetett (53). AZ EPIGENETIKAI TERÁPIA NÉHÁNY LEHETŐSÉGE Az epigenetikai módosításokért felelős enzimeket célzó gyógyszerek terápiás alkalmazását összefoglalóan epi genetikai terápiának nevezzük (7). Legfőbb csoportjait a DNMT, HAT, HDAC, HMT és a HDM enzimek gátlószerei képezik (3. táblázat). Többségüket a mindennapi gyakorlatban még nem alkalmazzák, hatékonyságukat egyre növekvő számú preklinikai és klinikai vizsgálat során tanulmányozzák. 3. táblázat. Az epigenetikai terápia lehetőségei DNMT-inhibitor HAT-inhibitor HDAC-inhibitor HMT-inhibitor HDM-inhibitor 5-azacitidin, 5-aza-2-deoxicitidin, 5,6-dihidro- 5-azacitidin, decitabin, RG108, SGI-1027, zebularin C646 AN-9, belinostat, depsipeptide, entinostat, mocetinostat, nátrium-butirát, nátriumfenilbutirát, panobinostat, pracinostat, SAHA, SelSA, trichostatin A, valproát 3-deazaneplanocin A, AzaAdoMet, BIX-01294, chaetocin, Sinefungin, UNC0224, UNC fenilciklopropilamin, N-oxalilglicin A DNMT-inhibitorok a sejtekben trifoszfáttá alakuló nukleozidanalógok, melyek a replikáció során inkor po rálód nak a DNS-be (7, 34, 54, 55). A biztató előzetes eredmények ellenére fontos szem előtt tartanunk, hogy a genom általános hipometilációja következtében előre nem megjósolható betegségek alakulhatnak ki mellékhatásként (54). Jóval kevesebb HAT-inhibitor molekulát ismerünk. A C646 lehetséges alkalmazásáról az AML1/ETO fúziós protein képződésével társuló leukémiában számoltak be (56). Professional Publishing Hungary
7 Epigenetikai szabályozási zavarok leukémiában 105 A HDAC-inhibitorokat kémiai szerkezetük szerint csoportosítjuk. Megkülönböztetünk rövid szénláncú zsír savakat, észtereket, ciklikus tetrapeptideket és a ben zami dok családjába tartozó molekulákat (1, 6, 7, 57). A pra ci nos tat újonnan azonosított, nagy hatékonyságú HDAC-in hi bitor. AML-ben a JAK2-FLT3-inhibitor pacri tinib bel szinergista terápiás hatást fejt ki a JAK2 és az FLT3 fehérjék szignali zációs útvonala aktivitásának csökkentésén keresztül (58). CLL-ben a hipoacetilált E-cadhe rin gén expressziós szintjének megnövekedését érték el HDAC-inhi bitor alkalmazásával (26). Terápiás dózisban a HDAC-inhibitorok érzékenyebbé teszik a sejteket az ionizáló sugárzás, a topoizomerázok és a ciszplatin hatásával szemben (59). Mellékhatásaik közé tartozik az anémia, a trom bocito pénia és a limfopénia (27). HMT-inhibitorok a 3-deazaneplanocin A, chaetocin és a Sinefungin, HDM-inhibitorokra példa a 2-fenil cik lo propi la min és az N-oxalilglicin (4, 6). Számos vizsgálat eredménye utal arra, hogy a jövőben lehetőség lesz az epigenetikai terápia különböző csoportjaiba tartozó szereket mind egymással, mind konvencionális kemoterápiás gyógyszerekkel kombinációban alkalmazni (7). In vitro kísérletek szerint a HDAC és HMT enzimek egyidejű gátlása sikerrel alkalmazható lehet a leukémia terápiájában (60). Szintén biztató eredményeket értek el a DNMT és HDAC enzimek egyidejű gátlása során promielocitás leukémia (HL-60) sejtvonalon, az inhibitorok all-transzreténsavval történő együttes alkalmazásakor (61). Az epigenetikai terápia a lehetőségek mellett komoly veszélyeket is hordoz, melyeknek egy jelentős része a nem kellő mértékű szelektivitásból adódik. Bekövetkezhet normálisan csendes gének reaktivációja, illetve más gyógyszerekhez hasonlóan ezekkel szemben is kialakulhat rezisztencia (7, 62). A konvencionális gyógyszerekre adott reakciókhoz hasonlóan az itt felsorolt szerek esetében is jelentős egyéni különbségek várhatók ugyanazon betegcsoporton belül is. Ezért feltétlenül szükséges olyan biomarkerek azonosítása, melyek segítségével kiválasztható az epigenetikai terápiával sikeresen kezelhető csoport (49). MEGBESZÉLÉS Az DNS szekvenciájának módosulása és a kódolt információ kifejeződését meghatározó rendszer hibái egyaránt a fiziológiás körülmények között jellemző génexpressziós mintázat megváltozását, végeredményben pedig betegségek kialakulását okozzák. A karcinogenezis régóta ismert etiológiai tényezői mellett (pl. tumorszuppresszor gének és pro to onko gének mutációi, környezeti hatások) mára elfogadott nézetté vált, hogy a malignus betegségek, köztük a leukémia patogenezisének az epigenetikai szabályozó mechaniz mu sok kisiklása is nélkülözhetetlen elemét jelenti. A vérképző rendszeri sejtek megfelelő differenciálódásához a transzkripciós faktorok, mikro-rns-ek és a kroma tin állomány megfelelő hozzáférhetőségéért felelős enzimek összehangolt, zavartalan működése szükséges (43, 63). Leukémiában e tényezők mindegyikének érintettségét igazolták. A gének promoter régiójában található CpG-szigetek metilációja a génexpresszió gátlását eredményezi (54). A hisztonmodifikáció a transzkripciót aktiválhatja vagy gátolhatja, a módosítás természetétől és az érintett oldalláncoktól függően (19). A génexpressziót szabályozó epi genetikai mechanizmusok egymással és a transzlokációk révén képződő fúziós onkoproteinekkel is sokszoros kölcsönhatásban állnak, ami az ismert genetikai eltéréseket is új megvilágításba helyezi. A leukémia különböző altípusaiban a DNS-metilációs mintázat és a hisztonkód jellegzetes eltéréseit figyelték meg (22, 64). Az epigenetikai módosításokért felelős enzimek, illetve a mikro-rns-ek megváltozott expressziós szintje szintén nagyon gyakran fellelhető. Sok esetben azonban további vizsgálatok szükségesek annak tisztázására, hogy egy adott eltérés a betegség patogenezisének pontosan mely szakaszával áll összefüggésben. A leukémia egyes altípusaira jellemző epigenetikai eltérések ismerete új szempontokkal bővítheti a prognosztikai klasszifikációs rendszert, ami a betegség kimenetelének pontosabb előrejelzését segíti elő. A kromatin szerkezetét befolyásoló gyógyszerek a potenciális terápiás lehetőségek újonnan felfedezett, bőséges tárházát képezik (27). Az epigenetikai terápiába vetett reményt növeli, hogy a genetikai változásokkal szemben a DNS-metilációs mintázat és a hisztonkód eltérései reverzibilisek. Emellett a mikro- RNS-ek expressziós szintjének növelése, illetve csökkentése is lehetséges. Az epigenetikai eltérések említett klinikai alkalmazásai hozzájárulhatnak az onkohematológiai kórképekben szenvedő betegek egyre inkább személyre szabott kezelésének megvalósulásához, ezáltal a túlélők számának és életminőségének javulásához. IRODALOM 1. Brait M, Sidransky D. Cancer epigenetics: above and beyond. Toxicol Mech Methods 21: , Gaál Zs, Oláh É. Mikro-RNS-ek és szerepük hematológiai malignus betegségekben. Orv Hetil 153: , Bird A. DNA methylation patterns and epigenetic memory. Genes Dev 16:6 21, Popovic R, Shah MY, Licht JD. Epigenetic therapy of hematological malignancies: where are we now? Ther Adv Hematol 4:81 91, 2013
8 106 Gaál és Oláh 5. Ting AH, McGarvey KM, Baylin SB. The cancer epigenome components and functional correlates. Genes Dev 20: , Florean C, Schnekenburger M, Grandjenette C, et al. Epigenomics of leukemia: from mechanisms to therapeutic applications. Epigenomics 3: , Taby R. Cancer epigenetics. CA Cancer J Clin 60: , Esteller M. Profiling aberrant DNA methylation in hematologic neoplasms: a view from the top of the iceberg. Clin Immunol 109:80 88, Melki JR, Clark SJ. DNA methylation changes in leukemia. Semin Cancer Biol 12: , Suetake I, Shinozaki F, Miyagawa J, et al. DNMT3L stimulates the DNA methylation activity of DNMT3a and DNMT3b through a direct interaction. J Biol Chem 279: , Rouhi A, Mager DL, Humphries K, et al. MiRNAs, epigenetics, and cancer. Mamm Genome 19: , Miremadi A, Oestergaard MZ, Pharoah PD, et al. Cancer genetics of epigenetic genes. Hum Mol Genet 16 Spec No 1:R28 49, Hashimoto H, Vertino PM, Cheng X. Molecular coupling of DNA methylation and histone methylation. Epigenomics 2: , Villa R, De Santis F, Gutierrez A, et al. Epigenetic gene silencing in acute promyelocytic leukemia. Biochem Pharmacol 68: , Mizuno S, Chijiwa T, Okamura T, et al. Expression of DNA methyltransferases DNMT1, 3A and 3B in normal hematopoiesis and in acute and chronic myelogenous leukemia. Blood 97: , Kn H, Bassal S, Tikellis C, et al. Expression analysis of the epigenetic methyltransferases and methyl-cpg binding protein families in the normal B-cell and B-cell chronic lymphocytic leukemia (CLL). Cancer Biol Ther 3: , Singh R, Mortazavi A, Telu KH, et al. Increasing the complexity of chromatin: functionally distinct roles for replication-dependent histone H2A isoforms in cell proliferation and carcinogenesis. Nucleic Acids Res 41: , Morgan BA, Mittman BA, Smith MM. The highly conserved N-terminal domains of histones H3 and H4 are required for normal cell cycle progression. Mol Cell Biol 11: , Herceg Z, Murr R. Mechanisms of histone modifications. In: Handbook of Epigenetics: The New Molecular and Medical Genetics. Academic Press, London-Burlington-San Diego, 2011, pp Munshi A, Shafi G, Aliya N, et al. Histone modifications dictate specific biological readouts. J Genet Genomics 36:75 88, Agirre X, Martínez-Climent JÁ, Odero MD, et al. Epigenetic regulation of mirna genes in acute leukemia. Leukemia 26: , Linggi BE, Brandt SJ, Sun ZW, et al. Translating the histone code into leukemia. J Cell Biochem 96: , Pelletier N, Champagne N, Lim H, et al. Expression, purification, and analysis of MOZ and MORF histone acetyltransferases. Methods 31:24 32, Barneda-Zahonero B, Parra M. Histone deacetylases and cancer. Mol Oncol 6: , Mascarenhas J, Roper N, Chaurasia P, et al. Epigenetic abnormalities in myeloproliferative neoplasms: a target for novel therapeutic strategies. Clin Epigenet 2: , Jordaan G, Liao W, Sharma S. E-cadherin gene re-expression in chronic lymphocytic leukemia cells by HDAC inhibitors. BMC Cancer 13:88. DOI: / , Summers AR, Fischer MA, Stengel KR, et al. HDAC3 is essential for DNA replication in hematopoietic progenitor cells. J Clin Invest 123: , Son HJ, Kim JY, Hahn Y, et al. Negative regulation of JAK2 by H3K9 methyltransferase G9a in leukemia. Mol Cell Biol 32: , Arteaga MF, Mikesch JH, Qiu J, et al. The histone demethylase PHF8 governs retinoic acid response in acute promyelocytic leukemia. Cancer Cell 23: , Harris WJ, Huang X, Lynch JT, et al. The histone demethylase KD- M1A sustains the oncogenic potential of MLL-AF9 leukemia stem cells. Cancer Cell 21: , Zou Y, Ma X, Huang Y, et al. Effect of phenylhexyl isothiocyanate on aberrant histone H3 methylation in primary human acute leukemia. J Hematol Oncol 5:36. DOI: / , Chen J, Li J, Han Q, et al. Enhancer of zeste homolog 2 is overexpressed and contributes to epigenetic inactivation of p21 and phosphatase and tensin homolog in B-cell acute lymphoblastic leukemia. Exp Biol Med 237: , Di Croce L. Chromatin modifying activity of leukaemia associated fusion proteins. Hum Mol Genet 14 Spec No 1:R77 84, Fathi AT, Abdel-Wahab O. Mutations in epigenetic modifiers in myeloid malignancies and the prospect of novel epigenetic-targeted therapy. Adv Hematol 2012: DOI: /2012/469592, Liu HW, Zhang J, Heine GF. et al. Chromatin modification by SUMO- 1 stimulates the promoters of translation machinery genes. Nucleic Acids Res 40: , Dawson MA, Bannister AJ, Göttgens B, et al. JAK2 phosphorylates histone H3Y41 and excludes HP1alpha from chromatin. Nature 461: , Martinez-Zamudio R, Ha HC. Histone ADP-ribosylation facilitates gene transcription by directly remodeling nucleosomes. Mol Cell Biol 32: , Guccione E, Bassi C, Casadio F, et al. Methylation of histone H3R2 by PRMT6 and H3K4 by an MLL complex are mutually exclusive. Nature 449: , Lujambio A, Ropero S, Ballestar E, et al. Genetic unmasking of an epigenetically silenced microrna in human cancer cells. Cancer Res 67: , Li X, Liu J, Zhou R, et al. Gene silencing of MIR22 in acute lymphoblastic leukaemia involves histone modifications independent of promoter DNA methylation. Br J Haematol 148:69 79, Sampath D, Liu C, Vasan K, et al. Histone deacetylases mediate the silencing of mir-15a, mir-16a, and mir-29b in chronic lymphocytic leukemia. Blood 119: , Lopez-Serra P, Esteller M. DNA methylation-associated silencing of tumor-suppressor micrornas in cancer. Oncogene 31: , Nervi C, Fazi F, Grignani F. Oncoproteins, heterochromatin silencing and micrornas. Epigenetics 3:1 4, Zhang H, Chen Y. New insight into the role of mirnas in leukemia. Sci China C Life Sci 52: , Babashah S, Sadeghizadeh M, Tavirani MR, et al. Aberrant micro- RNA expression and its implications in the pathogenesis of leukemias. Cell Onkol 35: , Nguyen AT, Taranova O, He J, et al. DOT1L, the H3K79 methyltransferase, is required for MLL-AF9-mediated leukemogenesis. Blood 117: , Bayly R, Chuen L, Currie RA, et al. E2A-PBX1 interacts directly with the KIX domain of CBP/p300 in the induction of proliferation in primary hematopoietic cells. J Biol Chem 279: , Fabbri M, Croce CM, Calin GA. MicroRNAs in the ontogeny of leukemias and lymphomas. Leuk Lymphoma 50: , McDevitt MA. Clinical applications of epigenetic markers and epigenetic profiling in myeloid malignancies. Semin Oncol 39: , Figueroa ME, Lugthart S, Li Y, et al. DNA methylation signatures identify biologically distinct subtypes in acute myeloid leukemia. Cancer Cell 17:13 27, 2010 Professional Publishing Hungary
9 Epigenetikai szabályozási zavarok leukémiában Van Damme M, Crompot E, Meuleman N, et al. HDAC isoenzyme expression is deregulated in chronic lymphocytic leukemia B-cells and has a complex prognostic significance. Epigenetics 7: , Bozkurt S, Ozkan T, Ozmen F, et al. The roles of epigenetic modifications of proapoptotic BID and BIM genes in imatinib-resistant chronic myeloid leukemia cells. Hematology 18: , Zhou F, Mei H, Wu Q, et al. Expression of histone H2AX phosphorylation and its potential to modulate adriamycin resistance in K562/A02 cell line. J Huazhong Univ Sci Technol Med Sci 31: , Li XQ, Guo YY, De W. DNA methylation and micrornas in cancer. World J Gastroenterol 18: , Jurkowski TP, Meusburger M, Phalke S, et al. Human DNMT2 methylates trna(asp) molecules using a DNA methyltransferase-like catalytic mechanism. RNA 14: , Gao XN, Lin J, Ning QY, et al. A histone acetyltransferase p300 inhibitor C646 induces cell cycle arrest and apoptosis selectively in AML1- ETO-positive AML cells. PLoS One 8:e55481, Desai D, Salli U, Vrana KE, et al. SelSA, selenium analogs of SAHA as potent histone deacetylase inhibitors. Bioorg Med Chem Lett 20: , Novotny-Diermayr V, Hart S, Goh KC, et al. The oral HDAC inhibitor pracinostat (SB939) is efficacious and synergistic with the JAK2 inhibitor pacritinib (SB1518) in preclinical models of AML. Blood Cancer J 2:e69, Bhaskara S, Knutson SK, Jiang G, et al. Hdac3 is essential for the maintenance of chromatin structure and genome stability. Cancer Cell 18: , Tran HT, Kim HN, Lee IK, et al. Improved therapeutic effect against leukemia by a combination of the histone methyltransferase inhibitor chaetocin and the histone deacetylase inhibitor trichostatin A. J Korean Med Sci 28: , Savickiene J, Treigyte G, Borutinskaite VV, et al. Antileukemic activity of combined epigenetic agents, DNMT inhibitors zebularine and RG108 with HDAC inhibitors, against promyelocytic leukemia HL-60 cells. Cell Mol Biol Lett 17: , Hackanson B, Rimmele L, Benkißer M, et al. HDAC6 as a target for antileukemic drugs in acute myeloid leukemia. Leuk Res 36: , Saeed S, Logie C, Francoijs KJ, et al. Chromatin accessibility, p300, and histone acetylation define PML-RARα and AML1-ETO binding sites in acute myeloid leukemia. Blood 120: , Melki JR, Vincent PC, Clark SJ. Concurrent DNA hypermethylation of multiple genes in acute myeloid leukemia. Cancer Res 59: , 2006
Epigenetikai Szabályozás
 Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában
 Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában Czimmerer Zsolt, Csenki-Bakos Zsolt, Urbányi Béla TOX 2017 Tudományos Konferencia 2017.10.12. Bükfürdő A sejtek
Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában Czimmerer Zsolt, Csenki-Bakos Zsolt, Urbányi Béla TOX 2017 Tudományos Konferencia 2017.10.12. Bükfürdő A sejtek
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
DOKTORI ÉRTEKEZÉS TÉZISEI. Az MDR1 gén kromatin szerkezetének tanulmányozása gyógyszerérzékeny és gyógyszerrezisztens humán sejtekben.
 DOKTORI ÉRTEKEZÉS TÉZISEI Az MDR1 gén kromatin szerkezetének tanulmányozása gyógyszerérzékeny és gyógyszerrezisztens humán sejtekben Tóth Mónika Témavezető: Dr. Bálint Éva SZTE TTIK Biológia Doktori Iskola
DOKTORI ÉRTEKEZÉS TÉZISEI Az MDR1 gén kromatin szerkezetének tanulmányozása gyógyszerérzékeny és gyógyszerrezisztens humán sejtekben Tóth Mónika Témavezető: Dr. Bálint Éva SZTE TTIK Biológia Doktori Iskola
Epigenetikai szabályozás
 Epigenetikai szabályozás 1. A Transzkripció epigenetikai szabályozása Dia 1 A kromatin szerkezete A sejtciklus S fázisában egyetlen sejtben kb 4x1 méter hosszúságú DNS található 4x23 darabra vágva (4N
Epigenetikai szabályozás 1. A Transzkripció epigenetikai szabályozása Dia 1 A kromatin szerkezete A sejtciklus S fázisában egyetlen sejtben kb 4x1 méter hosszúságú DNS található 4x23 darabra vágva (4N
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Epigenetikai tényezők jelentősége az immunológiában
 Epigenetikai tényezők jelentősége az immunológiában Falus András Falus András Semmelweis Egyetem GSI Intézet Former concept: ontogeny is a one-way event Waddington, 1940 REPROGRAMING INDUCED PLURIPOTENT
Epigenetikai tényezők jelentősége az immunológiában Falus András Falus András Semmelweis Egyetem GSI Intézet Former concept: ontogeny is a one-way event Waddington, 1940 REPROGRAMING INDUCED PLURIPOTENT
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
Daganatok kialakulásában szerepet játszó molekuláris folyamatok
 Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
TÉMAKÖRÖK. Ősi RNS világ BEVEZETÉS. RNS-ek tradicionális szerepben
 esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban
 mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban Sebestyén A, Márk Á, Nagy N, Hajdu M, Csóka M*, SticzT, Barna G, Nemes K*, Váradi Zs*, KopperL
mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban Sebestyén A, Márk Á, Nagy N, Hajdu M, Csóka M*, SticzT, Barna G, Nemes K*, Váradi Zs*, KopperL
Heveny myeloid leukaemiás betegeink kezelésével szerzett tapasztalataink (2007 2013)
 EREDETI KÖZLEMÉNY Heveny myeloid leukaemiás betegeink kezelésével szerzett tapasztalataink (2007 2013) Selmeczi Anna dr. 1 Udvardy Miklós dr. 1 Illés Árpád dr. 1 Telek Béla dr. 1 Kiss Attila dr. 1 Batár
EREDETI KÖZLEMÉNY Heveny myeloid leukaemiás betegeink kezelésével szerzett tapasztalataink (2007 2013) Selmeczi Anna dr. 1 Udvardy Miklós dr. 1 Illés Árpád dr. 1 Telek Béla dr. 1 Kiss Attila dr. 1 Batár
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A doktori értekezés tézisei. A növényi NRP fehérjék lehetséges szerepe a hiszton defoszforiláció szabályozásában, és a hőstressz válaszban.
 A doktori értekezés tézisei A növényi NRP fehérjék lehetséges szerepe a hiszton defoszforiláció szabályozásában, és a hőstressz válaszban. Bíró Judit Témavezető: Dr. Fehér Attila Magyar Tudományos Akadémia
A doktori értekezés tézisei A növényi NRP fehérjék lehetséges szerepe a hiszton defoszforiláció szabályozásában, és a hőstressz válaszban. Bíró Judit Témavezető: Dr. Fehér Attila Magyar Tudományos Akadémia
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
A genomiális medicina szép új világa
 A genomiális medicina szép új világa HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012 2014 2015. ÁPRILIS 16. Falus András Semmelweis Egyetem Genetikai Sejt és Immunbiológiai Intézet A medicina
A genomiális medicina szép új világa HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012 2014 2015. ÁPRILIS 16. Falus András Semmelweis Egyetem Genetikai Sejt és Immunbiológiai Intézet A medicina
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Terhesség és emlőrák genetikai szempontok. Kosztolányi György PTE Orvosi Genetikai Intézet
 erhesség és emlőrák genetikai szempontok Kosztolányi yörgy PE Orvosi enetikai Intézet Előfordulás 1 emlőrák / 3000 várandós fokozódása várható: öröklődő emlőrák diagnózisa családon belül : I. generáció
erhesség és emlőrák genetikai szempontok Kosztolányi yörgy PE Orvosi enetikai Intézet Előfordulás 1 emlőrák / 3000 várandós fokozódása várható: öröklődő emlőrák diagnózisa családon belül : I. generáció
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
A C1 orf 124/Spartan szerepe a DNS-hiba tolerancia útvonalban
 Ph.D. tézisek A C1 orf 124/Spartan szerepe a DNS-hiba tolerancia útvonalban Írta: Juhász Szilvia Témavezető: Dr. Haracska Lajos Magyar Tudományos Akadémia Szegedi Biológiai Kutatóközpont Genetikai Intézet
Ph.D. tézisek A C1 orf 124/Spartan szerepe a DNS-hiba tolerancia útvonalban Írta: Juhász Szilvia Témavezető: Dr. Haracska Lajos Magyar Tudományos Akadémia Szegedi Biológiai Kutatóközpont Genetikai Intézet
Kappelmayer János. Malignus hematológiai megbetegedések molekuláris háttere. MOLSZE IX. Nagygyűlése. Bük, 2005 szeptember
 Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Orvosi Genomtudomány 2014 Medical Genomics 2014. Április 8 Május 22 8th April 22nd May
 Orvosi Genomtudomány 2014 Medical Genomics 2014 Április 8 Május 22 8th April 22nd May Hét / 1st week (9. kalendariumi het) Takács László / Fehér Zsigmond Magyar kurzus Datum/ido Ápr. 8 Apr. 9 10:00 10:45
Orvosi Genomtudomány 2014 Medical Genomics 2014 Április 8 Május 22 8th April 22nd May Hét / 1st week (9. kalendariumi het) Takács László / Fehér Zsigmond Magyar kurzus Datum/ido Ápr. 8 Apr. 9 10:00 10:45
Epigenetika kihívások az ökotoxikológiában
 Epigenetika kihívások az ökotoxikológiában Bakonyi Gábor és Szabó Borbála Szent István Egyetem, Gödöllő Állattani és Állatökológiai Tanszék V. ÖKOTOXIKOLÓGIAI KONFERENCIA, MAGYAR ÖKOTOXIKOLÓGIAI TÁRSASÁG,
Epigenetika kihívások az ökotoxikológiában Bakonyi Gábor és Szabó Borbála Szent István Egyetem, Gödöllő Állattani és Állatökológiai Tanszék V. ÖKOTOXIKOLÓGIAI KONFERENCIA, MAGYAR ÖKOTOXIKOLÓGIAI TÁRSASÁG,
SOLiD Technology. library preparation & Sequencing Chemistry (sequencing by ligation!) Imaging and analysis. Application specific sample preparation
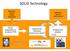 SOLiD Technology Application specific sample preparation Application specific data analysis library preparation & emulsion PCR Sequencing Chemistry (sequencing by ligation!) Imaging and analysis SOLiD
SOLiD Technology Application specific sample preparation Application specific data analysis library preparation & emulsion PCR Sequencing Chemistry (sequencing by ligation!) Imaging and analysis SOLiD
Az ADA2b adaptor fehérjéket tartalmazó hiszton acetiltranszferáz komplexek szerepének vizsgálata Drosophila melanogaster-ben
 Az ADA2b adaptor fehérjéket tartalmazó hiszton acetiltranszferáz komplexek szerepének vizsgálata Drosophila melanogaster-ben DOKTORI TÉZIS Pankotai Tibor Témavezető: Dr. Boros Imre Miklós Szeged, 2007
Az ADA2b adaptor fehérjéket tartalmazó hiszton acetiltranszferáz komplexek szerepének vizsgálata Drosophila melanogaster-ben DOKTORI TÉZIS Pankotai Tibor Témavezető: Dr. Boros Imre Miklós Szeged, 2007
Fehérje expressziós rendszerek. Gyógyszerészi Biotechnológia
 Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere
 I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Epigenetikai plaszticitás és az immunválasz
 Epigenetikai plaszticitás és az immunválasz Falus András Falus András Semmelweis Egyetem GSI Intézet Genome-wide association studies (GWAS) 2017 márciusáig 1980 SNP-t (genetikai variációt) tártak fel,
Epigenetikai plaszticitás és az immunválasz Falus András Falus András Semmelweis Egyetem GSI Intézet Genome-wide association studies (GWAS) 2017 márciusáig 1980 SNP-t (genetikai variációt) tártak fel,
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
Spondylitis ankylopoeticahoz társuló osteoporosis
 Spondylitis ankylopoeticahoz társuló osteoporosis Szántó Sándor DE OEC, Reumatológiai Tanszék 2013.11.05. Szeminárium Csontfelszivódás és csontképzés SPA-ban egészséges előrehaladott SPA Spondylitis ankylopoetica
Spondylitis ankylopoeticahoz társuló osteoporosis Szántó Sándor DE OEC, Reumatológiai Tanszék 2013.11.05. Szeminárium Csontfelszivódás és csontképzés SPA-ban egészséges előrehaladott SPA Spondylitis ankylopoetica
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Mutagenezis és s Karcinogenezis kutatócsoport. Haracska Lajos.
 Mutagenezis és s Karcinogenezis kutatócsoport SZBK Genetikai Intézete (429 dolgozó,, Tel: 62-599666) haracska@brc.hu Haracska Lajos www.brc.hu/lajoslab Evolúci ció és s karcinogenezis: közös k s gyökerek
Mutagenezis és s Karcinogenezis kutatócsoport SZBK Genetikai Intézete (429 dolgozó,, Tel: 62-599666) haracska@brc.hu Haracska Lajos www.brc.hu/lajoslab Evolúci ció és s karcinogenezis: közös k s gyökerek
A PET szerepe a gyógyszerfejlesztésben. Berecz Roland DE KK Pszichiátriai Tanszék
 A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
RNS-ek. 1. Az ősi RNS Világ: - az élet hajnalán. 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek
 RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
3. Főbb Jelutak. 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3.
 Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Vérszérum anyagcseretermékek jellemzése kezelés alatt lévő tüdőrákos betegekben
 http://link.springer.com/article/10.1007/s11306-016-0961-5 - Nyitott - Ingyenes Vérszérum anyagcseretermékek jellemzése kezelés alatt lévő tüdőrákos betegekben http://link.springer.com/article/10.1007/s11306-016-0961-5
http://link.springer.com/article/10.1007/s11306-016-0961-5 - Nyitott - Ingyenes Vérszérum anyagcseretermékek jellemzése kezelés alatt lévő tüdőrákos betegekben http://link.springer.com/article/10.1007/s11306-016-0961-5
HUMAN IMMUNODEFICIENCY VIRUS (HIV) ÉS AIDS
 HUMAN IMMUNODEFICIENCY VIRUS (HIV) ÉS AIDS Dr. Mohamed Mahdi MD. MPH. Department of Infectology and Pediatric Immunology University of Debrecen 2010 Történelmi tények a HIV-ről 1981: Első megjelenés San
HUMAN IMMUNODEFICIENCY VIRUS (HIV) ÉS AIDS Dr. Mohamed Mahdi MD. MPH. Department of Infectology and Pediatric Immunology University of Debrecen 2010 Történelmi tények a HIV-ről 1981: Első megjelenés San
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Doktori értekezés tézisei
 Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
OTKA ZÁRÓJELENTÉS
 NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Fehérje O-Glikoziláció (O-GlcNAc) szerepe különböző betegségekben, detektálási lehetőségei
 Fehérje O-Glikoziláció (O-GlcNAc) szerepe különböző betegségekben, detektálási lehetőségei Nagy T., Frank D., Miseta A., Kovács GL. Laboratóriumi Medicina Intézet, ÁOK, Pécsi Tudományegyetem, Pécs 2010
Fehérje O-Glikoziláció (O-GlcNAc) szerepe különböző betegségekben, detektálási lehetőségei Nagy T., Frank D., Miseta A., Kovács GL. Laboratóriumi Medicina Intézet, ÁOK, Pécsi Tudományegyetem, Pécs 2010
OTKA ZÁRÓJELENTÉS (F48921)
 OTKA ZÁRÓJELENTÉS (F48921) Salamon Dániel F48921 1. A korábbi munkáinkban leírt, jól karakterizált látens Epstein-Barr vírus (EBV) genomokat hordozó, I. látencia-típusú Rael és Mutu-BL-I-cl-216 Burkitt
OTKA ZÁRÓJELENTÉS (F48921) Salamon Dániel F48921 1. A korábbi munkáinkban leírt, jól karakterizált látens Epstein-Barr vírus (EBV) genomokat hordozó, I. látencia-típusú Rael és Mutu-BL-I-cl-216 Burkitt
Molekuláris biológiai alapok
 Biokémiai és Molekuláris Biológiai Intézet Molekuláris biológiai alapok Sarang Zsolt Dimenziók a biológiában Fehérjék (kb. 50 ezer különböző fehérje a szervezetben 21 féle aminosavból épül fel) Élő szervezetek
Biokémiai és Molekuláris Biológiai Intézet Molekuláris biológiai alapok Sarang Zsolt Dimenziók a biológiában Fehérjék (kb. 50 ezer különböző fehérje a szervezetben 21 féle aminosavból épül fel) Élő szervezetek
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. szeptember 15. 1 1. Azonosítószám:
A krónikus myeloid leukémia kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. szeptember 15. 1 1. Azonosítószám:
A dsaga SPECIFIKUS HISZTON ACETILÁCIÓ GÉNMŰKÖDÉS SZABÁLYOZÁSBAN BETÖLTÖTT FUNKCIÓJÁNAK VIZSGÁLATA. Zsindely Nóra
 Doktori értekezés tézisei A dsaga SPECIFIKUS HISZTON ACETILÁCIÓ GÉNMŰKÖDÉS SZABÁLYOZÁSBAN BETÖLTÖTT FUNKCIÓJÁNAK VIZSGÁLATA Zsindely Nóra Témavezető: Dr. Boros Imre Miklós tanszékvezető egyetemi tanár
Doktori értekezés tézisei A dsaga SPECIFIKUS HISZTON ACETILÁCIÓ GÉNMŰKÖDÉS SZABÁLYOZÁSBAN BETÖLTÖTT FUNKCIÓJÁNAK VIZSGÁLATA Zsindely Nóra Témavezető: Dr. Boros Imre Miklós tanszékvezető egyetemi tanár
B-sejtek szerepe az RA patológiás folyamataiban
 B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata
 Ph.D. ÉRTEKEZÉS TÉZISEI A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata Buzás-Bereczki Orsolya Témavezetők: Dr. Bálint Éva Dr. Boros Imre Miklós Biológia
Ph.D. ÉRTEKEZÉS TÉZISEI A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata Buzás-Bereczki Orsolya Témavezetők: Dr. Bálint Éva Dr. Boros Imre Miklós Biológia
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA. Dr. Győrffy Balázs
 A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
DNS replikáció. DNS RNS Polipeptid Amino terminus. Karboxi terminus. Templát szál
 DNS replikáció DNS RNS Polipeptid Amino terminus Templát szál Karboxi terminus Szuper-csavarodott prokarióta cirkuláris DNS Hisztonok komplexe DNS hisztonokra történő felcsvarodása Hiszton-kötött negatív
DNS replikáció DNS RNS Polipeptid Amino terminus Templát szál Karboxi terminus Szuper-csavarodott prokarióta cirkuláris DNS Hisztonok komplexe DNS hisztonokra történő felcsvarodása Hiszton-kötött negatív
CML: A KEZELÉS MELLÉKHATÁSAI
 CML: A KEZELÉS MELLÉKHATÁSAI 2 MILYEN MELLÉK- HATÁSOK JELENTKEZ- HETNEK? KÖZELMÚLTBAN DIAGNOSZTIZÁLT, CML- ES BETEGKÉNT KEZDETBEN MILYEN MELLÉKHATÁSOKRA SZÁMÍTHATOK? A krónikus mieloid leukémiás (CML-es)
CML: A KEZELÉS MELLÉKHATÁSAI 2 MILYEN MELLÉK- HATÁSOK JELENTKEZ- HETNEK? KÖZELMÚLTBAN DIAGNOSZTIZÁLT, CML- ES BETEGKÉNT KEZDETBEN MILYEN MELLÉKHATÁSOKRA SZÁMÍTHATOK? A krónikus mieloid leukémiás (CML-es)
- Conrad Hal Waddington számára a gének fizikai háttere még ismeretlen volt (Watson-Crick-Franklin 1953), így próbálta leírni a sejt specializációt=>
 1 - Conrad Hal Waddington számára a gének fizikai háttere még ismeretlen volt (Watson-Crick-Franklin 1953), így próbálta leírni a sejt specializációt=> a sejtek sorsa meg van határozva, mint egy üveggolyó,
1 - Conrad Hal Waddington számára a gének fizikai háttere még ismeretlen volt (Watson-Crick-Franklin 1953), így próbálta leírni a sejt specializációt=> a sejtek sorsa meg van határozva, mint egy üveggolyó,
A HLTF koordinált fehérje és DNS átrendezése és aktivitásának összehasonlítása a Bloom szindróma helikáz fehérjével
 A HLTF koordinált fehérje és DNS átrendezése és aktivitásának összehasonlítása a Bloom szindróma helikáz fehérjével Ph.D disszertáció tézisei Yathish Jagadheesh Achar Témavezető: Dr. Haracska Lajos Magyar
A HLTF koordinált fehérje és DNS átrendezése és aktivitásának összehasonlítása a Bloom szindróma helikáz fehérjével Ph.D disszertáció tézisei Yathish Jagadheesh Achar Témavezető: Dr. Haracska Lajos Magyar
Phenotype. Genotype. It is like any other experiment! What is a bioinformatics experiment? Remember the Goal. Infectious Disease Paradigm
 It is like any other experiment! What is a bioinformatics experiment? You need to know your data/input sources You need to understand your methods and their assumptions You need a plan to get from point
It is like any other experiment! What is a bioinformatics experiment? You need to know your data/input sources You need to understand your methods and their assumptions You need a plan to get from point
A Huntington kór patogenezisének vizsgálata Drosophila modell felhasználásával
 Bodai László A Huntington kór patogenezisének vizsgálata Drosophila modell felhasználásával a doktori (PhD) értekezés tézisei Szegedi Tudományegyetem, Természettudományi Kar Biológia Doktori Iskola Témavezető:
Bodai László A Huntington kór patogenezisének vizsgálata Drosophila modell felhasználásával a doktori (PhD) értekezés tézisei Szegedi Tudományegyetem, Természettudományi Kar Biológia Doktori Iskola Témavezető:
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk.
 A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
Biológus MSc. Molekuláris biológiai alapismeretek
 Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
TRANSZGENERÁCIÓS EPIGENEZIS. 2016. 03. 29. Dr. Tóth Sára Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet
 TRANSZGENERÁCIÓS EPIGENEZIS 2016. 03. 29. Dr. Tóth Sára Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet EPIGENETIKA Olyan jelenségekkel foglalkozik, amelyek következtében anélkül nő a genom
TRANSZGENERÁCIÓS EPIGENEZIS 2016. 03. 29. Dr. Tóth Sára Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet EPIGENETIKA Olyan jelenségekkel foglalkozik, amelyek következtében anélkül nő a genom
A disszertációban leírtakkal kapcsolatban észrevételeimet és kérdéseimet a szövegben való előfordulás sorrendjében teszem meg.
 OPPONENSI VÉLEMÉNY Hegedűs Attila: A csonthéjas gyümölcsök antioxidáns hatásában megnyilvánuló genetikai variabilitás jellemzése c. akadémiai doktori értekezéséről Az értekezésben Hegedűs Attila sok éves
OPPONENSI VÉLEMÉNY Hegedűs Attila: A csonthéjas gyümölcsök antioxidáns hatásában megnyilvánuló genetikai variabilitás jellemzése c. akadémiai doktori értekezéséről Az értekezésben Hegedűs Attila sok éves
Miben különbözünk az egértől? Szabályozás a molekuláris biológiában
 Az atomoktól a csillagokig, 2010. október 28., ELTE Fizikai Intézet Miben különbözünk az egértől? Szabályozás a molekuláris biológiában brainmaps.org Homo sapiens (Miroslav Klose) Mus musculus Farkas Illés
Az atomoktól a csillagokig, 2010. október 28., ELTE Fizikai Intézet Miben különbözünk az egértől? Szabályozás a molekuláris biológiában brainmaps.org Homo sapiens (Miroslav Klose) Mus musculus Farkas Illés
Roche Personalised Healthcare Megfelelő kezelést az egyénnek 2009 szeptember 9
 Roche Personalised Healthcare Megfelelő kezelést az egyénnek 2009 szeptember 9 dr Kollár György Elvárás az egészségügytől Több hatékonyabb és biztonságosabb gyógyszer legyen elérhető 80 Kezelésre válaszolók
Roche Personalised Healthcare Megfelelő kezelést az egyénnek 2009 szeptember 9 dr Kollár György Elvárás az egészségügytől Több hatékonyabb és biztonságosabb gyógyszer legyen elérhető 80 Kezelésre válaszolók
A sertések lágyék- és heresérv tünetegyüttesének genetikai háttere
 Nagy Szabolcs 1 Benedek Zsuzsanna 2 Polgár J. Péter 3 Magnus Andersson 4 A sertések lágyék- és heresérv tünetegyüttesének genetikai háttere Genetic background of scrotal and inguinal hernia in swine nagy.szabolcs@georgikon.hu
Nagy Szabolcs 1 Benedek Zsuzsanna 2 Polgár J. Péter 3 Magnus Andersson 4 A sertések lágyék- és heresérv tünetegyüttesének genetikai háttere Genetic background of scrotal and inguinal hernia in swine nagy.szabolcs@georgikon.hu
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Sejtmag, magvacska magmembrán
 Sejtmag, magvacska magmembrán Láng Orsolya Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet Kompartmentalizáció Prokaryóta Cytoplazma Eukaryóta Endomembrán Kromatin Plazma membrán Eredménye
Sejtmag, magvacska magmembrán Láng Orsolya Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet Kompartmentalizáció Prokaryóta Cytoplazma Eukaryóta Endomembrán Kromatin Plazma membrán Eredménye
Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise
 Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise Varga Eszter IV. éves gyógyszerészhallgató DE-GYTK GYÓGYSZERÉSZI KÉMIAI TANSZÉK Témavezető: Dr. Borbás Anikó tanszékvezető, egyetemi
Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise Varga Eszter IV. éves gyógyszerészhallgató DE-GYTK GYÓGYSZERÉSZI KÉMIAI TANSZÉK Témavezető: Dr. Borbás Anikó tanszékvezető, egyetemi
OncotypeDX és más genetikai tesztek emlőrákban és azon túl. Dr. Nagy Zoltán Med Gen-Sol Kft.
 OncotypeDX és más genetikai tesztek emlőrákban és azon túl Dr. Nagy Zoltán Med Gen-Sol Kft. 2 A betegek leggyakoribb kérdései! Kiújul a betegségem?! Kell kemoterápiát kapnom?! A beteg és környezete életét,
OncotypeDX és más genetikai tesztek emlőrákban és azon túl Dr. Nagy Zoltán Med Gen-Sol Kft. 2 A betegek leggyakoribb kérdései! Kiújul a betegségem?! Kell kemoterápiát kapnom?! A beteg és környezete életét,
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei)
 Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A köpenysejtes limfómákról
 A köpenysejtes limfómákról Dr. Schneider Tamás Országos Onkológiai Intézet Lymphoma Centrum Limfóma Világnap 2014. szeptember 15. Limfómám van! Limfómám van! Igen? De milyen típusú? Gyógyítható? Nem gyógyítható?
A köpenysejtes limfómákról Dr. Schneider Tamás Országos Onkológiai Intézet Lymphoma Centrum Limfóma Világnap 2014. szeptember 15. Limfómám van! Limfómám van! Igen? De milyen típusú? Gyógyítható? Nem gyógyítható?
Új terápiás lehetőségek (receptorok) a kardiológiában
 Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Mely humán génvariációk és környezeti faktorok járulnak hozzá az allergiás megbetegedések kialakulásához?
 Mely humán génvariációk és környezeti faktorok járulnak hozzá az allergiás megbetegedések kialakulásához? Falus András Genetikai, Sejt- és Immunbiológiai Intézet Semmelweis Egyetem Antal Péter Hadadi Éva
Mely humán génvariációk és környezeti faktorok járulnak hozzá az allergiás megbetegedések kialakulásához? Falus András Genetikai, Sejt- és Immunbiológiai Intézet Semmelweis Egyetem Antal Péter Hadadi Éva
Biomolekuláris nanotechnológia. Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium
 Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 61 Tudományos következtetések Háttér-információ A ponatinib egy tirozin-kináz inhibitor (TKI), amelyet a natív BCR-ABL, valamint minden mutáns variáns kináz beleértve
IV. melléklet Tudományos következtetések 61 Tudományos következtetések Háttér-információ A ponatinib egy tirozin-kináz inhibitor (TKI), amelyet a natív BCR-ABL, valamint minden mutáns variáns kináz beleértve
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Xenobiotikum transzporterek vizsgálata humán keratinocitákban és bőrben
 DOKTORI (PHD) ÉRTEKEZÉS TÉZISEI Xenobiotikum transzporterek vizsgálata humán keratinocitákban és bőrben Bebes Attila Témavezető: Dr. Széll Márta tudományos tanácsadó Szegedi Tudományegyetem Bőrgyógyászati
DOKTORI (PHD) ÉRTEKEZÉS TÉZISEI Xenobiotikum transzporterek vizsgálata humán keratinocitákban és bőrben Bebes Attila Témavezető: Dr. Széll Márta tudományos tanácsadó Szegedi Tudományegyetem Bőrgyógyászati
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
ALK+ tüdőrák a klinikai gyakorlatban. Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest
 ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
Ismert molekula új lehetőségekkel Butirát a modern baromfitakarmányozásban
 Ismert molekula új lehetőségekkel Butirát a modern baromfitakarmányozásban Dr. Mátis Gábor, PhD SZIE Állatorvos-tudományi Kar Élettani és Biokémiai Tanszék CEPO Konferencia Keszthely, 213. október 18.
Ismert molekula új lehetőségekkel Butirát a modern baromfitakarmányozásban Dr. Mátis Gábor, PhD SZIE Állatorvos-tudományi Kar Élettani és Biokémiai Tanszék CEPO Konferencia Keszthely, 213. október 18.
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
SZEMÉLYRE SZABOTT ORVOSLÁS II.
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 SZEMÉLYRE SZABOTT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 SZEMÉLYRE SZABOTT
Supporting Information
 Supporting Information Cell-free GFP simulations Cell-free simulations of degfp production were consistent with experimental measurements (Fig. S1). Dual emmission GFP was produced under a P70a promoter
Supporting Information Cell-free GFP simulations Cell-free simulations of degfp production were consistent with experimental measurements (Fig. S1). Dual emmission GFP was produced under a P70a promoter
A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban
 BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
(11) Lajstromszám: E 004 705 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000470T2! (19) HU (11) Lajstromszám: E 004 70 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 81479 (22) A bejelentés napja: 0.
!HU00000470T2! (19) HU (11) Lajstromszám: E 004 70 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 81479 (22) A bejelentés napja: 0.
TAF10 fehérjék szerepe Drosophila melanogaster-ben
 TAF10 fehérjék szerepe Drosophila melanogaster-ben Páhi Zoltán Gábor Doktori (Ph.D.) értekezés tézisei Témavezetők: Prof. Dr. Boros Imre Miklós tanszékvezető egyetemi tanár Dr. Pankotai Tibor tudományos
TAF10 fehérjék szerepe Drosophila melanogaster-ben Páhi Zoltán Gábor Doktori (Ph.D.) értekezés tézisei Témavezetők: Prof. Dr. Boros Imre Miklós tanszékvezető egyetemi tanár Dr. Pankotai Tibor tudományos
A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése
 A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése Madas Balázs Gergely XXXIX. Sugárvédelmi Továbbképző Tanfolyam Hajdúszoboszló, Hunguest Hotel Béke 2014.
A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése Madas Balázs Gergely XXXIX. Sugárvédelmi Továbbképző Tanfolyam Hajdúszoboszló, Hunguest Hotel Béke 2014.
SZAKMAI ÖNÉLETRAJZ, PUBLIKÁCIÓK
 SZAKMAI ÖNÉLETRAJZ, PUBLIKÁCIÓK Név: Dr. SIMON ÁGNES Születési hely, idő: Nyíregyháza,1969. november 20. Állampolgárság: magyar Telefon, e-mail: +36-70/369-7408, simonagi70@hotmail.com Iskolák: Középiskola:
SZAKMAI ÖNÉLETRAJZ, PUBLIKÁCIÓK Név: Dr. SIMON ÁGNES Születési hely, idő: Nyíregyháza,1969. november 20. Állampolgárság: magyar Telefon, e-mail: +36-70/369-7408, simonagi70@hotmail.com Iskolák: Középiskola:
