5. ENZIMEK, KOENZIMEK, VITAMINOK
|
|
|
- Dénes Papp
- 8 évvel ezelőtt
- Látták:
Átírás
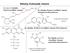
1 5. EZIMEK, KEZIMEK, VITAMIK 5.1. Enzimek Az enzimek általános tulajdonságai Az enzimek a globuláris fehérjék körébe tartoznak. A szervezet folyamataiban fontos szerepet játszanak, mint biokatalizátorok. Feladatuk abban áll, hogy a sejtekben végbemenı biokémiai reakciók a fiziológiai körülmények között megfelelı sebességgel végbemehessenek. A katalitikus folyamat során a peptidláncban egymástól távoli aminosavrészek kerülnek olyan térhelyzetbe, hogy együttesen fejthetik ki hatásukat. A fehérje felületén egy olyan sajátos szerkezeti részlet alakul ki, amelyhez a szubsztrát molekula illeszkedik, és az enzimhez kapcsolódik. Ez a kötıhely. A kötıhely a molekulában lévı ún. katalitikus hellyel együtt, ahol lejátszódhat a katalitikus reakció, az enzim aktív centrumát képezi. A katalitikus helyen azok a funkciós csoportok találhatók, amelyek a szubsztrátum átalakításában közvetlenől részt vesznek. Az enzimek királis molekulák, képesek különbséget tenni enantiotóp csoportok és felületek között, mintegy 96-98%-os sztereoszelektivitással. Az enzimmőködés részletes folyamatát a tripszin és a kimotripszin-a példáján mutatjuk be (5.1. és 5.2. ábra). Mindkét enzim a szerinproteázok csoportjába tartozik. evük onnan ered, hogy egyrészt proteázok, mert polipeptidek, proteinek hidrolízisét katalizálják. Másrészt pedig azért különböztethetık meg a többi proteáztól, mert a katalitikus reakcióban a szerin aminosav oldallánca játszik döntı szerepet. Mindkét enzimben a katalitikus helyen a láncban egyébként távoli három aminosav a három-dimenziós szerkezetben térközeli helyzetbe kerül: az aszparaginsav (Asp-102), a hisztidin (is-57) és a szerin (Ser-195). Alapvetı különbség a két enzim között a kötıdési hely szerkezetében található. A tripszin elınyösen olyan peptidkötést bont, melynek szomszédságában bázikus oldalláncot tartalmazó aminosav, pl. lizin, vagy arginin helyezkedik el. Ekkor a kötıhely és a szubsztrát között oulomb-féle ionos kölcsönhatások alakulnak ki. A kimotripszin-a esetében pedig az enzim felületén olyan zsebszerő képzıdmény keletkezik, mely hidrofób kölcsönhatás révén rögzíti a szubsztrátot: a kimotripszin-a így olyan peptidkötést bont, 101
2 melynek szomszédságában pl. fenilalanin van. Ez illeszkedhet a hidrofób falhoz az enzim felületén. A kötıdési hely szerkezetében található alapvetı különbség határozza meg a szerinproteázok specifikusságát. A két különbözı típusú kötıhely az alábbi ábrán látható: 5.1. Ábra. A tripszin és a kimotripszin-a kötıhelyének részlete. (5.2. ábra). A katalitikus reakció mechanizmusát a kimotripszin-a példáján mutatjuk be A kimotripszin-a hatásmechanizmusa Szerkezete régóta ismert ben artley megállapította az aminosav-sorrendet, a térszerkezetét Blow határozta meg 1967-ben. A kimotripszin-a a hasnyálmirigybıl kristályosan izolálható, mintegy 245 aminosavat tartalmazó fehérjebontó enzim. árom peptidláncból áll, melyeket diszulfán-kötések rögzítenek. Az aktív centrum részét itt is a Ser-195, a is-57 és az Asp-102 aminosavak alkotják. Proteináz és peptidáz (hidroláz) szerepe van: kedvezményezetten olyan helyeken bont, ahol a karboxilcsoport aromás aminosav része: pl. fenilalanin, tirozin. Az enzim felületén a szubsztrát kötıdési helye egyúttal a sztereospecifikusságot is meghatározza. a D-aminosav van jelen ebben a helyzetben, az oldallánc rossz irányban, a zsebbel ellenkezı oldalon helyezkedik el. Ezért 102
3 a szerinproteázok D-aminosavakat nem hidrolizálnak. Észter-kötést is bontanak, észteráz aktivitásuk is van. A peptidkötés hidrolízisének összegzett reakciója a következı: Q + 2 enzim + 2 Q Az egyenletben = az -terminális, Q = a -terminális peptid fragmens. Az aromás oldallánc szerepe, mint említettük, abban rejlik, hogy a kötıhelyen az aromás győrő a kötıhely hidrofób falához kapcsolódik. A folyamatot az 5.2. ábrán mutatjuk be. Az I-es képen a kiindulási állapotot tüntettük fel. A hidrolizálandó peptidkötést tartalmazó fehérje aromás győrőjével már a kötıhelyhez kapcsolódott nem kovalens kötéssel. Az enzim peptidláncában egymástól távol álló, de a térszerkezetben egymáshoz közel került három aminosav, melyeket már említettünk, így kifejtheti katalitikus hatását. A hisztidin imidazol-győrője egy proton-felvétellel és egy proton-vesztéssel járó lépésben vesz részt, és kialakul a II-es képen látható enzim-szubsztrát komplexben a nukleofil szerinoldallánc. Az alkoholát anion a peptid-karbonilcsoport szénatomja ellen intéz nukleofil támadást, melynek eredménye az un. elsı átmeneti állapot, vagy tetrahedrális (tetragonális) átmeneti állapot, amely a III-as képen látható. Ezután a proton a -terminális fragmenshez kapcsolódik, mely a szén-nitrogén kötés hasadása után eltávozik. Az - terminális rész észterkötéssel kapcsolódik az enzimhez és így kialakul a gyakran acilenzim intermediernek nevezett vegyület, melyben a szubsztrátot és az enzimet kovalens kötés köti össze (IV). A szerin tulajdonképpen alkoholízissel bontotta el az amid-kötést. A következı lépésben keletkezik az V acil-enzim-víz komplexnek nevezett struktúra, a hisztidin egy vízmolekulát deprotonál (V), és a keletkezett hidroxidion újabb nukleofil támadással az észter szénatomhoz kötıdik. Ez egy észter-hidrolízis kezdı lépése. Kialakul az un. második átmeneti állapot (VI), melynek stabilizálódása során a második peptidfragmens is szabaddá válik és eltávozik, miközben a proton a hisztidinrıl a szerin hidroxilcsoportjára vándorol. Visszajutunk a VII-es képen bemutatott alapállapothoz: az enzim készen áll a következı amid kötés hasítására. 103
4 I II EZIM EZIM Ser is-57 2 α terminális terminális Ser is-57 2 terminális α terminális Asp -102 Asp -102 III IV EZIM EZIM Ser is-57 2 terminális α terminális Ser is-57 2 terminális α terminális Asp -102 Asp-102 V VI EZIM EZIM Ser is-57 2 α terminális Ser is-57 2 α terminális Asp-102 Asp Ábra. A kimotripszin-a hatásmechanizmusa. 104
5 (az 5.2. ábra folytatása) VII EZIM Ser α terminális is-57 Asp -102 Fontosak a hisztidin reakciói. Ebben az imidazolgyőrő a fiziológiás p-n könnyő protoncserét tesz lehetıvé, mivel konjugált savának a pk a értéke 6,2. Az imidazol erısen polarizálja a szerin hidroxilcsoportját, növeli ennek nukleofilitását. Minthogy a szerin hidroximetil-csoportja rendszerint nem túlságosan reaktív, a hisztidin imidazolgyőrőjének a szerin hidroxilcsoportján a negatív töltés kialakításában alapvetıen döntı szerepe van. Ez a protonátmenet valószínőtlen, azonban az aszparaginsav (Asp-102) negatív töltésével stabilizálni képes a hisztidin heterociklusos győrőjének protonálási folyamatát. Az enzim centrumában végeredményben két egymást követı katalitikus reakció játszódik le: egy bázis-katalizált átészterezés, majd egy bázis-katalizált alkoholízis, melyben bázisként a hisztidin szerepel. A kimotripszin-a reakciómechanizmusa jó példája az enzimek mőködésének. Látható, hogy az aktivált állapotok energetikai stabilizálása és a reaktánsok meghatározott, pontos térhelyzetben történı rögzítése mennyire fontos az aktiválási szabadenergia csökkentésében. Említettük, hogy a kimotripszin-a észterhidrolízist is katalizál. Az alábbi egyszerő példa jól bizonyítja a szerin szerepét. A trimetilecetsav-p-nitrofenil-észterét a kimotripszin A-val reagáltatva, a reakció során az oldatban a p-nitrofenolát anion szabadul fel, mely UV-spetroszkópiával jól követhetı. a ezután a reakcióelegybıl visszanyerjük az enzimet, azt tapasztalhatjuk, hogy 105
6 az elvesztette aktivitását akár amid-, akár észterhidrolízises reakciókra. Így, miután a trimetilacetil molekularész sem szabadult fel, gyanítható, hogy az enzim valamely elsırendő fontosságú funkciós csoportja acilezıdött, megszüntetve az aktivitást. Végül is röntgenvizsgálatokkal derült ki, hogy ez a szerkezeti rész pontosan a szerin-195 hidroxilcsoportja E(nzim) E ( 3 ) Ezt a tényt az a kísérleti tapasztalat is alátámasztotta, hogy az így inaktivált enzimet az erısen nukleofil hidroxilaminnal reagáltatva megkapták a trimetilecetsav hidroxámsavszármazékát, és ugyanakkor az ebben a reakcióban visszanyert enzim újra aktívnak bizonyult. E E + 3 ( 3 ) 3 3 Másik lehetısége az enzim gátlásának a tetrahedrális köztiterméken alapul. Ezt támasztja alá a formilcsoport szerepe a gátlásban. Ez a gátló hatású aldehid polipeptidhez kötött, mégpedig oly módon, hogy a formilcsoport szomszédságában aromás győrő kell, hogy legyen. Az ilyen típusú vegyületek az aldehid-hidrát- ill. acetál képzıdését használják fel a tetrahedrális állapot kialakítására, és így az enzim nem képes a valódi szubsztráttal kapcsolatba kerülni. polipeptid 2 106
7 Ser Az irreverzibilis, kovalensen kötıdı inhibitorok közül a foszfátokat említhetjük meg, melyek tipikusan kompetitív inhibitorok. Ilyenek a diizopropil-fluorofoszfát (DFP) és a szarin (harci gáz), melyek szintén a szerin hidroxilcsoportjához kapcsolódnak és azt blokkolják. Ezek a vegyületek minden olyan enzim inhibitorai, melyek az aktív helyen szerint tartalmaznak. Gátolják a szerin-proteázokat, így az acetilkolin-észterázt is, mely utóbbi idegi ingerület-átvitelben játszik fontos szerepet: az említett foszforvegyületekkel történı bénítása során az inhibíció az életfunkciók gyors összeomlását eredményezi. Felhasználási területük a rovarölık és ideggázok gyártása. F P F P 3 diizopropil-fluorofoszfát (DFP) szarin 5.2. Koenzimek Az enzimek nagy részénél a katalitikus funkciók mőködéséhez egy kisebb, nem fehérje természető molekulára is szükség van. Ez az un. koenzim, mely valamilyen módon kapcsolódik a fehérjéhez (az apoenzimhez) és így alakul ki a mőködésképes holoenzim. A koenzimek egy része nukleotid-származék, más része pedig a további fejezetben szereplı koenzim funkciójú vitamin ikotinsav-amid tartalmú koenzimek ikotinsav-amidot tartalmaz a nikotin-adenin-dinukleotid (AD + ) és 2 -foszfátja, a nikotin-adenin-dinukleotid-foszfát (ADP + ). 107
8 2 4 5' P P 1'' 1' 2' 2 nikotin-adenin-dinukleotid 2 1'' 4 P AD P 5' 2' 1' 2 P nikotin-adenin-dinukleotid-foszfát ADP 5.3. Ábra. A AD + és a ADP + szerkezete. Ezek a vegyületek voltaképpen pszeudonukleotidoknak is nevezhetık, hiszen tartalmaznak DS-ben, S-ben elıforduló bázist, azonban a molekulákban található másik heterociklus nem sorolható a nukleinsav-bázisok körébe. (Az 5.3. ábrán kékkel jelöltük a nikotinamid-részt és pirossal a 2 -foszfát helyettesítıt.) Ezek a koenzimek oxidációs-redukciós folyamatokban vesznek részt, miközben hidrogént vesznek fel ill. adnak le. A redox folyamat végeredményben a piridin-győrőn játszódik le. A nitrogénatom pozitív töltése hatására a 4-es helyrıl elektronvándorlás indul meg a nitrogén irányába. Ennek következtében a 4-es hely felé hidridanion (két elektron és egy proton) intéz nukleofil támadást, mely eredményeképpen az aromás rendszer felbomlik, kinoidális szerkezet alakul ki és a hidrogén a 4-es szénatomhoz kapcsolódik. 108
9 pro e + 2 AD + AD AD + A2 A + AD Ábra. A piridingyőrő szerepe a AD + redukciójában. Ilyen folyamat megy végbe pl. a májban az etil-alkohol acetaldehiddé történı oxidációjakor. Ennek a folyamatnak deutériummal jelzett vegyületek segítségével történt vizsgálata során megállapították, hogy az alkohol pirossal jelzett pro-s hidrogénje vándorol a piridingyőrőre és a folyamat az alábbi reakcióegyenlettel írható fel: AD AD + A AD esetén a 4-es helyzető szénatomhoz kapcsolódó hidrogének nem ekvivalensek, hanem enantiotópok. Ezt példázza a piroszılısav tejsavvá történı redukciója is, mely a glikolízis során megy végbe. Ekkor a karbonil szénatomot mindig a pro- hidrogén támadja. Így az enantiotóp felületet képezı karbonilcsoport szénatomját a tér olyan oldaláról éri a reagens (ebben az esetben a hidrogén) támadása, mely lehetıvé teszi a sztereospecifikus reakció végbemenetelét, vagyis azt, hogy a reakcióban ne racém, hanem L-tejsav képzıdjön. 109
10 3 L 3 enzim 3 is 3 AD pro- Glu 5.5. Ábra. A piroszılısav redukciója tejsavvá. Megemlítjük, hogy ebben a reakcióban a szubsztrátot ionos kölcsönhatások rögzítik a kötıhelyhez az enzim bázikus aminosav-oldalláncai segítségével, és a folyamatban fontos szerep jut a protoncserében szerepet játszó hisztidinnek (is), valamint a glutaminsavnak (Glu) Flavin-adenin-dinukleotid edox-folyamatok koenzimje a flavin-adenin-dinukleotid (FAD): A vegyület csak egy nukleinsav-bázist tartalmaz, ez az adenin, mely ribofuranóz és foszfátrészeken keresztől kapcsolódik az ábrán kékkel jelılt riboflavinhoz, mely a B 2 - vitamin. A másik heterociklusos győrő az izoalloxazin, melynek alapja a pteridinváz. Ez utóbbi pirazin és pirimidin kondenzációjával írható fel az alábbi módon: 110
11 ' 1 2 2' 3' 4' 5' 2 P P B2-vitamin: riboflavin 2 adenozin-difoszfát 1 4 pirazin d 5 3 c b 2 a 1 6 pirimidin pteridin = pirazino[2,3-d]pirimidin alloxazin benzo[g]pteridin-2,4(1,3)-dion izoalloxazin benzo[g]pteridin-2,4(3,9)-dion 5.6. Ábra. A FAD szerkezete. 111
12 Külön figyelmet érdemel a cukorrész, mely a ribóz redukált alakja, a D-ribit(ol), mely a D- vagy L-ribóz redukciójakor keletkezik, optikailag inaktív cukoralkohol: D-ribóz D-ribit(ol) mutatjuk be. A koenzim mőködésének mechanizmusát részletesen a vitaminok tárgyalásánál A Koenzim-A szerkezete Az egyik legismertebb koenzim a koenzim-a (oa) (5.7. ábra). Tartalmaz egy adenin-tartalmú nukleotid részt. Az 1940-es években F. Lipmann izolálta, szintézisére ben került sor (Khorana). A ribofuranozid-győrő a 3 -helyzetben foszforilezve van és az 5 - helyzethez kapcsolódó két foszforsav-csoport köti össze a vitaminként is ismert pantoténsavval, amelyet a béltraktus baktériumai termelnek. A pantoténsav, melyet az ábrán kékkel jelöltünk, két részbıl áll: egy hidroxisavból, mely a D-2,4-dihidroxi- 3,3-dimetilbutánsav, és az aminosavaknál már megismert β-alaninból, mely a 3-aminopropionsav. A pantoténsav β-ala karbonilcsoportjához kéntartalmú amin kapcsolódik: ez a ciszteamin, mely a ciszteinbıl vezethetı le (az ábrán narancssárga színnel jelölve). Fontos szerepe az acilcsoport szállítása, e szerepében legismertebb származéka az acetil-koenzim-a (oa-sac). Ez a vegyület energiagazdag észter, így igen reakcióképes. A tiolésztert a kénatom molekulapályáinak az oxigénétıl eltérı tulajdonságai destabilizálják a csak oxigént tartalmazó észterekhez képest, ezért a tiolészter szabadenergiája a hidrolitikus folyamatokban megnı. 112
13 S pantoténsav 2 ciszteamin P P koenzim-a 3' P P P 3' P 2 S 3 acetil-koenzim-a 5.7. Ábra. A koenzim-a és az acetil-koenzim-a szerkezete Vitaminok A vitaminok általános tulajdonságai lyan szerves molekulák, melyeket a szervezet többnyire nem képes szintetizálni, és amelyekre azonban, ha kis mennyiségben is, de a biológiai folyamatokhoz alapvetıen szükségünk van. Ezek a vegyületek az élethez nélkülözhetetlen, esszenciális anyagok. 113
14 Elégtelen mennyíségük jellegzetes hiánybetegségeket okoz, pl. az elızıekben már megismert -vitamin hiánya skorbutot, a D-vitamin hiánya az angolkórt. A farkasvakság az A-vitamin, különbözı ideggyulladások pedig D-vitaminok hiányára utalhatnak. A fenti problémák elsısorban a régebbi idıkben léptek fel, azonban ma is felelıssé tehetı néhány kórképben a vitaminhiány, pl. a -vitamin hiánya szerepet játszhat a fogínyvérzések kialakulásában. Ezek a panaszok azonban a helyes táplálkozással gyakorlatilag megszüntethetık. a a vitaminhiány részleges, azaz a vitamin bevitele a szervezet igénye alatt marad, hipovitaminózisról beszélünk. Ezek a tünetek megfelelı mennyiségő vitamin szedésével megszüntethetık. A teljes vitaminhiány, az avitaminózis, ma már nagyon ritka. Ez a tünetegyüttes azonban a fontosabb vitaminok teljes bevitele hiányában már irreverzibilis változásokat okozhat a szervezet mőködésében és így végzetes következményekkel járhat. éhány vitamin, pl. az A- és D-vitaminok hatékony formája a szervezetben képzıdik és olyan receptorokon hatnak, melyeken a hormonok. A szervezetbe kerülı, több esetben kiindulási vegyületnek tekinthetı formát, melyet sokszor régebben a már aktív vitaminnak tekintettek, provitaminnak nevezzük. A szervezet a vitamin aktív formáját ezekbıl a vegyületekbıl képes szintetizálni. Ilyen pl. az A-vitamin esetén a β-karotin, vagy a D-vitaminok körében a még nem hidroxilezett, de már győrőfelnyílt struktúrák. Sok esetben a vitaminok a fejlıdésben is fontosak, gondoljunk csak a D 2 - és D 3 - vitaminokra. Egyes vitaminok a szervezet káros anyagai elleni védekezésben játszanak jelentıs szerepet (A-, - és E-vitaminok: un. gyökfogók). Ezek a káros anyagok többek között oxigén felhasználásával képzıdhetnek, ilyenek a hidroxil-, hidroperoxi- és peroxid-gyökök, melyek jelenlétének mutagén (a genetikai kódot megváltoztató), teratogén (magzatkárosító) ill. cancerogén (karcinogén: rákot okozó) hatás tulajdonítható. Ezeket figyelembe véve a vitaminok nemcsak a szervezet normális mőködéséhez szükségesek, hanem azért is, hogy a károsító anyagok hatására aktivizálódó kóros folyamatok ne léphessenek fel, ill. ezek hatását csökkentsék. Ezért hívjuk ezeket az anyagokat preventív (megelızı hatású) szereknek is. 114
15 A vitaminok csoportosítása A vitaminok hagyományosan három nagy csoportba sorolhatók: a) vízoldható vitaminok (pl. a B-vitaminok), b) vízben nem, hanem zsírban oldódó vitaminok (pl. A-, D- E-, K-vitaminok), c) vitaminszerő anyagok (vitogének). A vízoldható vitaminok feleslege többnyire kiürül a vizelettel, azonban a zsíroldható vitaminok túladagolására ügyelni kell, mivel ezek a zsírszövetekben (mint látni fogjuk, szerkezetükbıl adódóan) elıszeretettel felhalmozódnak, és ezért nem ürülnek ki a szervezetbıl, kifejtve a szükségesnél több mennyiségben jelentkezı káros (!) hatásukat. A tipikus túladagolási jelenség a hipervitaminózis, D-vitaminok esetén pl. a kóros meszesedési folyamatok. A vízoldható vitaminok nagyobb része enzimek koenzimjének felépítésében vesz részt és így fejtik ki hatásukat, melyek részletes reakciómechanizmusát a következıkben ismertetni fogjuk. Az alábbiakban összefoglaljuk a vízoldható vitaminok néhány jellegzetes hiánybetegségét, koenzim formáját és legfontosabb biokémiai reakcióit. 1. B 1 -vitamin (tiamin): hiánya beri-berit okoz, koenzimje a tiamin-difoszfát (tiaminpirofoszfát, a továbbiakban: TPP), reakciója: = melletti - kötés létesítése és bontása, 2. B 2 -vitamin (riboflavin): hiánya dermatitiszt, növekedési problémákat okoz, koenzimje a FAD, reakciója: oxidációs-redukciós reakciók, hidrogéngyök és 1 vagy 2 elektrontranszfer, 3. ikotinsavamid (B 3 -vitamin): hiánybetegsége a pellagra (gyomor-bél tünetekkel, bırés nyálkahártya-elváltozással, idegrendszeri tünetekkel járó betegség) és dermatitisz, koenzimje a AD +, reakciója oxidációs-redukciós reakciók, hidridanion-transzfer, 4. Pantoténsav (B 5 -vitamin): hiányakor idegrendszeri problémák léphetnek fel, koenzimje a koenzim-a, reakciója: acetilcsoport szállítása, 5. B 6 -vitamincsoport (piridoxin): hiánya idegrendszeri megbetegedéseket okoz, koenzimje a piridoxál-foszfát, reakciói: transzaminálás, dekarboxilezés, izomerizáció, racemizálás, 115
16 6. liponsav: hiányára növekedési problémák vezethetık vissza, koenzimje a lipoamid, reakciója: oxidáció-redukció, hidrogén és acilcsoport átvitel, 7. Biotin (-vitamin): hiánybetegsége a humán dermatitisz, koenzimje a biotin-karboxilszállító protein, reakciói: karboxilcsoport beépítése és szállítása, 8. Fólsav: hiánya anémiát (vérszegénység) okoz, koenzimje a tetrahidrofólsav, reakciója: egy szén-egység (metil-, hidroximetil-, formil- és metiléncsoport) átvitele, szállítása, 9. B 12 -vitamin: hiánybetegsége a vészes vérszegénység, koenzimjében adenozin kapcsolódik hozzá (ld. ott), reakciói: kötéshasítások ill. átrendezıdések, 10. -vitamin (aszkorbinsav): hiánya a legendás skorbut volt, ma több más káros anyag leküzdésében tulajdonítanak neki szerepet, reakciói: pl. hidroxilezés, gyökfogás Vízben oldható vitaminok B 1 -vitamin A B 1 -vitamint vagy tiamint 1912-ben asimir Funk írta le, mint az élethez nélkülözhetetlen vital amin -t, és B-vitaminnak nevezte. A vegyület neve késıbb lett B 1 - vitamin, amikor több nitrogént tartalmazó vízoldható vitamint is felfedeztek l S B1-vitamin : TIAMI pirimidin tiazol (pka : 2,4) A vitamin két heterociklusos győrőbıl áll: helyettesített pirimidinbıl és tiazolból, melyeket a tiazol nitrogénjén keresztül metiléncsoport köt össze. Tiamin-pirofoszfát koenzim formájában az α-ketosavak (piroszılısav) oxidatív dekarboxilezésében játszik szerepet. 116
17 2 3 tiamin 3 2 l S 2 2 P P ATP AMP koenzim forma : tiamin-pirofoszfát (TPP) Korpában, gabonacsírában, élesztıben és nem utolsósorban a rizs héjában fordul elı. Tartalmazzák a bab, borsó és a kukorica is. Állati szövetekben, így a májban, szívben és vesében is megtalálható. Az erıs fızés roncsolja. api 1-3 mg szükséges a szervezet számára, de ez a mennyiség függ a táplálkozástól: szénhidrát-fogyasztás növeli, zsír-, fehérje- és alkoholfogyasztás csökkenti a szükségletet. Általában idegrendszeri károsodások kezelésére használják. Ilyen a polineuritisz (ideggyulladás), neuralgia (idegi fájdalom), isiász (ülıideg zsába) herpesz zoszter (övsömör), szklerózis multiplex (idegrendszeri kórfolyamat: az idegek velıs hüvelyének elvesztése), ill. alkoholizmus idegrendszeri következményei. iánybetegsége a beri-beri, melynek két változata ismert. A száraz változat tünetei az izomgyengeség, súlycsökkenés és idegrendszeri zavarok, míg a nedves beri-beri esetén ödéma, szívelégtelenség lép fel. Az ismertetett tüneteket végeredményben a piroszılısav felszaporodása okozza. Távol-Keleti betegség, a rizs hántolása okozta, hiszen ott ez a fı energiaforrás. A modern táplálkozás egyik forrása azonban a hántolatlan rizs, melynek fogyasztásával ezek a problémák elkerülhetık. Koenzimje a tiamin-pirofoszfát (TPP), mely a tiamin adenozin-trifoszfáttal (ATP) történı reakciójában keletkezik, eközben az ATP adenozin-monofoszfáttá (AMP) alakul. eakciójában a tiazolgyőrő -2 poziciója játszik döntı szerepet (5.8. ábra). A szomszédos elektronszívó csoport hatására a 2-es helyzető hidrogén protonként lehasad, és az így keletkezett tiamin-pirofoszfát (TPP) karbanion nukleofil támadást intéz a piroszılısav karbonilcsoportjának szénatomja ellen. Lejátszódik a nukleofil addíció, majd egy protonfelvételt követıen dekarboxiláz enzim közremőködésével a vegyület dekarboxilezıdik és kialakul az A közti termék. 117
18 PP PP 3 1 S 2 - S + 3 piroszılısav PP PP PP 3 S + S 3 dekarboxiláz -2 3 A S + PP PP S 3 "aciloil-tiamin" - S + 3 B acil-anion szintézis-ekvivalens S S ( 2 ) 4 liponsav PP 3 S S S -TPP ( 2 ) 4 + S-oA 3 S S ( 2 ) 4 S S + 3 S oa ( 2 ) 4 dihidro-liponsav 5.8. Ábra. A piroszılısav dekarboxilezésének mechanizmusa. Ebbıl protonfelvétellel az un. aciloil-tiamin keletkezik, mely protonleadás után a B acil-anion szintézis-ekvivalenssé alakul (A és B egyébként a mezoméria viszonyában állnak). A B inverz polározottságú acetil-szinton (Umpolung!) ezután, mint nukleofil a 118
19 liponsav kénatomjára támad, a liponsav 1,2-ditiolángyőrője felnyílik és a vegyület a liponsav redukált (felnyílt) formájához kapcsolódik. A liponsav a szervezetben proteinhez kapcsolódik a proteinben található lizin aminosavon keresztül: ez a lipoxin. Errıl a továbbiakban a TPP lehasad, a dihidroliponsavhoz kötött acetilcsoport a oa-ra kerül a dihidrolipoil-transzaciláz enzim segítségével. A reakció eredménye tehát acetil-koenzim-a és dihidroliponsav. Ez utóbbi FAD koenzim és dihidrolipoil-dehidrogenáz enzim közremőködésével visszaalakul liponsavvá és a keletkezett FAD 2 -t a AD + koenzim FAD-dá oxidálja. Így felírhatók ezek a részfolyamatok is: dihidro-liponsav + FAD dihidrolipoildehidrogenáz liponsav + FAD2 FAD2 + AD FAD + AD + A bemutatott reakciók a következıképpen összegezhetık: 3 + S oa + AD liponsav TPP FAD AcS oa + AD A folyamat során a piruvát dehidrogenáz ciklusról van szó: az oxidatív dekarboxilezéskor az energiadús tioészter, az acetil-oa keletkezik ( G = -33,5 kj/mol). A reakció lényege, hogy az umpolung segítségével az acilanion-ekvivalens a liponsav felhasználásával az acetil-oa-t eredményezi. A folyamat jelentısége abban áll, hogy az acetil-koenzim-a, mely a citromsav-ciklus üzemanyaga, összeköti a glükóz- és a zsírsavmetabolizmust, a 2-oxoborostyánkısav (oxálacetát) citromsavvá alakulásához ezúton szolgáltatva az acetil-oa-t. 119
20 GLÜKÓZ ZSISAV-METABLIZMUS PISZİLİSAV AETIL-KEZIM-A 2 S KoA AcS-oA 2 2 oxál-ecetsav 2 2 citroil-koenzim-a citromsav A fenti biokémiai folyamatból a szerves kémia, mint általánosítható umpolung reakciót, a Stetter-reakciót (5.9. ábra) használja 1,4-dikarbonilvegyületek elıállítására. Br S Et3 Br S - Br S Ph Ph Ph Br S + 2 Et Et Ph 5.9. Ábra. A Stetter-reakció. Ez a reakció jól modellezi a tiaminból keletkezı acil-anion szinton reakcióképességét. A negatív polározottságú szénatom α,β-telítetlen észterekre intéz 120
21 nukleofil támadást a β-szénatomon keresztül, és az addíciós reakcióban a karbonilcsoportot páros helyzetben tartalmazó oxoésztereket kapunk B 2 -vitamin A B 2 -vitamin, más néven riboflavin a FAD koenzim része, szerkezetével már ott találkoztunk. övényekben, gombákban fordul elı és a májban is megtalálható. A bélbaktériumok szintetizálják. iánya dermatitiszt, vakságot és idegrendszeri problémákat okozhat. élkülözhetetlen a növekedésben. iányában a nyelv és az ajak duzzadása, súlyos béltünetek, fáradtság, a hemoglobinszint csökkenése is felléphet. Mőködésének alapja: oxidációs és redukciós reakciókban koenzimként funkcionál. A teljes reakció két hidrogénatom (két elektron és két proton) 1,4-addíciója. A reakció a pteridinvázas heterocikluson megy végbe, ahol = a FAD koenzim tárgyalásánál már megismert oldallánc sárga oxidált forma szintelen redukált flavin FAD FAD2 Katalizátora a következı folyamatoknak: 1.) észt vesz a triptofán oxidatív dekarboxilezésében, mely során indol-3-acetamid keletkezik: 2 2 L- (vagy S) triptofán 2 triptofán-oxidáz- -dekarboxiláz 2 2 indol-acetamid 121
22 2.) A xantin húgysavvá történı átalakításában. A húgysav volt az elsı, vizeletbıl izolált purinvázas vegyület, amelynek szerkezetét szintézissel is igazolták xantin-oxigenáz 22 xantin húgysav Másik funkciója az elektrontranszfer reakciók körébe tartozik. Elsı lépésben a 10-es helyzető nitrogénatom protonálódik, és a megfelelı konjugált sav keletkezik. Az így kialakult pozitív töltéső vegyület felírható egy másik mezomer határszerkezettel is. 10 e FAD Ábra. A FAD 2 keletkezése FAD redukciójával. szemikinon Egy elektron felvételével az un. szemikinon intermediert eredményezi. A páratlan elektront tartalmazó gyök egy hidrogénatomot vesz fel ez idáig nem teljesen tisztázott 122
23 folyamatban, és a FAD redukált formája, a FAD 2 a reakciósor végeredménye. A folyamatot az ábrán vázoltuk fel. 3.) A rendszer képes egyelektronos oxidációval a nem hemoglobinhoz kötött vas(ii)-t vas(iii)-má oxidálni: FeII FeIII 4.) észt vesz kétszer egyelektronos redukcióban: az oxigént hidrogén-peroxiddá alakítja. 2 2 e Így oxidáz és dehidrogenáz reakciókban, pl. a AD redukáló ágens és a Fe 3+ egy elektronos oxidáló ágens között intermedierként funkcionál. Ez a szerepe a mitokondriális elektrontranszportban Pantoténsav A koenzim-a alkotórésze. B 5 -vitaminnak is nevezik. Két szerkezeti egységbıl tevıdik össze, egyik az ábrán lilával jelzett β-alanin, mely amidkötéssel kapcsolódik a dihidroxisavhoz. A koenzim-a felépítéséhez szükséges, szabályozza az élesztı növekedését. Bélbaktériumok is termelik. β-ala pantoténsav iánya az élı szervezetekben a növekedés és a szaporodás gátlását idézi elı. Az egészséges szervezet mindenféle sejtjében megtalálható. Gazdag forrása az élesztı, a máj és a tojássárgája, valamint a zöld növényi részek. 123
24 iacinamid A niacinamid vagy B 3 -vitamin tulajdonképpen nikotinamid, a nikotin-adenindinukleotid (AD + ) és 2'-foszfátja a ADP + koenzimek fontos része. A koenzimeknél már tisztáztuk az oxidációs és redukciós reakciókban betöltött szerepét. Sav formája a niacin, vagy nikotinsav. 2 nikotinsavamid : niacinamid nikotinsav : niacin A "vitamin" fogalomtól eltérıen az emberi szervezet képes szintetizálni a triptofánból B 6 -vitamin segítségével. övényekben és állati szervezetekben is széleskörően megtalálható, így a rizskorpában, búzakorpában, élesztıben, májban, húsfélékben, vesében és a halakban (elsısorban a heringben). iánya elsısorban a nagyrészt kukorica alapú táplálékon élıkön mutatkozik. Fáradtság, gyomor-bélrendszeri zavarok, száj- és nyálkahártya gyulladások a tünetek. Fellép a pellagra két formája: érdes bır és fekete elszínezıdések a nyelven és a bırön, a nyelv dagadása, hasmenés, valamint idegrendszeri zavarok is észlelhetık. A tünetek a niacin vagy a niacinamid adagolására elmúlnak. Miután a biológiai rendszerekben a savamid (niacinamid) fordul elı, ezért ezt tekintik vitaminnak annak ellenére, hogy a sav (niacin) amidálása az állati szervezetben könnyen végbemenı folyamat B 6 -vitamincsoport Ebbe a csoportba a következı piridin-származékok tartoznak: Ide sorolható a piridoxál, mely a 4-es helyzetben könnyen karbonsavvá oxidálódható aldehid-csoportot tartalmaz, a piridoxin vagy piridoxol, az elıbbi alkohollá redukált formája, valamint a piridoxamin, amelyben aminometil-csoport a reakciókban résztvevı funkciós csoport. Mindhárom vegyület további fenolos hidroxil- ill. metilcsoport helyettesítıket tartalmaz. 124
25 piridoxál piridoxin vagy piridoxol piridoxamin Koenzimjeként a 3-as helyen lévı hidroximetil-csoport alkoholos hidroxilcsoportjának foszforilezett származéka, a piridoxál-foszfát szerepel. 2 ATP 2 P 3 3 koenzim forma: piridoxál-foszfát övényi magvakban fordul elı. iánybetegsége során, amely ritkán figyelhetı meg, bırelváltozások, vérszegénység, gyengeség, idegrendszeri bántalmak léphetnek fel. A szervezetnek általában kevés B 6 -vitaminra van szüksége, melyet a normális étrend többnyire fedez, azonban bizonyos gyógyszerek szedése növelheti az igényt. Ilyen például a tuberkulózis kezelésére használatos IZIAZID, melynek szerkezete izonikotinsavhidrazid. A vegyület a piridoxál aldehidcsoportjával hidrazont képezve blokkolja a vitamint, mely ebben a formában nem képes a megfelelı biokémiai folyamatokban részt venni. Biokémiai reakciói során az aminosavak metabolizmusában vesz részt. A transzaminálás során oxosavakból aminosavak keletkeznek, a bemutatott példában glutaminsav és oxálecetsav reakciójában α-ketoglutársav és aszparaginsav keletkezik. A folyamatban a glutaminsav az amindonor aminosav, az oxálecetsav pedig az akceptor. A reakcióban a glutamin-aszparagin-transzamináz vagy aminotranszferáz enzim is részt vesz. A glutaminsav (vagy ahogy a biokémia tankönyvekben a fiziológiás körülmények között elıforduló anionos formáját helyesen emlegetik, a glutamát), mint az ammónia-asszimiláció 125
26 terméke kulcsszerepet játszik a transzaminálásban. Legtöbbször, de nem mindig, aminosav/ketosav párként a glutamát/α-oxoglutársav (vagy α-oxoglutarát; α-ketoglutarát) pár az aminotranszferázok szubsztrátja. Ugyanígy szerepel az aszpartát (aszparaginsav anionos formája) ill. az oxálacetát is ebben a rendszerben, valamint az alanin/piruvát (piroszılısav anionos formája) is. Az ezekhez az oxosav/aminosav párokhoz kapcsolódó enzimek fontosak a klinikai diagnosztikában. Ilyenek a humán megbetegedésekben jellemzı mértékő szérum glutamát-oxálacetát transzamináz (SGT) és a szérum glutamát-piruvát transzamináz (SGPT) aktivitások. Ezek az enzimek, melyek nagy mennyiségben megtalálhatók a szív és a máj szöveteiben, a sejtek sérülése esetén, melyeket pl. a miokardiális infarktus ill. a fertızı májgyulladás, esetleg más szerv kóros állapota okoz, felszabadulnak a sejtbıl. Ezen enzimek aktivitásának mérése a vér szérumban felhasználható egyrészt a diagnózis felállításában, másfelıl pedig a beteg kezelés hatására történı reagálásának nyomon követésére is glutamin-aszparagin- -transzamináz glutaminsav (donor aminosav) oxálecetsav (akceptor) α keto-glutársav aszparaginsav A következı katalizált reakció, a dekarboxilezés során aminosavakból aminok, mégpedig un. biogén aminok keletkeznek, melyeknek a szervezet mőködésében igen fontos szerepük van. A glutaminsav ezen az úton alakul át γ-aminovajsavvá a glutamindekarboxiláz enzim közremőködésével, mely aminovegyületet az angol elnevezése (γaminobutyric acid) alapján GABA rövidítéssel használnak. A GABA rendkívül fontos idegi ingerületátvivı anyagként mőködik a szervezetben. Ebbe a folyamatba avatkozik be pl. a gyilkos galóca a mérgezés során. 126
27 2 glutamin-dekarboxiláz (γ-amino-vajsav) GABA Végül példaként megemlítjük az aminosavak izomerizációs ill. racemizációs reakcióit is, melyekben e vitamincsoportnak szintén szerepe van. A reakciók részletes mechanizmusát az ábrán mutatjuk be. A piridoxál Schiff-bázist képez az apoenzim lizin aminosavjának ω-aminocsoportjával, ily módon kötıdve az enzimhez. A lizin helyére az átalakítandó aminosav addíciós-eliminációs reakcióval kerül át, szintén aldimint képezve. Az intermediert stabilizálja a fenolos hidroxilcsoport segítségével kialakult hidrogénhíd kötés. E forma stabilizálásában gyakran fémionok, pl. Al 3+ és u 2+ ionok is szerepet játszanak. Ezután a molekula kétféle köztitermékké alakulhat, attól függıen, hogy milyen folyamatot katalizál az összetett reakcióban résztvevı enzim. A protonálódott nitrogénatom irányába történı elektronáramlás hatására megtörtént dekarboxilezést követı protonfelvétel és az imin kötés hidrolízise a megfelelı biogén aminhoz vezet. Másfelıl a kiindulási aminosav-piridoxál Schiff-bázis protonvesztéssel az ábrán látható kinoidális intermedierré alakulhat át. Ekkor az aminosav α-szénatomja és az α-helyzető nitrogénatom között kettıs kötés jön létre. Ez a planáris szerkezet sztereotóp felületként szerepel a következı protonfelvétel során. A bekapcsolódó proton ugyanis a planáris struktúra két oldaláról közelítheti meg a támadás helyét. Amennyiben az enzimkomplexben van kitüntetett támadási iránya a reagensnek, esetünkben a hidrogénnek, úgy optikailag aktív aminosav keletkezik. a a reakció egyforma valószínőséggel játszódik le a sík mindkét oldala irányából, akkor racemizáció történik. Bár a piridoxál-foszfát ezekben a reakciókban koenzimként mőködik, a reaktív forma mégsem az aldehid, hanem inkább az aldimin struktúra, amely a vitamin és az átalakítandó aminosav között jön létre. a pl. az így keletkezett aldimin szén-nitrogén kettıs kötését (=) nátrium-tetrahidrido-boráttal (ab 4 ) redukáljuk, az irreverzibilis változás következtében (eltőnik a kettıs kötéses planáris felület) a rendszer elveszti aktivitását, és alkalmatlanná válik aminosavak átalakítására. 127
28 apoenzim LIZI 2 P (L) 3 enzim-lys (Ad + E) 2 P, P (dekarboxilezés) (biogén amin) 2 P + α 2 P + 2 (izomerizáció v. racemizáció) (kinoidális intermedier) 2 P + (D)- vagy racém aminosav Ábra. A B 6 -vitamin szerepe aminosavak dekarboxilezésében és izomerizációjában. A vitamin által katalizált reakciókba a transzaminálás is beletartozik. Ekkor a piridoxamin forma játszik fontos szerepet, melyben az aminofunkció adja az oxosavval történı kapcsolódás lehetıségét szintén imin formájában. Végeredményben ez a vitamincsoport mintegy 60 specifikus reakció katalízisében vesz részt. 128
29 Liponsav idrogénezési, dehidrogénezési folyamatok koenzimje. Az apoenzimhez történı kapcsolódása az oldalláncban elhelyezkedı karbonsav funkción keresztül történik lizin aminocsoportjával savamid formájában (lipoxin). Az ábrán az oxidált és a redukált formáját tüntettük fel. S S S S liponsav dihidro-liponsav Az emberi szervezet, eltérıen a többi vitamintól képes szintetizálni. A máj és az élesztı gazdag liponsavban, egyúttal néhány baktérium növekedési faktoraként is ismert. Szerepét az α-ketosavak dekarboxilezésében (acetilcsoport átvitel) már a tiamin tárgyalásakor bemutattuk Biotin A vitamint -vitaminnak is nevezik, biotinként mégis jobban ismert. Fıleg az élesztıben és a májban fordul elı. iánya bırbetegséget okoz, ilyenkor gyulladásos pír lép fel az egész testen (dermatitisz: bırgyulladás), valamint hámlás, szırkihullás és körömsérülések is tapasztalhatók. Innen a -vitamin név. émetül a bır ui. aut. Biciklusos vegyület, telített imidazol és telített tiofén kondenzációjával vezethetı le. A győrőkapcsolat cisz-konfigurációjú, a sztereocentrumok 2S,3S,4-konfigurációjúak. Jobbra forgató, optikailag aktív molekula. 1' 5 4 2' 3 S 1 3' 2 6 (+)-2S,3S,4-biotin
30 5.12. Ábra. A biotin térbeli szerkezete. A biotin a tojásfehérje egyik összetevıjével, az avidin nevő fehérjével komplexet képez, így biológiailag inaktívvá válik: az avidin (mint bázikus protein) tehát erıs antagonistája a biotinnak (amely karboxilcsoportot tartalmaz). Pl. a sok madártejfogyasztás esetén biotinhiány léphet fel. A tojásfehérje leköti a biotint, azonban melegítés hatására, amikor denaturálódás következik be, a vegyület újra szabad állapotba kerül. A biotin a karboxilcsoportja segítségével protein lizin aminosav aminocsoportjához kötıdik peptidkötéssel, így a protein és a biotin proteidet alkot (lipoxin). Biokémiai funkciója karboxilcsoport bevitele ( 2 beépítése), a reakciót a biotinfüggı karboxiláz enzim katalizálja. A reakció mechanizmusa során a biotin molekulán elıször karboxilátcsoport épül az 1'-helyzetbe (5.13. ábra). Ennek forrása a széndioxid felvételével keletkezı hidrokarbonátion, valamint a folyamathoz adenozin-trifoszfát (ATP) is szükséges. A biotin 1'-helyzető nitrogénatom szabad elektronpárja irányából elektronátmenet indul a hidrokarbonát-ion karbonil szénatomja felé. Ebben a lépésben alakul ki a biotin-1-karboxilát, mely diacilaminként viselkedve erıs acilezıszer. 130
Vitaminok meghatározása és csoportosítása
 Vitaminok Vitaminok meghatározása és csoportosítása A vitaminok a(z emberi) szervezet számára nélkülözhetetlen, kis molekulatömegű, változatos összetételű szerves vegyületek, melyeket a táplálékkal kell
Vitaminok Vitaminok meghatározása és csoportosítása A vitaminok a(z emberi) szervezet számára nélkülözhetetlen, kis molekulatömegű, változatos összetételű szerves vegyületek, melyeket a táplálékkal kell
BIOMOLEKULÁK KÉMIÁJA. Novák-Nyitrai-Hazai
 BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
A vitaminok és az élelmiszerek kapcsolatáról
 A vitaminok és az élelmiszerek kapcsolatáról Rengeteg tévinformáció "marketing szöveg" és áltudományos szenzáció található a világhálón a vitaminokról és forrásaikról. Cikkünkben megpróbálunk a tényekre
A vitaminok és az élelmiszerek kapcsolatáról Rengeteg tévinformáció "marketing szöveg" és áltudományos szenzáció található a világhálón a vitaminokról és forrásaikról. Cikkünkben megpróbálunk a tényekre
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Grilla Stúdiója - gyógytorna, szülésfelkészítés
 Az éltetõ vitaminok A vitaminok olyan szerves vegyületek, amelyek feltétlenül szükségesek testünk kifogástalan mûködéséhez. A vitamin elnevezés a vita (élet) és az amin (NH2-tartalmú kémiai gyök) szavakból
Az éltetõ vitaminok A vitaminok olyan szerves vegyületek, amelyek feltétlenül szükségesek testünk kifogástalan mûködéséhez. A vitamin elnevezés a vita (élet) és az amin (NH2-tartalmú kémiai gyök) szavakból
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
P O O O. OAc A O. OAc
 6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Fehérjék. SZTE ÁOK Biokémiai Intézet
 Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
ENZIMSZINTŰ SZABÁLYOZÁS
 ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
A biokémiai folyamatokat enzimek (biokatalizátorok) viszik véghez. Minden enzim. tartalmaz fehérjét. Két csoportjukat különböztetjük meg az enzimeknek
 1 A biokémiai folyamatokat enzimek (biokatalizátorok) viszik véghez. Minden enzim tartalmaz fehérjét. Két csoportjukat különböztetjük meg az enzimeknek a./ Csak fehérjébıl állók b./ Fehérjébıl (apoenzim)
1 A biokémiai folyamatokat enzimek (biokatalizátorok) viszik véghez. Minden enzim tartalmaz fehérjét. Két csoportjukat különböztetjük meg az enzimeknek a./ Csak fehérjébıl állók b./ Fehérjébıl (apoenzim)
Vitaminok leírása, hatásai
 Vitaminok leírása, hatásai A vitaminok két nagyobb csoportra oszthatók, vízben oldódó és zsírban oldódó vitaminokra. &amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp
Vitaminok leírása, hatásai A vitaminok két nagyobb csoportra oszthatók, vízben oldódó és zsírban oldódó vitaminokra. &amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
, mitokondriumban (peroxiszóma) citoplazmában
 -helye: máj, zsírszövet, vese, agy, tüdő, stb. - nem a β-oxidáció megfordítása!!! β-oxidáció Zsírsav-szintézis -------------------------------------------------------------------------------------------
-helye: máj, zsírszövet, vese, agy, tüdő, stb. - nem a β-oxidáció megfordítása!!! β-oxidáció Zsírsav-szintézis -------------------------------------------------------------------------------------------
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
R R C X C X R R X + C H R CH CH R H + BH 2 + Eliminációs reakciók
 Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
Zsírsav szintézis. Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P. 2 i
 Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
6. FONTOSABB DEFINICIÓK
 6. FONTOSABB DEFINICIÓK ACP: acyl carrier protein. Zsírsavak felépítésében résztvevı fehérje, melyre az acilcsoport(ok) rákapcsolódnak. Akirális: olyan molekulák, amelyek fedésbe hozhatók tükörképükkel,
6. FONTOSABB DEFINICIÓK ACP: acyl carrier protein. Zsírsavak felépítésében résztvevı fehérje, melyre az acilcsoport(ok) rákapcsolódnak. Akirális: olyan molekulák, amelyek fedésbe hozhatók tükörképükkel,
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
Általános jellemzés, fogalom Tartós tengeri út Skorbut Hántolt rizs fogyasztása beriberi (1896)
 Vitaminok Általános jellemzés, fogalom Tartós tengeri út Skorbut Hántolt rizs fogyasztása beriberi (1896) Megelőzhetők étrend kiegészítéssel Rizskorpa kivonat megelőzi a beriberit Hatóanyag: aminvegyület
Vitaminok Általános jellemzés, fogalom Tartós tengeri út Skorbut Hántolt rizs fogyasztása beriberi (1896) Megelőzhetők étrend kiegészítéssel Rizskorpa kivonat megelőzi a beriberit Hatóanyag: aminvegyület
A gasztrointesztinális (GI) rendszer élettana IV. Táplálkozás élettan.
 A gasztrointesztinális (GI) rendszer élettana IV. Táplálkozás élettan. A táplálékfelvétel célja: Nyersanyagok biztosítása a test számára a növekedéshez a szöveti regenerációhoz az ivarsejtek képzéséhez
A gasztrointesztinális (GI) rendszer élettana IV. Táplálkozás élettan. A táplálékfelvétel célja: Nyersanyagok biztosítása a test számára a növekedéshez a szöveti regenerációhoz az ivarsejtek képzéséhez
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
Táplálkozás. SZTE ÁOK Biokémiai Intézet
 Táplálkozás Cél Optimális, kiegyensúlyozott táplálkozás - minden szükséges bevitele - káros anyagok bevitelének megakadályozása Cél: egészség, jó életminőség fenntartása vagy visszanyerése Szükséglet és
Táplálkozás Cél Optimális, kiegyensúlyozott táplálkozás - minden szükséges bevitele - káros anyagok bevitelének megakadályozása Cél: egészség, jó életminőség fenntartása vagy visszanyerése Szükséglet és
1. A nitrogén körforgása
 1. A nitrogén körforgása 2. Fehérjék lebontása Táplálékfehérjék lebontása aminosavakká Saját fehérjék lebontása Féléletidő szabályozása Ubikvitin konjugáció Proteaszómális lebontás 3. Aminosavak lebontása
1. A nitrogén körforgása 2. Fehérjék lebontása Táplálékfehérjék lebontása aminosavakká Saját fehérjék lebontása Féléletidő szabályozása Ubikvitin konjugáció Proteaszómális lebontás 3. Aminosavak lebontása
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből.
 Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
AMINOSAVAK, FEHÉRJÉK
 AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Glikolízis. emberi szervezet napi glukózigénye: kb. 160 g
 Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Mire költi a szervezet energiáját?
 Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
Az AS nitrogénjének eltávolítása
 AMINOSAV ANYAGCSERE Az AS nitrogénjének eltávolítása 1. Hidrolízis (NH 3 eltávolítás az Asn és Gln amid csoportjából) 2. Transzamináció (amino és oxo csoport cseréje; AS és ketosav párok, transzamináz
AMINOSAV ANYAGCSERE Az AS nitrogénjének eltávolítása 1. Hidrolízis (NH 3 eltávolítás az Asn és Gln amid csoportjából) 2. Transzamináció (amino és oxo csoport cseréje; AS és ketosav párok, transzamináz
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Aminosavak általános képlete NH 2. Csoportosítás: R oldallánc szerkezete alapján: Semleges. Esszenciális aminosavak
 Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
Dr. Mandl József BIOKÉMIA. Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek.
 Dr. Mandl József BIOKÉMIA Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek Semmelweis Kiadó Semmelweis Orvostudományi Egyetem Orvosi Vegytani, Molekuláris
Dr. Mandl József BIOKÉMIA Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek Semmelweis Kiadó Semmelweis Orvostudományi Egyetem Orvosi Vegytani, Molekuláris
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
VITAMINOK JELENTŐSÉGE ÉS FORRÁSAIK
 VITAMINOK JELENTŐSÉGE ÉS FORRÁSAIK KÉSZÍTETTE: GAÁL ELEONÓRA OKLEVELES TÁPLÁLKOZÁSTUDOMÁNYI SZAKEMBER DEBRECENI EGYETEM Egészséges alapanyagok egészséges táplálkozás mintaprojekt a közétkeztetés minőségi
VITAMINOK JELENTŐSÉGE ÉS FORRÁSAIK KÉSZÍTETTE: GAÁL ELEONÓRA OKLEVELES TÁPLÁLKOZÁSTUDOMÁNYI SZAKEMBER DEBRECENI EGYETEM Egészséges alapanyagok egészséges táplálkozás mintaprojekt a közétkeztetés minőségi
A légzési lánc és az oxidatív foszforiláció
 A légzési lánc és az oxidatív foszforiláció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet intermembrán tér Fe-S FMN NADH mátrix I. komplex: NADH-KoQ reduktáz
A légzési lánc és az oxidatív foszforiláció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet intermembrán tér Fe-S FMN NADH mátrix I. komplex: NADH-KoQ reduktáz
KARBONIL-VEGY. aldehidek. ketonok O C O. muszkon (pézsmaszarvas)
 KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Vitaminok csoportosítása
 Vitaminok A vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiai összetételű biológiailag aktív szerves vegyületek. Az emberi szervezetbe a vitaminokat a táplálékkal
Vitaminok A vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiai összetételű biológiailag aktív szerves vegyületek. Az emberi szervezetbe a vitaminokat a táplálékkal
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Táplálkozási ismeretek. Fehérjék. fehérjéinek és egyéb. amelyeket
 Táplálkozási ismeretek haladóknak I. Az előző három fejezetben megismerkedtünk az alapokkal (táplálék-piramis, alapanyag-csere, napi energiaszükséglet, tápanyagok energiatartalma, naponta szükséges fehérje,
Táplálkozási ismeretek haladóknak I. Az előző három fejezetben megismerkedtünk az alapokkal (táplálék-piramis, alapanyag-csere, napi energiaszükséglet, tápanyagok energiatartalma, naponta szükséges fehérje,
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
6. Előadás Oligonukleotidok szintézise, koenzimek, vitaminok
 6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
A koenzim Q10 fél évszázados története
 A koenzim Q10 fél évszázados története A koenzim Q10 a sejtek optimális működéséhez nélkülözhetetle A koenzim Q10 (KoQ10) vitaminszerű vegyület. Az ubikinonok k 1 / 8 A Nobel-díjas Dr. Peter Mitchell Kémiailag
A koenzim Q10 fél évszázados története A koenzim Q10 a sejtek optimális működéséhez nélkülözhetetle A koenzim Q10 (KoQ10) vitaminszerű vegyület. Az ubikinonok k 1 / 8 A Nobel-díjas Dr. Peter Mitchell Kémiailag
Purin nukleotidok bontása
 Dr. Sasvári MáriaM Purin nukleotidok bontása 24 1 Purin nukleotidok bontása AMP B r -p 5 nukleotidáz GMP P i adenozin (6-amino) ADA 2 adenozin deamináz 3 B r guanozin P i inozin (6-oxo) P i PP P i purin
Dr. Sasvári MáriaM Purin nukleotidok bontása 24 1 Purin nukleotidok bontása AMP B r -p 5 nukleotidáz GMP P i adenozin (6-amino) ADA 2 adenozin deamináz 3 B r guanozin P i inozin (6-oxo) P i PP P i purin
Integráció. Csala Miklós. Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet
 Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
A KOLESZTERIN SZERKEZETE. (koleszterin v. koleszterol)
 19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
Helyettesített karbonsavak
 elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
IX. Szénhidrátok - (Polihidroxi-aldehidek és ketonok)
 IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekIKözgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekIKözgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Enzimek. Enzimek! IUBMB: szisztematikus nevek. Enzimek jellemzése! acetilkolin-észteráz! legalább 10 nagyságrend gyorsulás. szubsztrát-specificitás
 Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Louis Camille Maillard ( )
 Maillard reakció Louis Camille Maillard (1878-1936) 1913-ban, PhD. tanulmányaiban közölte le, hogy ha egy cukor és amin elegyét hevítjük, egy idő után mindkét reakciópartner eltűnik az oldatból és új termékek
Maillard reakció Louis Camille Maillard (1878-1936) 1913-ban, PhD. tanulmányaiban közölte le, hogy ha egy cukor és amin elegyét hevítjük, egy idő után mindkét reakciópartner eltűnik az oldatból és új termékek
4. FEHÉRJÉK. 2. Vázanyagok. Az izmok alkotórésze (pl.: a miozin). Inak, izületek, csontok szerves komponensei, az ún. vázfehérjék (szkleroproteinek).
 4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
TAKARMÁNYOZÁSTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Vitaminok jelentősége kis mennyiségben előforduló biológiailag aktív anyagok esszenciálisak ( vital amines =létfontosságú
TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Vitaminok jelentősége kis mennyiségben előforduló biológiailag aktív anyagok esszenciálisak ( vital amines =létfontosságú
Sporttáplálkozás. Étrend-kiegészítők. Készítette: Honti Péter dietetikus. 2015. július
 Sporttáplálkozás Étrend-kiegészítők Készítette: Honti Péter dietetikus 2015. július Étrend-kiegészítők Élelmiszerek, amelyek a hagyományos étrend kiegészítését szolgálják, és koncentrált formában tartalmaznak
Sporttáplálkozás Étrend-kiegészítők Készítette: Honti Péter dietetikus 2015. július Étrend-kiegészítők Élelmiszerek, amelyek a hagyományos étrend kiegészítését szolgálják, és koncentrált formában tartalmaznak
Testünk építőkövei: A vitaminok
 Testünk építőkövei: A vitaminok Vitamin A vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiai összetételű biológiailag aktív szerves vegyületek. Az emberi szervezetbe
Testünk építőkövei: A vitaminok Vitamin A vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiai összetételű biológiailag aktív szerves vegyületek. Az emberi szervezetbe
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
A Magyar Élelmiszerkönyv 1-1-90/496 számú elıírása az élelmiszerek tápérték jelölésérıl
 1. melléklet a 152/2009. (XI. 12.) FVM rendelethez A Magyar Élelmiszerkönyv 1-1-90/496 számú elıírása az élelmiszerek tápérték jelölésérıl A rész I. 1. Ez az elıírás a végsı fogyasztók számára szánt élelmiszerek
1. melléklet a 152/2009. (XI. 12.) FVM rendelethez A Magyar Élelmiszerkönyv 1-1-90/496 számú elıírása az élelmiszerek tápérték jelölésérıl A rész I. 1. Ez az elıírás a végsı fogyasztók számára szánt élelmiszerek
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll.
 KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll.
 KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Élelmiszer-fehérjék átalakulása a feldolgozás és tárolás során
 Élelmiszer-fehérjék átalakulása a feldolgozás és tárolás során Az aminosavak átalakulása a feldolgozás és tárolás során A fehérjék hőkezelése aminosavak deszulfurálódása, dezaminálódása, izomerizációja,
Élelmiszer-fehérjék átalakulása a feldolgozás és tárolás során Az aminosavak átalakulása a feldolgozás és tárolás során A fehérjék hőkezelése aminosavak deszulfurálódása, dezaminálódása, izomerizációja,
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
10. Előadás. Heterociklusos vegyületek.
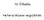 0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
A biokémia alapjai. Typotex Kiadó. Wunderlich Lívius Szarka András
 A biokémia alapjai Wunderlich Lívius Szarka András Összefoglaló: A jegyzet elsősorban egészségügyi mérnök MSc. hallgatók részére íródott, de hasznos segítség lehet biomérnök és vegyészmérnök hallgatók
A biokémia alapjai Wunderlich Lívius Szarka András Összefoglaló: A jegyzet elsősorban egészségügyi mérnök MSc. hallgatók részére íródott, de hasznos segítség lehet biomérnök és vegyészmérnök hallgatók
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll.
 KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
