Prognosztikai faktorok fej-nyaki laphámrákokban, szerepük a terápia tervezésében
|
|
|
- Júlia Gulyás
- 8 évvel ezelőtt
- Látták:
Átírás
1 Prognosztikai faktorok fej-nyaki laphámrákokban, szerepük a terápia tervezésében Ph.D. doktori értekezés Írta: Dr. Kraxner Helga Témavezető: Dr. Szende Béla egyetemi tanár Programvezető: Dr. Jeney András egyetemi tanár Semmelweis Egyetem Doktori Iskola 8/1 Patológiai Tudományok Budapest 2002
2 Tartalomjegyzék 1. BEVEZETÉS CÉLKITŰZÉSEK IRODALMI ÁTTEKINTÉS AZ APOPTÓZIS ÁLTALÁNOS JELLEMZŐI IONIZÁLÓ SUGÁRZÁS ÁLTAL INDUKÁLT APOPTÓZIS A DNS-KÁROSODÁS LÉTREJÖTTE ÉS FELISMERÉSE (INTRANUKLEÁRIS SZENZOROK) EXTRANUKLEÁRIS SZENZOROK ÉS AZ ÁLTALUK KIVÁLTOTT SZIGNÁL-TRANSZDUKCIÓ A CERAMID SZINTETÁZ ENZIM SZEREPE A CERAMID-SZINTÉZIS SZABÁLYOZÁSA. ANTI-APOPTOTIKUS JELÁTVITEL A KALPAIN SZEREPE A KÖZÖS ÚT - KASZPÁZOK SZEREPE A MITOKONDRIUM SZEREPE AZ ÁLTALUNK VIZSGÁLT PROGNOSZTIKAI FAKTOROK IRODALMI ÖSSZEFOGLALÁSA APOPTÓZIS-INDEX MITÓZIS-INDEX P53 FEHÉRJE A SEJTENKÉNTI DNS MEGOSZLÁS SAJÁT VIZSGÁLATOK HUMÁN KLINIKOPATOLÓGIAI KUTATÁSOK I IRODALMI BEVEZETÉS CÉLKITŰZÉS ANYAG ÉS MÓDSZER BETEGCSOPORT PATOLÓGIAI ELJÁRÁS A VIZSGÁLATOK ÉRTÉKELÉSÉNEK MÓDSZEREI EREDMÉNYEK HISZTOLÓGIA TNM BEOSZTÁS TUMOR-REGRESSZIÓ P53-EXPRESSZIÓ DNS-HISZTOGRAM PARAMÉTEREK APOPTÓZIS-INDEX (AI) MITÓZIS-INDEX (MI) MEGBESZÉLÉS KÖVETKEZTETÉSEK HUMÁN KLINIKOPATOLÓGIAI KUTATÁSOK II IRODALMI BEVEZETÉS CÉLKITŰZÉS ANYAG ÉS MÓDSZER BETEGCSOPORT PATOLÓGIAI ELJÁRÁS STATISZTIKAI ANALÍZIS EREDMÉNYEK KLINIKAI PARAMÉTEREK HAGYOMÁNYOS HISZTOLÓGIAI PARAMÉTEREK MUTÁNS P53-EXPRESSZIÓ A SEJTENKÉNTI DNS-TARTALOM VIZSGÁLATA MEGBESZÉLÉS KÖVETKEZTETÉSEK
3 4.3. DBD ÉS SUGÁRKEZELÉS KOMBINÁCIÓJÁVAL VÉGZETT IN VITRO VIZSGÁLATOK IRODALMI BEVEZETÉS VIZSGÁLATUNK CÉLKITŰZÉSE ANYAG ÉS MÓDSZER SEJTVONAL ÉS SEJTKULTÚRA BESUGÁRZÁS DIBRÓMDULCIT KEZELÉS SEJTSZÁM MEGHATÁROZÁS APOPTÓZIS- ÉS MITÓZIS-INDEX MEGHATÁROZÁS KÍSÉRLETI TERV BCL-2, PCNA, P53 ÉS RB FEHÉRJE-MEGHATÁROZÁS A VIZSGÁLATOK ÉRTÉKELÉSÉNEK MÓDSZEREI - ÖSSZEFOGLALÁS EREDMÉNYEK CO SUGÁRZÁSSAL VÉGZETT ELŐKÍSÉRLETEK. DÓZIS-VÁLASZ DBD-VEL VÉGZETT ELŐKÍSÉRLETEK. TÁJÉKOZÓDÓ, DÓZIS-KERESŐ VIZSGÁLAT AZ EGYEDI ÉS KOMBINÁLT KEZELÉSEK HATÁSA MEGBESZÉLÉS KÖVETKEZTETÉSEK EREDMÉNYEK ÉS KÖVETKEZTETÉSEK ÖSSZEFOGLALÁSA KÖSZÖNETNYILVÁNÍTÁS IRODALOMJEGYZÉK A SZERZŐ ÉRTEKEZÉSSEL KAPCSOLATOS KÖZLEMÉNYEI ÉS ELŐADÁSAI AZ ÉRTEKEZÉSBEN ELŐFORDULÓ RÖVIDÍTÉSEK JEGYZÉKE ÖSSZEFOGLALÓ SUMMARY
4 1. Bevezetés Vizsgálataink klinikai beteganyagába a Semmelweis Egyetem Fül-, orr-, gégészeti és Fej- Nyaksebészeti Klinikájának betegei közül a gége-, az algarat-, a középgarat- és a szájüregi tumoros eseteket választottuk be. Ennek oka egyrészről az ezekben a lokalizációkban előforduló malignómák hasonló etiológiája, szöveti szerkezete amely több, mint 90 %-ban laphámrák (elszarusodó, illetve el nem szarusodó) -, hasonlók a terápiás elvek és módok is (174, 208, 47). Másrészről jelentőségüket előfordulásuk gyakorisága adja (184), a klinikán kezelt daganatos betegségek közül is ezek a tumorok alkotják a legnagyobb csoportot. Vizsgálati anyagunkba nem kerültek be az Európában jóval ritkábban előforduló, és többnyire más szövettani típusú orrgarat, orr- és orrmelléküreg tumoros esetek, valamint - az egyébként jelentős csoportot képező - bőrtumoros, pajzsmirigy-, és nyálmirigy daganatos betegek sem. A továbbiakban fejnyaki tumorok alatt tehát a gége-, az algarat-, a középgarat- és a szájüreg laphám eredetű karcinómái értendők. Ezen régiók laphámrákjai gyakori, rossz prognózisú daganatok. Incidenciájuk folyamatosan emelkedik, egyre agresszívebb, gyorsan progrediáló formák jelennek meg (184). Hazánkban 1996-ban az összes férfi rákhalálozás 9.9%-át, a női rákhalálozásnak pedig 1.9%-át tették ki, ezzel mindkét nem esetében Magyarország áll az első helyen Európában (184). A fej-nyaki daganatok előfordulása összefüggést mutat környezeti tényezőkkel, a dohányzás és az alkoholfogyasztás jelenti a két legfontosabb etiológiai faktort (174, 208). Ezen kívül felvetik a herpes simplex és a humán papillomavírus (1, 125), valamint szájüregi- és garatrákok esetében a rossz szájhigiéne kóroki szerepét is. Keveset tudunk azokról a prognosztikai tényezőkről, amelyek a fej-nyaki malignómák klinikai lefolyását érintik. Sok egyéb tényező mellett széles körben vizsgált a klinikai TNM stádium (157), a patológiai TNM stádium, a szövettani grading, az apoptózis- és mitózis-index (145), bizonyos géntermékek, többek között a p53 (142), bcl-2 (34), Rb (retinoblastoma), mdm2 (murine double minute 2) prognosztikai értéke. Ugyanígy 4
5 kutatják a sejtenkénti DNS-tartalom (ploidia, DNS-index, S-fázis arány) 1 (178); a proliferációs aktivitásra jellemző antigének (PCNA - Proliferating Cell Nuclear Antigen, Ki-67) (12) és számos, tumormarkerként ismert antigén (pl. CEA - Carcinoembrionalis Antigen, SCCA - Squamous Cell Carcinoma Antigen, CYFRA 21-1), enzim (pl. NSE - Neuronspecifikus Enoláz) és metabolit (pl. LASA Lipid-associated Sialic Acid) (153, 205) jelentőségét is a fej-nyaki daganatos betegségek lefolyása, kimenetele szempontjából. Mindezidáig azonban a prognózist egyértelműen előrejelző faktort (ill. faktorokat) nem sikerült találni. A prognosztikai faktorok minél pontosabb megismerésének jelentősége lehet az alkalmazott terápia megválasztása szempontjából is. A fej-nyaki laphámrákok rossz prognózisú daganatok, különösen, ha előrehaladott állapotban kerülnek felismerésre. A legtöbb esetben a sebészi eltávolítás jelenti a primer terápiát. Ha ez nem végezhető el a daganat kiterjedése, vagy a beteg rossz általános állapota miatt, esetleg a beteg nem egyezik bele a műtétbe, a következő választandó terápiás lehetőség a sugárkezelés. Az egyes daganatok sugárérzékenysége azonban hasonló klinikai paraméterek, azonos lokalizáció, azonos szövettani típus, azonos grádus mellett is különböző lehet (13). Irodalmi adatok alapján a fej-nyaki karcinómák %-a sugárrezisztens (25). Amennyiben sikerülne a sugárérzékenységet meghatározó prognosztikai faktort vagy faktorokat találni, azok vizsgálata a kezelés megkezdése előtt segíthetne a legmegfelelőbb egyéni, személyre szabott terápia megválasztásában. Ha egy daganat - a faktorok vizsgálata alapján - sugárérzékenynek bizonyul, akkor a sugárkezelés esetleg elsőként választandó terápiás lehetőség is lehetne, amelynek jelentősége lehet a súlyosan csonkító beavatkozások elkerülése, szervmegtartás, funkciómegőrzés szempontjából. Más esetekben továbbra is műtéti, ill. egyéb terápia (pl. citosztatikus kezelés), esetleg több terápiás modalitás kombinálása (pl. műtét és citosztatikum; vagy citosztatikummal kiegészített sugárkezelés) jöhet szóba. Így lehetővé válna az individuális terápia kidolgozása. Ezekből a megfontolásokból kiindulva klinikopatológiai munkám során prognosztikai faktorok vizsgálatával, valamint terápiás jelentőségük kutatásával foglalkoztam. Emellett in vitro kísérletes modellen tanulmányoztam az irradiáció és a citosztatikus kezelés 1 A fogalmak definíciója, rövid magyarázata az értekezés 8. oldalán olvasható. 5
6 együttes hatását, a terápiás hatékonyság fokozásának lehetőségét többféle modalitás kombinálásával. A vizsgálatok egy részét paraffinba ágyazott szövetblokkokon, másik részét sejttenyészeteken végeztem. A szövettani mintavétel a Semmelweis Egyetem Fül-, orr-, gégészeti és Fej-, Nyaksebészeti Klinika betegeiből történt, a minták feldolgozását szövetblokkokká a II. számú Pathologiai Intézet munkatársai végezték. Az apoptózis- és mitózis-indexet minden esetben az I. számú Pathologiai és Kísérleti Rákkutató Intézetben határoztam meg Szende Béla professzor úr irányítása mellett. A kóros p53 fehérje jelenlétét és a sejtenkénti DNS-tartalmat az Országos Onkológiai Intézet Molekuláris Pathologiai Osztályán vizsgáltam Szentirmay Zoltán tanár úr vezetésével. A sejtkultúrákon végzett kísérletek során a tenyészetek besugárzását és citosztatikus kezelését az Országos Sugárbiológiai és Sugáregészségügyi Kutató Intézetben végeztem Hidvégi Egon professzor úr és Dr. Sáfrány Géza szakmai segítségével. Az onkoproteinek vizsgálata az I. számú Pathologiai és Kísérleti Rákkutató Intézetben történt Jeney András professzor úr irányítása mellett. Formai megjegyzések Az értekezésben az ábrákat és a táblázatokat arab számokkal jelöltem, amelyeket kiemeltem félkövér betűkkel. Azokban az esetekben, amikor egy korábban szereplő ábrára, vagy táblázatra visszautalok, azok oldalszámát is feltüntettem. Az idézett közleményeket a szövegben szintén arab számokkal, kurzív betűtípussal jelöltem. Az orvosi szavak írásmódjában az MTA ajánlásait követtem (Brencsán: Új orvosi szótár, 2002). Törekedtem a magyar helyesírás szabályainak megfelelő, kiejtés szerinti írásmód alkalmazására azoknál a szavaknál, amelyek esetében az ajánlás ezt lehetővé teszi (pl. limfocita, limfoid). Amelyeknél nem, ott a hagyományos, latin, görög, esetleg angol írásmódot követtem (pl. lymphoma). A rövidítések, mozaikszavak magyarázata e szavak első előfordulása alkalmával, közvetlenül azokat követően szerepel zárójelben, valamint a dolgozat végén, rövidítésjegyzékben is megtalálható, összefoglalva. Azok a patológiai fogalmak (pl. gének, receptorok) amelyek az irodalomban több néven is előfordulnak, az értekezésben a jobb áttekinthetőség céljából egyféleképpen szerepelnek: pl. p21/waf1/cip1 helyett p21, vagy CD95/Fas/APO1 helyett Fas. 6
7 2. Célkitűzések 1) Humán klinikopatológiai kutatásaink során első ízben arra kerestünk választ, hogy melyek azok a faktorok, amelyek fej-nyaki daganatok sugárérzékenységét a terápia megkezdése előtt jelezhetik, sugárterápián átesett betegek esetében a prognózist befolyásolhatják. Prospektív vizsgálatunkba azokat a fej-nyak rákos betegeket vontunk be, akik primer radioterápiában részesültek. Az első sugárkezelés előtt vett biopsziás anyagban olyan faktorokat vizsgáltunk, amelyeknek irodalmi adatok szerint prognosztikai jelentősége lehet: apoptózis-index 1,2 (145) mitózis-index 3 (186) p53 tumorszuppresszor gén expressziója (17, 112) DNS-index 4 (93), ploidia 5 (29, 93) S-fázis arány 6 (43, 108) Mivel irodalmi adatok szerint nemcsak a kezelést megelőzően meghatározott apoptózis-index érték, hanem az apoptózis indukálhatósága is szerepelhet prognosztikai faktorként bizonyos tumorok esetében (145), felmerült annak a lehetősége, hogy ezt a szempontot fej-nyaki daganatok prognosztikájában is figyelembe vegyük. Feltételezésünk szerint a besugárzás apoptózist fokozó hatása már az első kezelés után kimutatható. Ebből kiindulva az irradiáció első, 2Gy dózisú frakcióját követően ismételten meghatároztuk az apoptózis-indexet. Mitózis-index meghatározást és p53 immunhisztokémiai vizsgálatot is végeztünk ebben az időpontban. Ezt követően több kérdésre kerestük a választ: Az apoptózis- és mitózis-index változása az első 2Gy irradiációt követően használható-e prognosztikai faktorként? A kezelés előtti és az első kezelés utáni paraméterek összehasonlításával lehet-e következtetni korai időpontban a terápiás hatékonyságra az egyes daganatok esetében, így fennállhat-e individuális terápia kidolgozásának lehetősége? Változik-e a p53 expresszió a besugárzás első frakcióját követően? Van-e összefüggés a p53 expresszió és a többi vizsgált paraméter között? 7
8 2) Második humán klinikopatológiai vizsgálat-sorozatunkban retrospektív módon értékeltük a p53 expresszió sejtenkénti DNS-tartalom prognosztikai szerepét különbözőképpen kezelt, többségében műtéti terápián átesett fej-nyaki laphámrákos betegeken. 3) Tekintettel a fej-nyaki daganatok primer sugárterápiáját követően tapasztalható gyenge túlélési eredményekre, felvetődött a sugárkezelés kombinálása citosztatikummal. In vitro modellen a Co irradiációból és DBD-ből (1,6- dibróm-1,6-didezoxi-dulcit) álló kezelési kombináció hatékonyságát hasonlítottuk össze a radio-monoterápia, valamint az önmagában alkalmazott DBD kezelés hatékonyságával. Az egyes kezelések effektivitására a különböző időpontokban meghatározott sejtszám, apoptózis-index és mitózis-index értékek alapján következtettünk. Mindenek előtt arra kerestünk választ, hogy a kombinált kezelés hatékonyabb lehet-e az önmagában alkalmazott sugárkezelésnél. Emellett vizsgáltuk az egyes kezelési módok hatását több - a sejtproliferációt és az apoptózist befolyásoló - onkoprotein (p53, Rb, bcl-2, PCNA) expressziójára. Indexszel ellátott fogalmak rövid áttekintése 1 Apoptózis: Programozott sejthalál, amelyet meghatározott morfológiai elváltozások kísérnek (95). 2 Apoptózis-index: 2000 tumorsejtben az apoptotikus sejtek száma százalékban kifejezve. 3 Mitózis-index: 2000 tumorsejtben a mitotikus sejtek száma százalékban kifejezve. 4 DNS-index (DI): A megváltozott (tumoros) és ép G0,1-fázisú sejtek átlagos DNSértékének a hányadosa (67). 5 Ploidia: az adott daganatos sejt kromoszóma tartalma normális-e, vagy ettől eltérő. Euploid sejtekben a DNS-index (DI) egész szám, a diploid sejtek DI-értéke 1. Az aneuploid sejtek DNS-indexe legalább 10%-os eltérést mutat az egész számtól. 6 S-fázis arány: A DNS hisztogram analíziskor kapott S-fázisú sejtek %-os aránya (szubpopulációnként). 8
9 3. Irodalmi áttekintés Első, prospektív klinikopatológiai vizsgálataink során, valamint in vitro kísérleteinkben is az ionizáló sugárzás sejtpusztító, apoptózist indukáló hatása állt figyelmünk középpontjában. Ezért a fejezet első részében - az apoptózis általános jellemzőinek összefoglalása után - az ionizáló sugárzás sejtkárosító hatásmechanizmusával kapcsolatos irodalom áttekintése olvasható. Ezt követi az általunk vizsgált prognosztikai faktorok irodalmi összefoglalója. Az in vitro kísérleteinkhez használt citosztatikummal (DBD) kapcsolatos irodalom áttekintése - mivel szorosan csak ahhoz a kísérletsorozathoz tartozik - közvetlenül a laphámrák sejtvonalon végzett vizsgálatok ismertetése előtt található. Az ionizáló sugárzás sejtkárosító hatását széles körben vizsgálták és vizsgálják. A sugárzás a sejtben több szinten okozhat elváltozást: egyrészt ismert DNS-károsító hatása, emellett elváltozást okozhat a sejtmembrán egyes összetevőiben, valamint a víz radiolízise útján reaktív oxigéngyökök képződése által is károsíthatja a sejtet (199). Adott helyen a károsodás létrejöttekor tisztázatlan mechanizmus útján ún. alarm szignál generálódik (182), amely képes jelátvivő utakat aktiválni. A folyamat végső kimenetelét a sejtre és a károsító ágensre jellemző tényezők határozzák meg; többek között függ a sejt típusától, valamint a károsodás mértékétől. Pl. a besugárzásra keletkező kisebb genetikai hibákat a sejtek képesek kijavítani, nagyobb - a repair kapacitást meghaladó - károsodás esetén aktív sejthalál (apoptózis) figyelhető meg, míg bizonyos sugárdózis felett nekrotizálnak a sejtek Az apoptózis általános jellemzői Az apoptózist Kerr és Wyllie írta le 1972-ben (95). Az apoptózis az aktív sejthalál egyik fő formája, amelyet meghatározott morfológiai és biokémiai változások sorozata jellemez. Fontos szerepet tölt be különböző biológiai rendszerek széles skálájában, többek között normál sejtek turnoverében, az immunrendszerben, embrionális fejlődés során, hormon-dependens atrófiában, citosztatikumok és egyéb kémiai szerek által okozott sejthalálban (28). Sok humán betegségben megfigyelhető kóros mértékű 9
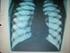
10 apoptózis, pl. neurodegeneratív kórképekben (Alzheimer-kór), isémiás károsodásban, autoimmun betegségekben, rákos megbetegedések különböző formáiban. Az apoptózist indukálhatják különböző fiziológiai és stressz-ingerek, amelyek több különböző szignálút aktiválásán keresztül vezethetnek aktív sejthalálhoz (59). Az apoptózis 2 lépésben történik: először a sejt elkötelezetté válik a sejthalál irányába, ezt követi az effektor fázis, amelyet a sejtszerkezetben bekövetkező sztereotíp morfológiai változások jellemeznek (28). Ez egy közös effektor mechanizmus létét feltételezi különböző sejtekben, ami cisztein proteázok egy csoportja (kaszpázok) és nukleázok aktiválódását foglalhatja magában (199). A folyamat eredménye a szubcellulláris struktúrák rendezett dezintegrációja, membránnal körülvett, ép sejtalkotókat tartalmazó apoptotikus testek létrejötte, amelyet a környező sejtek fagocitálnak. Az apoptózist a nukleáris kromatin kondenzációja és fragmentációja, a citoplazmatikus sejtalkotók tömörülése, az endoplazmatikus retikulum dilatációja, a sejt volumenének csökkenése jellemzi (1. ábra). A plazmamembránban olyan változások jönnek létre, amelyek alapján az apoptotikus sejteket a fagociták felismerik és fagocitálják, gyulladásos reakció nélkül. A folyamatot nem kíséri a környező sejtekre nézve toxikus anyagok felszabadulása (94). Az apoptózis folyamatában részt vevő biokémiai események sorozata kalcium- és magnézium-dependens endonukleázok aktiválódásához vezet (59), ezek az enzimek végzik a nukleáris kromatin fragmentálását. A fragmentálás szelektíven az internukleoszomális linker-régiókban történik, ami által bázispárból, valamint azok többszöröseiből álló nukleáris fragmentumok keletkeznek, amelyek agaróz gél elektroforézisen létra-diagram formájában jelennek meg (94). Úgy tűnik, hogy az internukleoszomális DNS hasítás az apoptózis folyamatának relatíve késői eseménye, de egyszerű kimutathatósága miatt a legtöbb szerző ezt tartja a fő kritériumnak annak eldöntésére, hogy egy sejt apoptotikus-e vagy sem. 10
11 1. ábra 1 Az apoptózis folyamata. Ultrastruktúrális változások a sejtben apoptózis során. 1. Normál sejt. 2. Az apoptózis kezdeti lépései: a kromatinállomány feltöredezése, tömörülése a maghártya belső felszíne mentén. A citoplazma kondenzálódása, enyhe behúzódások létrejötte a sejtmembrán és a maghártya felületén. 3. A folyamat gyors progressziója a nucleus fragmentálódásával, a sejtmembrán felszínének kifejezett behúzódásaival, amely eredményeként a sejtből membránnal körülvett, ép citoplazmatikus sejtalkotókat és nukleáris fragmentumokat tartalmazó apoptotikus testek keletkeznek. 4. Az apoptotikus testek fagocitózisa a környező sejtek által. 1 Átvéve: Kerr J.F.R., Harmon B.V.: Definition and incidence of apoptosis: an historical perspective. 1. ábra In: Apoptosis, the Molecular Basis of Cell Death. Current Communications 3 in Cell and Molecular Biology (ed.: Tomei L., Cope F.O.) p7, Cold Spring Harbor Laboratory Press, New York (1991) (94) 11
12 A sejtalkotók közül a mitokondrium központi helyet foglal el a sejthalál folyamatában, ez alapján az apoptózist 3 fázisra oszthatjuk (199): (a) pre-mitokondriális fázisra, ami sejthalált indukáló inger hatására a különböző jelátvivő (szignál-transzdukciós) utak aktiválódását foglalja magába; (b) mitokondriális fázisra, amikor a mitokondrium membránpotenciálja elvész; (c) poszt-mitokondriális fázisra, amely során a mitokondriumból felszabaduló proteinek aktiválják a kaszpázokat és nukleázokat, szisztematikus celluláris destrukciót eredményezve. Sokáig a kaszpázok szerepét esszenciálisnak gondolták az apoptózis folyamatában, de létezik kaszpáz-independens apoptózis is (36) Ionizáló sugárzás által indukált apoptózis Az ionizáló sugárzás többféle úton képes sejtkárosodást okozni, apoptózist kiváltani (199). Egyrészt DNS-károsító hatása által, ami olyan szignálutak összehangolt aktiválását eredményezi, amelyek felelősek a sejtciklus leállásáért, a DNS-repair folyamatok aktiválásáért, az apoptózisért és a stresszreakcióért. A DNS-károsodást felismerő és jeltovábbító rendszerek a sejtciklust meghatározott ellenőrzési pontokon kontrollálják, az ezeken a helyeken észlelt hibák sejthalálhoz vezethetnek (199). A DNS hibáit felismerő rendszer elemei a károsodás intranukleáris szenzorainak tekinthetők (182). Közéjük tartozik a poli(adp-ribóz) polimeráz (PARP), a DNS-dependens protein kináz (DNA-PK), az ATM (ataxia teleangiectasia mutated) gén fehérjeterméke és a p53 fehérje. A károsodás felismerése együtt jár ún. alarm szignálok keletkezésével, amely poli(adp-ribóz) polimerek szintézisét, valamint foszforilációs kaszkádok protein kinázok által történő elindítását foglalhatja magába (182). Léteznek az irradiáció kiváltotta sejtkárosodásnak extranukleáris szenzorai is. Ennek megfelelően alarm szignál nemcsak a DNS-károsodás helyén, hanem extranukleárisan is generálódhat, részben a sejtmembránban, részben a citoplazmában (182). A sejtmembránban kezdődő, apoptózishoz vezető jelátvivő út indulhat membránhoz kötött kinázok (tirozin kinázok), valamint a szfingomyelináz enzim aktiválódásán keresztül is. A szfingomyelináz a szfingomyelin bontását végzi, amely során ceramid keletkezik. A ceramid - több sejttípus esetében - a másodlagos messenger szerepét tölti be az apoptózis indukció mediálásában irradiációt követően (59, 199). Az ionizáló sugárzás a 12
13 citoplazmában a víz radiolízise útján, reaktív oxigéngyökök generálásán keresztül képes apoptózishoz vezetni (199). Egyelőre nem ismert a pontos mechanizmus, amellyel a besugárzás a különböző szignálutakat aktiválni képes. Ezek közül a sejtek egyet vagy többet is használhatnak sejttípustól, differenciáltsági foktól, környezettől, sugárdózistól függően. Mérsékelt dózisú besugárzás például, amely már mérhető DNS károsodást okoz és a sejtek túlélését jelentősen csökkenti, nem biztos, hogy komoly károsodáshoz vezet a sejtmembránban, vagy a citoplazmatikus sejtalkotókban (182). Ebben az értelemben a feltételezett alarm-szignál generációja nem szükségszerűen jelenti citoplazmatikus struktúrák károsodását. A p53 molekula központi helyet foglal el a posztirradiációs jelátvitelben, de léteznek p53-independens szignálutak is. A p53-dependens és -independens jelátvivő utak hálózatának összehangolt működése szükséges a sugárzás által indukált sejtválasz létrejöttéhez (182). A sejtválasz magában foglalja bizonyos gének aktiválódását, a sejtprogresszió kontrollját a sejtciklus ellenőrzési pontjain keresztül, replikáció- és transzkripció-gátlást, apoptózis indukciót (182). Az apoptózis bonyolult szabályozás alatt áll, a pro-apoptotikus szignálutak mellett minden sejtben többféle anti-apoptotikus jelátvivő rendszer is működik, amely szabályozza a folyamatot. Végül a pro- és anti-apoptotikus folyamatok egyensúlya határozza meg bármilyen mikrokörnyezeti feltétel esetén az apoptotizáló sejtek arányát (11) A DNS-károsodás létrejötte és felismerése (intranukleáris szenzorok) A DNS-károsodás létrejötte Az ionizáló sugárzás által okozott celluláris DNS károsodás kb %-a indirekt módon, víz radiolízise által keletkezett szabadgyökök, főként hidroxilgyökök útján jön létre. Ilyenek pl. a purin- és pirimidingyűrű károsodásai, a DNS egyeslánc-törés, a bázisvesztés. Ezekről a károsodásokról azt gondoljuk, hogy nincs nagy jelentőségük az 13
14 ionizáló sugárzás sejtpusztító és mutagén hatása szempontjából (197). Több ok lehetséges, amelyekre tekintettel a szabadgyökök által indukált DNS-károsodásokat nem tartjuk a sejtre nézve letálisnak: egyrészt az így keletkezett hibák nagyon hasonlóak az oxidatív metabolizmus során létrejövő károsodásokhoz, amelyekből különböző becslések alapján naponta keletkezik spontán egy humán sejtben. Ezekhez az értékekhez képest ionizáló besugárzás esetén, a celluláris közepes letális dózis alkalmazása mellett a szabadgyökök indukálta DNS hibák száma alacsony (197). A keletkezett hibákat egy nagyon hatékonyan működő repair rendszer (BER: base excision repair) kijavítja. Ennek a rendszernek a feladata az endogén DNS-károsodások (pl. spontán purin-vesztés, amin-vesztés, alkiláció) kijavítása is, amelyek egyébként potenciálisan citotoxikusak és mutagének lennének (197). Egy DNS károsodás biológiai konzekvenciáját a repair folyamatok hatékonysága, és a ki nem javított hibák DNS replikációs apparátussal való interakciója határozza meg (197). Egy adott lézió potenciális citotoxicitása és mutagenitása attól függ, hogy egy DNS polimeráz enzim át tudja-e hidalni a léziót, és ha igen, akkor milyen bázist illeszt be. Feltehetően az tekinthető adott sejtre nézve potenciálisan letális léziónak, amely blokkolja a DNS polimerázokat. Ha a léziót egy polimeráz át tudja hidalni, de nem a megfelelő bázist illeszti be, akkor a lézió potenciálisan mutagén. Egy DNS polimeráznak az a képessége, hogy át tud-e hidalni egy adott léziót egy bizonyos bázis beültetésével komplex folyamat, függ a lézió struktúrájától, magától a DNS polimeráztól, valamint a lézió környezetében levő bázisszekvenciától (197). Az ionizáló sugárzás citotoxikus hatásával az általa okozott DNS kettőslánc-törések vannak összefüggésben, ezt tartjuk a primer léziónak a sejthalál folyamatában (197). Martin és Haseltine 125 I izotóp segítségével igazolták, hogy ionizáló sugárzás képes DNS kettőslánc-törést okozni (121), a kettőslánc-törés pedig képes apoptózist indukálni (147). A besugárzás hatására direkt módon keletkező kettőslánc-törések mennyisége azonban olyan kicsi, hogy nem tehető az irradiáció okozta sejtpusztulás kizárólagos felelősévé (198). Valószínű, hogy egyéb módon is keletkeznek kettőslánc-törések besugárzás folyamán, pl. egymáshoz közeli szemközti, egyébként nem letális léziók létrejöttekor (pl. szabadgyökök által okozott egyeslánc-törések, bázisvesztések), vagy azok repair folyamata során. Ez különösen azokon a helyeken lehetséges, ahol a DNS halmozottan 14
15 károsodik a víz - DNS közeli helyen történő - ionizációja és szabadgyökök felszabadulása miatt (197). A DNS-károsodás felismerése Az ionizáló sugárzás hatására keletkező DNS-károsodást a sejt DNS-figyelő (monitorozó) rendszere felismeri, alarm szignált generál, amely két, egymással kölcsönösen összefüggő úton indít el válaszreakciót (182). Egyrészt DNS repair-enzimek koncentrálódnak a károsodás helyén az eredeti DNS struktúra helyreállítása céljából. Másrészt jelátvivő kaszkádok indulnak el, amelyek gének egy csoportjának aktiválódásán keresztül a sejtciklus leállását eredményezik - lehetővé téve a DNS hiba kijavítását -, nagyfokú károsodás esetén pedig a sejt apoptózisához vezetnek. Azok az enzimek, amelyek a DNS-lánc törésekor aktiválódnak, az irradiáció okozta DNS-károsodás potenciális szenzorainak tekinthetők. A DNS-károsodás felismerésében a poli(adp-ribóz) polimeráz (PARP), a DNS-dependens protein kináz (DNA-PK), az ATM (ataxia teleangiectasia mutated) protein és a p53 játszanak kulcsfontosságú szerepet (182), amely fehérjék szoros kapcsolatban vannak egymással. A PARP, a DNA- PK és az ATM a p53 szabályozásán keresztül hatnak, míg a p53 további génekre ill. fehérjetermékeikre fejt ki hatást (ezek közé tartozik a későbbiekben említésre kerülő p21, Rb, bax, mdm2, GADD45 fehérje) (199). A szenzorproteinek közül a PARP a lánctörés helyén kötődik a DNS-hez, ami poli(adpribóz) polimerek szintézisét eredményezi (6). Ezt követően a PARP-hoz kötött polimerek több olyan nukleáris proteint vonzanak a DNS-károsodás helyéhez, amelyek képesek a polimereket megkötni. A kötődés egy 22 aminosavból álló polimerkötő szekvencián keresztül történik, amelyhez a poli(adp-ribóz) molekulák non-kovalensen kapcsolódnak. Ilyen szekvenciát tartalmaznak például a p53, a p21, a DNA-PK és a hiszton fehérjék is. A polimerkötés átmenetileg megváltoztatja a proteinek funkcióját, módosíthatja a protein-protein kölcsönhatást egészen addig a lépésig, amikor a poli(adp-ribóz) glikohidroláz enzim lebontja a polimereket, és megszűnik a fehérjekötés (6). Althaus és mtsai leírták, hogy a p53 molekulának három polimerkötő helye van, kettő a szekvencia-specifikus DNS-kötő doménen, egy pedig a tetramer formációért 15
16 felelős doménen (6). A p53-hoz kötődő poli(adp-ribóz) polimerek megváltoztatják a p53 DNS-kötő funkcióját, emellett valószínűleg védik a molekulát a degradációtól, ami nélkülözhetetlen a megfelelő p53 funkció szempontjából DNS károsodást követően (6). A PARP egy másik feltételezett funkciója, hogy a DNS-törés helyét elfoglalva addig is megakadályozza a szabálytalan rekombinációt, amíg a repair enzimek a sérülés körül koncentrálódnak, és kijavítják a hibát (161). A DNA-PK (DNS-dependens protein kináz) szintén szenzor protein, amely képes egy foszforilációs kaszkádot kezdeni, szignál-transzdukciót elindítani (182). A DNS kettőslánc-törés törvégeinek újraegyesítésében van szerepe G 1 és S-fázisban. Az enzim egy - a DNS szabad végeihez kötődő - Ku alegységet tartalmaz, amely egy 70 és egy 86 kda-os alegységből álló heterodimer, valamint egy 460 kda-os katalitikus alegységet (DNA-PKcs) (28). A potenciális szenzor mechanizmus a Ku-kötés. A PARP és a DNA- PK Ku alegysége egymással kompetícióban állnak a szabad DNS-végek kötéséért. A katalitikus alegység (DNA-PKcs) a repair folyamatban, a DNS végek újraegyesítésében szerepet játszó XRCC4 (X-ray repair cross-complementing gene 4) - ligáz IV proteinkomplexet köti (182). A p53 fehérje a p53 tumorszuppresszor gén produktuma, szintén a DNS-károsodás potenciális szenzora. Fontos szerepet játszik az irradiáció hatására létrejövő celluláris válaszban. Sugár hatására - főként poszt-transzlációs mechanizmus útján - p53 szintemelkedés következik be, megnövekszik a p53 fehérje transzportja a sejtmagba, a sejt halad a repair folyamatokat lehetővé tevő sejtciklus leállás, ill. az apoptózis irányába (182, 199). Már egyetlen kettőslánc-törés a nukleáris genomban elegendő lehet a p53 aktiválásához (182). Szoros kapcsolat van a DNA-PK, az alábbiakban részletezésre kerülő ATM (ataxia teleangiectasia mutated) protein és a p53 funkció között (199). A DNA-PK és az ATM a p53 foszforilációját végzi a 15-ös szerinen, ami csökkenti a kötődést az mdm2-höz (az mdm2 a p53 negatív regulátora, a degradációját segíti elő), így stabilizálja a p53 fehérjét. A DNA-PK az mdm2 foszforilációjára is képes a 17-es szerinen, amely ezáltal nem tud a p53-hoz kötődni. Feltételezik, hogy in vivo a DNA-PK addig képes fenntartani a foszforilációt, amíg a DNS-törvégek újraegyesülnek, ekkor inaktiválódik a kináz. Ezt 16
17 követően az mdm2 a p53-hoz kötődik és annak gyors degradációját okozza (65, 106), így a DNS-károsodás által beindított szignálút inaktiválódik. Az ATM (ataxia teleangiectasia mutated) fehérje egy protein kináz, amely szintén a DNS-károsodás detektálásában részt vevő faktorok hálózatához tartozik (126, 182, 199). A fehérjét kódoló gén ép működése esetén az ATM megteremti a kapcsolatot a DNSkárosodás felismerése és olyan szignálutak aktiválódása között, amelyek a sejtprogresszió leállásához vezetnek a sejtciklus G 1 /S, S és G 2 /M ellenőrzési pontjain, valamint a DNS repair aktiválódását eredményezik (182). Besugárzás kiváltotta DNS-károsodásnál normál ATM funkció esetén az ATM protein a G 1 /S fázis határán p53 által mediált módon (a p53 foszforilációját végzi a 15-ös szerinen) indukálja p21-et, amely képes a ciklin-cdk (ciklin-dependens kináz) komplexek megkötésére, és gátolja a kinázok (cdk1, 2, 4, 6) aktivitását (56, 75). A ciklind-cdk4 komplex egyik szubsztrátja a retinoblastoma (Rb) fehérje, amely foszforilációja szükséges ahhoz, hogy az E2F (S-fázis specifikus) transzkripciós faktor képes legyen róla leválni és aktiválódni. Az E2F biológiai funkciója a sejtproliferációt elősegítő gének expressziójának beindítása. A cdk4 gátlása esetén az Rb fehérje hipofoszforilált állapotban marad, továbbra is kötődik az E2F-fel, gátolva a proliferációhoz szükséges génaktivációt. A sejtciklus pedig megáll G 1 fázisban, aktiválódnak a repair folyamatok, súlyos károsodás esetén a sejt apoptózissal elpusztul (139). Ataxia teleangiectasiás betegek - normál ATM funkció hiányában - extrém módon érzékenyek besugárzásra, irradiációt követően hiányzik, vagy késleltetett a p53 válasz (199). Az ataxia teleangiectasiához hasonló tünetekkel jár az autoszómális recesszív módon öröklődő Nijmegen breakage szindróma (NBS), amelynek fő jellemzői a kromoszóma instabilitás, sugárérzékenység, daganatos betegségek iránti fogékonyság. Az NBS fehérje valószínűleg ugyanazon a szinten játszik szerepet a DNS károsodásra bekövetkező alarm-szignál generációjában, mint az ATM protein (182). Az NBS fehérjét kódoló gén mutációjának következménye a p53 által mediált sejtválasz elmaradása irradiációindukálta DNS károsodást követően (199). A hiányzó NBS funkció nem helyettesíthető ATM proteinnel. 17
18 Több kutatócsoport vizsgálatai alapján mind az ATM, mind a DNA-PK képes reakcióba lépni a c-abl fehérjével (10, 96, 167). A c-abl egy non-receptor tirozin kináz, amely regulátor szerepét feltételezik DNS-károsodás indukálta apoptózisban. Az ATM és a DNA-PK proteinek komplexet képeznek a c-abl-lal, amit foszforiláció útján aktiválnak. Az aktív enzim további foszforilációt végez a p53 és a Rb proteineken, gátló hatást fejt ki a sejtciklus progressszióra a G 1 /S fázis átmenetben. Besugárzást követő DNS károsodás után a G 2 fázis megnyúlása is észlehető, amiben szintén szerepe van az ATM proteinnek, és ami az ép, ún. vad típusú p53 fehérje hiányában is megfigyelhető (75). A sejtek G 2 fázison történő átjutásához, a mitózis fázisába való belépéséhez aktív ciklinb1-cdk1 komplexek létrejötte szükséges. Ez teszi lehetővé, hogy a cdk1 fehérje ki tudja fejteni kináz aktivitását, és létrejöjjön a H1 hisztonok foszforilációja. A foszforilált H1 hisztonok funkcionális jelentősége valószínűleg a mitotikus kromoszóma kondenzáció erősítése lehet (56). Guo és mtsai úgy találták, hogy ionizáló sugárzást követően a foszforilált H1-szint ATM-dependens, p53-independens módon, reverzibilisen lecsökken, amely hátterében kimutatták a H1 hisztonok foszforilációját eredményező kináz aktivitás csökkenését, valamint a foszfatáz aktivitás növekedését (56). A folyamat valószínűleg a sugár indukálta DNS károsodással kezdődik, amelyet az ATM fehérje érzékel, és a megfelelő jelátvivő utak aktiválásával végül a H1 hisztonok foszforilációs szintjének csökkenéséhez vezet. Ennek eredményeképpen feltehetően könnyebben hozzáférnek a DNS repair faktorok a károsodás helyéhez (mivel a H1 hisztonok defoszforilációja a kromatin dekondenzációját eredményezi). A H1 foszforilációt lehetővé tevő aktív ciklinb1-cdk1 komplexek kialakulásának - így a sejt G 2 fázison történő átjutásának - regulációját illetően leírták, hogy amennyiben a sejt nincs kitéve DNS károsító ágensnek, az aktív komplexek létrejöttét segíti egyrészt a ciklinb1 szintjének a G 2 fázisban bekövetkező 10- szeres emelkedése (75). Másrészt sorozatos foszforilációk útján szabályozott a cdk1 aktivitása. Az első foszforiláció a 161-es pozíciójú treoninon történik, amely a CAK (Cyclin-dependent kinase Activating Kinase) által katalizált. Amikor a cdk1 fehérje kötődik a ciklinb1-hez, gátló jellegű foszforilációk következnek be a 14-es treoninon és a 15-ös tirozinon. A komplex akkor válik enzimatikusan aktívvá, amikor a cdc25 (cell division cycle 25) foszfatáz mindkét gátló foszfátot lehasítja. Irradiációt követően a cdc25 aktivitása - amely szintén foszforilációk által szabályozott - lecsökken, a cdk1 18
19 fehérje tartós foszforilációját eredményezve. Így a komplex nem tud aktiválódni, aktív ciklinb1-cdk1 hiányában pedig a sejtciklus leáll G 2 fázisban. A gátolt cdc25 funkcióval kapcsolatban Peng és mtsai kimutatták, hogy a sugár hatására bekövetkező DNS károsodás - feltehetően az ATM protein közreműködésével - aktiválja a chk1 (checkpoint kinase 1) enzimet, amely foszforilálja a cdc25-öt a 216-os szerinen (144). Ez a foszforiláció gátolja a cdc25 aktivitását, mivel lehetővé teszi a protein család tagjainak kapcsolódását a cdc25-höz, amely kötődés feltehetően megakadályozza a serkentő jellegű foszforilációk bekövetkeztét a molekulán (144). Matsuoka és mtsai irradiáció hatására bekövetkező DNS károsodás követően a chk2 (checkpoint kinase 2) fehérje ATM-dependens foszforilációját és aktiválódását mutatták ki (122). A chk2-nek a chk1-hez hasonló funkciót tulajdonítanak: szintén képes a cdc25-öt a 216-os szerinen foszforilálni, ezáltal gátolni a cdc25 aktivitását, ami megakadályozza aktív ciklinb1- cdk1 komplexek kialakulását. Ennek következtében a sejt nem tud továbbhaladni G 2 -ből a mitózis fázisába. Valószínű tehát, hogy besugárzást követően a G 2 fázis megnyúlása a cdk1 foszforilációja útján szabályozott, amit a cdc25 foszforilációja kontrollál. A csökkent cdc25 aktivitás mellett besugárzást követő G 2 megnyúlás során csökkent ciklinb1 szintet is tapasztaltak (75). A G 2 fázis megnyúlásának biológiai szerepe nem teljesen tisztázott. Feltehetően a sejtek genetikai stabilitását, DNS-károsodást követő túlélését, radioszenzitivitását befolyásolja (75). A fent leírt, DNS-károsodást felismerő és jeltovábbító fehérjék közül több is az apoptózis során aktiválódó cisztein proteázok (kaszpázok) targetje, például a PARP, a DNA-PK, a Rb és az ATM protein (199). p53-hoz kapcsolódó szignálutak A korábbiakban említett, DNS károsodást felismerő rendszerek a már részben ismertetett módokon - további jelátvivő utakat aktiválnak, amely nyomán létrejön a besugárzás által indukált sejtválasz. A p53 molekula központi helyet foglal el a posztirradiációs jelátvitelben, de léteznek p53-independens szignálutak is. A p53- dependens és -independens jelátvivő utak hálózatának összehangolt működése szükséges a sejtválasz létrejöttéhez (182). A sejtválasz magában foglalja bizonyos gének 19
20 aktiválódását, a sejtprogresszió kontrollját a sejtciklus ellenőrzési pontjain keresztül, replikáció- és transzkripció-gátlást, apoptózis indukciót. A p53 a TP53 tumorszuppresszor gén fehérjeterméke. A DNS-károsodáskor keletkező alarm szignált egy - apoptózisra vagy sejtciklus leállásra - specifikus szignálút közvetíti a p53 felé (126). A DNS-károsodásra bekövetkező p53-szint emelkedés különböző gének transzkripciójának aktiválódásához vezet (182). Az egyik legfontosabb target a korábbiakban említett p21 gén, amelynek promoter régiójához kötődve a p53 fokozza a gén transzkripcióját. A p21 protein a ciklindependens kinázokat gátolja, aminek következtében a Rb fehérje foszforilációja - amely szükséges lenne az E2F S-fázis specifikus transzkripciós faktor leválásához és aktiválódásához - elmarad, így a sejtciklus leáll G 1 fázisban (139, 182, 199). A repair enzimek helyreállítják az eredeti DNS struktúrát, súlyos károsodás esetén bekövetkezik az apoptózis. Ezt követően a hipofoszforilált Rb fehérjét a kaszpázok (a fejezetben összefoglalt cisztein proteázok) hasítják (199). A kaszpázok által történő hasítás érzékenyebbé teszi a retinoblastoma fehérjét egyéb proteázok hasító hatásával szemben is. A Rb fehérje overexpressziója valószínűleg a hasító enzimekért való kompetíció által gátolja a p53-dependens apoptózist. Lehetséges, hogy a p53 expresszió a G 2 fázis megnyúlásához is hozzájárul (75). Egyrészt a ciklin-dependens kináz inhibitor p21 indukálásával, ami - bár erősebb gátlást fejt ki a cdk2, 4 és 6-ra -, kisebb affinitással a cdk1 gátlására is képes. Másrészt DNS károsodást követően a normál p53 a családba tartozó szigma fehérje mrns-ének indukciójára is képes (75). A fehérje a korábbiakban említett módon gátolja a cdc25 foszfatáz működését, ezzel megakadályozza az aktív ciklinb1-cdk1 komplexek kialakulását, így a sejtciklus leáll G 2 fázisban. A p53 a pro-apoptotikus bax protein transzkripcióját fokozza. A bax fehérje a bcl-2 család egyéb proteinjeivel áll kapcsolatban. A családba tartozó pro- és anti-apoptotikus fehérjék egymással dimereket alkotnak, a különböző dimerek aránya határozza meg az adott sejt apoptózisra való hajlamát (182). /A p53 képes lehet pro-apoptotikus szignálátvitelre a bax-indukciótól független úton is. Ezt támasztja alá az a megfigyelés is, hogy bax-/- timocitákban a p53-dependens apoptózis zavartalanul végbement (199)/. 20
21 A p53 a GADD45 (growth arrest DNA-damage) csoportba tartozó fehérjék szintézisét serkenti, amelyek megkötik a DNS replikációban szerepet játszó PCNA-t (proliferating cell nuclear antigen), így blokkolják a replikációt (182). A p53 fokozza az mdm2 (murine double minute 2) protein szintézisét, amely a p53 negatív regulátora. Aktiválja olyan gének transzkripcióját is, amelyek által kódolt (ún. redox related) proteinek reaktív oxigéngyökök keletkezését eredményezik. A reaktív oxigéngyökök a mitokondrium komponenseinek oxidatív degradációjához vezetnek. A sugárzás a víz radiolízisével direkt módon is okozhat reaktív oxigéngyök-felszabadulást és mitokondrium károsodást (182). p53-tól független tumorszuppresszorok által mediált szignálutak A p53 mellett, attól függetlenül egyéb tumorszuppresszor gének fehérjetermékei is szerepet játszhatnak besugárzás után a jelátvitelben (182). Egyik képviselőjük, az IRF-1 (interferon regulatory factor-1) funkciója részben átfedésben áll a p53 funkciójával. IRF-1 hiányos egér embrió fibroblasztok - a p53 hiányos sejtekhez hasonlóan - képtelenek a p21-dependens sejtciklus leállásra - sugárzást követően. A két tumorszuppresszor valószínűleg együttműködik a DNS károsodásra adott sejtválaszban. A nukleáris proteineket kódoló BRCA1 és BRCA2 (breast cancer susceptibility) gének fehérjetermékei közül a BRCA1 egy transzkripciós faktor, amely képes a p21 gén transzkripciójának aktiválására p53-tól független úton, ezzel hozzájárul a sejtciklus leállásához G 1 fázisban. A BRCA1 hiányos egerek már az embrionális fejlődés során elpusztulnak. BRCA2 hiányában is megáll az embrionális fejlődés, a sejtek fokozottan radioszenzitívek, fenotípusukat tekintve az ATM hiányos sejtekre hasonlítanak. Mindkét BRCA gén által kódolt fehérje képes lehet kapcsolatot teremteni a sejtciklus kontroll és a DNS repair között (182). Az XRCC4-ligázIV komplexben - amely a DNS végeket egyesítő mechanizmus része - ugyanazon a BRCT (BRCA carboxy terminus) 21
22 doménen keresztül kötődik a ligáz IV az XRCC4-hez, ami jelen van a BRCA1-ben is és számos DNS repair enzimben. DNS-károsító hatásra sejttípustól, károsító ágenstől függően más-más jelátvivő utak aktiválódásával jöhet létre apoptózis. A p53-independens apoptózist leírták pédául p53- deficiens egerek mitogénekkel aktivált T-limfocitáiban, besugárzást követően szintén p53 hiányos egerek gasztrointesztinális epitheliumában, humán colorectalis adenoma és karcinóma sejtvonalban, prosztata sejtekben, endotel sejtekben (199) Extranukleáris szenzorok és az általuk kiváltott szignál-transzdukció Ionizáló sugárzásnak kitéve a sejteket, léteznek a DNS-károsodástól különböző faktorok, amelyek képesek a p53 protein citoplazmából a sejtmagba történő transzlokációjának serkentésére. Ezek játszhatják a károsodás extranukleáris szenzorainak szerepét (182). Az irradiáció hatására induló extranukleáris alarm-szignálok generációjának pontos mechanizmusa még nem tisztázott. A citoplazmában ionizáló sugárzás hatására a víz radiolízise által direkt módon reaktív oxigéngyökök keletkezhetnek, amelyek celluláris károsodást, mitokondriális- és sejtmembrán-károsodást okoznak (8). A reaktív oxigéngyökök képződésével járó ionizáló besugárzás után a p53 transzlokációja következik be a citoplazmából a sejtmagba. A bcl-2, amely citoplazmatikus membránfehérje (onkoprotein), képes meggátolni a p53 nukleáris importját, a reaktív oxigéngyökök által okozott celluláris károsodást és apoptózist (182). Besugárzáskor a sejtmembránban keletkező egyik extranukleáris alarm-szignál a szfingomyelináz enzim aktiválódása, amely ceramid-képződést eredményez, és apoptózishoz vezet (11). A ceramid metabolizmusát a 2. ábra mutatja. A ceramid a sejtmembránban koncentrálódó szfingomyelin lebontása útján keletkezik. A jelátvitelhez szükséges gyors ceramid-generáció egy szfingomyelin-specifikus foszfolipáz C (szfingomyelináz) aktiválódása útján történik, amely a szfingomyelin foszfodiészter 22
23 kötésének hidrolízisével ceramidot és foszforilkolint hoz létre. A szfingomyelináz enzimnek 2 típusát írták le, amelyek a ph optimumuk alapján különíthetők el egymástól. A savas szfingomyelináz enzimet (ph optimum: ) eredetileg mint lizoszomális hidrolázt azonosították, amely a celluláris membránok turnoveréhez szükséges, azonban a plazmamembránban is jelen van. Aktiválása összefügg a Fas, CD28, TNF (tumornekrózis faktor) és IL-1 (interleukin-1 ) receptorokon történő jelátvitellel és az ionizáló sugárzással. Egy genetikai betegségben, a Niemann-Pick kórban a savas szfingomyelinázt kódoló gén mutációját találták. A neutrális szfingomyelináz (ph optimuma 7.4) egy Mg 2+ -dependens enzim, amely a plazmamembrán külső rétegében helyezkedik el, aktiválása a Fas, TNF- és IL-1 receptorok által indukált sejtválasszal van összefüggésben. 2. ábra A ceramid metabolizmusa 23
24 Nem teljesen tisztázott az a mechanizmus, amellyel a receptorok ingerlése a szfingomyelináz enzim aktiválódásával párosul. A TNF- esetében leírtak egy proteint (FAN: Factor Associated with N-sphingomyelinase activation), amely a TNF- receptort a neutrális szfingomyelinázhoz kapcsolja, míg az ún. TRADD (TNF Receptor Associated Death Domain) protein és a FADD (Fas Associated Death Domain) protein a nevükben jelzett receptor és a savas szfingomyelináz enzim között képes kapcsolatot teremteni (199). Niemann-Pick kóros betegekből vett limfoblasztokon és savas szfingomyelináz deficiens egerekből vett tüdőszöveten végzett vizsgálatokból valószínűsíthető, hogy az ionizáló sugárzás a savas szfingomyelináz enzim aktiválódásával párosul (199), de a pontos mechanizmus nem tisztázott. Az enzim aktiválódása útján keletkező ceramid a másodlagos messenger szerepét töltheti be. Mind a reaktív oxigéngyökök, mind a ceramid a mitokondriumok membránpotenciálját csökkenti az ioncsatornák megnyitásával, amely az apoptózis korai fázisának obligát lépése (182). A szfingomyelináz enzim aktiválódása mellett szintén a sejtmembránban generálódó alarm-szignál a membránhoz kötött tirozin kinázok (epidermális növekedési faktor receptor, Bruton s tirozin kináz) aktivációja. Ezek közül a Bruton s tirozin kináz B-sejtes lymphomában nélkülözhetetlennek tűnik sugár indukálta apoptotikus válasz kiváltásában (199). Sejtmembrán-károsodás által generált apoptózis Ashwell és mtsai (8) megfigyelték, hogy az ionizáló sugárzás hatására keletkezett oxigéngyökök károsították a sejtmembrán foszfolipid rétegét és apoptózist váltottak ki B-limfocitákban. A ceramidnak, mint másodlagos messengernek a szerepe a TNF- által indukált apoptózis mechanizmusának vizsgálatával kapcsolatosan vetődött fel (133). Haimovitz-Friedman és mtsai (57) vizsgálatai szintén a ceramidnak, mint másodlagos messengernek a szerepét igazolták ionizáló sugárzás indukálta apoptózisban. BAEC (bovine aortic endothelial cells) és U937 humán mieloid leukémia sejteket sugaraztak be különböző dózisokkal, amelyet követően másodperceken belül megindult a 24
25 szfingomyelin dózis-függő hidrolízise ceramiddá. A protein kináz C (PKC) aktiválása TPA-val (12-O-tetradekanoil-phorbol-13-acetát) teljesen blokkolta a szfingomyelináz aktiválódását, a ceramid keletkezését és az apoptózist, míg a sejtek kezelése exogén ceramiddal visszaállította az apoptózisra való hajlamot. BL30A Burkitt-lymphoma sejtekben TPA-val szintén sikerült meggátolni a sugár-indukálta ceramid generációt és az apoptózist (199). Annak alátámasztására, hogy a szfingomyelináz enzim aktiválódása és a ceramid generációja az ionizáló sugárzás és a sejtmembrán interakciójának következménye lehet, Haimovitz-Friedman és mtsai felállítottak egy kísérletes modellt (58). Sejtmagtól megfosztott humán leukémia sejtek sejtmembrán preparátumait besugarazták, és mérték a ceramid-szint emelkedését. Sugárkezelést követően a ceramidszint másodperceken belül elkezdett emelkedni a preparátumokban, 4 perc elételtével az emelkedés mértéke ugyanakkora volt, mint ép sejtek besugárzása esetén. A ceramid szerepének direkt bizonyítékát in vitro a Niemann-Pick kóros betegekből - akik savas szfingomyelináz hiányban szenvednek öröklött módon - vett limfoblasztokon végzett vizsgálatok jelentették (159). A sejtekben még nagydózisú (20 Gy) besugárzást követően sem volt ceramid-szint emelkedés, valamint apoptózis. A szfingomyelináztermelés helyreállítását követően (az enzimet kódoló cdns-t retrovírusokkal juttatták a sejtekbe) azonban a ceramid generációja a normál szintre állt vissza, és apoptózist is a normál sejtekkel megegyező mértékben tudtak kimutatni. Santana és mtsai in vivo kísérletek során igazolták, hogy a sugárzás legalább 2 egymástól független szignáltranszdukciós úton válthat ki apoptózist, valamint kimutatták a ceramidnak mint másodlagos messengernek a szerepét szfingomyelináz által mediált apoptózisban (159). Savas szfingomyelináz deficiens egerekben vizsgálták a sugár hatására létrejövő ceramid generációt és apoptózist. Normál állatokban a tüdő 20 Gy besugárzását követően a szöveti ceramid-szint 2.3-szorosára emelkedett, és extenzív apoptózist tapasztaltak, míg szfingomyelináz deficiens egerekben sem ceramid-szint emelkedést, sem apoptózist nem tudtak kimutatni még 30 Gy besugárzást követően sem. Összehasonlították továbbá az apoptózisra való hajlamot teljes test besugárzást követően savas szfingomyelináz deficiens és p53 deficiens egerekben. Arra a következtetésre jutottak, hogy a savas szfingomyelináz és a p53 által mediált apoptózis egymástól függetlenül, különböző utakon megy végbe: míg az endocardialis sejtekben, a tüdő endoteliális, valamint a pleura és a pericardium serosus sejtjeiben az apoptózis 25
26 szfingomyelináz által mediált (és p53 negatív állatokban zavartalan), addig a tímusz T- sejtjeiben az apoptózis p53-dependens, és a szfingomyelinázt kódoló gén deléciója nem befolyásolja. Ezzel ellentétes következtetésre jutottak Dbaibo és mtsai, akik úgy találták, hogy Molt-4 humán leukémia és L929 patkány fibroblaszt sejtekben -irradiációt követően a ceramid akkumulációja p53-dependens módon zajlott, csak normál p53 funkcióval rendelkező sejtekben volt megfigyelhető (32). Magyarázatára a szerzők feltételezik, hogy az általuk (sugárkezelés után) megfigyelt p53-dependens ceramid-felszaporodás valószínűleg nem a savas, hanem a neutrális szfingomyelináz aktiválódásával állhat kapcsolatban. Ugyanakkor - szintén Dbaibo és mtsai - megfigyeltek p53-independens ceramidakkumulációt is: L929 sejtekben TNF kezelést követően, Molt-4 sejtekben szérum megvonás után (32). Ezek alapján elképzelhetőnek tartják, hogy a kétféle szfingomyelináz enzim aktiválódása függhet a sejtkárosító ágenstől, valamint ugyanolyan károsító hatást követően egy adott sejttípusra, szövetre nézve jellemző lehet. Valószínű, hogy azokban az esetekben, amikor a p53 fehérjének kulcsszerepe van a sejtválasz létrejöttében különböző sejtkárosító hatásokat követően, a p53 a ceramid felett helyezkedhet el a jelátviteli kaszkádban, szabályozza a ceramid generációját, és nem fordítva (32). Humán leukémia és endotel sejtekben kimutatták, hogy a membránkárosodást okozó ionizáló sugárzás (és egyéb stresszhatások, pl. UV sugárzás, hősokk, ozmotikus sokk, növekedési faktor megvonás) apoptózist kiváltó hatásához a SAPK (Stress Activated Protein Kinase) kaszkád tagjainak: SAPK kináz kináz, SAPK kináz, SAPK és JUN foszforiláció útján történő szekvenciális aktiválódása is szükséges (59). Az ionizáló sugárzás gyors ceramid generációt indukál, amely aktiválja a kaszkád tagjait és apoptózist okoz. A kaszkád szerepét támasztja alá, hogy JUN negatív U937 leukémia sejtekben sem stresszhatás, sem exogén ceramid nem váltott ki apoptózist annak ellenére, hogy maga a ceramid képződés és a SAPK aktiváció zavartalan volt. Hallahan és mtsai humán epiteliális tumorsejteken végzett vizsgálatainak eredményei szintén a - transzkripciós faktorokat kódoló - JUN géncsalád szignáltranszducer szerepére utalnak ionizáló sugárzás kiváltotta sejtválaszban (60). Besugárzást követően órán belül a JUN gének expressziójának fokozódását tapasztalták. Cuvillier és mtsai feltételezik, hogy a sejtek apoptotizáló hajlamát végül a pro-apoptotikus SAPK, és a pontban 26
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Apoptózis. 1. Bevezetés 2. Külső jelút 3. Belső jelút
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia. Dr. Sáfrány Géza OKK - OSSKI
 Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia Dr. Sáfrány Géza OKK - OSSKI Az ionizáló sugárzás biológiai hatásai Determinisztikus hatás Sztochasztikus hatás Sugársérülések
Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia Dr. Sáfrány Géza OKK - OSSKI Az ionizáló sugárzás biológiai hatásai Determinisztikus hatás Sztochasztikus hatás Sugársérülések
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Prognosztikai faktorok fej-nyaki laphámrákokban, szerepük a terápia tervezésében
 Prognosztikai faktorok fej-nyaki laphámrákokban, szerepük a terápia tervezésében Ph.D. Doktori értekezés tézisei Írta: Dr. Kraxner Helga Témavezető: Dr. Szende Béla egyetemi tanár Programvezető: Dr. Jeney
Prognosztikai faktorok fej-nyaki laphámrákokban, szerepük a terápia tervezésében Ph.D. Doktori értekezés tézisei Írta: Dr. Kraxner Helga Témavezető: Dr. Szende Béla egyetemi tanár Programvezető: Dr. Jeney
Jelutak. 2. A jelutak komponensei Egy tipikus jelösvény sémája. 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Immunológia alapjai előadás. A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és
 Immunológia alapjai 15-16. előadás A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és csíracentrum reakció, affinitás-érés és izotípusváltás. A B-sejt fejlődés szakaszai HSC Primer
Immunológia alapjai 15-16. előadás A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és csíracentrum reakció, affinitás-érés és izotípusváltás. A B-sejt fejlődés szakaszai HSC Primer
Immunológia alapjai. Az immunválasz szupressziója Előadás. A szupresszióban részt vevő sejtes és molekuláris elemek
 Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
A citoszol szolubilis fehérjéi. A citoplazma matrix (citoszol) Caspase /Kaszpáz/ 1. Enzimek. - Organellumok nélküli citoplazma
 A citoplazma matrix (citoszol) A citoszol szolubilis fehérjéi 1. Enzimek - Organellumok nélküli citoplazma -A sejt fejlődéstani szempontból legősibb része (a sejthártyával együtt) Glikolízis teljes enzimrendszere
A citoplazma matrix (citoszol) A citoszol szolubilis fehérjéi 1. Enzimek - Organellumok nélküli citoplazma -A sejt fejlődéstani szempontból legősibb része (a sejthártyával együtt) Glikolízis teljes enzimrendszere
A herpes simplex vírus és a rubeolavírus autofágiára gyakorolt in vitro hatásának vizsgálata
 A herpes simplex vírus és a rubeolavírus autofágiára gyakorolt in vitro hatásának vizsgálata Dr. Pásztor Kata Ph.D. Tézis Szegedi Tudományegyetem, Általános Orvostudományi Kar Orvosi Mikrobiológiai és
A herpes simplex vírus és a rubeolavírus autofágiára gyakorolt in vitro hatásának vizsgálata Dr. Pásztor Kata Ph.D. Tézis Szegedi Tudományegyetem, Általános Orvostudományi Kar Orvosi Mikrobiológiai és
A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata
 Ph.D. ÉRTEKEZÉS TÉZISEI A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata Buzás-Bereczki Orsolya Témavezetők: Dr. Bálint Éva Dr. Boros Imre Miklós Biológia
Ph.D. ÉRTEKEZÉS TÉZISEI A TATA-kötő fehérje asszociált faktor 3 (TAF3) p53-mal való kölcsönhatásának funkcionális vizsgálata Buzás-Bereczki Orsolya Témavezetők: Dr. Bálint Éva Dr. Boros Imre Miklós Biológia
Daganatok kialakulásában szerepet játszó molekuláris folyamatok
 Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
A programozott sejthalál mint életfolyamat
 APOPTOSIS Réz Gábor A programozott sejthalál mint életfolyamat A sejteknek, legyenek bár prokarióták vagy eukarióták, öröklött képességük van arra, hogy belső vagy külső jelek hatására beindítsák a programozott
APOPTOSIS Réz Gábor A programozott sejthalál mint életfolyamat A sejteknek, legyenek bár prokarióták vagy eukarióták, öröklött képességük van arra, hogy belső vagy külső jelek hatására beindítsák a programozott
H 2 O e aq + H 2 O + Ionizáció (e aq = hidratált elektron) H 2 O H 2 O OH + H Excitácót követő disszociáció
 Az ionizáló sugárzás biológiai hatásai Az ionizáló sugárzás biológiai hatásai Dr. Sáfrány Géza OSSKI Determinisztikus hatás Sztochasztikus hatás Az Ionizáló Sugárzás Direkt és Indirekt Hatásai Közvetlen
Az ionizáló sugárzás biológiai hatásai Az ionizáló sugárzás biológiai hatásai Dr. Sáfrány Géza OSSKI Determinisztikus hatás Sztochasztikus hatás Az Ionizáló Sugárzás Direkt és Indirekt Hatásai Közvetlen
http://www.rimm.dote.hu Tumor immunológia
 http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
OTKA ZÁRÓJELENTÉS
 NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
A TERMÉSZETES SEJTHALÁL LEGGYAKORIBB FORMÁJA AZ APOPTÓZIS Fésüs László
 A TERMÉSZETES SEJTHALÁL LEGGYAKORIBB FORMÁJA AZ APOPTÓZIS Fésüs László Összefoglaló Az emberi szervezet sejtjeinek nagy többsége meghatározott idő után természetes módon elhal, helyette új sejtek képződnek.
A TERMÉSZETES SEJTHALÁL LEGGYAKORIBB FORMÁJA AZ APOPTÓZIS Fésüs László Összefoglaló Az emberi szervezet sejtjeinek nagy többsége meghatározott idő után természetes módon elhal, helyette új sejtek képződnek.
Sejtek öregedése és apoptózis
 Sejtek öregedése és apoptózis Láng Orsolya Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet Külső hatások Belső hatások A sejt válasza Szignál molekulák Szignál molekulák hiány hiánya vagy
Sejtek öregedése és apoptózis Láng Orsolya Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet Külső hatások Belső hatások A sejt válasza Szignál molekulák Szignál molekulák hiány hiánya vagy
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 4. előadás. Kacskovics Imre
 Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Spondylitis ankylopoeticahoz társuló osteoporosis
 Spondylitis ankylopoeticahoz társuló osteoporosis Szántó Sándor DE OEC, Reumatológiai Tanszék 2013.11.05. Szeminárium Csontfelszivódás és csontképzés SPA-ban egészséges előrehaladott SPA Spondylitis ankylopoetica
Spondylitis ankylopoeticahoz társuló osteoporosis Szántó Sándor DE OEC, Reumatológiai Tanszék 2013.11.05. Szeminárium Csontfelszivódás és csontképzés SPA-ban egészséges előrehaladott SPA Spondylitis ankylopoetica
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai
 Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
A sejtciklus szabályozása
 Molekuláris sejtbiológia A sejtciklus szabályozása? Dr. habil.. Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtciklus fázisai S G 2 G 0 G 1 M G = gap gap S = synthesis
Molekuláris sejtbiológia A sejtciklus szabályozása? Dr. habil.. Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtciklus fázisai S G 2 G 0 G 1 M G = gap gap S = synthesis
Az endomembránrendszer részei.
 Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
Immunológia 4. A BCR diverzitás kialakulása
 Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Hivatalos Bírálat Dr. Gődény Mária
 Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény
 A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával
 Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
sejt működés jovo.notebook March 13, 2018
 1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
DNS replikáció. DNS RNS Polipeptid Amino terminus. Karboxi terminus. Templát szál
 DNS replikáció DNS RNS Polipeptid Amino terminus Templát szál Karboxi terminus Szuper-csavarodott prokarióta cirkuláris DNS Hisztonok komplexe DNS hisztonokra történő felcsvarodása Hiszton-kötött negatív
DNS replikáció DNS RNS Polipeptid Amino terminus Templát szál Karboxi terminus Szuper-csavarodott prokarióta cirkuláris DNS Hisztonok komplexe DNS hisztonokra történő felcsvarodása Hiszton-kötött negatív
Sugárterápia. Ionizáló sugárzások elnyelődésének következményei
 Sugárterápia Sugárterápia: ionizáló sugárzások klinikai alkalmazása malignus daganatok eltávolításában. A sugárkezelés során célunk az ionizáló sugárzás terápiás dózisának elérése a kezelt daganatban a
Sugárterápia Sugárterápia: ionizáló sugárzások klinikai alkalmazása malignus daganatok eltávolításában. A sugárkezelés során célunk az ionizáló sugárzás terápiás dózisának elérése a kezelt daganatban a
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Apoptózis Bevezetés Apoptózis jelutak (1) belső jelút (1a) (1b) (2) külső jelút Programozott sejthalál ( apoptózis és autofágia
 Apoptózis Bevezetés (DIA 1) A többsejtű szervezetek testének kialakulását egy jól meghatározott genetikai/epigenetikai program irányítja. Ez a folyamat nem csupán új sejtek előállításából áll, hanem a
Apoptózis Bevezetés (DIA 1) A többsejtű szervezetek testének kialakulását egy jól meghatározott genetikai/epigenetikai program irányítja. Ez a folyamat nem csupán új sejtek előállításából áll, hanem a
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM. Jelutak. 1. a sejtkommunikáció alapjai
 Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
67. Pathologus Kongresszus
 A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA NOVEMBER
 Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
4. A humorális immunválasz október 12.
 4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
A sejtciklus szabályozása
 A sejtciklus szabályozása (kék: DNS, piros: tubulin, zöld: metafázis ellenőrzőpont fehérje) G2 fázis: nincs DNS szintézis RNS és fehérje szintézis folytatódik M fázis: a mitózis és a citokinézis két sejtet
A sejtciklus szabályozása (kék: DNS, piros: tubulin, zöld: metafázis ellenőrzőpont fehérje) G2 fázis: nincs DNS szintézis RNS és fehérje szintézis folytatódik M fázis: a mitózis és a citokinézis két sejtet
Vásárhelyi Barna. Semmelweis Egyetem, Laboratóriumi Medicina Intézet. Az ösztrogénekimmunmoduláns hatásai
 Vásárhelyi Barna Semmelweis Egyetem, Laboratóriumi Medicina Intézet Az ösztrogénekimmunmoduláns hatásai Ösztrogénhatások Ösztrogénhatások Morbiditás és mortalitási profil eltérő nők és férfiak között Autoimmun
Vásárhelyi Barna Semmelweis Egyetem, Laboratóriumi Medicina Intézet Az ösztrogénekimmunmoduláns hatásai Ösztrogénhatások Ösztrogénhatások Morbiditás és mortalitási profil eltérő nők és férfiak között Autoimmun
Sugárterápia. Ionizáló sugárzások elnyelődésének következményei. Konzultáció: minden hétfőn 15 órakor. 1. Fizikai történések
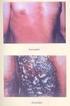 Sugárterápia 40% 35% 30% 25% 20% 15% % 5% 0% 2014/2015. tanév FOK biofizika kollokvium jegyspektruma 5 4,5 4 3,5 3 2,5 2 1,5 1 Konzultáció: minden hétfőn 15 órakor Ionizáló sugárzások elnyelődésének következményei
Sugárterápia 40% 35% 30% 25% 20% 15% % 5% 0% 2014/2015. tanév FOK biofizika kollokvium jegyspektruma 5 4,5 4 3,5 3 2,5 2 1,5 1 Konzultáció: minden hétfőn 15 órakor Ionizáló sugárzások elnyelődésének következményei
Vezikuláris transzport
 Molekuláris Sejtbiológia Vezikuláris transzport Dr. habil KŐHIDAI László Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet 2005. november 3. Intracelluláris vezikul uláris transzport Kommunikáció
Molekuláris Sejtbiológia Vezikuláris transzport Dr. habil KŐHIDAI László Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet 2005. november 3. Intracelluláris vezikul uláris transzport Kommunikáció
XIII./5. fejezet: Terápia
 XIII./5. fejezet: Terápia A betegek kezelésekor a sebészi kezelés, a kemoterápia (klasszikus citotoxikus és a biológiai terápia), a radioterápia és ezek együttes alkalmazása egyaránt szóba jön. A gégének
XIII./5. fejezet: Terápia A betegek kezelésekor a sebészi kezelés, a kemoterápia (klasszikus citotoxikus és a biológiai terápia), a radioterápia és ezek együttes alkalmazása egyaránt szóba jön. A gégének
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Receptorok, szignáltranszdukció jelátviteli mechanizmusok
 Receptorok, szignáltranszdukció jelátviteli mechanizmusok Sántha Péter 2016.09.16. A sejtfunkciók szabályozása - bevezetés A sejtek közötti kommunikáció fő típusai: Endokrin Parakrin - Autokrin Szinaptikus
Receptorok, szignáltranszdukció jelátviteli mechanizmusok Sántha Péter 2016.09.16. A sejtfunkciók szabályozása - bevezetés A sejtek közötti kommunikáció fő típusai: Endokrin Parakrin - Autokrin Szinaptikus
A sejtfelszíni receptorok három fő kategóriája
 A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
Programozott sejthalál formák és kulcsfehérjéinek kapcsolata - fókuszban a ferroptózis és az autofágia. V. MedInProt Konferencia November 19.
 Programozott sejthalál formák és kulcsfehérjéinek kapcsolata - fókuszban a ferroptózis és az autofágia Dr. Szarka András Dr. Kapuy Orsolya V. MedInProt Konferencia 2016. November 19. Bevezetés Bevezetés
Programozott sejthalál formák és kulcsfehérjéinek kapcsolata - fókuszban a ferroptózis és az autofágia Dr. Szarka András Dr. Kapuy Orsolya V. MedInProt Konferencia 2016. November 19. Bevezetés Bevezetés
Platina bázisú kemoterápia hatása különböző biomarkerek expressziójára tüdőrákokban
 Platina bázisú kemoterápia hatása különböző biomarkerek expressziójára tüdőrákokban Pápay J. 1, Sápi Z. 1 Gyulai M. 5, Egri G. 2, Szende B. 1, Tímár J. 4 Moldvay J. 3 1: Semmelweis Egyetem, I.sz.Patológiai
Platina bázisú kemoterápia hatása különböző biomarkerek expressziójára tüdőrákokban Pápay J. 1, Sápi Z. 1 Gyulai M. 5, Egri G. 2, Szende B. 1, Tímár J. 4 Moldvay J. 3 1: Semmelweis Egyetem, I.sz.Patológiai
Epigenetikai Szabályozás
 Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
A PROGRAMOZOTT SEJTHALÁL
 A PROGRAMOZOTT SEJTHALÁL A programozott sejthalál (programmed cell death; PCD) alapvetően intracelluláris (endogén) program által szabályozott folyamat, ami a sejtproliferáció antagonistájaként a szervezet
A PROGRAMOZOTT SEJTHALÁL A programozott sejthalál (programmed cell death; PCD) alapvetően intracelluláris (endogén) program által szabályozott folyamat, ami a sejtproliferáció antagonistájaként a szervezet
Az Oxidatív stressz hatása a PIBF receptor alegységek összeszerelődésére.
 Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Neoplazma - szabályozottság nélküli osztódó sejt
 9. előadás Rák Rák kialakulása: A szervezet 10 14 sejtet tartalmaz, ezek mutálnak és osztódnak A rákos sejt nem követi a sejtosztódás korlátait és végül a rákos sejtek elfoglalják a normál szövetek helyét.
9. előadás Rák Rák kialakulása: A szervezet 10 14 sejtet tartalmaz, ezek mutálnak és osztódnak A rákos sejt nem követi a sejtosztódás korlátait és végül a rákos sejtek elfoglalják a normál szövetek helyét.
S-2. Jelátviteli mechanizmusok
 S-2. Jelátviteli mechanizmusok A sejtmembrán elválaszt és összeköt. Ez az információ-áramlásra különösen igaz! 2.1. A szignál-transzdukció elemi lépései Hírvivô (transzmitter, hormon felismerése = kötôdés
S-2. Jelátviteli mechanizmusok A sejtmembrán elválaszt és összeköt. Ez az információ-áramlásra különösen igaz! 2.1. A szignál-transzdukció elemi lépései Hírvivô (transzmitter, hormon felismerése = kötôdés
INTRACELLULÁRIS PATOGÉNEK
 INTRACELLULÁRIS PATOGÉNEK Bácsi Attila, PhD, DSc etele@med.unideb.hu Debreceni Egyetem, ÁOK Immunológiai Intézet INTRACELLULÁRIS BAKTÉRIUMOK ELLENI IMMUNVÁLASZ Példák intracelluláris baktériumokra Intracelluláris
INTRACELLULÁRIS PATOGÉNEK Bácsi Attila, PhD, DSc etele@med.unideb.hu Debreceni Egyetem, ÁOK Immunológiai Intézet INTRACELLULÁRIS BAKTÉRIUMOK ELLENI IMMUNVÁLASZ Példák intracelluláris baktériumokra Intracelluláris
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Kutatási beszámoló ( )
 Kutatási beszámoló (2008-2012) A thrombocyták aktivációja alapvető jelentőségű a thrombotikus betegségek kialakulása szempontjából. A pályázat során ezen aktivációs folyamatok mechanizmusait vizsgáltuk.
Kutatási beszámoló (2008-2012) A thrombocyták aktivációja alapvető jelentőségű a thrombotikus betegségek kialakulása szempontjából. A pályázat során ezen aktivációs folyamatok mechanizmusait vizsgáltuk.
ÖSSZ-TARTALOM. 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3.
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere
 I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE
 Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Hús és hústermék, mint funkcionális élelmiszer
 Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
3. Főbb Jelutak. 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3.
 Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Antigén, Antigén prezentáció
 Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Az ophthalmopathia autoimmun kórfolyamatára utaló tényezôk Bizonyított: A celluláris és humorális autoimmun folyamatok szerepe.
 Az ophthalmopathia autoimmun kórfolyamatára utaló tényezôk Bizonyított: A celluláris és humorális autoimmun folyamatok szerepe. szemizom, retrobulbaris kötôszövet, könnymirigy elleni autoantitestek exophthalmogen
Az ophthalmopathia autoimmun kórfolyamatára utaló tényezôk Bizonyított: A celluláris és humorális autoimmun folyamatok szerepe. szemizom, retrobulbaris kötôszövet, könnymirigy elleni autoantitestek exophthalmogen
Mutagenezis és s Karcinogenezis kutatócsoport. Haracska Lajos.
 Mutagenezis és s Karcinogenezis kutatócsoport SZBK Genetikai Intézete (429 dolgozó,, Tel: 62-599666) haracska@brc.hu Haracska Lajos www.brc.hu/lajoslab Evolúci ció és s karcinogenezis: közös k s gyökerek
Mutagenezis és s Karcinogenezis kutatócsoport SZBK Genetikai Intézete (429 dolgozó,, Tel: 62-599666) haracska@brc.hu Haracska Lajos www.brc.hu/lajoslab Evolúci ció és s karcinogenezis: közös k s gyökerek
A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése
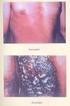 A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése Madas Balázs Gergely XXXIX. Sugárvédelmi Továbbképző Tanfolyam Hajdúszoboszló, Hunguest Hotel Béke 2014.
A vérképző rendszerben ionizáló sugárzás által okozott mutációk kialakulásának numerikus modellezése Madas Balázs Gergely XXXIX. Sugárvédelmi Továbbképző Tanfolyam Hajdúszoboszló, Hunguest Hotel Béke 2014.
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél
 Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél Dr. Mangel László 1,2, Prof. Dr. Dóczi Tamás 3, Dr. Balogh Zsolt 4, Dr. Lövey József 2, Dr. Sipos László 5 Pécsi Tudományegyetem, Onkoterápiás
Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél Dr. Mangel László 1,2, Prof. Dr. Dóczi Tamás 3, Dr. Balogh Zsolt 4, Dr. Lövey József 2, Dr. Sipos László 5 Pécsi Tudományegyetem, Onkoterápiás
Dr. Fröhlich Georgina
 Sugárbiol rbiológia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Az ionizáló sugárzás biológiai hatásai - determinisztikus
Sugárbiol rbiológia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Az ionizáló sugárzás biológiai hatásai - determinisztikus
Új, sejthalált befolyásoló tumor-asszociált fehérjék azonosítása. Dr. Szigeti András. PhD tézis. Programvezető: Dr. Balázs Sümegi, egyetemi tanár
 Új, sejthalált befolyásoló tumor-asszociált fehérjék azonosítása Dr. Szigeti András PhD tézis Programvezető: Dr. Balázs Sümegi, egyetemi tanár Pécsi Tudományegyetem, Biokémiai és Orvosi Kémiai Intézet
Új, sejthalált befolyásoló tumor-asszociált fehérjék azonosítása Dr. Szigeti András PhD tézis Programvezető: Dr. Balázs Sümegi, egyetemi tanár Pécsi Tudományegyetem, Biokémiai és Orvosi Kémiai Intézet
Doktori értekezés tézisei
 Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
NÖVÉNYÉLETTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 NÖVÉNYÉLETTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Sejtfal szintézis és megnyúlás Környezeti tényezők hatása a növények növekedésére és fejlődésére Előadás áttekintése
NÖVÉNYÉLETTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Sejtfal szintézis és megnyúlás Környezeti tényezők hatása a növények növekedésére és fejlődésére Előadás áttekintése
ÚJDONSÁGOK ELŐREHALADOTT NEM KISSEJTES TÜDŐRÁK KOMPLEX ONKOLÓGIAI KEZELÉSÉBEN
 ÚJDONSÁGOK ELŐREHALADOTT NEM KISSEJTES TÜDŐRÁK KOMPLEX ONKOLÓGIAI KEZELÉSÉBEN Ph.D. Tézis /rövidített változat/ Dr. Maráz Anikó Témavezető: Dr. Hideghéty Katalin, Ph.D. Szegedi Tudományegyetem Általános
ÚJDONSÁGOK ELŐREHALADOTT NEM KISSEJTES TÜDŐRÁK KOMPLEX ONKOLÓGIAI KEZELÉSÉBEN Ph.D. Tézis /rövidített változat/ Dr. Maráz Anikó Témavezető: Dr. Hideghéty Katalin, Ph.D. Szegedi Tudományegyetem Általános
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
HORMONKEZELÉSEK. A hormonkezelés típusai
 HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
